玉米须(Stigma Maydis)又称玉麦须、蜀黍须,是禾本科植物玉米雌花的花柱和柱头。玉米是我国最主要的粮食作物之一,种植面积广、产量高,主要分布在我国东北、山东、四川等地区,玉米须作为玉米加工过程中的副产品,原料来源稳定,有利于规模化生产和深加工。其次玉米须具有很高的营养和药用价值,能生产出高附加值的产品,不仅可以提升经济效益,还能够减少废弃物的排放[1]。玉米须的药用记载始于《滇南木草》,是一种来源丰富、价格低廉、易于采集的中药材,具有广泛的生物活性,包括降血糖、降血脂、抗氧化、缓解炎症等[2-3]。研究表明,玉米须中含有丰富的生物活性成分,如多糖、多酚、黄酮、生物碱、维生素和氨基酸等,其中多糖是玉米须中主要活性成分之一,有巨大的研究价值[4-6]。植物多糖因其广泛的药理活性和较少的副作用而受到广泛关注。国内外研究表明,玉米须多糖(corn silk polysaccharide,CSP)安全无毒,在食品加工中具有保健养生的功效,如抗氧化、降血糖、降血脂、保护肝肾、抗肿瘤、抗疲劳、免疫调节和抗高尿酸血症等生物活性[6-9]。随着糖化学和糖生物学技术的快速发展,CSP的结构特征和药理活性作用的研究引起了科研工作者的广泛关注。近年来,科研工作者对CSP的提取工艺优化、结构表征和药理活性评价等方面进行了大量的研究,并取得了一定的进展。因此,本文基于近年来CSP的研究现状进行归纳总结,为CSP在食品、医药等领域的进一步研究和应用开发提供思路和依据。
1 CSP提取纯化
提取方法对多糖的性质影响很大,不同提取工艺得到的多糖具有不同的结构与性质[10]。图1总结了CSP提取、纯化、结构特征及生物活性示意图。目前CSP的提取方法主要有水提醇沉法、超声波辅助提取法、酶辅助提取法及微波辅助提取法等,表1总结了CSP的主要提取方法。其中热水提法最为常用,操作最简单且经济成本低。但存在提取时间长、多糖损失率高等缺点。为了提高多糖得率,通常采用高新技术进行辅助提取,超声辅助提取、微波辅助提取、酶辅助提取以及亚临界流体萃取。如李亚平等[11]对比在相同提取工艺下,酸法提取的多糖得率明显高于热水提取,这可能是因为在强酸条件下导致细胞壁破损促使多糖充分溶出。但结构分析表明酸法提取导致多糖降解,使多糖组成及结构发生改变,且生物活性降低。因此在植物多糖提取过程中不能单纯追求多糖得率,应在多糖结构活性不改变的前提下,提高多糖得率。侯敏娜等[12]采用超声辅助提取CSP,在最佳条件(提取时间33 min,超声温度60 ℃,料液比1∶25)时该工艺得到的多糖提取率为5.53%;此外,陈珊珊等[13]采用响应面优化微波-超声波协同提取CSP,最佳提取条件为微波功率451.81 W,提取时间18.40 min,料液比1∶37.75(g∶mL),多糖提取率为5.98%。与传统水提法相比,微波和超声波辅助可以缩短提取时间、提高多糖得率。酶法辅助提取效率高、专一性好,比大多数物理提取方法效率更高,再加上回流技术可以避免提取液挥发,节省用量。王晴等[14]和李劭彤等[15]采用纤维素酶消化-回流法提取CSP,最终得到了相同的最佳提取条件,即料液比1∶30(g∶mL),回流时间2 h,回流温度90 ℃。然而王晴等[14]的多糖提取率更高,表明相同提取工艺,不同品种、生长周期、预处理方法的不同也会对多糖得率产生影响。
表1 玉米须多糖的提取方法
Table 1 Extraction method of polysaccharides from corn silk
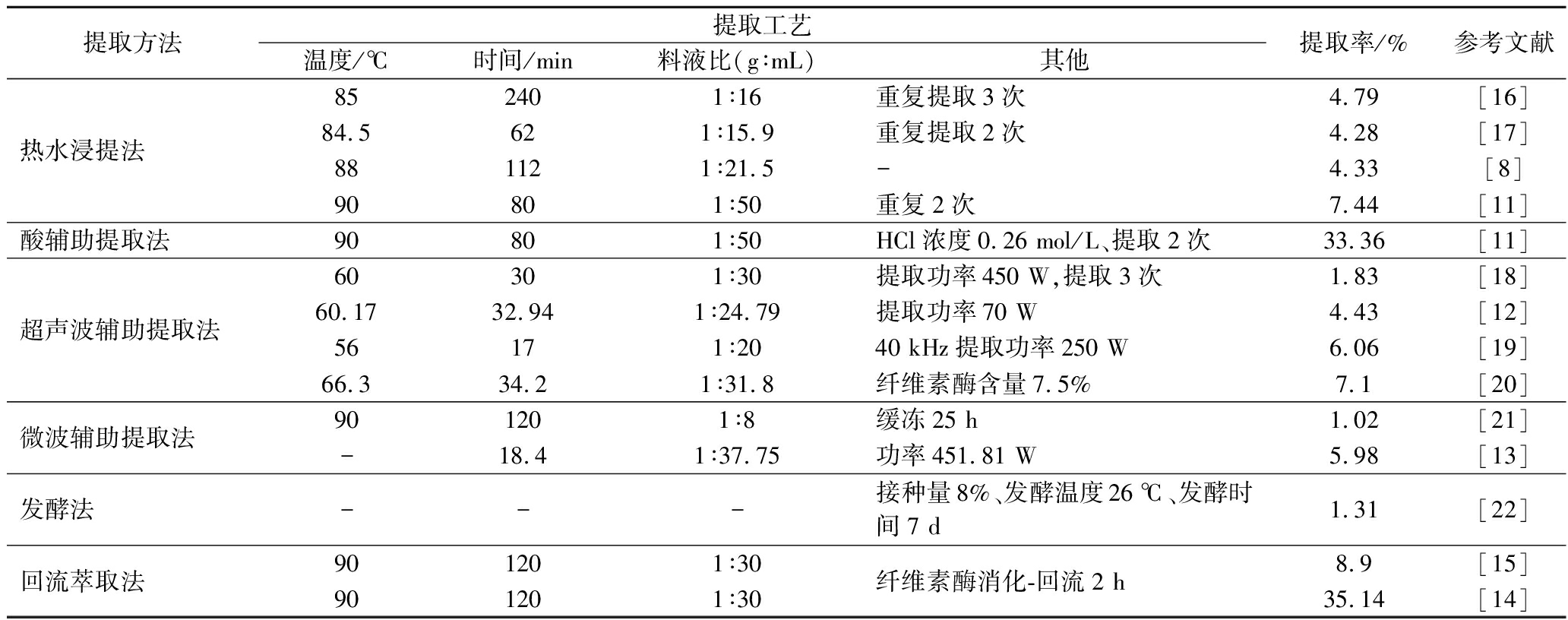
提取方法提取工艺温度/℃时间/min料液比(g∶mL)其他提取率/%参考文献热水浸提法852401∶16重复提取3次4.79[16]84.5621∶15.9重复提取2次4.28[17]881121∶21.5-4.33[8]90801∶50重复2次7.44[11]酸辅助提取法90801∶50HCl浓度0.26 mol/L、提取2次33.36[11]超声波辅助提取法60301∶30提取功率450 W,提取3次1.83[18]60.1732.941∶24.79提取功率70 W4.43[12]56171∶2040 kHz提取功率250 W6.06[19]66.334.21∶31.8纤维素酶含量7.5%7.1[20]微波辅助提取法901201∶8缓冻25 h1.02[21]-18.41∶37.75功率451.81 W5.98[13]发酵法---接种量8%、发酵温度26 ℃、发酵时间7 d1.31[22]回流萃取法901201∶30901201∶30纤维素酶消化-回流2 h8.9[15]35.14[14]
注:-表示无法获得数据,下同。
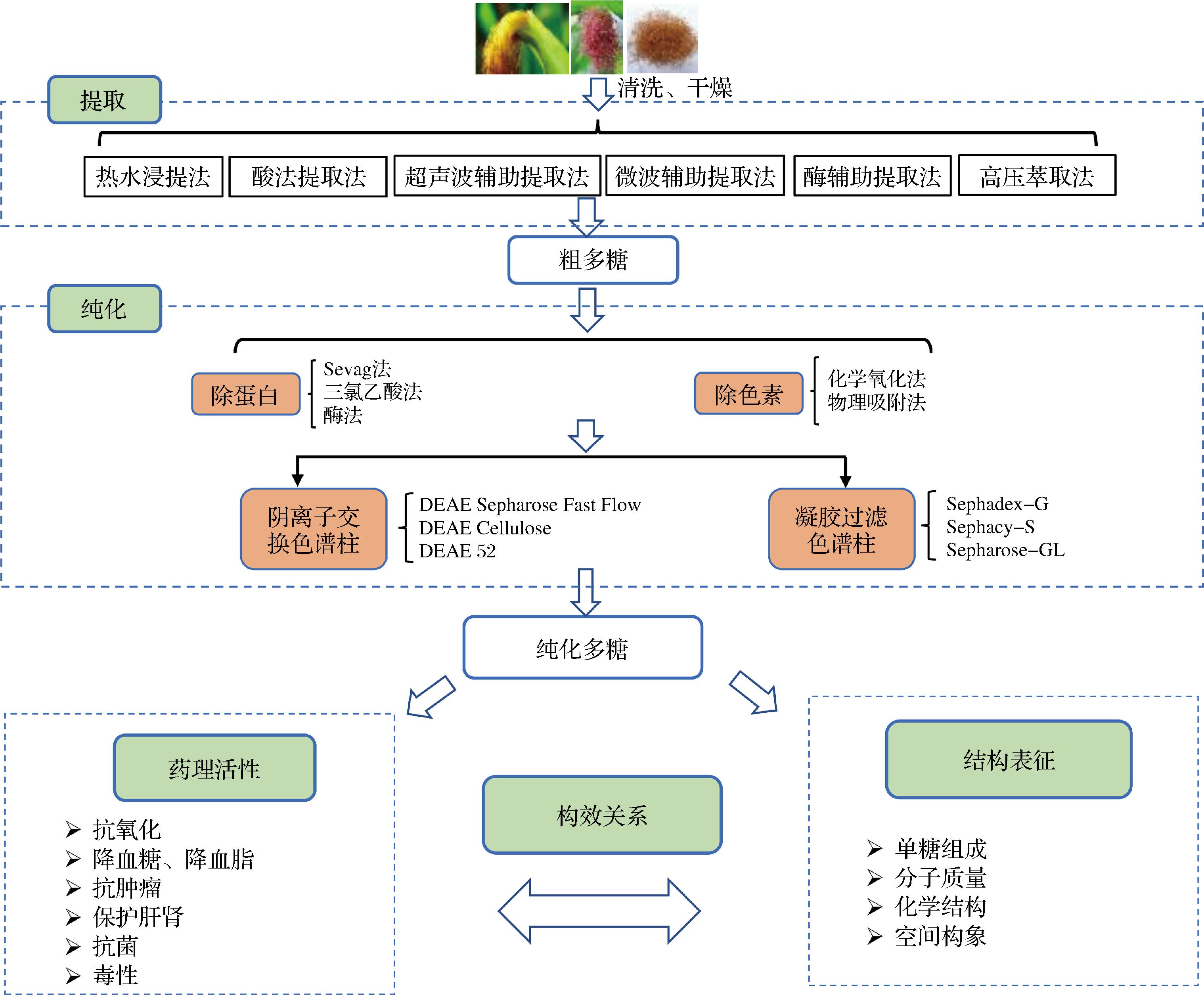
图1 玉米须多糖提取、纯化、结构特征及生物活性示意图
Fig.1 Schematic diagram of extraction, purification, structural characteristics, and biological activity of corn silk polysaccharides
通过以上方法获得的粗多糖一般含有蛋白质、色素、核酸等杂质,它们对多糖结构表征及生物活性的研究会造成一定的影响,需要对其进行初步纯化[23]。目前除蛋白方法有Sevag法、三氯乙酸法和酶法,一般需要重复多次才能达到去除效果,且不同种类多糖中的蛋白质含量和性质可能有所不同,需要根据具体情况调整沉淀剂的种类和用量。其中Sevag法是除蛋白最常用的方法,与其他方法相比,对多糖结构破坏较小,但多糖损失多[24]。色素一般通过物理吸附法和氧化法去除,在脱色过程中可能会损失部分多糖,其中玉米多糖中含有较多色素,对脱色剂的选择和用量需要精确控制,以避免CSP的降解。另外,为了进一步纯化粗多糖,一般会采用柱层析法、膜过滤法以及分步沉淀法,其中柱层析法是多糖分离纯化最常见的方法,其分为离子交换色谱法和凝胶过滤色谱法。例如通过DEAE-52和DEAE-Cellulose色谱柱分离出酸性糖和中性糖,然后根据分子质量范围使用Sephadex-G或Sephacy-S系列进一步纯化获得高纯度的多糖纯化组分,并研究结构和生物活性。
2 玉米须多糖结构表征
天然植物多糖结构表征主要包括多糖的单糖组成、分子质量、糖苷键的类型、位置和多糖重复结构单元。由于原料和提取方法的不同导致多糖结构存在差异,进而影响多糖的生物活性。因此需对其结构进行深入研究,探究玉米须多糖构效关系。目前多糖的结构主要通过甲基化分析、Smith降解、高碘酸盐氧化、红外光谱、紫外光谱、气相色谱、高效液相色谱、扫描电子显微镜和核磁共振等方法表征[25]。近年来,许多研究对不同提取纯化的CSP进行了不同程度的结构表征。表2全面总结了近年来CSP的结构特性和生物活性等相关信息。
表2 玉米须多糖的结构表征
Table 2 Structural characterization of polysaccharide from corn silk
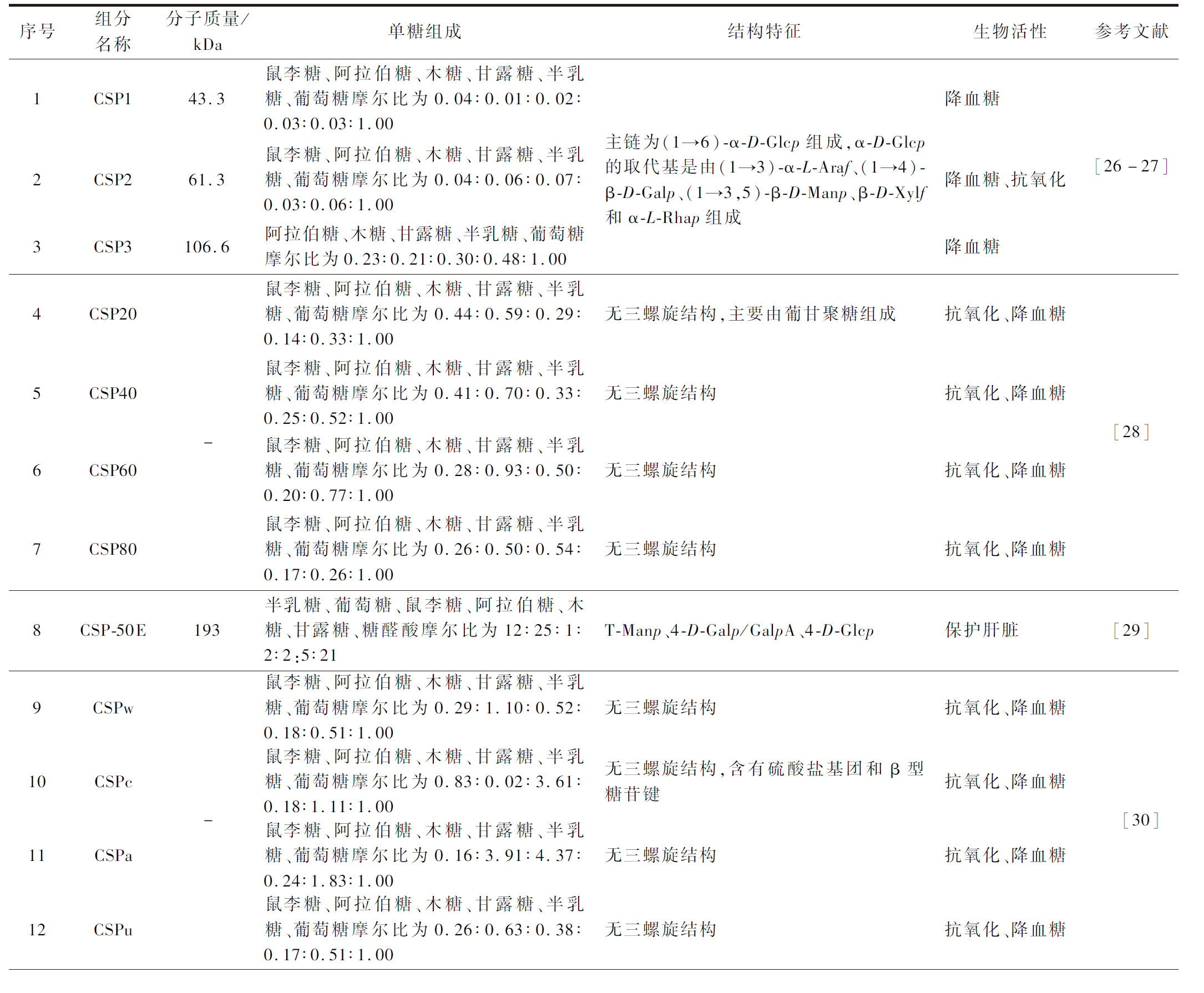
序号组分名称分子质量/kDa单糖组成结构特征生物活性参考文献1CSP143.3鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.04∶0.01∶0.02∶0.03∶0.03∶1.00降血糖2CSP261.3鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.04∶0.06∶0.07∶0.03∶0.06∶1.00主链为(1→6)-α-D-Glcp组成,α-D-Glcp的取代基是由(1→3)-α-L-Araf、(1→4)-β-D-Galp、(1→3,5)-β-D-Manp、β-D-Xylf和α-L-Rhap组成降血糖、抗氧化3CSP3106.6阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.23∶0.21∶0.30∶0.48∶1.00降血糖[26-27]4CSP20鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.44∶0.59∶0.29∶0.14∶0.33∶1.00无三螺旋结构,主要由葡甘聚糖组成抗氧化、降血糖5CSP40鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.41∶0.70∶0.33∶0.25∶0.52∶1.00无三螺旋结构抗氧化、降血糖6CSP60-鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.28∶0.93∶0.50∶0.20∶0.77∶1.00无三螺旋结构抗氧化、降血糖7CSP80鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.26∶0.50∶0.54∶0.17∶0.26∶1.00无三螺旋结构抗氧化、降血糖[28]8CSP-50E193半乳糖、葡萄糖、鼠李糖、阿拉伯糖、木糖、甘露糖、糖醛酸摩尔比为12∶25∶1∶2∶2:5∶21T-Manp、4-D-Galp/GalpA、4-D-Glcp保护肝脏[29]9CSPw鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.29∶1.10∶0.52∶0.18∶0.51∶1.00无三螺旋结构抗氧化、降血糖10CSPc-鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.83∶0.02∶3.61∶0.18∶1.11∶1.00无三螺旋结构,含有硫酸盐基团和β型糖苷键抗氧化、降血糖11CSPa鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.16∶3.91∶4.37∶0.24∶1.83∶1.00无三螺旋结构抗氧化、降血糖12CSPu鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.26∶0.63∶0.38∶0.17∶0.51∶1.00无三螺旋结构抗氧化、降血糖[30]
续表2
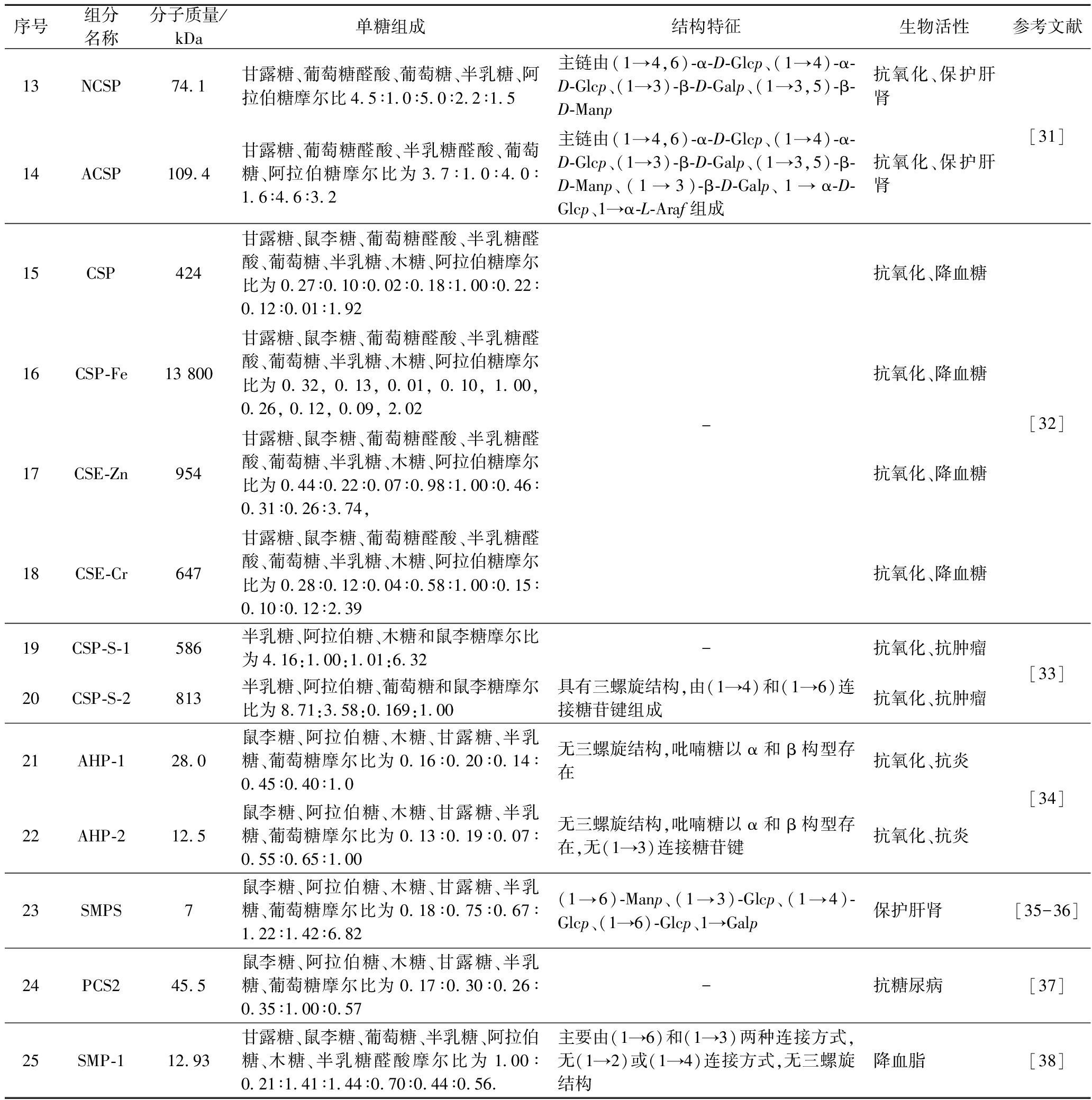
序号组分名称分子质量/kDa单糖组成结构特征生物活性参考文献13NCSP74.1甘露糖、葡萄糖醛酸、葡萄糖、半乳糖、阿拉伯糖摩尔比4.5∶1.0∶5.0∶2.2∶1.5主链由(1→4,6)-α-D-Glcp、(1→4)-α-D-Glcp、(1→3)-β-D-Galp、(1→3,5)-β-D-Manp抗氧化、保护肝肾14ACSP109.4甘露糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、阿拉伯糖摩尔比为3.7∶1.0∶4.0∶1.6∶4.6∶3.2主链由(1→4,6)-α-D-Glcp、(1→4)-α-D-Glcp、(1→3)-β-D-Galp、(1→3,5)-β-D-Manp、(1→3)-β-D-Galp、1→α-D-Glcp、1→α-L-Araf组成抗氧化、保护肝肾[31]15CSP424甘露糖、鼠李糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、半乳糖、木糖、阿拉伯糖摩尔比为0.27∶0.10∶0.02∶0.18∶1.00∶0.22∶0.12∶0.01∶1.92抗氧化、降血糖16CSP-Fe13 800甘露糖、鼠李糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、半乳糖、木糖、阿拉伯糖摩尔比为0.32, 0.13, 0.01, 0.10, 1.00, 0.26, 0.12, 0.09, 2.02-抗氧化、降血糖17CSE-Zn954甘露糖、鼠李糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、半乳糖、木糖、阿拉伯糖摩尔比为0.44∶0.22∶0.07∶0.98∶1.00∶0.46∶0.31∶0.26∶3.74,抗氧化、降血糖18CSE-Cr647甘露糖、鼠李糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、半乳糖、木糖、阿拉伯糖摩尔比为0.28∶0.12∶0.04∶0.58∶1.00∶0.15∶0.10∶0.12∶2.39抗氧化、降血糖[32]19CSP-S-1586半乳糖、阿拉伯糖、木糖和鼠李糖摩尔比为4.16:1.00:1.01:6.32-抗氧化、抗肿瘤20CSP-S-2813半乳糖、阿拉伯糖、葡萄糖和鼠李糖摩尔比为8.71:3.58:0.169:1.00具有三螺旋结构,由(1→4)和(1→6)连接糖苷键组成抗氧化、抗肿瘤[33]21AHP-128.0鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.16∶0.20∶0.14∶0.45∶0.40∶1.0无三螺旋结构,吡喃糖以α和β构型存在抗氧化、抗炎22AHP-212.5鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.13∶0.19∶0.07∶0.55∶0.65∶1.00无三螺旋结构,吡喃糖以α和β构型存在,无(1→3)连接糖苷键抗氧化、抗炎[34]23SMPS7鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.18∶0.75∶0.67∶1.22∶1.42∶6.82(1→6)-Manp、(1→3)-Glcp、(1→4)-Glcp、(1→6)-Glcp、1→Galp保护肝肾[35-36]24PCS245.5鼠李糖、阿拉伯糖、木糖、甘露糖、半乳糖、葡萄糖摩尔比为0.17∶0.30∶0.26∶0.35∶1.00∶0.57-抗糖尿病[37]25SMP-112.93甘露糖、鼠李糖、葡萄糖、半乳糖、阿拉伯糖、木糖、半乳糖醛酸摩尔比为1.00∶0.21∶1.41∶1.44∶0.70∶0.44∶0.56.主要由(1→6)和(1→3)两种连接方式,无(1→2)或(1→4)连接方式,无三螺旋结构降血脂[38]
2.1 分子质量
分子质量是多糖化学性质的关键参数,其方法主要包括液相、气相、凝胶色谱法等。如表2所示,CSP分子质量分别较广,主要分布在7~813 kDa之间或与其他物质复合分子质量>424 kDa。如GUO等[26]选择挤压法和酶消化法对玉米须进行预处理,热水法提取粗多糖。采用DEAE柱层析纯化得到CSP1、CSP2和CSP3三种多糖组分,其分子质量分别为13.3、61.3和106.6 kDa。LI等[33]从玉米丝中提取多糖,采用DEAE-52和Sephadex G-150分离纯化得到分子质量分别为586和813 kDa的两种组分多糖(CSP-S-1和CSP-S-2)。JIA等[34]采用酸法水解玉米多糖,并通过Sephadex G-25色谱柱分离纯化玉米水解多糖得到分子质量为28.0和12.5 kDa两种多糖AHP-1和AHP-2。此外,JIA等[32]研究金属离子与CSP络合对多糖结构和活性的影响。结果表明CSP与Fe3+、Zn2+和Cr3+络合多糖分子质量由424 kDa增加到13 800、954、647 kDa。综上所述,不同的提取纯化条件对CSP分子质量产生显著的影响。
2.2 单糖组成
单糖组成分析是多糖结构解析的基础,能够特异性地反映多糖的结构特征,尤其是单糖的组成和比例。多糖通过酸水解破坏多糖的糖苷键,然后进行中和、过滤、衍生化后通过气相色谱、液相色谱、质谱等技术确定单糖组成。由表2可知,CSP主要由两种或两种以上单糖(如甘露糖、半乳糖、阿拉伯糖、葡萄糖、鼠李糖以及半乳糖醛酸)组成。ZHAO等[39]从玉米须中分离纯化出抗疲劳活性多糖PCS,对其结构信息进行了表征,结果表明PCS多糖含量为58.6%,由鼠李糖、阿拉伯糖、木糖、甘露糖、葡萄糖、半乳糖组成,摩尔比为0.17∶0.30∶0.26∶0.35∶1.00∶0.57。PAN等[37]从玉米须中分离出多糖组分PCS2,结果表明PCS2由半乳糖、甘露糖、葡萄糖、木糖、阿拉伯糖和鼠李糖组成,摩尔比为1.00∶0.67∶0.63∶0.42∶0.16∶0.08。DENG等[38]采用水提醇沉法从玉米须中得到水溶性多糖-1(stigma maydis polysaccharide-1,SMP-1),高效凝胶渗透色谱显示其呈对称单峰,主要由甘露糖、鼠李糖、葡萄糖、半乳糖、阿拉伯糖、木糖和半乳糖醛酸以摩尔比1.00∶0.21∶1.41∶1.44∶0.70∶0.44∶0.56组成。ZHANG等[29]从玉米丝中分离出一种具有保肝活性的酸性多糖CSP-50E,单糖分析结果表明其主要由半乳糖、葡萄糖、鼠李糖、阿拉伯糖、木糖、甘露糖和醛酸组成,摩尔比为12∶25∶1∶2∶2∶5∶21。综上所述,CSP之间单糖组成和摩尔比的差异主要由原料、分离和纯化方法的差异造成。
2.3 一级结构
目前关于CSP化学结构和空间构象信息较少,且多糖结构表征主要集中在多糖的一级结构,通常采用红外光谱、核磁共振、扫描电镜、甲基化分析和气质联用等方法对其结构进行表征[23]。GUO等[26-27]对CSP2进行了进一步的结构表征,CSP2的一维和二维核磁共振结构分析表明,CSP2主链由(1→6)-α-D-Glcp组成,α-D-Glcp的取代基是由(1→3)-α-L-Araf、(1→4)-β-D-Galp、(1→3,5)-β-D-Manp、β-D-Xylf和α-L-Rhaf组成。WANG等[31]从玉米须中分离出两种高活性多糖分别为中性多糖(neutral polysaccharides,NCSP)和酸性多糖(acid polysaccharides,ACSP),核磁共振结果分析表明,NCSP主链由(1→4,6)-α-D-Glcp、(1→4)-α-D-Glcp、(1→3)-β-D-Galp、(1→3,5)-β-D-Manp组成;ACSP主链由(1→4,6)-α-D-Glcp、(1→4)-α-D-Glcp、(1→3)-β-D-Galp、(1→3,5)-β-D-Manp、(1→3)-β-D-Galp、1→α-D-Glcp、1→α-L-Araf组成,且NCSP在抗高尿酸血症中表现出更高的活性,可以改善肾脏损伤,图2为NCSP的预测结构。与此同时,ZHANG等[29]从玉米须中分离出一种具有保肝活性的酸性多糖CSP-50E,甲基化结构分析表明CSP-50E主要由T-Manp、4-D-Galp/GalpA和4-D-Glcp组成。王恒禹等[35]从玉米须中分离出一种保护肾脏的多糖组分SMP,结构分析表明其主要由甘露糖、半乳糖、葡萄糖的重复单元构成,如(1→6)-Manp、(1→3)-Glcp、(1→4)-Glcp、(1→6)-Glcp、1→Galp。此外,DENG等[38]研究表明,SMP-1残基主要通过(1→6)和(1→3)键连接,摩尔比为1∶1.47,且无(1→2)或(1→4)连接方式,无三螺旋结构。综上所述,关于CSP结构研究不够深入,主要停留在单糖组成以及糖苷键的连接方式,后续可对不同分离纯化方式、不同来源的CSP结构进行系统的研究,对其构象及高级结构进行深入研究,为研究多糖构效关系奠定基础。
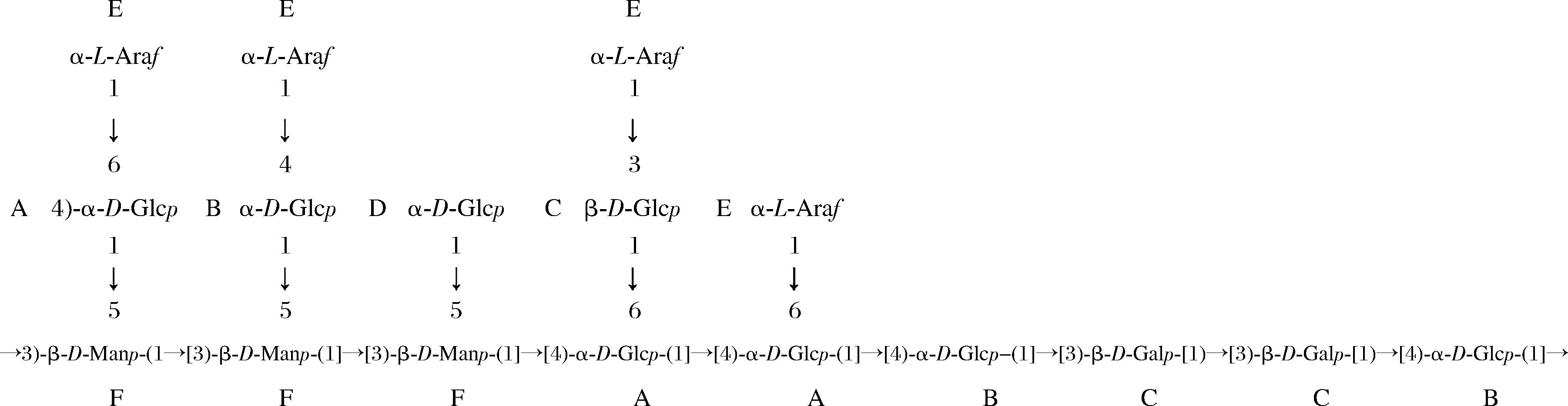
图2 NCSP[31]的预测结构
Fig.2 The predicted structure of NCSP[31]
3 CSP生物活性
植物多糖是一种强大的药理工具,具有显著的治疗潜力。从植物中提取的多糖被认为是关系到人体营养和健康的主要活性成分。近年来,部分专家学者对CSP进行探索,发现其具有多种生物和药理活性,包括抗氧化、降血糖、降血脂、抗肿瘤、免疫调节和多种其他活性作用。本节总结了CSP的生物学和药理活性及其潜在的作用机制。
3.1 抗氧化
体内氧化应激和自由基失衡是导致老化、炎症和癌症等疾病的主要因素。多糖的体外抗氧化能力通常通过各种自由基测试评估,体内抗氧化能力主要包括测定多种抗氧化酶的活性和水平[40]。ZHANG等[8]通过响应面优化法从玉米须中提取具有抗氧化活性的多糖CSP。体外抗氧化实验表明CSP具有较强的超氧阴离子自由基、DPPH自由基和羟自由基清除能力,且呈剂量依赖性;体内研究表明,CSP能够提高超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)活性以及总抗氧化能力(total antioxidant capacity,T-AOC)水平,降低丙二醛(malondialdehyde,MDA)水平,从而改善小鼠的氧化反应。CHEN等[9]通过超声降解CSP得到不同分子质量多糖组分,其中CSP3对DPPH、ABTS和羟基自由基表现出良好的抗氧化活性,且能够增加人肾近曲小管细胞(human kidney 2,HK-2)的活力并降低细胞中的活性氧(reactive oxygen species,ROS)水平。此外,JIA等[34]从玉米须中分离出AHP-1和AHP-2两个多糖组分,体外抗氧化实验表明,AHP-2具有较强的抗氧化能力,由于AHP-2具有较小的分子质量,相同浓度下,分子质量越低,自由基就越多,提供的供体就越多。且在细胞实验中,AHP-2能够降低大鼠小肠隐窝上皮细胞(intestinal epithelial cell 6,IEC-6)的ROS水平,减少氧化应激损伤诱导的细胞凋亡。
3.2 降血糖、降血脂
在研究CSP对非胰岛素依赖型糖尿病患者餐后血糖的影响时,发现其可以抑制小肠中α-葡萄糖苷酶活性,显著降低餐后血糖[41]。PAN等[37]从玉米须中分离出具有抗糖尿病的多糖组分PCS2。体外研究表明PCS2具有明显的α-淀粉酶抑制活性;体内研究表明PCS2能不同程度降低小鼠血清胰岛素水平,减轻胰岛素抵抗,促进原糖合成。JIA等[28]研究发现CSP可以与α-葡萄糖苷酶结合形成稳定的复合物,从而抑制α-葡萄糖苷酶活性达到降血糖作用。如CSP80能够引起α-葡萄糖苷酶的空间构象转变,从而抑制α-葡萄糖苷酶活性。此外,CSP与金属离子形成的络合物也能够抑制α-葡萄糖苷酶活性,从而起到降血糖作用[32]。DENG等[38]经过分离纯化CSP得到具有良好降血脂活性的多糖组分SMP-1。研究表明SMP-1对高脂血症小鼠表现出良好的改善作用,显著降低了高脂血症小鼠的总胆固醇、甘油三酯和低密度脂蛋白胆固醇水平,并适度增加了高密度脂蛋白胆固醇水平。且SMP-1喂食剂量达到300 mg/kg以上,可显著减少高脂血症小鼠肝脏中的脂肪积累。此外,赵绮等[7]通过超声辅助H2O2-维生素C降解CSP,得到不同分子质量的多糖组分。其中,CSP-3分子质量为5.9 kDa的多糖组分具有较强的降脂能力,研究发现分子质量越小,其降血脂活性越强。通过研究CSP-3的降脂机制发现,其能够提高脂蛋白脂肪酶(lipoprteinlipase,LPL)和肝脂酶(hepaticlipase,HL)的活性,从而降低血清总胆固醇(total cholesterol,TC)、甘油三脂(triglyceride,TG)和低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)水平,升高高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,LDL-C)水平,调节血脂平衡。
3.3 抗肿瘤
目前癌症已经成为人类全球公共卫生的一大挑战,尽管对癌症的诊断和治疗取得了巨大进展,但长期使用化学药物干预会对机体产生巨大损伤。研究表明,天然植物多糖具有低毒性及良好的抗肿瘤活性,越来越受到人们重视[42]。海拉细胞(HeLa)引起的人类宫颈癌是女性最常见的恶性肿瘤之一,LI等[33]采用DEAE-52和Sephadex G-150层析柱从玉米须中分离出分子质量不同的多糖组分。研究表明CSP-S-2具有较强的体外抗氧化能力及抑制HeLa细胞的增殖,且呈剂量依赖性。此外,YANG等[43]探究CSP对小鼠肝癌细胞(Hepatoma-22,H22)生长和免疫功能的影响。结果表明,CSP不仅能抑制肿瘤生长,还能增加小鼠胸腺指数和脾脏指数促进血清细胞因子产生(如IL-22、IL-6和TNF-α)以及延长H22肝癌荷瘤小鼠生存时间。吴先闯等[44]也证实了CSP对H22实体瘤小鼠具有显著的抑瘤作用,抑制率达到34.78%。综上CSP可以提升H22荷瘤小鼠的免疫功能,增强其抗肿瘤活性。与此同时,TAO等[45]进一步探讨了玉米须多糖S1的体内外抗胰腺癌活性。研究表明,S1能够显著抑制胰腺癌细胞(PANC-1、SW1990和BxPC-3)的细胞活力,并且S1对BxPC-3具有显着的细胞毒性。进一步研究表明,S1可能通过阻断表皮生长因子受体/磷脂酰肌醇3-激酶/蛋白激酶B/环磷腺苷效应元件结合蛋白信号通路,抑制胰腺癌细胞迁移和侵袭,诱导细胞凋亡,并将细胞周期进程阻滞在S期。
3.4 保护肝肾
ZHANG等[29]通过体外细胞模拟探究玉米丝酸性多糖CSP-50E的保肝活性。体外实验表明,CSP-50E能够显著降低模型IL-6、TNF-α含量、门冬氨酸氨基转移酶(aspartate transaminase,AST)和谷氨酸氨基转移酶(alanine aminotransferase,ALT)活性以保护乙醇诱导的肝细胞损伤。CSP-50E通过胱天蛋白酶级联和介导线粒体凋亡途径表现出酒精诱导的保肝活性,且护肝活性与糖醛酸含量和多糖结构有关。黄小强等[46]探究玉米须对缓解脂多糖诱导的小鼠肺损伤,结果表明,与正常组小鼠相比,喂食CSP的小鼠血清中TNF-α和IL-1β水平、肺组织中髓过氧化物酶(myeloperoxidase,MPO)活性均显著性降低。舒涛等[47]研究CSP对非酒精性脂肪肝的影响,结果表明,CSP能够显著提高肝脏miR-146a的基因表达,同时下调NADPH氧化酶4(NADPH oxidase 4,NOX4)表达及ROS水平。CSP抑制非酒精性脂肪肝的发生发展,可能与其对miR-146a/NOX4/ROS通路的调控有关。此外,曲萌等[48]探究玉米须来源的SMP在高糖刺激下对大鼠肾小球系膜细胞HBZY-1的影响。SMP能够下调炎症因子单核细胞趋化因子-1(monocytechemoattractantprotein-1,MCP-1)和IL-6的表达,并抑制高糖诱导的HBZY-1细胞增殖,从而延缓糖尿病肾病的发病。温宪春等[49]探究CSP对2型糖尿病肾病大鼠肾组织TGF-βl/Smad信号通路的影响。CSP能够降低大鼠肾组织中TGF-β1和纤维连接蛋白的表达量,进而对肾脏具有一定的保护作用。梁衍锋等[50]进一步研究CSP对糖尿病肾病的影响。CSP可能通过影响胰岛素样生长因子1受体(insulin-like growth factor 1,IGF-1R)活性和生长因子受体结合蛋白(growth factor receptor-bound protein,Grb)表达,从而达到改善链脲菌素诱导的小鼠糖尿病肾病及保护肾脏作用。
3.5 其他生物活性
徐彬等[51]研究新鲜CSP的抗菌作用。结果表明,CSP对金黄色葡萄球菌的最小抑菌浓度和最小杀菌浓度分别为3.13 mg/mL和1.56 mg/mL,对大肠杆菌的最小抑菌浓度和最小杀菌浓度均为6.25 mg/mL。魏浩[52]研究了CSP对老年痴呆症大鼠学习记忆能力的影响。CSP每天400 mg/kg灌胃,可显著改善阿尔茨海默病小鼠在Morris水迷宫中的表现。其作用机理可能是CSP能够增高大鼠脑组织中乙酰胆碱转移酶含量,降低胆碱酯酶含量,导致乙酰胆碱含量增加。
4 CSP毒性研究
到目前为止,已经有大量的研究揭示了CSP的结构和多种生物活性,但对CSP毒性的研究较少。ZHAO等[39]对CSP急性毒性进行了研究。分别对小鼠给予不同剂量浓度的CSP,在实验过程中均未发现动物死亡和行为异常,且食物摄入量与体重增加量以及重要器官相对重量均在正常水平,无显著差异。CSP给药后各项生化指标未见异常,这些结果表明CSP安全可靠,对小鼠无明显毒性。此外,还需临床试验对CSP毒理学进行验证。
5 总结与展望
CSP具有广泛生物活性,在保健食品和医药领域有巨大应用潜力。本文总结了CSP的提取工艺与方法、结构表征、生物活性及毒理学等方面的研究。目前CSP的研究已取得很大的进展,但仍有许多挑战亟需解决。首先,大量实验研究表明多糖结构和生物活性受到提取纯化方法影响较大,因此提取方法的选择应适当。其次,目前对CSP的结构研究主要集中在分子质量、单糖组成等一级结构分析上,还需运用高新技术对CSP结构进行完整解析,对更清晰结构的研究是进一步推动CSP发展的研究方向。最后,关于CSP构效关系的探索较少。因此,结构分析和深层活性机制验证是CSP开发中需要解决的重要问题。
[1] 班歆甜, 柴军红, 姜浩, 等.玉米须多糖的化学结构及药理活性研究进展[J].中医药学报, 2022, 50(4):96-102.BAN X T, CHAI J H, JIANG H, et al.Research progress on chemical structure and pharmacological activity of stigma maydis polysaccharides[J].Acta Chinese Medicine and Pharmacology, 2022, 50(4):96-102.
[2] 何子涵, 吴星霖, 向志宇, 等.玉米须生物活性成分、功效与提取方法的研究进展[J].北方农业学报, 2023, 51(4):96-104.HE Z H, WU X L, XIANG Z Y, et al.Research progress on corn silk bioactive components, efficacy and extraction method[J].Journal of Northern Agriculture, 2023, 51(4):96-104.
[3] 高云霜, 王俊雪, 牛佳楠, 等.玉米须活性成分及药理作用研究进展[J].人参研究, 2023, 35(4):59-61.GAO Y S, WANG J X, NIU J N, et al.Research progress on active ingredients and pharmacological effects of corn silk[J].Ginseng Research, 2023, 35(4):59-61.
[4] GULATI A, SINGH J, RASANE P, et al.Anti-cancerous effect of corn silk:A critical review on its mechanism of action and safety evaluation[J].3 Biotech, 2023, 13(7):246.
[5] AL-OQAIL M M, AL-SHEDDI E S, FARSHORI N N, et al.Corn silk (Zea mays l.) induced apoptosis in human breast cancer (MCF-7) cells via the ROS-mediated mitochondrial pathway[J].Oxidative Medicine and Cellular Longevity,2019:9789241.
[6] 刘东琦, 王喜庆, 石俊姣, 等.玉米须多糖生物活性与应用研究进展[J].吉林农业科技学院学报, 2023, 32(1):18-22.LIU D Q, WANG X Q, SHI J J, et al.Research progress on biological activity and application of corn stigma polysaccharide[J].Journal of Jilin Agricultural Science and Technology University, 2023, 32(1):18-22.
[7] 赵绮, 赵则月, 关颖, 等.不同分子量玉米须多糖降血脂比较及机制研究[J].中国食品添加剂, 2023, 34(5):241-248.ZHAO Q, ZHAO Z Y, GUAN Y, et al.Effects of corn silk polysaccharides with different molecular weight on hypolipidemic and its mechanism[J].China Food Additives, 2023, 34(5):241-248.
[8] ZHANG L, YANG Y, WANG Z Y.Extraction optimization of polysaccharides from corn silk and their antioxidant activities in vitro and in vivo[J].Frontiers in Pharmacology, 2021, 12:738150.
[9] CHEN J Y, SUN X Y, OUYANG J M.Modulation of calcium oxalate crystal growth and protection from oxidatively damaged renal epithelial cells of corn silk polysaccharides with different molecular weights[J].Oxidative Medicine and Cellular Longevity, 2020:6982948
[10] 刘东琦, 韩雪, 石俊姣, 等.玉米须多糖不同提取方法对体外活性的影响[J].农产品加工, 2021(7):36-38.LIU D Q, HAN X, SHI J J, et al.Effects of different extraction methods in vitro activity of polysaccharides from stigmata maydis[J].Farm Products Processing, 2021(7):36-38.
[11] 李亚平, 周鸿立.玉米须多糖酸提取工艺及其抗氧化活性的研究[J].粮食与油脂, 2020, 33(8):86-90.LI Y P, ZHOU H L.Acidic extraction and antioxidant activity of polysaccharides from Corn silk[J].Cereals &Oils, 2020, 33(8):86-90.
[12] 侯敏娜, 李永梅, 辛新.响应曲面法优化超声-辅助提取玉米须多糖的工艺研究[J].世界中医药, 2017, 12(8):1923-1926; 1932.HOU M N, LI Y M, XIN X.Optimization of ultrasonic assisted extraction of polysaccharides from corn silk by response surface methodology[J].World Chinese Medicine, 2017, 12(8):1923-1926; 1932.
[13] 陈珊珊, 宋冬晶, 葛鹏玲.玉米须多糖的微波-超声波协同提取工艺优化探究[J].食品安全导刊, 2021(15):142-145.CHEN S S, SONG D J, GE P L.Optimization of microwave ultrasonic collaborative extraction process for corn silk polysaccharides[J].China Food Safety Magazine, 2021(15):142-145.
[14] 王晴, 钱玉梅, 李红侠, 等.玉米须多糖高效提取工艺及生物活性研究[J].佳木斯大学学报(自然科学版), 2020, 38(2):110-113;163.WANG Q, QIAN Y M, LI H X, et al.Study on efficient extraction process for polysaccharides from corn silk and its biological activity[J].Journal of Jiamusi University (Natural Science Edition), 2020, 38(2):110-113;163.
[15] 李劭彤, 王婧怡, 康凯, 等.玉米须多糖提取及抗氧化性分析[J].中国食品工业, 2022(20):90-92;47.LI S T, WANG J Y, KANG K, et al.Extraction and antioxidant analysis of corn silk polysaccharides[J].China Food Industry, 2022(20):90-92;47.
[16] 金萍, 刘政, 于小磊.响应面法优化玉米须多糖提取工艺及抑菌效果的研究[J].食品工业, 2022, 43(8):97-102.JIN P, LIU Z, YU X L.Optimization of extraction process and antibacterial effect of corn whisker polysaccharide by response surface methodology[J].The Food Industry, 2022, 43(8):97-102.
[17] 陈燕萌, 招幸辰, 张鹏.响应面优化水提法提取玉米须多糖的工艺研究[J].山东化工, 2021, 50(11):49-52;57.CHEN Y M, ZHAO X C, ZHANG P.Study on the technology of extracting corn silk polysaccharide by response surface optimization water extraction method[J].Shandong Chemical Industry, 2021, 50(11):49-52;57.
[18] 宫春宇, 单佳明, 余世锋, 等.超声波提取玉米须多糖工艺及活性研究[J].粮食与油脂, 2020, 33(5):85-89.GONG C Y, SHAN J M, YU S F, et al.Study on ultrasonic extracting process and bioactivity of ploysaccharides from Stigma Maydis[J].Cereals &Oils, 2020, 33(5):85-89.
[19] PRAKASH MARAN J, MANIKANDAN S, THIRUGNANASAMBANDHAM K, et al.Box-Behnken design based statistical modeling for ultrasound-assisted extraction of corn silk polysaccharide[J].Carbohydrate Polymers, 2013, 92(1):604-611.
[20] CHEN S H, CHEN H X, TIAN J G, et al.Enzymolysis-ultrasonic assisted extraction, chemical characteristics and bioactivities of polysaccharides from corn silk[J].Carbohydrate Polymers, 2014, 101:332-341.
[21] 张琰, 宋金玉.缓冻协同微波辅助提取玉米须多糖工艺的研究[J].山西职工医学院学报, 2018, 28(5):79-80.ZHANG Y, SONG J Y.Study on the technology of delayed freezing and microwave assisted extraction of corn silk polysaccharides[J].Journal of Shanxi Medical College for Continuing Education, 2018, 28(5):79-80.
[22] 胡楠楠, 亓伟华, 尤丽新, 等.玉米须多糖发酵工艺优化及其抗氧化活性研究[J].中国酿造, 2022, 41(10):159-164.HU N N, QI W H, YOU L X, et al.Optimization of fermentation technology and antioxidant activity of Stigma maydis polysaccharide[J].China Brewing, 2022, 41(10):159-164.
[23] 郭建行, 贾颂华, 李博润, 等.红海藻多糖提取、分离纯化及生物活性研究进展[J].食品研究与开发, 2022, 43(16):216-224.GUO J H, JIA S H, LI B R, et al.Research progress on extraction, purification, and bioactivity of polysaccharides from red seaweed[J].Food Research and Development, 2022, 43(16):216-224.
[24] 周鸿立, 杨晓虹.玉米须多糖中蛋白质脱除的Sevag与酶法联用工艺优化[J].食品科学, 2011, 32(8):129-132.ZHOU H L, YANG X H.Removal of proteins from corn silk polysaccharide by A combined enzymatic-sevag method[J].Food Science, 2011, 32(8):129-132.
[25] 冀晓龙, 郭建行, 田静源, 等.植物多糖降解方法及降解产物特性研究进展[J].轻工学报, 2023, 38(3):55-62.JI X L, GUO J H, TIAN J Y, et al.Research progress on degradation methods and product properties of plant polysaccharides[J].Journal of Light Industry, 2023, 38(3):55-62.
[26] GUO Q W, MA Q Q, XUE Z H, et al.Studies on the binding characteristics of three polysaccharides with different molecular weight and flavonoids from corn silk (Maydis stigma)[J].Carbohydrate Polymers, 2018, 198:581-588.
[27] GUO Q W, XU L L, CHEN Y, et al.Structural characterization of corn silk polysaccharides and its effect in H2O2 induced oxidative damage in L6 skeletal muscle cells[J].Carbohydrate Polymers, 2019, 208:161-167.
[28] JIA Y N, XUE Z H, WANG Y J, et al.Chemical structure and inhibition on α-glucosidase of polysaccharides from corn silk by fractional precipitation[J].Carbohydrate Polymers, 2021, 252:117185.
[29] ZHANG Y, YAO L M, LIU Y F, et al.Acidic polysaccharide from corn silk:Structural &conformational properties and hepatoprotective activity[J].International Journal of Biological Macromolecules, 2023, 236:123851.
[30] JIA Y N, GAO X D, XUE Z H, et al.Characterization, antioxidant activities, and inhibition on α-glucosidase activity of corn silk polysaccharides obtained by different extraction methods[J].International Journal of Biological Macromolecules, 2020, 163:1640-1648.
[31] WANG X Z, YUAN L Y, BAO Z J, et al.Screening of uric acid-lowering active components of corn silk polysaccharide and its targeted improvement on renal excretory dysfunction in hyperuricemia mice[J].Journal of Functional Foods, 2021, 86:104698.
[32] JIA Y N, LI N N, WANG Q R, et al.Effect of Fe (III), Zn (II), and Cr (III) complexation on the physicochemical properties and bioactivities of corn silk polysaccharide[J].International Journal of Biological Macromolecules, 2021, 189:847-856.
[33] LI Y P, HU Z Y, WANG X X, et al.Characterization of a polysaccharide with antioxidant and anti-cervical cancer potentials from the corn silk cultivated in Jilin province[J].International Journal of Biological Macromolecules, 2020, 155:1105-1113.
[34] JIA Y N, WANG Y J, LI R L, et al.The structural characteristic of acidic-hydrolyzed corn silk polysaccharides and its protection on the H2O2-injured intestinal epithelial cells[J].Food Chemistry, 2021, 356:129691.
[35] 王恒禹, 罗云凤, 姜京华, 等.玉米须多糖的提取纯化及结构研究[J].首都师范大学学报(自然科学版), 2019, 40(1):44-49.WANG H Y, LUO Y F, JIANG J H, et al.Extraction, purification and structural characterization analysis of stigma maydis polysaccharide[J].Journal of Capital Normal University (Natural Science Edition), 2019, 40(1):44-49.
[36] WANG X Z, HUANG L Y, QI Y, et al.Nutritional intervention with acidic stigma maydis polysaccharide (ASMP-1) in membranous nephropathy:Targeting the PI3K/AKT/mTOR pathway[J].Food Bioscience, 2023, 56:103278.
[37] PAN Y X, WANG C, CHEN Z Q, et al.Physicochemical properties and antidiabetic effects of a polysaccharide from corn silk in high-fat diet and streptozotocin-induced diabetic mice[J].Carbohydrate Polymers, 2017, 164:370-378.
[38] DENG W W, YANG X, ZHU Y, et al.Structural characterization and hypolipidemic activities of purified stigma maydis polysaccharides[J].Food Science &Nutrition, 2019, 7(8):2674-2683.
[39] ZHAO H P, ZHANG Y, LIU Z, et al.Acute toxicity and anti-fatigue activity of polysaccharide-rich extract from corn silk[J].Biomedicine &Pharmacotherapy, 2017, 90:686-693.
[40] 周鸿立, 张硕, 胡乐安, 等.玉米须粗多糖体外抗氧化活性研究[J].食品研究与开发, 2015, 36(18):11-14.ZHOU H L, ZHANG S, HU L A, et al.Study on the in vitro antioxidant activity of corn silk crude polysaccharides[J].Food Research and Development, 2015, 36(18):11-14.
[41] 丁琳. 玉米须及其多糖降血糖、降血脂作用研究[D].哈尔滨:黑龙江中医药大学, 2016.DING L.Study on the hypoglycemic and lipid-lowering effects of corn silk and its polysaccharides[D].Harbin:Heilongjiang University of Chinese Medicine, 2016.
[42] 韩宇鹏, 林佩莹, 崔保威, 等.牛蒡多糖类膳食纤维制备、结构特性与生理学活性研究进展[J].食品与发酵工业, 2023, 49(12):345-351.HAN Y P, LIN P Y, CUI B W, et al.Research progress on preparation, structure characterization, and physiological activity of Arctium lappa polysaccharide dietary fiber[J].Food and Fermentation Industries, 2023, 49(12):345-351.
[43] YANG J Y, LI X, XUE Y, et al.Anti-hepatoma activity and mechanism of corn silk polysaccharides in H22 tumor-bearing mice[J].International Journal of Biological Macromolecules, 2014, 64:276-280.
[44] 吴先闯, 杜钢军, 郝海军, 等.玉米须多糖对H22荷瘤小鼠的肿瘤抑制作用及其对小鼠免疫功能的影响[J].华西药学杂志, 2015, 30(1):26-29.WU X C, DU G J, HAO H J, et al.Effects of polysaccharides extracts from corn silk on the growth of H22 liver cancer and immune function[J].West China JOurnal of Pharmaceutical Sciences, 2015, 30(1):26-29.
[45] TAO H, CHEN X, DU Z Y, et al.Corn silk crude polysaccharide exerts anti-pancreatic cancer activity by blocking the EGFR/PI3K/AKT/CREB signaling pathway[J].Food &Function, 2020, 11(8):6961-6970.
[46] 黄小强, 黄涛, 王丽, 等.玉米须缓解脂多糖诱导的小鼠急性肺损伤[J].山东化工, 2020, 49(16):8-10.HUANG X Q, HUANG T, WANG L, et al.Corn silk alleviates lipopolysaccharide induced acute lung injury in mice[J].Shandong Chemical Industry, 2020, 49(16):8-10.
[47] 舒涛, 王浩然, 李恩丞, 等.玉米须多糖对非酒精性脂肪肝大鼠肝脏miR-146a/NOX4/ROS通路的影响[J].黑龙江医药科学, 2020, 43(4):10-12.SHU T, WANG H R, LI E C, et al.The effect of corn silk polysaccharides on the miR-146a/NOX4/ROS pathway in the liver of non-alcoholic fatty liver rats[J].Heilongjiang Medicine and Pharmacy, 2020, 43(4):10-12.
[48] 曲萌, 侯勤龙, 翁诗雅, 等.玉米须多糖对高糖诱导的肾小球系膜细胞增殖及炎症因子表达的影响[J].北华大学学报(自然科学版), 2020, 21(4):461-465.QU M, HOU Q L, WENG S Y, et al.Effects of stigma maydis polysaccharide on high glucose-induced proliferation of mesangium cells and expression of inflammatory factors[J].Journal of Beihua University (Natural Science), 2020, 21(4):461-465.
[49] 温宪春, 徐磊, 夏美莹, 等.玉米须水提物对2型糖尿病肾病大鼠转化生长因子-β1和纤维连接蛋白表达的影响[J].中国现代医学杂志, 2015, 25(13):8-12.WEN X C, XU L, XIA M Y, et al.Effect of aqueous extract from stigma maydis on expressions of TGF-β1 and FN in renal lesion of type 2 diabetic nephropathy rats[J].China Journal of Modern Medicine, 2015, 25(13):8-12.
[50] 梁衍锋, 张东东, 马小茹, 等.玉米须多糖对糖尿病肾病小鼠IGF-1R和Grb10表达的影响[J].黑龙江医药科学, 2019, 42(2):6-8.LIANG Y F, ZHANG D D, MA X R, et al.Effects of corn stigma polysaccharide on the expressions of IGF-1R and Grb10 in mouse with diabetes and nephropathy[J].Heilongjiang Medicine and Pharmacy, 2019, 42(2):6-8.
[51] 徐彬, 连帅, 袁建彬, 等.新鲜玉米须多糖提取工艺及体外抗菌、抗氧化活性研究[J].饲料研究, 2018, 41(5):48-53.XU B, LIAN S, YUAN J B, et al.Extraction process and in vitro antibacterial and antioxidant activities of fresh corn silk polysaccharides[J].Feed Research, 2018, 41(5):48-53.
[52] 魏浩. 玉米须多糖对老年痴呆症大鼠学习记忆能力的影响及机制[J].中医临床研究, 2022, 14(34):33-35.WEI H.Effects and mechanism of corn silk polysaccharide on learning and memory ability of senile dementia rats[J].Clinical Journal of Chinese Medicine, 2022, 14(34):33-35.