蛋白质和多糖是食品中重要的生物大分子,在乳液体系中,蛋白质通常以其优异的乳化性能而闻名,而多糖由于其强亲水性而经常用作增稠剂或稳定剂[1]。大量研究表明,用多糖-蛋白质共价复合物制备乳液会诱导分子间相互作用(静电相互作用、疏水相互作用以及氢键等),从而有利于增强乳液的稳定性[2]。然而,由于多糖及蛋白质的种类繁多且结构复杂,对多糖与蛋白质基于乳化特性构效机制的研究仍有待进一步深入。
大豆分离蛋白(soy protein isolate,SPI)是最常见的蛋白产品之一,与动物蛋白相比,SPI因其营养价值高、成本低而受到广泛关注。SPI可作为乳化剂制备具有良好扩散和吸附能力的水包油乳液,以稳定油水界面;其在油水界面具有良好的吸附能力,并通过较厚的保护层降低了界面张力[3]。尽管天然SPI表现出优异的功能特性,但由于对温度、pH和离子强度等环境条件高度敏感,严重限制其在食品工业中的应用[4]。因此,大量研究聚焦于选择合适的方式来增强SPI稳定性。
研究表明添加多糖能显著提高SPI乳液的稳定性和功能性。茄替胶(gum ghatti,GG)是一种从宽叶树上渗出的树胶,也被称为印度树胶,具有较高的溶解度[5],其乳化性也优于阿拉伯树胶(gum arabic,GA)。溶液中的GG浓度仅为GA的25%时,即可以有效地产生稳定乳液[6]。因此,GG可以应用于替代GA等其他商用树胶,特别是在难以稳定的非常规乳液中应用前景更为广阔。但目前,GG与蛋白的相互作用机理尚未明确,严重限制了其在食品中的应用。综上所述,本文在详细解析GG及其改性后的分子结构的基础上,通过美拉德反应(maillard reaction,MR)制备GG-SPI共价复合物,阐明其结构与乳化功能之间的作用机制。
1 材料与方法
1.1 材料与试剂
GG,印度新德里水胶体种植基地;大豆分离蛋白(纯度≥90%),北京索莱宝生物有限公司;所有其他化学试剂,除非另有说明,均为分析纯,天津江天化学科技有限公司。
1.2 仪器与设备
1-14离心机,长沙高新技术产业开发区;Alpha 2-4 LD plus快速冷冻干燥机,德国CHRIST公司;IS50傅里叶变换红外光谱仪,美国赛默飞公司;BT-9300H全自动激光粒度分析仪,丹东百特仪器有限公司;LC-20A高效凝胶排阻色谱仪,岛津公司;zeta电位分析仪,英国马尔文仪器有限公司;AH-BASICI高压均质机,ATS工业系统有限公司;ICS-5000+离子色谱仪,美国Thermo Scientific公司。
1.3 实验方法
1.3.1 GG的酸水解
配制质量分数为1%的GG溶液,分别加入三氟乙酸(trifluoroacetic acid,TFA)使溶液中TFA终浓度为0.05、0.075、0.1 mol/L,加热至100 ℃后水解20、60、120 min。水解完成后将样品溶液调pH至中性,透析72 h后冷冻干燥,根据高效凝胶排阻色谱(high performance size exclusion chromatography,HPSEC)结果选择分子质量具有明显差异性的样品,命名为GGA1(0.05 mol/L-20 min,484.9 kDa)、GGA2(0.05 mol/L-60 min,393.3 kDa)、GGA3(0.05 mol/L-120 min,294.3 kDa)、GGA4(0.075 mol/L-120 min,73.5 kDa)、GGA5(0.1 mol/L-20 min,43.1 kDa)。
1.3.2 改性GG的结构分析
1.3.2.1 化学组成分析
苯酚-硫酸比色法[7]测定样品总糖含量;间羟基联苯法[8]测定糖醛酸含量;BCA蛋白定量试剂盒测定蛋白质含量[9]。
1.3.2.2 分子质量测定
使用配备RID-20A检测器的高效凝胶排阻色谱仪测定样品的分子质量。使用Ultrahydrogel Linear色谱柱(7.8 mm×300 mm)和Ultrahydrogel保护柱(6 mm×40 mm)。将2 mg样品溶于1 mL 0.1 mol/L NaNO3溶液进行检测。
1.3.2.3 单糖组成分析
1.5 mg样品于120 ℃用1.5 mL 2 mol/L TFA水解5 h。待水解产物干燥后加入0.5 mL甲醇,重复3次除去所有TFA并获得甲醇脱乙酰基物。将甲醇衍生物完全溶解在超纯水中,然后使用配备有脉冲安培检测的离子色谱仪进行分析。
1.3.2.4 傅里叶变换红外光谱分析
将1 mg样品和150 mg KBr置于研钵中充分研磨,压片进行测量。在4 000~500 cm-1的波数范围内通过32次扫描记录红外光谱,分辨率设置为4 cm-1。
1.3.2.5 甲基化分析
参照GUO等[10]的方法进行甲基化分析。采用QIAN等[11]的方法进行支化度(degree of branching,DB)的计算,计算如公式(1)如示:
(1)
式中:Y,支化度;B、T、L分别为支化糖残基、末端糖残基、线性糖残基的摩尔分数。
1.3.3 GG-SPI混合物及共价复合物的制备
物理混合样品的制备:将SPI和GG(GG、GGA1、GGA2、GGA3、GGA4、GGA5)按1∶2的质量比于蒸馏水中混匀,冷冻干燥,得到多糖-蛋白质混合物样品(命名为GG-SPI-M、GGA1-SPI-M、GGA2-SPI-M、GGA3-SPI-M、GGA4-SPI-M、GGA5-SPI-M)。共价复合物样品的制备:将上述多糖-蛋白质冻干粉置于干燥器中(湿度为79%),80 ℃加热5 h,得到多糖-蛋白质共价复合物样品(命名为GG-SPI-S、GGA1-SPI-S、GGA2-SPI-S、GGA3-SPI-S、GGA4-SPI-S、GGA5-SPI-S)。
1.3.4 共价复合物的结构测定
1.3.4.1 傅里叶变换红外光谱分析
多糖-蛋白质共价复合物的红外光谱测定方法参照1.3.2.4节。
1.3.4.2 十二烷基硫酸钠-聚丙烯酰氨凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis, SDS-PAGE)
根据ZHANG等[12]的方法,并适当修改,进行SDS-PAGE。将溶解好的样品(包括GG、SPI、GG-SPI混合物以及GG-SPI共价复合物)分别与上样缓冲液按体积比1∶1混合。沸水浴加热5 min,离心后取6 μL上清液加入凝胶孔中,凝胶(质量分数为12%分离胶和质量分数为5%浓缩胶)在80 V下运行30 min,在120 V下运行20 min,将凝胶在R250考马斯亮蓝染色液中孵育1 h以染色蛋白质,并用脱色液(体积分数为40%甲醇、体积分数为10%乙酸和体积分数为50%蒸馏水)脱色1 h,最后在蒸馏水中过夜。
1.3.5 共价复合物功能特性研究
1.3.5.1 表面疏水性测定
采用荧光探针法测定多糖-蛋白共价复合物的表面疏水性。配制0.2、0.5、1.0 mg/mL的样品溶液,分别加入20 μL 8-苯胺基-1-萘磺酸(8-anilino-1-naphthalenesulfonic acid,ANS)溶液,室温避光储存30 min,于375 nm激发波长下,记录465 nm荧光强度。按照1.3.2.1节中蛋白含量的测定方法分别测得各个浓度样品的蛋白浓度,以不同浓度样品的蛋白浓度为横坐标,荧光强度为纵坐标做线性回归,其斜率为表面疏水性。
1.3.5.2 蛋白质溶解度测定
按照LIU等[13]的方法,并适当修改。配制2 mg/mL的样品溶液。用1 mol/L的HCl溶液或1 mol/L的NaOH溶液将样品溶液的pH值调至7.0和4.5,搅拌30 min后12 000 r/min离心,收集上清液,按照1.3.2.1节中的方法分别测定离心前样品的蛋白含量和上清液的蛋白含量。样品蛋白质溶解度计算如公式(2)所示:
样品蛋白质溶解度![]() 100
100
(2)
1.3.5.3 粒径和zeta电位分析
准确称取0.2 g样品(SPI、GG、GA、GG-SPI混合物、GG-SPI共价复合物),70 ℃溶于100 mL蒸馏水中,随后加入1.0 g葵花籽油,使用高速剪切机剪切2 min,1.8×107 Pa均质3 min后得到样品乳液。
使用激光粒度分析仪和zeta电位分析仪对乳液的粒径和电位值进行测量。将水和葵花籽油的折射率分别设为1.333和1.449,加样至遮光率为15%~20%。通过体积加权平均直径D4,3来监测14 d内液滴大小分布的变化。
1.3.6 统计分析
使用SPSS软件将3次重复实验的数据表示为“平均值±标准差”。根据邓肯多重检验,P<0.05时具有显著差异性,其结果具有统计学意义。
2 结果与分析
2.1 GG的结构表征
2.1.1 GG及其酸水解产物的化学组成和分子质量
GG的化学组成和分子质量如表1所示,从中可以看出,GG的总糖、蛋白质、糖醛酸含量分别为(97.59±1.54)%、(4.07±0.95)%、(8.27±0.32)%,表明GG是一种结合有少量蛋白的酸性多糖。
表1 不同酸解程度的GG的化学组成及分子质量
Table 1 Chemical composition and molecular weight of GG with different degrees of acid hydrolysis
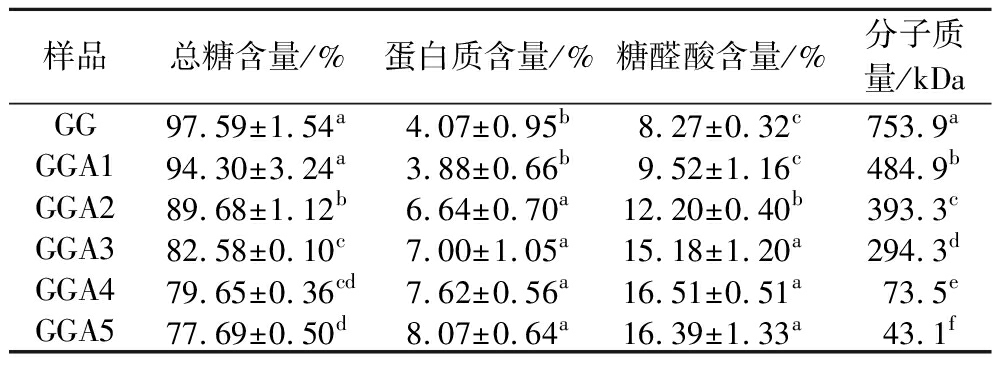
样品总糖含量/%蛋白质含量/%糖醛酸含量/%分子质量/kDaGG97.59±1.54a4.07±0.95b8.27±0.32c753.9aGGA194.30±3.24a3.88±0.66b9.52±1.16c484.9bGGA289.68±1.12b6.64±0.70a12.20±0.40b393.3cGGA382.58±0.10c7.00±1.05a15.18±1.20a294.3dGGA479.65±0.36cd7.62±0.56a16.51±0.51a73.5eGGA577.69±0.50d8.07±0.64a16.39±1.33a43.1f
注:表中不同字母代表差异显著(P<0.05)(下同)。
此外,随着酸浓度的提高和处理时间的延长,GG蛋白含量和糖醛酸含量逐渐增加,分子质量显著下降,这意味着酸水解导致GG分子结构发生变化。糖醛酸含量增加归因于糖醛酸在C-5位置上连接的—COOH基团对质子进攻形成了较大的空间位阻,且较低的酸浓度使糖醛酸在反应过程中保持其原有结构而不被水解[14]。蛋白含量增高可能是由于与多糖共价连接的蛋白随着酸解程度增大逐渐被暴露。
2.1.2 GG及其酸水解产物的单糖组成
如表2所示,GG及降解后的5个组分均由阿拉伯糖、半乳糖、木糖、甘露糖和葡萄糖醛酸组成,随着酸浓度的提高和处理时间的延长,大部分阿拉伯糖被除去,半乳糖含量增加。木糖和甘露糖的相对含量增加。所有这些结果表明,半乳糖、甘露糖和木糖可能位于分子的骨架或核心部分,而阿拉伯糖位于分子的外围。
表2 不同酸解程度的GG的单糖组成 单位:%
Table 2 Monosaccharide composition of GG with different degrees of acid hydrolysis

样品阿拉伯糖半乳糖木糖甘露糖葡萄糖醛酸GG40.02±0.04a38.34±1.00c2.77±0.34b12.33±0.70b6.64±0.68cGGA132.35±0.50b34.37±0.92d6.36±0.75a11.37±0.88b15.46±0.21bGGA214.76±0.28c40.75±0.90bc7.32±0.75a20.38±0.17a16.72±0.0.53bGGA312.5±1.00d41.25±1.00bc7.74±0.69a17.92±0.63a20.51±0.51aGGA410.48±0.76e42.55±0.78ab6.36±0.28a19.05±0.30a21.48±0.22aGGA57.38±0.70f45.41±0.81a6.21±0.72a19.56±0.79a21.43±0.72a
2.1.3 GG及其酸水解产物的官能团组成
如图1所示,3 420 cm-1处的O—H的伸缩振动和2 930 cm-1处的C—H伸缩振动表明GG及5种水解产物具有多糖的典型特征吸收峰[15]。在1 630 cm-1处较强的吸收峰属于C![]() O的伸缩振动。在1 440 cm-1处的COO—伸缩振动表明多糖中存在糖醛酸[16],且降解后的GG在1 140 cm-1处的峰强度变大,与单糖组成的测定结果一致。
O的伸缩振动。在1 440 cm-1处的COO—伸缩振动表明多糖中存在糖醛酸[16],且降解后的GG在1 140 cm-1处的峰强度变大,与单糖组成的测定结果一致。
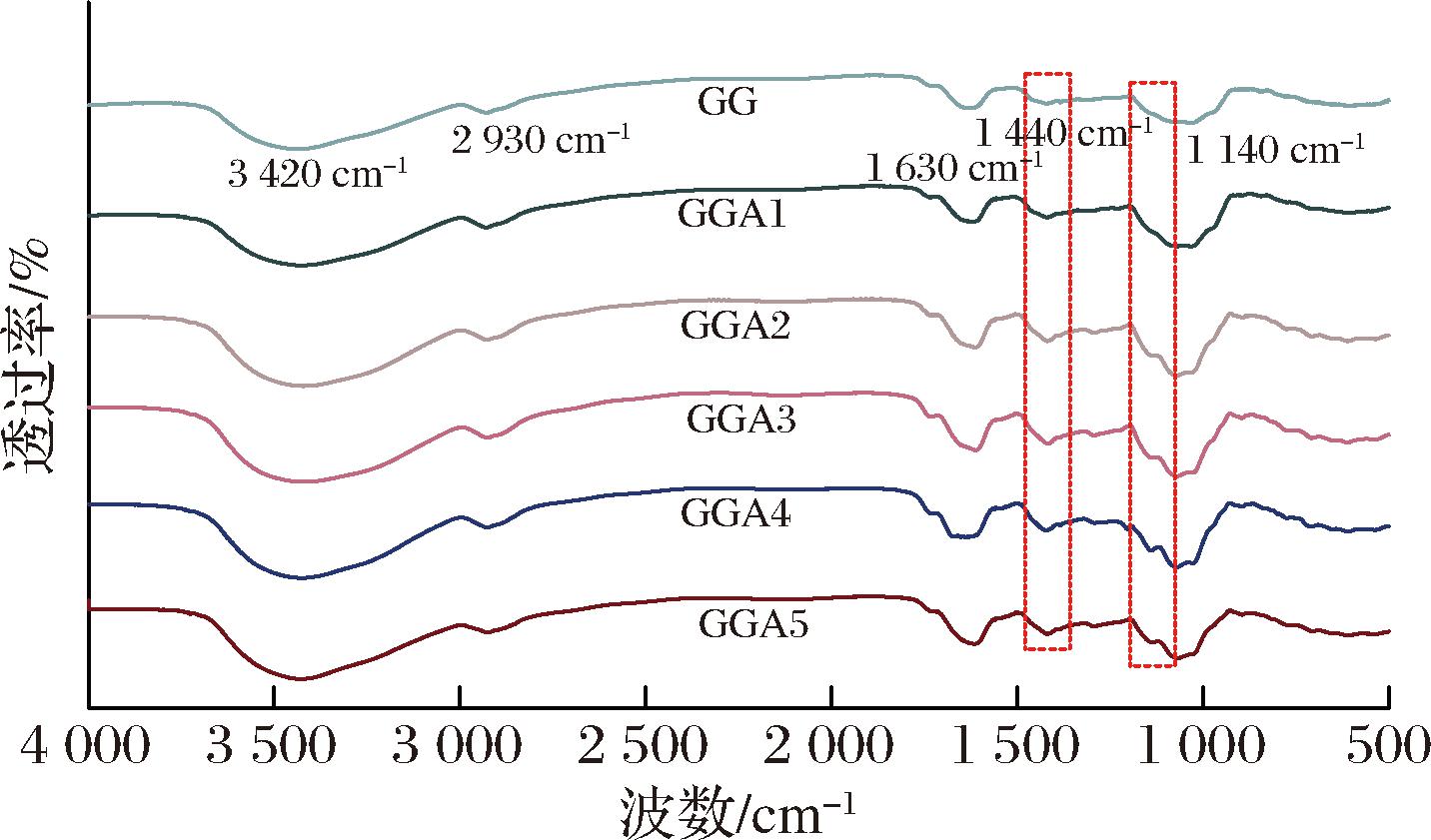
图1 不同酸解程度GG的红外光谱
Fig.1 The infrared spectra of GG at different degrees of acid hydrolysis
2.1.4 糖苷键连接方式分析
甲基化结果见表3,研究表明,GG具有高度支化的分子结构。其主链由1,6-Galp组成,支链最多的糖残基是3,4,6-Galp,占总糖残基的18.78%。在3,4,6-Galp的3-O和4-O位置上有两个侧链。由表3可知,经过酸水解后,末端残基T-Araf的比例逐渐减少,6-Galp逐渐增多,与间羟基联苯比色法得到的结果一致。总的Ara相对含量逐渐降低,结合GG的分子结构特征,GG中的Ara位于支链,首先与酸溶液充分接触,因而更快被水解。此外,Ara以呋喃糖环的形式存在,一般而言,呋喃糖环形成的糖苷键水解速度往往>吡喃糖环形成的糖苷键[17]。随着酸解程度的升高GG的支化度从0.83降低至0.34,证明酸解将GG的侧链几乎完全打断。
表3 不同酸解程度的GG的糖苷键连接方式含量变化
Table 3 The content of glucosidic linkage of GG changed with different acidolysis degree
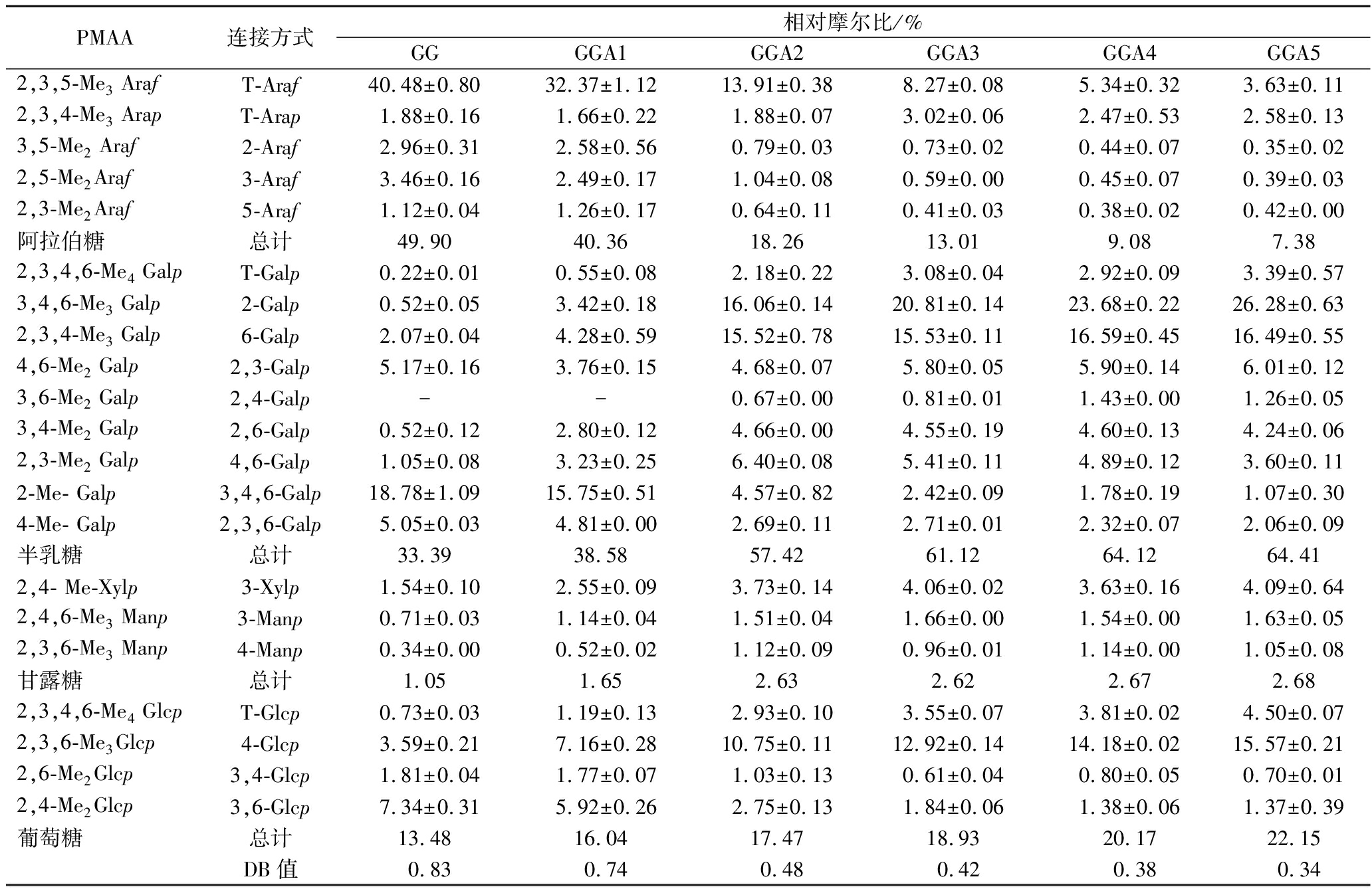
PMAA连接方式相对摩尔比/%GGGGA1GGA2GGA3GGA4GGA52,3,5-Me3 ArafT-Araf40.48±0.8032.37±1.1213.91±0.388.27±0.085.34±0.323.63±0.112,3,4-Me3 ArapT-Arap1.88±0.161.66±0.221.88±0.073.02±0.062.47±0.532.58±0.133,5-Me2 Araf2-Araf2.96±0.312.58±0.560.79±0.030.73±0.020.44±0.070.35±0.022,5-Me2Araf3-Araf3.46±0.162.49±0.171.04±0.080.59±0.000.45±0.070.39±0.032,3-Me2Araf5-Araf1.12±0.041.26±0.170.64±0.110.41±0.030.38±0.020.42±0.00阿拉伯糖总计49.9040.3618.2613.019.087.382,3,4,6-Me4 GalpT-Galp0.22±0.010.55±0.082.18±0.223.08±0.042.92±0.093.39±0.573,4,6-Me3 Galp2-Galp0.52±0.053.42±0.1816.06±0.1420.81±0.1423.68±0.2226.28±0.632,3,4-Me3 Galp6-Galp2.07±0.044.28±0.5915.52±0.7815.53±0.1116.59±0.4516.49±0.554,6-Me2 Galp2,3-Galp5.17±0.163.76±0.154.68±0.075.80±0.055.90±0.146.01±0.123,6-Me2 Galp2,4-Galp--0.67±0.000.81±0.011.43±0.001.26±0.053,4-Me2 Galp2,6-Galp0.52±0.122.80±0.124.66±0.004.55±0.194.60±0.134.24±0.062,3-Me2 Galp4,6-Galp1.05±0.083.23±0.256.40±0.085.41±0.114.89±0.123.60±0.112-Me- Galp3,4,6-Galp18.78±1.0915.75±0.514.57±0.822.42±0.091.78±0.191.07±0.304-Me- Galp2,3,6-Galp5.05±0.034.81±0.002.69±0.112.71±0.012.32±0.072.06±0.09半乳糖总计33.3938.5857.4261.1264.1264.412,4- Me-Xylp3-Xylp1.54±0.102.55±0.093.73±0.144.06±0.023.63±0.164.09±0.642,4,6-Me3 Manp3-Manp0.71±0.031.14±0.041.51±0.041.66±0.001.54±0.001.63±0.052,3,6-Me3 Manp4-Manp0.34±0.000.52±0.021.12±0.090.96±0.011.14±0.001.05±0.08甘露糖总计1.051.652.632.622.672.682,3,4,6-Me4 GlcpT-Glcp0.73±0.031.19±0.132.93±0.103.55±0.073.81±0.024.50±0.072,3,6-Me3Glcp4-Glcp3.59±0.217.16±0.2810.75±0.1112.92±0.1414.18±0.0215.57±0.212,6-Me2Glcp3,4-Glcp1.81±0.041.77±0.071.03±0.130.61±0.040.80±0.050.70±0.012,4-Me2Glcp3,6-Glcp7.34±0.315.92±0.262.75±0.131.84±0.061.38±0.061.37±0.39葡萄糖总计13.4816.0417.4718.9320.1722.15DB值0.830.740.480.420.380.34
2.2 共价复合物的结构特征
2.2.1 官能团组成分析
GG和SPI在美拉德反应期间的化学反应导致共价复合物的傅里叶变换红外光谱发生变化(图2)。在SPI光谱中观察到蛋白质的典型条带,包括1 640 cm-1(酰胺Ⅰ区,C—O伸缩)、1 535 cm-1(酰胺Ⅱ区,N—H弯曲和C—N伸缩)和1 240~1 450 cm-1(酰胺Ⅲ区,N—H变形和C—N伸缩)[18]。经美拉德反应后的共价复合物,位于O—H和N—H基团的宽吸收峰(酰胺A区域,3 700~3 200 cm-1)发生偏移,归属于酰胺Ⅱ和Ⅲ区域的吸收峰强度明显降低,归因于多糖的羰基与蛋白的氨基进行共价结合,交联后会引起糖环内O—H键的变形振动并导致C—N键的伸缩振动,证实了GG和SPI之间的相互作用。
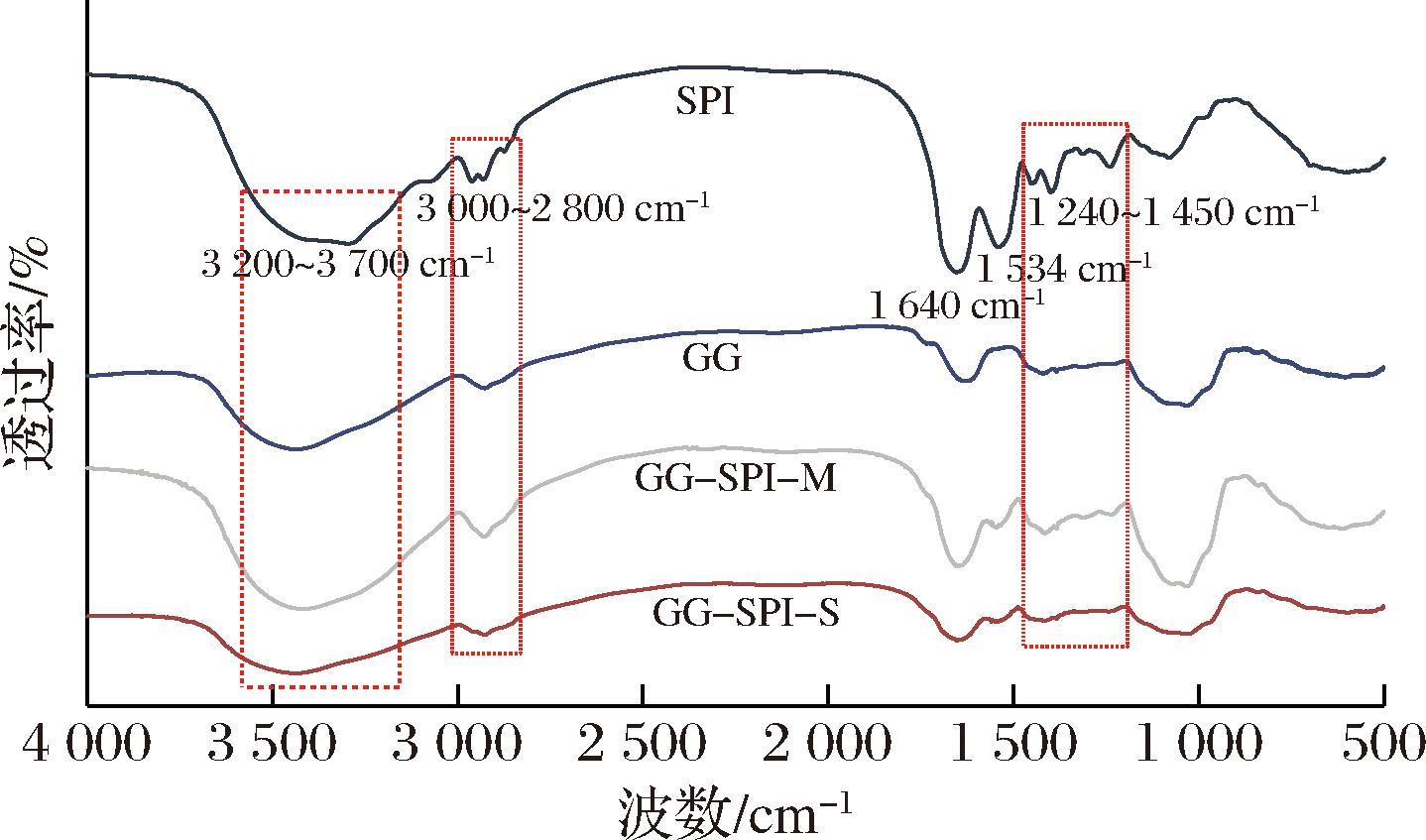
图2 不同样品的红外光谱
Fig.2 The infrared spectra of different samples
2.2.2 SDS-PAGE分析
SDS-PAGE如图3所示,结果显示SPI(泳道13)分别在78、75、48、35、11 kDa显示5条清晰的条带,对应SPI的主要蛋白质组分大豆球蛋白和β-伴大豆球蛋白。多糖-蛋白质混合物(泳道1、3、5、7、9、11)的电泳图谱均显示出SPI的特征条带,经过美拉德反应后的复合物样品(泳道2、4、6、7、8、10、12)中蛋白条带强度逐渐变弱直至消失,表明这些蛋白质组分参与了接枝过程,且支链度较小的GG具有更高的反应活性。这归因于酸性条件下,考马斯亮蓝以非共价方式与蛋白质分子上的活性基团(如游离氨基和巯基)结合,并呈现蓝色,SPI与GG之间的美拉德反应可减少蛋白质分子中的游离氨基。因此,考马斯亮蓝与蛋白质分子的结合位点减少,颜色变浅,证实了多糖与蛋白质的共价结合[19]。

a-GG-SPI混合物、GG-SPI共价复合物、SPI的SDS-PAGE;b-GG、SPI的SDS-PAGE
图3 不同样品的SDS-PAGE
Fig.3 SDS-PAGE of different samples
2.3 共价复合物的功能特性
2.3.1 表面疏水性
蛋白质的表面疏水性是影响其结构的最重要特征之一,并极大地影响蛋白质的界面性[20]。如图4所示,GG-SPI混合物的表面疏水性低于SPI本身,归因于GG的引入可以增加混合物亲水基团的数量,从而降低疏水性。与GG进行共价复合后,GG-SPI共价复合物表面疏水性显著下降(P<0.05),归因于多糖链结合到蛋白质分子表面,导致蛋白质表面疏水基团被覆盖,抑制ANS对这些基团的可及性。支链度较低的GG显著降低了蛋白质的表面疏水性,可能是由于:(a)支链度较低的GG反应活性较高,增强了多糖链与蛋白质结合的产生的屏蔽效应;(b)由于蛋白质在美拉德反应过程中聚集,有效疏水区域被掩埋;(c)低支链度的GG与SPI美拉德反应程度较高,形成更多表面疏水性很小的晚期糖化产物或类黑素[21]。
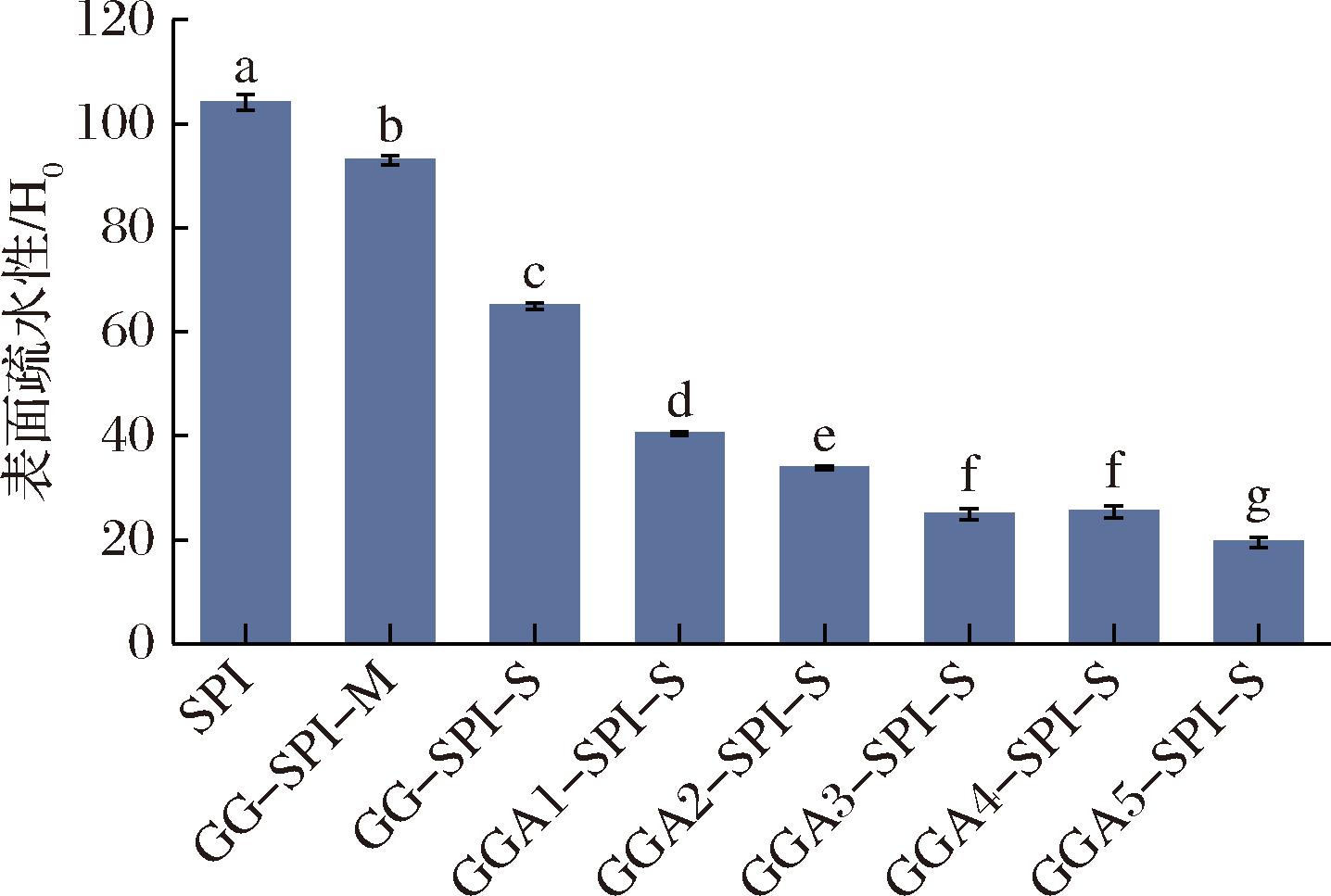
图4 不同样品表面疏水性
Fig.4 Surface hydrophobicity of different samples
注:图中不同字母代表差异显著(P<0.05)(下同)。
2.3.2 蛋白质溶解度
图5为样品在pH 7和pH 4.5条件下蛋白质的溶解度,如图所示,GG-SPI共价复合物的溶解度高于SPI和GG-SPI混合物,这归因于共价结合过程中蛋白质分子结构发生变化,蛋白质倾向于在等电点附近聚集,溶解度较低,SPI与GG结合导致SPI的游离巯基暴露量降低,从而防止分子间蛋白质-蛋白质(疏水)相互作用,抑制蛋白质的聚集[22]。与SPI共价交联的GG支链度越低,形成的共价复合物溶解度越高,这归因于较低支链度GG中含量较高的蛋白质会附着在油表面上并作为乳化稳定剂[6],其溶解度也随之升高。在等电点(pH 4.5)附近,GG-SPI共价复合物溶解度显著高于SPI和GG-SPI混合物,证明GG的加入还可以改善SPI在较宽pH范围内的溶解度。
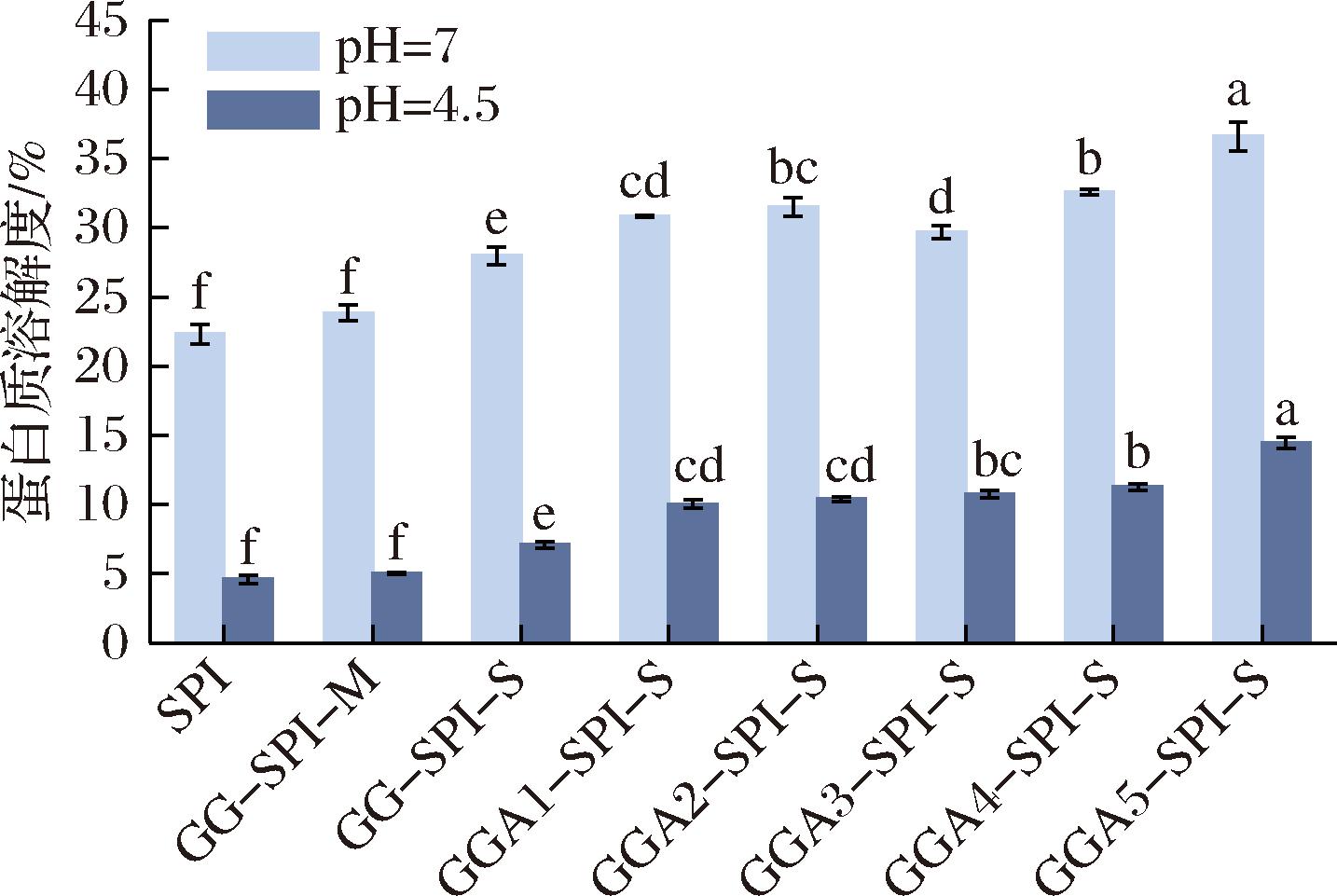
图5 不同样品蛋白质溶解度
Fig.5 Protein solubility of different samples
2.3.3 乳化性能
2.3.3.1 粒径分布
如图6所示,GG乳液的D4,3
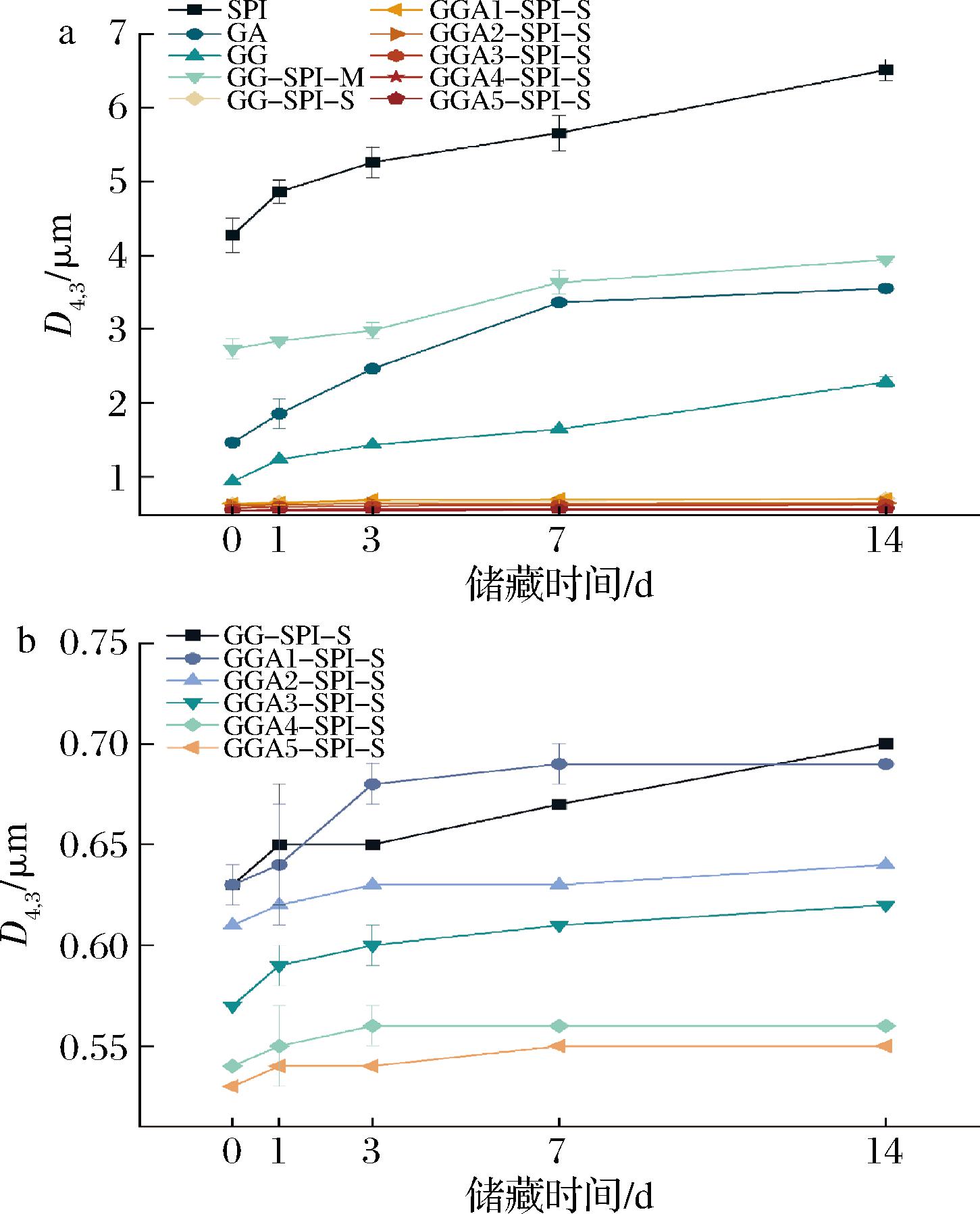
a-SPI、GA、GG、酸解前后GG-SPI混合物及共价复合物的 乳液粒径;b-酸解前后GG-SPI共价复合物的乳液粒径
图6 不同样品的乳液粒径
Fig.6 Emulsion particle size of different samples
2.3.3.2 zeta电位
乳液中电荷分布情况可通过影响分子间的静电斥力影响乳液体系的稳定性,研究表明,zeta绝对电位值高于30 mV时,乳液趋于稳定[23]。如图7所示,以SPI和GA作为对照,GG的绝对电位值显著高于GA,说明相同浓度下GG形成的乳液更加稳定。GG-SPI共价复合物的绝对电位值>SPI,这归因于SPI与大量带负电荷的GG分子的结合增加了离子间的静电斥力,从而增加了绝对电势[24]。静电斥力的增加会抑制油滴的聚集和沉积,使乳液体系更稳定[25]。经过酸水解处理后的GG与SPI的共价复合物绝对电位值逐渐升高,与粒径变化基本一致。可能由于部分酸水解使GG从聚集趋向分散,糖醛酸和蛋白质含量显著增加,导致共价复合物电负性增强,使分子间斥力增大。
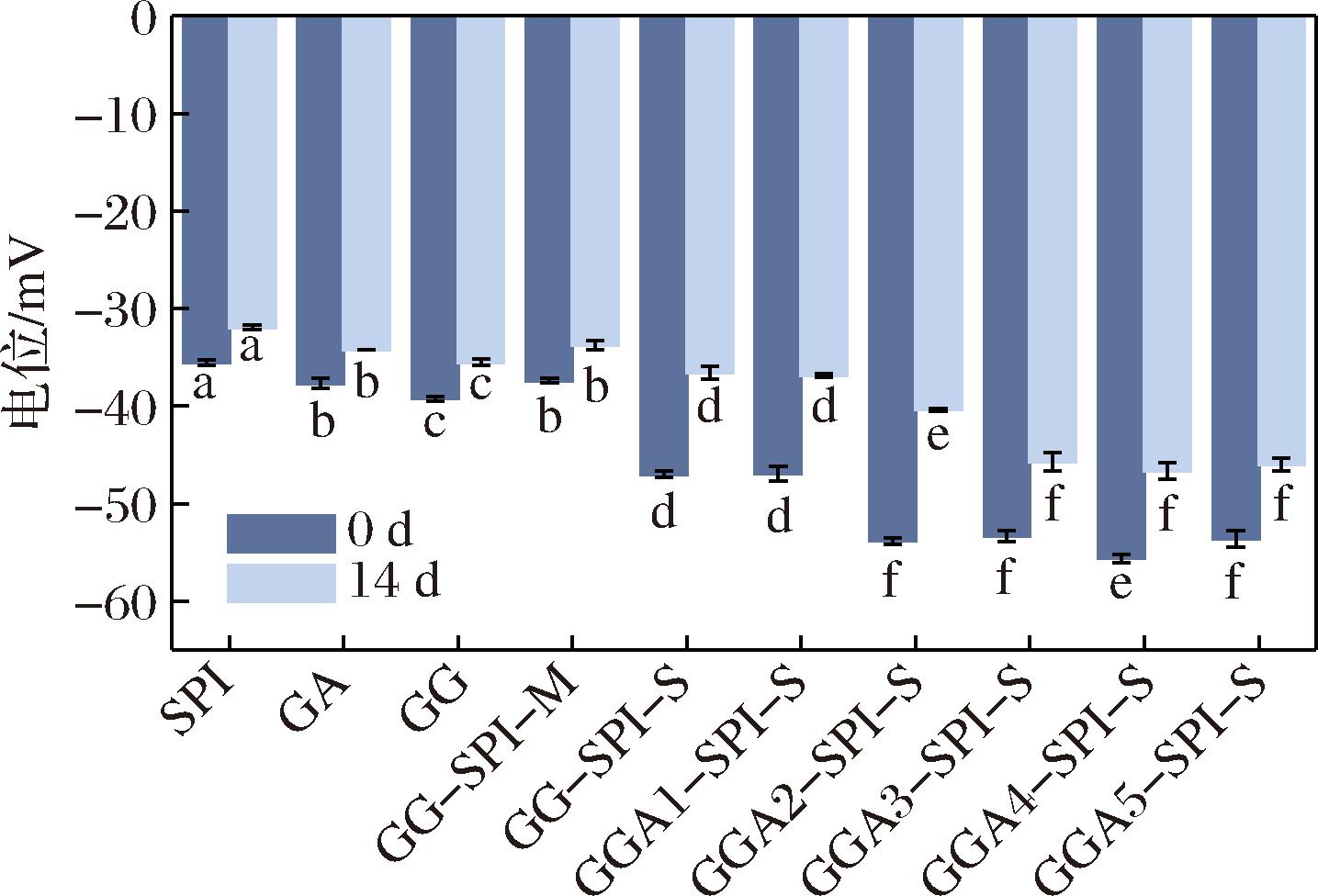
图7 不同样品的zeta电位值
Fig.7 Zeta potential of different samples
3 结论
本研究通过部分酸水解获得不同结构的GG,随着酸浓度的增大和处理时间的延长,GG中蛋白质和糖醛酸含量增加,末端阿拉伯糖残基含量降低,支化度降低,分子质量显著下降。GG-SPI复合物的红外光谱和SDS-PAGE图谱的变化证实了共价复合物的形成。蛋白质溶解度和表面疏水性结果表明,酸水解处理后的GG与蛋白质结合后可以显著提高复合物的乳化性,这可能与GG多种结构因素的综合作用有关,酸水解破坏了GG的分子结构,分子质量降低使GG更容易迁移到油水界面,降低了界面自由能。而糖醛酸和蛋白质等带电基团含量升高使液滴间斥力增加。通过水包油乳液评价不同降解程度GG对共价复合物乳化性能的影响,粒径与zeta电位结果表明,支链度越低的GG与SPI的复合物的乳化能力越好,并且具有更好的乳化稳定性,可能有以下原因:a)支链度较低的GG的主链中所含较多的蛋白质会附着在油滴表面上并作为乳化稳定剂;b)大量亲水性羟基的GG分子链共价结合到SPI分子表面,提供了足够多的亲水性羟基;c)支链度较低的GG具有更强的负电荷,使复合物与乳液之间静电排斥作用增强,抑制了乳液的聚集和沉积。本研究为GG的开发利用及多糖的降解提供实验依据,为更好地开发GG资源、深入研究其构效关系奠定基础。
[1] TAO X, CAI Y J, LIU T X, et al.Effects of pretreatments on the structure and functional properties of okara protein[J].Food Hydrocolloids, 2019, 90:394-402.
[2] CAI Y J, DENG X L, LIU T X, et al.Effect of xanthan gum on walnut protein/xanthan gum mixtures, interfacial adsorption, and emulsion properties[J].Food Hydrocolloids, 2018, 79:391-398.
[3] HUANG L H, CAI Y J, LIU T X, et al.Stability of emulsion stabilized by low-concentration soybean protein isolate:Effects of insoluble soybean fiber[J].Food Hydrocolloids, 2019, 97:105232.
[4] LI Q Y, ZHENG J B, GE G, et al.Impact of heating treatments on physical stability and lipid-protein co-oxidation in oil-in-water emulsion prepared with soy protein isolates[J].Food Hydrocolloids, 2020, 100:105167.
[5] AL-ASSAF S, PHILLIPS G O, AMAR V.Gum ghatti[M].Handbook of Hydrocolloids.Amsterdam:Elsevier, 2009:477-494.
[6] AL-ASSAF S, AMAR V, PHILLIPS G O.Characterisation of gum ghatti and comparison with gum Arabic[M].Gums and Stabilisers for the Food Industry 14.The Royal Society of Chemistry, 2008:280-290.
[7] GUO Q B, CUI S W, WANG Q, et al.Extraction, fractionation and physicochemical characterization of water-soluble polysaccharides from Artemisia sphaerocephala Krasch seed[J].Carbohydrate Polymers, 2011, 86(2):831-836.
[8] SUN H Q, SONG W W, ZHANG L J, et al.Structural characterization and inhibition on α-glucosidase of a novel oligosaccharide from barley malt[J].Journal of Cereal Science, 2018, 82:82-93.
[9] CORTÉS-R OS J, Z
OS J, Z RATE A M, FIGUEROA J D, et al.Protein quantification by bicinchoninic acid (BCA) assay follows complex kinetics and can be performed at short incubation times[J].Analytical Biochemistry, 2020, 608:113904
RATE A M, FIGUEROA J D, et al.Protein quantification by bicinchoninic acid (BCA) assay follows complex kinetics and can be performed at short incubation times[J].Analytical Biochemistry, 2020, 608:113904
[10] GUO Q B, CUI S W, KANG J, et al.Non-starch polysaccharides from American ginseng:Physicochemical investigation and structural characterization[J].Food Hydrocolloids, 2015, 44:320-327.
[11] QIAN K Y, CUI S W, NIKIFORUK J, et al.Structural elucidation of rhamnogalacturonans from flaxseed hulls[J].Carbohydrate Research, 2012, 362:47-55.
[12] ZHANG R J, CHENG L R, LUO L, et al.Formation and characterisation of high-internal-phase emulsions stabilised by high-pressure homogenised quinoa protein isolate[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2021, 631:127688.
[13] LIU Y, ZHAO G L, ZHAO M M, et al.Improvement of functional properties of peanut protein isolate by conjugation with dextran through Maillard reaction[J].Food Chemistry, 2012, 131(3):901-906.
[14] 张宏媛, 钱佳俊, 李哲远, 等.部分酸水解对桃胶多糖结构和乳化功能的影响[J].食品科学, 2023, 44(4):99-106.ZHANG H Y, QIAN J J, LI Z Y, et al.Effect of partial acid hydrolysis on the structure and emulsifying function of peach gum polysaccharide[J].Food Science, 2023, 44(4):99-106.
[15] WANG L, LIU H M, QIN G Y.Structure characterization and antioxidant activity of polysaccharides from Chinese quince seed meal[J].Food Chemistry, 2017, 234:314-322.
[16] GUO R, CAO N N, WU Y, et al.Optimized extraction and molecular characterization of polysaccharides from Sophora alopecuroides L.seeds[J].International Journal of Biological Macromolecules, 2016, 82:231-242.
[17] 冯卫生, 吴锦忠.天然药物化学[M].2版.北京:中国医药科技出版社, 2018.
[18] QU P, HUANG H Y, WU G F, et al.Effects of hydrolysis degree of soy protein isolate on the structure and performance of hydrolyzed soy protein isolate/urea/formaldehyde copolymer resin[J].Journal of Applied Polymer Science, 2015, 132(7):e41469.
[19] LI R, CUI Q, WANG G R, et al.Relationship between surface functional properties and flexibility of soy protein isolate-glucose conjugates[J].Food Hydrocolloids, 2019, 95:349-357.
[20] MA X B, HOU F R, ZHAO H H, et al.Conjugation of soy protein isolate (SPI) with pectin by ultrasound treatment[J].Food Hydrocolloids, 2020, 108:106056.
[21] CHEN L, CHEN J S, WU K G, et al.Improved low pH emulsification properties of glycated peanut protein isolate by ultrasound Maillard reaction[J].Journal of Agricultural and Food Chemistry, 2016, 64(27):5531-5538.
[22] TANG C H.Emulsifying properties of soy proteins:A critical review with emphasis on the role of conformational flexibility[J].Critical Reviews in Food Science and Nutrition, 2017, 57(12):2636-2679.
[23] ZHENG J C, XIAO N, LI Y, et al.Free radical grafting of whey protein isolate with tea polyphenol:Synthesis and changes in structural and functional properties[J].LWT, 2022, 153:112438.
[24] DAI T T, LI T, LI R Y, et al.Utilization of plant-based protein-polyphenol complexes to form and stabilize emulsions:Pea proteins and grape seed proanthocyanidins[J].Food Chemistry, 2020, 329:127219.
[25] DAI S C, LIAO P L, WANG Y L, et al.Soy protein isolate-catechin non-covalent and covalent complexes:Focus on structure, aggregation, stability and in vitro digestion characteristics[J].Food Hydrocolloids, 2023, 135:108108.