大豆是世界上最重要的粮油作物之一,同时是优质植物蛋白的来源[1]。大豆不仅富含蛋白质、脂肪和糖类,还含有多酚、异黄酮、皂苷和低聚糖等多种活性成分,具有抗氧化、降血糖、抗炎症、抗癌等生理活性[2]。豆浆又称原浆豆奶,是以大豆为原料,不添加食品辅料和食品添加剂,加工制成的产品。发酵原浆豆奶是以大豆为主要原料,可添加食糖,不添加其他食品辅料和食品添加剂,经发酵制成的产品。发酵调制豆奶是以大豆为主要原料,可添加营养强化剂、食品添加剂和其他食品辅料,经发酵制成的产品。[参考GB/T 30885—2014《植物蛋白饮料 豆奶和豆奶饮料》]
阿尔茨海默症(alzheimer’s disease,AD)是一种进行性多因素的神经退行性疾病,主要引起患者认知障碍和记忆力衰退[3]。AD的发病因素之一是体内神经递质乙酰胆碱水平降低,因此抑制乙酰胆碱酯酶(acetylcholinesterase,AChE)活性有利于提高乙酰胆碱水平,从而缓解AD[4]。目前,临床上用于治疗AD的药物主要是AChE抑制剂,如加兰他敏、他克林、卡巴拉汀和多奈哌齐[5]。然而,长期服用这些合成类AChE抑制剂容易导致患者出现恶心、腹泻和肌肉痉挛等不良反应[6]。因此,筛选并开发植物来源的食源性天然AChE抑制剂对AD的预防或辅助治疗有重要意义。
豆浆乳酸菌发酵过程中,在微生物作用下发生一系列生物转化作用,包括蛋白质被水解为氨基酸和肽,大豆异黄酮则被水解为苷元等。已有研究表明,乳酸菌发酵能增强植物基的抗氧化和酶抑制活性。周瑶等[7]用乳酸菌发酵番木瓜汁,发酵后番木瓜汁对α-葡萄糖苷酶和酪氨酸酶的抑制活性显著增强;DUAN等[8]研究发现,乳酸菌发酵枸杞汁的抗氧化活性、α-葡萄糖苷酶和胰脂肪酶抑制活性均高于非发酵枸杞汁。因此,植物基食品乳酸菌发酵不仅可以改善食品的感官特性,还能提高活性成分的转化和生物利用度[9]。
超高效液相色谱-质谱联用技术(ultra high performance liquid chromatography-mass spectrometry,UPLC-MS)常用于复杂成分的分离和鉴定,是一种选择性高和灵敏度好的分析检测方法。分子对接技术常用于探究小分子与酶蛋白的结合能力及相互作用机制,已成为计算机辅助药物研究的一项重要技术。将液相色谱-质谱联用技术和分子对接技术相结合,能够快速筛选植物来源的天然酶抑制剂。KASHYAP等[10]采用超高效液相色谱-四极杆飞行时间质谱联用技术(ultra-performance liquid chromatography-quadrupole-time-of-flight-mass spectrometry, UPLC-QTOF-MS)和分子对接技术从莎草、芍药和飞燕草的提取物中分离鉴定出香附烯酮、翠雀花宁和翠雀宾等化学成分,这些成分与AChE有较强的亲和能力;TERZIC等[11]研究表明,白屈菜中的对香豆酰酪胺与AChE的结合能为-9.5 kcal/mol,该化合物主要通过氢键、疏水相互作用和范德华力与氨基酸残基相互作用。UPLC-MS与分子对接技术结合,为发现新型AChE抑制剂做出重要贡献。
本课题探究了豆浆发酵前后AChE抑制活性的变化,采用UPLC-QTOF-MS技术对豆浆和发酵豆浆提取物进行成分鉴定,通过化学计量学方法找出发酵前后含量出现差异的成分,再利用分子对接技术,研究这些差异成分与AChE的亲和能力、结合位点和相互作用力,从中发现对AChE有抑制作用的活性成分。本研究将为大豆和大豆发酵制品功能性质的进一步开发提供理论依据。
1 材料与方法
1.1 材料与试剂
大豆,无锡本地市场;蔗糖、葡萄糖、大豆肽、酵母浸粉,浙江一诺生物科技有限公司;直投式发酵剂(含嗜热链球菌和保加利亚乳杆菌),市售;无水乙醇、NaH2PO4、Na2HPO4均为分析纯,国药集团化学试剂有限公司;AChE、加兰他敏,上海麦克林生化科技股份有限公司;碘代硫代乙酰胆碱(acetylthiocholine iodide,ATCI)、5,5-二巯基-2,2-二硝基苯甲酸(5, 5-dimercapto-2, 2-dinitrobenzoic acid,DTNB),上海源叶生物科技有限公司。
1.2 仪器与设备
AB104-N电子分析天平、FE28K梅特勒pH计,梅特勒-托利多仪器有限公司;HHS恒温水浴锅,江苏省金坛市医疗仪器厂;JYL-Y5打浆机,九阳股份有限公司;超净工作台,无锡一净设备有限公司;K9840半自动凯氏定氮仪、手提式不锈钢压力蒸汽灭菌锅,济南海能仪器股份有限公司;SC202-2电热恒温干燥箱,江苏南通实验电器厂;Himac CR21GⅡ型冷冻离心机,日本HITACHI公司;超高效液相串联四极杆飞行时间质谱仪,美国沃特世公司;N-1100-D型旋转蒸发仪,巩义瑞德仪器设备有限公司;SCIENTZ-10 ND真空冷冻干燥机,宁波新芝生物科技股份有限公司。
1.3 实验方法
1.3.1 豆浆制备
大豆→清洗→浸泡(豆水质量比为1∶3,25 ℃,12 h)→打浆(豆水质量比为1∶6)→过滤(100目)→生浆→灭酶(95 ℃,10 min)→豆浆。
1.3.2 乳酸菌发酵豆浆制备
豆浆→调整蛋白质含量为2.5%→混料(蔗糖7.5%,葡萄糖1.5%,Na2HPO4 0.1%,柠檬酸钠0.1%,均为质量分数)→灭菌(95 ℃,10 min)→冷却→接种→发酵(42 ℃,6 h)→4 ℃冷藏→后熟12 h。
1.3.3 乙醇提取物制备
将豆浆和发酵豆浆的pH值调到7.0,加入无水乙醇,乙醇终体积分数为70%,超声波提取(50 ℃,1 h),离心(10 000 r/min,15 min),收集上清液。将残渣重复提取,合并上清液,4 ℃保存备用。
1.3.4 AChE抑制活性测定
体外AChE抑制活性测定参照文献[12-13]的方法并略有调整。底物ATCI、显色剂DTNB和AChE均用PBS(0.1 mol/L,pH 8.0)配制,样品溶液用PBS稀释成不同待测浓度。在96孔板中依次加入120 μL PBS、20 μL不同浓度的样品溶液和15 μL AChE溶液(1 U/mL),37 ℃孵育20 min,随后加入20 μL ATCI溶液和70 μL DTNB溶液,37 ℃孵育20 min后,用酶标仪测定反应混合液在412 nm处的吸光度。样品对照组为等量的PBS代替AChE溶液,阴性组为等量的PBS代替样品溶液,阴性对照组为等量的PBS代替样品溶液和AChE溶液。以加兰他敏作为阳性对照。AChE抑制率的计算如公式(1)所示:
AChE抑制率![]()
(1)
式中:A1,阴性组吸光度;A2,阴性对照组吸光度;B1,样品组吸光度;B2,样品对照组吸光度。
1.3.5 UPLC-QTOF-MS分析
将豆浆和发酵豆浆的乙醇提取液用0.22 μm微孔滤膜过滤,进样检测。
色谱条件:色谱柱为BEH C18柱(100 mm×2.1 mm,1.7 um);流动相A为乙腈,流动相B为0.1%(体积分数)甲酸水溶液;梯度洗脱程序:0~0.5 min 5% A,0.5~10 min 5%~20% A,10~18 min 20%~100% A,18~21 min 100% A,21~21.5 min 5% A;流速0.3 mL/min;柱温35 ℃;进样量2 μL。
质谱条件:质谱信号采集模式为正离子扫描模式,喷雾电压2.5 KV;进样电压40 V;碰撞电压4 eV;离子源温度110 ℃;去溶剂温度450 ℃;载气流量800 L/h;质量扫描范围50~1 200 m/z;扫描时间0.5 s,间隔时间0.02 s。
1.3.6 分子对接
分子对接的分子结构选择、参数设置和结果分析方法参照文献[14]进行,并略有调整。从RCSB蛋白数据库(https://www.rcsb)中下载AChE的3D晶体结构(PDB ID:1EVE),选择A链作为受体,将其导入PyMOL软件,除去受体蛋白AChE中的配体、水分子和其他原子,保存为PDB格式后,用AutoDock Tools软件给受体蛋白AChE加上氢原子,计算AChE的总电荷,保存为pdbqt格式。从PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)中下载小分子的3D结构,或用其中Draw Structure功能绘制小分子的2D结构,再用Open Babel软件转化为3D结构,用AutoDock Tools软件给小分子3D结构添加氢原子和设置可旋转键,保存为pdbqt格式。用AutoDock Tools中的Auto Grid模块来创建对接盒子,以center x=5.927,center y=67.348,center z=55.772 为中心,构建65×65×65的盒子。采用AutoDock Vina进行分子对接,根据分子对接结果选择结合能最低的构象进行对接结果分析。
1.3.7 数据处理与分析
将UPLC-QTOF-MS的原始数据导入UNIFI软件,用UNIFI软件的内置数据库来筛选、匹配和鉴定化合物,加和离子选择+H,+Na。结合UNIFI鉴定信息、文献数据、相关质谱数据库和化合物的裂解规律来分析鉴定化合物结构。采用SIMCA软件进行差异成分分析,采用Excel 2021、SPSS 26.0和origin 2022软件处理数据和绘图,采用PyMOL和Discovery Studio软件对分子对接结果进行可视化分析。
2 结果与分析
2.1 AChE抑制活性测定
测定抑制剂浓度对AChE抑制率的影响,并由此得到半数抑制浓度IC50值,用IC50值来表征抑制剂对AChE的抑制活性。IC50值是指AChE抑制率为50%时所对应的抑制剂浓度,即IC50值越小,AChE抑制活性越强。图1为加兰他敏、豆浆与发酵豆浆提取物浓度对AChE抑制率的影响。随着加兰他敏和提取物浓度增大,AChE抑制率均逐渐提高,与豆浆提取物相比,相同浓度下的发酵豆浆提取物对AChE的抑制活性更强。此外,得到加兰他敏的IC50值为2.25 μg/mL,与文献报道的1.062 μg/mL较为接近[15]。豆浆和发酵豆浆提取物的IC50值分别为3.24 mg/mL和2.55 mg/mL,表明豆浆经乳酸菌发酵后AChE抑制活性得到增强,两个提取物的IC50值均大于加兰他敏,可能是因为提取物中成分复杂且含有较多糖类。邹磊等[16]分别用水、甲醇和乙醇提取豆豉中能抑制AChE的活性成分,发现乙醇提取物抑制AChE的IC50值最小,为0.023 mg/mL,且多种市售豆豉的乙醇提取物均对AChE有一定抑制效果。
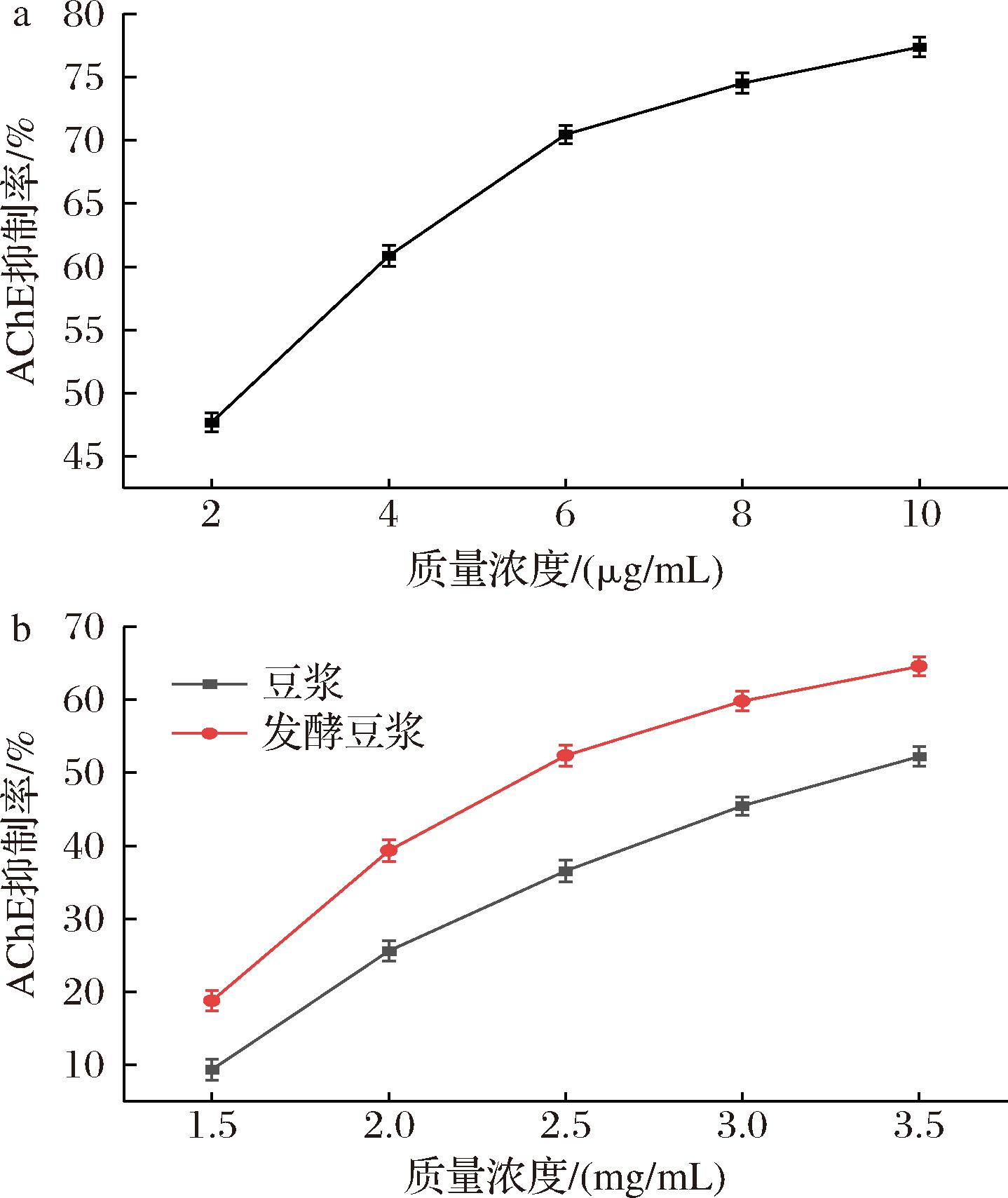
a-加兰他敏;b-豆浆与发酵豆浆
图1 加兰他敏、豆浆和发酵豆浆对AChE的抑制活性测定
Fig.1 Determination of the inhibitory activity of galanthamine, soymilk, and fermented soymilk on AChE
2.2 提取物成分鉴定
采用UPLC-QTOF-MS对豆浆和发酵豆浆的乙醇提取物进行成分鉴定,共鉴定出84种化合物,总离子流图如图2所示,鉴定结果如表1所示。
表1 成分鉴定结果
Table 1 Table of composition identification

序号保留时间/min分子式质量偏差质谱碎片化合物名称10.92C16H12O8-5.3333.264 1[M+H]+,317.427 1,289.319 3,274.234 1,271.201 5,5,6,7,3′,4′-五羟基-3-甲氧基黄酮21.03C7H6O4-4.8155.128 3[M+H]+,137.002 6,93.073 52,4-二羟基苯甲酸31.07C7H7NO2-1.3138.230 1[M+H]+,120.062 8,92.045 22-氨基苯甲酸41.11C11H10O5-2.1223.325 1[M+H]+,180.168 2,162.064 8,118.158 23-O-乙酰基-咖啡酸51.17C12H16O82.8289.182 6[M+H]+,127.039 5,109.072 13,4-二羟基苯乙基-3-O-β-D-吡喃葡糖苷61.25C9H10O5-4.7199.173 2[M+H]+,154.062 8,136.268 1,108.082 5没食子酸乙酯71.27C10H12O5-4.2213.028 3[M+H]+,182.102 1,164.082 7,136.089 1,106.062 82-羟基-3,4-二甲氧基苯甲酸甲酯81.31C5H8O3-1.1117.052 8[M+H]+,99.158 2,71.173 64-羟甲基-γ-丁内酯91.32C15H18O8-3.7327.091 5[M+H]+,165.082 4,147.025 1,103.026 44-O-β-D-葡萄糖基-4-香豆素101.35C9H10O2-6.3151.173 5[M+H]+,133.036 7,118.151 62-羟基-4-甲基苯乙酮111.37C9H10O43.4183.035 7[M+H]+,165.125 3,137.057 1,122.015 3高香草酸121.39C8H8O-2.7121.152 7[M+H]+,92.027 3对甲基苯甲醛132.36C9H8O3-3.5165.024 1[M+H]+,147.036 1,119.194 6对香豆酸143.99C17H14O46.2283.037 1[M+H]+,267.026 3,239.048 1,221.085 36,7-二羟基-2-(2-苯基乙基)色酮155.21C19H18O4-4.1311.073 5[M+H]+,283.149 1,268.048 2,253.008 46-甲氧基-2-[2-(3′-甲氧基苯基)乙基]色酮166.36C19H18O32.1295.104 5[M+H]+,267.042 6,249.005 71,7-双(4-羟基苯基)-庚-4E,6E-二烯-3-酮176.69C21H22O103.9435.024 8[M+H]+,273.068 2,245.194 7,227.037 1柚皮素-7-O-葡萄糖苷187.12C22H22O10-4.3447.005 2[M+H]+,285.048 5,257.095 7,239.104 7,224.110 3樱黄素-4′-葡萄糖苷199.29C15H12O5-2.2273.047 4[M+H]+,229.005 7,211.048 7,183.027 4柚皮素209.49C12H14O3-3.7207.048 3[M+H]+,189.007 2,173.084 9,145.105 24-羟基-3-丁基邻苯二甲酸酯219.71C22H18O10-2.9443.048 2[M+H]+,290.058 2,274.037 1,256.102 37-O-没食子酰基儿茶素229.78C14H10O9-3.1323.038 1[M+H]+,154.003 7,136.037 2,108.048 5双没食子酸239.87C20H32O3-2.8321.108 4[M+H]+,303.055 4,259.036 42-羟基-6-三癸基苯甲酸249.89C33H40O19-2.7741.038 2[M+H]+,595.002 1,287.042 2,259.036 2山奈酚-3-O-(2G-α-L-鼠李糖基)-芸香糖苷259.95C30H50O3-3.9459.042 3[M+H]+,441.047 2,413.102 4大豆甾醇B2610.02C12H182.9163.037 1[M+H]+,134.003 3,119.033 21,2,4-三乙基苯2710.32C48H52O231.7981.037 2[M+H]+,953.046 1,935.005 2苯丙素糖苷2810.57C8H6O3-4.2151.120 3[M+H]+,123.047 2,105.006 35-羟基-苯并呋喃-2-酮2910.86C12H16O4-1.6225.010 3[M+H]+,168.042 3,150.102 1,122.030 52-羟基-5-丁氧基苯乙酸3011.23C8H8O4-3.6169.041 2[M+H]+,151.030 5,107.040 2,92.1042,64.041 3香草酸3111.29C10H12O3-1.6181.046 2[M+H]+,137.027 4,119.034 5,91.102 2水杨酸异丙酯3211.39C10H10O2-4.8163.038 2[M+H]+,148.001 2,120.101 4反式-2-甲氧基肉桂醛3311.55C22H22O102.9447.022 3[M+H]+,301.031 5,285.003 2,257.024 5,239.005 6鼠李柠檬素-3-O-鼠李糖甙3411.76C37H60O11-4.7681.065 6[M+H]+,549.038 5,521.002 4,503.010 724-O-乙酰基-亚氨基-3-O-β-D-吡喃木糖苷3512.18C40H64O11-5.6721.033 5[M+H]+,589.014 6,457.103 2,413.103 1齐墩果酸-3-O-β-D-吡喃木糖基-(1→2)-α-L-吡喃阿拉伯糖苷3612.27C30H46O7-6.3519.033 4[M+H]+,475.378 2,457.034 12-羟基丁二酸3712.29C22H20O13-1.3493.146 2[M+H]+,302.042 6,274.148 2,256.024 3槲皮素-3-O-葡萄糖醛酸6″-甲酯3812.39C26H24O15-5.2577.055 7[M+H]+,424.083 7,271.173 8,253.125 44,6-二-O-没食子酰基熊果苷3912.43C30H48O2-3.2441.004 7[M+H]+,423.037 2,379.006 3去氧齐墩果酸4012.48C30H36O74.6509.004 7[M+H]+,481.047 2,463.174 9苦参醇 M4112.49C48H77O17-2.3926.103 7[M+H]+,780.047 2,618.057 2,426.065 4大豆皂苷 Ⅰ4212.54C26H28O15-1.4581.184 6[M+H]+,432.372 8,270.046 2木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷4312.59C28H32O16-1.2625.136 8[M+H]+,479.037 2,317.008 4,289.064 2 异鼠李素-3-O-β-芸香糖苷4412.63C14H16O3-4.3233.294 6[M+H]+,187.057 2,169.112 5,159.094 6,131.264 9梣酮4512.71C27H28O16-5.5609.057 2[M+H]+,463.104 8,287.057 2,259.058 2,241.110 3山奈酚3-O-α-L-鼠李糖基-(1→2)-β-D-葡萄糖醛酸苷
续表1

序号保留时间/min分子式质量偏差质谱碎片化合物名称4612.88C10H14O2.5151.058 2[M+H]+香芹酮4713.39C29H32O15-5.3621.110 4[M+H]+,475.058 2,444.119 3,268.048 2,224.006 2芹菜素-7-O-α-L-鼠李糖(1→4)-6″-O-乙酰基-β-D-葡萄糖苷4813.54C13H20O3-3.7225.047 3[M+H]+,207.103 9Vomifoliol4913.72C18H16O4-4.9297.047 7[M+H]+,269.184 7,251.047 2,236.006 36-羟基-7-甲氧基-2-(2-苯基乙基)色酮5013.94C34H26O10-4.5595.026 6[M+H]+,567.056 2,549.006 5,519.035 77,4′,7″,4‴-四-O-穗花杉双黄酮5114.53C4H6O6-3.5151.046 5[M+H]+,133.002 5,89.041 9,61.093 12,3-二羟基琥珀酸5214.83C15H10O4-4.6255.057 4[M+H]+,237.008 2,193.103 8,165.037 2白杨素5315.06C18H20O5-3.1317.103 8[M+H]+,299.047 7,271.058 7,226.008 32′-羟基-4,4′,6′-三甲氧基二羟基查尔酮5415.46C12H14O4-3.3223.113 8[M+H]+,205.047 4,175.047 5,147.006 84-(4′-羟基-3′-,5′-二甲氧基苯基)-3-丁烯-2-酮5515.63C10H10O32.9179.005 8[M+H]+,151.284 6,136.068 9,118.047 9反式-阿魏醛5615.89C7H6O30.8139.047 1[M+H]+,121.008 7,93.046 3,65.046 9对羟基苯甲酸5715.91C13H16O53.7253.105 8[M+H]+,235.104 7,220.058 1,192.048 83,4,5-三甲氧基肉桂酸甲酯5816.23C22H22O103.3447.005 6[M+H]+,285.057 8,257.105 8,239.104 9,224.004 7刺槐素-7-葡萄糖苷5916.37C42H68O14-5.2797.005 9[M+H]+,434.036 1,159.004 2,121.036 4,115.001 8大豆皂苷 Ⅲ6016.51C9H8O2-2.7149.068 2[M+H]+,131.051 3,103.028 4肉桂酸6116.86C33H40O20-1.6757.388 2[M+H]+,595.005 8,449.047 2,287.007 1,山奈酚-3-芦丁-7-葡萄糖苷6217.09C33H39O20-5.3756.082 6[M+H]+,610.092 7,464.047 2,302.077 2,274.077 4槲皮素-3-O-(2G-α-L-鼠李糖基)-芸香糖苷6317.42C8H10O3-2.5155.001 3[M+H]+,137.012 5,109.011 73,4-二羟基苯乙醇6417.69C14H20O-2.8205.003 7[M+H]+,190.003 12-(对苯甲酰基)-5-甲基-1-己烯6517.97C13H22O2.7195.048 3[M+H]+,177.098 2香叶基丙酮6618.26C19H22O3-7.2321.061 4[M+H]+,303.036 1,275.003 76-香叶草基-7-羟基香豆素6718.49C11H18O22.6183.004 7[M+H]+,165.016 3桉醛6818.73C15H10O8-3.4319.071 5[M+H]+,291.027 4,273.057 1杨梅素6918.97C10H12O2-3.6165.008 5[M+H]+,147.093 7,132.000 54-羟基-3-甲氧基-1-丙烯基苯7019.22C6H6O2-0.6111.050 2[M+H]+,93.005 8,65.017 3儿茶酚7119.29C20H18O61.8355.104 7[M+H]+,327.104 1,299.037 2,281.040 88-异戊烯基山奈酚7219.47C13H162.3173.057 2[M+H]+,158.069 11,1,6-三甲基-1,2-二氢萘7319.51C19H22O6-3.8347.010 1[M+H]+,329.060 2,301.004 7,256.104 734-二羟基-3-(3′,4′-二甲氧基苄基)-7-甲氧基-色满7419.54C12H16O74.4273.105 7[M+H]+,111.058 2,93.054 6熊果苷7519.69C22H22O6-4.2383.284 6[M+H]+,339.057 7,321.096 3,306.094 7甘草利酮7619.87C15H10O8-3.9319.050 2[M+H]+,291.078 3,263.008 7,245.057 26-羟基槲皮素7720.06C41H80NO8P-1.8746.193 6[M+H]+,491.174 2,475.041 2磷脂酰乙醇胺7820.28C20H32O2-1.6305.036 1[M+H]+,287.005 8,243.047 1花生四烯酸7920.53C21H32O30.5333.058 2[M+H]+,302.036 2,284.051 112-羟基枞酸甲酯8020.85C6H12O21.4117.036 2[M+H]+,99.047 9,55.005 7己酸8120.88C20H40O-4.2297.005 2[M+H]+,281.015 2,249.005 8植醇8221.09C30H50O2.8427.173 9[M+H]+,409.058 3新羽扇豆醇8321.66C20H30O25.5303.004 7[M+H]+,285.001 3,257.058 2枞酸8421.93C16H22O4-1.1279.005 3[M+H]+,206.051 4邻苯二甲酸二丁酯

a-豆浆;b-发酵豆浆
图2 豆浆和发酵豆浆总离子流图
Fig.2 The total ion chromatogram of soymilk and fermented soymilk
84种化合物以黄酮类和有机酸类为主,其中黄酮类成分是AChE抑制剂中的一大类。李程勋等[17]通过UPLC-QTOF-MS从蚕豆花提取物中鉴定出107种成分,主要以黄酮类和生物碱类为主。
2.3 差异成分分析
为研究豆浆发酵前后成分变化,从鉴定得到的84个化合物中筛选差异成分,以变量影响投影(variable influence on projection,VIP)作为选择依据,选择VIP>1的成分作为差异成分。如图3所示,发现19个成分的含量在豆浆发酵前后存在明显差异。裴浩田[18]采用乙醇溶剂对莲不同部位(莲子心、去心莲子和莲房等)进行提取,随后通过UPLC-QTOF-MS鉴定各提取物中的化学成分主要是黄酮类成分,并通过差异成分分析得到31种差异成分。
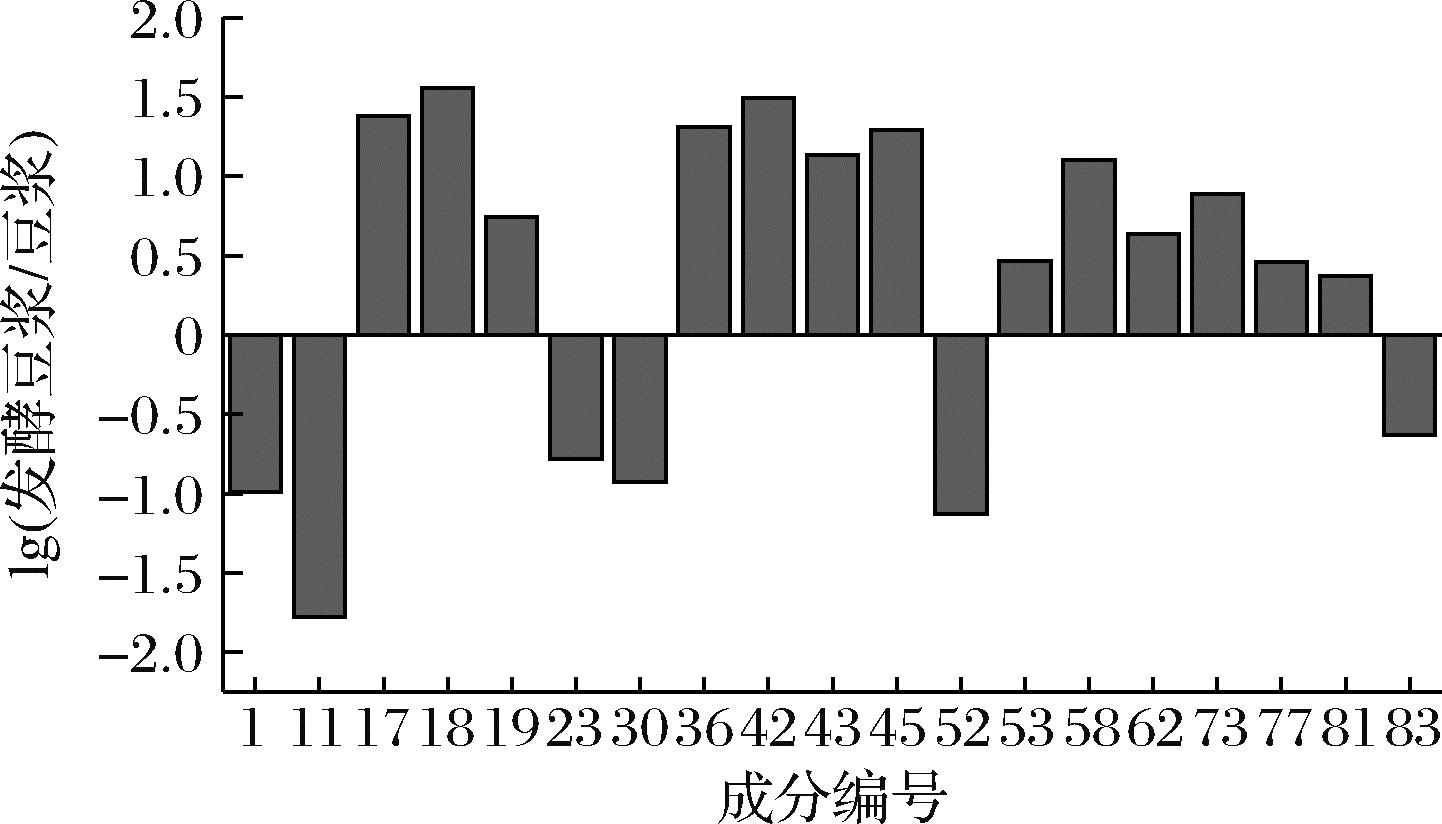
图3 豆浆与发酵豆浆差异成分分析
Fig.3 Analysis of the difference components between soymilk and fermented soymilk
由图3可知,发酵后含量明显增加的成分有13个,分别是刺槐素-7-葡萄糖苷(58)、樱黄素-4′-葡萄糖苷(18)、木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷(42)、柚皮素-7-O-葡萄糖苷(17)、2-羟基丁二酸(36)、山奈酚3-O-α-L-鼠李糖基-(1→2)-β-D-葡萄糖醛酸苷(45)、异鼠李素-3-O-β-芸香糖苷(43)、3,4-二羟基-3-(3′,4′-二甲氧基苄基)-7-甲氧基-色满(73)、柚皮素(19)、槲皮素-3-O-(2G-α-L-鼠李糖基)-芸香糖苷(62)、2′-羟基-4,4′,6′-三甲氧基二羟基查尔酮(53)、磷脂酰乙醇胺(77)和植醇(81)。发酵后含量明显减少的成分有6个,分别是枞酸(83)、2-羟基-6-三癸基苯甲酸(23)、香草酸(30)、5,6,7,3′,4′-五羟基-3-甲氧基黄酮(1)、白杨素(52)和高香草酸(11)。这些成分的变化主要是由于乳酸菌发酵引起的。乳酸菌发酵过程会产生多种酶系,从而破坏植物细胞壁,释放出可萃取多酚。并且乳酸菌能够将葡萄糖转化为丙酮酸,再经乳酸脱氢酶作用转化为乳酸,酸性环境可缓解酚类物质的氧化降解,因此发酵后酚类成分含量增加[19-20]。同时发酵产生的酶系会水解蛋白质产生游离氨基酸和短肽,氨基酸会进一步转化成各种醇类物质,与有机酸反应生成酯,从而引起发酵后枞酸、2-羟基-6-三癸基苯甲酸和香草酸等有机酸含量降低[21]。
2.4 分子对接
分子对接的结合能(负值)的绝对值越大,表示小分子与蛋白质的亲和能力越强。结合能≤-7 kcal/mol,表明小分子与蛋白质具有强相互作用,-7 kcal/mol<结合能≤-5 kcal/mol,表明小分子与蛋白质具有较强相互作用[22]。
图4为加兰他敏和19个差异成分与AChE的分子对接结果。从图4可知,加兰他敏与AChE的亲和能力最强,结合能为-10.6 kcal/mol,与文献报道的-10.4 kcal/mol接近[22]。在发酵后含量增加的13个成分中,有5个成分与AChE的结合能均低于-7 kcal/mol,即与AChE有强相互作用,分别是木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷(42)、樱黄素-4′-葡萄糖苷(18)、柚皮素-7-O-葡萄糖苷(17)、刺槐素-7-葡萄糖苷(58)和柚皮素(19),有6个成分与AChE的结合能在-7 kcal/mol和-5 kcal/mol之间,即与AChE有较强相互作用,分别是2-羟基丁二酸(36)、异鼠李素-3-O-β-芸香糖苷(43)、山奈酚3-O-α-L-鼠李糖基-(1→2)-β-D-葡萄糖醛酸苷(45)、槲皮素-3-O-(2G-α-L-鼠李糖基)-芸香糖苷(62)、3,4-二羟基-3-(3′,4′-二甲氧基苄基)-7-甲氧基-色满(73)和植醇(81)。在发酵后含量减少的6个成分中,白杨素(52)和枞酸(83)易与AChE结合,其结合能分别为-7.4 kcal/mol和-8.1 kcal/mol,即与AChE有强相互作用。因此,在发酵后含量增加的13个成分中,有11个成分易与AChE紧密结合,发酵后含量减少的6个成分中,有2个成分易与AChE紧密结合。豆浆经乳酸菌发酵后AChE抑制活性增强是各活性成分综合作用的效果。
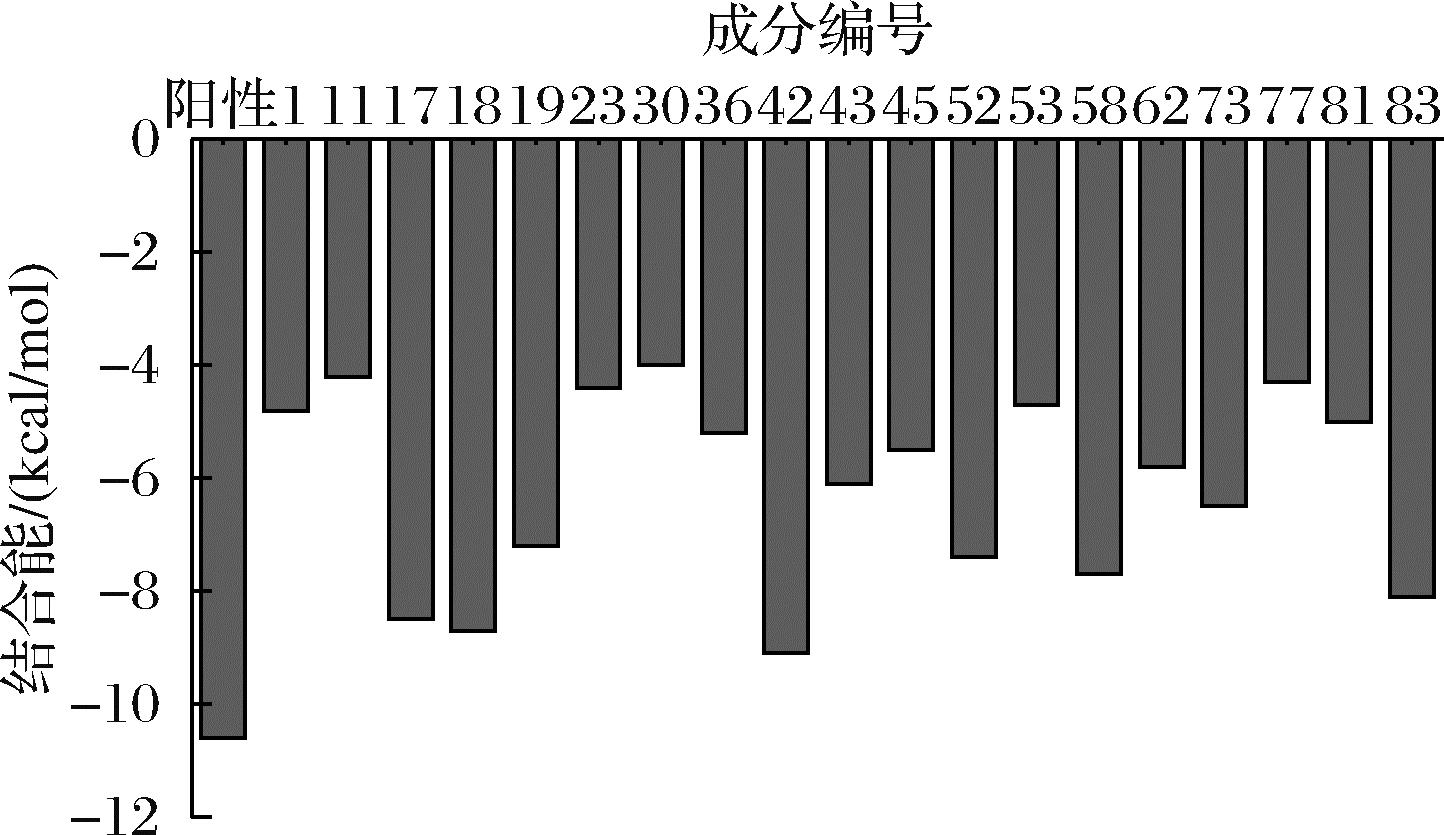
图4 加兰他敏和差异成分与AChE分子对接结合能
Fig.4 The binding energy of galantamine and different components molecule docking with AChE
结合图3差异成分分析和图4分子对接结合能可知,在结合图3差异成分分析和图4分子对接结合能可知,在11个含量增加的活性成分中,有3个成分的含量增长幅度最大且结合能低于-7 kcal/mol,分别是木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷(42)、樱黄素-4′-葡萄糖苷(18)、柚皮素-7-O-葡萄糖苷(17)。此外,发酵后有2个活性成分含量降低。图5为加兰他敏和这5个活性成分(化合物42、18、17、52和83)与AChE的分子对接可视化分析,表2为加兰他敏和这5个活性成分与AChE相互作用力归纳分析。研究表明,AChE有CAS和PAS两个活性位点,活性位点内的氨基酸残基为Asp72、Tyr334、Tyr121、Trp279、Trp84、Phe331、Ser200、Gly118、Glu327、His440,当化合物与这些氨基酸残基相互作用时,能阻碍AChE水解乙酰胆碱,从而降低AChE活性[23-24]。由图5和表2可知,5种活性成分在AChE上的结合位置与加兰他敏一致,均能结合到AChE的活性口袋内,且主要通过氢键和疏水相互作用与Asp72、Tyr334、Tyr121、Trp279、Phe331等氨基酸残基相结合,表现出较强的抑制效果。LI等[25]将加兰他敏、槲皮素和杨梅素与AChE进行分子对接,得到加兰他敏、槲皮素与杨梅素的结合能分别是-8.65、-6.74和-5.64 kcal/mol,可视化分析显示3个化合物均结合到AChE的活性位点,且主要通过氢键与AChE活性位点中的氨基酸残基相互作用。
表2 加兰他敏、活性成分与AChE相互作用力分析
Table 2 The interaction analysis of galantamine and active ingredients molecular docking with AChE

化合物ΔG/(kcal/mol)氢键作用力残基疏水作用力残基加兰他敏-10.6Tyr334、Phe331Asp72、Ser286Trp279、Tyr121木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷-9.1Tyr121、Asn85、Asp72、Phe330、Phe288、Arg289、Tyr70Trp279、Tyr121樱黄素-4′-葡萄糖苷-8.7Phe-288His-440Trp-279、Tyr-334、Phe-331柚皮素-7-O-葡萄糖苷-8.5Trp-84、Trp-279、Phe-331Trp-279、Tyr-334白杨素-7.4His440Phe330、Phe331、Tyr334、Gly117枞酸-8.1Tyr334Trp279、Phe331、Phe330、Phe290

a-加兰他敏-AChE;b-木犀草素-7-O-[β-D-吡喃葡萄糖基(1→6)]-β-D-葡萄糖苷-AChE;c-樱黄素-4′-葡萄糖苷-AChE; d-柚皮素-7-O-葡萄糖苷-AChE;e-白杨素-AChE;f-枞酸-AChE
图5 加兰他敏、活性成分与AChE的分子对接和相互作用力分析
Fig.5 The interaction analysis of galantamine and active ingredients molecular docking with AChE
3 结论
豆浆经乳酸菌发酵后AChE抑制活性显著增强,从豆浆与发酵豆浆提取物中鉴定出的化学成分主要是黄酮苷类和有机酸类,并从中筛选出19个成分在发酵前后存在明显含量变化,分子对接显示在发酵后含量增加的成分中有11个活性成分,在发酵后含量减少的成分中有2个活性成分,且这些活性成分主要通过氢键和疏水相互作用与AChE结合,进而抑制AChE活性。后期通过调整发酵菌株和发酵时间等手段,有望促进活性成分含量增加或抑制活性成分含量降低,从而更有利于增强发酵豆浆的AChE抑制活性。本研究表明发酵豆浆含有较多能抑制AChE的活性成分,因此,老年人群饮用发酵豆浆可有助于预防AD或辅助治疗AD,同时本研究为豆浆和发酵豆浆生理功能的进一步开发提供理论依据。
[1] WEN L R, BI H M, ZHOU X S, et al.Structure and activity of bioactive peptides produced from soybean proteins by enzymatic hydrolysis[J].Food Chemistry Advances, 2022, 1:100089.
[2] CHEN J X, CHEN Y L, HU J J, et al.Solid-state fermentation with Rhizopus oryzae HC-1 improves the metabolites profiling, antioxidant activity and gut microbiota modulation effect of soybeans[J].LWT, 2023, 187:115253.
[3] WANG M X, REN Q G, SHI Y C, et al.The effect of Alzheimer’s disease risk factors on brain aging in normal chineses:Cognitive aging and cognitive reserve[J].Neuroscience Letters, 2022, 771:136398.
[4] ZAVALA-OCAMPO L M, AGUIRRE-HERN NDEZ E, L
NDEZ E, L PEZ-CAMACHO P Y, et al.Acetylcholinesterase inhibition and antioxidant activity properties of Petiveria alliacea L.[J].Journal of Ethnopharmacology, 2022, 292:115239.
PEZ-CAMACHO P Y, et al.Acetylcholinesterase inhibition and antioxidant activity properties of Petiveria alliacea L.[J].Journal of Ethnopharmacology, 2022, 292:115239.
[5] AHMAD ALHAZMI H, ALBRATTY M.An update on the novel and approved drugs for Alzheimer disease[J].Saudi Pharmaceutical Journal, 2022, 30(12):1755-1764.
[6] YIANNOPOULOU K G, PAPAGEORGIOU S G.Current and future treatments in Alzheimer disease:An update[J].Journal of Central Nervous System Disease, 2020, 12:1179573520907397.
[7] 周瑶, 李娟, 贾凤霞, 等.单一及混合乳酸菌发酵对番木瓜汁品质的影响[J].食品与机械, 2024, 40(1):175-182;225.ZHOU Y, LI J, JIA F X, et al.Lactic acid fermentation of papaya juice using single and mixed Lactic acid bacteria[J].Food and Machinery, 2024, 40(1):175-182;225.
[8] DUAN W H, GUAN Q J, ZHANG H L, et al.Improving flavor, bioactivity, and changing metabolic profiles of goji juice by selected lactic acid bacteria fermentation[J].Food Chemistry, 2023, 408:135155.
[9] ZHENG Z J, WEI L Y, ZHU M L, et al.Effect of lactic acid bacteria co-fermentation on antioxidant activity and metabolomic profiles of a juice made from wolfberry and Longan[J].Food Research International, 2023, 174:113547
[10] KASHYAP P, CHOUDHARY H, KUMAR S.Dual anticholinesterase and antioxidant activity of selected plants used in Unani medicines and in silico studies of identified compounds from UPLC-QTOF analysis[J].Journal of Herbal Medicine, 2023, 41:100709.
[11] TERZIC M, FAYEZ S, FAHMY N M, et al.Chemical characterization of three different extracts obtained from Chelidonium majus L.(Greater celandine) with insights into their in vitro, in silico and network pharmacological properties[J].Fitoterapia, 2024, 174:105835.
[12] MEZIANT L, BACHIR-BEY M, BENSOUICI C, et al.Assessment of inhibitory properties of flavonoid-rich fig (Ficus carica L.) peel extracts against tyrosinase, α-glucosidase, urease and cholinesterases enzymes, and relationship with antioxidant activity[J].European Journal of Integrative Medicine, 2021, 43:101272.
[13] 黄淋. 核桃多肽及多酚对乙酰胆碱酯酶抑制作用研究[D].广州:华南理工大学, 2022.HUANG L.Inhibitory effect of walnut peptides and polyphenols on acetylcholinesterase[D].Guangzhou:South China University of Technology, 2022.
[14] GRELLA MIRANDA C, DOS SANTOS P D F, DO PRADO SILVA J T, et al.Influence of nanoencapsulated lutein on acetylcholinesterase activity:in vitro determination, kinetic parameters, and in silico docking simulations[J].Food Chemistry, 2020, 307:125523.
[15] 林紫兰, 沙小梅, 张志斌, 等.茅莓根提取物的体外抗氧化活性和α-葡萄糖苷酶、乙酰胆碱酯酶抑制能力研究[J].食品与发酵工业, 2021, 47(12):83-89.LIN Z L, SHA X M, ZHANG Z B, et al.In vitro antioxidant activities and inhibitory activities of α-glucosidase and acetylcholinesterase in Rubus parvifolius L.root extract[J].Food and Fermentation Industries, 2021, 47(12):83-89.
[16] 邹磊, 汪立君, 程永强, 等.豆豉提取物对乙酰胆碱酯酶的抑制能力[J].食品科学, 2006, 27(3):87-90.ZOU L, WANG L J, CHENG Y Q, et al.Acetylcholinesterase inhibitory activities of Douchi, a traditional Chinese food[J].Food Science, 2006, 27(3):87-90.
[17] 李程勋, 徐晓俞, 李爱萍, 等.蚕豆花水提取物的UPLC-ESI-QTOF质谱联用分析及抗氧化活性研究[J].热带亚热带植物学报, 2022, 30(5):663-675.LI C X, XU X Y, LI A P, et al.UPLC-ESI-QTOF mass spectrometry analysis and antioxidant activity of water extract from Vicia faba flowers[J].Journal of Tropical and Subtropical Botany, 2022, 30(5):663-675.
[18] 裴浩田. 莲不同部位的化学成分及去心莲子安神作用的研究[D].长春:吉林大学, 2021.PEI H T.Chemical constituents of differents parts from Nelumbo Nucifera Gaertn.and sedative effect of nelumbinis semen[D].Changchun:Jilin University, 2021.
[19] LIN S M, ZHANG X X, WANG J R, et al.Effect of lactic acid bacteria fermentation on bioactive components of black rice bran (Oryza sativa L.) with different milling fractions[J].Food Bioscience, 2024, 58:103684.
[20] ZHANG J P, XIA N, TENG J W, et al.Effect of lactic acid bacteria fermentation on extractable and non-extractable polyphenols of soybean milk:Influence of β-glucosidase and okara[J].Food Bioscience, 2023, 56:103326.
[21] 张盼玲. 发酵鹰嘴豆豆浆香气成分及代谢物变化研究[D].石河子:石河子大学, 2023.ZHANG P L.Research on aroma composition and metabolites of fermented chickpea milk changes[D].Shihezi:Shihezi University, 2023.
[22] 方洪, 韩沅沅, 谷丽华, 等.石菖蒲中乙酰胆碱酯酶抑制剂的筛选[J].中成药, 2022, 44(3):836-841.FANG H, HAN Y Y, GU L H, et al.Screening of acetylcholinesterase inhibitors in root of Acorus tatarinowii[J].Chinese Traditional Patent Medicine, 2022, 44(3):836-841.
[23] 李若雨, 邓萍.乙酰胆碱酯酶抑制剂多奈哌齐衍生物的理性设计[J].原子与分子物理学报, 2023, 40(2):7-11.LI R Y, DENG P.Rational design of acetylcholinesterase inhibitor based on donepezil[J].Journal of Atomic and Molecular Physics, 2023, 40(2):7-11.
[24] ABD EL-KARIM S S, ANWAR M M, AHMED N S, et al.Discovery of novel benzofuran-based derivatives as acetylcholinesterase inhibitors for the treatment of Alzheimer’s disease:Design, synthesis, biological evaluation, molecular docking and 3D-QSAR investigation[J].European Journal of Medicinal Chemistry, 2023, 260:115766.
[25] LI N N, YANG J, WANG C Y, et al.Screening bifunctional flavonoids of anti-cholinesterase and anti-glucosidase by in vitro and in silico studies:Quercetin, kaempferol and myricetin[J].Food Bioscience, 2023, 51:102312.