谷氨酰胺转氨酶(transglutaminase,TGase)是一种催化蛋白质之间的氨基与酰基间形成异型肽键,使蛋白质之间发生交联的酶[1]。由于这一特性,TGase被广泛应用于食品、制药、纺织等多个工业领域[2]。
在过去20年中,TGase因具有多种底物特异性、催化效率高和成本效益等特点而备受关注。自然界中TGase广泛存在,其中,微生物谷氨酰胺转氨酶(microbial TGase,MTGase)因具有不依赖Ca2+激活的特性而被广泛使用。MTGase主要来自链霉菌属(Streptomyces spp.)[3]和芽孢杆菌属(Bacillus spp.)[4]。日本味之素公司于1989年在S.mobaraenesis S-8112中发现了MTGase[5],并在1993年开始MTGase的工业化发酵生产,成为世界上最大的TGase生产商。随后,新的MTGase生产菌株也不断出现,其中包括:枯草芽孢杆菌(Bacillus subtilis)、链轮丝霉菌(S.ladakanum)、吸水链霉菌(Streptomyces hygroscopicus)等。不同来源的MTGase虽都具有非Ca2+依赖性,但其在酶学性质等方面存在着差异。同时,MTGase具有催化率高、底物特异性低等特点,备受研究者青睐[6]。国内对MTGase生产菌株的研究相对较晚,至2008年国内企业才真正实现MTGase的产业化生产。MTGase具有分子质量小以及空间结构灵活等优点,使它更加适合于工业化应用。在食品行业中的肉制品加工中,MTGase能够改变肉类蛋白质的功能,使肉制品的质构、风味以及外观得到改善,由此来提高产品的附加值,在乳制品和面制品等加工中也具有提高产品品质的功能。
本研究针对实验室现有两株茂源链霉菌:S.mobaraenesis CGMCC4.1851和S.mobaraenesis ATCC27441来源的TGase展开研究,首先确认菌株产TGase的催化能力并对其酶性质进行测定比较,之后将具有较优酶学性质的S.mobaraenesis CGMCC4.1851来源的TGase基因在大肠杆菌(Escherichia coli)BL21(DE3)中进行异源活性表达,为后续研究及工业化生产提供参考。
1 材料与方法
1.1 材料
1.1.1 菌株和质粒
S.mobaraenesis CGMCC4.1851,中国普通微生物菌种保藏管理中心(CGMCC);S.mobaraenesis ATCC27441,北京中原公司;质粒pET28a、pCDFDuet-1、pCOLDⅡ、pET-22b(+)、pET32a、pGEX-4T-1,TaKaRa公司;E.coli DH5α、E.coli BL21(DE3),美国Novagen公司。
1.1.2 主要试剂
N-carboxybenzoyl-L-glutaminyl-glycine(N-CBZ-Gln-Gly),吉尔生化(上海)有限公司;L-谷氨酸-γ-单羟胺酸,Sigma-Aldrich公司;还原型谷胱甘肽,上海麦克林生化科技股份有限公司;标准分子质量蛋白和12%(质量分数)Tris-glycine SDS-PAGE预制胶,ThermoFisher公司(上海);质粒小量抽提试剂盒、细菌基因组DNA提取试剂盒、DNA胶回收试剂盒,南京诺唯赞生物科技股份有限公司;氨苄青霉素、溶菌酶,生工生物工程(上海)股份有限公司;限制性内切酶、DNA连接酶、DNA聚合酶,TaKaRa(大连)公司;BeyoZonaseTM超级核酸酶肠激酶,碧云天生物技术有限公司;Enterokinase,翌圣生物科技(上海)股份有限公司;胰蛋白胨、麦芽提取物和酵母提取物,Oxoid(英国)公司;其他试剂均为国产分析纯。
1.1.3 仪器与设备
MiniAmp Plus Thermal Cycler PCR仪、miniGEL TANK蛋白质电泳系统,美国ThermoFisher公司;ALL SHENG Nano-300微量分光光度计,杭州奥盛;Tanon 2500B凝胶成像仪,上海天能;5427R高速冷冻微量离心机,德国Eppendorf公司;TU-100C恒温金属浴、LRH-250生化培养箱,上海一恒科学仪器有限公司;AKTA start蛋白纯化仪,美国Cytiva公司;Synergy H1酶标仪,美国Biotek公司。
1.1.4 培养基
高氏一号固体培养基(g/L):可溶性淀粉20、NaCl 0.5、KNO3 1、K2HPO4·3H2O 0.5、MgSO4·7H2O 0.5、FeSO4·7H2O 0.01,琼脂粉20,调节pH值至7.4~7.6。
LB固体培养基(g/L):胰蛋白胨10、酵母粉5、NaCl 10、琼脂粉20,pH 7.0。
S.mobaraenesis种子培养基(g/L):甘油25、蛋白胨20、酵母粉5、玉米浆2.5、MgSO4·7H2O 2.5、K2HPO4·3H2O 2,调节pH值至7.4。
S.mobaraenesis发酵培养基(g/L):甘油20、蛋白胨20、酵母粉5、玉米浆5、(NH4)2SO4 2.5、MgSO4·7H2O 2、K2HPO4·3H2O 4、KH2PO4·H2O 2、CaCO3 2,调节pH值至7.4。
LB培养基(g/L):胰蛋白胨10、酵母粉5、NaCl 10,pH 7.0。
1.2 实验方法
1.2.1 天然TGase的生产与纯化
将菌株S.mobaraenesis CGMCC4.1851和S.mobaraenesis ATCC27441的孢子涂布于高氏固体平板,30 ℃培养8 d,用无菌生理盐水收集平板上的孢子,分别接种于装有50 mL种子培养基的250 mL摇瓶中,30 ℃,200 r/min培养24 h。培养好的种子液按10%(体积分数)的接种量接入装有25 mL发酵培养基的250 mL摇瓶中,于30 ℃,200 r/min培养64 h。
将发酵液经7 000 r/min离心30 min后,取上清,在10~15 ℃下,经过分子质量为10 kDa超滤膜浓缩4倍后,加入一定体积预冷的无水乙醇(乙醇终体积分数60%),离心取沉淀,沉淀用20 mmol/L pH 8.0的Tris-HCl缓冲液溶解,9 000 r/min离心10 min去除不溶物后过0.22 μm滤膜,待用。使用离子交换柱SP70进行离子交换纯化。上样样品用含1.0 mol/L NaCl、20 mmol/L pH 8.0 Tris-HCl缓冲液的溶液作为洗脱液进行线性洗脱,并用Superdex 75柱(10/300GL,直径10 mm,长度300 mm)进行脱盐。
1.2.2 大肠杆菌重组菌的构建
1.2.2.1 编码成熟tg表达载体的构建与转化
由苏州金唯智公司基因合成S.mobaraenesis CGMCC4.1851基因组中的tg基因片段,并进行大肠杆菌密码子优化,命名为基因tgLD。以该片段为模板,设计分别含有两个不同酶切位点的两端引物,扩增得到TGase的成熟区序列。表达载体和目的基因进行双酶切并分别胶回收后,通过T4酶在16 ℃下连接2 h,连接产物转化到E.coli DH5α中,挑取抗性板上的单菌落进行菌落PCR,挑取阳性单克隆菌落送至测序得到测序正确的质粒。本实验中尝试了6种不同的质粒表达tgLD,所得表达质粒转化E.coli BL21(DE3),得到6株重组菌E.coli BL21(DE3) (pET28a((+)-tgLD)、E.coli BL21(DE3) (pCDFDuet-1-tgLD)、E.coli BL21(DE3) (pET32a-tgLD)、E.coli BL21(DE3) (pGEX-4T-1-tgLD)、E.coli BL21(DE3) (pCOLDⅡ-tgLD)和E.coli BL21(DE3) (pET-22b(+)-tgLD)。构建时所用的引物、质粒抗性等如表1所示。
表1 基因tg表达载体构建中所用引物
Table 1 Primers used in the construction of gene tg expression plasmids

质粒抗性酶切位点引物序列pET28a((+)-tgLDKan+Nco IL-1-F:atatCCATGGACTCAGATGATCGTGTTACXho IL-1-R:atatCTCGAGTTACGGCCAGCCCTGTTTAACpCDFDuet-1-tgLDStr+Nde IL-2-F:cgcgCATATGGACTCAGATGATCGTXho IL-2-R:atatCTCGAGCATCATCACCATCACCACTTACGGCCAGCCCTGpET32a-tgLDAmp+Nco IL-3-F:atatCTCGAGGACTCAGATGATCGTGTTACXba IL-3-R:cgcgTCTAGATTACGGCCAGCCCTGTTTAACpGEX-4T-1-tgLDAmp+BamH IL-4-F:aattGGATCCGACTCAGATGATCGTXho IL-4-R:atatCTCGAGTTACGGCCAGCCCTGpCOLDⅡ-tgLDAmp+Nde IL-5-F:cgcgCATATGGACTCAGATGATCGTXho IL-5-R:atatCTCGAGTTACGGCCAGCCCTGpET-22b(+)-tgLDAmp+Nco IL-6-F:atatCCATGGACTCAGATGATCGTGTTACXho IL-6-R:atatCTCGAGCGGCCAGCCCTGTTTAAC
1.2.2.2 含有基因pro-tg的重组质粒的构建与转化
以基因tgLD为模板,用引物L-7-F/R和L-8-F/R扩增得到含有肠激酶位点的pro区序列,分别克隆至表达载体pET-22b (+) Xho I位点和pCOLDⅡ Nde I-Xho I位点,得到表达载体pET-22b(+)-pro-EK和pCOLDⅡ-pro-EK。以pET-22b(+)-tgLD为模板,引物L-9-F/R、L-10-F/R分别扩增得到含有相应同源臂的基因tgLD。将上述两种质粒经双酶切线性化后与tgLD基因片段通过一步重组酶在37 ℃反应30 min进行连接,连接产物转化到E.coli DH5α中,得到测序正确的质粒,转化E.coli BL21(DE3),得到重组菌E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)和E.coli BL21(DE3) (pET-22b(+)-pro-EK-tgLD)。构建过程所用引物序列见表2。
表2 含有基因pro-tg的重组质粒构建中所用引物
Table 2 Primers used in the construction of recombinant plasmids with gene pro-tg

质粒酶切位点引物序列pET-22b(+)-pro-EKNco IL-7-F:ATATCCATGGACTCAGATGATCGTGTTACXho IL-7-R:ATATCTCGAGTTACGGCCAGCCCTGTTTAACpCOLDⅡ-pro-EKNde IL-8-F:cagcCATATGgacaatggcgcggggXho IL-8-R:TATACTCGAGTTTATCATCATCGTCGGGGGCCCGGAACGACGpET-22b(+)-pro-EK-tgLDXho IL-9-F:GTGGTGGTGGTGGTGCGGCCAGCCCTGTTTAACL-9-R:CGACGATGATGATAAAGACTCAGATGATCGTGTTACpCOLDⅡ-pro-EK-tgLDEcoR IL-10-F:GACGATGATGATAAAGACTCAGATGATCGTGTTACXho IL-10-R:CAGGTCGACAAGCTTGAATTCTTACGGCCAGCCCTGTTTAA
1.2.3 重组酶TGase与pro-TGase的表达
从-80 ℃保藏的重组菌甘油管中蘸取一环菌液,在LB平板活化后,挑取单克隆接入50 mL离心管(含5 mL LB培养基),200 r/min、37 ℃,培养过夜。以1%(体积分数)的接种量接至250 mL三角瓶中(含50 mL LB培养基),200 r/min、37 ℃培养。当菌体OD600达到一定值时,加入一定量的IPTG,诱导培养18 h。培养过程中使用的LB培养基需添加终质量浓度为100 μg/mL的氨苄青霉素。
1.2.4 重组菌细胞破壁
将发酵液于6 000 r/min离心10 min,收集菌体并用50 mmol/L pH 8.0 Tris-HCl缓冲液洗涤2次,沉淀加入裂解液[7](50 mmol/L Tris-HCl,2 mmol/L MgCl2,pH 8.0,1 mg/mL溶菌酶和10 U/mL benzonase),于200 r/min、37 ℃处理1 h后,6 000 r/min离心10 min,取上清液。
1.2.5 Pro-TGase体外活化
取200 μL含重组pro-TGase上清液加入2 μL的肠激酶Enterokinase(0.1 U/μL,25 mmol/L Tris-HCl,8.0)溶液,混合均匀,25 ℃过夜酶切(完全酶切需要16~24 h)。
1.2.6 TGase活力测定
TGase酶活力检测方法具体参照Folk and Cole的比色法进行检测[8]。10 μL TGase酶液,与100 μL A液(200 mmol/L pH 6.0 Tris-HCl、100 mmol/L盐酸羟胺、10 mmol/L还原型谷胱甘肽、30 mmol/L CBZ-Gln-Gly),在37 ℃条件下反应10 min,加入100 μL的终止液B(50 g/L) FeCl3溶液,含有3 mol/L HCl∶120 g/L三氯乙酸∶0.1 mol/L HCl=1∶1∶1,体积比)。反应体积为200 μL。采用酶标仪检测525 nm下的吸光值A525。酶活力定义为:在上述条件下每分钟催化1 μmol底物生产产物所需的酶量为一个酶活力单位U。
1.2.7 TGase酶学性质的测定
TGase的最适反应温度的测定,将纯化后的TGase溶于200 mmol/L Tris-HCl缓冲液(pH 6.0)中,分别测定25、37、40、45、50、55、60 ℃的酶活力。对于酶的热稳定性测定,将TGase溶液分别在25、37、40、45、50、55、60 ℃孵育30 min,37 ℃测定其残余酶活力。以热处理前酶液的酶活力为100%。
TGase的最适pH的测定,将纯化后的TGase分别溶于pH 3~8磷酸盐-柠檬酸缓冲液、pH 7~9 Tris-HCl缓冲液和pH 9~12 Gly-NaOH的缓冲液中,测定酶活力,确定酶的最适pH。对于酶的pH稳定性测定,将纯化后的TGase分别溶于pH 3~8磷酸盐-柠檬酸缓冲液、pH 7~9 Tris-HCl 缓冲液和pH 9~12 Gly-NaOH的缓冲液中放置60 min,37 ℃测定其残余酶活力。以pH处理前酶液的酶活力为100%。
酶半衰期测定方法:将纯化后的TGase溶于200 mmol/L Tris-HCl缓冲液(pH 6.0),将酶溶液分别置于50、55及60 ℃水浴中,每隔一定时间,37 ℃测定其残余酶活力。以热处理前酶液的酶活力为100%。用软件Origin 2019进行对数拟合,确定TGase在各温度下的半衰期。
酶动力学参数测定方法:用200 mmol/L Tris-HCl缓冲液(pH 6.0)配制不同浓度(5、10、15、20、30、50、100、150 mmol/L)的底物(CBZ-Gln-Gly),37 ℃条件下,分别测定酶催化不同浓度CBZ-Gln-Gly生成氧肟酸的速率。用软件Origin 2019进行非线性回归拟合,确定酶动力学参数Km值和kcat值。
1.2.8 蛋白浓度及SDS-PAGE电泳分析
使用Bradford蛋白试剂盒测定蛋白含量。将20 mg/mL的BSA母液稀释到终质量浓度为1、0.8、0.6、0.4、0.2、0.1 mg/mL,分别吸取10 μL不同浓度的蛋白标准样品与300 μL Bradford Reagent振荡混匀后,室温放置5~10 min,用酶标仪测定595 nm处的吸光值,以不含BSA的光吸收值为空白对照。使用12% NuPAGE Bis-Tris凝胶搭配NuPAGE MES SDS running buffer,200 V电压,进行35 min SDS-PAGE电泳。用NuPAGE凝胶进行变性凝胶电泳时,使用NuPAGE LDS样品缓冲液(4×)制备样品。
2 结果与分析
2.1 S.mobaraenesis来源的TGase纯化
将来源于菌株S.mobaraenesis CGMCC 4.1851和S.mobaraenesis ATCC27441的发酵液经过醇沉和离子交换后得到纯化的TGase,分别命名为TGLD和TGLC。SDS-PAGE电泳结果显示(图1),纯化后的TGase只含有单一蛋白条带,分子质量约为38 kDa,与理论分子质量一致。
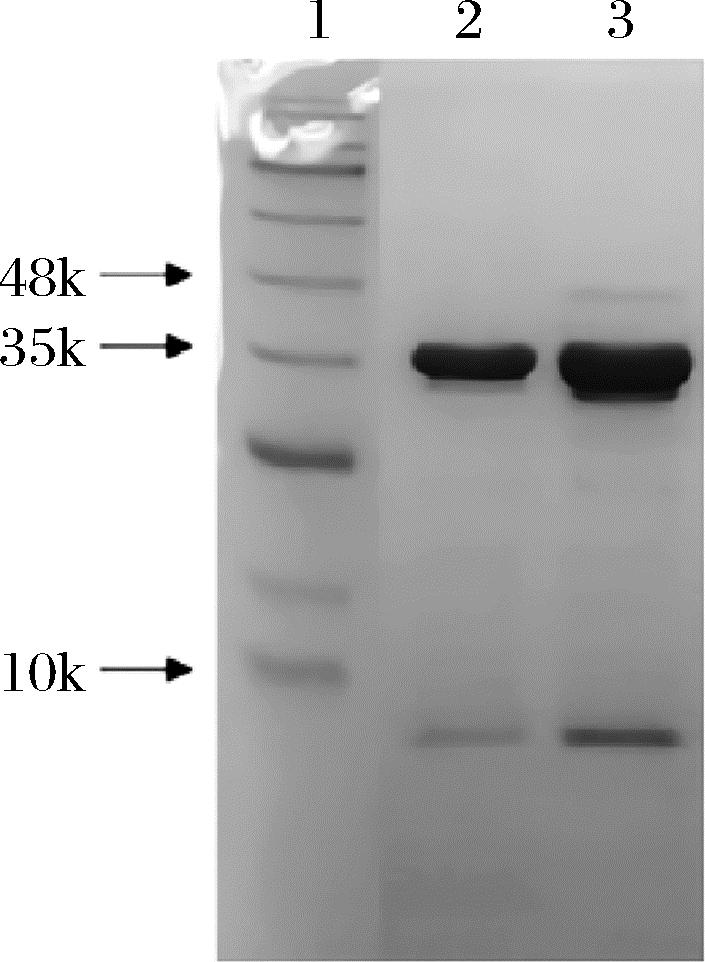
1-标准分子质量蛋白(Maker);2-纯化后TGLC酶液; 3-纯化后TGLD酶液
图1 纯化后TGLC和TGLD酶液的SDS-PAGE图
Fig.1 SDS-PAGE of purified TGLC and TGLD
2.2 TGase酶学性质分析
对纯化后TGLC和TGLD的酶学性质进行分析,检测包括最适反应pH、pH稳定性、最适反应温度、热稳定性及酶的动力学参数。如表3所示,TGLD的Km值为13.45 mmol/L 低于TGLC的Km值(18.54 mmol/L),说明TGLD对于底物的亲合力高于TGLC。TGLD的kcat值为18.49 s-1,高于TGLC的kcat值(13.76 s-1),并且TGLD的kcat/Km值为1 375 L/(mol·s),高于TGLC的kcat/Km值[742 L/(mol·s)]。这表明,TGLD的催化效率显著优于TGLC。如图2-a和图2-b所示,TGLC的最适反应温度为45 ℃,最适反应pH值为6.0。TGLD的最适反应温度为50 ℃,最适反应pH值为7.0。如图2-c所示,在55 ℃孵育30 min后,TGLD的相对残留酶活力为52%,而TGLC的相对残留酶活力只有34%。TGLD在50 ℃和55 ℃时的半衰期(t1/2)分别为130 min和20 min,分别比TGLC高3.1倍和2.6倍(表3)。TGLD的pH稳定性也要高于TGLC(图2-d)。TGLD可以在pH 5~12的范围内保持相对残留酶活力大于80%,而TGLC只能在pH 5~11的范围内保持同样的水平。以上结果均表明,TGLD表现出较好的稳定性。本研究纯化得到的两种TGase的最适温度与pH与已报道的S.hygroscopicus和S.mobaraenesis的TGase相似[5],而与来源于其他微生物如枯草芽孢杆菌(Bacillus subtilis)的TGase(最适温度为55 ℃,最适pH值为8.2)[9]和来源于动植物的TGase(最适温度为50 ℃和55 ℃,最适pH值为8.0和7.6)有显著区别[10-11]。
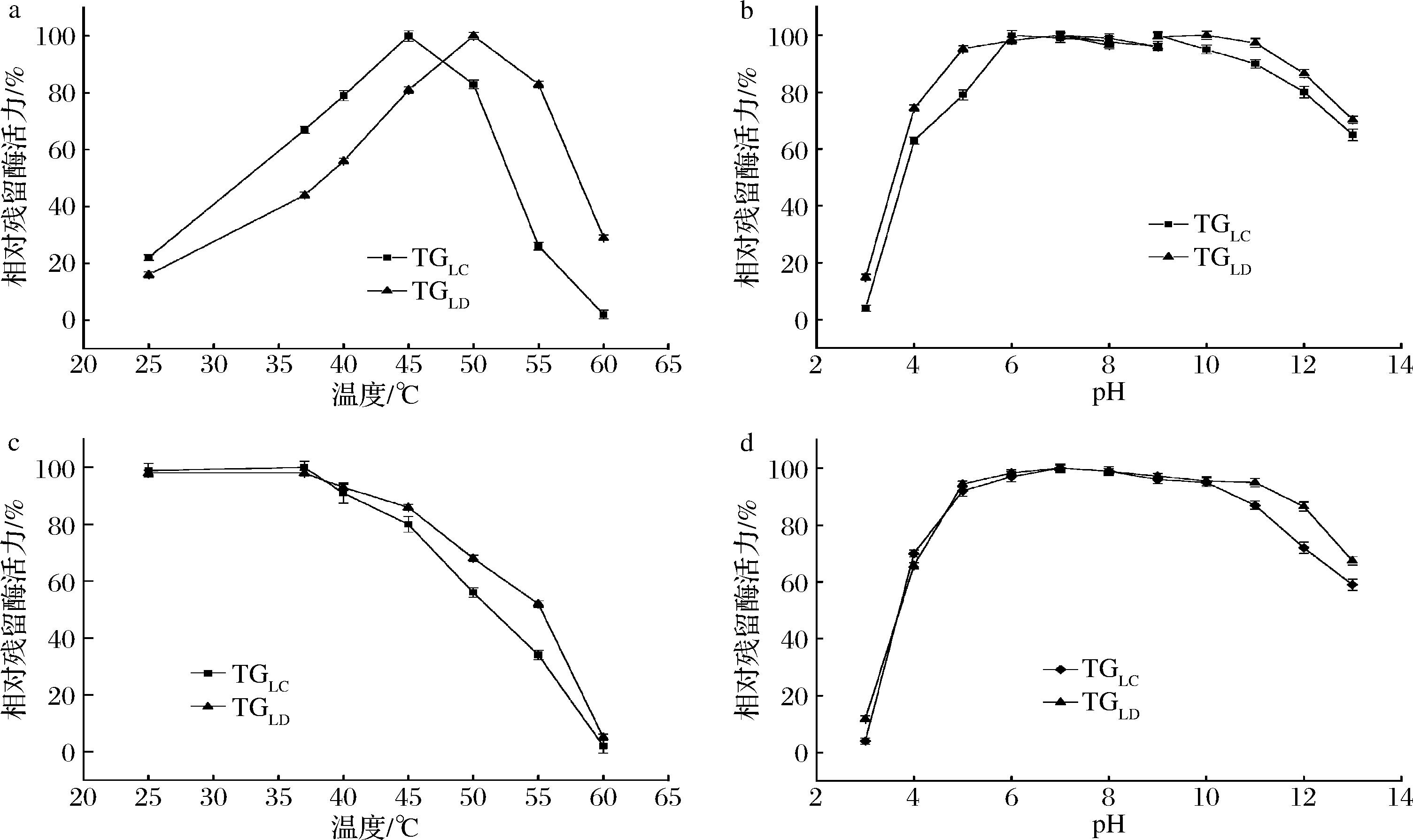
a-最适反应温度;b-最适反应pH;c-热稳定性;d-pH稳定性
图2 TGLD和TGLC的酶学性质对比
Fig.2 Comparison of properties between TGLD and TGLC
表3 不同TGases的半衰期 (t1/2)与动力学参数
Table 3 Half-life (t1/2) and kinetic parameters of different TGases

酶t1/2(min, 50 ℃)t1/2(min, 55 ℃)t1/2(min, 60 ℃)Km/(mmol/L)kcat/(S-1)kcat/Km [L/(mol·s)]TGLC325.51.718.54±1.2713.76742TGLD13020313.45±3.5918.491 375
综上,两株菌所产的TGase性质明显不同,TGLD较TGLC具有较高的催化效率和热稳定性,在食品、纺织和制药等行业有着更为广阔的应用前景。但TGLD的出发菌株S.mobaraenesis CGMCC 4.1851产量较低(2.07 U/mL),是限制其在工业领域应用关键因素,因此解决TGLD生产菌效价低的问题是主要的研究工作。接下来实验尝试在E.coli中异源表达TGLD,以期实现TGLD在E.coli中的高效活性表达。
2.3 TGLD在E.coli中的可溶性表达
采用6种不同的表达质粒,比较不同质粒对TGLD异源表达的影响。通常,TGase可以pro-TGase或TGase两种形式表达,当以pro-TGase形式表达,产生的pro- TGase通过外源蛋白酶处理后具有催化活性[12-13]。当以TGase形式进行表达,虽然简化了外源蛋白酶活化处理的步骤,但是其活性较差[14]。本研究首先考察了成熟TGLD在E.coli中是否可以成功表达,并获得具有活性的TGase。当在E.coli中利用具有不同特性的6种表达载体表达成熟tgLD基因时,重组菌株E.coli BL21(DE3) (pET28a(+)-tgLD)、E.coli BL21(DE3) (pCDFDuet-1-tgLD)、E.coli BL21(DE3) (pGEX-4T-1-tgLD)、E.coli BL21(DE3) (pCOLDⅡ-tgLD)、E.coli BL21(DE3) (pET-22b(+)-tgLD)和E.coli BL21(DE3) (pET32a-tgLD)在37 ℃培养至OD600达到0.6~0.7,添加IPTG至终浓度0.2 mmol/L,分别选择15、25 ℃诱导16 h,考察不同重组菌发酵生产重组TGLD的情况。在上述诱导温度下,E.coli BL21(DE3) (pET32a-tgLD)的发酵上清液检测到有活性目的酶蛋白,但其他5株重组菌的发酵液上清液均以无活性目的蛋白出现。其结果可能是由于那5株重组菌不适合重组TGLD的折叠和转运,表达的目的蛋白均以包涵体形式存在[15]。
如图3-a所示,重组菌E.coli BL21(DE3) (pET32a-tgLD)表达成熟TGase时,在全细胞、破壁上清及沉淀中有可溶性目的蛋白条带(55~70 kDa)。由表达载体pET32a-tgLD的图谱(图3-b)可知,TGLD与促溶标签TrxA以融合形式(TrxA-TGLD)表达,大小56 kDa。由此可推断出,重组菌E.coli BL21(DE3) (pET32a-tgLD)在添加0.2 mmol/L IPTG时,25 ℃诱导16 h后,表达的可溶性目的蛋白即为融合蛋白TrxA-TGLD。而TGLD与促溶标签TrxA之间存在肠激酶EK酶切位点,酶切后可得到活性TGLD。如图3-c所示,融合蛋白酶切后,56 kDa处条带随着酶切作用逐渐形成38 kDa处的条带,与成熟TGase条带大小一致,酶切前后TGLD的酶活力分别为0.23 U/mL和0.26 U/mL(图3-d)。

a-E.coli BL21(DE3) (pET32a-tgLD)中表达的SDS-PAGE[1-标准分子质量蛋白(Maker);2-pET32a未诱导;3-pET32a诱导; 4-pET32a-tgLD未诱导;5-pET32a-tgLD诱导;(2~5为全细胞);6-pET32a未诱导;7-pET32a诱导;8-pET32a-tgLD未诱导; 9-pET32a-tgLD诱导;(6~9为破壁上清液);10-pET32a未诱导;11-pET32a诱导;12-pET32a-tgLD未诱导;13-pET32a-tgLD诱导; (10~13为破壁沉淀)14-TGase标样];b-pET32a-tgLD部分质粒图谱;c-融合蛋白TrxA-TGLD肠激酶酶切前后的SDS-PAGE (1-标准分子质量蛋白(Maker);2-肠激酶酶切前;3/4-肠激酶酶切后);d-融合蛋白TrxA-TGLD肠激酶酶切前后的酶活力
图3 重组TGLD在E.coli BL21(DE3) (pET32a-tgLD)中的表达
Fig.3 Expression of recombinant TGLDin E.coli BL21 (DE3) (pET32a-tgLD)
为提高重组菌E.coli BL21(DE3) (pET32a-tgLD)的酶表达水平,对诱导温度、诱导剂浓度及诱导时间进行了优化(图4)。在重组菌E.coli BL21(DE3) (pET32a-tgLD)中诱导表达TGLD的最佳条件为:添加IPTG终浓度为0.2 mmol/L,25 ℃下诱导8 h,重组TGLD的酶活力为0.45 U/mL。虽然经过一系列的优化措施,实现了在E.coli中直接表达成熟TGase,但表达量较低,在表达过程中重组蛋白以不溶的包涵体为主要存在形式,这与KAWAI等[14]的研究结果一致。MARX等[16]研究已表明,pro-TGase可在E.coli中可溶性表达,但是pro-TGase需要进行体外活化才能得到活性TGase。为实现TGase在E.coli中高效表达,接下来尝试在E.coli中先表达pro-TGase,然后再建立相对简便可控的体外TGase活化体系。
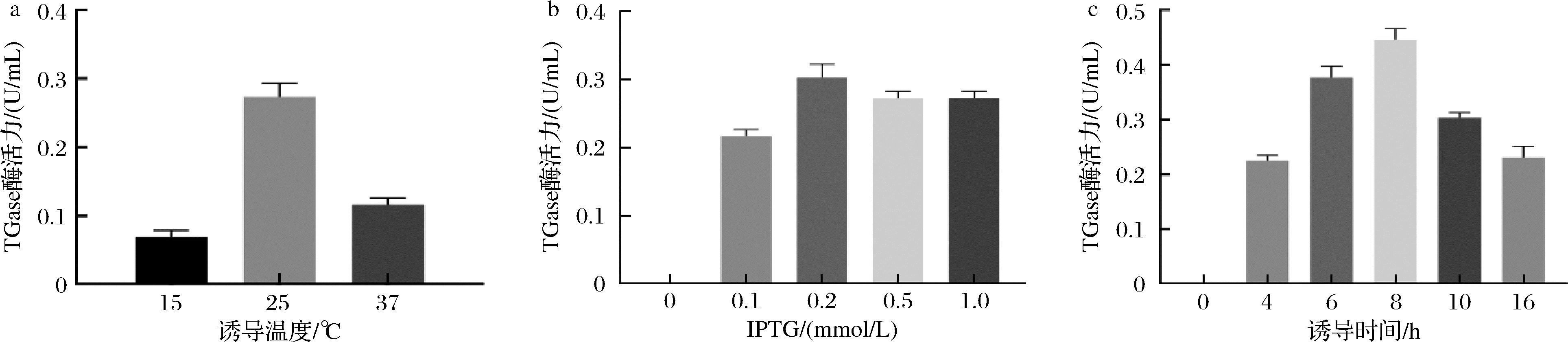
a-不同诱导温度的影响;b-不同IPTG浓度的影响;c-不同诱导时间的影响
图4 E.coli BL21(DE3) (pET32a-tgLD)表达TGLD的诱导条件优化
Fig.4 Optimization of the induction conditions of TGLD expression in E.coli BL21(DE3) (pET32a-tgLD)
2.4 Pro-TGLD在E.coli中的可溶性表达
2.4.1 Pro-TGLD体外特异性活化质粒的构建
S.mobaraensis来源的TGase合成方式为:首先以无活性的酶原pro-TGase的形式分泌到胞外,通过菌体自身的金属蛋白酶(TAMEP)去除pro区的41个氨基酸后形成具有活性的FRAP-TGase,而剩余的FRAP需要四肽酶去除,完成TGase的活化过程。目前报道的能够激活pro-TGase的蛋白酶主要有胰蛋白酶、蛋白酶K、TAMEP、dispase(来源于Bacillus polymyxa)等。在这些蛋白酶中,胰蛋白酶和蛋白酶K都是对酶原进行的非特异性切割,会导致MTG的不稳定。TAMEP目前不能实现体外制备,而dispase不仅表达量少,而且会切除C端His标签中的组氨酸残基,不利于后续的纯化[7]。参照WANG等[17]的研究,在pro-TGase的酶原区和成熟酶区之间插入一种特定的蛋白酶的识别位点(肠激酶、Enterokinase EK、DDDDK),实现了pro-TGase的特异性激活。
将tgLD的pro区分别克隆至pET-22b(+)和pCOLDⅡ的Nco I-Xho I和Nde I-Xho I酶切位点之间,连接转化。提取质粒,pET-22b(+)-pro-EK经Xho I,pCOLDⅡ-pro-EK经EcoR I和Xho I酶切后,分别与TGLD成熟区基因片段进行同源重组,PCR验证pro-EK-tgLD已成功连接至表达载体(图5)。凝胶电泳结果显示,pET-22b(+)-pro-EK-tgLD和pCOLDⅡ-pro-EK-tgLD中pro-EK-tgLD序列正确。
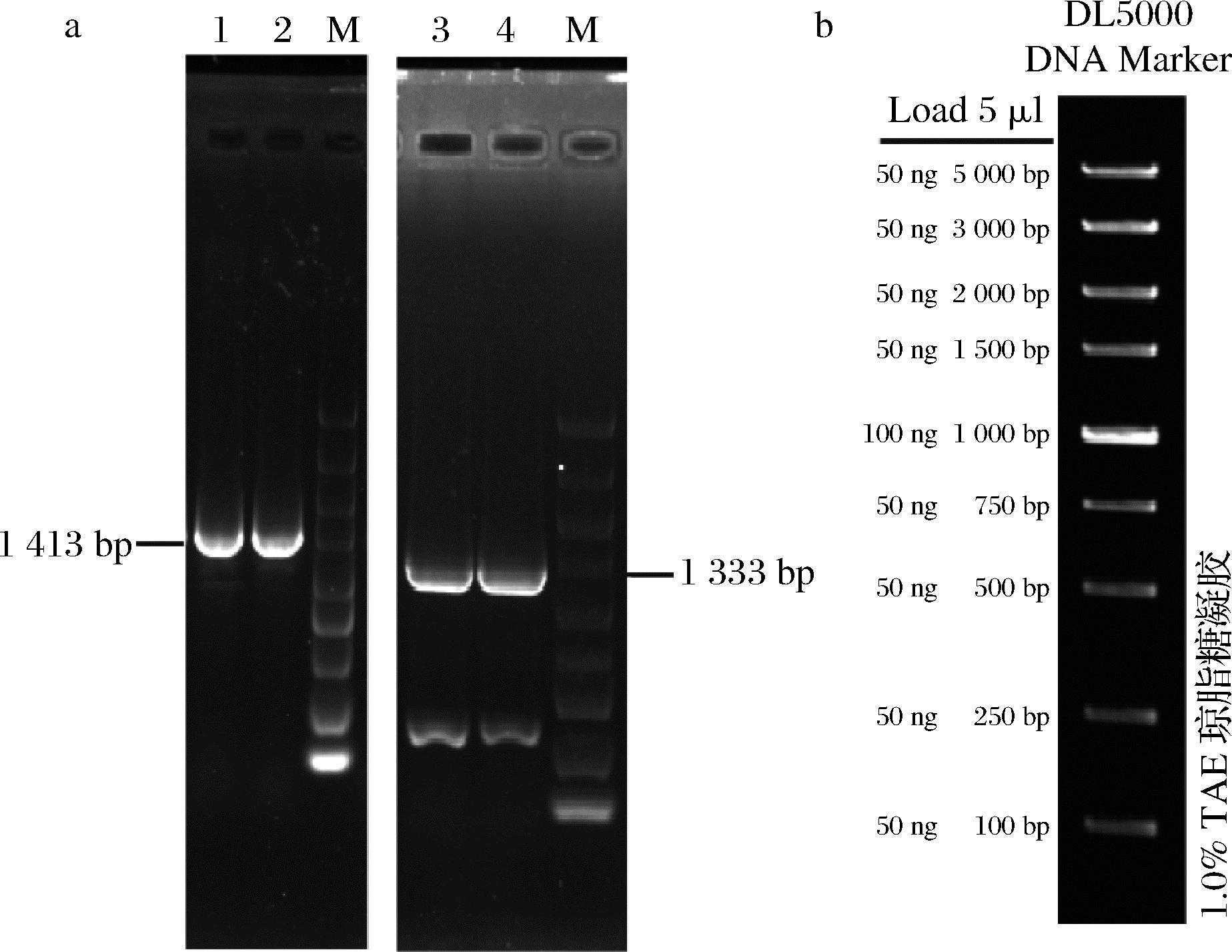
a-不同表达载体的验证(M-DL5000 DNA标准分子质量; 1、2-pET-22b(+)-pro-EK-tgLD的验证产物;3、4-pCOLDⅡ- pro-EK-tgLD的验证产物);b-DL5000 DNA Marker条带放大展示
图5 表达载体pET-22b(+)-pro-EK-tgLD和 pCOLDⅡ-pro-EK-tgLD验证
Fig.5 Validation of expression plasmids pET-22b(+)- pro-EK-tgLD and pCOLDⅡ-pro-EK-tgLD
2.4.2 重组Pro-TGLD在E.coli BL21(DE3) (pET-22b(+)-pro-EK-tgLD)中的表达
E.coli BL21(DE3) (pET-22b(+)-pro-EK-tgLD)在37 ℃培养至OD600值达到0.6~0.7时,添加IPTG至终浓度0.2 mmol/L,25 ℃诱导表达16 h。诱导后菌体破壁后的上清液中有目的条带(45 kDa)的表达(图6)。破壁上清液无法检测到酶活力,符合预期。而上清液经过肠激酶EK过夜酶切后,TGLD的酶活力为1.97 U/mL,结果表明,破壁上清液中的重组pro-TGLD可被肠激酶EK转化为活性TGase。
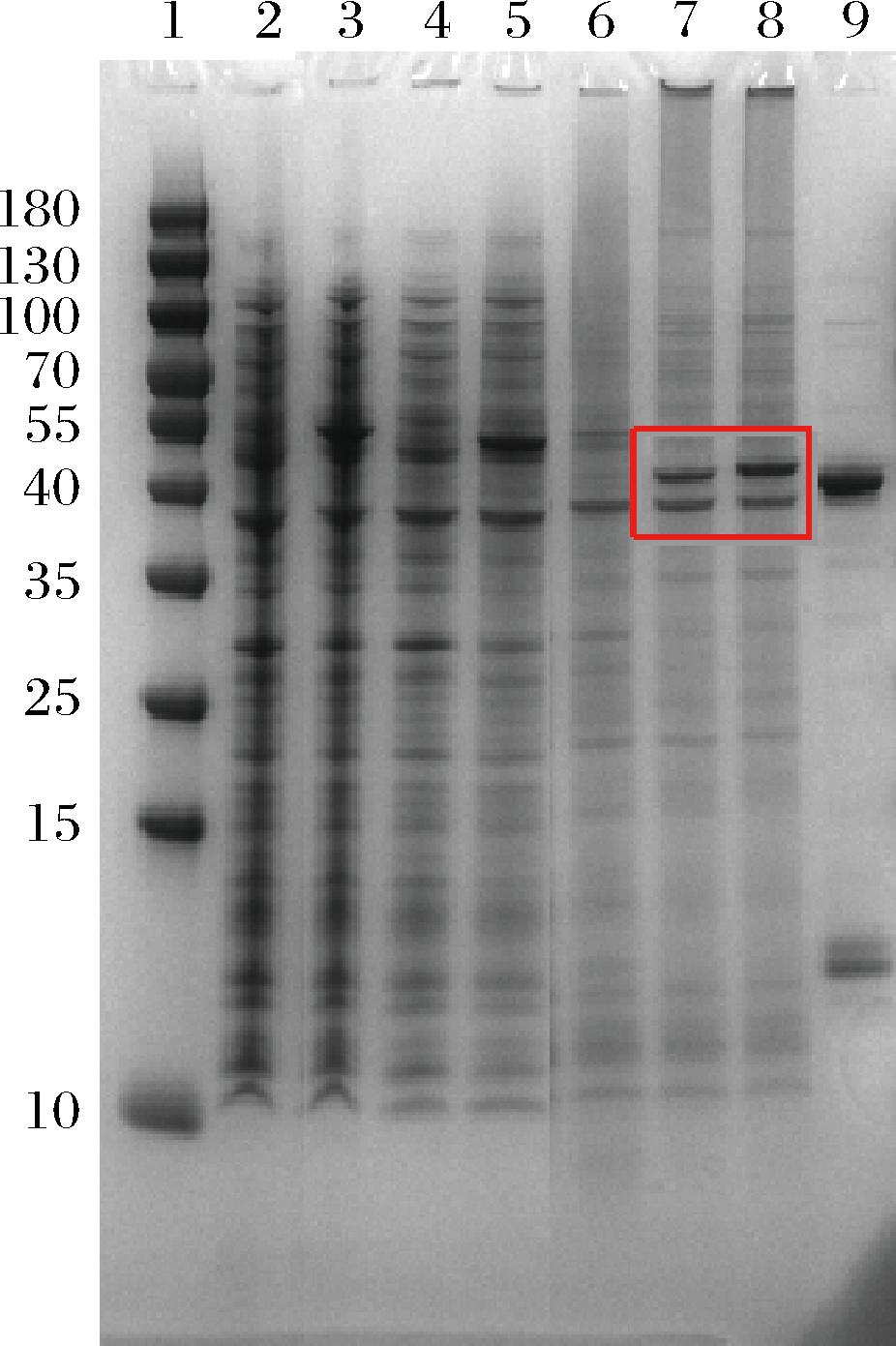
1-标准分子质量蛋白(Maker);2-pET-22b(+)空质粒发酵全细胞; 3-重组菌发酵全细胞;4-pET-22b(+)空质粒破壁上清液; 5-重组细胞破壁上清;6、7/8-经肠激酶处理的空质粒和 重组菌的破壁上清液;9-TGase标样
图6 重组pro-TGLD在E.coli BL21(DE3) (pET-22b(+)- pro-EK-tgLD)中表达及肠激酶体外活化的SDS-PAGE验证
Fig.6 SDS-PAGE validation of recombinant pro-TGLD expression in E.coli BL21(DE3) (pET-22b(+)-pro-EK-tgLD) and in vitro activationby EK
2.4.3 重组Pro-TGLD在E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)中的表达
E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)在37 ℃培养至OD600值达到0.6~0.7时,在冰水中冷却培养液到15 ℃,放置30 min,添加0.2 mmol/L IPTG,15 ℃诱导表达24 h。如图7所示,诱导后菌体破壁后的上清液中有目的条带(45 kDa)的表达。破壁上清液经过肠激酶EK过夜酶切后,TGLD的酶活为25.23 U/mL,结果表明,破壁上清中的重组pro-TGLD可被肠激酶EK高效转化为活性TGase。E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)中pro-TGLD的表达量显著高于E.coli BL21(DE3) (pET-22b(+)-pro-EK-tgLD)。
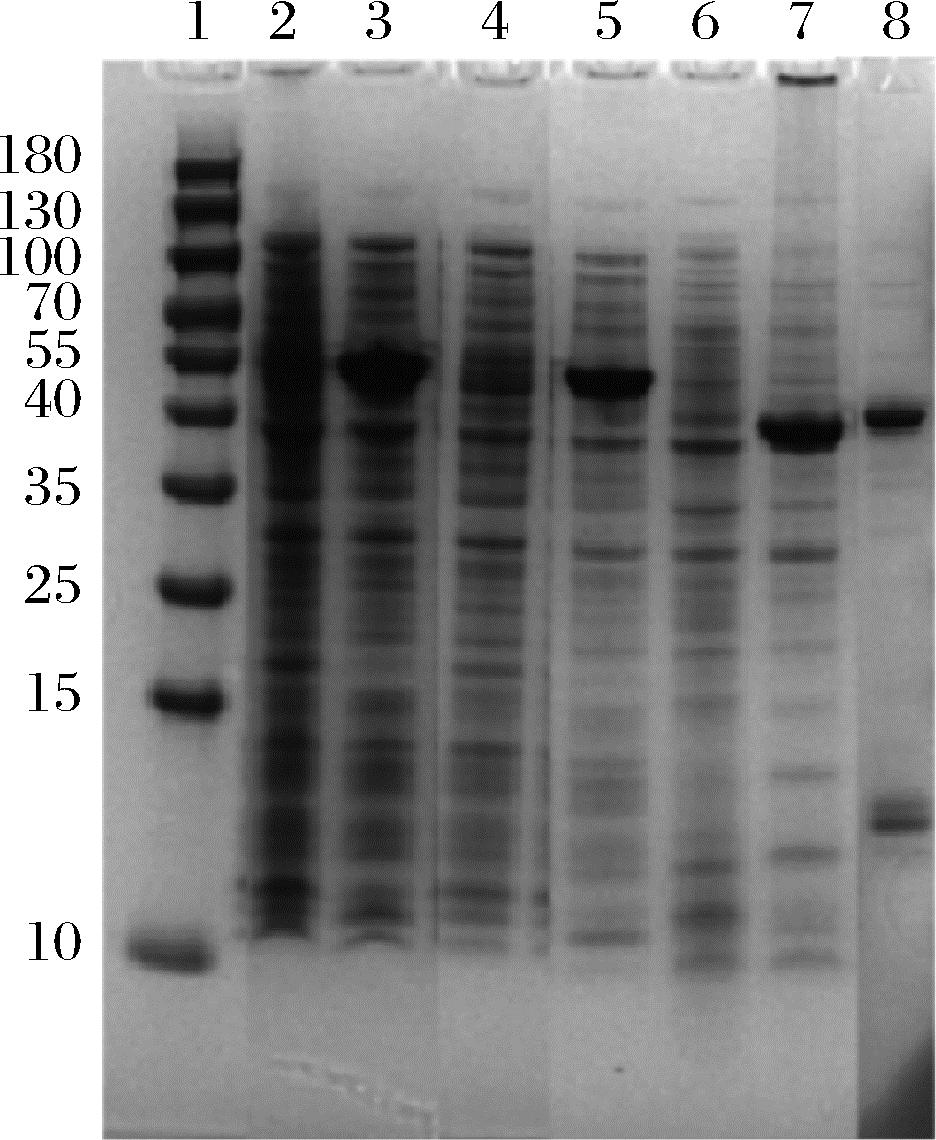
1-标准分子质量蛋白(Maker);2-pCOLDⅡ空质粒发酵全细胞; 3-重组菌发酵全细胞;4-pCOLDⅡ空质粒破壁上清液; 5、重组细胞破壁上清液;6、7-经肠激酶处理的空质粒和 重组菌的破壁上清液;8-TGase标样
图7 重组pro-TGLD在E.coli BL21(DE3) (pCOLDⅡ- pro-EK-tgLD)中表达及肠激酶体外活化的SDS-PAGE验证
Fig.7 SDS-PAGE validation of recombinant pro-TGLD expression in E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD) and in vitro activationby EK
目前链霉菌属的TGase或Pro-TGase基因己经在E. coli、B.subtilis、谷氨酸棒杆菌(Corynebacterium glutamicum)、酵母菌等多个宿主中成功表达(表4)。TGase在食品级表达宿主C. glutamicum和解脂酵母菌(Candida lipolytica)中的研究相对较少,但在这两种表达系统中统中产生的杂蛋白少。特别是C. glutamicum因其GRAS(Generally Recognized as Safe)的特性,生长速度快、营养需求低等优势,可能更容易实现异源表达TGase的工业生产。E.coli和B.subtilis两种表达系统是目前异源表达研究的首选,TGase在这两种底盘细胞中表达的研究较多,但在这两种表达系统中想获得活性TGase也较困难。本研究与已报道的将MTGase在E.coli 表达系统成功表达的案例相比(表4),表达量也是最高,说明通过重组E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)可以实现pro-TGase的高效可溶性表达。同时,也可以方便快捷地实现pro-TGase的活化,对后续研究具有一定的参考价值。值得考虑的是,在后期研究中需要探索更加高效且经济的方案,实现活性TGase在E.coli 中表达效率的进一步提高。
表4 MTGase在不同菌株中的异源表达
Table 4 Heterogenous expression of MTGase in different strains

载体表达菌株来源菌株酶活力或比活力/(U/mg)参考文献pET-28aE.coli BL21(DE3)S.mobaraenesis 1.51[18]pET-22bE.coli BL21(DE3)S.mobaraenesis 21.30[19]pET-32aE.coli Transsetta (DE3)S.mobaraenesis 3.03[20]Pmal-c5EvE.coli Star(DE3)S.mobaraenesis22.70[21]pWB980B.subtilis WB600S.mobaraenesis16.10[22]pINA1297Yarrowia lipolytica Po1 hS.mobaraenesis49.78[23]Pxmj19LC.glutamicum ATCC13032S.mobaraenesis54.80[24]
3 结论
本研究通过比较两个不同S.mobaraensis来源的TGase的酶学性质,筛选获得来源于S.mobaraenesis CGMCC 4.1851的TGase-TGLD,其具有较好的稳定性以及较高的催化活性。将TGLD基因分别构建到6种表达载体中,并将其转化E.coli BL21 (DE3),筛选获得重组菌E.coli BL21(DE3) (pET32a-tgLD)可以直接表达出有活性的成熟酶TGase,经过诱导条件优化,TGase酶活力达0.45 U/mL。改变TGase的表达形式,在重组菌E.coli BL21(DE3) (pCOLDⅡ-pro-EK-tgLD)中实现了pro-TGase的高效可溶性表达。经EK特异性活化,TGase酶活力达25.23 U/mL,与野生菌表达的TGLD相比较,其效价提高了11.19倍。
[1] YOKOYAMA K, NIO N, KIKUCHI Y.Properties and applications of microbial transglutaminase[J].Applied Microbiology and Biotechnology, 2004, 64(4):447-454.
[2] GASPAR A L C, DE G ES-FAVONI S P.Action of microbial transglutaminase (MTGase) in the modification of food proteins:A review[J].Food Chemistry, 2015, 171:315-322.
ES-FAVONI S P.Action of microbial transglutaminase (MTGase) in the modification of food proteins:A review[J].Food Chemistry, 2015, 171:315-322.
[3] CUI L, DU G C, ZHANG D X, et al.Purification and characterization of transglutaminase from a newly isolated Streptomyces hygroscopicus[J].Food Chemistry, 2007, 105(2):612-618.
[4] DE BARROS SOARES L H, ASSMANN F, Z CHIA AYUB M A.Purification and properties of a transglutaminase produced by a Bacillus circulans strain isolated from the Amazon environment[J].Biotechnology and Applied Biochemistry, 2003, 37(Pt 3):295-299.
CHIA AYUB M A.Purification and properties of a transglutaminase produced by a Bacillus circulans strain isolated from the Amazon environment[J].Biotechnology and Applied Biochemistry, 2003, 37(Pt 3):295-299.
[5] ANDO H, ADACHI M, UMEDA K, et al.Purification and characteristics of a novel transglutaminase derived from microorganisms[J].Agricultural and Biological Chemistry, 1989, 53(10):2613-2617.
[6] FOLK J E, CHUNG S I.Molecular and catalytic properties of transglutaminases[J].Advances in Enzymology and Related Areas of Molecular Biology, 1973, 38:109-191.
[7] MARX C K, HERTEL T C, PIETZSCH M.Random mutagenesis of a recombinant microbial transglutaminase for the generation of thermostable and heat-sensitive variants[J].Journal of Biotechnology, 2008, 136(3-4):156-162.
[8] FOLK J E, COLE P W.Transglutaminase:Mechanistic features of the active site as determined by kinetic and inhibitor studies[J].Biochimica et Biophysica Acta, 1966, 122(2):244-264.
[9] SUZUKI S, IZAWA Y, KOBAYASHI K, et al.Purification and characterization of novel transglutaminase from Bacillus subtilis spores[J].Bioscience, Biotechnology, and Biochemistry, 2000, 64(11):2344-2351
[10] WORRATAO A, YONGSAWATDIGUL J.Purification and characterization of transglutaminase from tropical Tilapia (Oreochromis niloticus)[J].Food Chemistry, 2005, 93(4):651-658.
[11] ICEKSON I, APELBAUM A.Evidence for transglutaminase activity in plant tissue[J].Plant Physiology, 1987, 84(4):972-974.
[12] ZOTZEL J, KELLER P, FUCHSBAUER H L.Transglutaminase from Streptomyces mobaraensis is activated by an endogenous metalloprotease[J].European Journal of Biochemistry, 2003, 270(15):3214-3222.
[13] ZOTZEL J, PASTERNACK R, PELZER C, et al.Activated transglutaminase from Streptomyces mobaraensis is processed by a tripeptidyl aminopeptidase in the final step[J].European Journal of Biochemistry, 2003, 270(20):4149-4155.
[14] KAWAI M, TAKEHANA S, TAKAGI H.High-level expression of the chemically synthesized gene for microbial transglutaminase from Streptoverticillium in Escherichia coli[J].Bioscience, Biotechnology, and Biochemistry, 1997, 61(5):830-835.
[15] TAKEHANA S, WASHIZU K, ANDO K, et al.Chemical synthesis of the gene for microbial transglutaminase from Streptoverticillium and its expression in Escherichia coli[J].Bioscience, Biotechnology, and Biochemistry, 1994, 58(1):88-92.
[16] MARX C K, HERTEL T C, PIETZSCH M.Soluble expression of a pro-transglutaminase from Streptomyces mobaraensis in Escherichia coli[J].Enzyme and Microbial Technology, 2007, 40(6):1543-1550.
[17] WANG K, WANG B, YANG H L, et al.New strategy for specific activation of recombinant microbial pro-transglutaminase by introducing an enterokinase cleavage site[J].Biotechnology Letters, 2013, 35(3):383-388.
[18] 舒畅. 谷氨酰胺转氨酶在大肠杆菌中的表达研究[D].合肥:合肥工业大学, 2016.SHU C.Study on the expression of transglutaminase in Escherichia coli[D].Hefei:Hefei University of Technology, 2016.
[19] 杜建辉. 谷氨酰胺转氨酶高效表达及热稳定性改造[D].无锡:江南大学, 2021.DU J H.High-level expression of transglutaminase and its thermal stability improvement[D].Wuxi:Jiangnan University, 2021.
[20] XUE T, ZHENG X H, SU X M, et al.Directed evolution of the transglutaminase from Streptomyces mobaraensis and its enhanced expression in Escherichia coli[J].Food Biotechnology, 2020, 34(1):42-61.
[21] SATO R, MINAMIHATA K, ARIYOSHI R, et al.Recombinant production of active microbial transglutaminase in E.coli by using self-cleavable zymogen with mutated propeptide[J].Protein Expression and Purification, 2020, 176:105730.
[22] FU L H, WANG Y, JU J S, et al.Extracellular production of active-form Streptomyces mobaraensis transglutaminase in Bacillus subtilis[J].Applied Microbiology and Biotechnology, 2020, 104(2):623-631.
[23] 任蕊蕊. Streptomyces mobaraense谷氨酰胺转氨酶在解脂耶氏酵母中的高效表达及分子改造[D].无锡:江南大学, 2018.REN R R.High expression and molecular modification of Streptomyces mobaraense transglutaminase in Yersinia lipolytica[D].Wuxi:Jiangnan University, 2018.
[24] 单孟颖. 谷氨酰胺转氨酶的定向进化及突变体结构与功能关系的研究[D].天津:天津科技大学, 2020.SHAN M Y.Directional evolution of transglutaminase and the relationship between mutant structure and function[D].Tianjin:Tianjin University of Science &Technology, 2020.