木质纤维素因具有可再生、储量大、成本低等优点已被用来生产一系列具有高附加值的生化产品[1]。但水解液制备过程中产生多种有毒物质,醛类物质如糠醛等能够引起细胞内活性氧(reactive oxygen species,ROS)积累,造成氧化胁迫[2-3],酚类物质如香草醛等会影响ATP合成继而抑制菌株生长发酵[4]。目前,主要通过水解液脱毒或菌株基因改造以提高菌株利用水解液的发酵性能,由于前者存在程序复杂,设备要求高的问题,通过基因工程提高微生物耐受性,是更加经济可行的途径[5-6]。
甘油是一种重要的平台化合物,被应用于国防、化妆、医药等多个领域的2 000多种产品的生产[7-8]。产甘油假丝酵母(Candida glycerinogenes)发酵生产甘油性能优良,具有转化率高、生产强度大等优点,在工业条件下甘油产量可达110 g/L以上,转化率超过50%[9]。且与其他传统酵母(如酿酒酵母)相比,对高渗、高温、酸、氧化胁迫等压力具有更强的耐受性,是一株可供开发抗逆基因的优良菌株[10-11]。
传统发酵法合成甘油的原料为淀粉、糖类等,成本较高[9],竞争粮食资源。以木质纤维素为原料,使用性能优良的改造菌株高效发酵纤维素水解液合成甘油,将解决甘油的生物合成竞争粮食资源的问题,并大大节省生产成本,更具有经济效益及可行性。
根据前期产甘油假丝酵母转录组学数据,选择7个对有机酸、醛类、酚类及过氧化物胁迫有潜在响应的基因CgGLNI、CgHLA5、CgGRX5、CgGCN4、CgGIS1、CgGTR1和CgDIP5,在C.glycerinogenes中过表达,并在胁迫条件下筛选出抗性效果较好的基因CgGCN4,进一步通过探究胁迫条件下过表达菌株的发酵生长性能,检测胞内ROS积累及细胞膜完整性探索过表达菌株的耐受机制,将其应用于未脱毒纤维素水解液开放式发酵,为未脱毒纤维素水解液的利用提供新思路及遗传资源。
1 材料与方法
1.1 材料
1.1.1 试剂与仪器
蛋白胨、酵母提取物,Oxiod公司;高浓酸性纤维素酶,夏盛酶制剂;丙三醇,上海阿拉丁化学试剂有限公司;玉米粉,北京鸿润宝顺科技有限公司;甘蔗渣,广西远特农业科技有限公司;尿素、柠檬酸、柠檬酸钠,国药集团上海化学试剂公司;DNA凝胶回收试剂盒、质粒提取试剂盒,江苏康为世纪生物科技有限公司;限制性内切酶,大连宝生物工程有限公司;碘化丙啶、ROS检测试剂盒,广州硕普有限公司;其他试剂均为国产分析纯,所用引物由亦欣生物科技(上海)有限公司合成。
EPORATOR PCR扩增仪,德国Ependorf公司;JY96-Ⅱ高效液相色谱仪,美国Agilent公司;TU-1810分光光度计,北京普析通用公司;synergy TMH4多功能酶标仪,美国伯腾仪器有限公司。
1.1.2 菌株与质粒
本研究中所使用的菌株和质粒如表1所示。
表1 本研究所用的菌株和质粒
Table 1 Strains and plasmids used in this study
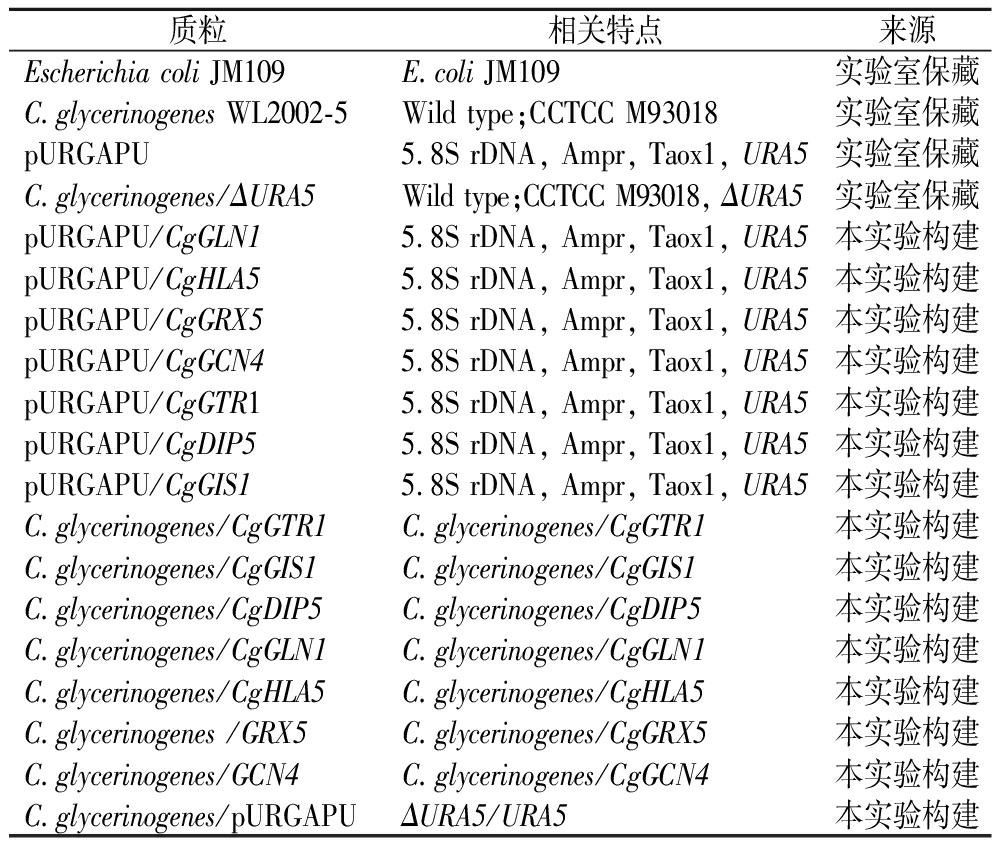
质粒相关特点来源Escherichia coli JM109E.coli JM109实验室保藏C.glycerinogenes WL2002-5Wild type;CCTCC M93018实验室保藏pURGAPU5.8S rDNA, Ampr, Taox1, URA5实验室保藏C.glycerinogenes/ΔURA5Wild type;CCTCC M93018, ΔURA5实验室保藏pURGAPU/CgGLN15.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgHLA55.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgGRX55.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgGCN45.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgGTR15.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgDIP55.8S rDNA, Ampr, Taox1, URA5本实验构建pURGAPU/CgGIS15.8S rDNA, Ampr, Taox1, URA5本实验构建C.glycerinogenes/CgGTR1C.glycerinogenes/CgGTR1本实验构建C.glycerinogenes/CgGIS1C.glycerinogenes/CgGIS1本实验构建C.glycerinogenes/CgDIP5C.glycerinogenes/CgDIP5本实验构建C.glycerinogenes/CgGLN1C.glycerinogenes/CgGLN1本实验构建C.glycerinogenes/CgHLA5C.glycerinogenes/CgHLA5本实验构建C.glycerinogenes /GRX5C.glycerinogenes/CgGRX5本实验构建C.glycerinogenes/GCN4C.glycerinogenes/CgGCN4本实验构建C.glycerinogenes/pURGAPUΔURA5/URA5本实验构建
本研究中所使用的引物如表2所示。
表2 本研究所用引物
Table 2 Primers used in this study

引物名称引物(5′~3′)酶切位点GRX5-FAACAAACACAATTACAAAAAATGTTTGCACGTTCTTTACTCCGGRX5-RGGTACCGCGGCCGCAGATCTCTCTTCCAAAGGTATAAGGGCATTTGCKPN1GLN1-FAACAAACACAATTACAAAAAATGTCTCCATTATTAGAAAAATCCCAAACGLN1-RGGTACCGCGGCCGCAGATCTCTCTTGAACTCTTGGTACATGTCAGCKPN1HLA5-FAACAAACACAATTACAAAAAATGAGTACAAATAGACATCTGCAGCCHLA5-RGGTACCGCGGCCGCAGATCTGATTGAGAGCTTTTCTCTCAAGGCATGKPN1GIS1-FAAAACACACAAACAAACACAATTACAAAAAATGGAAGCACCAGTGCTTGIS1-RGGTACCGCGGCCGCAGATCTCACATTCTCCTCGACAAGGAGGKPN1GTR1-FAAACAAACACAATTACAAAAAATGTCGTCAGGAAAGAAATTGTTGCTAATGGGGTR1-RGGTACCGCGGCCGCAGATCTATTGACAGTTTTGTTTTCAATTTTCTCAAATAAAKPN1DIP5-FAAACAAACACAATTACAAAAAATGATTCCTGCAAAAGACAATACACAAADIP5-RGGTACCGCGGCCGCAGATCTACACAACCAATAGTAGACTTTCATAATCCAGKPN1GCN4-FAACAAACACAATTACAAAAAATGTTACTCGGTGAAAATTTATATGCTACCAAGCN4-RGGTACCGCGGCCGCAGATCTAACTTTGGAATCTAGCAACTTCTTTAAATGTTCKPN1
1.1.3 培养基与培养方法
种子培养基(g/L):葡萄糖100.0,尿素2.0,玉米粉5.0。
高糖发酵培养基(g/L):葡萄糖250.0,尿素2.0,玉米粉5.0。根据实验需要添加糠醛3.0或香草醛2.0或乙酸3.5或同时添加以上3种毒性物质。
YPD培养基(g/L):葡萄糖20.0,蛋白胨20.0,酵母粉10.0。
MM培养基(g/L):YNB(无氨基氮源)6.7,葡萄糖20.0。
LB培养基(g/L):NaCl 10.0,蛋白胨20.0,酵母粉10.0。
未脱毒纤维素水解液发酵培养基(g/L):浓缩至葡萄糖浓度为100的纤维素水解液(经检测其中约含有糠醛1.2、乙酸1.4、酚类0.8),尿素2.0,玉米粉5.0。
除纤维素水解液培养基外,上述培养基均经120 ℃,灭菌15 min。
种子培养:从YPD固体平板上挑取单菌落转接到种子培养基,32 ℃,125 r/min(往复式)培养18 h。
摇瓶发酵培养:250 mL三角瓶中装液量为20 mL,接种时保持初始OD600值为0.2;32 ℃,125 r/min(往复式)培养。每12 h取样用于检测菌株生长及发酵情况分析。
点板验证:从YPD平板上挑取单菌落于种子培养基中培养12~18 h,取1 mL培养液离心收集菌体,PBS缓冲液洗涤2次并稀释至OD600值为1,随后按照10-4~100进行梯度稀释,取1 μL点种于分别含3.0 g/L糠醛,2.0 g/L香草醛,3.5 g/L乙酸或同时含3.0 g/L糠醛,2.0 g/L香草醛,3.5 g/L乙酸的YPD培养基平板上,点种于无添加毒性物质的YPD平板上作为空白对照实验组,30 ℃培养48~72 h。
1.2 实验方法
1.2.1 菌株改造
以基因GCN4为例,使用GCN4-F/GCN4-R从C.glycerinogenes基因组中PCR扩增获得CgGCN4基因片段,纯化后,片段经KPNI单酶切,与同样经KPNI单酶切的载体pURGAP连接,获得重组载体pURGAP-CgGCN4。重组载体经KPNI单酶切纯化后,转化进入感受态C.glycerinogenes URA5中,获得重组菌C.glycerinogenes/CgGCN4。
1.2.2 未脱毒蔗渣纤维素水解液制备
微波碱预处理:甘蔗渣磨碎过60目筛,105 ℃烘干至恒重,备用。恒重蔗渣与3%NaOH溶液的固液比保持为1∶20 (g∶mL),混合均匀。微波功率539 W处理10 min,静置至恒温后8 000 r/min离心10 min固液分离滤除黑液,得到固体部分为预处理后的粗纤维。使用1 mol/L盐酸调节粗纤维pH值至中性,留待后续使用。
酶水解:将经碱预处理后的甘蔗渣粗纤维不进行水洗按照原料质量补充0.1 mol/L柠檬酸-柠檬酸钠缓冲体系至其比例为1∶20 (g∶mL),50 ℃,180 r/min,添加酸性纤维素酶25 FPU/g,酶解72 h,固液分离后所得液体为纤维素水解液,60 ℃磁力搅拌器加热浓缩至葡萄糖质量浓度为100 g/L,储存在-20 ℃待用。
1.2.3 胞内ROS水平测定
参考WANG等[12]方法进行测定。
1.2.4 细胞膜完整性检测
参考WU等[13]的方法进行调整。4 ℃,6 000 r/min离心2 min收集在添加3.0 g/L糠醛、2.0 g/L香草醛、3.5 g/L乙酸及未添加毒性物质的高糖培养基中培养至对数期的菌体。PBS溶液洗涤2次后重悬于其中,调整细胞浓度使OD600为0.5~1.0,加入碘化丙啶染色液。4 ℃避光10 min。PBS溶液洗涤2次后再次重悬。使用多功能酶标仪在激发波长530 nm,发射波长620 nm,增益80的条件下检测荧光强度的变化。
1.2.5 分析方法
OD600利用分光光度计测定发酵液在波长600 nm下的吸光度。
用高效液相色谱示差法检测发酵液中葡萄糖、甘油,色谱柱为Aminex HPX-87H,柱温60 ℃,进样量10 μL。流动相为5.0 mmol/L H2SO4溶液,流速为0.6 mL/min。使用高效液相色谱紫外法检测水解液中糠醛、乙酸,流动相、条件等同上。用Folin-Ciocalteu比色法[14]测定水解液中酚类。
2 结果与分析
2.1 C.glycerinogenes对糠醛、香草醛、乙酸及未脱毒水解液的耐受性能
如图1所示,在添加1.0 g/L香草醛的高渗甘油发酵培养基进行发酵时,C.glycerinogenes生长被抑制率为20.0%,在2.0 g/L香草醛的胁迫下,OD600值最高仅为22.3,菌株生长被抑制率达到52.4%;在1.8 g/L糠醛胁迫下,菌株生长被抑制率为19.2%,在3.5 g/L糠醛胁迫下,OD600最高为27.5,菌株生长被抑制率达到41.3%;在2.5 g/L乙酸的胁迫下,菌株被抑制程度仅为6.2%,在5.0 g/L乙酸胁迫下,OD600最高为40.0,菌株生长被抑制率仅为14.8%。当菌株在浓缩至葡萄糖质量浓度为100 g/L的纤维素水解液中发酵时,菌株生物量相当于普通高糖发酵的52.5%,而浓缩至葡萄糖质量浓度为250 g/L的未脱毒纤维素水解液中菌株无生长现象。
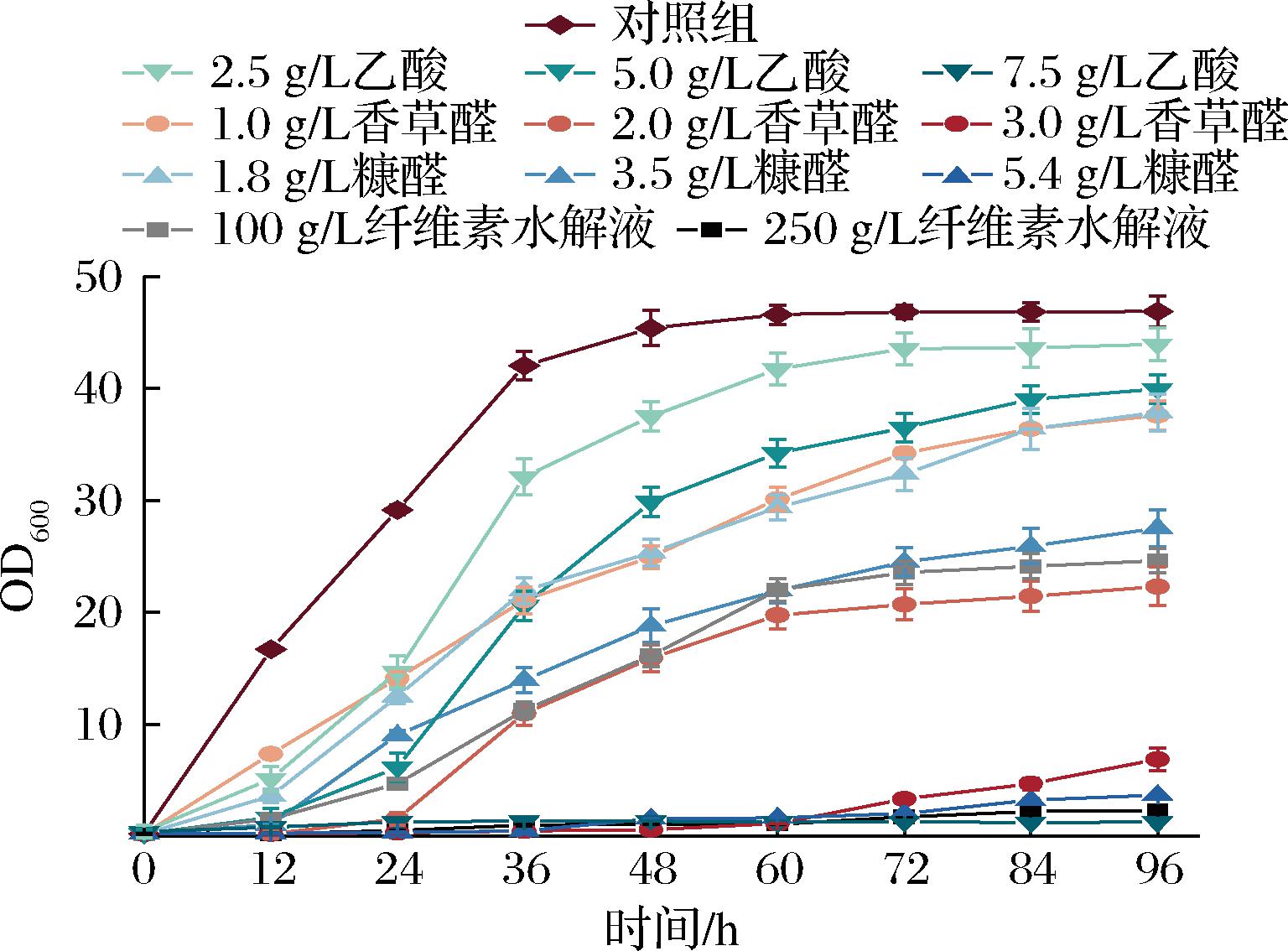
图1 高渗下乙酸、糠醛、香草醛及高度浓缩的未脱毒 纤维素水解液对C.glycerinogenes的生长抑制作用
Fig.1 Growth inhibition of C.glycerinogenes by acetic acid, furfural, vanillin under hyperosmotic conditions and high concentration undetoxified hydrolysate
当香草醛、糠醛、乙酸的添加量翻倍时,菌株生长被抑制率增加至2倍以上,延滞期增加至12 h以上。当毒性物质添加量至初始添加量的3倍,除添加3.0 g/L香草醛时菌株在60 h后出现生长情况外,添加5.4 g/L糠醛和7.5 g/L乙酸的条件下,C.glycerinogenes生长被抑制率达90%以上。而未脱毒纤维素水解液中所含毒性物质种类多,经浓缩后对于菌株抑制程度更大。因此针对水解液中的毒性物质进行抗性基因筛选,构建抗性重组菌株是改善C.glycerinogenes发酵利用未脱毒纤维素水解液性能的有效方法。
2.2 抗性工程菌的构建及筛选
过表达前期转录组学数据中潜在的相关抗逆基因CgGLNI、CgHLA5、CgGRX5、CgGCN4、CgGIS1、CgGTR1和CgDIP5。为筛选性能优良的抗性工程菌株,将以上重组菌株点种于同时添加有1.2 g/L糠醛、1.4 g/L乙酸、0.8 g/L香草醛的复合抑制的模拟水解液培养基平板上。
在10-3、10-4梯度下C.glycerinogenes/GLN1、C.glycerinogenes/GCN4、C.glycerinogenes/GRX5、C.glycerinogenes/HLA5均表现出比对照菌株更好的生长效果,且C.glycerinogenes/GCN4、C.glycerinogenes/GRX5在10-4浓度下表现出相比于其余改造菌株更好的生长情况,说明对于模拟水解液,这两株重组菌株具备更好的抗胁迫能力(图2)。

图2 重组菌模拟水解液培养基中的耐受性
Fig.2 Tolerance of resistant recombinant C.glycerinogenes in simulated hydrolysate
对2株性能良好的重组菌株进一步进行点板,结果表明,在YPD培养基中,改造菌株与对照菌株生长情况良好,在分别添加有2.0 g/L香草醛,3.0 g/L糠醛,3.5 g/L乙酸的抗性平板中,C.glycerinogenes/GRX5、C.glycerinogenes/GCN4都展现出比对照菌株更好的抗胁迫能力,且C.glycerinogenes/GCN4的生长性能明显优于C.glycerinogenes/GRX5。同时添加3种毒性物质的抗性平板中,由于毒性物质的协同抑制作用超过菌株耐受范围,3株菌株均未出现生长现象(图3)。下文近一步对抗胁迫能力最优的重组菌株C.glycerinogenes/GCN4的性能进行考察。

图3 重组菌株在不同物质胁迫条件下的耐受性
Fig.3 Tolerance of recombinant C.glycerinogenes under different material stress conditions
2.3 过表达CgGCN4对C.glycerinogenes发酵及生长性能的影响
为进一步考察过表达CgGCN4对于产甘油假丝酵母的生长发酵性能的影响,分别在未添加胁迫条件的高渗培养基中、添加3.0 g/L糠醛或2.0 g/L香草醛或3.5 g/L乙酸的高渗培养基中进行发酵。
无胁迫条件下,发酵96 h,重组菌株耗糖速率比对照菌株降低14.3%(图4-a);甘油产量提高17.9%,达到95.7 g/L(图4-b);生物量提高5.2%(图4-c),表明无胁迫条件下,过表达CgGCN4的重组菌株不能增强对葡萄糖的摄取,但可促进菌株生长,提高甘油产量。
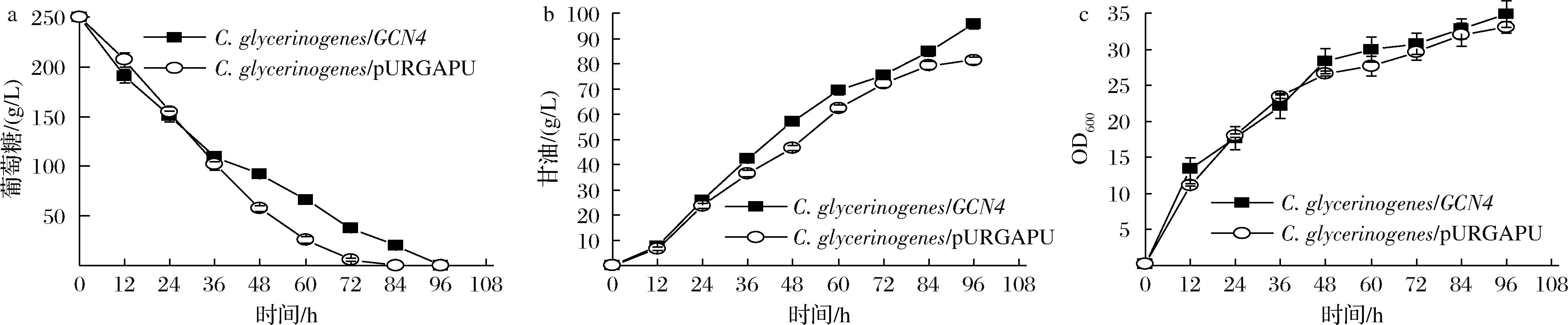
a-葡萄糖消耗;b-甘油生成;c-生长曲线
图4 无胁迫条件下C.glycerinogenes/GCN4及对照菌株的生长发酵情况
Fig.4 Growth and fermentation of C.glycerinogenes/GCN4 and control strains under stress-free conditions
在3.0 g/L糠醛的胁迫下,发酵96 h,C.glycerinogenes/GCN4、对照菌株分别耗糖210.0、191.0 g/L。与对照菌株相比,改造菌株耗糖速率提高了9.9%,达到2.2 g/(L·h)(图5-a);改造菌株甘油产量提高了23.4%,达到62.7 g/L(图5-b);与对照菌株生物量为20.6相比,改造菌株生物量提高了25.2%,OD600值达到25.8(图5-c)。表明过表达CgGCN4对于糠醛的胁迫抗逆性有正向作用,且可提高糠醛胁迫条件下的甘油的生产性能。
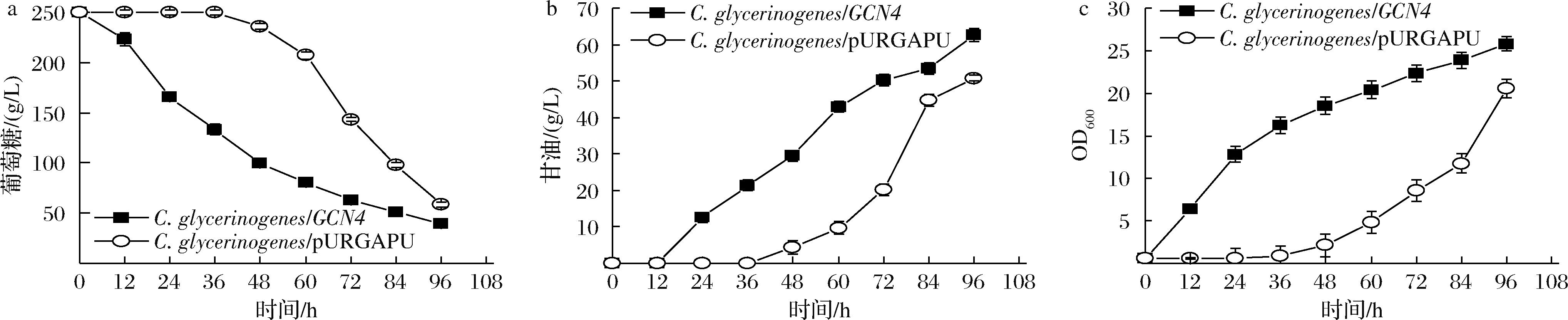
a-葡萄糖消耗;b-甘油生成;c-生长曲线
图5 添加3.0 g/L糠醛的高糖培养基中C.glycerinogenes/GCN4的生长发酵情况
Fig.5 Growth and fermentation of C.glycerinogenes/GCN4 in high glucose medium supplemented with 3.0 g/L furfural
在2.0 g/L香草醛的胁迫下,发酵96 h,C.glycerinogenes/GCN4、对照菌株发酵96 h分别耗糖247.7、234.2 g/L。与对照菌株耗糖速率为2.4 g/(L·h)相比,改造菌株耗糖速率提高了5.5%,达到2.6 g/(L·h)(图6-a);改造菌株甘油产量为53.7 g/L,比对照菌株降低了10.6%(图6-b);与对照菌株生物量为19.8相比,改造菌株生物量提高了14.6%,达到22.7(图6-c)。表明过表达CgGCN4对于香草醛的胁迫抗逆性有正向作用,且可提高香草醛胁迫条件下的菌株生长性能。
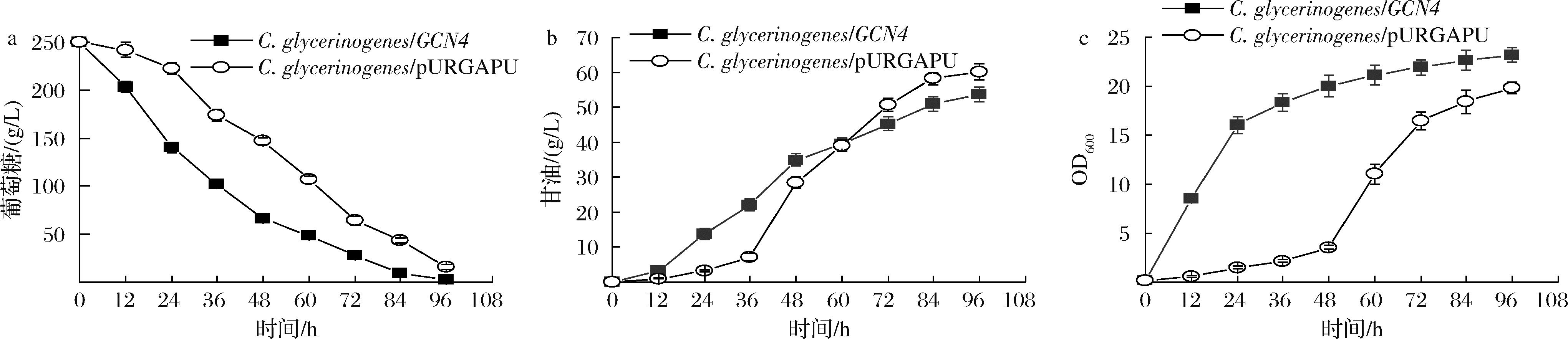
a-葡萄糖消耗;b-甘油生成;c-生长曲线
图6 添加2.0 g/L香草醛的高糖培养基中抗性菌株的生长发酵情况
Fig.6 Growth and fermentation of C.glycerinogenes/GCN4 in high glucose medium supplemented with 2.0 g/L vanillin
在3.5 g/L乙酸的胁迫下,发酵96 h,过表达CgGCN4的重组菌株耗糖速率提高13.1%(图7-a);甘油产量降低22.8%,达到61.9 g/L(图7-b);生物量提高了5.2%,OD600值达到26.9(图7-c)。表明过表达CgGCN4改善了乙酸胁迫下的生长性能,对抗乙酸胁迫具有正向作用。
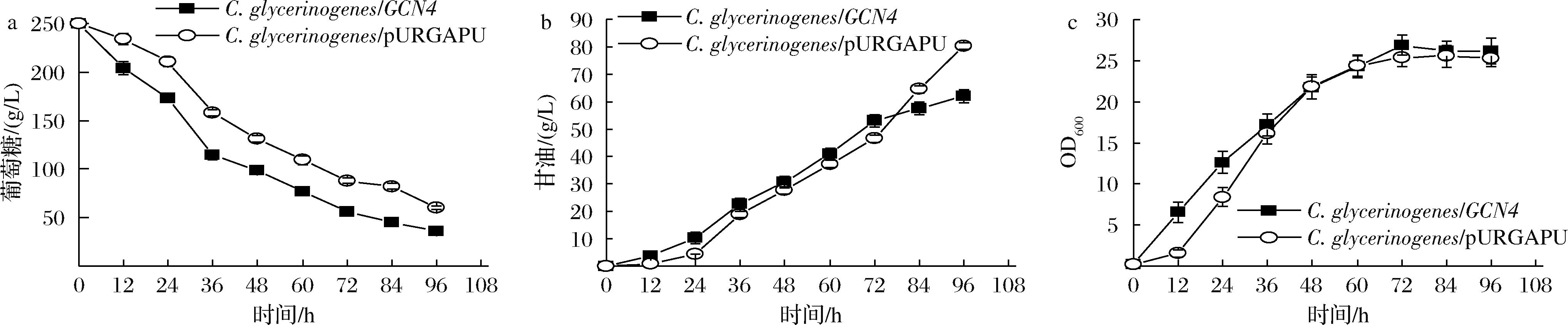
a-葡萄糖消耗;b-甘油生成;c-生长曲线
图7 添加3.5 g/L乙酸的高糖培养基中C.glycerinogenes/GCN4的生长发酵情况
Fig.7 Growth and fermentation of C.glycerinogenes/GCN4 in high glucose medium supplemented with 3.5 g/L acetic acid
为进一步探究C.glycerinogenes/GCN4在糠醛、香草醛或乙酸胁迫下生长或发酵性能提升的原因,分别在未添加毒性物质,在分别添加3.0 g/L糠醛或2.0 g/L香草醛或3.5 g/L乙酸的高糖发酵培养基下测定对照菌株及C.glycerinogenes/GCN4的胞内ROS水平及细胞膜完整性。在3种毒性物质的胁迫下,菌株胞内ROS水平剧增,细胞膜更易受损,过表达CgGCN4使菌株胞内ROS水平递增程度分别减缓了35.2%、28.0%、15.3%(图8-a)。使碘化丙啶穿过细胞膜与DNA结合的相对荧光强度的增加程度分别降低60.3%、25.7%、20.5%(图8-b)。说明过表达CgGCN4可有效减缓胁迫环境引起的ROS激增,维持胁迫条件下细胞膜的完整性。
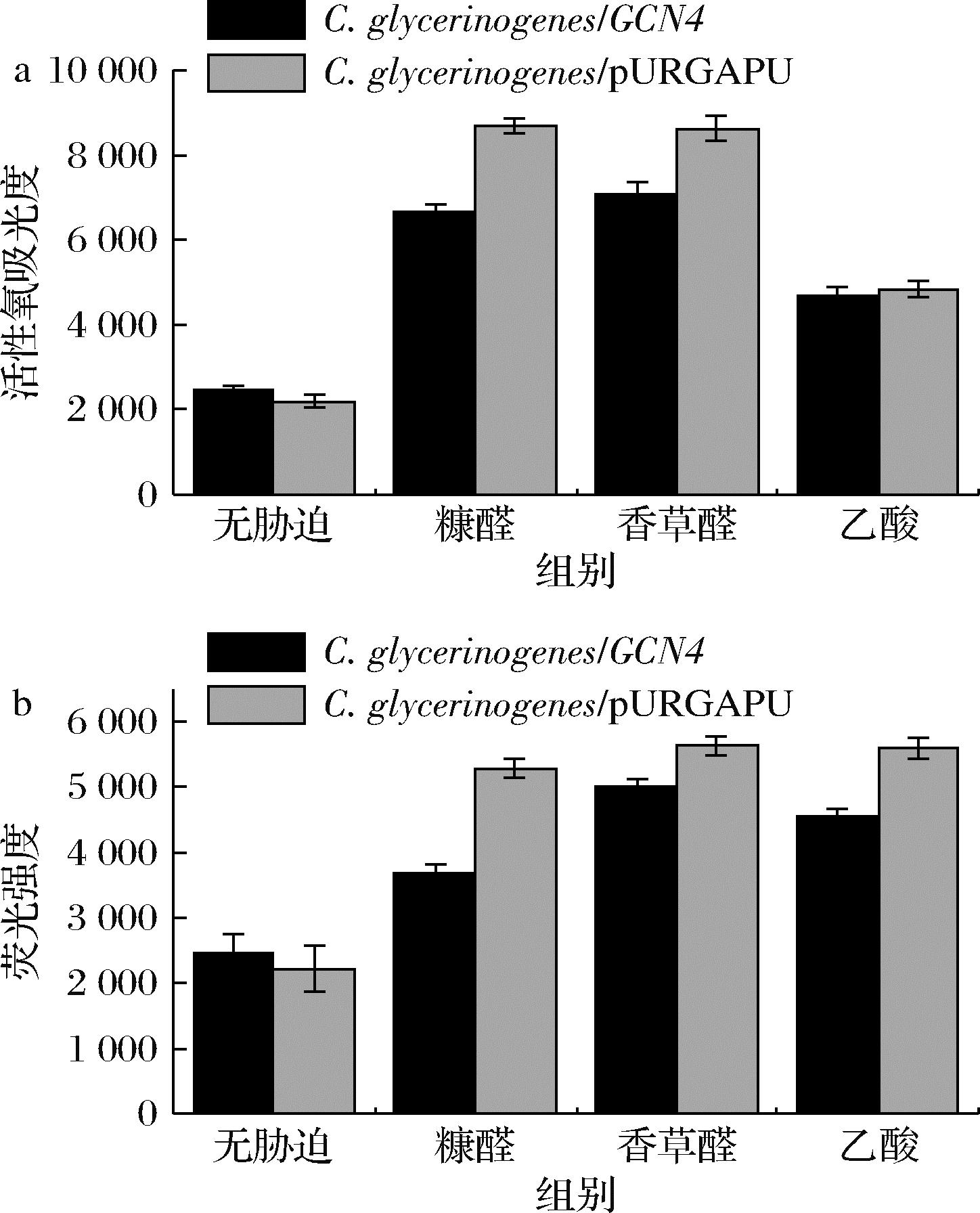
a-胞内ROS含量;b-荧光强度
图8 香草醛(2.0 g/L)或糠醛(3.0 g/L)或乙酸(3.5 g/L)胁 迫下C.glycerinogenes/GCN4胞内ROS含量和细胞膜完整性
Fig.8 Intracellular ROS content cell membrane integrity of C.glycerinogenes/GCN4 under vanillin (2.0 g/L) or furfural (3.0 g/L) stresses or acetic acid (3.5 g/L)
2.4 重组菌株未脱毒甘蔗渣水解液开放式发酵产甘油
将重组菌株及对照菌株同时用于开放式发酵未脱毒纤维素水解液,结果表明,重组菌株在未脱毒纤维素水解液内所受抑制较小,并表现出良好的发酵性能。过表达CgGCN4可缩短发酵时间12 h,使葡萄糖消耗速率提升20%,达到1.7 g/(L·h);与对照菌株甘油产量为21.8 g/L相比,过表达CgGCN4使甘油产量提高21.7%,达到26.5 g/L,与对照菌株甘油生产强度0.30 g/(L·h)相比,过表达CgGCN4使甘油生产强度提高13.9%,达到0.44 g/(L·h)(图9-a)。过表达CgGCN4也提高了菌株在未脱毒纤维素水解液中的生长性能,使生物量由21.2提升至23.8,相比提高12.3%(图9-b)。
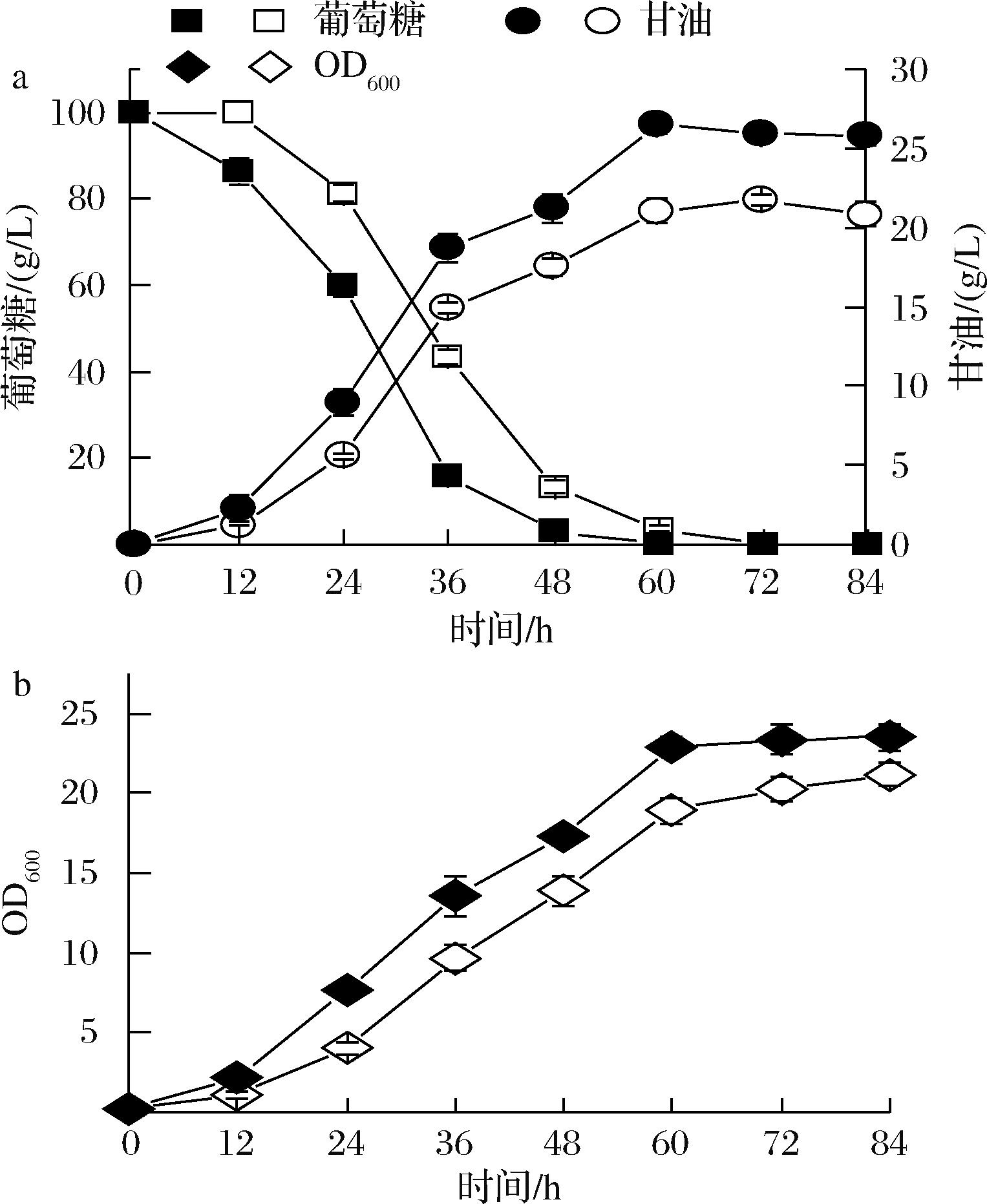
a-发酵情况;b-生长曲线
图9 未脱毒纤维素水解液下重组菌株发酵情况和生长曲线
Fig.9 Recombinant strains under undetoxified hydrolysate fermentation and growth curves
注:空心:C.glycerinogenes/pURGAPU;实心:C.glycerinogenes/GCN4。
3 结论与讨论
未脱毒水解液中所含的代表性有毒物质乙酸、糠醛或香草醛等能够引起细胞内ROS积累,造成氧化胁迫,引发细胞膜损伤,抑制糖酵解及TCA循环进而抑制微生物代谢与发酵[15-17]。GCN4是响应氧化应激或饥饿刺激的转录激活因子,在维持酿酒酵母胞内氨基酸稳态的信号传导及氧化应激中有重要作用[18-19]。
在糠醛或香草醛或乙酸或未脱毒纤维素水解液的胁迫条件下,点板和摇瓶结果都表明过表达CgGCN4的菌株表现出优于对照菌株的生长和发酵性能,说明CgGCN4是参与抵抗糠醛、香草醛及乙酸胁迫的潜在基因。糠醛、乙酸、香草醛或未脱毒纤维素水解液胁迫条件下耗糖速率的提升表明过表达CgGCN4可通过强化糖酵解途径,增强菌株对葡萄糖的摄取,以积累更多能量、NAD(P)H和重要的代谢产物,从而提高C.glycerinogenes的耐受性,改善菌株在胁迫下的生长发酵性能。
在糠醛胁迫下甘油产量的提高说明,过表达菌株可能通过激活HOG1调控的甘油快速合成机制加速甘油合成[20],一方面甘油作为渗透调节剂可平衡细胞内外渗透压,另一方面,Hog途径的激活可能上调抗氧化应激相关基因的转录水平维持胞内氧化还原平衡进而提高菌株耐受性,从而改善糠醛条件下的菌株生长发酵情况[21]。而香草醛或乙酸胁迫下,重组菌株更倾向于通过提高糖酵解途径的强度来改善菌株的生长发酵性能。另一方面,甘油产量未见提升,菌株可能更倾向于积累其他相容性物质如海藻糖等以改善菌株在胁迫条件下的解毒性能[22]。
细胞可调节抗氧化系统以适应低浓度ROS,而胁迫条件下,细胞内氧化应激产生的ROS浓度过高,超过细胞调节能力时,对胞内蛋白质、DNA及膜脂质等细胞组分造成严重损害,进而影响细胞代谢,甚至导致死亡[23]。过表达CgGCN4的菌株在糠醛、乙酸和香草醛刺激下ROS水平递增程度较对照菌株低,说明过表达CgGCN4可有效缓解糠醛、乙酸及香草醛胁迫造成的氧化损伤。且进一步实验表明,2种胁迫条件下过表达菌株更能维持细胞膜完整性而保护细胞免受糠醛、香草醛、乙酸及未脱毒纤维素水解液的危害[24]。
将重组菌株用于开放式发酵未脱毒蔗渣水解液时,甘油产量及生物量相比于对照菌株的有效提高,进一步证实了重组菌株在胁迫条件下生长发酵性能的稳定性。
[1] AMORIM H V, LOPES M L, DE CASTRO OLIVEIRA J V, et al.Scientific challenges of bioethanol production in Brazil[J].Applied Microbiology and Biotechnology, 2011, 91(5):1267-1275.
[2] LIU Z L.Molecular mechanisms of yeast tolerance and in situ detoxification of lignocellulose hydrolysates[J].Applied Microbiology and Biotechnology, 2011, 90(3):809-825.
[3] HADI S M, SHAHABUDDIN, REHMAN A.Specificity of the interaction of furfural with DNA[J].Mutation Research Letters, 1989, 225(3):101-106.
[4] KLINKE H B, THOMSEN A B, AHRING B K.Inhibition of ethanol-producing yeast and bacteria by degradation products produced during pre-treatment of biomass[J].Applied Microbiology and Biotechnology, 2004, 66(1):10-26.
[5] WANG X, LI B Z, DING M Z, et al.Metabolomic analysis reveals key metabolites related to the rapid adaptation of Saccharomyce cerevisiae to multiple inhibitors of furfural, acetic acid, and phenol[J].Omics, 2013, 17(3):150-159.
[6] JÖNSSON L J, ALRIKSSON B, NILVEBRANT N O.Bioconversion of lignocellulose:Inhibitors and detoxification[J].Biotechnology for Biofuels, 2013, 6(1):16.
[7] TAHERZADEH M J, ADLER L, LIDÉN G.Strategies for enhancing fermentative production of glycerol—a review[J].Enzyme and Microbial Technology, 2002, 31(1-2):53-66.
[8] ANITHA M, KAMARUDIN S K, KOFLI N T.The potential of glycerol as a value-added commodity[J].Chemical Engineering Journal, 2016, 295:119-130.
[9] WANG Z X, ZHUGE J, FANG H Y, et al.Glycerol production by microbial fermentation: A review[J].Biotechnology Advances, 2001, 19(3):201-223
[10] JIANG D Q, WANG M Y, ZHAO X H, et al.Glycerol production from undetoxified lignocellulose hydrolysate by a multiresistant engineered Candida glycerinogenes[J].Journal of Agricultural and Food Chemistry, 2024, 72(3):1630-1639.
[11] ZHAO M L, SHI D C, LU X Y, et al.Ethanol fermentation from non-detoxified lignocellulose hydrolysate by a multi-stress tolerant yeast Candida glycerinogenes mutant[J].Bioresource Technology, 2019, 273:634-640.
[12] WANG Y Q, ZHANG Z Y, LU X Y, et al.Transcription factor Hap5 induces gsh2 expression to enhance 2-phenylethanol tolerance and production in an industrial yeast Candida glycerinogenes[J].Applied Microbiology and Biotechnology, 2020, 104(9):4093-4107.
[13] WU C D, ZHANG J, WANG M, et al.Lactobacillus casei combats acid stress by maintaining cell membrane functionality[J].Journal of Industrial Microbiology &Biotechnology, 2012, 39(7):1031-1039.
[14] 张国友, 唐玲, 陈玮, 等.分光光度法测定蒙古栎叶中多酚的含量[J].中国科学院研究生院学报, 2009, 26(3):319-322.ZHANG G Y, TANG L, CHEN W, et al.Spectrophotometric determination of polyphenols in Quercus mongolicus Fisch leaves by means of Folin-ciocalteu reagent[J].Journal of University of Chinese Academy of Sciences, 2009, 26(3):319-322.
[15] ZHANG M M, ZHANG K Y, MEHMOOD M A, et al.Deletion of acetate transporter gene ADY2 improved tolerance of Saccharomyces cerevisiae against multiple stresses and enhanced ethanol production in the presence of acetic acid[J].Bioresource Technology, 2017, 245:1461-1468.
[16] UJOR V C, OKONKWO C C.Microbial detoxification of lignocellulosic biomass hydrolysates:Biochemical and molecular aspects, challenges, exploits and future perspectives[J].Frontiers in Bioengineering and Biotechnology, 2022, 10:1061667.
[17] LIMA C S, NEITZEL T, PIROLLA R, et al.Metabolomic profiling of Spathaspora passalidarum fermentations reveals mechanisms that overcome hemicellulose hydrolysate inhibitors[J].Applied Microbiology and Biotechnology, 2022, 106(11):4075-4089.
[18] NATARAJAN K, MEYER M R, JACKSON B M, et al.Transcriptional profiling shows that Gcn4p is a master regulator of gene expression during amino acid starvation in yeast[J].Molecular and Cellular Biology, 2001, 21(13):4347-4368.
[19] QI S H, HE L, ZHANG Q, et al.Cross-pathway control gene CPC1/GCN4 coordinates with histone acetyltransferase GCN5 to regulate catalase-3 expression under oxidative stress in Neurospora crassa[J].Free Radical Biology and Medicine, 2018, 117:218-227.
[20] JI H, LU X Y, WANG C Y, et al.Identification of a novel HOG1 homologue from an industrial glycerol producer Candida glycerinogenes[J].Current Microbiology, 2014, 69(6):909-914.
[21] ENJALBERT B, SMITH D A, CORNELL M J, et al.Role of the Hog1 stress-activated protein kinase in the global transcriptional response to stress in the fungal pathogen Candida albicans[J].Molecular Biology of the Cell, 2006, 17(2):1018-1032.
[22] 何艳艳, 孜力汗, 张宝会, 等.过表达长链鞘氨醇激酶基因LCB4提高酿酒酵母抑制物耐受性[J].生物工程学报, 2018, 34(6):906-915.HE Y Y, ZI L H, ZHANG B H, et al.Improvement of inhibitors tolerance of Saccharomyces cerevisiae by overexpressing of long chain sphingoid kinases encoding gene LCB4[J].Chinese Journal of Biotechnology, 2018, 34(6):906-915.
[23] PELICANO H, CARNEY D, HUANG P.ROS stress in cancer cells and therapeutic implications[J].Drug Resistance Updates, 2004, 7(2):97-110.
[24] WANG X H, CUI S Q, HU J J, et al.Saccharides in straw hydrolysate decrease cell membrane damage by phenolics by inducing the formation of extracellular matrix in yeast[J].Carbohydrate Polymers, 2019, 219:414-422.