一次性塑料制品的大量生产导致了其在环境中的积累,仅在2023年全球生产了约4.003亿t的塑料[1]。废弃的塑料制品对空气、土壤、河流等都造成巨大的污染[2-3]。聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET),属于聚酯家族,在塑料分类中编号为1号,由对苯二甲酸(terephthalic acid,TPA)和乙二醇(ethylene glycol,EG)缩聚而成[4]。由于PET具有成本低、耐用、可铸造性好等优点,因此在包装、建筑、汽车、农业等众多市场中具有广泛的应用[5-6]。常见的PET回收方法主要包括物理和化学回收法,其中物理回收法是在不改变PET分子结构的前提下通过填埋、机械研磨、燃烧等方法处理PET[7],该方法缺少特异性且无法实现PET的循环利用。化学回收法则是通过热解法、胺解法、水解法、醇解法等方法将PET聚酯降解为聚酯单体,但在回收过程中产生有害副产物且反应条件苛刻[8]。相比之下生物技术可以在更加温和的条件下进行反应[9],能够从混合材料或者废物中回收PET,回收成本低且不会对环境造成污染,因此具有更大的应用潜力[10]。
早在2016年,已有文章报道以PET为主要碳源的萨凯埃迪奥内拉菌201-F6菌株(Ideonella sakaiensis 201-F6, I. sakaiensis)能够分泌两种降解PET的水解酶,分别为PETase和MHETase,其中PETase可以降解PET,得到中间产物单(2-羟乙基)对苯二甲酸酯[mono(2-hydroxyethyl) terephthalate, MHET]和双-2-9(羟乙基)对苯二甲酸酯[bis(2-hydroxyethyl) terephthalate,BHET],MHETase可以进一步降解MHET,将其转化为TPA和EG[11]。PETase的热稳定性较差,在30 ℃条件下极其不稳定,且在37 ℃条件下孵育24 h后就会失去活性[12],于是对其热稳定性的提高成为了大家关注的焦点。研究人员通过基因突变[13-15]、分子修饰[5,16]、以及酶固定化[17-18]等技术提高PETase水解活性以及热稳定性。其中,LU等[19]对PETase进行定点突变,得到的突变体FAST-PETase(PETaseS121E/D186H/R224Q/N233K/R280A)表现出较高的水解活性。
除了酶的改造工作外,酶固定化技术在生物催化技术中也具有广泛的应用,用于提高酶的活性,稳定性以及重复利用率[20]。与传统的酶固定方法相比,微生物表面展示技术可以省去酶的纯化、浓缩等步骤,具有更简单的工艺流程。目前常见的用于表面展示的宿主细胞主要有噬菌体[21]、细菌[22]、酵母[23]和枯草芽孢杆菌芽孢[24]等。在本实验室前期的研究中,利用酿酒酵母dit1Δ缺陷型菌株构建酵母孢子表面展示系统。当二倍体酿酒酵母在饥饿条件下,会启动减数分裂程序产生称为孢子(单倍体)的休眠细胞,DIT1基因与孢子壁最外层二酪氨酸层的合成有关,当DIT1基因缺失时形成dit1Δ孢子,原本应该被二酪氨酸层覆盖的壳聚糖层会暴露在最外层。此时在孢子中表达带有信号肽的目的蛋白会因为静电吸附作用展示在孢子表面。该系统可用于大分子质量的蛋白,且对有机试剂表现出良好的抗性[25]。
本研究利用酿酒酵母dit1Δ突变菌株建立了一个更加稳定的孢子表面展示系统,将其成功地应用于BHET的水解中,并对孢子固定化FAST-PETase的酶学性质和重复使用能力进行研究,为PET塑料的长期降解提供了新的思路。
1 材料与方法
1.1 菌株和质粒
本实验所用到的菌株和质粒分别见表1和表2。
表1 实验所用到的酵母菌株
Table 1 S.cerevisiae strains used in this study

菌株基因型来源S.cerevisiae HW3(dit1Δ)MATα/MATa ARG4/arg4-NspI his3 ΔSK/his3 ΔSK ho::LYS2/ho::LYS2 leu2/leu2 lys2/lys2 RME1/rme1::LEU2 trp1::hisGtrp1::hisG ura3/ura3 dit1Δ::his5+/dit1Δ::his5+本实验室S.cerevisiae HW3-4B(dit1Δ-α)MATα ura3 leu2 trp1 his3Δsk arg4-NspI lys2 ho::LYS2 rme1::LEU2 dit1Δ::his5+本实验室S.cerevisiae HW3-16D(dit1Δ-a)MATa ura3 leu2 trp1 his3Δsk lys2 ho::LYS2 dit1Δ::his5+本实验室dit1Δ/FAST-PETaseS.cerevisiae dit1Δ 含有质粒pRS306-TEF1pr-ss-/FAST-PETase本研究dit1Δ/RFPS.cerevisiae dit1Δ含有质粒pRS306-TEF1pr-ss-RFP本研究
表2 实验所用的质粒
Table 2 Plasmids used in this study

质粒名称性质来源pRS306-TEF1prURA3标记,整合型,含有TEF1启动子本实验室pRS306-TEF1pr-ss-RFPpRS306-TEF1pr携带N端融合分泌信号肽的RFP基因本研究pRS306-TEF1pr-ss-FAST-PETasepRS306-TEF1pr携带N端融合分泌信号肽的FAST-PETase基因本研究
1.2 培养基
酵母浸出粉胨葡萄糖培养基(yeast extract peptone dextrose medium, YPD)(g/L):10酵母提取物,20蛋白胨,20葡萄糖,湿热灭菌(121 ℃,20 min)。
尿嘧啶缺陷型合成葡萄糖基础培养基(yeast synthetic drop-out medium without uracil, SD-U):2.01 g无氨基酸酵母氮源(yeast nitrogen base without amino acids, YNB),0.6 g缺Ura的氨基酸混合物粉末,6 g葡萄糖,6 g琼脂粉(固体培养基),去离子水定容至300 mL,湿热灭菌(121 ℃,20 min)。
腺嘌呤和亮氨酸缺陷型合成葡萄糖基础培养基(yeast synthetic drop-out medium without adenine and leucine, SD-AL):2.01 g YNB,0.6 g缺Arg和Leu的氨基酸混合物粉末,6 g葡萄糖,6 g琼脂粉(固体培养基),去离子水定容至300 mL,湿热灭菌(121 ℃,20 min)。
酵母浸出粉蛋白胨醋酸盐培养基(yeast extract peptone acetate medium, YPAce)(g/L):10酵母提取物,20蛋白胨,20醋酸钾,湿热灭菌(121 ℃,20 min)。
20 g/L液体醋酸钾培养基:20 g醋酸钾,去离子水定容至1 L,湿热灭菌(121 ℃,20 min)。
1.3 试剂和仪器
PrimeSTAR GXL DNA聚合酶、2×Taq聚合酶、限制性核酸内切酶等,宝日医生物技术有限公司;即用型无缝克隆试剂盒、PCR产物纯化试剂盒,生工生物工程技术有限公司;胶回收、质粒抽提试剂,北京全式金生物技术有限公司;藤黄节杆菌溶壁酶(arthrobacter luteus lyticase)、对苯二甲酸双(2-羟乙基)酯(BHET,CAS:959-26-2),Sigma-Aldrich公司。
DS-Ri2荧光倒置显微镜,Nikon公司;SCIENTZ-IID超声波细胞粉碎机,宁波新芝生物科技股份有限公司;FD-1000冷冻干燥机,EYELA公司;Waters 2489高效液相色谱仪、Waters Symmetry C18色谱柱(4.6 mm×250 mm, 5 μm),沃特世科技有限公司。
1.4 质粒构建
来源于I.sakaiensis的FAST-PETase(PETaseS121E/D186H/R224Q/N233K/R280A)[19]的基因序列经酿酒酵母密码子偏好性进行优化并从安升达(中国苏州)订购。
Spr1蛋白的信号肽(SS, MVSFRGLTTLTLLFTKLVNCN)可以在产孢的过程中将目的蛋白分泌到胞外,因此在基因合成时将其融合在目的蛋白N端。以合成基因为模板,PCR扩增得到ss-FAST-PETase基因,pRS306-TEF1pr载体经Spe I和BamH I双酶切后,使用无缝克隆酶将目的基因连接到pRS306载体上,得到重组质粒pRS306-TEF1pr-ss-FAST-PETase。RFP相关质粒构建同上,RFP基因为本实验室保存。
1.5 酵母产孢与孢子纯化
重组质粒pRS306-TEF1pr-ss-FAST-PETase,线性化后使用醋酸锂法分别转入酵母单倍体细胞dit1Δ-a/dit1Δ-α菌株中,使用SD-U缺陷型培养基筛选菌株,之后将单倍体菌落在SD-AL缺陷型培养基上融合成二倍体dit1Δ,此后选取单个菌落的酵母细胞在5 mL YPD中30 ℃培养过夜,为了诱导产孢,将2 mL的酵母细胞液转移到100 mL的YPAce培养基中30 ℃培养24 h后9 000 r/min,5 min离心收获细胞,然后在50 mL的20 g/L液体醋酸钾培养基中重悬,30 ℃培养24 h得到子囊孢子,光学显微镜下测定产孢效率。表达RFP蛋白的孢子在水洗两次后使用荧光显微镜观察荧光。
为了得到单个孢子,将上述子囊孢子5 000 r/min,1 min离心收集后重悬在5 mL原生质体缓冲液(50 mmol/L磷酸钾缓冲液,pH 7.5, 1.4 mol/L山梨醇,40 mmol/L β-巯基乙醇)中,并与裂解酶(10 U, Sigma-Aldrich)在37 ℃下孵育2 h。然后用原生质体缓冲液洗涤孢子两次,再用5 mL原生质体缓冲液重悬孢子,并用超声波破碎仪破坏子囊膜获得单个孢子。根据先前描述的方法,通过Percoll梯度离心纯化孢子。将孢子在-80 ℃冷冻箱内冷冻2 h以上,然后在25 Pa压力下冷冻干燥24 h。
1.6 孢子固定化FAST-PETase的活性测定以及HPLC条件
选用BHET作为底物,通过检测生成的产物MHET量来检测FAST-PETase孢子的酶活,BHET溶解于DMSO中[12]。
反应体系:称取6 mg冻干孢子与2.5 g/L BHET在50 mmol/L Na2HPO4-H3PO4(pH 8.0)中50 ℃孵育1 h。终止反应:加入相同体积的终止反应缓冲液(160 mmol/L Na2HPO4-H3PO4, pH 2.5, 20% DMSO),15 000 r/min,5 min离心得到上清,80 ℃加热10 min 后15 000 r/min离心10 min进行HPLC分析[5,18]。反应体系为300 μL,反应缓冲液为磷酸盐缓冲液,首先检测2.5~30 g/L不同孢子浓度条件下,MHET的产量,其次是在20 g/L孢子条件下分别反应10~240 min 后MHET的产量。
高效液相色谱分析条件:流动相为70%(体积分数)超纯水、20%(体积分数)乙腈、10%(体积分数)甲酸,流速为1.0 mL/min,在254 nm波长处检测到芳香族化合物(BHET、MHET)。
1.7 温度和pH对孢子固定化FAST-PETase活性的影响
使用上述反应体系,在30~80 ℃条件下检测温度对孢子固定化FAST-PETase酶活性的影响。为了测定pH对孢子固定化FAST-PETase活性的影响,在pH 5.0~9.0条件下进行酶活性检测。具体使用的缓冲液如下:50 mmol/L NaH2PO4-NaOH(pH 5.0),50 mmol/L Na2HPO4-HCl(pH 6.0~8.0),50 mmol/L甘氨酸-NaOH(pH 9.0~10.0)[18]。
1.8 金属离子对孢子固定化FAST-PETase活性的影响
分别向1.6节所述反应体系中添加2 mmol/L常见的二价金属离子(Mn2+、Cu2+、Ca2+、Zn2+、Ni2+、Fe2+、Co2+),检测其对孢子固定化FAST-PETase活性的影响,分别向1.6节所述反应体系中添加1、2、5、10、15 mmol/L Ca2+,检测高浓度金属离子对孢子固定化FAST-PETase活性的影响,将未添加二价金属离子的孢子酶活性定义为100%,计算添加后孢子的相对酶活性。
1.9 孢子固定化FAST-PETase的热稳定性以及pH耐受性
对于孢子固定化FAST-PETase的温度稳定性,将孢子分别在30~80 ℃条件下孵育12 h后,使用上述反应体系测定孢子的残留活性。对于pH耐受性,将孢子置于上述缓冲液中,并在4 ℃下孵育12 h,之后同样使用上述反应体系测定孢子的残留活性。将未经处理孢子的酶活定义为100%,计算其余条件下孢子固定化酶的相对活性。
1.10 孢子固定化FAST-PETase洗涤剂、有机试剂耐受性以及重复使用能力
将孢子分别在50 mmol/L磷酸盐缓冲液(pH 8.0),0.1%(质量分数)吐温-20、70%(体积分数)乙酸乙酯、1%(质量分数)十二烷基硫酸钠(sodium dodecyl sulfate,SDS)中,25 ℃条件下孵育24 h,6 000 r/min离心10 min收集孢子并用水洗两次后冷冻干燥,之后使用上述反应条件检测孢子的残留活性,确定孢子固定化FAST-PETase对洗涤剂、有机试剂的耐受性。
对于孢子可重复使用能力的测定,取6 mg冻干孢子在50 mmol/L磷酸盐缓冲液(pH 8.0)中于2.5 g/L BHET反应1 h后,9 000 r/min离心5 min从反应溶液中回收孢子,用水洗两次后,在同样的条件进行下一轮的反应,将第1次反应的酶活定义为100%,误差线来自3次独立实验。
2 结果与分析
2.1 孢子表面展示体系的建立
在本实验室前期的研究中,利用游离型质粒pRS426在酿酒酵母孢子表面构建展示系统,但游离型质粒在细胞培养以及产孢过程中容易丢失,为了完善孢子表面展示体系,本研究使用整合型质粒pRS306在孢子内表达红色荧光蛋白RFP,结果如图1所示,所有孢子都有荧光表达,且大部分荧光均可在孢子表面被观察到。结果表明,整合型质粒能够将RFP基因插入到酵母基因组中使其更稳定的表达。因此,采用这种更稳定的表达载体有望提高酿酒酵母孢子表面的展示效率。
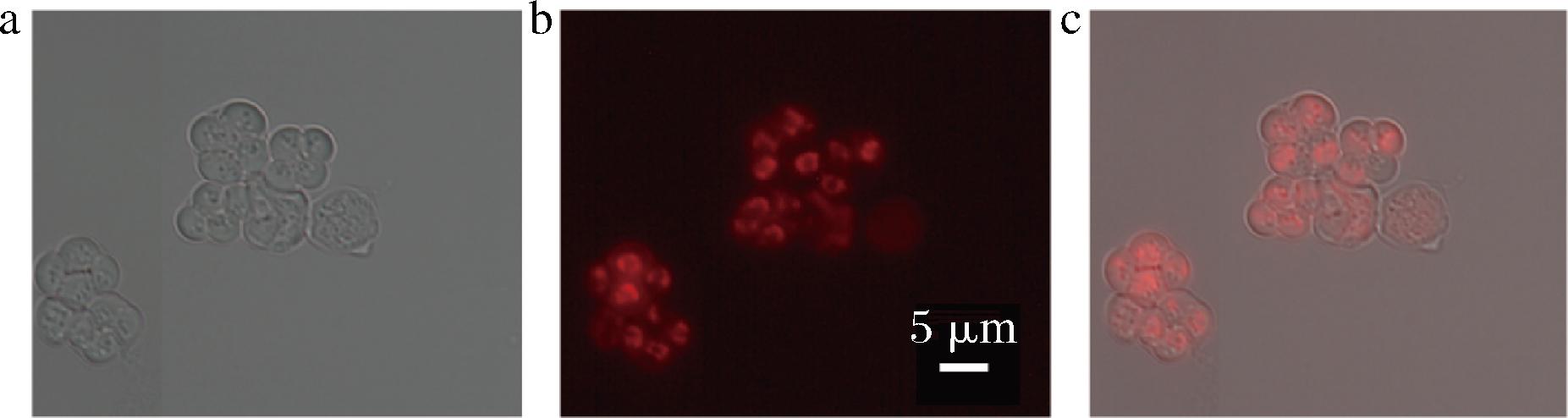
a-白光;b-红光;c-合并
图1 质粒pRS306-TEF1pr-ss-RFP在dit1Δ菌株中 表达的孢子荧光图
Fig.1 Fluorescence microscopy images of spores expressing plasmid pRS306-TEF1pr-ss-RFP in dit1Δ strain
2.2 孢子浓度及反应时间对孢子固定化FAST-PETase的影响
如图2-a所示,在PET的降解过程中,PETase能够催化PET生成BHET和MHET,而BHET可进一步被PETase水解成MHET和TPA。这些单体化合物具有回收再利用的潜力,可用于重新生成PET。本研究以BHET的水解为模型,选取活性最高的PETase突变体FAST-PETase,将其固定在酿酒酵母孢子表面,并研究孢子固定化FAST-PETase的酶学性质。
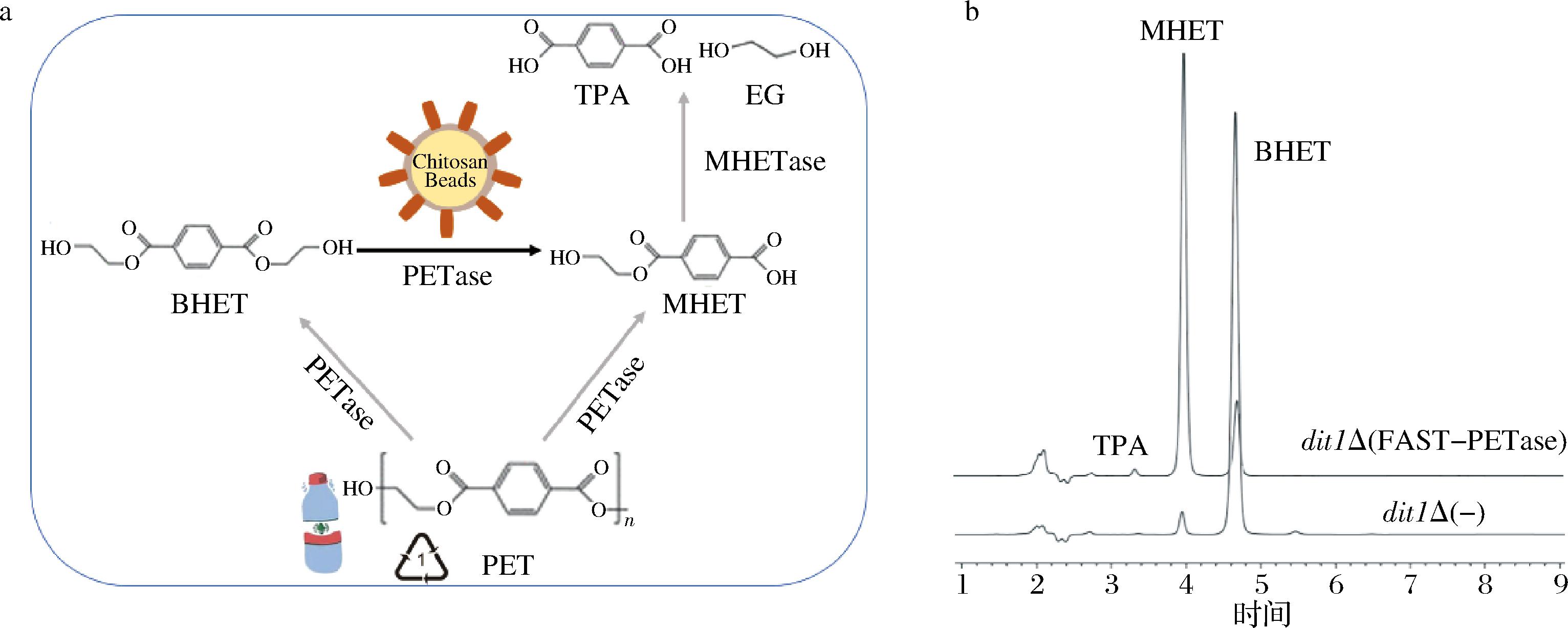
a-PET降解示意图;b-HPLC谱图
图2 孢子固定化FAST-PETase的酶活力检测
Fig.2 Enzyme activity detection of immobilized FAST-PETase on spores
首先,检测孢子固定化FAST-PETase的活性,dit1Δ空孢子作为对照,HPLC检测结果如图2-b所示,FAST-PETase主要是将BHET降解为MHET,少量TPA的产出说明FAST-PETase对MHET有一定的活性。值得注意的是,在对照组中也有少量MHET的产出,这是因为BHET自身会发生水解,在后续的实验中所有结果都会减去BHET自身水解得到的MHET。
其次,检测了不同孢子固定化酶浓度条件下MHET的产量,结果如图3-a所示,随着孢子质量浓度的升高,反应体系中MHET的浓度也随之升高,在孢子质量浓度达到20 g/L时反应达到平衡,因此选用20 g/L孢子质量浓度进行后续实验。图3-b表明,随着反应时间的增加,反应体系中MHET的浓度也随之升高,在反应时间1 h达到平衡,因此后续实验的反应时间均采用1 h。
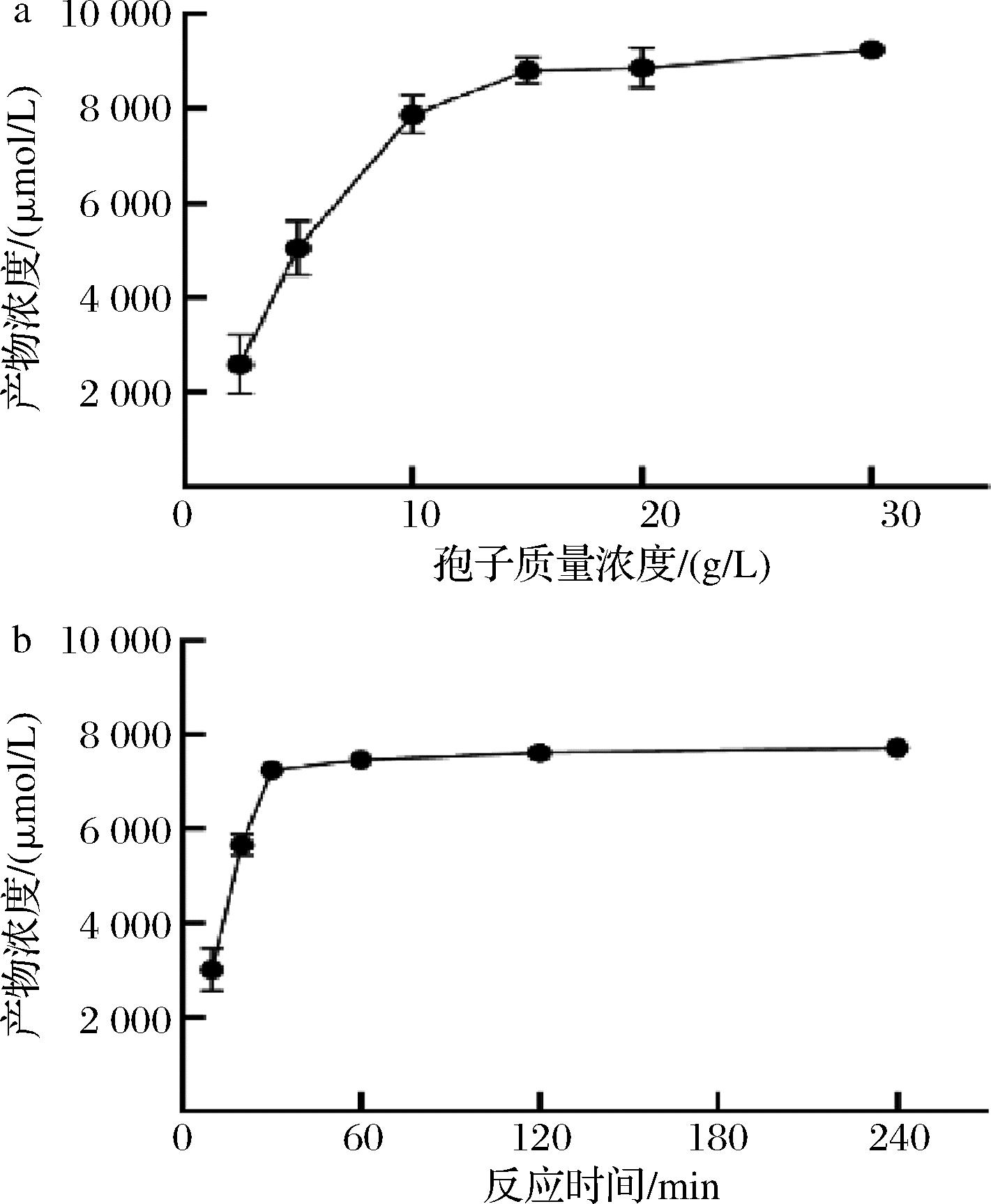
a-孢子质量浓度;b-反应时间
图3 孢子质量浓度和反应时间对孢子固定化 FAST-PETase活性的影响
Fig.3 Effects of spore concentration and reaction time on the activity of immobilized FAST-PETase on spores
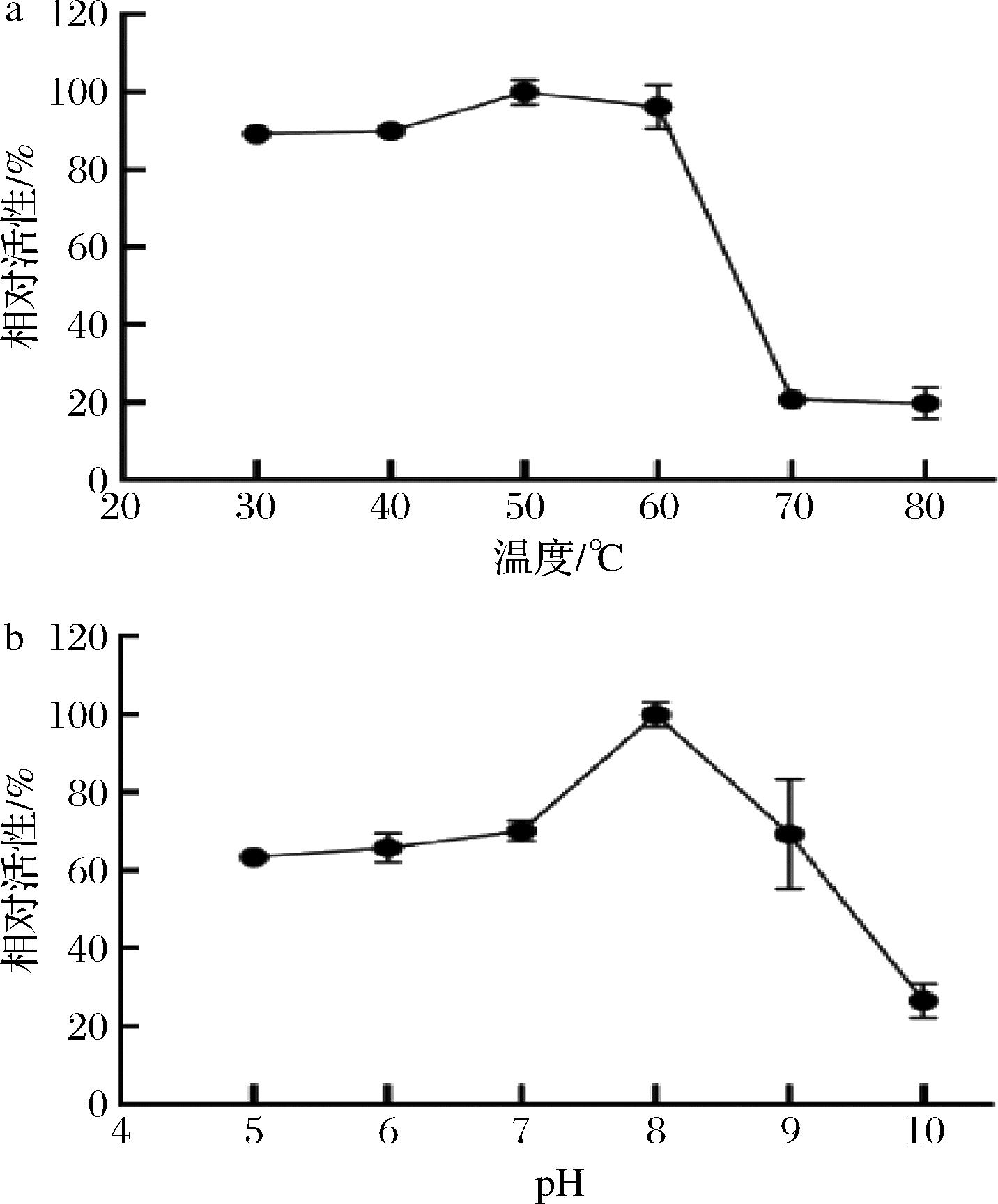
a-温度;b-pH
图4 温度和pH对孢子固定化FAST-PETase活性的影响
Fig.4 Effects of temperature and pH on the activity of immobilized FAST-PETase on spores
2.3 温度和pH对孢子固定化FAST-PETase的影响
反应温度对孢子固定化FAST-PETase的影响如图4-a所示,在50 ℃条件下孢子活性达到最高,这与文献所报道的游离FAST-PETase结果一致,孢子固定化FAST-PETase在30~60 ℃都保持较高的活性,有利于其在实际环境中的应用。pH条件对孢子固定化FAST-PETase的影响结果如图4-b所示,孢子固定化FAST-PETase的最适反应条件为pH 8.0,孢子固定化FAST-PETase在pH 5.0~9.0范围内也可保持较高的活性,有较宽的作用范围。
2.4 金属离子对孢子固定化FAST-PETase的影响
在实际的催化反应中,溶液中可能存在多种金属阳离子,这些离子对酶的催化活性具有不同程度的影响。同时,考虑金属离子可能会干扰目的蛋白与孢子表面壳聚糖层的结合过程。因此,研究金属离子对孢子表面展示FAST-PETase的作用至关重要。如图5-a所示,当在反应体系中分别添加2 mmol/L的常见二价金属离子时,发现这些离子对孢子表面展示的FAST-PETase的酶活性影响并不显著。随后选择Ca2+进行浓度梯度的研究,发现在高浓度的Ca2+存在下,孢子固定化的FAST-PETase活性并未发生明显变化(图5-b)。这表明孢子固定化的FAST-PETase对常见的金属离子具有良好的耐受性。
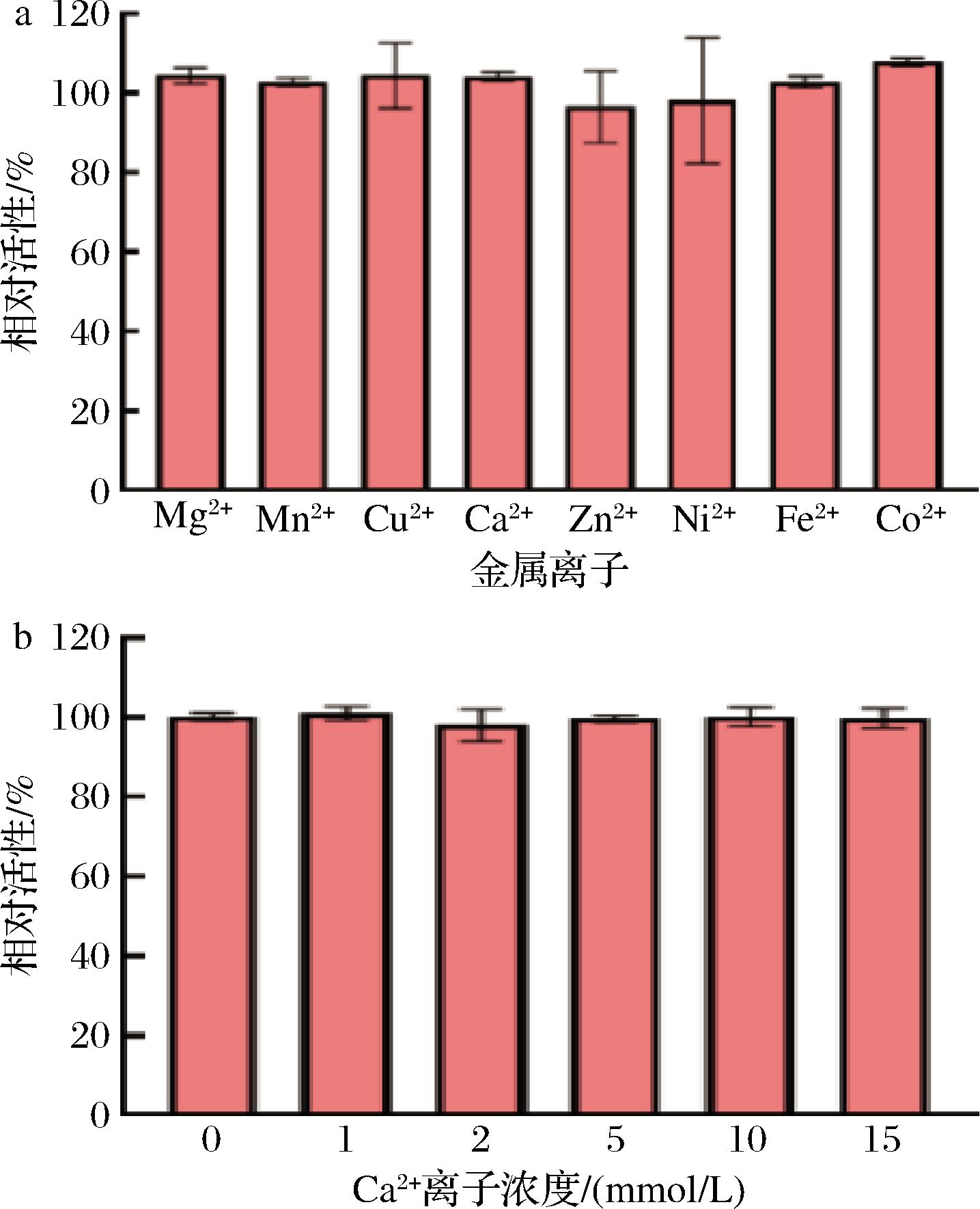
a-金属离子;b-Ca2+浓度
图5 金属离子对孢子固定化FAST-PETase活性的影响
Fig.5 Effects of metal ions on the activity of immobilized FAST-PETase on spores
2.5 孢子固定化FAST-PETase的热稳定性和pH耐受性
对于孢子固定化FAST-PETase的热稳定性分析如图6-a所示,经过12 h的孵育,在30~80 ℃的不同温度下,孢子固定化FAST-PETase分别保留了原始活性的84.16%、84.59%、85.80%、85.24%、84.82%和81.98%。由此可知孢子固定化酶表现出优异的热稳定性,热稳定性增强的一个可能原因是酶和壳聚糖层之间形成共价键,这可能增加酶的构象刚性和热变性所需的活化能。pH也是酶维持其催化活性的另一个关键因素,因此对孢子固定化FAST-PETase的pH耐受性进行分析,如图6-b所示,经过12 h的孵育,在pH 5.0~10.0的不同条件下,孢子固定化FAST-PETase分别保留了原始活性的78.43%、79.99%、81.11%、86.95%、80.92%和79.34%。由此可知孢子固定化酶具有很好的pH耐受性。孢子固定化酶优异的热稳定性和pH耐受性为其在实际环境中对PET废弃塑料的降解提供了理论基础。
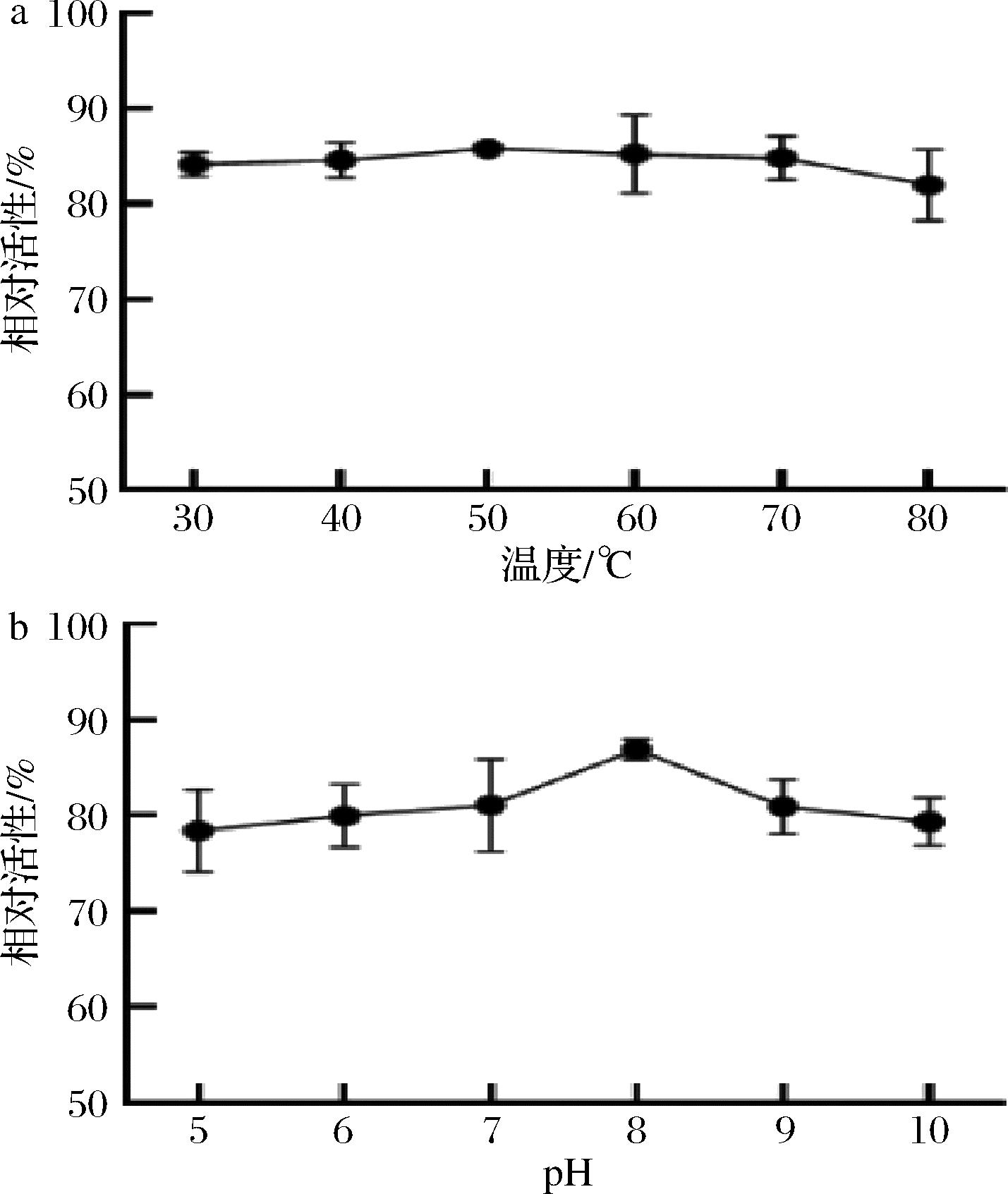
a-热稳定性;b-pH稳定性
图6 孢子固定化FAST-PETase的热稳定性和pH稳定性
Fig.6 Thermal stability and pH stability of immobilized FAST-PETase on spores
2.6 孢子固定化FAST-PETase的洗涤剂/有机试剂耐受性
废弃的PET包装材料在回收之前会使用一些洗涤剂或者化学试剂清洗。在生物法降解回收过程中可能会有洗涤剂或者化学试剂的残留,因此在实际应用中,对于酶体系洗的涤剂/有机试剂耐受性有一定的要求,因此研究了孢子固定化FAST-PETase在一些常见的洗涤剂/化学试剂条件下的稳定性,这些试剂可能用于清洗使用过的PET。以孢子在pH 8.0的磷酸盐缓冲液中孵育12 h的孢子作为对照。孢子固定化FAST-PETase在含有0.1% Tween 20、1% SDS和70%的乙酸乙酯的的反应缓冲液中孵育24 h后,测定剩余酶活性。
如图7所示,游离酶和孢子固定化酶都在0.1% Tween 20孵育24 h后,孢子固定化酶保留有80%的活性,而游离酶剩余活性是对照组的60%,1% SDS对FAST-PETase的影响较大,SDS处理后游离酶只剩下2%的活性,而孢子固定化FAST-PETase保留有16%的活性,至于70%乙酸乙酯处理后,游离酶剩余25%的活性,而孢子固定化酶保留有52%的活性。由此可知,孢子固定化FAST-PETase对常见的洗涤剂和一些有机试剂表现出较强的抗性。这进一步体现了孢子固定化FAST-PETase在实际应用中的可能性。
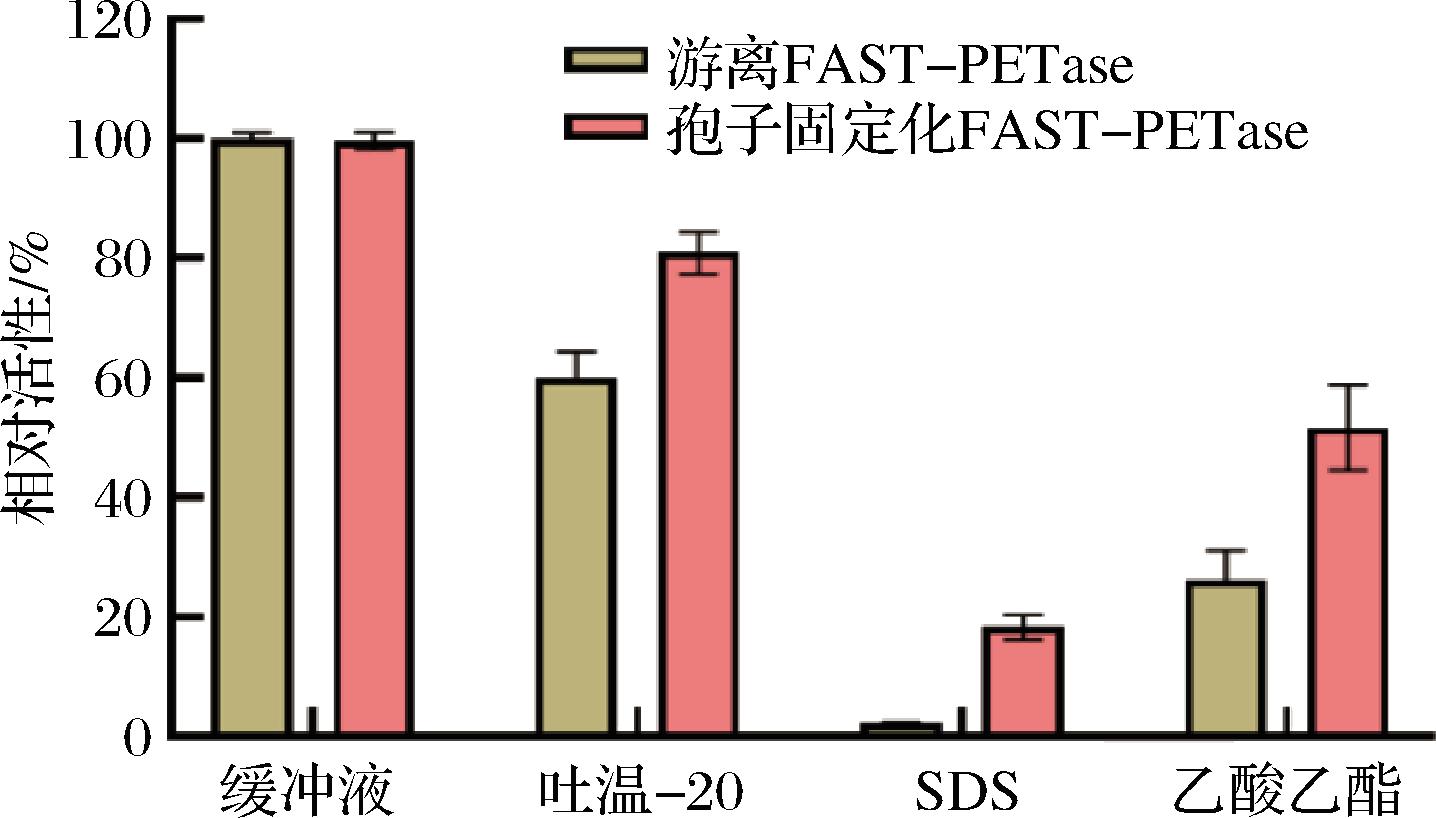
图7 孢子固定化FAST-PETase对洗涤剂/有机 试剂的耐受能力
Fig.7 Tolerance of immobilized FAST-PETase on spores to detergents/organic reagents
2.7 孢子固定化FAST-PETase的重复使用能力
在实际应用中,游离PETase在反应后若想实现回收再利用,通常需经过离心、过滤或色谱分离等繁琐且成本高昂的纯化过程,相比之下,酵母孢子的回收过程极其简单,通过离心即可收集。通过检测孢子固定化FAST-PETase在每轮回收过程中的剩余活性来判断其重复使用能力。如图8所示,在重复使用7次之后孢子固定化FAST-PETase仍然保留有原始活性的35%,这一结果表明,孢子固定化酶具有优异的可重复使用能力,在实际应用中,孢子固定化酶的可重复使用性可极大的降低成本。

图8 孢子固定化FAST-PETase的重复使用能力
Fig.8 Reusability of immobilized FAST-PETase on spores
3 结语
酿酒酵母孢子表面展示技术,可以通过静电吸附作用将目标蛋白展示在dit1Δ酿酒酵母孢子表面的壳聚糖层上,不需要蛋白纯化浓缩以及固定化等工艺流程,可以在蛋白表达的同时实现固定化。聚对苯二甲酸乙二醇酯(polyethylene glycol terephthalate,PET)是世界上使用最广泛的塑料之一,由于其具有耐用的特点,在被废弃后不易被自然界降解,对空气、土壤、河流等造成污染,进而威胁到人类的生存。本文在酿酒酵母孢子表面展示PET水解酶FAST-PETase,并将其应用于BHET的降解中,孢子固定化酶具有良好的热稳定性以及pH耐受性,且对一些常见二价金属离子、洗涤剂以及有机试剂具有一定的耐受性。酿酒酵母孢子表面展示FAST-PETase为PET的有效生物回收提供了一条有前途的途径。基于这一结果,未来可以在酿酒酵母孢子表面将两个PET水解酶组装在一起,为实现对BHET更高效率的水解以及对PET塑料的长期降解。
[1] Plastics European.Plastics—The fast facts 2023[EB/OL].(2024-01-23)[2024-02-20].https://plasticseurope.org/knowledge-hub/plastics-the-fast-facts-2023/.
[2] SAMAK N A, JIA Y P, SHARSHAR M M, et al.Recent advances in biocatalysts engineering for polyethylene terephthalate plastic waste green recycling[J].Environment International, 2020, 145:106144.
[3] LEBRETON L, ANDRADY A.Future scenarios of global plastic waste generation and disposal[J].Palgrave Communications, 2019, 5(1):6.
[4] SINHA V, PATEL M R, PATEL J V.Pet waste management by chemical recycling:A review[J].Journal of Polymers and the Environment, 2010, 18(1):8-25.
[5] CHEN K, QUAN M Q, DONG X Y, et al.Low modification of PETase enhances its activity toward degrading PET:Effect of conjugate monomer property[J].Biochemical Engineering Journal, 2021, 175:108151.
[6] TANIGUCHI I, YOSHIDA S, HIRAGA K, et al.Biodegradation of PET:Current status and application aspects[J].ACS Catalysis, 2019, 9(5):4089-4105.
[7] DAMAYA N, WU H S.Strategic possibility routes of recycled PET[J].Polymers, 2021, 13(9):1475.
[8] GEYER B, LORENZ G, KANDELBAUER A.Recycling of poly(ethylene terephthalate)-A review focusing on chemical methods[J].Express Polymer Letters, 2016, 10(7):559-586.
[9] WEI R, ZIMMERMANN W.Biocatalysis as a green route for recycling the recalcitrant plastic polyethylene terephthalate[J].Microbial Biotechnology, 2017, 10(6):1302-1307
[10] CARNIEL A, DE ABREU WALDOW V, DE CASTRO A M.A comprehensive and critical review on key elements to implement enzymatic PET depolymerization for recycling purposes[J].Biotechnology Advances, 2021, 52:107811.
[11] YANG Y, YANG J, JIANG L.Comment on “a bacterium that degrades and assimilates poly(ethylene terephthalate)”[J].Science, 2016, 353(6301):759.
[12] SON H F, CHO I J, JOO S, et al.Rational protein engineering of thermo-stable PETase from Ideonella sakaiensis for highly efficient PET degradation[J].ACS Catalysis, 2019, 9(4):3519-3526.
[13] BROTT S, PFAFF L, SCHURICHT J, et al.Engineering and evaluation of thermostable Is PETase variants for PET degradation[J].Engineering in Life Sciences, 2021, 22(3-4):192-203.
[14] MENG X X, YANG L X, LIU H Q, et al.Protein engineering of stable IsPETase for PET plastic degradation by Premuse[J].International Journal of Biological Macromolecules, 2021, 180:667-676.
[15] AUSTIN H P, ALLEN M D, DONOHOE B S, et al.Characterization and engineering of a plastic-degrading aromatic polyesterase[J].Proceedings of the National Academy of Sciences of the United States of America, 2018, 115(19):E4350-E4357.
[16] CHEN K, HU Y, DONG X Y, et al.Molecular insights into the enhanced performance of EKylated PETase toward PET degradation[J].ACS Catalysis, 2021, 11(12):7358-7370.
[17] HAN W, ZHANG J, CHEN Q, et al.Biodegradation of poly (ethylene terephthalate) through PETase surface-display:From function to structure[J].Journal of Hazardous Materials, 2024, 461:132632.
[18] CHEN Z Z, WANG Y Y, CHENG Y Y, et al.Efficient biodegradation of highly crystallized polyethylene terephthalate through cell surface display of bacterial PETase[J].Science of the Total Environment, 2020, 709:136138.
[19] LU H Y, DIAZ D J, CZARNECKI N J, et al.Machine learning-aided engineering of hydrolases for PET depolymerization[J].Nature, 2022, 604(7907):662-667.
[20] RODRIGUES R C, ORTIZ C, BERENGUER-MURCIA  , et al.Modifying enzyme activity and selectivity by immobilization[J].Chemical Society Reviews, 2013, 42(15):6290-6307.
, et al.Modifying enzyme activity and selectivity by immobilization[J].Chemical Society Reviews, 2013, 42(15):6290-6307.
[21] LI Z D, YEH M.Construction and diversity analysis of a murine IgE phage surface display library[J].Cell Research, 1997, 7(2):161-170.
[22] CHEN Y L, LING Z M, MAMTIMIN T, et al.Chitooligosaccharides production from shrimp chaff in chitosanase cell surface display system[J].Carbohydrate Polymers, 2022, 277:118894.
[23] KAJIWARA K, AOKI W, KOIKE N, et al.Development of a yeast cell surface display method using the SpyTag/SpyCatcher system[J].Scientific Reports, 2021, 11(1):11059.
[24] LIN P, YUAN H B, DU J K, et al.Progress in research and application development of surface display technology using Bacillus subtilis spores[J].Applied Microbiology and Biotechnology, 2020, 104(6):2319-2331.
[25] LI Z J, LI W J, WANG Y S, et al.Establishment of a novel cell surface display platform based on natural "chitosan beads" of yeast spores[J].Journal of Agricultural and Food Chemistry, 2022, 70(24):7479-7489.