1,6-己二醇(1,6-hexanediol,1,6-HDO)是重要的化工中间体之一,可作为原料合成高附加值产品,例如聚酯多元醇和UV固化材料[1],可替代1,4-丁二醇、乙二醇、聚己内酯等产品,具有重要的工业价值。预计到2025年1,6-己二醇的市场规模将达到14.01亿美元,复合年增长率为8%。随着中国经济的迅速发展,尤其是下游应用领域的不断增加,国内1,6-己二醇需求量不断增长。然而据统计,我国约80%的1,6-己二醇仍需要从国外进口。目前,工业上己二醇的合成主要依靠己二酸二甲酯加氢反应[2],该方法虽然工艺成熟,但仍存在一些技术缺陷,例如催化剂回收和再生困难、副反应多,而且其生产需要高压甲级防爆装置,往往还存在设备腐蚀严重等问题,而环氧己烷加氢制己二醇[3]也存在高毒性、易燃、易爆等安全隐患[4],因此,生物法合成1,6-己二醇的研究受到广泛关注。
与化学法合成1,6-己二醇相比,生物法合成1,6-己二醇具有绿色、无污染、反应条件温和的等优点[5]。目前,生物法合成1,6-己二醇的研究仍处于起步阶段[6-8]。ZHANG等[6]从头设计了一锅法生物催化环己烷合成1,6-己二醇的工艺路线,经过酶的优化筛选,30 mmol/L底物在10 h内生成了13 mmol/L HDO,但该途径涉及8个酶,反应链较长,底物利用率较低。KHUSNUTDINOVA等[7]用纯化的羧酸还原酶(carboxylic acid reductase, CAR)结合辅因子再生系统、无机焦磷酸酶和醛酮还原酶(aldo-keto reductase, AKR),在体外催化己二酸还原为6-羟基己酸和1,6-己二醇的混合物,转化率达到76%;同时,在大肠杆菌体内构建CARs表达系统,催化己二酸还原为6-羟基己酸和1,6-己二醇的混合物,转化率达到54%~57%。KRAMER等[8]建立了一种基于NADPH消耗的生长耦合酶工程选择策略,并对来源于Mycobacterium avium subsp.Paratuberculosis的羧酸还原酶(MAV CAR)进行改造,使得6-羟基己酸和1,6-己二醇的综合转化率达到87%。然而,在上述研究中主要以羧酸还原酶为对象,而对于催化醛基生醇的醛酮还原酶关注较少。RODRIGUEZ等[9]对52个在大肠杆菌基因组中注释为还原酶、氧化还原酶和脱氢酶的候选基因进行了全面筛选,发现了与短链脂肪醇的形成有关的13个基因(adhe、adhP、beta、eutG、fuO、yeaY、yjgB、yqhD、yahk、yebO、gldA、dkgA和yghA)。同时,FATMA等[10]研究发现,adhe和yqhD与大肠杆菌中短链脂肪醇的形成密切相关。因此,开展己二醇合成相关醛酮还原酶研究具有重要意义。
本团队前期通过异源途径挖掘和代谢工程改造,实现了己二酸的全生物法合成,在本研究中,通过对羧酸还原酶和醛酮还原酶进行适配组装和开展发酵过程强化,利用生物基己二酸构建了1,6-己二醇的全细胞催化人工通路。与体外催化相比,全细胞催化避免了辅因子的额外添加,操作更为简便,本研究为后续1,6-己二醇的生物合成奠定了基础。
1 材料与方法
1.1 实验材料
1.1.1 菌株与质粒
本研究采用大肠杆菌BL21(DE3)来进行表达,采用大肠杆菌JM109来保藏质粒。
本研究中所使用的菌株列于表1中。
表1 菌株
Table 1 Strains

菌株基因型来源E.coli JM109endA1 glnV44 thi-1 relA1 gyrA96 recA1 mcrB+ Δ(lac-proAB) e14-[F’ traD36 proAB+ lacIq lacZΔM15] hs-dR17(rK- mK+)本实验室保存E.coli BL21(DE3)E.coli B F-ompT gal dcm lon hsdSB (rB-mB-) λ (DE3[lacI lacUV5-T7 gene 1 ind1 sam7 nin5])本实验室保存质粒pETDuet-1ColE1 ori, lacI, T7lac, AmpR本实验室保存pRSFDuet-1RSF ori, lacI, T7lac, KanR本实验室保存pRSF-MSMpRSF harboring the optimized gene of CAR from Mycolicibacterium smegmatis MC2 155, KanR本研究pET-adhEpETDuet-1 harboring genes adhE from E.coli MG1655, AmpR本研究pET-yajOpETDuet-1 harboring genes yajO from Pseudomonas putida, AmpR本研究pET-ahrpETDuet-1 harboring genes ahr from E.coli MG1655, AmpR本研究pET-yahKpETDuet-1 harboring genes yahK from E.coli MG1655, AmpR本研究pET-frmApETDuet-1 harboring genes frmA from E.coli MG1655, AmpR本研究pET-yqhDpETDuet-1 harboring genes yqhD from E.coli MG1655, AmpR本研究
1.1.2 工具酶及试剂
抗生素[氨苄青霉素(Amp)、卡那霉素(Kan)],上海生工生物工程有限公司;葡萄糖、MgCl2、K2HPO4,上海国药集团化学试剂有限公司;胰蛋白胨、酵母提取物,英国oxoid公司。
分子生物学工具:DNA marker、DNA聚合酶PrimeSTAR Max、限制性内切酶,宝日医生物技术(北京)有限公司;T4 DNA连接酶,上海生工生物工程有限公司;同源重组酶C115,南京诺唯赞生物科技股份有限公司。
试剂盒:质粒小量提取试剂盒、DNA片段纯化试剂盒,上海生工生物工程有限公司。
1.1.3 培养基
LB培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,pH值调至7.0。若需要固体培养基,添加20 g/L琼脂粉。
SOB培养基(g/L):酵母粉5,蛋白胨20,KCl 0.186,NaCl 0.5,MgCl2·6H2O 2.03,pH值调至7.0。
M9培养基(g/L):Na2HPO4 6.78,KH2PO4 3,NaCl 0.5,NH4Cl 1,MgSO4 0.24,CaCl2 0.0115,葡萄糖4,pH值调至7.0。MgSO4、CaCl2、葡萄糖单独配制灭菌。
TB培养基(g/L):K2HPO4·3H2O 16.34,KH2PO4 2.31,酵母粉24,蛋白胨12,甘油 4 mL/L。
以上培养基灭菌条件为121 ℃, 20 min。
1.1.4 PCR引物
本实验所用PCR引物如表2所示。
表2 引物序列
Table 2 List of DNA oligo nucleotide primers

引物名称引物序列Vector-FCATATGGCAGATCTCAATTGGVector-RGAATTCCCATGGTATATCTCCTTCadhE-FGAAGGAGATATACCATGGGAATTCATGGCTGTTACTAATGTCGCTGAACadhE-RCAATTGAGATCTGCCATATGTTAAGCGGATTTTTTCGCTTTTTTCTCAGCahr-FGAAGGAGATATACCATGGGAATTCATGTCGATGATAAAAAGCTATGCCGCahr-RGATATCCAATTGAGATCTGCCATATGTCAAAAATCGGCTTTCAACACCACyahK-FGAAGGAGATATACCATGGGAATTCATGAAGATCAAAGCTGTTGGTGCATATTCyahK-RCCAATTGAGATCTGCCATATGTCAGTCTGTTAGTGTGCGATTATCGATAACfrmA-FGAAGGAGATATACCATGGGAATTCATGAAATCACGTGCTGCCGTTGfrmA-RGATATCCAATTGAGATCTGCCATATGTCAGTAACGAATTACGGTTCGAATGGyqhD-FGAAGGAGATATACCATGGGAATTCATGAACAACTTTAATCTGCACACCCyqhD-RCCAATTGAGATCTGCCATATGTTAGCGGGCGGCTTCGTATATAC
1.1.5 仪器与设备
UV2450紫外可见光分光光度计,日本Shimadzu公司;Eppendorf高速离心机、PCR仪、5424台式高速离心机,德国 Eppendorf(艾本德)公司;Nexis GC-2030型气相色谱仪,岛津公司;G154DWS 立式压力蒸汽灭菌锅,美国致微有限公司;DYY-6C型电泳仪,北京六一电泳仪厂;GelDoc Go凝胶成像系统,美国Bio-Rad公司;HYL-C3组合式摇床,太仓市强乐实验设备有限公司;恒温培养箱,上海医疗器械研究所。
1.2 实验方法
1.2.1 质粒的构建
来源于Mycolicibacterium smegmatis MC2 155的羧酸还原酶(MSM CAR)的核苷酸序列交由上海生工合成,其两端带有限制性内切酶位点Nco I和BamH I。利用Nco I和BamH I对合成的基因和pRSFDuet-1质粒进行双酶切,产物纯化后使用T4 DNA连接酶连接。将连接产物导入大肠杆菌JM109中,通过菌落PCR和Sanger测序进行筛选,最终构建质粒pRSF-MSM。
两端带有限制性内切酶位点Nde I和Kpn I的醛酮还原酶yajO的核苷酸序列交由上海生工合成。利用Nde I和Kpn I对合成的yajO基因和pETDuet-1质粒进行双酶切,产物纯化后使用T4 DNA连接酶连接。将连接产物导入大肠杆菌JM109中,通过菌落PCR和Sanger测序进行筛选,最终构建质粒pET-yajO。
以Vector-F和Vector-R为引物,以pETDuet-1为模板扩增5.2 kb的PCR片段。以adhE-F和adhE-R为引物,以大肠杆菌MG1655单菌落为模板扩增2.7 kb 的PCR片段;以ahr-F和ahr-R为引物,以大肠杆菌MG1655单菌落为模板扩增1.1 kb的PCR片段;以yahK-F和yahK-R为引物,以大肠杆菌MG1655单菌落为模板扩增1.1 kb的PCR片段;以frmA-F和frmA-R为引物,以大肠杆菌MG1655单菌落为模板扩增1.2 kb的PCR片段;以yqhD-F和yqhD-R为引物,以大肠杆菌MG1655单菌落为模板扩增1.2 kb的PCR片段。利用同源重组的方法,分别将pETDuet-1扩增片段与基因扩增片段用C115酶进行组装,将产物导入大肠杆菌JM109中,通过菌落PCR和Sanger测序进行筛选,最终构建质粒pET-ahr、pET-yahK、pET-frmA、pET-yqhD、pET-adhE。
1.2.2 菌株培养方法
取甘油管菌液50 μL接入20 mL LB培养基中,于37 ℃,250 r/min摇床振荡培养过夜,作为种子液;将1 mL种子液转接于含有50 mL LB培养基的250 mL烧瓶中,外加6 g/L葡萄糖。在37 ℃,250 r/min条件下进行摇瓶发酵实验,培养2 h后,加1 mmol/L的异丙基-β-D-硫代半乳糖苷(isopropyl β-D-1-thiogalactopyranoside,IPTG)诱导并添加2 g/L的己二酸底物,转至30 ℃,250 r/min条件下进行摇瓶发酵实验。
1.2.3 发酵液处理方法
取1 mL发酵液样品,将样品在8 000 r/min下离心10 min,使菌体与上清液充分分离,取500 μL上清液,用500 μL正丁醇萃取,充分振荡后静置,以确保水相与有机相充分分离。取上层有机相,并使用0.22 μm滤膜过滤,对经过处理后的样品进行气相分析。
1.2.4 发酵液中己二醇含量检测方法
气相检测通过使用气相色谱仪进行。色谱柱为 SH-Wax 毛细管柱(30 m×0.25 mm,0.25 μm)。色谱条件为初始温度80 ℃,保持1 min,以10 ℃/min的升温速率升至230 ℃,并保持10 min。气相载气为N2,流速1.2 mL/min。进样器温度230 ℃,进样量1 μL。检测器采用火焰离子化检测器,检测器温度300 ℃。
1.2.5 大肠杆菌的己二醇耐受检测方法
设计两组实验以检测己二醇对发酵菌株的影响作用。其中A组实验:在菌株对数生长期,即2.5 h诱导时分别加入0、10、20、30、40、50 g/L 1,6-己二醇,通过测定OD600值,观察菌株的生长情况变化;B组实验:在12 h时分别加入0、10、20、30、40、50 g/L 1,6-己二醇,通过测定OD600值,观察菌株的生长情况变化。
1.2.6 己二醇合成发酵强化
培养基优化:为探究不同培养基类型对1,6-己二醇产量的影响,分别使用LB、SOB、M9、TB培养基进行摇瓶发酵,同时控制底物质量浓度为2 g/L、初始糖质量浓度为6 g/L、诱导时间为2 h,并通过GC检测1,6-己二醇的最终产量。
底物浓度优化:为探究底物浓度对1,6-己二醇产量的影响,控制底物己二酸的质量浓度为2、4、6、8、10、12、14 g/L,使用TB培养基进行摇瓶发酵,同时控制初始糖质量浓度为6 g/L、诱导时间为2 h的条件,并通过GC检测1,6-己二醇的最终产量。
初始糖浓度优化:为探究不同初始糖浓度对1,6-己二醇产量的影响,分别设置初始糖质量浓度为2、4、6、8、10 g/L,使用TB培养基进行摇瓶发酵,同时控制底物质量浓度为10 g/L、诱导时间为2 h的条件,并通过GC检测1,6-己二醇的最终产量。
诱导时间优化:为探究不同诱导时间对1,6-己二醇产量的影响,分别设置诱导时间为1.5、2、2.5、3、3.5、4 h,使用TB培养基进行摇瓶发酵,同时控制底物质量浓度为10 g/L、初始糖质量浓度为8 g/L,并通过GC检测1,6-己二醇的最终产量。
2 结果与分析
2.1 大肠杆菌的己二醇耐受性分析
大肠杆菌BL21 (DE3)作为一种常用的候选宿主,具有遗传背景清晰、生产周期短、效率高和成本低等显著优势[11]。为了探究大肠杆菌对1,6-己二醇的耐受性,本研究在大肠杆菌生长过程中分别加入了不同浓度的1,6-己二醇,如图1所示,当1,6-己二醇质量浓度低于20 g/L时,在诱导时期以及培养12 h时分别加入1,6-己二醇,大肠杆菌的菌浓度均没有明显减低,表明该浓度下己二醇对大肠杆菌的生长没有较大影响,从而表现出良好的耐受性,因此大肠杆菌可以用作1,6-己二醇生产的出发菌株。但当1,6-己二醇质量浓度高于30 g/L时,大肠杆菌生长抑制明显,表明高浓度的己二醇可能与其他醇类物质相似,会对微生物的细胞膜造成一定程度的破坏,导致细胞内部物质泄漏,还可能干扰微生物的生物代谢过程,影响其正常细胞功能的发挥[12]。
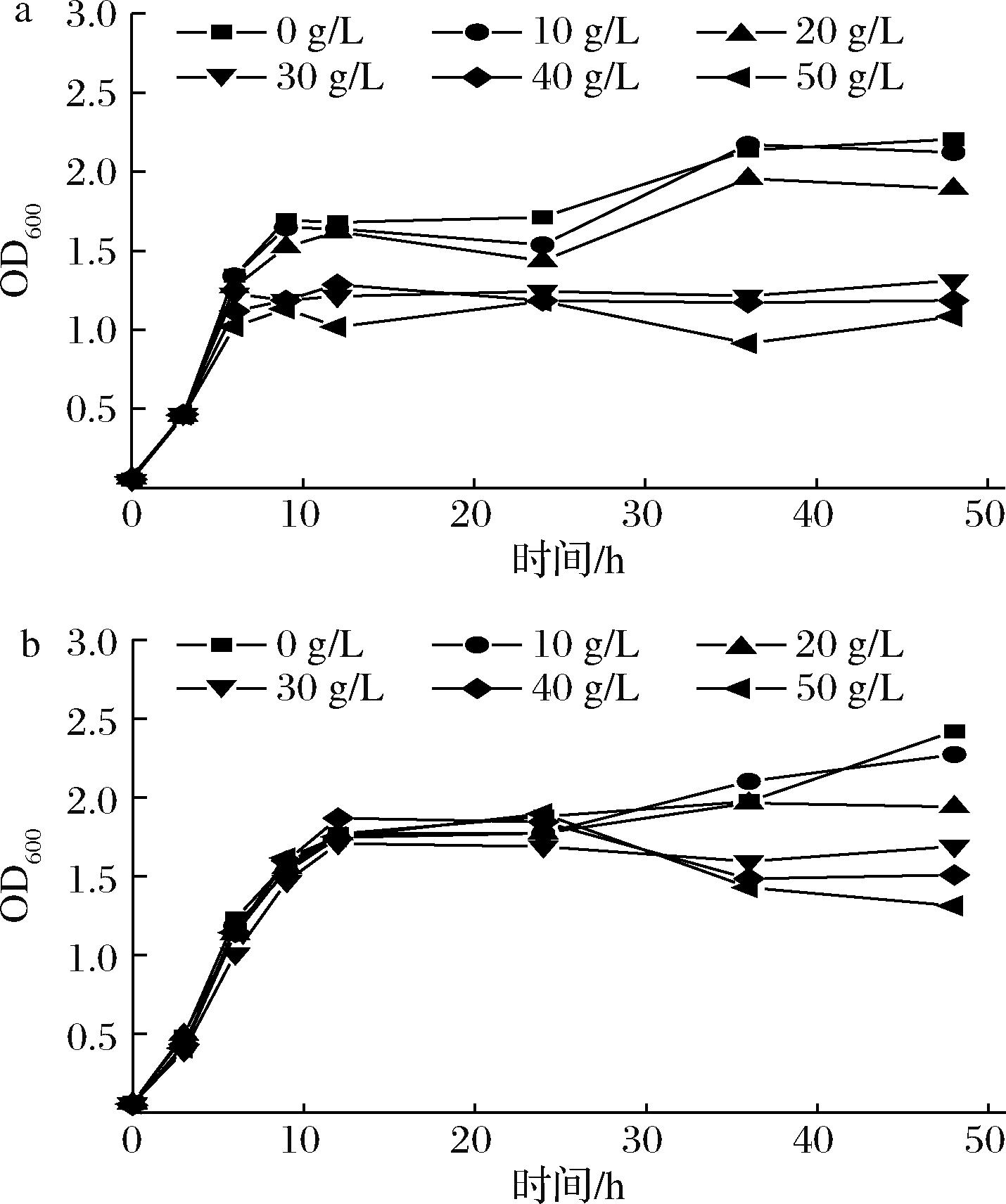
a-3 h时加入己二醇的生长情况;b-12 h时加入己二醇的生长情况
图1 大肠杆菌的己二醇耐受性
Fig.1 The hexanediol tolerance in E. coli
2.2 己二醇生物合成路径的构建
本研究利用来源于M. smegmatis MC2 155的羧酸还原酶(MSM CAR)和来源于E.coli MG1655的醛酮还原酶(AdhE),将两者基因在大肠杆菌中进行异源表达,初步构建了1,6-己二醇生物合成工程菌株MSM-adhE。在该生物合成途径(图2)中,己二酸首先被羧酸还原为己酸半醛,己酸半醛在醛酮还原酶的作用下转化为6-羟基己酸,6-羟基己酸再经过进一步的羧酸还原反应合成6-羟基己醛,最后6-羟基己醛经醛酮还原作用合成1,6-己二醇。
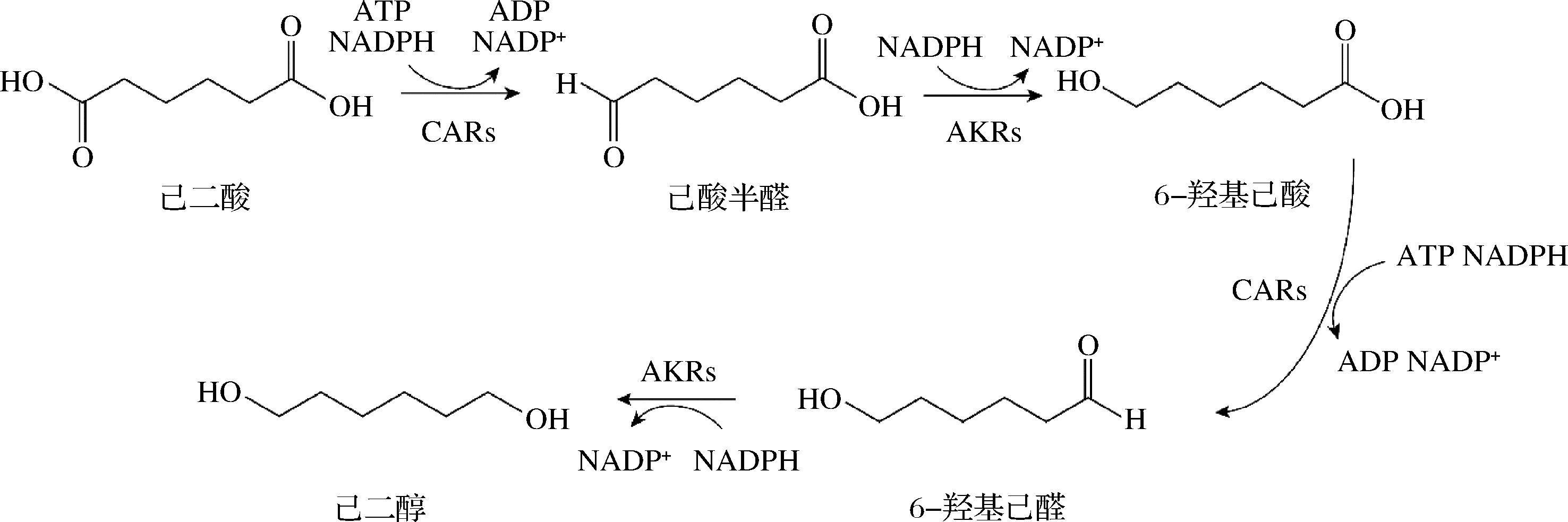
图2 在大肠杆菌中构建的己二醇生物合成途径
Fig.2 Hexadiol biosynthetic pathway constructed in E. coli
为了确定1,6-己二醇的生成和代谢途径的成功构建,将工程菌株MSM-adhE进行发酵,利用GC-MS进行检测与分析(图3)。通过质谱(图3-a、图3-b)鉴定大肠杆菌BL21(DE3)的发酵液样品,发现了1,6-己二醇的3个特征离子碎片(m/z 67、41、42)。同时,发酵液样品与1,6-己二醇标样均在相同时间出峰(图3-c、图3-d)。上述结果证实1,6-己二醇在大肠杆菌BL21(DE3)工程菌株中的成功制备,经检测其产量为9.66 mg/L,为进一步的研究奠定了基础。
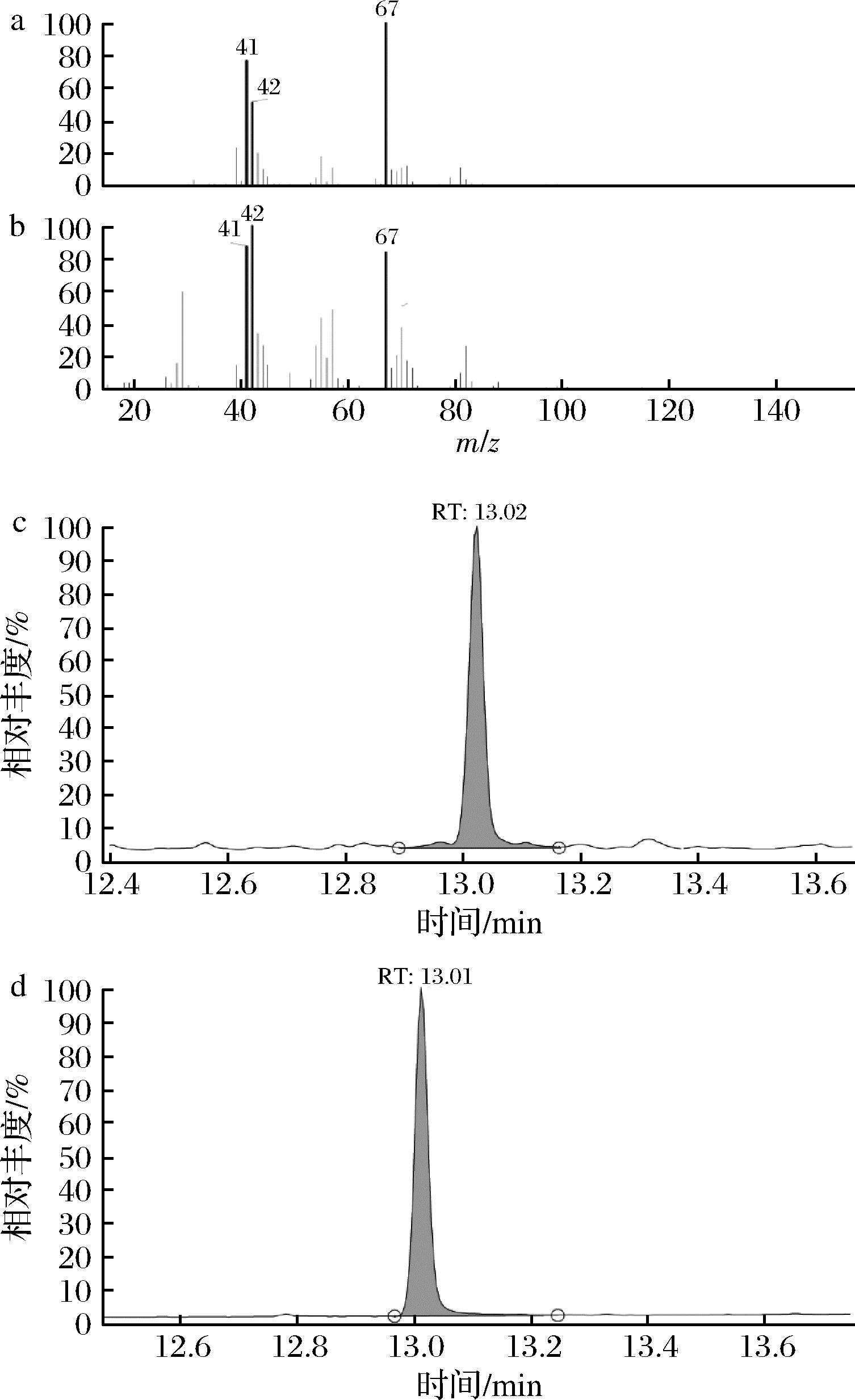
a-发酵样品质谱图;b-1,6-己二醇标准品质谱图; c-发酵样品气相图谱;d-1,6-己二醇标准品气相图谱
图3 工程菌株MSM-adhE发酵产物的GC-MS分析
Fig.3 GC-MS analysis of fermentation products of the engineered strain MSM-adhE
2.3 醛酮还原酶同工酶的筛选
在己二醇合成途径中,醛酮还原酶参与两步生醇反应,对己二醇的合成影响较大,因此结合底物相似性和文献报道[13-16],分别选择了5种AKR来构建 MSM CAR-AKR级联体系,以提高己二醇的生产效率,包括来源于E. coli的醛还原酶(yqhD,GenBank ID:947493)、来源于E. coli的醛还原酶(yahK,GenBank ID:944975)、来源于E. coli的醛还原酶(yahK,GenBank ID:948802)、来源于E. coli的S-(羟甲基)谷胱甘肽脱氢酶(frmA,GenBank ID:944988)、来源于Pseudomonas putida的醛酮还原酶(yajO,GenBank ID:83679922)。以大肠杆菌BL21(DE3)为宿主菌株,将上述AKR的编码基因与MSM CAR的编码基因分别在大肠杆菌BL21(DE3)中共表达,并对工程菌株进行摇瓶发酵。结果如图4所示,不同工程菌株1,6-己二醇产量存在显著差异,其中,工程菌株MSM-yqhD的己二醇产量最高达到61.8 mg/L,是出发菌株的6.4倍,表明醛酮还原酶yqhD生醇效果较好。yqhD偏好中长链底物[17],可以保护细胞免受脂质氧化生醛的毒性作用,在1,3-丙二醇和异丁醇[18-19]的生物合成中也表现出较好的效果。因此,利用菌株MSM-yqhD进行后续研究。
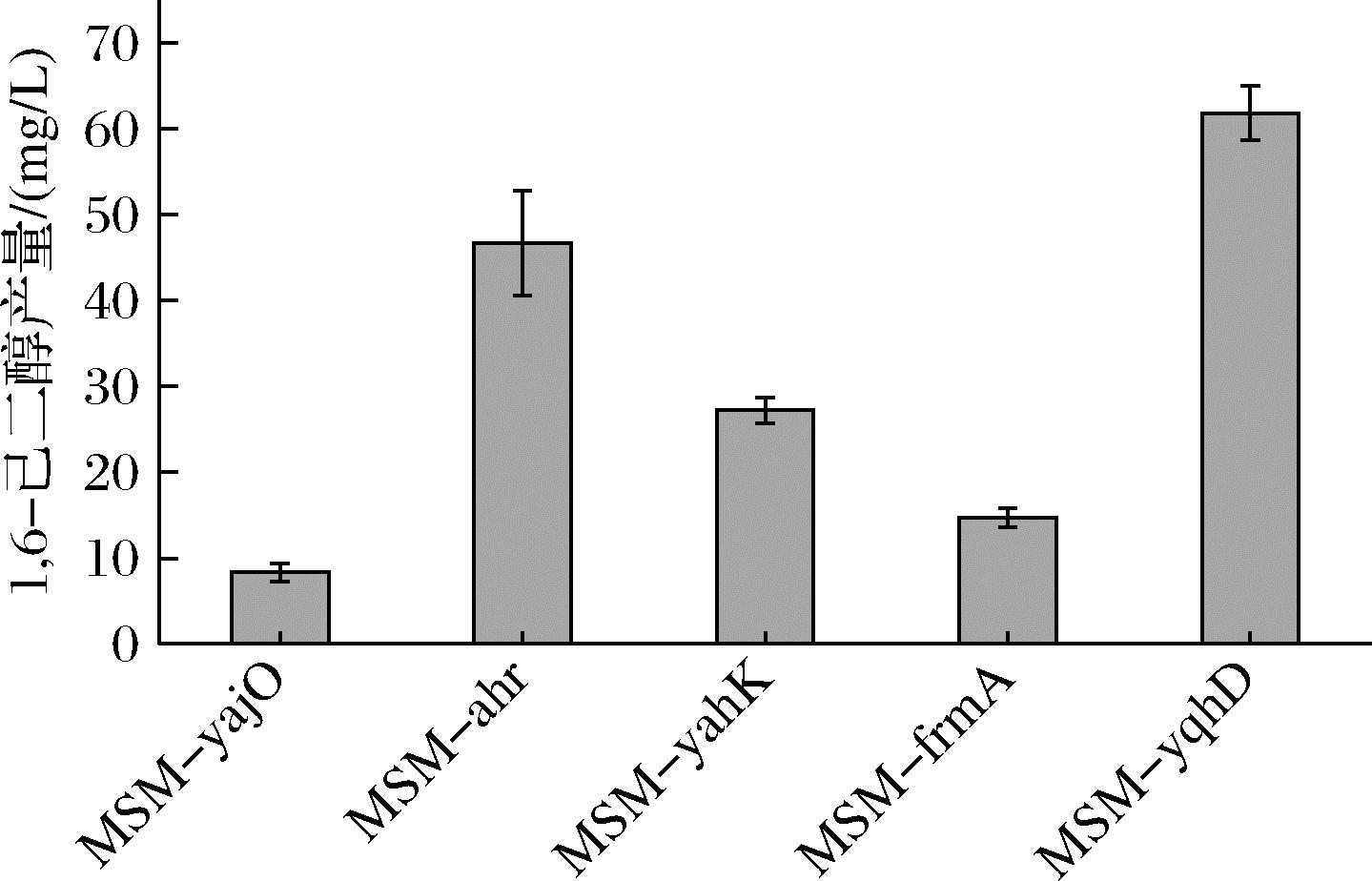
图4 AKR同工酶替换优化1,6-己二醇合成
Fig.4 Optimization of 1,6-hexanediol synthesis by AKR isozyme substitution
2.4 发酵优化
2.4.1 培养基种类对1,6-己二醇合成的影响
培养基是指供给微生物生长繁殖,由不同营养物质组合配制而成的基质,不同培养基可影响工程菌株的生长与基因表达。因此,本研究首先探究最适合1,6-己二醇合成的培养基类型。结果如图5所示,对比其他培养基,TB培养基中1,6-己二醇的产量最高为71.96 mg/L。与王杰明等[20]报道的利用霍氏肠杆菌产2,3-丁二醇的培养基优化结果一致,TB培养基含有丰富的营养成分,有利于菌体生长[21]。此外,TB培养基中含有甘油,其被菌体吸收后可以提供足够的还原力(NADH和NADPH),能够有效的促进羧酸还原酶和醛酮还原酶的催化过程。因此,在之后的研究中选择TB培养基作为主要培养基。
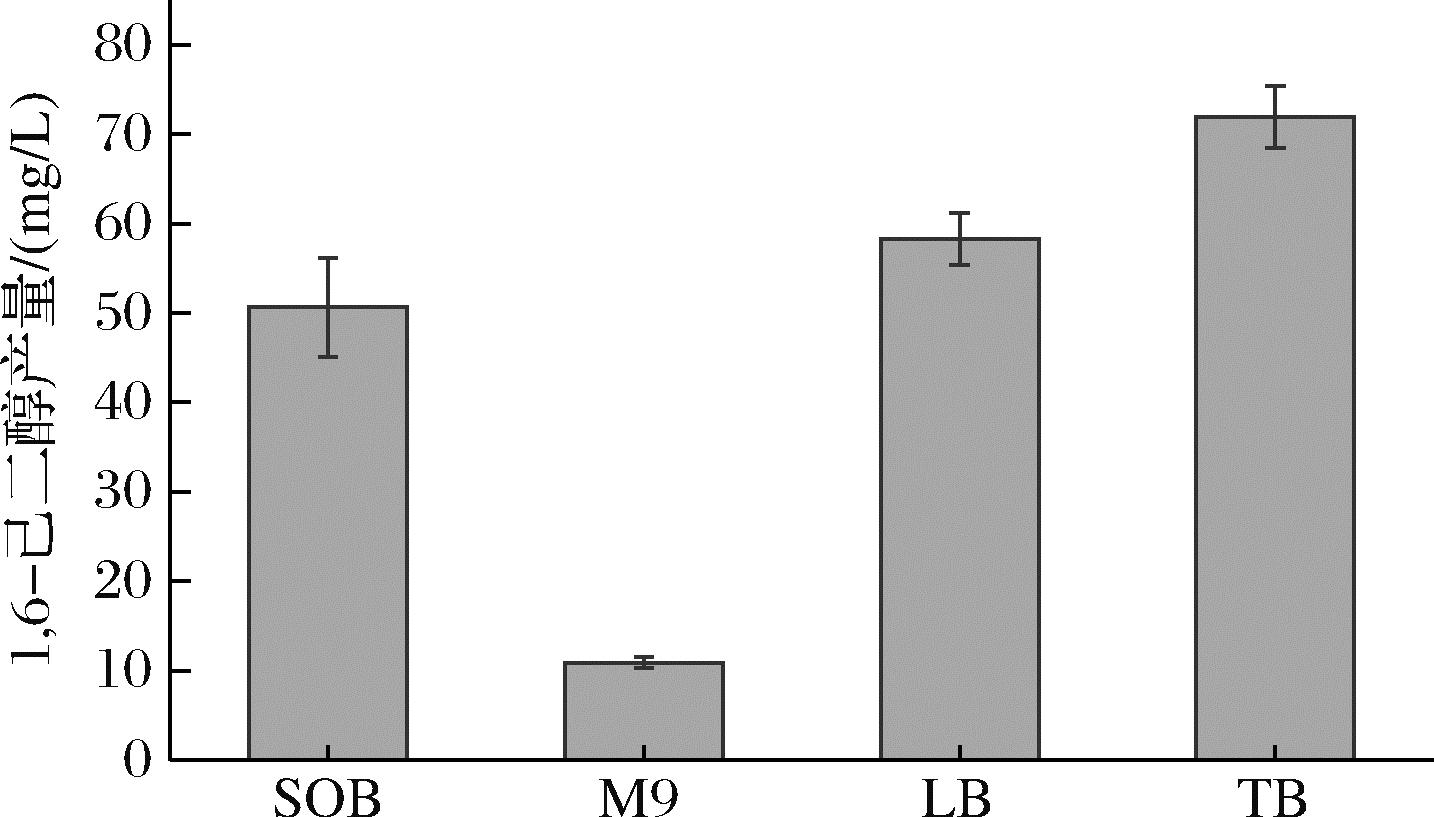
图5 培养基种类对1,6-己二醇合成的影响
Fig.5 Effect of medium type on the yield of 1,6-hexadiol
2.4.2 底物浓度对1,6-己二醇合成的影响
底物浓度是发酵过程中的一个重要影响参数。高浓度的底物通常会抑制微生物的生长从而影响催化进行,而低浓度的底物则不能满足菌体的合成消耗从而对最终产量产生影响。因此,需要确定1,6-己二醇生产过程中的最佳底物浓度。如图6所示,随着底物浓度的提高,发酵液中1,6-己二醇产量先升高后下降,在己二酸质量浓度为10 g/L时,己二醇产量达到最高为331.36 mg/L,与对照相比,产量提高4.4倍。当底物浓度较低时,随着底物浓度的提高,菌株能利用更多的底物来合成1,6-己二醇;而高浓度的己二酸可能与其他有机酸类似会对菌株的生长代谢产生影响作用[22],因此,确定其最佳初始底物质量浓度为10 g/L。
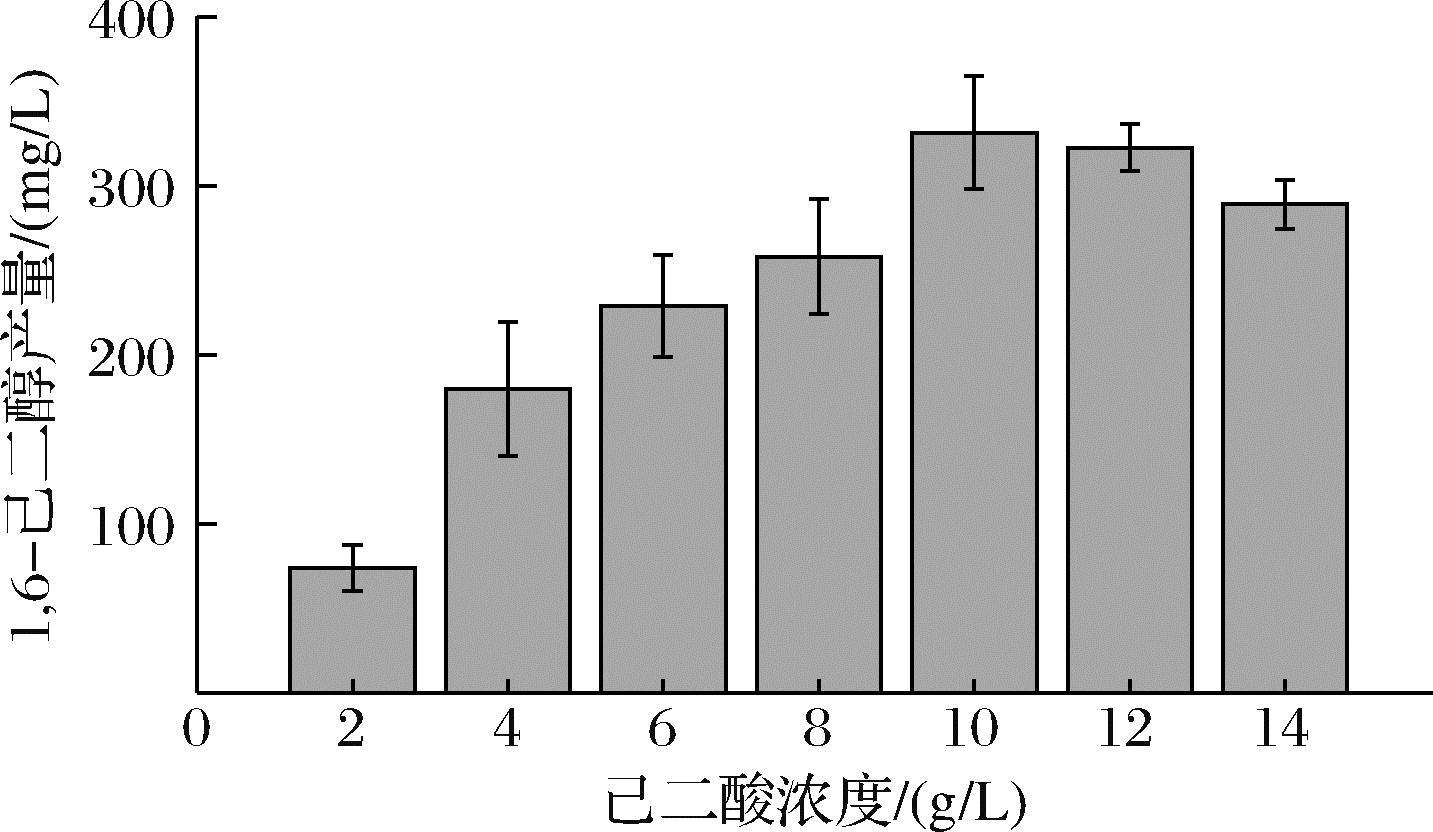
图6 底物浓度对1,6-己二醇合成的影响
Fig.6 Effect of substrate concentration on the yield of 1,6-hexadiol
2.4.3 初始糖浓度对1,6-己二醇合成的影响
碳源是重要的能量来源,被微生物吸收后可以被代谢网络转化用于微生物的生长代谢过程,葡萄糖是大肠杆菌发酵过程中的重要碳源,在大肠杆菌的生长代谢中发挥着重要影响作用,同时,大量研究[23-24]表明,利用葡萄糖和甘油作为碳源,更有利于提高目标产物产量和菌体的生长活力。因此,需要确定1,6-己二醇生产过程中的的最佳初始葡萄糖浓度。如图7所示,在一定范围内随着初始糖浓度的增加,发酵液中1,6-己二醇产量逐渐提高。当添加初始糖质量浓度为8 g/L时,1,6-己二醇产量最高达到669.88 mg/L。适量的葡萄糖能通过糖酵解途径提供ATP,有利于发酵菌株的生长以及过程酶CAR的催化;而更高浓度葡萄糖会引发“葡萄糖效应”,导致大量杂酸的产生,对目的产物的合成存在抑制作用,同时也会降低ATP产生的效率[25]。因此,选择初始糖浓度为8 g/L进行下一步的研究。
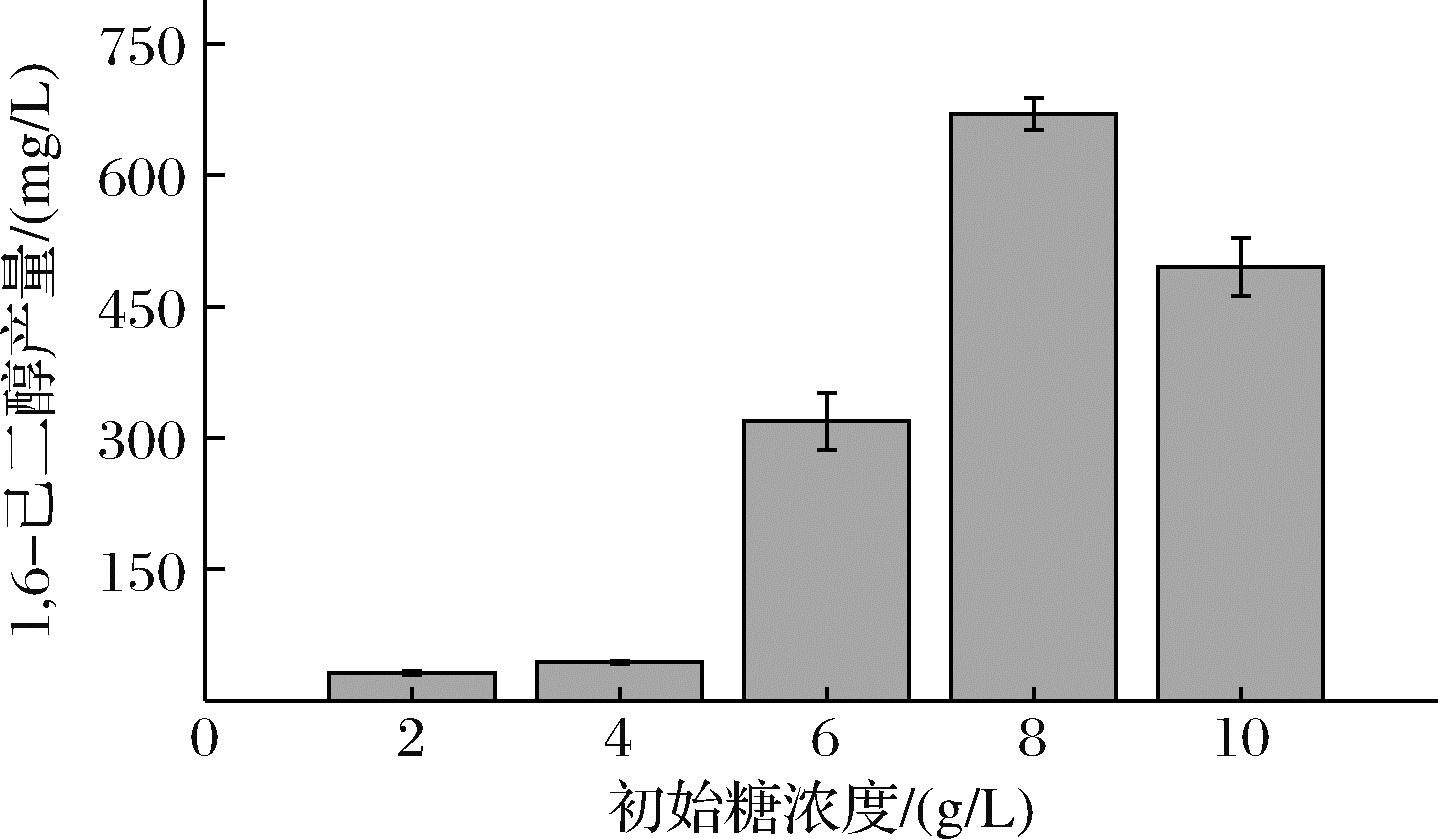
图7 初始糖浓度对1,6-己二醇合成的影响
Fig.7 Effect of initial sugar concentration on the yield of 1,6-hexadiol
2.4.4 诱导时间对1,6-己二醇合成的影响
大肠杆菌在其进入对数生长期时,菌体生长旺盛,增殖快,若过早诱导,菌体吸收的营养都用于表达外源蛋白,势必会严重影响菌体生长,总的外源蛋白表达量也会变少;而过晚诱导菌体蛋白表达量也会受到影响。因此,需要确定1,6-己二醇生产过程中的最佳诱导时间。结果如图8所示,诱导时间对1,6-己二醇合成的影响较大,在诱导时间为2.5 h时,产量最高达到818.16 mg/L。此时对发酵液中残余的己二酸进行检测,发现实际己二酸消耗量仅为1.19 g/L,经计算己二醇的摩尔转化率达到0.85 mol/mol。因此,确定工程菌株MSM-yqhD在摇瓶中发酵1,6-己二醇的最佳诱导时间为2.5 h。
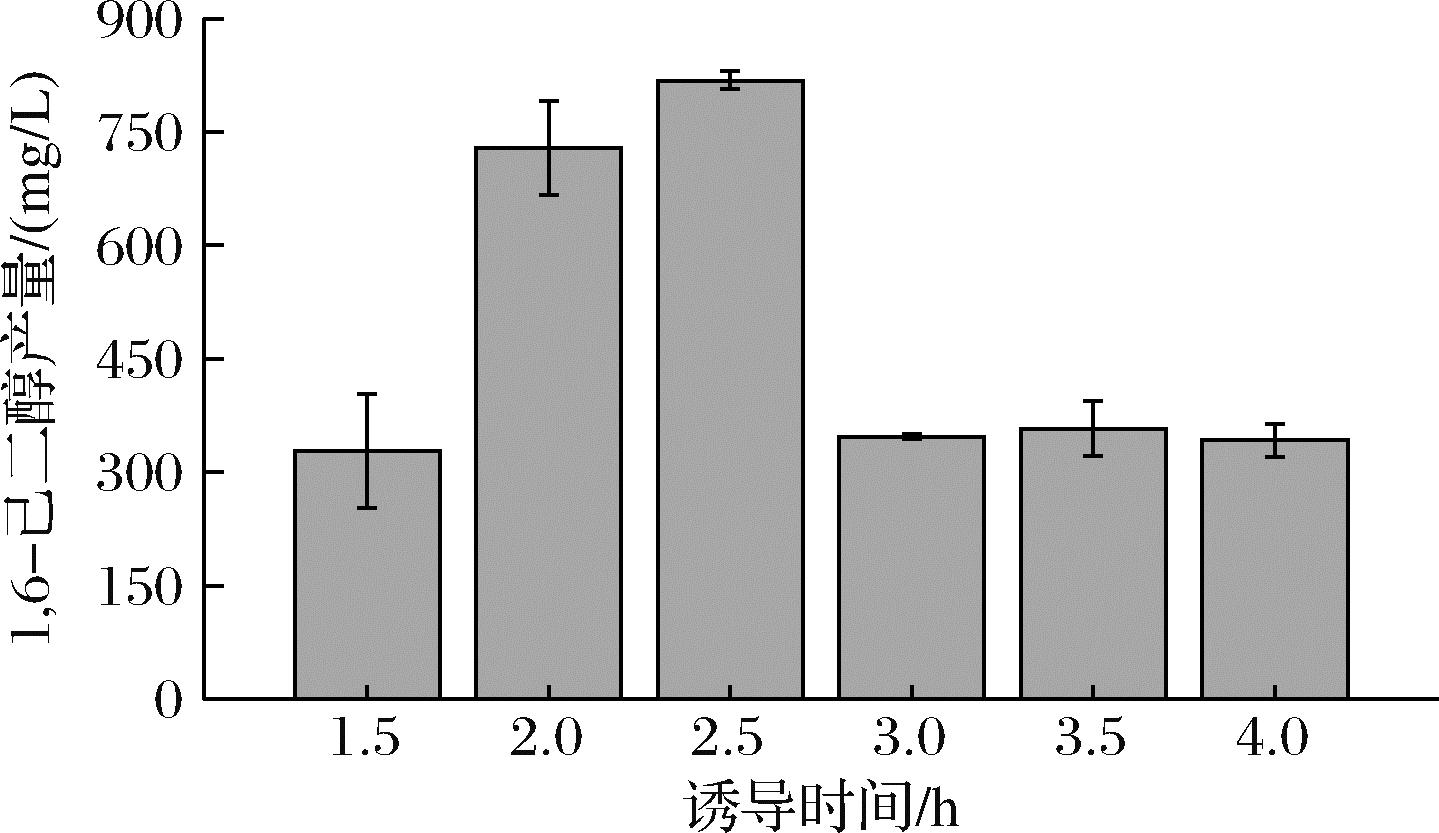
图8 诱导时间对1,6-己二醇合成的影响
Fig.8 Effect of induction time on the yield of 1,6-hexadiol
3 结果与分析
本研究通过共表达羧酸还原酶MSM CAR和醛酮还原酶AdhE,在大肠杆菌BL21(DE3)构建了生物基1,6-己二醇的全细胞人工途径。通过对AKR酶进行同工酶筛选,并与羧酸还原酶MSM CAR适配组装,1,6-己二醇产量达到61.8 mg/L,相对初始菌株提高6.4倍。通过发酵培养基优化,确定了最优培养基为TB培养基,最佳底物质量浓度为10 g/L,最佳初始糖质量浓度为8 g/L,最佳诱导时间为2.5 h,优化后1,6-己二醇产量达到818.16 mg/L,相较于初始菌株提高了84.7倍,摩尔转化率达到85%。本研究可为1,6-己二醇代谢途径功能酶的研究及其衍生物的合成提供参考。
[1] FIGUEIREDO F C A, JORD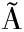 O E, CARVALHO W A.Adipic ester hydrogenation catalyzed by platinum supported in alumina, titania and pillared clays[J].Applied Catalysis A:General, 2008, 351(2):259-266.
O E, CARVALHO W A.Adipic ester hydrogenation catalyzed by platinum supported in alumina, titania and pillared clays[J].Applied Catalysis A:General, 2008, 351(2):259-266.
[2] BUNTARA T, NOEL S, PHUA P H, et al.Caprolactam from renewable resources:Catalytic conversion of 5-hydroxymethylfurfural into caprolactone[J].Angewandte Chemie (International Ed), 2011, 50(31):7083-7087.
[3] GODASE V P, KUMBHAR N M, GOVINDWAR S P, et al.Characterization reveals a putative epoxide hydrolase from Yarrowia lipolytica with the ability to convert rac-1, 2-epoxyhexane to (R)-diol[J].Process Biochemistry, 2023, 125:248-258.
[4] PARK J B, BÜHLER B, HABICHER T, et al.The efficiency of recombinant Escherichia coli as biocatalyst for stereospecific epoxidation[J].Biotechnology and Bioengineering, 2006, 95(3):501-512.
[5] SINGH V, CHAUDHARY D K, MANI I, et al.Recent advances and challenges of the use of cyanobacteria towards the production of biofuels[J].Renewable and Sustainable Energy Reviews, 2016, 60:1-10.
[6] ZHANG Z W, LI Q, WANG F, et al.One-pot biosynthesis of 1, 6-hexanediol from cyclohexane by de novo designed cascade biocatalysis[J].Green Chemistry, 2020, 22(21):7476-7483.
[7] KHUSNUTDINOVA A N, FLICK R, POPOVIC A, et al.Exploring bacterial carboxylate reductases for the reduction of bifunctional carboxylic acids[J].Biotechnology Journal, 2017, 12(11):1-12.
[8] KRAMER L, LE X, RODRIGUEZ M, et al.Engineering carboxylic acid reductase (CAR) through a whole-cell growth-coupled NADPH recycling strategy[J].ACS Synthetic Biology, 2020, 9(7):1632-1637.
[9] RODRIGUEZ G M, ATSUMI S.Isobutyraldehyde production from Escherichia coli by removing aldehyde reductase activity[J].Microbial Cell Factories, 2012, 11:90
[10] FATMA Z, JAWED K, MATTAM A J, et al.Identification of long chain specific aldehyde reductase and its use in enhanced fatty alcohol production in E.coli[J].Metabolic Engineering, 2016, 37:35-45.
[11] SHARAN S K, THOMASON L C, KUZNETSOV S G, et al.Recombineering:A homologous recombination-based method of genetic engineering[J].Nature Protocols, 2009, 4(2):206-223.
[12] YUAN Y B, BI C H, NICOLAOU S A, et al.Overexpression of the Lactobacillus plantarum peptidoglycan biosynthesis MurA2 gene increases the tolerance of Escherichia coli to alcohols and enhances ethanol production[J].Applied Microbiology and Biotechnology, 2014, 98(19):8399-8411.
[13] SHAH A, LIU W, KINLEY B, et al.Protein engineering of coenzyme-A-dependent aldehyde dehydrogenase for commercial scale 1,4-butanediol production in Escherichia coli[J].The FASEB Journal, 2015, 29(S1):720.
[14] NAKAMURA C E, WHITED G M.Metabolic engineering for the microbial production of 1, 3-propanediol[J].Current Opinion in Biotechnology, 2003, 14(5):454-459.
[15] ALEKU G A, ROBERTS G W, LEYS D.Biocatalytic reduction of α, β-unsaturated carboxylic acids to allylic alcohols[J].Green Chemistry, 2020, 22(12):3927-3939.
[16] SARAK S, PAGAR A D, KHOBRAGADE T P, et al.A multienzyme biocatalytic cascade as a route towards the synthesis of α, ω-diamines from corresponding cycloalkanols[J].Green Chemistry, 2023, 25(2):543-549.
[17] SULZENBACHER G, ALVAREZ K, VAN DEN HEUVEL R H H, et al.Crystal structure of E.coli alcohol dehydrogenase YqhD:Evidence of a covalently modified NADP coenzyme[J].Journal of Molecular Biology, 2004, 342(2):489-502.
[18] TANG X M, TAN Y S, ZHU H, et al.Microbial conversion of glycerol to 1, 3-propanediol by an engineered strain of Escherichia coli[J].Applied and Environmental Microbiology, 2009, 75(6):1628-1634.
[19] ATSUMI S, WU T Y, ECKL E M, et al.Engineering the isobutanol biosynthetic pathway in Escherichia coli by comparison of three aldehyde reductase/alcohol dehydrogenase genes[J].Applied Microbiology and Biotechnology, 2010, 85(3):651-657.
[20] 王杰明, 卢艳波, 杨小雁, 等.产2, 3-丁二醇霍氏肠杆菌的筛选及其发酵优化[J].食品与发酵工业, 2022, 48(21):30-35.WANG J M, LU Y B, YANG X Y, et al.Screening of 2, 3-butanediol-producing Enterobacter hormaechei and its fermentation optimization[J].Food and Fermentation Industries, 2022, 48(21):30-35.
[21] WANG F L, LEE S Y.High cell density culture of metabolically engineered Escherichia coli for the production of poly(3-hydroxybutyrate) in a defined medium[J].Biotechnology and Bioengineering, 1998, 58(2-3):325-328.
[22] WARNECKE T, GILL R T.Organic acid toxicity, tolerance, and production in Escherichia coli biorefining applications[J].Microbial Cell Factories, 2005, 4:25.
[23] KIM Y S, LEE J H, KIM N H, et al.Increase of lycopene production by supplementing auxiliary carbon sources in metabolically engineered Escherichia coli[J].Applied Microbiology and Biotechnology, 2011, 90(2):489-497.
[24] ZENG X, CHEN X S, REN X D, et al.Insights into the role of glucose and glycerol as a mixed carbon source in the improvement of ε-poly-L-lysine productivity[J].Applied Biochemistry and Biotechnology, 2014, 173(8):2211-2224.
[25] BORIRAK O, BEKKER M, ROLFE M D, et al.Dynamic changes of the Escherichia coli transcriptome and proteome exerted by glucose repression[J].The FASEB Journal, 2013, 27(1).DOI:10.1016/S0 140-6736(87)92065-4.