L-天冬酰胺酶 (L-asparaginase,EC.3.5.1.1 L-ASNase) 是一种酰胺水解酶,其主要功能是催化L-天冬酰胺水解,产生L-天冬氨酸和氨。在自然界中,L-ASNase分布广泛,主要存在于植物、动物和微生物中[1]。微生物来源的L-ASNase由于酶学性质优异、易于大规模生产、经济效益好等特点进而成为研究热点[2]。根据L-ASNase的分布位置和功能结构的不同,细菌来源的L-ASNase可以分为I型和Ⅱ型两种类型。I型L-ASNase存在于细胞质中,通常以二聚体的形式存在,古菌来源的I型L-ASNase具有超高的热稳定性,可应用于油炸食品工艺[3],然而具有较低的底物亲和力;Ⅱ型L-ASNase存在于周质空间中,通常以同源四聚体形式出现,具有较高的底物亲和力,对谷氨酰胺的活力远低于I型,因此被广泛用于临床治疗,如治疗急性淋巴细胞白血病和淋巴肉瘤等疾病[4]。
丙烯酰胺是一种酰胺类化合物,具有潜在的神经毒性、遗传毒性及致癌性[5]。丙烯酰胺主要通过美拉德反应中的天冬酰胺途径形成,其中L-天冬酰胺(L-asparagine,L-ASN)和还原糖是丙烯酰胺形成的主要前体物质[6]。根据欧洲食品安全局的数据,人类主要通过油炸马铃薯制品、烘焙食品和咖啡摄入丙烯酰胺[7]。在食品加工中,特别是在烘焙和油炸食品加工前使用L-ASNase进行处理,可以减少食品中的L-ASN含量,从源头上减少丙烯酰胺的生成。这种做法几乎不会影响食物的色泽、味道和营养特性[8]。
在油炸类食品的预处理环节,通过热烫 (>60 ℃)和酶处理相结合的方式可以减少食品中的L-ASN,从而间接抑制食品中丙烯酰胺的生成。然而,由于处理过程温度较高,需要酶在高温下具有较高的底物转化率和酶活力。目前国内外已有实现了商品化的L-ASNase,分别是帝斯曼公司的PreventASe®和诺维信公司的 Acrylaway®[9]。然而这两种L-ASNase均来源于嗜温微生物,其最适温度都在60 ℃以下,其在高温时的热稳定性较差,限制了其在工业生产中的应用[9];另一方面,来源于嗜热微生物的L-ASNase最适反应温度可达80~95 ℃,可满足油炸类食品的工艺需求。例如Thermococcus zilligii AN1 tziAN1_1来源的L-ASNase,这种酶在70~85 ℃均具有较好的热稳定性[10]。然而,此类来源的L-ASNase多为I型,对底物催化效率较低。因此,为了满足工艺需求,有必要对嗜热微生物来源的I型L-ASNase进行分子改造以提高其催化活性。
常见的酶分子改造策略包括定向进化、理性设计和半理性设计。定向进化不需要对蛋白结构有深入了解就可以进行酶工程改造,但需要引入随机突变和高通量筛选,工作量大且筛选效率较低[11]。理性设计可利用计算机技术针对性进行分子改造,能够有效减少筛选工作,但受到蛋白质信息限制,阳性突变率较低[12]。而半理性设计中和了两种方法的优缺点,在理性设计的基础上结合饱和突变构建高质量且容量小的突变体文库,可进一步提高阳性突变率和筛选效率[13]。ZHOU等[14]通过半理性设计构建突变体文库并利用组合突变获得催化效率提升6.32倍的突变体。PANG等[15]通过半理性设计构建了铜绿假单胞菌脂氧合酶 (lipoxygenase,LOX) 的突变体文库,最优突变体的kcat/Km增加了9.2倍。
为提高I型L-ASNase的催化活性,本研究选择吉利热球菌(Thermococcus zilligii)来源的L-ASNase (TzI) 作为研究对象,通过分子对接和虚拟氨基酸饱和突变方法获得对 L-ASNase催化效率有潜在影响的突变点以筛选催化效率显著提高的突变体,进一步通过分子动力学模拟分析突变酶催化效率提高的原因。最后利用商品酶、原始酶和突变酶分别对薯条进行酶处理以探究对油炸薯条中丙烯酰胺的影响。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与质粒
质粒 pET-28a(+)、菌株 E.coli JM109、E.coli BL21(DE3)均由本实验室保存。
1.1.2 主要试剂
质粒提取试剂盒、柱回收试剂盒、IPTG、一步克隆试剂盒、Dpn I限制性内切酶和硫酸卡纳霉素,上海生工生物工程股份有限公司;Prime STAR Max Premix DNA 聚合酶、Prime STAR HS DNA聚合酶、大肠杆菌感受态细胞制备试剂盒,北京宝日医生物技术有限公司;蛋白Marker、蛋白电泳 Loading buffer、Bis-Tris 预制凝胶,上海赛默飞世尔科技公司;HisTrap HP 5 mL预装式层析柱和脱盐柱HisTrap Desalting 5 mL,美国GE公司;Bradford 蛋白浓度测定试剂盒,上海碧云天生物技术有限公司;商品酶天门冬酰胺酶Acrylaway 3500 BG,大连诺维信生物技术有限公司;其他生物学试剂均购自上海国药集团化学试剂公司。
1.1.3 培养基及缓冲液
LB 培养基(g/L):酵母提取物 5,蛋白胨 10,NaCl 5,pH 7.0。固体培养基中添加质量分数1.5%~2%的琼脂。
TB 培养基(g/L):酵母提取物 24,蛋白胨 12,甘油 5,KH2PO4 2.31,K2HPO4·3H20 16.4。
0.05 mol/L Tris-HCl:6.057 g Tris 加超纯水定容至1 L,浓盐酸调节pH值至8.5。
1.5 mol/L TCA:称取 49.02 g 定容至 200 mL,避光保存。
缓冲液A:20 mmol/L KH2PO4-KH2PO4,pH 7.5。
缓冲液B:20 mmol/L KH2PO4-KH2PO4,500 mmol/L咪唑,pH 7.5。
20 mmol/L L-天冬酰胺溶液:称取 0.132 g L-天冬酰胺,并用50 mmol/L Tris-HCl (pH 8.5) 缓冲溶液定容至50 mL。
10 mmol/L 硫酸铵溶液:称取 0.066 1 g L-天冬酰胺,并用50 mmol/L Tris-HCl (pH 8.5) 缓冲溶液定容至50 mL。
Nessler 试剂:配 200 mL 需称取 28.06 g KOH 至 250 mL 烧杯中,加 100 mL 水溶解,冷却后,称取 14.16 g KHgI4,KOH 溶液加到 KHgI4中定容至 200 mL,配好后室温放置12 h 后再用,避光保存。
Carrez I:称取3.60 g Fe(SCN)2溶解到100 mL的超纯水中,室温避光保存。
Carrez II:称取7.20 g ZnSO4或12.82 g ZnSO4·7H2O溶解到100 mL的超纯水中,室温避光保存。
1.2 实验方法
1.2.1 引物设计
构建的引物如表1所示。
表1 文中所用引物
Table 1 Primers used in the paper

引物名称引物序列(5′-3′)T-FGAAGGAGATATACCATGGGCATGAAGATCCTGATCCTGGGCACT-RCAGTGGTGGTGGTGGTGGTGGGACTCCTTCTTGCCGATCTCApET-28a-FCACCACCACCACCACCACTGApET-28a-RGCCCATGGTATATCTCCTTCTTAAAGTTAAACJP-T-FCGTAGAGGATCGAGATCTCGATCCCJP-T-RTCAAGACCCGTTTAGAGGCCCSER155-TRP-FCTAGGGTCTGGAAAGTCCACTCCACCGGCCCCAASER155-TRP-RGTGGACTTTCCAGACCCTAGTGCCCAGCATGAGLU231-HIS-FATTATTTTGCATGGTTACGGCGCTGGTGGCATGLU231-HIS-RCCGTAACCATGCAAAATAATACCATGAGCTTTGTTAGCAACAGCGLN263-TRP-FATGACCACCTGGGCTCTCCATGGCGGAGTCGATCTGAGLN263-TRP-RTGGAGAGCCCAGGTGGTCATGACGACAGGCTGLU231-GLN-FATTATTTTGCAAGGTTACGGCGCTGGTGGCATGLU231-GLN-RCCGTAACCTTGCAAAATAATACCATGAGCTTTGTTAGCAACAGC
续表1

引物名称引物序列(5′-3′)GLN263-PHE-FATGACCACCTTCGCTCTCCATGGCGGAGTCGATCTGAGLN263-PHE-RTGGAGAGCGAAGGTGGTCATGACGACAGGCTGLU231-LEU-FATTATTTTGTTGGGTTACGGCGCTGGTGGCATGLU231-LEU-RCCGTAACCCAACAAAATAATACCATGAGCTTTGTTAGCAACAGCGLN263-LEU-FATGACCACCTTGGCTCTCCATGGCGGAGTCGATCTGAGLN263-LEU-RTGGAGAGCCAAGGTGGTCATGACGACAGGCTGLU231-ILE-FATTATTTTGATCGGTTACGGCGCTGGTGGCATGLU231-ILE-RCCGTAACCGATCAAAATAATACCATGAGCTTTGTTAGCAACAGCALA264-PRO-FACCACCCAACCTCTCCATGGCGGAGTCGATCTGATGAAGALA264-PRO-RCCATGGAGAGGTTGGGTGGTCATGACGACAGGLEU265-TRP-FACCCAAGCTTGGCATGGCGGAGTCGATCTGATGAAGTATGAGGLEU265-TRP-RCCGCCATGCCAAGCTTGGGTGGTCATGACGACM-JP-FTCACCCATGGCACCGATACTCM-JP-RACTCAGCTTCCTTTCGGGCTTT
注:粗体为突变位点。
1.2.2 重组表达菌株的构建
本章所使用的L-ASNase基因片段来自于T. zilligii,所用基因委托上海生工生物工程股份有限公司合成。将基因tzi与 pET28a(+)通过同源重组连接构成重组质粒载体 pET28a(+)-tzi。以重组质粒 pET28a(+)-tzi为模板,采用表1 中的引物进行反向 PCR。PCR 体系为:模板 1 μL,上游引物 1 μL,下游引物 1 μL,无菌水 22 μL,Prime STAR Max Premix DNA 聚合酶 25 μL。PCR 条件:98 ℃预变性 3 min,98 ℃变性 10 s,55 ℃退火 15 s,72 ℃延伸 1 min 30 s,30个循环,72 ℃继续延伸 10 min,4 ℃保温。将 PCR 后的产物加入 Dpn I 消化模板,消化后进行柱回收。将回收后的片段转 入 E.coli JM109(DE3) 感受态中,挑取长出的转化子过夜培养,提质粒送测序。将测序正确的转化子转入 E.coli BL21(DE3)得到重组菌。
1.2.3 重组酶与突变酶的表达及纯化
选取单菌落接种于10 mL LB液体培养基,在37 ℃、220 r/min条件下培养12 h。随后,取600 μL含有重组质粒的菌液接种于含有千分之一硫酸卡那霉素的30 mL TB培养基,继续在37 ℃、220 r/min下培养1.5~2 h,直至OD600值达到0.6~0.8。接着在TB培养基中添加IPTG使其终浓度达到1 mmol/L,将培养温度降至28 ℃继续诱导6 h。将发酵液进行高速离心获得菌体沉淀并利用PBS缓冲溶液 (pH 7.4) 进行重悬,接着利用高压匀质机在4 ℃下破碎10 min并高速离心后获得胞内上清液,并通过SDS-PAGE分析蛋白表达。选择上清液作为粗酶液,使用AKTA pure蛋白纯化仪,采用镍柱亲和层析技术对胞内粗酶液进行纯化。首先用缓冲液A平衡镍柱;随后使用不同梯度的缓冲液B来洗脱L-ASNase,将纯酶从镍层析柱中洗脱,并收集纯酶液;最后,利用Sephadex G-25层析填料的His Trap脱盐柱进行脱盐过程,去除其中的咪唑残留物。最终,经过这一系列步骤纯化后的野生型酶TzI和突变型酶L265W可进一步用于后续的酶学测定。
1.2.4 酶活力测定
配制400 μL的标准酶活反应体系,包括20 mmol/L L-天冬酰胺和50 mmol/L Tris-HCl 缓冲液 (pH 8.5) 及10 μL酶液。首先提前将20 mmol/L L-天冬酰胺50 mmol/L Tris-HCl 缓冲液(pH 8.5)在90 ℃金属浴中预热10 min,加入10 μL酶液反应5 min,后续加入100 μL 1.5 mol/L TCA终止反应。接着将反应液以 12 000 r/min离心30 s,取其中200 μL上清液加入另一个干净2 mL离心管中,并加入1 400 μL去离子水和200 μL Nessler试剂显色10 min,最后使用96孔酶标板于 450 nm 处检测吸光值,对照组先加TCA再加酶液。酶活力定义为在酶的最适反应条件下每分钟生成1 μmoL氨所需要的酶量。
1.2.5 最适反应温度测定
测定了原始酶TzI及突变酶L265W在不同温度下(40、50、60、70、80、85、90、95 ℃)的相对酶活力以获得最适反应温度。
1.2.6 热稳定性与半衰期的测定
将原始酶TzI和突变酶L265W置于 80 ℃的金属浴中热处理30~120 min,冰上冷却15 min后测定酶活力,以未处理的酶活力为100%,ln(残余酶活力)为纵坐标,t为横坐标进行线性拟合,计算 kd,得到 t1/2。
1.2.7 动力学参数测定
配制1、2、4、8、10、20、40、80 mmol/L的L-天冬酰胺,测定不同底物浓度下原始酶TzI及突变酶L265W的酶活力。利用 Origin 2021 进行非线性拟合,计算 Km、kcat及kcat/Km。
1.2.8 分子对接及突变位点的选择
为确认TzI的催化活性位点方便进行分子对接,利用多重序列比对工具ClustalW (https://www.genome.jp/tools-bin/clustalw) 及Espcript 3.0[16] (https://espript.ibcp.fr/ESPript/cgi-bin/ESPript.cgi) 将本研究T. zilligii (TzI:WP_010478656.1)、Thermococcus kodakarensis (ThA:WP_011250607.1)、Pyrococcus yayanosii (PyA:WP_013906452.1)、Pyrococcus horikoshii (PhA:BAA29135.1) 和Escherichia coli L-ASNase Ⅱ (EcA Ⅱ:AGE81914.1) 4种不同来源的L-ASNase序列进行比对。
使用SWISS-MODEL (https://swissmodel.expasy.org/) 对原始酶及突变酶进行同源建模获得蛋白质三级结构并使用SAVES服务器 (https://saves.mbi.ucla.edu/) 验证模型质量。三级结构利用PyMoL 2.6.0软件进行可视化。配体L-ASN的三级结构从化合物数据库PubChem (https://pubchem.ncbi.nlm.nih.gov/) 中获得,并使用Discovery Studio 2022的Minimize Ligands模块对配体L-ASN 进行构象优化。然后,基于CDOCKER模块进行半柔性对接获得10个蛋白质-配体复合物的构象,根据-CDOCKER_ENERGY得分进行排序,选择最高得分的构象进行下一步分析。
通过Discovery Studio 2022中的Calculate Mutation Energy (Binding) 模块,本文将最优的蛋白质-配体复合物的构象选中配体L-ASN周围所有氨基酸作为候选的突变点并进行虚拟饱和突变。将计算结果中的突变能从低到高进行排序,选择突变能最低的前10个突变体进行实验表征验证以获得最优突变体。使用web服务器DynaMut[17]分析点突变对 TzI稳定性和灵活性的影响。DynaMut 利用 Bio3D 和粗粒度弹性网络接触模型 (ENCoM) 两种方法,能够快速分析点突变对振动熵变化引起的蛋白质灵活性 (ΔΔS) 和稳定性 (ΔΔG) 的影响。
1.2.9 分子动力学模拟
使用GROMACS-2020[18]对酶进行分子动力学模拟。基于AmberTools 2021对底物L-ASN进行格式转换后,使用acpype (https://pypi.org/project/acpype/)获得了底物的力场文件和拓扑文件。底物和TzI(及其突变体)分别赋予了GAFF和FF14 sb力场。模型系统在一个填充SPC/E水模型的立方盒子里,盒子边界与酶复合物的距离为12 Å。然后使用钠离子和氯离子平衡体系的电荷,然后采用最速下降法进行能量最小化,正则系宗(canonical ensemble,NVT) 平衡和等温等压系宗(isothermal-isobaric ensemble,NPT) 平衡分别在300 K条件下进行了200 ps平衡。随后解除限制,在300 K条件下模拟了50 ns,用于分析均方根偏差 (root-mean-square deviation,RMSD) 和均方根波动 (root mean square fluctuation,RMSF)。
1.2.10 L-ASNase对油炸薯条中丙烯酰胺的影响
酶处理及薯条的油炸工艺流程参考ZUO等[10]的研究,从超市购买马铃薯进行清洗、去皮并切成0.5 cm×0.5 cm×6 cm长条状,然后浸泡在去离子水中约1 min将处理后的马铃薯长条在80 ℃的耐热L-ASNase酶液(10 U/mL)中热烫处理4 min,之后将处理后的样品在60 ℃下干燥15 min,以减少含水量。随后,在175 ℃的油炸锅中油炸1 min,沥干多余油脂之后,将薯条冷冻24 h,再在油炸锅中复炸5 min。最后,将样品沥去油脂冷却干燥,以备提取丙烯酰胺进行分析。
1.2.11 丙烯酰胺的提取与检测
丙烯酰胺提取方法参考WANG等[3]的研究,在研钵中捣碎油炸薯条样品,在50 mL离心管中称取1 g已混匀的样品并加入10 mL正己烷,利用漩涡振荡仪处理1 min。然后以10 000 r/min离心5 min并除去上清液中的正己烷,重复3次上述操作,静置样品在通风橱中直至正己烷完全挥发。随后,在样品中加入10 mL超纯水、500 μL Carrez I和500 μL Carrez Ⅱ,于30 ℃ 水浴摇床上以200 r/min 振荡30 min。最后,离心机以10 000 r/min离心30 min。利用1 mL注射器分离上清液,并通过0.22 μm微孔滤膜过滤。
丙烯酰胺的检测采用LC-MS/MS按照以下的色谱条件进行检测。色谱柱:HSS T3柱(1.8 μm,2.1 mm×100 mm);流动相A:水(含0.1%FA),流动相B:乙腈,洗脱梯度:0~2 min 5% B,2~5 min:95%B,5~8 min:5%B;柱温40 ℃;流速0.25 mL/min;进样体积2 μL。采用丙烯酰胺标准溶液建立的线性校准函数对丙烯酰胺进行定量,丙烯酰胺含量以μg/kg表示。
2 结果与分析
2.1 L-ASNase基因的克隆与表达
从NCBI数据库中检索T. zilligii来源 L-ASNase的基因序列,长度为990 bp,通过SignalP6.0预测该基因无信号肽,合成重组质粒 pET28a(+)-tzi,质粒构建过程如图1-a所示,图1-b为该质粒构建过程中需要的tzi基因扩增片段和pET-28a(+)载体的线性化片段,利用一步克隆试剂盒将两个片段进行同源重组并进一步转化至E.coli JM109 (DE3) 感受态细胞,经过菌落PCR及测序验证获得阳性转化子,其对应的重组质粒为pET28a(+)-tzi。将该重组质粒 pET28a(+)-tzi转入E.coli BL21 (DE3) 感受态细胞中,构建重组菌株E.coli BL21/pET28a(+)-tzi,获得的重组酶命名为TzI。按照1.2.3节方法对重组菌株进行诱导表达,发酵液经过离心取部分上清液样品进行酶活力测定,发现样品无酶活力,说明TzI在胞外不表达。接着将离心后的菌体沉淀利用PBS缓冲溶液进行重悬,利用高压匀质机破碎离心后获得胞内上清液,测得TzI胞内上清液酶活力为 1 364.75 U/mL(图2-a),经过SDS-PAGE分析发现TzI在分子质量 35.5 kDa 处有明显的蛋白条带,将TzI胞内上清液经过镍柱亲和层析纯化及脱盐后,获得条带单一的纯酶(图2-b),比酶活力为 2 124.92 U/mg。
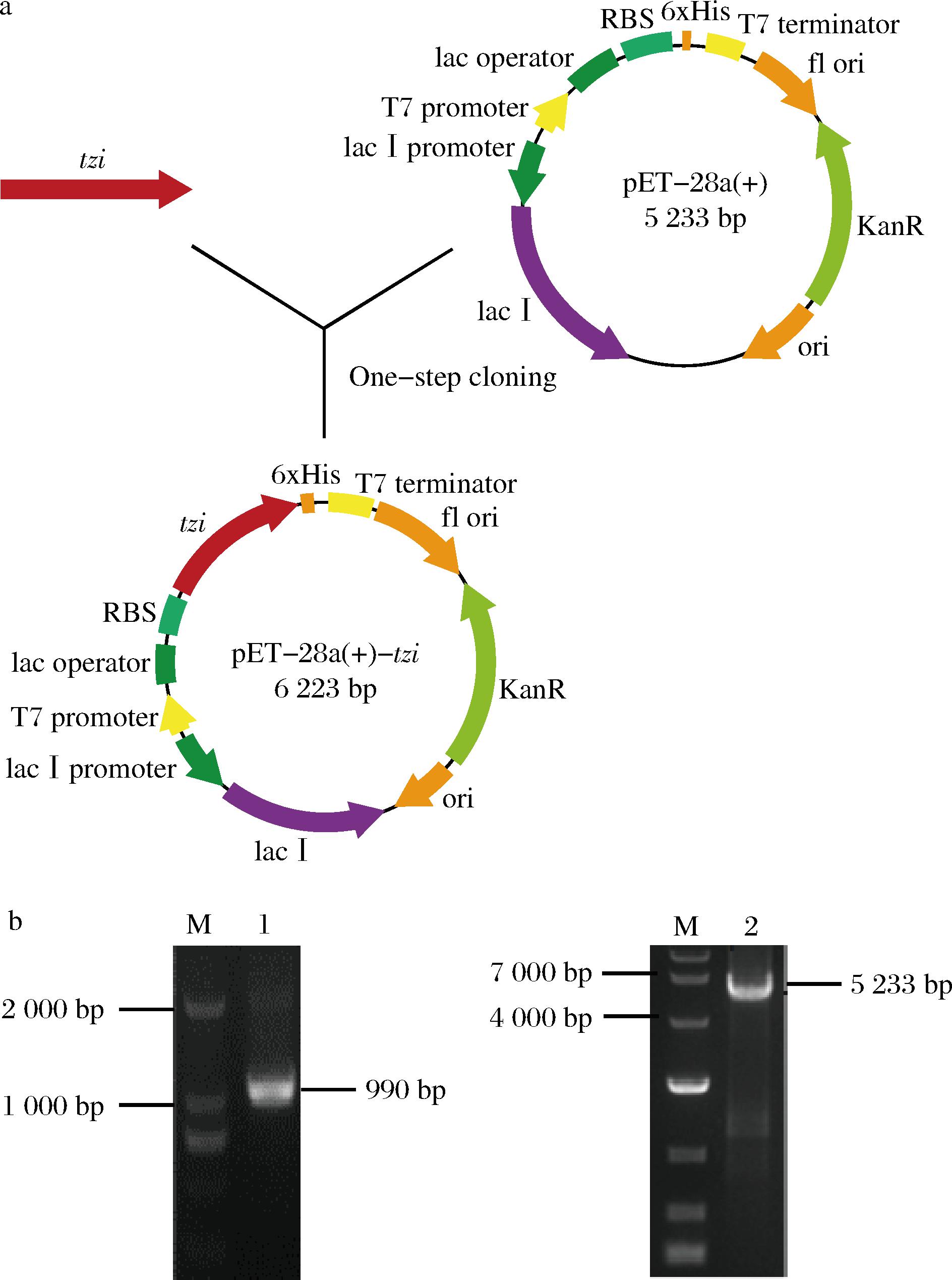
a-质粒构建示意图,M-DNA 2 000 bp标准Marker,泳道 1-tzi基因扩增片段;b-琼脂糖凝胶电泳图,M-DNA 10 000 bp标准Marker,泳道2-pET-28a(+)的线性化片段
图1 重组质粒的构建
Fig.1 Construction of recombinant plasmid
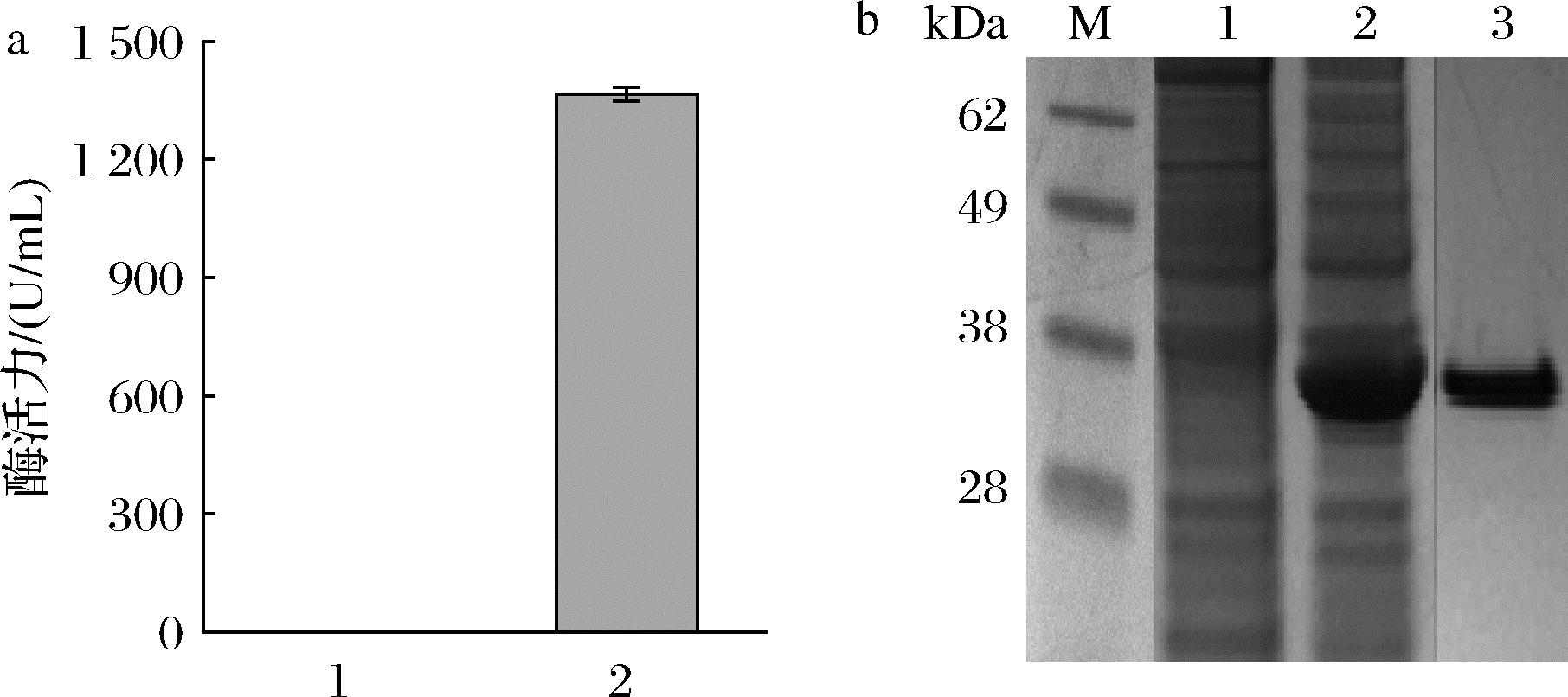
a-大肠杆菌胞内上清液酶活力测定;b-TzI粗酶液的 SDS-PAGE分析
图2 TzI在大肠杆菌中的表达与纯化
Fig.2 Expression and purification of TzI in Escherichia coli
注:样品1-BL21/pET-28a(+)的胞内上清液,样品2-BL21/pET-28a(+)-tzi的胞内上清液,样品3-BL21/pET-28a(+)-tzi 的纯酶, M-蛋白标准Marker。
2.2 突变体的预测和表征
为确定TzI的活性中心残基,通过ClustalW及Espcript 3.0在线工具将TzI与已报道的I型L-ASNase (ThA、PyA和PhA) 和Ⅱ型L-ASNase (EcA Ⅱ) 进行多重序列比对(图3),其中ThA的残基T11、Y21、S54、T55、T85、D86 和K156,以及邻近亚基的Tyr233’和Glu275’在L-ASNase结构中都是重要且高度保守的[19],PyA的活性中心残基为T11、Y21、S52、T83、D84和K154[20],ECA Ⅱ的活性中心残基为T12、Y25、S58、T89、D90和K162[21],TzI对应的活性中心残基为T11、Y21、S54、T85、D86和K156,这些残基均高度保守,本研究以此为基础将酶与底物进行分子对接。YAO等[22]对PhA的结构进行分析后发现,I型L-ASNase具有一个独特的柔性loop区(第9~28位氨基酸),这个柔性环通过β发夹结构以及与另一个亚单位上的α螺旋区域之间的相互作用来稳定酶的结构。在序列和结构上,这个柔性loop区相当于Ⅱ型酶中N端柔性loop区(第10~32位氨基酸),这一区域在底物与酶活性位点的结合中起着关键的作用。对PhA与TzI的结构进行序列比对后发现,TzI也具有一个类似的柔性loop区,该区域对应的是第9~28位氨基酸。

图3 不同微生物来源的L-ASNase多重序列对比
Fig.3 Comparison of L-ASNase multiple sequences from different microbial sources
注:黑色圆点表示TzI的活性中心残基,红色区域为保守氨基酸。
利用SWISS-MODEL网站以Thermococcus kodakarensis ASN (ThA) 的晶体结构 (PDB ID:5OT0,2.18 Å)为模板进行同源建模,得到原始酶TzI的三维结构模型(图4-a),同源性为77.37%,经过SAVES服务器验证,构建的模型质量均合格。在同源二聚体的接口处,一般有两个轴向相对并独立存在的活性中心[19, 23]。基于前面序列比对的结果已经确定TzI对应的活性中心残基为T11、Y21、S54、T85、D86和K156(图4-b),选择单聚体模型并利用Discovery Studio软件与底物L-ASN进行分子对接和单点虚拟饱和突变确定合适的氨基酸突变位点。根据与底物结合自由能变化选择小于-3 kcal/mol的前10个氨基酸突变位点:E231H、S155W、E231L、E231Q、Q231F、Q263W、L265W、A264P、Q263L、E231I(图4-c)。

a-同源二聚体建模(紫色和绿色卡通结构分别为二聚体的A链和B链);b-TzI与底物分子对接(天蓝色棍棒结构为TzI的活性催化位点, 彩色棍棒结构为底物L-天冬酰胺);c-突变体与底物结合自由能预测;d-原始酶与突变酶SDS-PAGE分析; e-原始酶与突变酶蛋白比酶活测定
图4 突变体的预测和表征
Fig.4 Prediction and characterization of mutants
按照1.2.2节所述方法构建了E231H、S155W、E231L、E231Q、Q231F、Q263W、L265W、A264P、Q263L、E231I共10个突变株。对突变菌株进行诱导表达和纯化后,发现除了E231H之外,其他9个突变株都能够正常表达。对收集到的纯化酶进行SDS-PAGE分析,结果显示蛋白条带大小均在35.5 kDa左右,与理论值相符(图4-d)。以L-天冬酰胺为底物,在pH 8.5、90 ℃条件下,对突变酶和原始酶的比酶活力进行测定,结果如图4-e所示,突变酶L265W的比酶活力为2 751.13 U/mg,与原始酶TzI相比提升了29%。
2.3 L-ASNase与突变酶的酶学性质研究
为了探究TzI突变前后酶学性质的差异,分别测定了原始酶TzI和突变酶L265W在不同温度下的酶活性(图5-a),结果显示它们的最适反应温度不变,均为90 ℃。同时为了探究两种酶在高温下的稳定性,我们在80、85、90 ℃条件下对它们进行了0~2 h的热处理,并每隔半小时取样测定残余酶活性。结果表明,在80 ℃时原始酶和突变酶的残余酶活性均相对稳定,2 h后仍保持在90%以上(图5-b)。在85 ℃条件下热处理2 h后,原始酶的残余活性下降至55%,而突变酶L265W的活性为72%(图5-c)。在90 ℃条件下热处理2 h后,原始酶的残余活性进一步下降至45%,而突变酶L265W的活性为55%(图5-d)。与原始酶相比,突变酶L265W在80、85、90 ℃下的半衰期分别提高了1.5倍、1.56倍和1.43倍,表明L265位点的突变显著提高了酶的热稳定性。此外,通过测定酶的反应动力学参数,发现突变酶的Km值有所增加,表明其对底物的亲和力有所下降。然而,突变酶的kcat(每分钟催化反应的次数)和kcat/Km(催化效率)均有所提升,相较于原始酶,催化效率提高了9%(表2)。
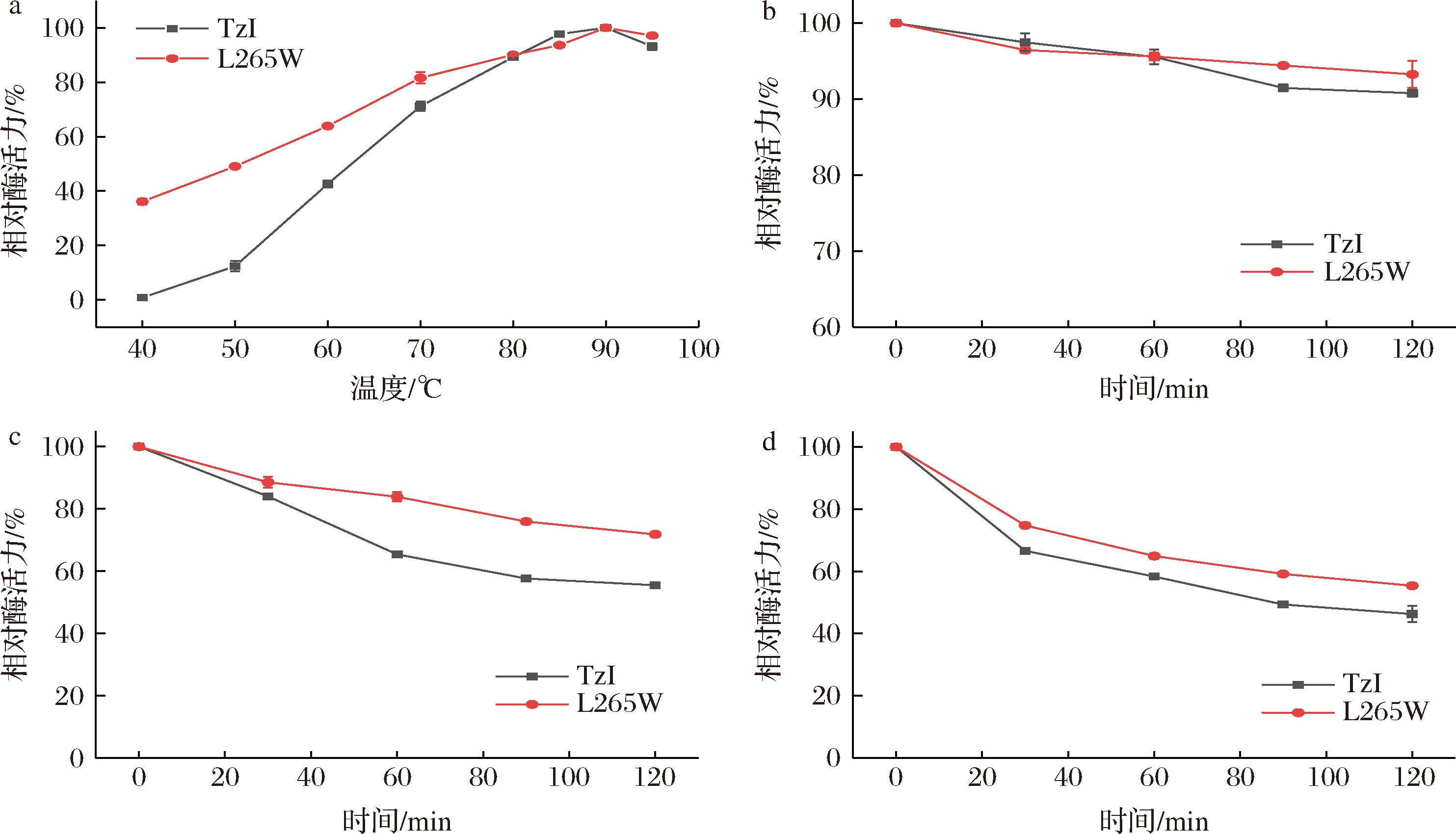
a-原始酶与突变酶的最适反应温度;b-原始酶与突变酶在80 ℃热稳定性;c-原始酶与突变酶在85 ℃热稳定性; d-原始酶与突变酶在90 ℃热稳定性
图5 原始酶与突变酶的热稳定性
Fig.5 Thermal stability of the original enzyme and the mutant enzyme
表2 TzI与L265W的半衰期与动力学参数
Table 2 Half-life and kinetic parameters of TzI and L265W

酶t1/2(80 ℃)/mint1/2(85 ℃)/mint1/2(90 ℃)/minKm/(mmol/L)kcat/(s-1)kcat/Km/[L/(mmol·s)]TzI770.16165.04103.451.28885.53691.82L265W1 155.25256.72147.481.571 187.74756.52
2.4 突变体构象分析
为了探究突变点对酶的构象影响,利用pymoL 2.6.0软件测定第265位氨基酸突变点与活性残基Lys156的空间距离,发现突变前后的空间距离不变,均为10.5 Å,属于远端突变(图6-a和图6-b)。距离活性残基超过10 Å的远端突变可能会显著影响酶的活性。为了研究远端突变的酶调节机制,WANG等[24]构建了一个远端突变数据库,即D3DistalMutation,该数据库将远端突变与酶活性相关联,大约80%的远端突变会影响酶的活性,6%的远端突变可以增加酶的活性。因此推测第265位氨基酸突变点与酶的活性密切相关。
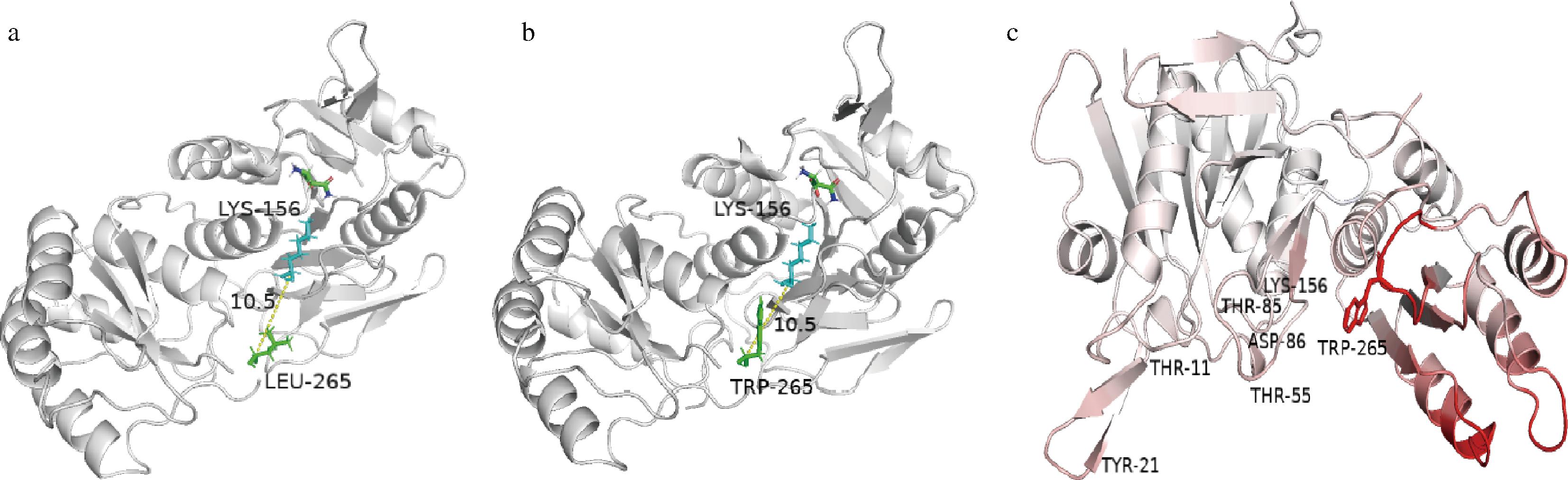
a-原始酶Leu265位点(蓝色棍棒结构)与活性残基Lys156(绿色棍棒结构)的空间距离;b-突变酶Trp265位点(蓝色棍棒结构)与活性残基 Lys156(绿色棍棒结构)的空间距离;c-突变位点对酶的灵活性影响,红色部分为柔性增加区域
图6 原始酶与突变酶的构象分析
Fig.6 Conformational analysis of primitive and mutant enzymes
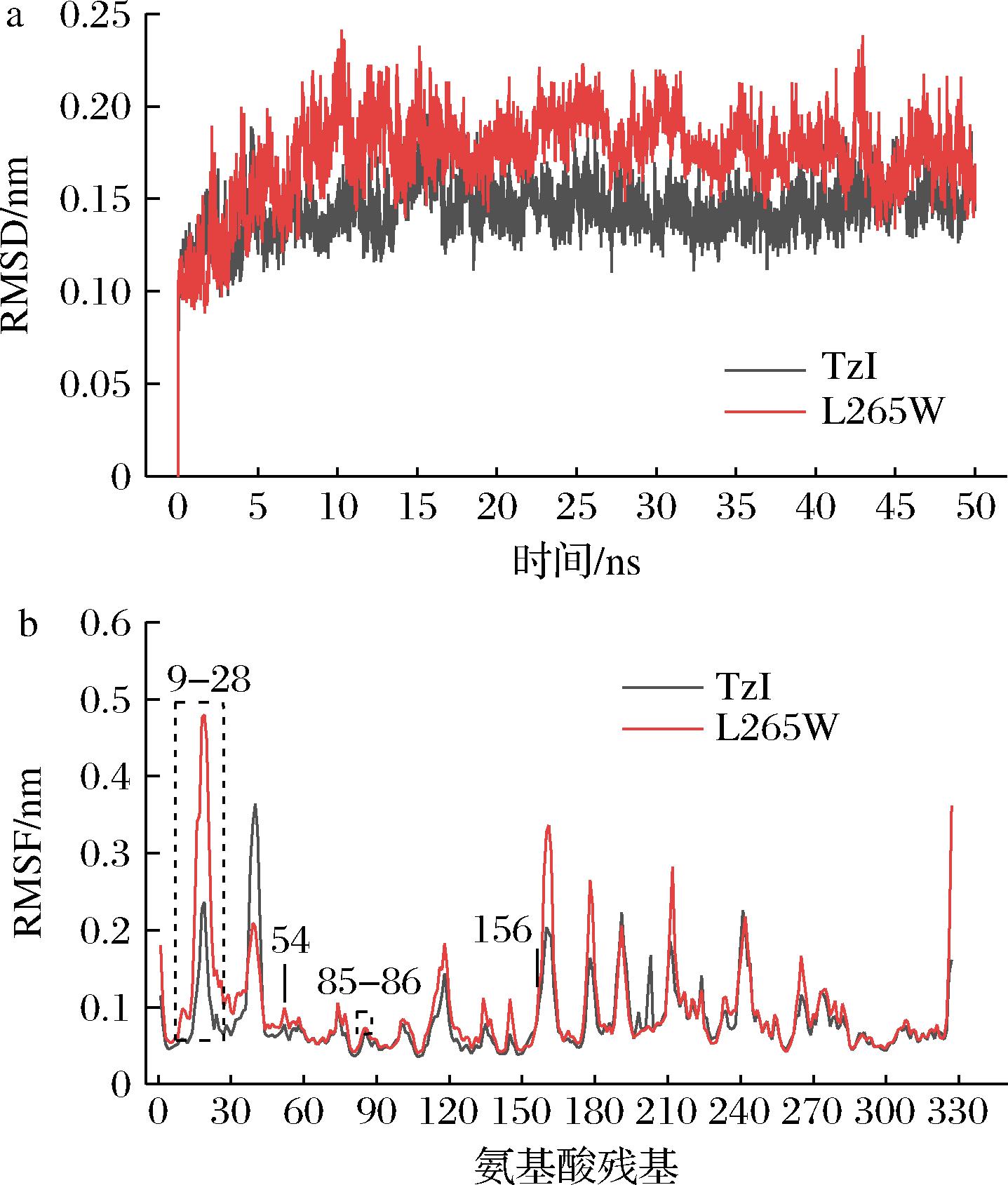
a-原始酶TzI和突变酶L265W的RMSD分析;b-原始酶TzI和 突变酶L265W的RMSF分析
图7 原始酶TzI和突变酶L265W的分子动力学模拟
Fig.7 Molecular dynamics simulation of original enzyme TzI and mutant enzyme L265W
利用web服务器 DynaMut评估L-ASNase第265位氨基酸由Leu突变为Trp后对蛋白质稳定性 (ΔΔG)和灵活性 (ΔΔS) 的影响。结果显示ΔΔG=0.010 kcal/mol,进一步验证突变酶稳定性提升的趋势。此外,ΔΔSVib ENCoM= 0.262 kcal/(mol·K),图6-c显示265突变位点的柔性显著增加,且催化活性位点处的柔性也有提升,说明远端突变降低了活性位点附近的空间位阻,更有利于底物进出口袋,从而提升酶的催化效率。
2.5 分子动力学模拟
为了探讨关键氨基酸突变提高TzI催化活性机制,突变酶L265W同样以Thermococcus kodakarensis ASN (ThA) 的晶体结构 (PDB ID:5OT0,2.18 Å) 为模板进行同源建模和分子对接,然后利用Gromacs-2020软件对原始酶TzI和突变酶L265W在300 K的温度下进行分子动力学模拟50 ns,原始酶和突变酶的RMSD分析结果如图7-a所示。观察两个酶的运动轨迹,原始酶TzI在17 ns趋于稳定,且在0.025 nm左右波动,突变酶在32 ns趋于稳定,且在0.05 nm左右波动,突变酶的振动幅度大于原始酶,说明突变后酶的整体构象更松散、更有利于催化。
原始酶和突变酶的RMSF分析的结果如图7-b所示,突变酶L265W的活性位点loop区(9~28位氨基酸)整体氨基酸波动变化高于原始酶TzI,其中活性中心残基T11和Y21 位于该区域内。此外,其他活性中心残基S54、T85、D86和K156和突变点265位氨基酸的RMSF也均高于野生型,进一步说明远端突变导致原始酶TzI的活性位点loop区的柔性增强,更利于底物与酶进行结合,从而提升酶的催化效率。
2.6 L-ASNase对油炸薯条中丙烯酰胺的影响
分别使用10 U/mL的商品酶、原始酶TzI和突变酶L265W及等体积的超纯水对薯条进行热烫处理,随后分别对薯条进行初炸和复炸,最后从油炸薯条中提取丙烯酰胺。利用液相色谱-串联质谱法 (LC-MS/MS) 检测薯条中的丙烯酰胺的含量,未进行热烫处理的薯条作为空白对照。在丙烯酰胺的液相定量测定中,以丙烯酰胺的标准样品测定出峰时间为2.08 min。并得出丙烯酰胺含量与峰面积的线性关系:y=7 777.2x+42 756;R2=0.999。峰面积和丙烯酰胺含量之间有良好的线性关系。
由于丙烯酰胺根据美拉德反应生成,可以根据美拉德反应的颜色深浅判断薯条中丙烯酰胺含量[25]。复炸5 min后对薯条未做任何处理的样品颜色偏深,经过突变酶处理的样品颜色较浅(图8-a),进一步说明薯条中的丙烯酰胺含量明显降低。
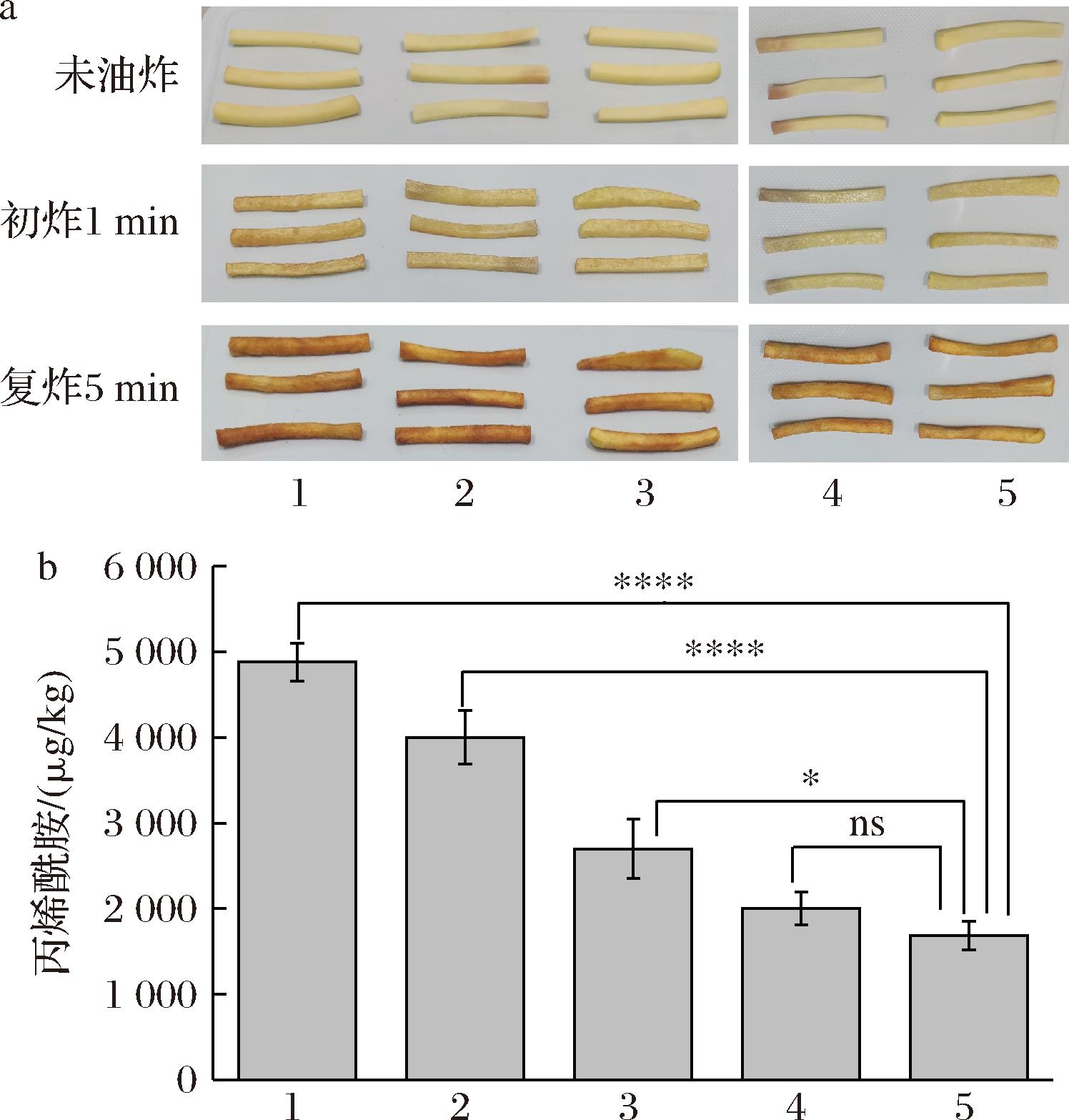
a-丙烯酰胺色谱图;b-丙烯酰胺标准曲线;c-不同L-ASNase 对薯条的预处理;d-L-ASNase对薯条中丙烯酰胺的影响
图8 L-ASNase对食品中丙烯酰胺影响
Fig.8 Effect of L-asparaginase on acrylamide in food
注:其中1、2、3、4、5分别指对薯条未做任何处理、对薯条热烫处理、对薯条同时进行热烫和诺维信商品酶处理、对薯条同时进行热烫和原始酶处理、对薯条同时进行热烫和突变酶处理,对样本之间的差异采用Excel中的Student’s t-test进行评估,其中ns表示差异不显著,*表示P<0.05,**表示P<0.01,***表示P<0.001,****分别表 示P<0.000 1。
与未处理的薯条相比,热烫处理后的薯条丙烯酰胺下降18%,商品酶处理后下降44%,TzI处理后下降59%,突变酶处理后下降65%,突变酶与未做任何处理的薯条、热烫处理的薯条和商品酶处理的薯条相比,其丙烯酰胺含量有显著降低,与原始酶处理效果相比有所提升但提升效果不显著(图8-b)。
3 结论与讨论
为了进一步提高I型L-ASNase对L-天冬酰胺的催化效率,本研究选择T. zilligii来源的L-ASNase并通过分子对接和虚拟氨基酸饱和突变技术进行分子改造,根据与底物结合自由能变化选择<-3 kcal/mol的前10个氨基酸突变位点并对它们进行了实验表征。结果显示,突变酶L265W的比酶活力较TzI提高了29%,催化效率提升了9%。进一步的构象分析和分子动力学模拟共同表明,突变L265W酶催化效率的提升可能是由于远端突变导致了酶的柔性增加,从而降低了活性位点附近的空间位阻,使得底物的进入和出口更为顺畅。在相同的酶量处理下,经L265W突变酶处理的油炸薯条中丙烯酰胺含量下降了65%,其效果相较于TzI有所提升。这一研究成果不仅提高了酶的催化效率,还显著降低了油炸食品中丙烯酰胺的含量,为其他酶的分子改造提供借鉴,也为食品安全提供了新的解决方案。
[1] BATOOL T, MAKKY E A, JALAL M, et al.A comprehensive review on L-asparaginase and its applications[J].Applied Biochemistry and Biotechnology, 2016, 178(5):900-923.
[2] SHAKAMBARI G, ASHOKKUMAR B, VARALAKSHMI P.L-asparaginase:A promising biocatalyst for industrial and clinical applications[J].Biocatalysis and Agricultural Biotechnology, 2019, 17:213-224.
[3] WANG Y M, WU H, ZHANG W L, et al.Efficient control of acrylamide in french fries by an extraordinarily active and thermo-stable L-asparaginase:A lab-scale study[J].Food Chemistry, 2021, 360:130046.
[4] CASTRO D, MARQUES A S C, ALMEIDA M R, et al.L-asparaginase production review:Bioprocess design and biochemical characteristics[J].Applied Microbiology and Biotechnology, 2021, 105(11):4515-4534.
[5] KAUR N, HALFORD N G.Reducing the risk of acrylamide and other processing contaminant formation in wheat products[J].Foods, 2023, 12(17):3264.
[6] LI R, ZHANG Z H, PEI X M, et al.Covalent immobilization of L-asparaginase and optimization of its enzyme reactor for reducing acrylamide formation in a heated food model system[J].Frontiers in Bioengineering and Biotechnology, 2020, 8:584758.
[7] DA CUNHA M C, DOS SANTOS AGUILAR J G, DE MELO R R, et al.Fungal L-asparaginase:Strategies for production and food applications[J].Food Research International, 2019, 126:108658.
[8] ABEDI E, MOHAMMAD BAGHER HASHEMI S, GHIASI F.Effective mitigation in the amount of acrylamide through enzymatic approaches[J].Food Research International, 2023, 172:113177.
[9] JIA R Y, WAN X, GENG X, et al.Microbial L-asparaginase for application in acrylamide mitigation from food:Current research status and future perspectives[J].Microorganisms, 2021, 9(8):1659
[10] ZUO S H, ZHANG T, JIANG B, et al.Reduction of acrylamide level through blanching with treatment by an extremely thermostable L-asparaginase during french fries processing[J].Extremophiles, 2015, 19(4):841-851.
[11] SELLÉS VIDAL L, ISALAN M, HEAP J T, et al.A primer to directed evolution:Current methodologies and future directions[J].RSC Chemical Biology, 2023, 4(4):271-291.
[12] BILAL M, ZHAO Y P, NOREEN S, et al.Modifying bio-catalytic properties of enzymes for efficient biocatalysis:A review from immobilization strategies viewpoint[J].Biocatalysis and Biotransformation, 2019, 37(3):159-182.
[13] XING H G, ZOU G, LIU C Y, et al.Improving the thermostability of a GH11 xylanase by directed evolution and rational design guided by B-factor analysis[J].Enzyme and Microbial Technology, 2021, 143:109720.
[14] ZHOU Y W, JIAO L S, SHEN J, et al.Enhancing the catalytic activity of type II L-asparaginase from Bacillus licheniformis through semi-rational design[J].International Journal of Molecular Sciences, 2022, 23(17):9663.
[15] PANG C P, LIU S, ZHANG G Q, et al.Improving the catalytic efficiency of Pseudomonas aeruginosa lipoxygenase by semi-rational design[J].Enzyme and Microbial Technology, 2023, 162:110120.
[16] ROBERT X, GOUET P.Deciphering key features in protein structures with the new ENDscript server[J].Nucleic Acids Research, 2014, 42(Web Server issue):W320-W324.
[17] RODRIGUES C H, PIRES D E, ASCHER D B.Dynamut:Predicting the impact of mutations on protein conformation, flexibility and stability[J].Nucleic Acids Research, 2018, 46(W1):W350-W355.
[18] ABRAHAM M J, MURTOLA T, SCHULZ R, et al.GROMACS:High performance molecular simulations through multi-level parallelism from laptops to supercomputers[J].SoftwareX, 2015, 1:19-25.
[19] GUO J X, COKER A R, WOOD S P, et al.Structure and function of the thermostable L-asparaginase from Thermococcus kodakarensis[J].Acta Crystallographica.Section D, Structural Biology, 2017, 73(Pt 11):889-895.
[20] LI X, ZHANG X, XU S Q, et al.Insight into the thermostability of thermophilic L-asparaginase and non-thermophilic L-asparaginase II through bioinformatics and structural analysis[J].Applied Microbiology and Biotechnology, 2019, 103(17):7055-7070.
[21] ANISHKIN A, VANEGAS J M, ROGERS D M, et al.Catalytic role of the substrate defines specificity of therapeutic L-asparaginase[J].Journal of Molecular Biology, 2015, 427(17):2867-2885.
[22] YAO M, YASUTAKE Y, MORITA H, et al.Structure of the type I L-asparaginase from the hyperthermophilic archaeon Pyrococcus horikoshii at 2.16 Å resolution[J].Acta Crystallographica.Section D, Biological Crystallography, 2005, 61(3):294-301.
[23] GRIBENKO A V, PATEL M M, LIU J J, et al.Rational stabilization of enzymes by computational redesign of surface charge-charge interactions[J].Proceedings of the National Academy of Sciences of the United States of America, 2009, 106(8):2601-2606.
[24] WANG X Y, ZHANG X B, PENG C, et al.D3DistalMutation:A database to explore the effect of distal mutations on enzyme activity[J].Journal of Chemical Information and Modeling, 2021, 61(5):2499-2508.
[25] BIGNARDI C, CAVAZZA A, GRIMALDI M, et al.Acrylamide determination in baked potatoes by HPLC-MS:Effect of steam and correlation with colour indices[J].European Food Research and Technology, 2019, 245(11):2393-2400.