水果和蔬菜的衰老和腐烂是一个复杂的生理过程,受到许多内源性因素和外源性影响[1],与丝裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)信号通路密切相关[2]。MAPK信号通路是植物中广泛存在的重要信号转导通路,通过一系列蛋白激酶级联将外部刺激信号转导到细胞中,从而调节基因表达和细胞生理过程[3]。它不仅广泛调节植物生长发育等多种过程,而且与植物免疫防御保持密切联系[4]。
当植物受到病原体、胁迫或其他外部刺激时,活化的MAPK磷酸化下游成分(如转录因子、蛋白激酶和其他调节蛋白),从而激活抗病相关基因的表达或影响植物的防御反应[5]。例如,拟南芥中的MPK3和MPK6能够通过磷酸化下游蛋白激酶来响应植物免疫和非生物胁迫[6]。当MAPK级联通路受到抑制时,玉米对禾谷镰刀菌的敏感性显著增加,许多毒素生物合成相关基因的表达减少,ZmWRKY79的表达也受到抑制[7]。随着研究的进展,植物MAPK级联通路与其他信号通路之间的相互作用及其对下游转录因子或基因的调控已逐渐成为全面了解植物MAPK串联通路机制作用的关键[8]。MAPK级联途径下游转录因子的鉴定在研究MAPK级联通路下游的调控网络中具有特别重要的意义。
目前,已经发现几个转录因子家族,包括WRKY、bZIP、ERF和ICE,与MAPK级联通路密切相关[9-12]。其中,WRKY家族是植物中最大的转录因子家族之一[13],大量报道表明其参与MAPK途径,在植物抵抗病原微生物中发挥着重要作用。在棉花中,GhWRKY41可以激活GhC4H和Gh4CL的表达,促进木质素和黄酮类化合物的积累,从而增强对大丽黄萎菌的抗性[14]。在玉米中,转录因子ZmWRKY83在赋予对禾谷镰刀菌感染的抗性方面发挥着至关重要的作用[15]。
在本实验室的初步研究中,发现胰蛋白酶可以作为一种有效的生物保鲜剂,减少氧化损伤,增强果实对非生物胁迫的抵抗力[16-17]。胰蛋白酶具有清除超氧阴离子的能力,可以调节火龙果皮中内源性活性氧的水平,抑制饱和脂肪酸的水平。它还诱导了参与苯丙烷途径的化合物的生物合成,如木质素、绿原酸[18]和类黄酮[19-20]。此外,它还可以影响黄酮类化合物清除DPPH自由基和ABTS阳离子自由基的活性[21-22],从而增强果实的抗性。大量研究表明,MAPK通路是苯丙素通路的上游信号通路,但胰蛋白酶通过MAPK通路调节苯丙素化合物合成从而影响果实抗性的确切机制仍有待阐明。
黄瓜营养丰富,含水量高但采后容易发生品质劣变和腐败[23]。本实验以黄瓜作为实验材料,通过对转录组数据分析,筛选出受胰蛋白酶调控的MAPK级联途径的表达差异基因,并通过GSEA和生物信息学分析筛选出了WRKY转录因子。其次利用广泛靶向代谢组学分析,筛选出差异代谢物。最后利用表达相关性分析和基因沉默(virus-induced gene silencing, VIGS)技术,初步证明CsWRKY33是胰蛋白酶调控MAPK途径诱导苯丙烷化合物合成的关键转录因子,提高了果实的抗性,为MAPK途径在胰蛋白酶保鲜中的调控机制提供新的理论依据。
1 材料与方法
1.1 材料与试剂
采用周边市场购买的同一批次的新鲜黄瓜(品种为中农27号),选择大小、形状相似、颜色相近、无机械损伤和虫害污染的黄瓜进行试验。
胰蛋白酶(牛源,5×105 U/g),美国Amersco公司。
1.2 实验方法
1.2.1 样品处理
用胰蛋白酶溶液(2.41×10-6 mol/L)浸泡黄瓜60 s,对照组用蒸馏水同样处理。25 ℃放置,每隔24 h,观察、拍照、记录、测失水率[24]。贮藏1周后,用手术刀切下处理过的黄瓜表皮,混匀,迅速放入液氮3~5 min,储存在-80 ℃下,为后续组学送样做准备。
1.2.2 转录组测序
真核mRNA测序是基于Illumina Novaseq 6000测序平台,对真核生物特定组织或细胞在某个时期转录出来的所有mRNA进行测序,测序实验采用Illumina TruseqTM RNA sample prep Kit方法进行文库构建,从组织样品中提取总RNA,利用Nanodrop 2000对所提RNA的浓度和纯度进行检测,琼脂糖凝胶电泳检测RNA完整性,Agilent 2100测定RIN值。Illumina Hiseq上机测序:a)文库富集,PCR扩增15个循环;b)2%琼脂糖胶回收目的条带(certified low range ultra agarose);c)TBS380(Picogreen)定量,按数据比例混合上机;d)cBot上进行桥式PCR扩增,生成clusters;e)Illumina Hiseq测序(PE文库,读长2×150 bp)。
1.2.3 胰蛋白酶调控基因与代谢物的网络分析
从I-Sanger云平台筛选出受胰蛋白酶调控的MAPK相关差异表达显著基因和差异代谢物,计算基因和代谢物间的相关性并导入Cytoscape软件进行网络可视化分析。网络图展示出基因与代谢物间的相互作用关系,并利用Cytoscape的插件cytoHubba计算互作网络中的关键节点。
1.2.4 CsWRKY33基因序列分析
从RNA-Seq数据中获得CsWRKY33的序列。通过基因特异性引物对克隆CsWRKY33序列的开放阅读框(open reading frame, ORF),并使用NCBI数据库(http://www.ncbi.nlm.nih.gov/)寻找相似序列,采用ClustalW进行多重序列比对,用MEGA6.0软件通过Neighbor_joining法构建系统发育树。此外,在http://web.expasy.org/Compute_pi/上预测CsWRKY33的理论等电点和相对分子质量。
1.2.5 VIGS载体构建
Trizol法提取黄瓜果皮总RNA,用HiFi-MMLV cDNA Kit合成cDNA,利用CsWRKY33特异性引物进行扩增。经EcoR I和BamH I限制性内切酶消化并回收的PCR产物和pTRV2载体使用T4 DNA连接酶连接,将连接产物转化大肠杆菌Top10,提取成功连接的WRKY33-pTRV2质粒,将其转化进农杆菌GV3101用于后续侵染[25]。
1.2.6 RT-qPCR验证
通过2-△△Ct用于计算差异基因表达水平的方法,实验重复了3次,引物如表1所示。
表1 实验所用引物序列表
Table 1 All primer sequences used in the experiment

基因基因ID引物序列CsWRKY33CsaV3_4G006110F:CCGGAATTCAAAGGGTGCAATGGAATACCAAR:CGCGGATCCAAGATGAGAAATGGAGGCTubulin beta chainCsaV3_1G037170F:GAGCCAAGTTCTGGGAGGTCATR:ACGAAGTTATCGGGACGGAAGACsWRKY27CsaV3_3G033000F:AATCCGAGGAATCTGGAGACAGTTGR:GCTTGGCAGGTCTGGTCGTATTCsWRKY10CsaV3_2G017720F:ATGATGGCTACAAGTGGAGGAAGTR:AGGCAGAGGTAAAGGATGGCAAT
续表1
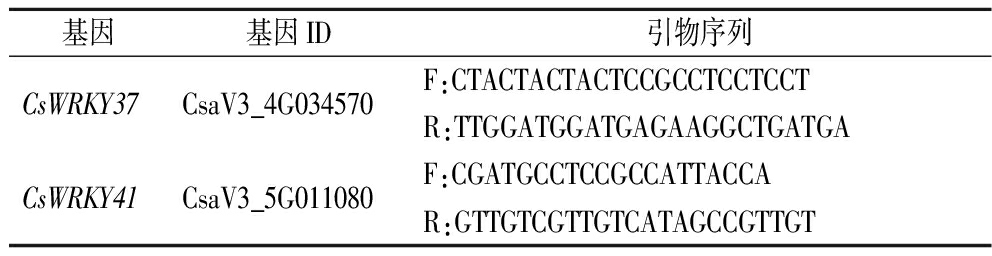
基因基因ID引物序列CsWRKY37CsaV3_4G034570F:CTACTACTACTCCGCCTCCTCCTR:TTGGATGGATGAGAAGGCTGATGACsWRKY41CsaV3_5G011080F:CGATGCCTCCGCCATTACCAR:GTTGTCGTTGTCATAGCCGTTGT
1.3 数据统计
统计分析采用SPSS统计软件进行。非参数检验(威尔科克森检验)用于分析整组样本之间的差异。使用配对样本T检验确定一个时间点样本间差异的显著性。显著或极显著差异分别用P<0.05或P<0.01评价。
2 结果与分析
2.1 转录组学概况
基于受胰蛋白酶诱导的基因表达谱,完成了表达量差异分析。首先,样本相关性分析结果表明了生物学重复样本之间具有很强的相关性(图1-a),主成分分析(principal component analysis, PCA)可以看出样品被分为两个独立组别(图1-b),并且两组之间差异显著(PC1=55.58%),而组内被相同颜色标记的样品彼此紧密靠近(PC2=12.63%)。从表达量差异分析中筛选出9 061个差异表达显著基因,其中上调基因有4 416个,下调基因有4 645个(图1-c)。将这些筛选出来的差异表达基因进行转录因子家族统计(图1-d),鉴定出排名前5的转录因子家族中,56个转录因子属于ERF家族,52个转录因子属于MYB家族,43个转录因子与MYB家族相关,39个转录因子属于bHLH家族,38个转录因子属于WRKY家族。随后又对筛选出来的9 061个差异表达显著基因进行KEGG功能富集分析,发现其分布在131条代谢通路上,其中有83个基因富集在MAPK信号途径中,将83个基因建立基因集并进一步分析。
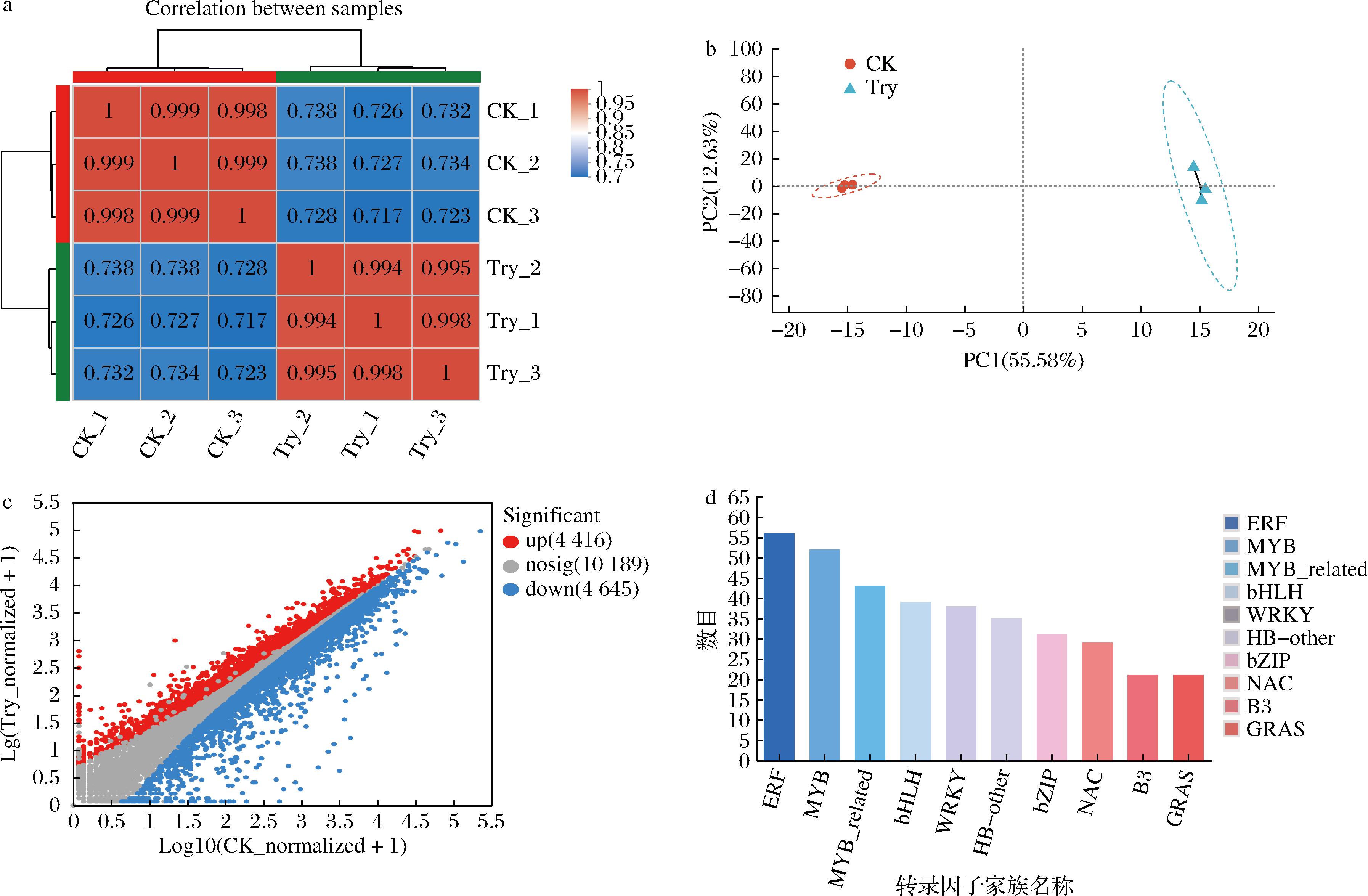
a-样本间相关性;b-样本间PCA;c-表达量差异散点;d-转录因子家族统计
图1 胰蛋白酶调节差异表达基因的转录组学分析
Fig.1 Transcriptomic analysis of differentially expressed genes regulated by trypsin
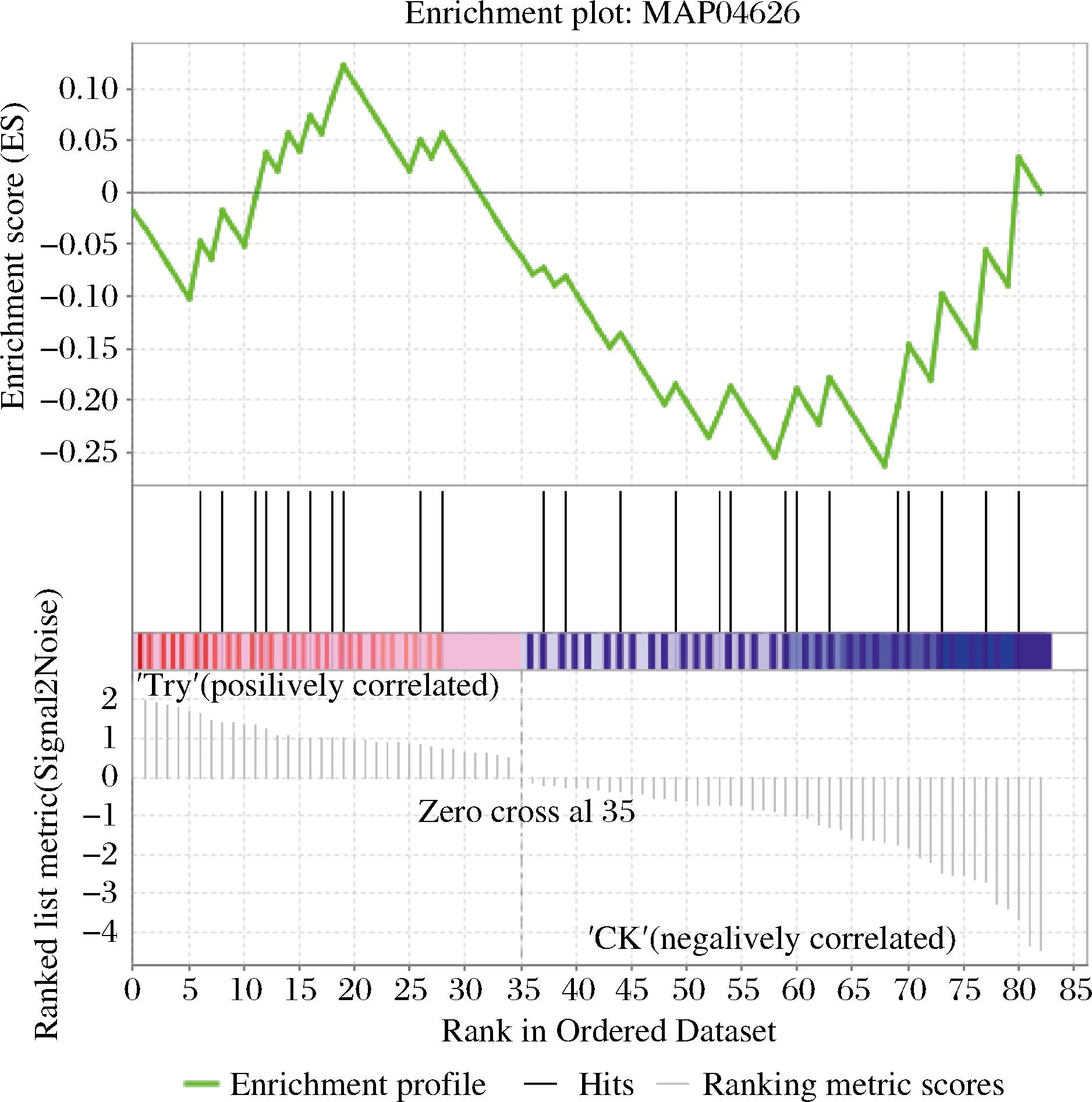
图2 植物-病原体互作通路GSEA富集图
Fig.2 GSEA of plant-pathogen interaction
注:上部曲线表示累计ES值的变化趋势,最高点即为基因集的ES 值;中部竖线表示先验基因集在排序后基因列表中的位置,用黑色 线条标记了先验基因集中每个基因出现在排序基因列表中的位置; 下部分热图+灰色面积图表示排序基因列表中基因的分布。
2.2 MAPK途径相关基因的GSEA
通过对富集在MAPK信号途径上的83个基因进行GSEA,结果显示除了注释在本身的MAPK途径(MAP04046)外,还分别注释到了植物-病原体互作(MAP04626)和植物激素信号转导(MAP04075)两条通路(表2)。共有9个基因富集在MAP04075通路的领头亚集中,其中被筛选到的MYC转录因子已被本实验室报道[25]。此外,从MAP04626通路中筛选出的领头亚集中共有8个基因,在这8个基因中,发现CsaV3_4G006110属于转录因子WRKY家族,在CHEN等[26]研究中将其名命为WRKY33。作为参与MAPK途径的重要转录因子,CsWRKY33可能影响了相关物质的合成代谢,从而提高了果实的抗病能力。
表2 83个MAPK途径富集基因的GSEA
Table 2 GSEA statistics of 83 MAPK pathway enriched genes
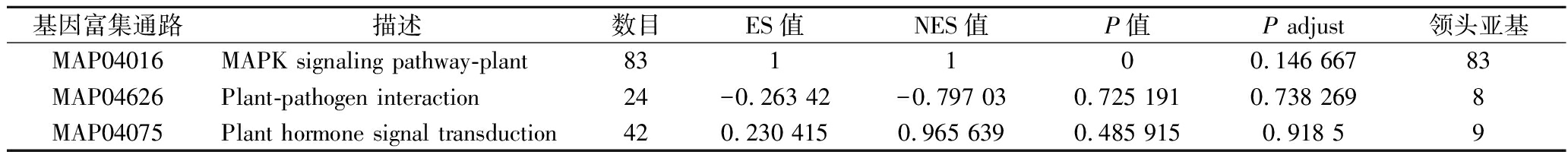
基因富集通路描述数目ES值NES值P值P adjust领头亚基MAP04016MAPK signaling pathway-plant831100.146 66783MAP04626Plant-pathogen interaction24-0.263 42-0.797 030.725 1910.738 2698MAP04075Plant hormone signal transduction420.230 4150.965 6390.485 9150.918 59
2.3 WRKY33与代谢物的共表达网络分析
经过代谢组学分析后,筛选出了175种显著差异代谢物,接下来将转录组数据中筛选出的83个基因与175种代谢物进行表达相关性分析,并构建共表达网络分析图(图3-a)。通过Cytoscape构建的共表达网络图由226个节点和811条边组成(图3-a)。将CsWRKY33和8种代谢物基于cytoHubba进行“EPC”排序(图3-b),从基因与代谢物之间的关系,可以看出CsWRKY33与大多数代谢物呈现负相关状态,其中负相关最显著的是2-羟基-3-苯基丙酸和香兰素,除此之外还有二氢查尔酮-4′-O-葡萄糖苷等物质,而这些物质在抗氧化和抗菌方面都发挥着积极地影响。
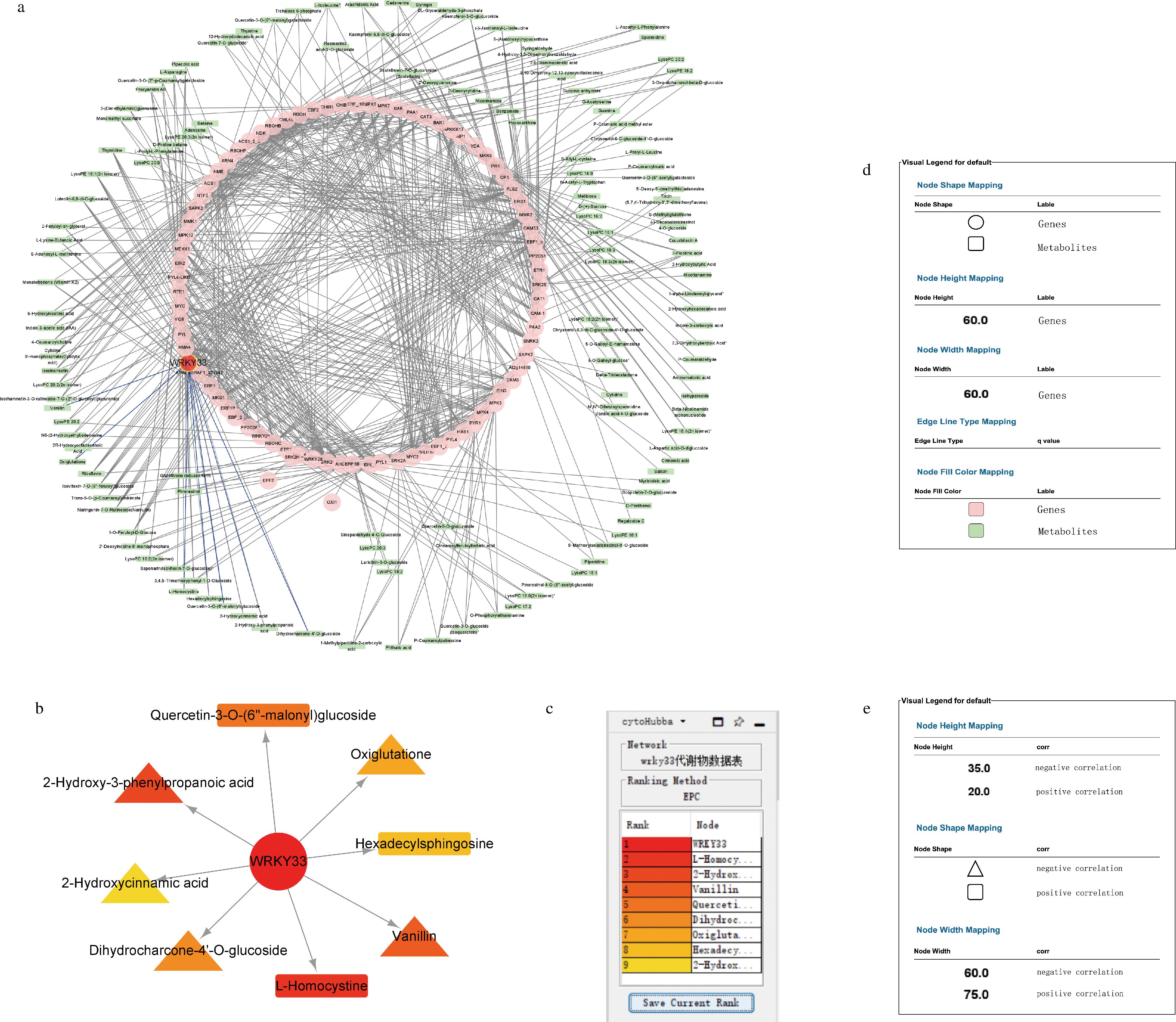
a-共表达总网络图(粉色代表基因,绿色代表代谢物,目标基因WRKY33为红色突出显示,紫色的线为WRKY33相关的8种代谢物); b-Top10蛋白网络互作图;c-Top10的排序信息;d, e-图注
图3 表达相关性网络分析
Fig.3 Expression correlation network analysis
在负相关排序靠前的物质中,2-羟基-3-苯基丙酸,即苯基乳酸(phenyllactic acid, PLA)是一种广谱的抗菌物质,对大多数革兰氏阳性菌、阴性菌和真菌都有很好的抑制效果[27]。香兰素具有广谱抗真菌作用,可通过增加细胞膜通透性和脂质过氧化,可显著抑制病原真菌的生长速率、菌丝体生物量和孢子萌发。香兰素可诱导苹果果实中苯丙氨酸解氨酶(phenylalamine ammonia lyase, PAL)、几丁质酶(chitin synthetase, CHI)和β-1,3-葡聚糖酶(β-1,3-GA)等防御相关酶活性升高,并增加总酚和类黄酮含量。而二氢查尔酮-4′-O-葡萄糖苷属于黄酮类化合物,研究表明,黄酮类化合物有提高动物机体抗氧化及清除自由基的能力[28]。在与CsWRKY33表达正相关的代谢物中,槲皮素-3-O-(6′-丙二酰基)葡萄糖苷的减少,能够减弱由多酚氧化酶及其底物酚类物质的存在引起酶促褐变现象[29],对果实的外观的表现起到一定作用。
2.4 CsWRKY33基因的生物信息学分析
CsWRKY33基因与CmWRKY22有很高的相似性(95.22%)。CsWRKY33的开放阅读框(ORF)全长810 bp,编码269个氨基酸的多肽,计算出其分子质量为30.31 kDa,理论等电点为6.323。CsWRKY33在N端有一个高度保守的WRKYGQK氨基酸序列,它是一个WRKY结构域,是WRKY TF的一个决定性特征。CsWRKY33还包含一个假定的锌指基序(C-X4-5-C-X22-23-H-X1-H)(图4-a)。通过NCBI上Blast在线比对工具,将检索到的13条与CsWRKY33同源性较高的蛋白进行多序列比对,使用MEGA 6.0软件构建进化树,结果表明黄瓜CsWRKY33与甜瓜的WRKY22同源性最高(图4-b)。


a-CsWRKY33与其他植物WRKY的序列比对(相同和相似的氨基酸分别用蓝色和红色表示,WRKY基序和锌指结构分别由红色方框和 黑色星号表示);b-WRKY的系统发育树(CsWRKY33蛋白用红色方框表示)
图4 CsWRKY33的生物信息学分析
Fig.4 Bioinformatics analysis of CsWRKY33
2.5 WRKY33沉默序列的克隆和载体的构建
接下来以黄瓜cDNA为模板,用CsWRKY33特异性引物扩增249 bp的cDNA片段,PCR产物的琼脂糖凝胶电泳结果如图5-b所示。对扩增得到的片段进行切胶回收,并送至生工生物工程(上海)股份有限公司测序,比对结果显示其为CsWRKY33基因的特异性片段。将切胶回收产物以及pTRV2质粒进行EcoR I、BamH I双酶切和纯化回收,然后经T4 DNA连接酶连接(图5-a),连接后转化Top10,将菌液PCR和质粒酶切检测均正确的重组质粒命名为pTRV2-CsWRKY33,并转化农杆菌GV3101。

a-CsWRKY33沉默片段克隆电泳;b-重组表达载体PTRV2-CsWRKY33构建示意图
图5 VIGS载体构建示意图
Fig.5 Schematic diagram of VIGS carrier construction
2.6 VIGS植株的表型观察和数据测定
贮藏初期,所有组别的黄瓜果实品质良好,色泽鲜艳。贮藏16 d后,空白对照组果实颜色泛黄明显,头部和靠近中部皱缩严重,并出现腐烂现象。胰蛋白酶处理后,果实整体新鲜程度最高,果皮泛黄皱缩程度最轻,表面无腐烂现象(图6-a)。沉默组保鲜效果也明显优于对照组,除根部有少许泛黄外,整体颜色泛黄较轻,头部轻微皱缩。随着贮藏时间的延长,各组的失重率呈显著上升趋势,空白对照组的果实失重率最大(43.36%),胰蛋白酶处理组的黄瓜失重率最低(22.55%);而沉默组果实的失重率则为30.33%(图6-b),结果表明VIGS处理后减缓了黄瓜果实的失水速率。

a-黄瓜不同处理后的表型变化(CK代表空白处理组,Try代表胰蛋白酶处理组,CsWRKY33i代表VIGS组);b-黄瓜失重率; c-WRKY33在不同处理组黄瓜中基因的表达;d, e-转录组质量验证
图6 不同组别黄瓜贮藏外观及失水率的影响
Fig.6 Effects of different groups of cucumber on storage appearance and water loss rate
注:*表示差异显著(P<0.05),**表示差异极显著(P<0.01)(下同)。
在本研究当中,胰蛋白酶对黄瓜有良好的保鲜效果,而转录组学结果显示,Try降低了CsWRKY33的表达,但是CsWRKY33的低表达是否能增强果实抗性,从而延缓果实的衰老腐败还需要进一步验证。因此,利用VIGS技术将CsWRKY33沉默,实验结果表明,沉默组的黄瓜在整体表现上与胰蛋白酶组的黄瓜表现趋势相同。在储存16 d后,沉默组黄瓜的外观明显优于对照组,并且失重率也低于对照组,果实的保存时间得到延长。后通过荧光定量PCR验证发现(图6-c),与对照组相比,经胰蛋白酶处理后WRKY33表达被抑制,而沉默组WRKY33表达情况与其一致,进一步证明胰蛋白酶可能通过抑制WRKY33的表达,从而起到保鲜作用。
3 结论
MAPK级联途径不仅能够广泛的调控植物生长和发育等过程,在植物防御病原体攻击的信号中也发挥重要作用。大量研究表明,MAPK途径可以调控下游WRKY家族转录因子,并且还是植物免疫反应的关键参与者[30]。这与本研究结果相同,富集在MAPK途径的表达差异基因通过GSEA,从植物-病原体互作(MAP04626)通路中,筛选出了WRKY33转录因子。生物信息学分析以及多序列比对结果显示,CsWRKY33的功能与WRKY22/29功能相似。大量研究表明WRKY22/29是丝裂原活化蛋白激酶(MAPK)介导的信号转导途径的重要下游成分,WRKY22参与病原体触发的免疫过程并对细菌病原体的抗性进行调节[31],在植物病害相关方面发挥十分重要的作用。在甜橙中的研究表明,CsWRKY22的部分敲除可以提高对柑橘黄单胞菌的抗性,而过表达CsWRKY22的植物却表现出矮小表型,叶片起皱和增厚,对该致病菌更敏感。并且CsWRKY22的表达还能够激活调节柑橘溃疡病易感性的关键基因CsLOB1的表达,最终使CsWRKY22通过促进宿主肥大和CsLOB1表达来增强对柑橘溃疡病的易感性[32]。这与本研究结果一致,胰蛋白酶很有可能抑制黄瓜CsWRKY33的表达减弱了果实的感病性,并促进香兰素、二氢查尔酮-4′-O-葡萄糖苷、2-羟基-3-苯基丙酸等物质的合成,进一步提高果实抗性,延缓腐败。但是CsWRKY33的低表达是否能增强果实抗性,从而延缓果实的衰老腐败还需要进一步验证。因此,通过VIGS技术将CsWRKY33沉默,并结合果实表型变化、失重率和RT-qPCR进行验证。实验结果表明,储存16 d后,沉默组的黄瓜在整体表现上与胰蛋白酶组的黄瓜表现趋势相同,外观明显优于对照组,并且失重率也低于对照组,果实的保存时间得到延长。
综上所述,CsWRKY33是胰蛋白酶调控MAPK途径诱导苯丙烷化合物的合成当中的关键转录因子,参与了植物-病原体互作通路,在胰蛋白酶的作用下减弱了黄瓜的感病性,并促使抗菌类物质和抗氧化的黄酮类物质含量提高,从而提高果实的抵抗能力,实现了延缓黄瓜衰老腐败的作用,本研究为胰蛋白酶提高果蔬保鲜机理提供了新的理论支撑。
[1] WANG Y, JI D C, CHEN T, et al.Production, signaling, and scavenging mechanisms of reactive oxygen species in fruit-pathogen interactions[J].International Journal of Molecular Sciences, 2019, 20(12):2994.
[2] XIE C, YANG L, GAI Y P.MAPKKKs in plants:Multidimensional regulators of plant growth and stress responses[J].International Journal of Molecular Sciences, 2023, 24(4):4117.
[3] HE X W, WANG C Z, WANG H B, et al.The function of MAPK cascades in response to various stresses in horticultural plants[J].Frontiers in Plant Science, 2020, 11:952.
[4] SUN T J, ZHANG Y L.MAP kinase cascades in plant development and immune signaling[J].EMBO Reports, 2022, 23(2):e53817.
[5] MAJEED Y, ZHU X, ZHANG N, et al.Harnessing the role of mitogen-activated protein kinases against abiotic stresses in plants[J].Frontiers in Plant Science, 2023, 14:932923.
[6] ZHANG M M, ZHANG S Q.Mitogen-activated protein kinase cascades in plant signaling[J].Journal of Integrative Plant Biology, 2022, 64(2):301-341.
[7] LI L, ZHU X M, ZHANG Y R, et al.Research on the molecular interaction mechanism between plants and pathogenic fungi[J].International Journal of Molecular Sciences, 2022, 23(9):4658.
[8] WANG L J, GUO D Z, ZHAO G D, et al.Group IIc WRKY transcription factors regulate cotton resistance to Fusarium oxysporum by promoting GhMKK2-mediated flavonoid biosynthesis[J].New Phytologist, 2022, 236(1):249-265.
[9] GUSAIN S, JOSHI S, JOSHI R.Sensing, signalling, and regulatory mechanism of cold-stress tolerance in plants[J].Plant Physiology and Biochemistry, 2023, 197:107646
[10] VEGA-SENDINO M, OLBRICH T, TILLO D, et al.The ETS transcription factor ERF controls the exit from the naïve pluripotent state in a MAPK-dependent manner[J].Science Advances, 2021, 7(40):eabg8306.
[11] WANG L Y, GUI Y, YANG B Y, et al.Mitogen-activated protein kinases associated sites of tobacco repression of shoot growth regulates its localization in plant cells[J].International Journal of Molecular Sciences, 2022, 23(16):8941.
[12] YAO D M, ZOU C, SHU Y N, et al.Wrky transcription factors in Nicotiana tabacum modulate plant immunity against whitefly via interacting with mapk cascade pathways[J].Insects, 2020, 12(1):16.
[13] JAVED T, GAO S J.WRKY transcription factors in plant defense[J].Trends in Genetics, 2023, 39(10):787-801.
[14] XIAO S H, MING Y Q, HU Q, et al.GhWRKY41 forms a positive feedback regulation loop and increases cotton defence response against Verticillium dahliae by regulating phenylpropanoid metabolism[J].Plant Biotechnology Journal, 2023, 21(5):961-978.
[15] BAI H, SI H L, ZANG J P, et al.Comparative proteomic analysis of the defense response to Gibberella stalk rot in maize and reveals that ZmWRKY83 is involved in plant disease resistance[J].Frontiers in Plant Science, 2021, 12:694973.
[16] LI X, ZHANG Y Y, WU Y, et al.Lipid metabolism regulated by superoxide scavenger trypsin in Hylocereus undatus through multi-omics analyses[J].Journal of Food Biochemistry, 2022, 46(7):e14144.
[17] LI X, ZHANG Y Y, ZHAO S J, et al.Omics analyses indicate the routes of lignin related metabolites regulated by trypsin during storage of pitaya (Hylocereus undatus)[J].Genomics, 2021, 113(6):3681-3695.
[18] LI X, LIU X R, YIN Y, et al.Transcriptomic analysis reveals key genes related to antioxidant mechanisms of Hylocereus undatus quality improvement by trypsin during storage[J].Food &Function, 2019, 10(12):8116-8128.
[19] PANG X Y, ZHAO S J, ZHANG M, et al.Catechin gallate acts as a key metabolite induced by trypsin in Hylocereus undatus during storage indicated by omics[J].Plant Physiology and Biochemistry, 2021, 158:497-507.
[20] ZHANG Y Y, LI B R, ZHANG M, et al.Transcriptome analyses and virus-induced gene silencing identify HuWRKY40 acting as a hub transcription factor in the preservation of Hylocereus undatus by trypsin[J].Journal of Food Biochemistry, 2022, 46(12):e14437.
[21] PANG X Y, LI X L, LIU X R, et al.Transcriptomic analysis reveals Cu/Zn SODs acting as hub genes of SODs in Hylocereus undatus induced by trypsin during storage[J].Antioxidants, 2020, 9(2):162.
[22] LI X, LIU X R, PANG X Y, et al.Transcriptomic analysis reveals hub genes and subnetworks related to ROS metabolism in Hylocereus undatus through novel superoxide scavenger trypsin treatment during storage[J].BMC Genomics, 2020, 21(1):437.
[23] FENG S J, ZHANG J P, MU Z H, et al.Recent progress on the molecular breeding of Cucumis sativus L.in China[J].Theoretical and Applied Genetics, 2020, 133(5):1777-1790.
[24] ZHANG J Q, WU Z C, HU F C, et al.Aberrant seed development in Litchi chinensis is associated with the impaired expression of cell wall invertase genes[J].Horticulture Research, 2018, 5:39.
[25] WANG J, TIAN P P, SUN J J, et al.CsMYC2 is involved in the regulation of phenylpropanoid biosynthesis induced by trypsin in cucumber (Cucumis sativus) during storage[J].Plant Physiology and Biochemistry, 2023, 196:65-74.
[26] CHEN C H, CHEN X Q, HAN J, et al.Genome-wide analysis of the WRKY gene family in the cucumber genome and transcriptome-wide identification of WRKY transcription factors that respond to biotic and abiotic stresses[J].BMC Plant Biology, 2020, 20(1):443.
[27] ZHU Y B, XU Y, WANG L M, et al.Biosynthesis of (R)-2-hydroxy-3-phenylpropionic acid using whole recombinant Escherichia coli cells in an aqueous/n-octane biphasic system[J].Journal of Zhejiang University.Science.B, 2018, 19(4):285-292.
[28] WANG X Y, ZHANG X M, SUN M, et al.Impact of vanillin on postharvest disease control of apple[J].Frontiers in Microbiology, 2022, 13:979737.
[29] WANG J, JIA J Y, SUN J J, et al.Trypsin preservation:CsUGT91C1 regulates Trilobatin Biosynthesis in Cucumis sativus during Storage[J].Plant Growth Regulation, 2023, 100(3):633-646.
[30] LIN L, WU J, JIANG M Y, et al.Plant mitogen-activated protein kinase cascades in environmental stresses[J].International Journal of Molecular Sciences, 2021, 22(4):1543.
[31] RAMOS R N, MARTIN G B, POMBO M A, et al.WRKY22 and WRKY25 transcription factors are positive regulators of defense responses in Nicotiana benthamiana[J].Plant Molecular Biology, 2021, 105(1-2):65-82.
[32] LONG Q, DU M X, LONG J H, et al.Transcription factor WRKY22 regulates canker susceptibility in sweet orange (Citrus sinensis Osbeck) by enhancing cell enlargement and CsLOB1 expression[J].Horticulture Research, 2021, 8(1):50.