嘌呤(C5H4N4)是由嘧啶环和咪唑环融合形成的杂环芳香族化合物,既是组成核酸的重要成分,又是生物体中的关键碱基,无论是动物还是植物,体内普遍含有嘌呤[1]。啤酒以麦芽为主要原料,经酵母发酵而成,富含如维生素、矿物质、碳水化合物、氨基酸等多种营养物质,是世界上消费最广泛、最受欢迎的酒精饮料之一[2]。啤酒中含有的嘌呤类物质容易被人体吸收,且会快速代谢生成尿酸,使得血清中尿酸水平升高,这可能导致高尿酸血症和痛风[3]。因此,科学地降低啤酒中的嘌呤类物质,这是啤酒生产以及市场和消费者的共同需求,对我国啤酒的快速、健康发展具有重要的意义。目前国内外对于降低啤酒中嘌呤的研究主要包括以下几个方面:调整原辅料比例、酶法处理和吸附法处理等[4-5]。国内的高辅料啤酒中较具代表性的是江苏大富豪啤酒有限公司所开发的一款产品,为辅料比例达65%的发泡酒,且成品酒的嘌呤含量约为30 mg/L,低于普通啤酒[6]。但辅料比例过高会影响麦汁营养成分,如α-氨基氮等营养因子的含量降低,影响酵母的代谢。特定的酶能够特异性地作用于啤酒中的嘌呤类物质,通过催化反应将嘌呤分解,从而显著降低啤酒中的嘌呤含量。但酶的生产、提取和纯化过程相对复杂,需要较高的技术和设备投入,导致酶的价格相对昂贵,间接增加了啤酒生产成本。而吸附法所用到的吸附材料成本低,且具有操作简便、安全高效等优点,是降低啤酒嘌呤最经济有效的方法。王海容等[7]在研究7种吸附剂吸附啤酒嘌呤时,发现活性炭和壳聚糖的吸附能力优于其他吸附材料,活性炭在最优吸附条件下对啤酒中嘌呤类物质的吸附率为68.2%,壳聚糖在最优吸附条件下对啤酒中嘌呤类物质的吸附率为42.8%。雷崑等[8]研究发现,壳聚糖能有效吸附啤酒中的核酸衍生物。当壳聚糖质量浓度为0.01 g/10 mL时,能去除啤酒中50%以上的核酸衍生物中的嘌呤。
在诸多吸附剂中,天然矿物因储量丰富、吸附能力好、天然易得和远低于其他吸附剂的价格而被广泛关注。蒙脱石(montmorillonite, Mt)是一种层状结构的硅酸盐黏土矿物,具有阳离子交换性、分散与悬浮性、稳定与无毒性等优良性能[9]。同时,蒙脱石存在大的比表面积和丰富的微孔结构,从而表现出优异的吸附能力,因此被作为吸附剂而广泛应用于环境、化工和食品等行业中。目前,对于蒙脱石的研究主要集中在食品工业中油类和酒类的澄清,污水处理中污染物的吸附等方面[10-11],但目前关于蒙脱石对啤酒中嘌呤的吸附研究却鲜有报道。蒙脱石在自然环境中易发生同晶替代现象,这种现象导致蒙脱石层间产生永久性负电荷,而嘌呤在啤酒的弱酸性条件下会发生质子化并带正电,二者可通过静电作用[12]实现吸附结合。此外,蒙脱石在酸处理的条件下,可使酸中的H+与蒙脱石层间Ca2+、Mg2+等离子发生离子交换并转变为可溶性酸盐溶出,由于H+半径小于被置换离子,因此蒙脱石层间晶格裂开,层间距扩大,改性后蒙脱石的比表面积和吸附能力显著增加[13],该方法在提升蒙脱石吸附能力的同时,不会引入额外的有机分子,这一特性在食品领域的材料改性中的应用是非常合适的。ZHAO等[14]以钠蒙脱石为原料,在80 ℃下用硝酸处理8 h,制备了具有大孔径、高比表面积的酸化蒙脱石,结果表明:酸化蒙脱石对苯酚的饱和吸附率达到了70%,而钠蒙脱石的饱和吸附率仅仅为40%,酸化增强了蒙脱石对于苯酚的吸附能力。但酸浓度过高则会因黏土矿物部分溶解引起的结构损害而降低吸附能力[15-16]。
因此,本文主要探究蒙脱石在温和的酸处理下的结构变化,评估其对嘌呤类物质的吸附能力,并根据酸改性蒙脱石吸附啤酒前后的嘌呤降低率和感官评分,优化其在啤酒后储阶段的添加工艺。同时通过检测理化指标和风味物质成分,对比吸附前后啤酒品质的变化,为后续开发更廉价环保、高效的啤酒嘌呤吸附材料提供科学依据。
1 材料与方法
1.1 材料与试剂
大麦麦芽为麦特卡夫麦芽,江苏省农垦麦芽有限公司;卡斯卡特酒花、马格鲁门酒花,美国雅基玛联合酒花有限公司;啤酒酵母S189,威海德科生物科技有限公司;蒙脱石,古丈县山麟石语矿产品有限公司;NaCl,国药集团化学试剂有限公司;2-辛醇,美国Sigma公司;C7~C30正构烷烃混合物(99%),国药控股化学试剂北京有限公司。
1.2 仪器与设备
单四极杆GC-MS,美国赛默飞科技有限公司;pH计,上海梅特勒-托利多仪器有限公司;YQ-PJ-6B型自动糖化仪,轻工业部西安轻机所光电公司; D8 Advance型X射线衍射(X-ray diffraction, XRD)仪,德国布鲁克公司;IRTracer 100型傅里叶变换红外光谱(Fourier transform infrared,FTIR)仪,日本岛津仪器有限公司;ZEISS sigma 300型场发射扫描电镜(scanning electron microscope, SEM),德国卡尔蔡司股份公司;BELSORP MaxII型比表面积及孔径分析仪(brunauer-emmett-teller,BET),日本麦奇克拜尔有限公司。
1.3 实验方法
1.3.1 酸改性蒙脱石样品制备
参考文献[17-18]的方法并稍作修改。称取蒙脱石原土20 g(固液比1∶14,g∶mL),加入浓度为0.4 mol/L的稀硫酸,66 ℃水浴中反应195 min,用保鲜膜覆盖烧杯口,以防止溶液蒸发,反应结束后将烧杯移出水浴并降温至室温,离心8 min(转速3 000 r/min),洗涤至近中性,在105 ℃下干燥、磨细、备用。
1.3.2 酸改性蒙脱石样品表征
采用XRD测定样品的物相组成;采用FTIR分析样品的谱学性能;采用SEM分析样品的微观形态;采用BET测试材料孔结构。
1.3.3 酸改性蒙脱石吸附效果分析
取Mt和A-Mt粉末各0.1、0.2、0.3、0.4、0.5、0.6、0.8、1、2 g加入至50 mL 50 mg/L且pH值调整为4左右的嘌呤混标溶液(腺嘌呤、鸟嘌呤、黄嘌呤、次黄嘌呤质量比为1∶1∶1∶1)中,在20 ℃条件下,100 r/min搅拌60 min后过滤,取1 mL溶液透过0.45 μm针头式过滤器于1.5 mL进样瓶,经过HPLC测定并通过对比标准曲线计算嘌呤含量。嘌呤检测的HPLC条件如下:流动相A为水、冰乙酸和四丁基氢氧化铵溶液的混合液,体积分别为991.5、7、1.5 mL。(共计1 L溶液,pH=3),同时与流动相B(甲醇)按照比例95∶5等度洗脱。流速为1.0 mL/min,柱温30 ℃,紫外检测波长为254 nm,进样量为10 μL。
吸附实验中,吸附效果的好坏通常用吸附率和吸附量来反映。吸附率是利用改性吸附剂吸附前后嘌呤浓度的比值,用于评估溶液中吸附质的去除程度[19]。其计算如公式(1)所示:
(1)
式中:X,嘌呤吸附率,%;ρ1,未经处理溶液中嘌呤质量浓度,mg/L;ρ2,吸附后嘌呤的平衡质量浓度,mg/L。
吸附量是单位质量吸附剂所能吸附的量,用于表征吸附剂的吸附性能[20]。其计算如公式(2)所示:
(2)
式中:q,平衡吸附量,mg/g;ρ1,未经处理溶液中嘌呤质量浓度,mg/L;ρ2,吸附后嘌呤的平衡质量浓度,mg/L;V,吸附溶液体积,L;m,吸附剂的质量,g。
1.3.4 啤酒工艺及酸改性蒙脱石吸附工艺优化
原料配比为60%大麦芽,40%糖浆,准确称取60 g大麦麦芽粉,以1∶3.5料水比(g∶mL)注入糖化仪并进行糖化,过滤洗糟得麦汁,将麦汁煮沸60 min,投入0.8‰的酒花,过滤并控制定型麦汁浓度在10Brix。在冷却后的麦汁中接入浓度为1×107 CFU/mL的啤酒酵母S189,发酵温度12 ℃,待日失重<0.2 g时发酵结束,置于4 ℃冰箱后储7 d,在后储结束前,取啤酒加入一定量的蒙脱石样品,并过滤得到成品酒。对照组,HB:不添加任何蒙脱石进行吸附并过滤得到的酒;蒙脱石吸附组,HB(Mt):后储结束前加入蒙脱石吸附并过滤得到的酒;酸改性蒙脱石吸附组,HB(A-Mt):后储结束前加入酸改性蒙脱石吸附并过滤得到的酒。
由于本研究只需考虑吸附剂添加量和吸附时间对吸附效果的影响。在啤酒发酵的后储期,分别以添加量为0、2、4、10、15、20、40 g/L,处理时间为0、10、30、45、50、60、120 min时分析啤酒的嘌呤含量变化以及感官评分变化,选出最合适的添加量和添加时间。
1.3.5 啤酒理化分析
酒精度、pH值、浊度和总酸参照GB/T 4928—2008《啤酒分析方法》测定。感官分析实验选取12名经过专业培训的感官鉴定员做出感官评价,对啤酒色泽、气味、口味以及澄清度4个方面进行评价分析,综合评估啤酒的感官属性。具体评分细则见表1。
表1 啤酒感官评分表
Table 1 Beer sensory rating table
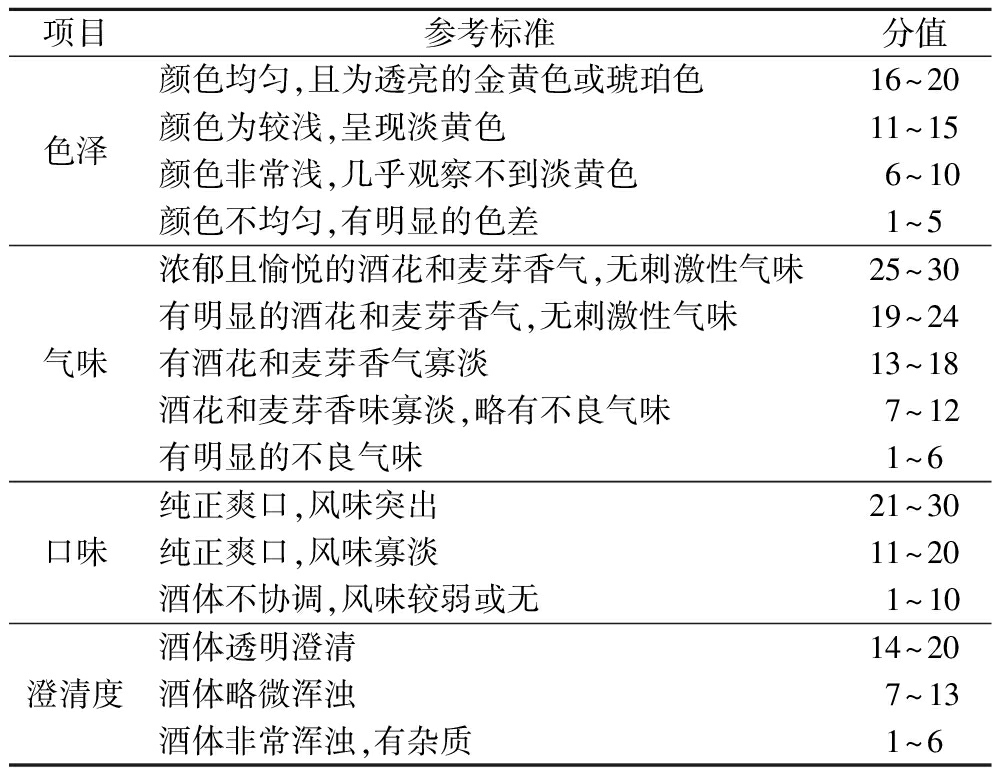
项目参考标准分值色泽颜色均匀,且为透亮的金黄色或琥珀色16~20颜色为较浅,呈现淡黄色11~15颜色非常浅,几乎观察不到淡黄色6~10颜色不均匀,有明显的色差1~5气味浓郁且愉悦的酒花和麦芽香气,无刺激性气味25~30有明显的酒花和麦芽香气,无刺激性气味19~24有酒花和麦芽香气寡淡13~18酒花和麦芽香味寡淡,略有不良气味7~12有明显的不良气味1~6口味纯正爽口,风味突出21~30纯正爽口,风味寡淡11~20酒体不协调,风味较弱或无1~10澄清度酒体透明澄清14~20酒体略微浑浊7~13酒体非常浑浊,有杂质1~6
1.3.6 啤酒风味分析
采用GC-MS进行分析[21]。量取8 mL啤酒样品和2.0 g NaCl固体放入20 mL顶空瓶中,加入200 μg/L 的2-辛醇作为内标。色谱条件为:使用50 μm/30 μm CAR/DVB/PDMS 的固相微萃取(SPME)纤维萃取头提取风味化合物。毛细管柱为TG-WAXA柱(60 m×0.25 mm×0.25 μm)。GC温度程序设置如下:初始温度为40 ℃,首先以3 ℃/min的速度增加到180 ℃,然后以20 ℃/min的速度增加到230 ℃并保持15 min。检测器的温度为250 ℃,载气为He(99.999%),流速为1.2 mL/min。质量选择探测器的离子源温度为260 ℃,电子电离能为70 eV。通过监测m/z在20~450范围内的总离子电流来记录色谱图。将实验质谱与NIST 14.0数据库进行比较并通过正构烷烃(C7~C30)对化合物进行定性,采用内标法进行相对定量计算。
1.3.7 数据处理
实验谱图均采用Origin软件绘图,文章中提供的数据是“平均值±标准差”,所有的测试至少进行3个平行,实验数据通过SPSS 26.0进行单因素方差分析,当P<0.05时,认为样本之间具有显著性差异。
2 结果与分析
2.1 蒙脱石与酸改性蒙脱石的表征
2.1.1 SEM分析
如图1所示,Mt和A-Mt在形状上非常相似,都是由颗粒堆叠形成的小块组成,表明蒙脱石是层状结构[22]。通过观察图1-a~图1-c发现Mt样品的蒙脱石薄片错落堆积,呈现出较为松散的颗粒聚集状态,颗粒表面相对较为平滑,结构紧实,未呈现出明显的孔隙或层状剥离特征。与Mt相比,A-Mt的颗粒分布同样松散,但颗粒之间的团聚情况似乎有所变化,部分颗粒之间的聚集程度有所增加(图1-d),可能是由于酸处理改变了颗粒表面性质和相互作用。在高放大倍数下,图1-e和图1-f中能看到A-Mt颗粒表面开始出现一些微小的孔洞、非均匀孔隙和侵蚀痕迹,这是由于酸改性过程中,硫酸中的H+溶解、影响了二八面体骨架结构,同时取代了层间域中的阳离子,导致蒙脱石晶层间键力减弱对蒙脱石结构产生影响。这些孔道相互连通,比表面积显著增加。这种多孔结构有利于蒙脱石吸附性能等功能的提升,因为更多的表面积意味着更多的活性位点可以与外界物质发生作用。

a-Mt放大倍数300×;b-Mt放大倍数1 000×;c-Mt放大倍数3 000×;d-A-Mt放大倍数300×;e-A-Mt放大倍数1 000×;f-A-Mt放大倍数3 000×
图1 Mt和A-Mt的SEM图
Fig.1 SEM images of Mt and A-Mt
2.1.2 XRD分析
为了全面了解蒙脱石改性前后的微观结构特征并评估改性效果,对改性前后的蒙脱石进行了表征分析。由图2可知,酸处理主要对001衍射峰产生影响,经过酸处理的蒙脱石001衍射峰位置角度有略微的下降(2θMt=5.838 5°;2θA-Mt=5.819°),通过布拉格方程计算得出,经酸处理后晶面间距d001从1.51 nm增大为1.52 nm。从蒙脱石的001晶面间距可判断原矿为钙基膨润土,峰型尖锐,相对强度高,意味着Mt中的蒙脱石晶体有序性良好。酸改性过程中,氢离子交换蒙脱石层间阳离子,可能导致层间膨胀,使该值略有增加[23]。同时,酸化后的蒙脱石001衍射峰的锐度降低且强度变小,说明酸促使蒙脱石部分溶解、重结晶,使得蒙脱石的结晶度降低。但在20°~25°范围并未出现明显的无定形二氧化硅的包峰。这说明酸化土主体矿物组成仍为蒙脱石,酸化过程虽然导致了晶体结构的变化,但片层结构并未完全崩塌。从图2也可以看出A-Mt的衍射峰有一定宽化。可能是由于酸造成蒙脱石颗粒细化而导致的,根据谢乐公式,晶粒尺寸减小会引起衍射峰宽化[24]。
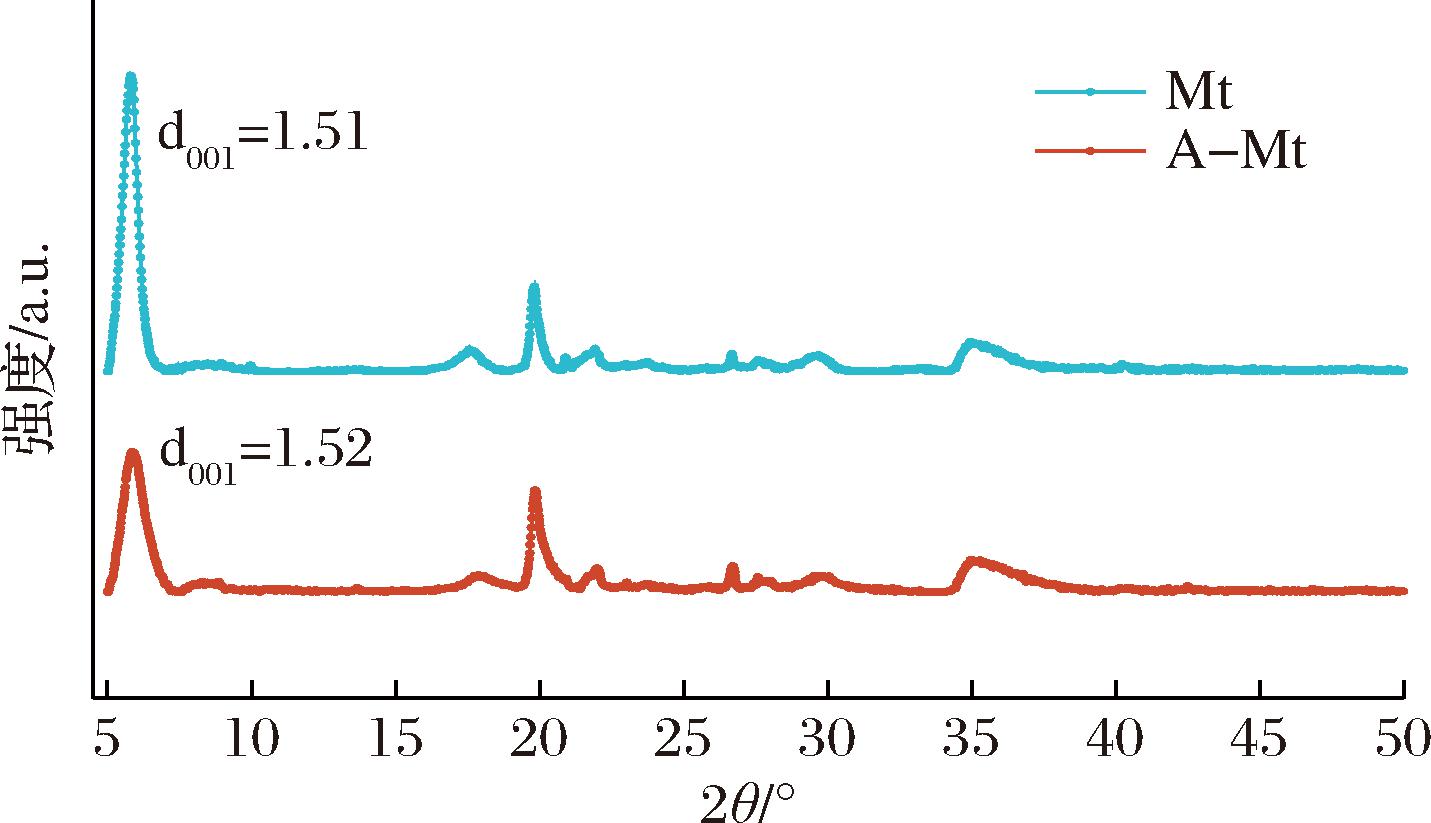
图2 Mt和A-Mt的XRD图谱
Fig.2 XRD patterns of Mt and A-Mt
总之,通过以上的分析可以发现,酸处理后的蒙脱石001晶面间距略微增大,结晶度有所降低。同时由于H+攻击结构羟基(—OH),导致四面体、八面体片层上与—OH相连的金属离子释放溶解,从而导致蒙脱石结构发生一定的改变[25],但温和的酸处理条件并没有明显扭曲黏土矿物片层结构。这保证了蒙脱石因层状结构而具有的比表面积,同时,结晶度的降低表示蒙脱石结构无序化,在此基础上可能会进一步增大比表面积,从而获得更多吸附位点,增强吸附能力。
2.1.3 FTIR分析
图3显示了Mt和A-Mt在500~4 000 cm-1范围内的红外吸收带。通过对比蒙脱石与酸改性蒙脱石的曲线发现,二者持有相似的红外光谱,这表明在本研究酸改性的过程中并未对蒙脱石的层状结构产生显著的影响,这与XRD分析结果一致。在这2个样本的光谱中,3 623 cm-1处的特征峰是由蒙脱石结构中的—OH的伸缩振动引起的,3 431 cm-1和1 640 cm-1处的特征峰是由于H—O—H的伸缩振动和弯曲振动引起的[25],仔细观察发现A-Mt的这几个峰强度较Mt有略微的上升,可能是由于酸处理后,八面体和四面体上的金属离子(如Mg2+、Al3+)被H+取代,从而释放出与之配位的水合羟基(—OH)[26]。KUMAR等[27]的研究也得到了类似的结果。794 cm-1为Si—O—Si的对称伸缩振动,可以看出酸化后峰强度明显增大,可能是由于酸化后Si—O—Si骨架含量增加所导致的[28]。
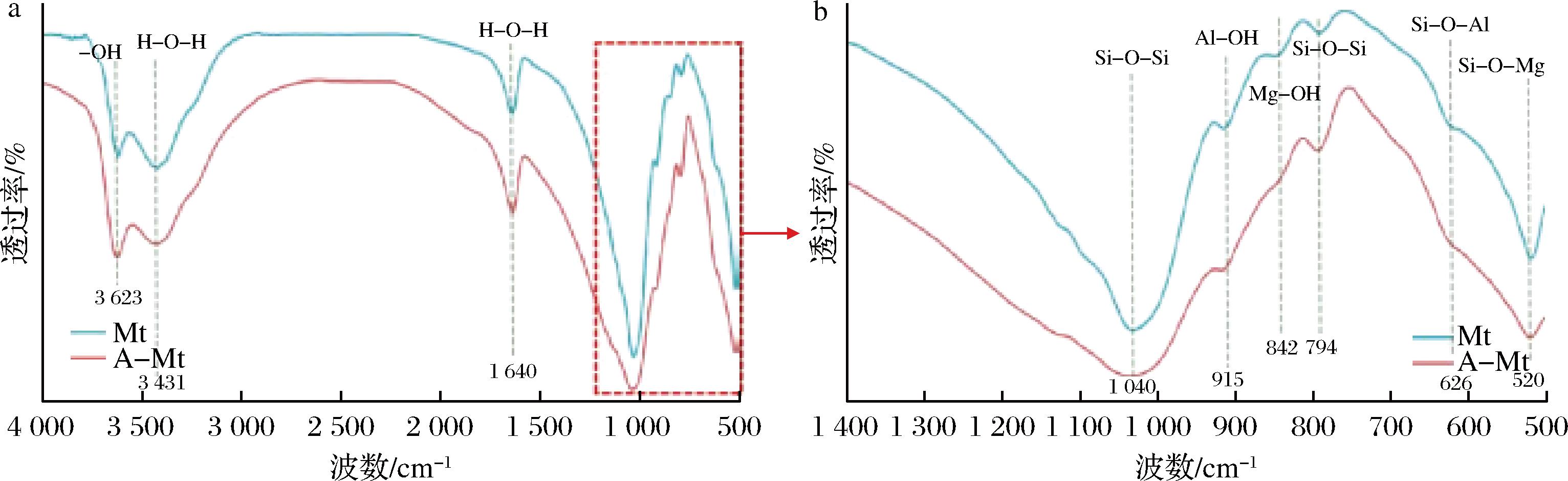
a-Mt和A-Mt的FT-IR图谱;b-500~1 400 cm-1部分放大
图3 Mt和A-Mt的FT-IR图谱
Fig.3 FT-IR spectra of Mt and A-Mt
红外光谱中部分特征峰减弱是由于结构单元层边缘处的铁、硅、铝与氢离子反应,出现了小部分溶解[29]。1 030~1 050 cm-1为Si—O—Si的反对称伸缩振动,915 cm-1和842 cm-1分别为八面体中Al—OH和Mg—OH的弯曲振动。626 cm-1为Si—O—Al的弯曲振动,520 cm-1为Si—O—Mg的弯曲振动。通过对比发现,酸处理后915、842、626、520 cm-1的4个位置的峰强度明显减弱,是由于H+取代了八面体上的金属离子Mg2+、Al3+,所以相应的振动变弱了[30],与前面的分析一致。其中可以发现,Mg—OH、Si—O—Mg所属的峰比Al—OH、Si—O—Al的减弱程度还大,说明八面体中阳离子的溶出顺序是Mg2+>Al3+。在1 040 cm-1处A-Mt的峰强度也有略微减弱的趋势,同样也是由于蒙脱石的硅氧骨架在H+作用下,Si—O键可能发生水解断裂,导致硅氧四面体的结构被破坏,但A-Mt的峰强度并未显著减弱,同样印证了蒙脱石的层状结构虽有影响,但并未遭到明显破坏的现象。FTIR的结果进一步证明,酸改性后H+取代了大部分八面体上的金属离子Mg2+、Al3+,导致表面电荷密度发生变化,使得蒙脱石所带的负电荷相应的增加,这有助于提升蒙脱石的吸附能力。
2.2 酸改性对蒙脱石嘌呤吸附效果的影响
通过改变Mt与A-Mt不同添加量得到的嘌呤含量,并代入公式(1)计算吸附率。以添加量为横坐标,得到的吸附率数据为纵坐标绘制折线图如图4所示。随着添加量的增加,Mt和A-Mt的吸附率均呈现出先增加后趋于平缓达到吸附率饱和的状态,此时吸附和脱附达到动态平衡时,吸附量不再变化,符合蒙脱石吸附过程的特点,这与LIAO等[31]的研究结果基本一致。同时,从图4中可以明显看出,A-Mt的最终饱和吸附率(96.21%)显著高于Mt的饱和吸附率(55.20%),且A-Mt在添加量为10 g/L时即达到饱和,Mt则在20 g/L达到饱和,A-Mt在添加量比Mt更少的情况下,能够达到更高的饱和吸附率量,说明酸改性能够显著提高蒙脱石的吸附效果。
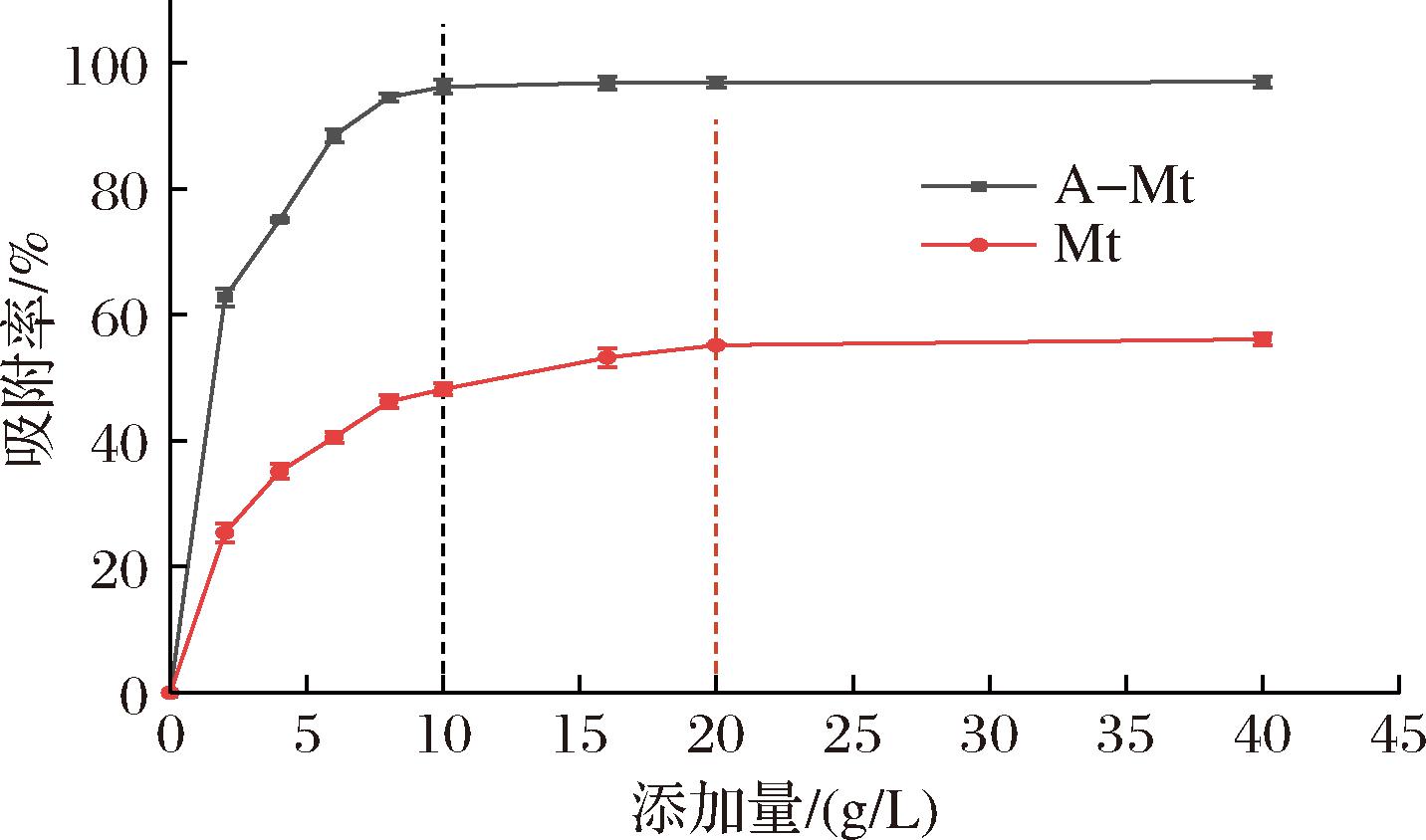
图4 蒙脱石改性前后吸附容量的变化
Fig.4 Changes in adsorption capacity before and after montmorillonite modification
同时取2种蒙脱石各自饱和吸附率位点的嘌呤浓度计算出4种嘌呤详细的吸附率汇入表2中,同时代入公式(2)中计算吸附量得到qMt为5.59 mg/g,qA-Mt为19.48 mg/g,A-Mt对于嘌呤物质的吸附量大幅提高。可能是由于酸改性后H+取代了大部分八面体上的金属离子Mg2+、Al3+,导致表面电荷密度发生变化,使得蒙脱石所带的负电荷相应的增加,而嘌呤物质在酸性环境下会因为质子化带正电荷,正因为这样的表面电荷的改变,提高了A-Mt对于嘌呤类物质的吸附能力[12]。除此之外,通过前文的表征数据得知,酸处理使得蒙脱石的层间结构发生变化,导致层间距增大和层间膨胀,同时又使A-Mt表面获得了更多微小孔洞、非均匀孔隙和更大的比表面积,这些都更有利于增加更多的吸附位点,层间距的扩大也为嘌呤物质进入蒙脱石层间提供了更有利的条件。
表2 蒙脱石改性前后对于嘌呤标准溶液的吸附效果
Table 2 Adsorption effect of montmorillonite on purine standard solution before and after modification
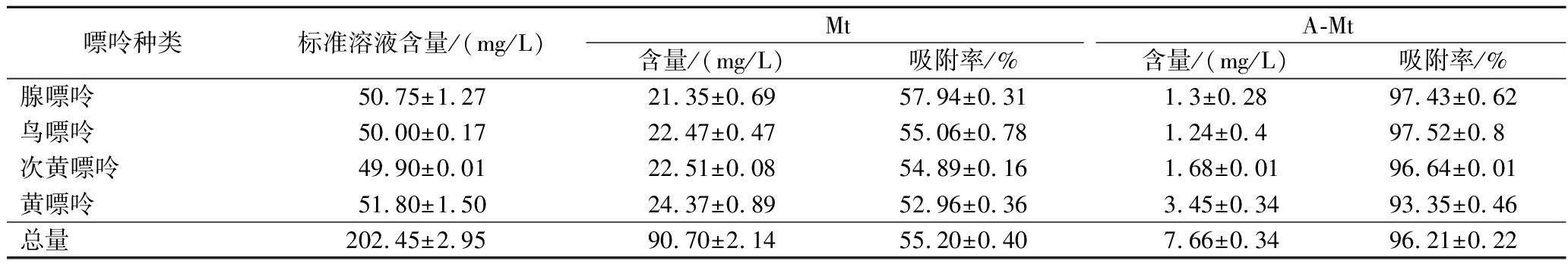
嘌呤种类标准溶液含量/(mg/L)MtA-Mt含量/(mg/L)吸附率/%含量/(mg/L)吸附率/%腺嘌呤50.75±1.2721.35±0.6957.94±0.311.3±0.2897.43±0.62鸟嘌呤50.00±0.1722.47±0.4755.06±0.781.24±0.497.52±0.8次黄嘌呤49.90±0.0122.51±0.0854.89±0.161.68±0.0196.64±0.01黄嘌呤51.80±1.5024.37±0.8952.96±0.363.45±0.3493.35±0.46总量202.45±2.9590.70±2.1455.20±0.407.66±0.3496.21±0.22
2.3 酸改性蒙脱石吸附工艺优化
本节选择HB作为实验对象。前文分析了酸改性蒙脱石在标准溶液中的吸附效果,而啤酒是一个复杂的体系,不单单只存在嘌呤类物质,色素、蛋白质、风味物质等也能够与蒙脱石进行作用,会存在竞争性的吸附[11, 25]。而作为食品的啤酒,嘌呤含量降低固然重要,也不能忽略消费者的直观感受。因此,在啤酒中的添加量与作用时间不仅需根据啤酒中的吸附效果重新评定,同时还要控制风味损失与嘌呤吸附的平衡。但由于风味的形成非常复杂,不仅依靠关键性风味物质的阈值,不同物质之间也会相互作用从而影响最终的感官体验[32],因此为了更直接地平衡风味与嘌呤吸附,本文采用了直接的感官评定作为风味的平衡点。同时,由于啤酒经过后储期、过滤到稀释工序时,pH值通常在4.0左右,并且环境一般为4 ℃。而吸附材料的使用需要在过滤前投入罐中发挥作用,为模拟实际生产中的作用环境,因此将溶液的pH值定为4.0,温度定为4 ℃。
表3展示了当添加量为10 g/L时,不同处理时间下啤酒的嘌呤含量及A-Mt的吸附率,表4展示了处理时间为1 h时,不同添加量下啤酒的嘌呤含量及A-Mt的吸附率。从表3和4中可以观察到,啤酒中的次黄嘌呤含量相比于其他3种嘌呤最少,鸟嘌呤含量相对最高。这与李萍[33]及杨祥根等[34]的研究结果一致。同时可以看出A-Mt对4种嘌呤均有一定的吸附作用,并随添加量和时间的增长而增长。表5展示了与表3和4相同条件下相应的啤酒感官评分变化,从表5中可以看出,随着添加量和处理时间的增长,啤酒的色泽、气味和口味的评分随之下降,但澄清度的评分随之上升。
表3 不同处理时间下啤酒的嘌呤含量及材料吸附率
Table 3 Purine content and material adsorption rate of beer under different processing times

不同处理时间/min腺嘌呤鸟嘌呤次黄嘌呤黄嘌呤总量对照组含量/(mg/L)14.03±0.0718.8±0.340.33±0.046.87±0.2240.03±0.150吸附率/%—————处理组3-1含量/(mg/L)14.01±0.7216.4±0.550.34±0.066.15±0.1436.9±0.0310吸附率/%0.16±4.6312.73±4.51-3.52±0.1510.44±0.757.81±0.42d处理组3-2含量/(mg/L)6.25±0.5212.36±0.130.32±0.065.23±0.1724.16±0.5130吸附率/%55.46±3.534.24±1.862.91±4.1223.77±4.8639.64±1.04c处理组3-3含量/(mg/L)4.12±0.18.56±0.640.28±0.045.12±0.4718.08±0.3145吸附率/%70.64±0.5654.49±2.5613.14±24.6325.52±4.4654.83±0.61b处理组3-4含量/(mg/L)2.12±0.035.36±0.040.11±0.013.56±0.4411.15±0.4150吸附率/%84.89±0.2871.49±0.2965.93±8.948.24±4.7672.14±1.13a处理组3-5含量/(mg/L)2.11±0.285.37±0.350.16±0.043.58±0.4411.22±0.4760吸附率/%84.96±2.0971.45±1.3751.75±6.447.74±8.0271.97±1.06a处理组3-6含量/(mg/L)2.15±0.185.27±0.40.15±0.063.61±0.0811.18±0.55120吸附率/%84.67±1.3971.94±2.6155.11±11.1647.39±2.8972.07±1.48a
注:表中同列不同字母表示差异显著(P<0.05);“—”表示该数据不被计算,此时添加量为10 g/L。
表4 不同添加量下啤酒的嘌呤含量及材料吸附率
Table 4 Purine content and material adsorption rate of beer under different addition amounts

不同添加量/(g/L)腺嘌呤鸟嘌呤次黄嘌呤黄嘌呤总量对照组含量/(mg/L)14.03±0.6918.8±0.810.33±0.036.87±0.4240.03±0.50吸附率/%—————处理组4-1含量/(mg/L)14.01±0.3117.45±0.820.34±0.066.15±0.3837.95±0.832吸附率/%0.08±2.717.19±0.38-3.49±0.9010.45±0.075.19±0.89d处理组4-2含量/(mg/L)8.79±0.3815.24±0.540.31±0.046.22±0.1730.56±1.05
续表4

不同添加量/(g/L)腺嘌呤鸟嘌呤次黄嘌呤黄嘌呤总量4吸附率/%37.21±5.8218.92±0.625.87±4.269.33±3.0823.66±1.65c处理组4-3含量/(mg/L)2.11±0.625.37±0.180.16±0.013.58±0.4811.22±0.0610吸附率/%85.05±3.771.43±0.2550.91±8.8147.99±3.8171.97±0.21b处理组4-4含量/(mg/L)1.89±0.454.52±0.080.11±0.013.45±0.259.97±0.6115吸附率/%86.43±3.8975.93±1.4866.59±1.2349.78±0.6375.10±1.21a处理组4-5含量/(mg/L)1.94±0.084.52±0.350.14±0.033.42±0.1110.02±0.5220吸附率/%86.14±1.2975.98±0.8557.62±4.7150.16±1.4174.97±0.99a处理组4-6含量/(mg/L)1.85±0.374.38±0.210.15±0.043.44±0.259.82±0.8840吸附率/%86.73±3.2876.70±0.1353.57±17.1749.93±0.6475.48±1.88a
注:表中同列不同字母表示差异显著(P<0.05);“—”表示该数据不被计算,此时处理时间为1 h。
表5 A-Mt不同添加量及不同处理时间下对啤酒感官的影响
Table 5 A-Mt effects of different dosage and different treatment time on sensory properties of beer
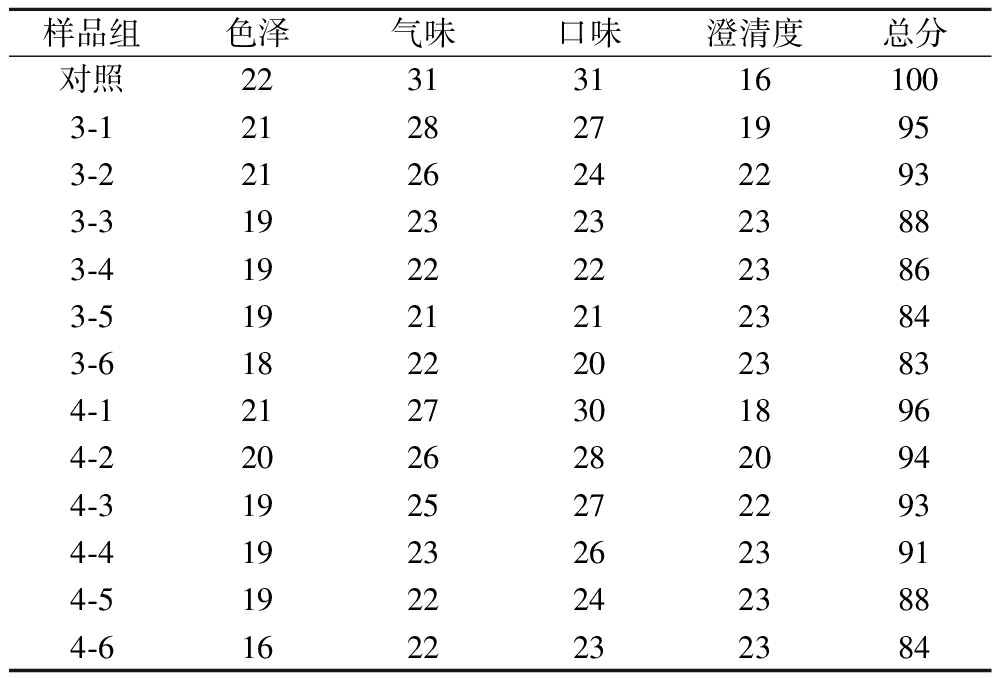
样品组色泽气味口味澄清度总分对照223131161003-121282719953-221262422933-319232323883-419222223863-519212123843-618222023834-121273018964-220262820944-319252722934-419232623914-519222423884-61622232384
为了更直观地对比,将表格中的数据按照不同处理时间和不同添加量绘制图5,其中感官评分选取了总评分进行比对。由图5可知,随着添加量和处理时间的增加,A-Mt吸附率呈现出先上升后饱和的趋势,这与前文在标准溶液中的吸附率变化趋势表现一致。而啤酒的感官评分呈现出下降的趋势,通过图5-a的分析发现,处理时间在50 min时,吸附率达到饱和(72.14%),处理时间从45 min升高至50 min时,吸附率显著增加(从54.83%增加至72.14%),而感官数据有所下降(93至91)鉴于吸附率的大幅上涨,因此我们选择50 min为最终的A-Mt处理时间。同样,对比图5-b发现,A-Mt添加量为15 g/L时达到饱和,当添加量由10 g/L升至15 g/L时,吸附率由71.97%升至75.1%,同时感官评分由88下降至86,两者均小幅度发生改变。同时考虑到成本问题,选择10 g/L作为A-Mt添加量。最终的添加工艺确定为10 g/L添加量,处理时间为50 min,此时的啤酒中的总嘌呤含量由40.03 mg/L降低至约11 mg/L,吸附率最高达72.14%,同时最高感官评分为91分。
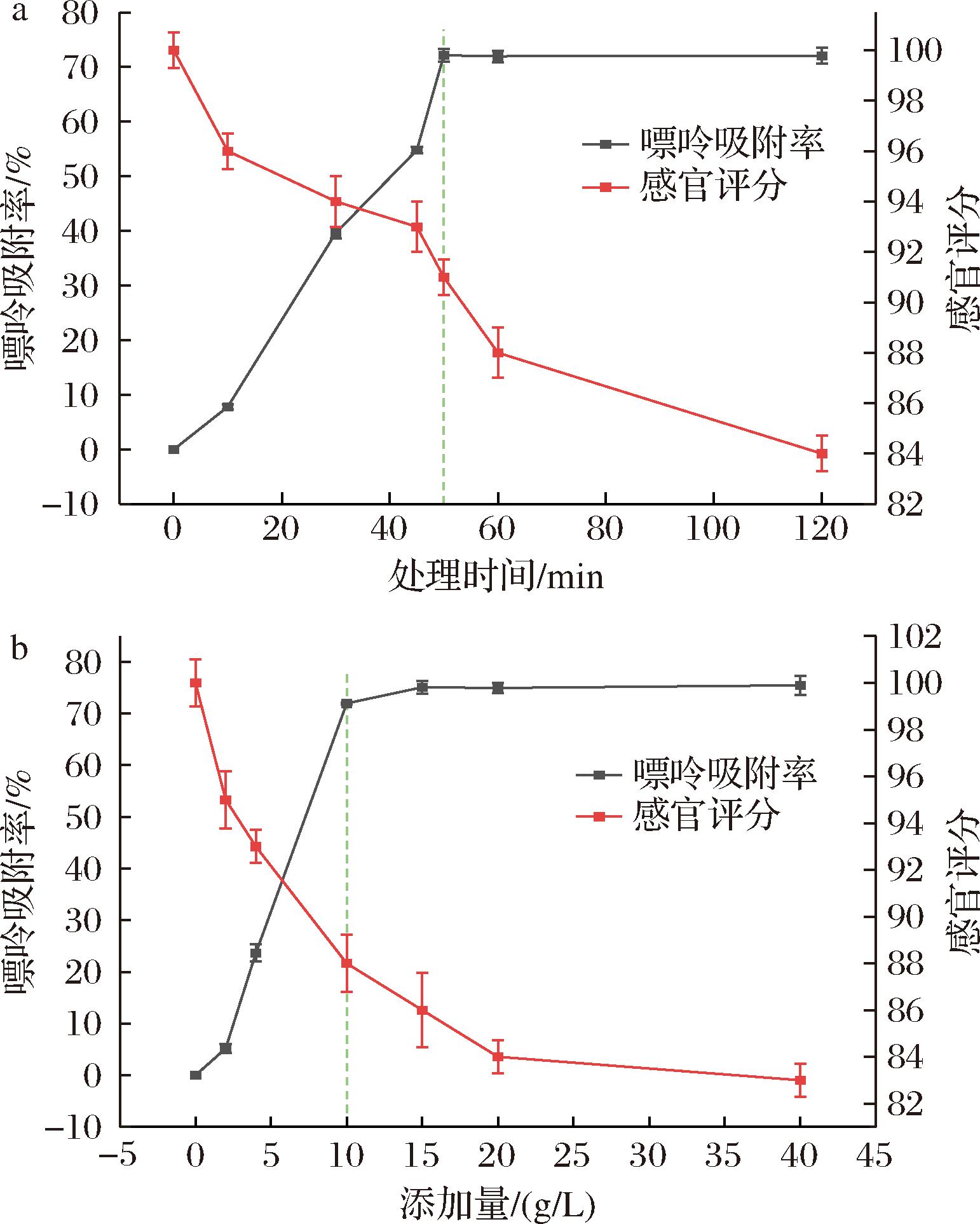
a-不同处理时间;b-不同添加量
图5 酸改性蒙脱石在啤酒中吸附条件的优化
Fig.5 Optimization of the adsorption conditions of acid-modified montmorillonite in beer
2.4 酸改性蒙脱石吸附对啤酒品质的影响
2.4.1 理化分析
在2.3节中确定了最终啤酒中A-Mt的添加工艺,为了更科学地分析蒙脱石改性以及此吸附工艺下对啤酒品质的影响,本节结合了风味以及理化数据对啤酒品质进行了详细分析,同样选取了HB作为样本进行对比。如表6所示,吸附对啤酒的pH、总酸以及酒精度的影响均没有显著性差异,但是就浊度而言,具有一定程度的下降[HB:5.86 EBC;HB (Mt):5.39 EBC;HB (A-Mt):5.40 EBC]。这与VALERO[35]研究蒙脱石能够通过降低浊度作为果汁中的澄清剂结果表现一致。说明蒙脱石具有一定降低浊度的能力,使啤酒呈现出清澈透明的状态,这同样也与前文感官数据中澄清度的评分结果基本一致。
表6 不同蒙脱石吸附前后啤酒的理化指标
Table 6 Physical and chemical indexes of beer before and after adsorption with different montmorillonite
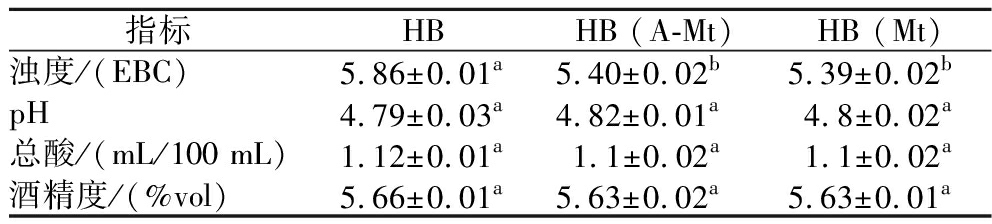
指标HBHB (A-Mt)HB (Mt)浊度/(EBC)5.86±0.01a5.40±0.02b5.39±0.02bpH4.79±0.03a4.82±0.01a4.8±0.02a总酸/(mL/100 mL)1.12±0.01a1.1±0.02a1.1±0.02a酒精度/(%vol)5.66±0.01a5.63±0.02a5.63±0.01a
注:表中同行不同字母表示差异显著(P<0.05)。
2.4.2 挥发性风味物质分析
风味物质根据SI及RSI值>700筛选,删去硅氧烷等柱流失峰,同时留下对啤酒风味有贡献的物质。如表7所示,GC-MS共分析检测出40种物质,包括醇、醛、酸、酮和酯类5种,2种蒙脱石吸附后均检测出37种物质。风味物质的个数和总风味物质含量见图6,结合图6和表7可以看出,吸附后啤酒中的风味物质种类均相应的减少,其中糠醛、月桂酸和醋酸正丙酯在吸附后无法被检测。对于总风味物质含量,HB中共检测到了9 864.22 μg/L的风味物质,在Mt吸附后总风味物质含量为8 441.57 μg/L;A-Mt吸附后总风味物质含量为8 538.94 μg/L,与对照组HB相比风味物质分别下降14.4%和13.4%。从图6也可以看出,HB在Mt与A-Mt吸附后的总风味物质含量均有一定程度的下降。总体来讲,Mt与A-Mt吸附后的风味物质在种类和含量上相较于对照样均有一定程度上的下降,但二者之间没有显著性的差异。
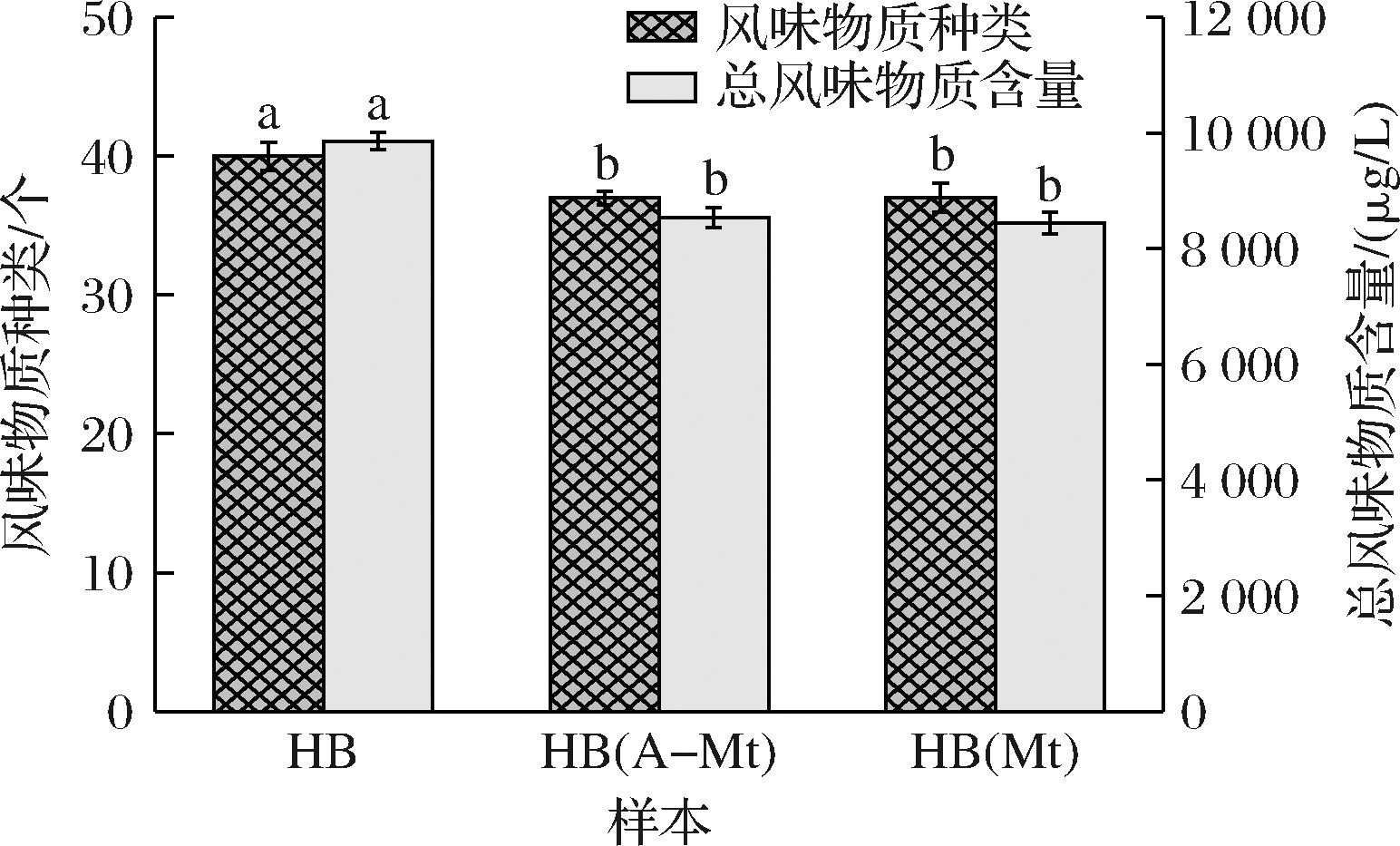
图6 不同啤酒吸附前后总风味物质的变化
Fig.6 Changes in the total flavor substances of different beers before and after adsorption
注:不同小写字母表示组间具有显著性差异(P<0.05)。
表7 蒙脱石吸附前后对啤酒的风味物质的影响 单位:μg/L Table 7 Effect of montmorillonite on flavor compounds of beer before and after adsorption

中文名CAS号含量HBHB (A-Mt)HB (Mt)乙醇64-17-54 103.42±45.533 598.51±85.013 580.82±110.19正丙醇71-23-819.68±0.2519.25±0.6418.22±0.33异丁醇78-83-147.09±3.3237.14±1.1534.23±2.02异戊醇123-51-31 367±19.121 034.31±13.941 028.69±6.55正己醇111-27-33.16±0.043.09±0.13.04±0.13芳樟醇78-70-610.52±0.2910.19±0.019.25±0.151-壬醇143-08-83.99±0.143.02±0.113.76±0.173-甲硫基丙醇505-10-26.28±0.176.25±05.92±0.081-癸醇112-30-18.78±0.048.39±0.277.48±0.11橙花醇106-25-22.52±0.062.44±0.012.18±0.42苯乙醇60-12-81 295.14±16.771 167.84±17.741 176.95±17.22月桂醇112-53-88.14±0.276.82±0.327.14±0.04(+)-雪松醇77-53-23.53±0.163.22±0.162.99±0.4醇类6 879.26±86.16a5 900.47±119.46b5 880.67±137.81b乙醛75-07-013.08±0.0111.48±0.4112.96±1.99
续表7
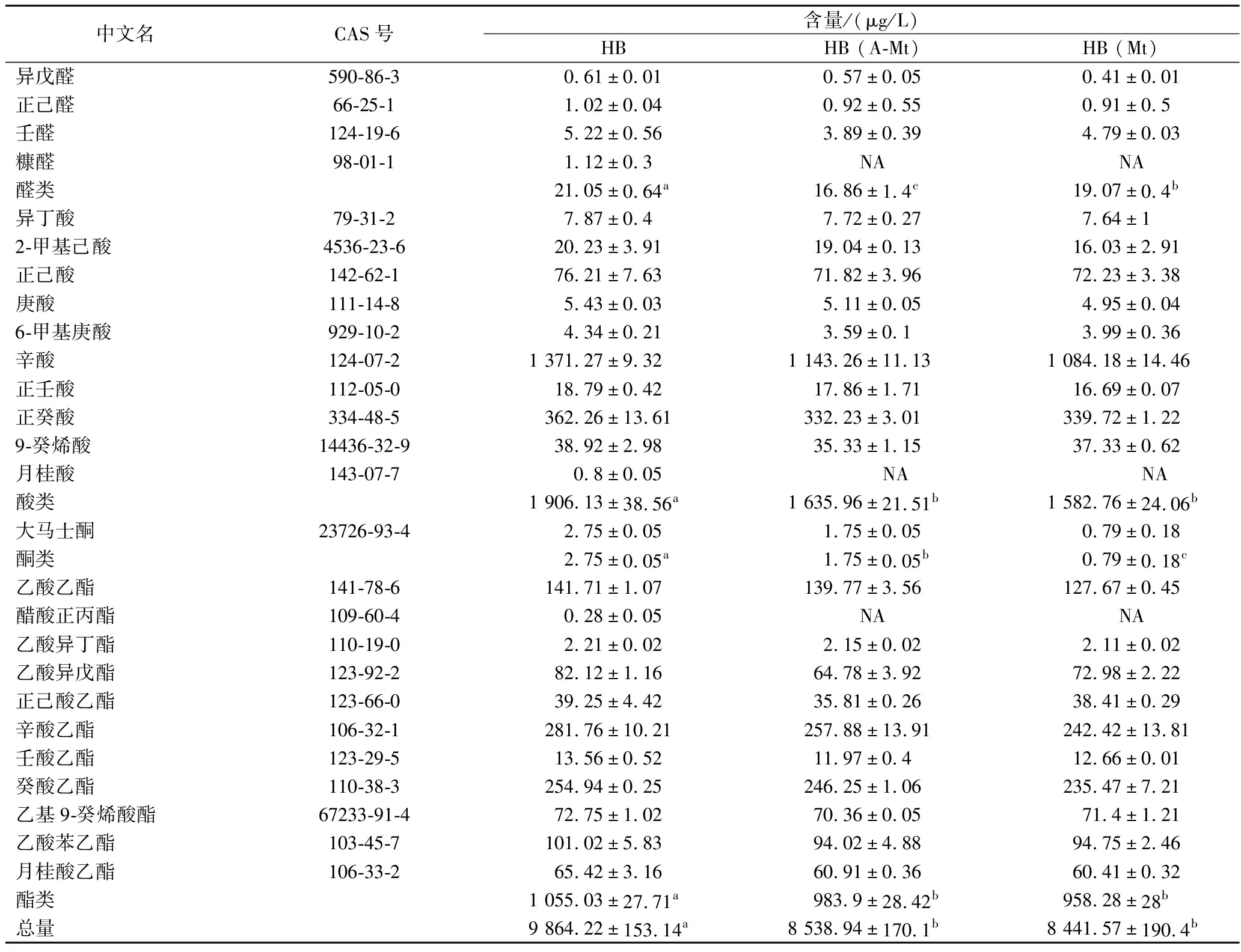
中文名CAS号含量/(μg/L)HBHB (A-Mt)HB (Mt)异戊醛590-86-30.61±0.010.57±0.050.41±0.01正己醛66-25-11.02±0.040.92±0.550.91±0.5壬醛124-19-65.22±0.563.89±0.394.79±0.03糠醛98-01-11.12±0.3NANA醛类21.05±0.64a16.86±1.4c19.07±0.4b异丁酸79-31-27.87±0.47.72±0.277.64±12-甲基己酸4536-23-620.23±3.9119.04±0.1316.03±2.91正己酸142-62-176.21±7.6371.82±3.9672.23±3.38庚酸111-14-85.43±0.035.11±0.054.95±0.046-甲基庚酸929-10-24.34±0.213.59±0.13.99±0.36辛酸124-07-21 371.27±9.321 143.26±11.131 084.18±14.46正壬酸112-05-018.79±0.4217.86±1.7116.69±0.07正癸酸334-48-5362.26±13.61332.23±3.01339.72±1.229-癸烯酸14436-32-938.92±2.9835.33±1.1537.33±0.62月桂酸143-07-70.8±0.05NANA酸类1 906.13±38.56a1 635.96±21.51b1 582.76±24.06b大马士酮23726-93-42.75±0.051.75±0.050.79±0.18酮类2.75±0.05a1.75±0.05b0.79±0.18c乙酸乙酯141-78-6141.71±1.07139.77±3.56127.67±0.45醋酸正丙酯109-60-40.28±0.05NANA乙酸异丁酯110-19-02.21±0.022.15±0.022.11±0.02乙酸异戊酯123-92-282.12±1.1664.78±3.9272.98±2.22正己酸乙酯123-66-039.25±4.4235.81±0.2638.41±0.29辛酸乙酯106-32-1281.76±10.21257.88±13.91242.42±13.81壬酸乙酯123-29-513.56±0.5211.97±0.412.66±0.01癸酸乙酯110-38-3254.94±0.25246.25±1.06235.47±7.21乙基9-癸烯酸酯67233-91-472.75±1.0270.36±0.0571.4±1.21乙酸苯乙酯103-45-7101.02±5.8394.02±4.8894.75±2.46月桂酸乙酯106-33-265.42±3.1660.91±0.3660.41±0.32酯类1 055.03±27.71a983.9±28.42b958.28±28b总量9 864.22±153.14a8 538.94±170.1b8 441.57±190.4b
注:表中同行不同字母表示差异显著(P<0.05);“NA”表示未检出。
由图7可知,每种风味物质在吸附后都有一定程度下降。其中,啤酒的高级醇和酯类物质是啤酒风味的主要贡献者。高级醇能够使啤酒口感丰满、香气协调,但含量过高会导致异杂味,甚至引起饮用后的不适感,如容易“上头”的现象[36]。通过对比分析发现HB的醇酯比约为6.52,而HB (Mt)约为6.14,HB (A-Mt)约为6.00。虽然在含量上,A-Mt和Mt吸附后每类风味物质相比于对照啤酒均有一定程度的下降,但醇酯比也相应地下降,更有助于协调啤酒的风味,降低其引发“上头”的不良反应。
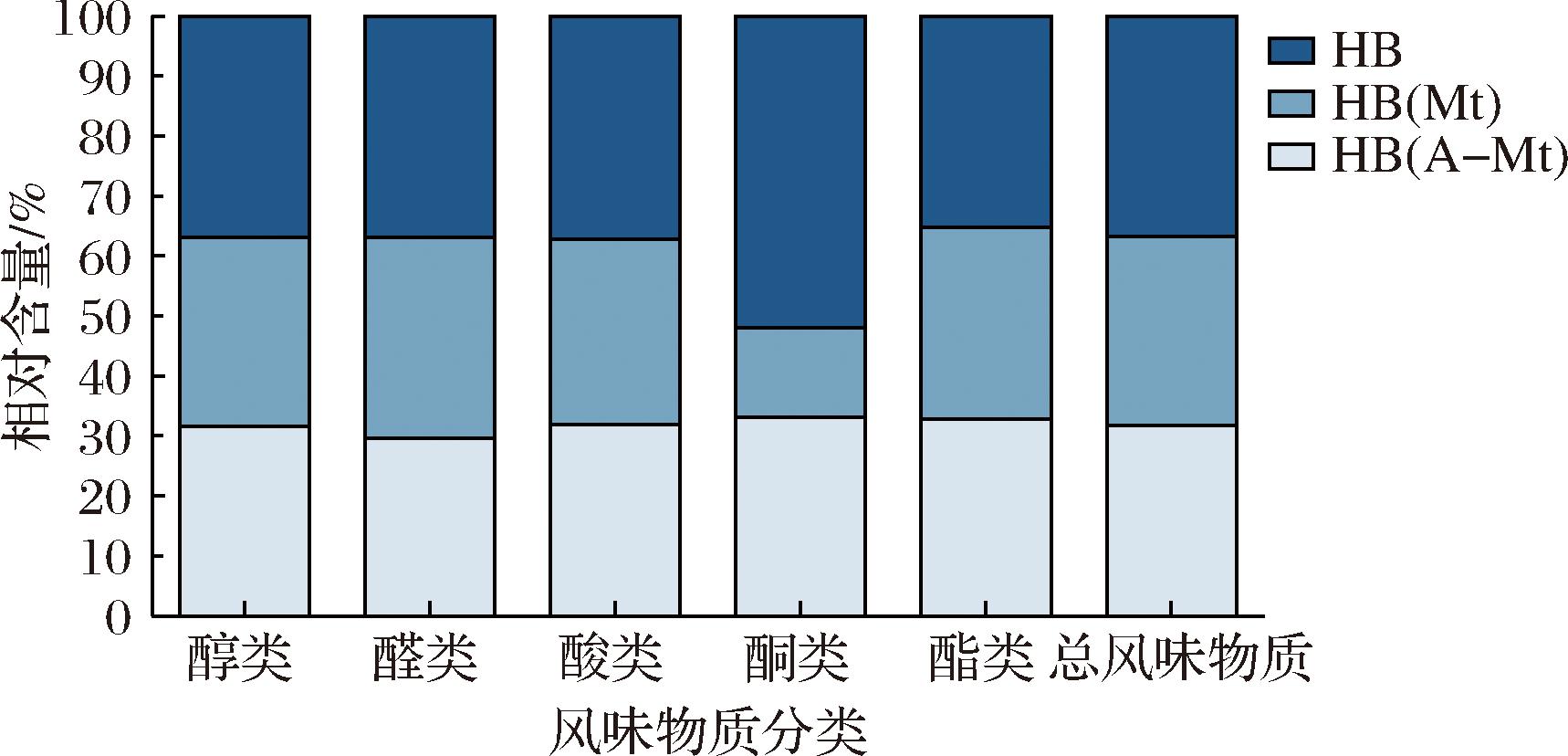
图7 不同啤酒吸附前后风味物质堆积图
Fig.7 Stacked chart of flavor substances of different beers before and after adsorption
3 结论
本文对蒙脱石进行酸改性,同时研究了蒙脱石改性前后对嘌呤类物质吸附作用的影响,并将其应用至啤酒中,通过平衡感官品评和嘌呤物质的吸附效果,优化了酸改性蒙脱石的添加工艺,且分析该工艺下的蒙脱石吸附对啤酒品质的影响。研究发现:
酸改性会使蒙脱石的晶面间距略有增长、使其结晶度降低,同时H+取代了八面体上的金属离子Mg2+、Al3+,使得蒙脱石所带的负电荷相应的增加。颗粒表面开始出现一些微小的孔洞、非均匀孔隙,虽然导致了蒙脱石晶体结构的变化,但片层结构并未完全崩塌。A-Mt的最终饱和吸附率(96.21%)显著高于Mt的饱和吸附率(55.20%),A-Mt在添加量比Mt更少的情况下,能够达到更高的饱和吸附率。同时计算出Mt吸附量为5.59 mg/g,而A-Mt吸附量提高到了19.48 mg/g。吸附后的啤酒在风味物质上有一定程度的下降[HB:9 864.22 μg/L;HB(Mt):8 441.57 μg/L;HB(A-Mt):8 538.94 μg/L],同时嘌呤吸附率达到72%,风味物质损失[HB(Mt):14.4%;HB(A-Mt):13.4%]。此时的啤酒中的总嘌呤含量由40.03 mg/L降低至约11 mg/L,同时最高感官评分为91分。酸改性提高了蒙脱石对于嘌呤类物质的吸附率,但是对风味物质的吸附效果没有显著影响。本研究对开发一种安全且高效的啤酒嘌呤吸附材料具有一定的参考意义。
[1] 刘红霞, 范秀芝, 殷朝敏, 等.高效液相色谱法同时检测食用菌中的4种嘌呤[J].食品安全质量检测学报, 2025, 16(2):178-186.LIU H X, FAN X Z, YIN C M, et al.Simultaneous detection of 4 kinds of purines in edible fungi by high performance liquid chromatography[J].Journal of Food Safety &Quality, 2025, 16(2):178-186.
[2] VIEIRA A C, PEREIRA A C, MARQUES J C, et al.Multi-target optimization of solid phase microextraction to analyse key flavour compounds in wort and beer[J].Food Chemistry, 2020, 317:126466.
[3] ALMEIDA C, NEVES M C, FREIRE M G.Towards the use of adsorption methods for the removal of purines from beer[J].Molecules, 2021, 26(21):6460.
[4] 李玉淼, 朱德伟, 朱洪康, 等.嘌呤核苷磷酸化酶的表达及其在啤酒中的应用[J].食品与生物技术学报, 2017, 36(12):1264-1268.LI Y M, ZHU D W, ZHU H K, et al.Expression of purine nucleoside phosphorylase and its application in beer[J].Journal of Food Science and Biotechnology, 2017, 36(12):1264-1268.
[5] 王吉龙. 低嘌呤啤酒工艺的开发研究[D].泰安:山东农业大学, 2014.WANG J L.Studies on the techniques of producing low-purine beer[D].Tai’an:Shandong Agricultural University, 2014.
[6] 易昕, 胡金成, 曹又新, 等.一种低嘌呤啤酒的生产方法:中国, CN1563321A[P].2005-01-12.YI X, HU J C, CAO Y X, et al.Production method of low-purine beer:China, CN1563321A[P].2005-01-12.
[7] 王海容, 付大友, 王蓉.吸附剂对啤酒中嘌呤类物质吸附的研究[J].酿酒科技, 2009(9):50-54.WANG H R, FU D Y, WANG R.Research on the absorption of purine compounds in beer by absorbents[J].Liquor-Making Science &Technology, 2009(9):50-54.
[8] 雷崑, 黄雅琳.壳聚糖对啤酒中嘌呤的吸附性能[J].安徽农业科学, 2006, 34(7):1431.LEI K, HUANG Y L.Reduction of purine content in beer by chitosan absorption[J].Journal of Anhui Agricultural Sciences, 2006, 34(7):1431.
[9] 张娟. 磁性蒙脱石的制备及其对四环素与环丙沙星的吸附性能研究[D].南京:南京理工大学, 2019.ZHANG J.Preparation of magnetic montmorillonite and its adsorption properties for tetracycline and ciprofloxacin[D].Nanjing:Nanjing University of Science and Technology, 2019.
[10] 张颖心, 张天胜.膨润土在环境污染治理方面的研究进展[J].工业水处理, 2002, 22(10):9-12.ZHANG Y X, ZHANG T S.Contaminated environment remediation with bentonite[J].Industrial Water Treatment, 2002, 22(10):9-12.
[11] 夏云梯, 朱克美, 陈卫平.膨润土在食品工业中的应用[J].食品研究与开发, 1985, 6(3):26-27.XIA Y T, ZHU K M, CHEN W P.Application of bentonite in food industry[J].Food Research and Development, 1985, 6(3):26-27.
[12] BA J P T, VILLAFA
J P T, VILLAFA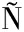 E-BARAJAS S A, DA COSTA A C S, et al.Adenine adsorbed onto montmorillonite exposed to ionizing radiation:Essays on prebiotic chemistry[J].Astrobiology, 2020, 20(1):26-38.
E-BARAJAS S A, DA COSTA A C S, et al.Adenine adsorbed onto montmorillonite exposed to ionizing radiation:Essays on prebiotic chemistry[J].Astrobiology, 2020, 20(1):26-38.
[13] BHATTI U H, KAZMI W W, MUHAMMAD H A, et al.Practical and inexpensive acid-activated montmorillonite catalysts for energy-efficient CO2 capture[J].Green Chemistry, 2020, 22(19):6328-6333.
[14] ZHAO Y H, MA F, TANG K.Preparation of acid-activated montmorillonite and its application[J].Marine Georesources &Geotechnology, 2016, 34(8):741-746.
[15] TYAGI B, CHUDASAMA C D, JASRA R V.Determination of structural modification in acid activated montmorillonite clay by FT-IR spectroscopy[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2006, 64(2):273-278.
[16] EL MOUZDAHIR Y, ELMCHAOURI A, MAHBOUB R, et al.Equilibrium modeling for the adsorption of methylene blue from aqueous solutions on activated clay minerals[J].Desalination, 2010, 250(1):335-338.
[17] BHATTACHARYYA K G, SENGUPTA S, SARMA G K.Interactions of the dye, Rhodamine B with kaolinite and montmorillonite in water[J].Applied Clay Science, 2014, 99:7-17.
[18] 田景斐, 孙红娟, 彭同江.酸处理对蒙脱石结构及理化性能的影响[J].化工矿物与加工, 2022, 51(1):12-17.TIAN J F, SUN H J, PENG T J.The effect of sulfuric acid treatment on the structure and physical &chemical properties of montmorillonite[J].Industrial Minerals &Processing, 2022, 51(1):12-17.
[19] ZVINOWANDA C M, OKONKWO J O, SHABALALA P N, et al.A novel adsorbent for heavy metal remediation in aqueous environments[J].International Journal of Environmental Science &Technology, 2009, 6(3):425-434.
[20] MANCOSKY D G, LUCIA L A.A novel and efficient approach for imparting magnetic susceptibility to lignocellulosic fibers[J].Carbohydrate Polymers, 2005, 59(4):517-520.
[21] 林睿, 吴殿辉, 彭政聪, 等.茶叶不同添加方式对太平猴魁绿茶啤酒风味影响[J].食品与发酵工业, 2025, 51(1):81-89.LIN R, WU D H, PENG Z C, et al.Effect of different tea addition methods on flavor of Taiping Houkui green tea beer[J].Food and Fermentation Industries, 2025, 51(1):81-89.
[22] MARTINS M G, MARTINS D O T A, DE CARVALHO B L C, et al.Synthesis and characterization of montmorillonite clay intercalated with molecular magnetic compounds[J].Journal of Solid State Chemistry, 2015, 228:99-104.
[23] D AZ F R V, SANTOS P D.Studies on the acid activation of Brazilian smectitic clays[J].Quimica Nova, 2001, 24(3):345-353.
AZ F R V, SANTOS P D.Studies on the acid activation of Brazilian smectitic clays[J].Quimica Nova, 2001, 24(3):345-353.
[24] 王立满, 莫伟, 马少健, 等.高纯钠基蒙脱石的剥离及其表征[J].矿产保护与利用, 2020, 40(4):124-133.WANG L M, MO W, MA S J, et al.Delaminating and characterizing of high purity sodium montmorillonite[J].Conservation and Utilization of Mineral Resources, 2020, 40(4):124-133.
[25] 林小琴, 王钺博, 朱建喜, 等.酸化蒙脱石对挥发性有机物的吸附研究[J].矿物学报, 2015, 35(3):281-287.LIN X Q, WANG Y B, ZHU J X, et al.Preparation and characterization of acid activated montmorillonites for VOCs removal[J].Acta Mineralogica Sinica, 2015, 35(3):281-287.
[26] DONGMO L M, JIOKENG S L Z, PECHEU C N, et al.Amino-grafting of montmorillonite improved by acid activation and application to the electroanalysis of catechol[J].Applied Clay Science, 2020, 191:105602.
[27] KUMAR S, PANDA A K, SINGH R K.Preparation and characterization of acid and alkaline treated Kaolin clay[J].Bulletin of Chemical Reaction Engineering &Catalysis, 2013, 8(1):61-69.
[28] ANGAJI M T, ZINALI A Z, QAZVINI N T.Study of physical, chemical and morphological alterations of smectite clay upon activation and functionalization via the acid treatment[J].World Journal of Nano Science and Engineering, 2013, 3(4):161-168.
[29] KOMADEL P.Acid activated clays:Materials in continuous demand[J].Applied Clay Science, 2016, 131:84-99.
[30] 吴平霄, 张惠芬, 郭九皋, 等.蒙脱石酸处理产物的微结构变化研究[J].无机材料学报, 1999, 14(6):909-914.WU P X, ZHANG H F, GUO J G, et al.Microstructure of montmorillonite and its acid treatment products[J].Journal of Inorganic Materials, 1999, 14(6):909-914.
[31] LIAO K L, AN J N, FU L P, et al.Adsorption of welan gum on montmorillonite and its influencing factors[J].Polymers, 2022, 14(13):2599.
[32] HOLT S, MIKS M H, DE CARVALHO B T, et al.The molecular biology of fruity and floral aromas in beer and other alcoholic beverages[J].FEMS Microbiology Reviews, 2019, 43(3):193-222.
[33] 李萍. 啤酒中嘌呤类物质的检测[J].中国食品工业, 2022(8):89-92.LI P.Detection of purines in beer[J].China Food Industry, 2022(8):89-92.
[34] 杨祥根, 密招顺.啤酒中嘌呤类物质的检测[J].啤酒科技, 2013(12):51-53.YANG X G, MI Z S.Detection of purines in beer[J].Beer Science and Technology, 2013(12):51-53.
[35] VALERO M.Clarification of pomegranate juice at industrial scale[J].Journal of Food Processing &Technology, 2014, 5(5):1000324.
[36] 廖剑桥, 雷宏杰, 黄豪, 等.碱性和支链氨基酸对啤酒高浓酿造酵母发酵性能的影响[J].中国酿造, 2020, 39(5):44-48.LIAO J Q, LEI H J, HUANG H, et al.Effect of alkaline and branched chain amino acids on fermentation performance of yeast during beer high gravity brewing[J].China Brewing, 2020, 39(5):44-48.