谷氨酰胺转氨酶(EC 2.3.2.13 transglutaminase,TGase)能够催化蛋白质谷氨酰胺残基与不同酰基受体之间形成ε-(γ-谷氨酸)异肽键[1],从而实现蛋白质的交联或通过小分子进行修饰[2]。微生物来源的TGase最初从茂原链霉菌(Streptomyces mobaraensis)中分离,相较于动植物来源的酶,其具有不依赖Ca2+、生产成本低等显著优势[1]。因此,S.mobaraensis的发酵成为商业TGase的主要来源。目前,TGase已广泛应用于肉类、乳制品和豆制品等蛋白基食品的质地改良[3],并在抗体-药物偶联[4]、组织工程[5]和蛋白质聚乙二醇化[6]等领域展现出广阔的应用前景。然而,野生型S.mobaraensis来源的TGase在高温条件下的稳定性较差,其在50、60 ℃的半衰期分别仅为41.8、2 min。在实际应用中,TGase常暴露于高温环境,例如牛肉凝胶的生产需在60 ℃进行[7],而豆腐加工中的交联反应需在50 ℃进行[8]。因此,开发高效、热稳定的TGase对于其工业应用具有重要意义。
目前,随机突变和半理性设计已被用于提高S.mobaraensis来源TGase的热稳定性。通过随机突变和组合突变,研究人员获得了热稳定突变体TGm1(S2P-S23V-Y24 N-S199A-K294L),其在60 ℃的半衰期达到24.3 min,是野生型的11.2倍[9];此外,基于理性设计,本研究通过脯氨酸扫描结合折叠能量分析构建了TGm2(S2P-S23V-Y24 N-E28T-S199A-A265P-A287P-K294L),其在60 ℃的半衰期达到66.87 min,比酶活力也较野生型提高了1.9倍(71.81 U/mg)[10]。在TGm2的基础上,再通过对远离底物结合口袋的柔性区域进行虚拟饱和突变获得TGm2A(FRAPD-TGm2-S116A-S179L),其在60 ℃下半衰期和比酶活力分别达到132.38 min和79.15 U/mg[11]。值得注意的是,上述热稳定突变体均在大肠杆菌(Escherichia coli)中表达,其安全性和生产效率仍有待进一步提升。
除了大肠杆菌,S.mobaraensis来源的TGase已在多种宿主中表达,包括变铅青链霉菌(Streptomyces lividans)[12]、乳酸乳球菌(Lactococcus lactis)[13]、枯草芽孢杆菌(Bacillus subtilis)[14]、毕赤酵母(Komagataella phaffii)[15]。在S.mobaraensis中,TGase以前体酶的形式合成,通过内源蛋白酶去除N端前体区域后转化为活性酶[16]。研究表明,成熟TGase区域的正确折叠依赖于前体区域,该区域还可通过抑制TGase活力降低细胞毒性[17]。然而,上述异源宿主中的TGase产量较低或以胞内蛋白形式存在。近年来,通过诱变育种和基因拷贝数优化,S.mobaraensis的TGase产量已提高至40 U/mL[18]。此外,S.mobaraensis是目前唯一被批准用于生产食品级TGase的菌株,相较于其他宿主,其在TGase生产中仍具显著竞争力。
前期研究对S.mobaraensis DSM40587进行常压室温等离子体(atmospheric and room temperature plasma,ARTP)诱变,产生 TGase 产生改善的突变菌株(smY2022);在此基础上,用 TGm2 替换了smY2022基因组中野生型TGase基因,所得重组菌胞外酶活力达61.7U/mL[19]。在本研究中,将热稳定性更好的TGm2A表达于smY2022Δtg,通过启动子工程和增加基因拷贝数等策略进一步提高其表达水平,并评估了重组酶的酶学性质和蛋白质交联性能。研究结果将有助于进一步推动TGase的工业化生产和应用。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与质粒
E.coli JM109用于基因克隆。E.coli ET12567/pUZ8002(Invitrogen,Carlsbad,USA)用于链霉菌接合转移[19]。S.mobaraensis TGase基因缺失菌株smY2022Δtg用于TGase表达。质粒pUC19和pET-28a(+)用作基因克隆。pUC-TGm2A是pUC19的衍生质粒,编码TGm2A基因(链霉菌密码子偏好性);pET-28a(+)-Promoters是pET-28a(+)的衍生质粒,编码启动子PrpsL、PkasO*、PermE*、PSP44和Pgapdh[20];TGm2A基因及启动子基因均由生工生物工程(上海)股份有限公司构建。质粒pSET152用于S.mobaraensis基因整合。质粒pCRISPomyces-2编码CRISPR/Cas9系统[21],用于S.mobaraensis基因整合。
1.1.2 主要试剂
高保真DNA聚合酶、一步克隆连接试剂盒,南京诺唯赞生物科技股份有限公司;质粒提取试剂盒、柱回收试剂盒、氯霉素、卡那霉素、安普霉素和氨苄青霉素,生工生物工程(上海)股份有限公司;大肠杆菌感受态细胞制备试剂盒、RNA提取试剂盒、反转录试剂盒和荧光PCR试剂盒,宝生物工程(大连)有限公司;蛋白Marker、蛋白电泳 Loading buffer、Bis-Tris 预制凝胶,赛默飞世尔科技(中国)有限公司;Bradford 蛋白浓度测定试剂盒,上海碧云天生物技术有限公司;酪蛋白,上海麦克林生化科技股份有限公司;PrePack SP Purose 6 Fast Flow阳离子交换柱,嘉兴千纯生物科技有限公司;其他生物学试剂均购自国药集团化学试剂公司。
1.1.3 培养基及缓冲液
LB培养基(g/L):酵母提取物 5,蛋白胨 10,NaCl 5,pH 7.0。固体培养基中添加1.5%~2%质量分数的琼脂。
GYM(glucose yeast malt)琼脂培养基(g/L):葡萄糖10,酵母粉4,麦芽粉3,琼脂粉20。
MS(murashige and skoog)琼脂培养基(g/L):甘露醇20,麦芽提取物2.5,大豆粉20,琼脂20;50 mmol/L MgCl。
种子培养基(g/L):甘油20,酵母粉5,胰蛋白胨20,K2HPO4 4,MgSO4 2,pH 7.2。
发酵培养基(g/L):甘油20,鱼粉蛋白胨25,酵母粉5,玉米浆粉5.5,(NH4)2SO4 5.5,K2HPO4 2,MgSO4 2,pH 7.2~7.4。
1.2 仪器与设备
AKTA 蛋白纯化仪,美国 GE Healthcare 公司;台式高速冷冻离心机,德国 Eppendorf 公司;Light Cycler 480 荧光定量PCR仪,瑞士罗氏公司;国产PCR仪,杭州博日科技。
1.3 实验方法
1.3.1 质粒构建
基于pSET152构建含有不同启动子的TGm2A整合表达质粒。用引物对rpsL-F/rpsL-R、kasO*-F/kasO*-R、ermE*-F/ermE*-R、SP44-F/SP44-R和gapdh-F/gapdh-R分别从pET-28a(+)-Promoters扩增启动子PrpsL、PkasO*、PermE*、PSP44和Pgapdh基因片段。通过引物对TGm2A-F/TGm2A-R从pUC-TGm2A扩增TGm2A基因片段。用引物smY2022-2-F/smY2022-2-R从smY2022基因组扩增启动子PsmY2022-2基因片段。用引物对zai-F/zai-R扩增pSET152质粒骨架片段。基于一步克隆试剂盒,将上述不同启动子、TGm2A编码基因和pSET152质粒骨架片段连接,获得含有不同启动子的TGm2A的整合质粒。通过引物对smY2022-F1/smY2022-R1和gapdh-F1/gapdh-R1分别从smY2022基因组和pET-28a(+)-Promoters扩增PsmY2022-2和Pgapdh基因片段,并与用引物对zai-F/zai-R从上述pSET152衍生质粒扩增含有TGm2A的pSET152质粒骨架片段连接,获得含融合启动子PsmY2022-2/gapdh的TGm2A整合表达质粒pSET152-PsmY2022-2/gapdh-TGm2A。类似地,通过smY2022-F2/smY2022-R2和gapdh-F2/gapdh-R2进行PCR扩增及基因克隆,构建得到含融合启动子Pgapdh/smY2022-2的TGm2A整合表达质粒pSET152-Pgapdh/smY2022-2-TGm2A。
基于pCRISPomyces-2构建attB整合质粒。使用CRISPOR(https://crispor.gi.ucsc.edu/)设计靶向smY2022Δtg TGase基因位点的sgRNA序列,并合成对应的引物对sgtg-F/sgtg-R。通过单链退火,形成带有黏性末端的双链sgRNA片段。将该双链sgRNA片段与经限制性内切酶Bbs Ⅰ切割后的pCRISPomyces-2连接,构建得到含有sgRNA的质粒pCRISPR-sgtg。以smY2022基因组为模板,通过引物tg-FF/tg-FR和tg-RF/tg-RR分别扩增融合attB(34 bp)的TGase基因上游L1000(1 kb)及下游同源臂R1000(1 kb)。同时,通过一步克隆试剂盒将L1000和R1000与经Xba Ⅰ切割的pCRISPR-sgtg连接,构建得到在TGase基因位点整合attB基因的质粒pCRISPR-attB。
上述质粒构建过程中所涉及引物序列如表1所示。
表1 本研究使用的引物序列
Table 1 Primers used in this study
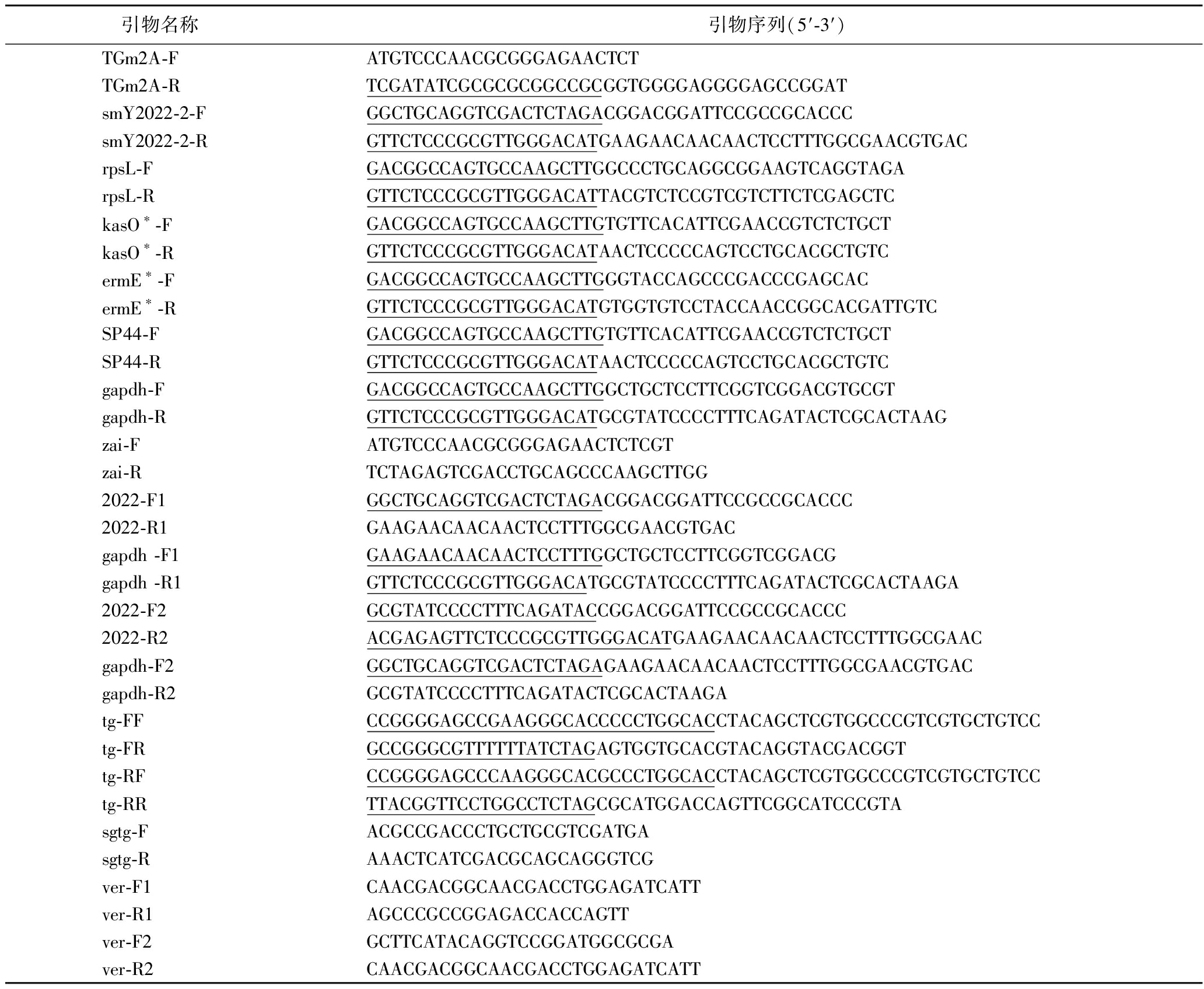
引物名称 引物序列(5′-3′)TGm2A-FATGTCCCAACGCGGGAGAACTCTTGm2A-RTCGATATCGCGCGCGGCCGCGGTGGGGAGGGGAGCCGGATsmY2022-2-FGGCTGCAGGTCGACTCTAGACGGACGGATTCCGCCGCACCCsmY2022-2-RGTTCTCCCGCGTTGGGACATGAAGAACAACAACTCCTTTGGCGAACGTGACrpsL-FGACGGCCAGTGCCAAGCTTGGCCCTGCAGGCGGAAGTCAGGTAGArpsL-RGTTCTCCCGCGTTGGGACATTACGTCTCCGTCGTCTTCTCGAGCTCkasO∗-FGACGGCCAGTGCCAAGCTTGTGTTCACATTCGAACCGTCTCTGCTkasO∗-RGTTCTCCCGCGTTGGGACATAACTCCCCCAGTCCTGCACGCTGTCermE∗-FGACGGCCAGTGCCAAGCTTGGGTACCAGCCCGACCCGAGCACermE∗-RGTTCTCCCGCGTTGGGACATGTGGTGTCCTACCAACCGGCACGATTGTCSP44-FGACGGCCAGTGCCAAGCTTGTGTTCACATTCGAACCGTCTCTGCTSP44-RGTTCTCCCGCGTTGGGACATAACTCCCCCAGTCCTGCACGCTGTCgapdh-FGACGGCCAGTGCCAAGCTTGGCTGCTCCTTCGGTCGGACGTGCGTgapdh-RGTTCTCCCGCGTTGGGACATGCGTATCCCCTTTCAGATACTCGCACTAAGzai-FATGTCCCAACGCGGGAGAACTCTCGTzai-RTCTAGAGTCGACCTGCAGCCCAAGCTTGG2022-F1GGCTGCAGGTCGACTCTAGACGGACGGATTCCGCCGCACCC2022-R1GAAGAACAACAACTCCTTTGGCGAACGTGACgapdh -F1GAAGAACAACAACTCCTTTGGCTGCTCCTTCGGTCGGACGgapdh -R1GTTCTCCCGCGTTGGGACATGCGTATCCCCTTTCAGATACTCGCACTAAGA2022-F2GCGTATCCCCTTTCAGATACCGGACGGATTCCGCCGCACCC2022-R2 ACGAGAGTTCTCCCGCGTTGGGACATGAAGAACAACAACTCCTTTGGCGAACgapdh-F2GGCTGCAGGTCGACTCTAGAGAAGAACAACAACTCCTTTGGCGAACGTGACgapdh-R2GCGTATCCCCTTTCAGATACTCGCACTAAGAtg-FFCCGGGGAGCCGAAGGGCACCCCCTGGCACCTACAGCTCGTGGCCCGTCGTGCTGTCCtg-FRGCCGGGCGTTTTTTATCTAGAGTGGTGCACGTACAGGTACGACGGTtg-RFCCGGGGAGCCCAAGGGCACGCCCTGGCACCTACAGCTCGTGGCCCGTCGTGCTGTCCtg-RRTTACGGTTCCTGGCCTCTAGCGCATGGACCAGTTCGGCATCCCGTAsgtg-FACGCCGACCCTGCTGCGTCGATGAsgtg-RAAACTCATCGACGCAGCAGGGTCGver-F1CAACGACGGCAACGACCTGGAGATCATTver-R1AGCCCGCCGGAGACCACCAGTTver-F2GCTTCATACAGGTCCGGATGGCGCGAver-R2CAACGACGGCAACGACCTGGAGATCATT
注:Gibson组装的同源序列用下划线突出显示。
1.3.2 S.mobaraensis转化
TGm2A整合表达质粒或attB整合质粒被分别转化至非甲基化的E.coli ET12567/pUZ8002中。在含有25 μg/mL氯霉素、50 μg/mL卡那霉素和100 μg/mL氨苄青霉素的LB培养基中于37 ℃培养2 h后,收集重组E.coli并与在50 ℃预热10 min的smY2022Δtg孢子悬浮液混合。将悬浮液涂布在MS琼脂培养基上,于30 ℃下培养16 h。最后,使用添加有10 μg/mL的安普霉素(apramycin,Apr)GYM琼脂培养基培养7~9 d。通过PCR验证和基因测序分析筛选出阳性转化子。其中,引物对ver-F2/ver-R2用于验证在TGase基因位点整合attB或TGm2A基因的转化子,ver-F1/ver-R1用于验证在attB基因位点整合TGm2A基因的转化子。
1.3.3 重组S.mobaraensis 摇瓶发酵
将S.mobaraensis阳性转化子接种于GYM平板,于30 ℃培养5~7 d。待菌落形成后,刮取孢子和菌丝,接种至含有30 mL种子培养基的250 mL摇瓶中,在30 ℃、220 r/min的条件下培养24 h。随后,以8%(体积分数)的接种量将种子液转接至含有30 mL发酵培养基的250 mL摇瓶中,置于30 ℃、220 r/min的摇床中进行发酵培养。培养期间,每隔12 h取样1次,共计培养96 h。取样后,将样品置于4 ℃、10 000 r/min的条件下离心10 min,收集上清液,用于后续分析。
1.3.4 蛋白纯化
利用PrePack SP Sepharose 6 Fast Flow阳离子交换柱,从S.mobaraensis发酵上清液中纯化野生型TGase或TGm2A [22]。首先,将发酵上清液与-20 ℃预冷的无水乙醇按3∶7体积比混合,置于4 ℃冰箱中静置30 min。随后,以10 000 r/min的转速离心10 min,收集蛋白沉淀。将沉淀溶解于50 mmol/L(pH 5.5)的乙酸盐缓冲液中,并使用0.2 μm针头式过滤器进行过滤,以去除杂质和颗粒。将过滤后的酶溶液以2 mL/min的流速加载至阳离子交换柱中。首先,用20 mL A液(50 mmol/L 乙酸-乙酸钠缓冲液,pH 5.5)平衡层析柱;接着,用10%(体积分数)B液(50 mmol/L 乙酸-乙酸钠缓冲液,pH 5.5;150 mmol/L NaCl)进行除杂处理,持续30 min;最后,用60%(体积分数)B液进行洗脱,收集目标蛋白。纯化后的蛋白溶液进一步通过10 kDa 超滤管进行脱盐处理,以去除盐等小分子杂质,得到高纯度的目标蛋白。
1.3.5 酶学性质测定
酶60 ℃半衰期测定方法如下:将纯化后的酶用50 mmol/L、pH 8.0的Tris-HCl缓冲液稀释至0.4~0.6 mg/mL,置于60 ℃恒温条件下孵育120 min。在孵育过程中,于特定时间点取样,并测定样品的TGase活力。残活性计算如公式(1)所示:
残余酶活力![]()
(1)
随后,利用Origin 2019软件中的ExpDec1函数对数据进行指数曲线拟合,通过拟合公式计算酶活力降至初始值50%时所需的时间(t1/2),以此确定酶的半衰期。为确定酶的最适反应温度,将野生型TGase和突变体TGm2A分别用50 mmol/L、pH 8.0的Tris-HCl缓冲液稀释至0.5 mg/mL,分别在37~70 ℃测定其相对酶活力。为确定酶的最适反应pH值,重组菌发酵上清液经过乙醇沉淀和冷冻干燥处理后制备成酶粉,并溶解于pH 3.5~8.0的50 mmol/L Tris-HCl缓冲液中。随后,将不同pH值的酶溶液分别加入对应pH值的底物中,在37 ℃下启动TGase反应,通过测定不同pH条件下的酶活力。
1.3.6 蛋白质交联分析
本实验以酪蛋白为底物,研究野生型TGase及TGm2A蛋白质交联能力。将酪蛋白溶解于100 mmol/L、pH 7.0的醋酸缓冲液中,使其终质量浓度为3 mg/mL,向上述各蛋白质溶液中加入纯化的酶液(终质量浓度为0.02 mg/mL),并在70 ℃恒温水浴中进行40 min的蛋白质交联反应。在反应过程中,分别于5、10、20、40 min取样,将样品与8 mol/L尿素按3∶1体积比混合后,进行SDS-PAGE分析。
1.3.7 TGase酶活力测定
本实验采用比色法测定TGase的活力,以N-CBZ-Gln-Gly和羟胺为底物[23]。具体操作如下:取150 μL底物溶液置于37 ℃金属浴中预热10 min,随后加入60 μL发酵上清液,混合均匀后在37 ℃下反应10 min。反应结束后,加入60 μL终止试剂,并在525 nm处测定吸光度。TGase酶活力单位定义为:在37 ℃下,每分钟催化生成1 μmol L-谷氨酸-γ-单羟肟酸所需的酶量。
1.3.8 蛋白质分析
本实验采用Bradford蛋白定量试剂盒测定蛋白浓度。取30 μL发酵上清液与10 μL 5×Loading Buffer混合均匀后,置于98 ℃加热10 min,备用。随后,使用10% SDS-PAGE凝胶在120 V电压下运行60 min分离蛋白。染色步骤采用X-Strain SDS-PAGE极速染色液进行染色。以SeeBlue Plus2预染蛋白标准(3~198 kDa)作为蛋白质标准分子。
1.3.9 实时荧光定量PCR
取1 mL发酵至36 h的发酵液样品,于4 ℃冷冻离心机中以1 000 r/min离心10 min,收集菌体备用。按照 MiniBEST Plant RNA Extraction Kit试剂盒说明书提取RNA,并检测其浓度。随后,使用PrimeScriptTM RT试剂盒将RNA逆转录为cDNA。最后,在Light Cycler 480系统中,采用SYBR Green Ⅰ嵌合荧光法进行实时荧光定量PCR分析。以S.mobaraensis基因组中的hrdB基因为内参基因,通过2-ΔΔCt法计算不同样品中目标基因的相对表达倍数变化。
2 结果与分析
2.1 启动子筛选提高TGm2A的表达
启动子是影响重组蛋白表达的关键因素,研究者已经挖掘或者改造多个链霉菌强启动子。其中,红霉素抗性基因启动子PermE应用最为广泛为组成型强启动子[24]。此外,PkasO*和PSP44[25]是在天蓝色链霉菌SARP型调节因子启动子PkasO基础上改造得到的强启动子。Pgapdh和PrpsL是分别来源于灰色链霉菌中高转录水平的甘油醛-3-磷酸脱氢酶和30S核糖体蛋白S12(rpsL)基因的启动子[26]。为了提高TGm2A的产量,本研究将PrpsL、PkasO*、PermE*、PSP44和Pgapdh 5种启动子,以及来自链霉菌smY2022的内源性启动子PsmY2022-2[27],分别融合至TGm2A基因的上游,并通过pSET152质粒整合至smY2022Δtg中attB基因位点(图1-a)。对所得重组S.mobaraensis进行摇瓶发酵,取发酵60 h的上清液进行TGase酶活力及SDS-PAGE分析。
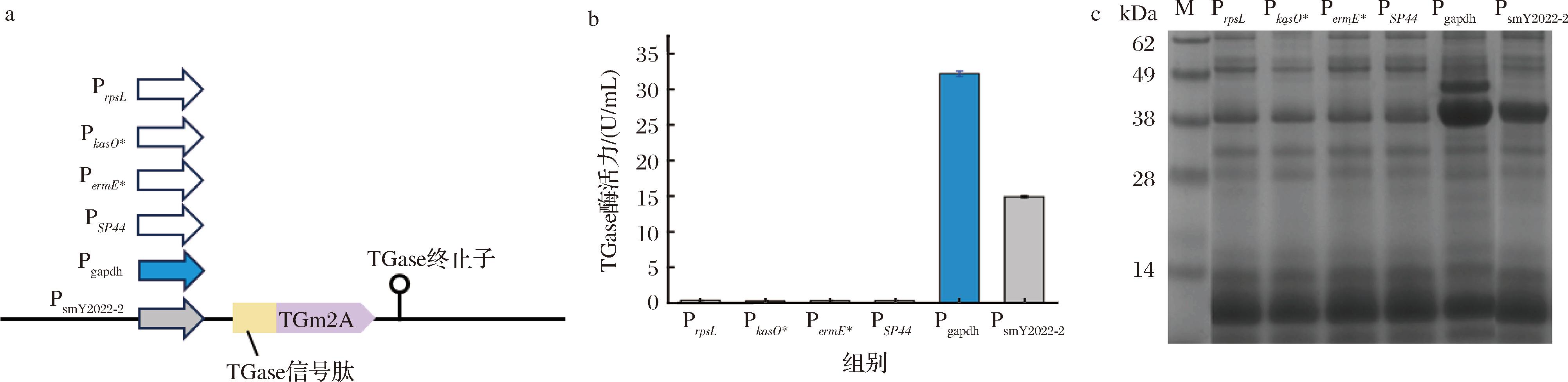
M为蛋白标准分子质量(Markeer,下同)。
a-TGm2A表达框结构;b-发酵上清液的TGase活力;c-发酵上清液SDS-PAGE分析
图1 启动子替换对TGm2A表达的影响
Fig.1 The effect of promoter substitution on the TGase expression
如图1-b所示,在Pgapdh和PsmY2022-2启动子的作用下,胞外TGase酶活力分别达到31.48、15.10 U/mL,而利用其他4种启动子的菌株均未在胞外检测到TGase活力(图1-b)。SDS-PAGE分析表明,采用Pgapdh和PsmY2022-2的菌株上清液呈现明显的TGm2A蛋白条带(38 kDa),且前者的条带更粗(图1-c)。因此,Pgapdh能有效提升TGm2A在S.mobaraensis中的表达水平。
2.2 启动子改造提高TGm2A的表达
串联启动子已被证明可以显著提高基因表达水平和蛋白质产量,并广泛应用于B.subtilis[28]、E.coli[29]、酿酒酵母[30]和K.phaffii[31]。在链霉菌中也有应用,TAO等[32]构建了一个诱导型启动子Ptip和组成型启动子PermE*的双启动子表达系统,用于磷脂酶D在S.lividans 中表达。为了提高TGm2A的表达水平,将高活性启动子Pgapdh与PsmY2022-2以不同顺序进行融合,分别得到串联启动子Pgapdh/smY2022-2和PsmY2022-2/gapdh(图2-a)。基于质粒pSET152将上述串联启动子表达框整合至smY2022Δtg的attB基因位点。对所得重组S.mobaraensis进行摇瓶发酵,取发酵上清液进行TGase酶活力及SDS-PAGE分析。
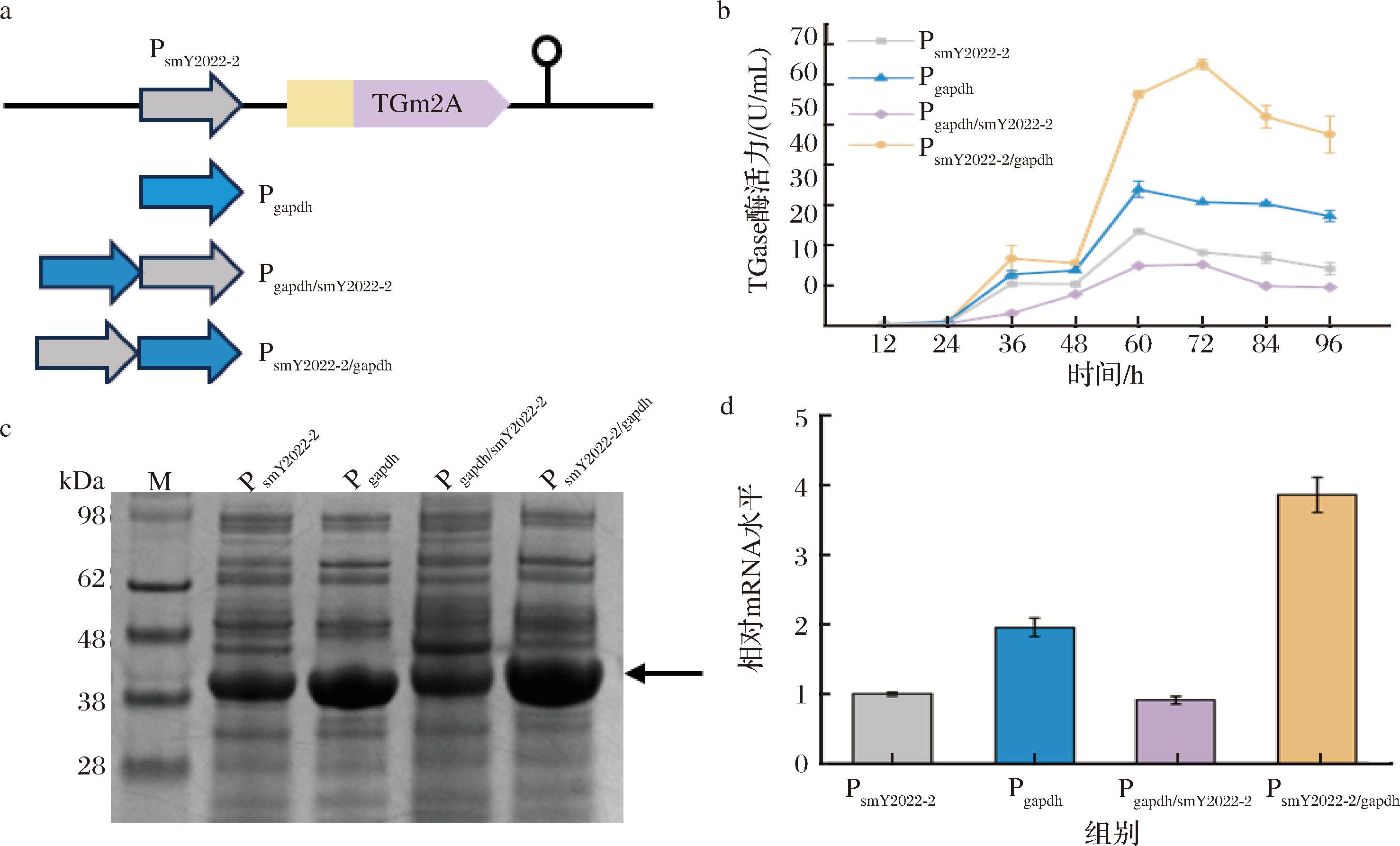
a-TGm2A表达框结构;b-发酵过程曲线;c-发酵上清液SDS-PAGE分析;d-TGm2A基因转录水平分析
图2 启动子串联对TGm2A表达量比较
Fig.2 The effect of promoter combination on the TGm2A expression
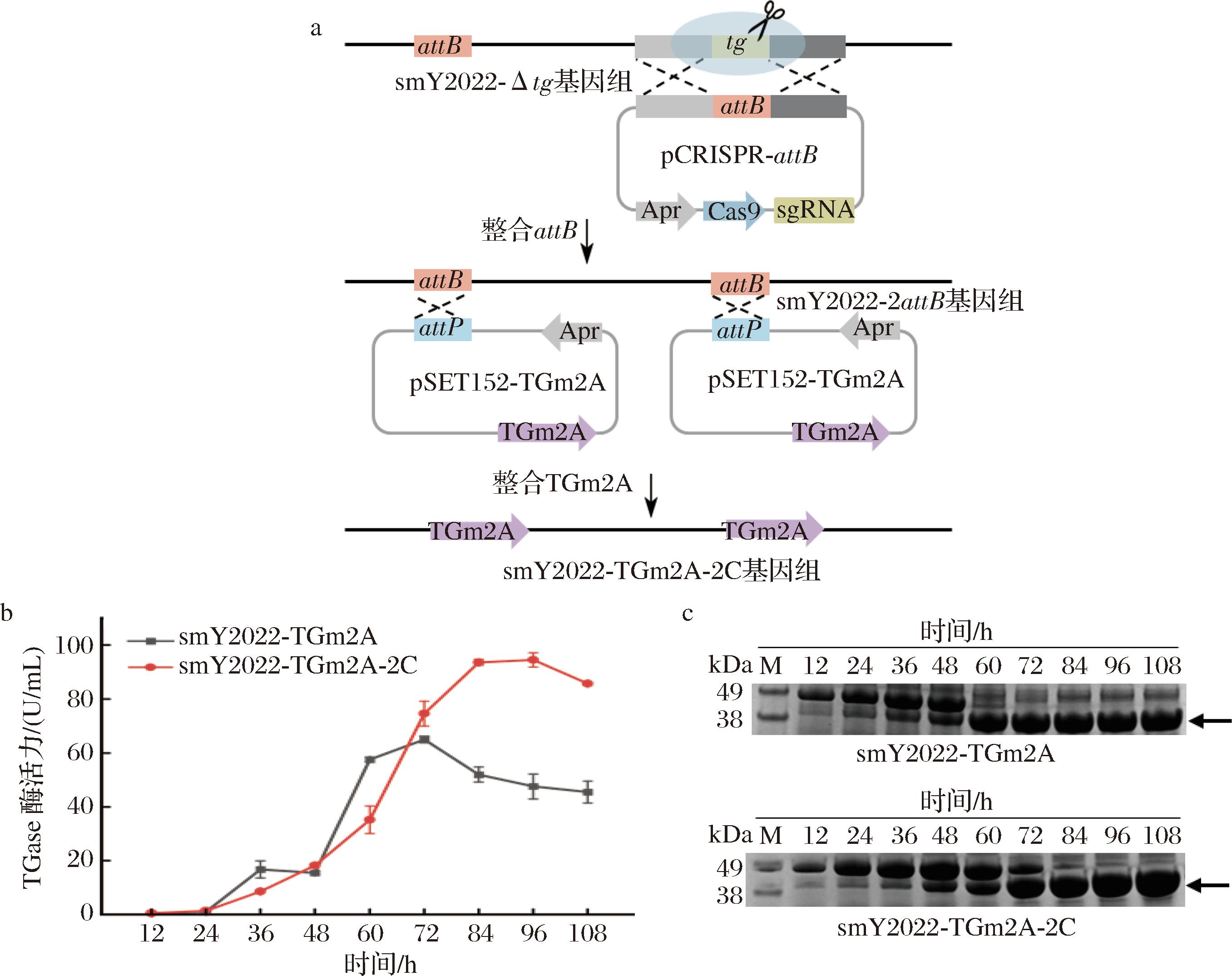
a-双拷贝菌株构建示意图;b-发酵过程曲线;c-发酵上清液的SDS-PAGE分析
图3 双位点整合对TGm2A表达的影响
Fig.3 The effect of double-site integration on the expression of TGm2A
结果表明,串联启动子PsmY2022-2/gapdh获得的TGase酶活力达到64.94 U/mL,分别是PsmY2022-2和Pgapdh的4.3倍和2.06倍(图2-b)。然而,Pgapdh/smY2022-2获得的TGase活性最低(图2-b)。SDS-PAGE分析表明,发酵60 h,PsmY2022-2/gapdh表达的TGm2A蛋白条带最粗,而Pgapdh/smY2022-2对应的蛋白条带最浅(图2-c)。上述结果,启动子串联能显著提高TGm2A的表达水平,启动子串连的顺序对其活性有重要影响。为进一步确认启动子强度,基于qRT-PCR分析了重组菌株发酵36 h胞内TGm2A的基因转录水平。如图2-d所示,各启动子对应的相对TGm2A mRNA水平差异与其表达差异基本一致。其中,PsmY2022-2/gapdh对应的相对mRNA水平分别是PsmY2022-2和Pgapdh的4.12倍和1.98倍(图2-d)。因此,串联启动子主要通过强化TGm2A基因转录水平来提高其表达量。
2.3 增加基因拷贝提高TGm2A的表达
研究表明,将多个基因拷贝整合到基因组中可以显著提高蛋白质产量[18]。在链霉菌中,位点特异性重组是最常用的整合方法。质粒pSET152中attP在整合酶的作用下,通过单交换特异性的整合到链霉菌基因组的attB位点[33],是目前链霉菌最高效的基因整合策略之一。然而,smY2022基因组中只有1个attB位点,限制了目的基因多拷贝整合。为实现TGm2A的多点整合表达,本研究利用CRISPR/Cas9系统在smY2022Δtg的TGase基因位点插入了额外的attB基因,然后通过质粒pSET152分别在2个attB位点整合采用串联启动子PsmY2022-2/gapdh的TGm2A表达框,得到重组菌smY2022-TGm2A-2C(图3-a)。将上述采用PsmY2022-2/gapdh启动子仅在smY2022Δtg天然attB位点整合表达TGm2A的菌株命名为smY2022-TGm2A。对重组S.mobaraensis进行摇瓶发酵,取发酵上清液进行TGase酶活力及SDS-PAGE分析。
发酵过程曲线如图3-b所示。在发酵前60 h,smY2022-TGm2A-2C胞外TGase酶活力略低于smY2022-TGm2A。在发酵72 h后,smY2022-TGm2A-2C的TGase酶活力超过smY2022-TGm2A,且酶活力快速升高,发酵84 h酶活力达到最大值(93.62 U/mL)(图3-b)。然而,smY2022-TGm2A则在在发酵72 h达到最大值(64.94 U/mL)。上述结果表明增加TGm2A基因拷贝数能有效提高其在S.mobaraensis中的表达水平。据研究所知,本研究构建的smY2022-TGm2A-2C是目前报道的TGase产量最高的菌株[19],将有力推进其工业化生产。
值得注意的是,smY2022-TGm2A-2C达到TGase酶活力最大值的时间点较smY2022-TGm2A推迟12 h。大量的研究表明,S.mobaraensis TGase以酶原形成合成,经内源蛋白酶的切割而转化活性的成熟酶。SDS-PAGE显示,smY2022-TGm2A-2C在发酵前72 h较smY2022-TGm2A形成了更多的酶原,在84 h基本转化为成熟酶(图3-c)。因此,smY2022-TGm2A-2C有限的活化蛋白酶可能不足以迅速切割其大量合成酶原,导致了TGase酶活力最高的延后。为进一步提高TGm2A的发酵效率,将在后期研究中过量表达其活化蛋白酶,从而加速酶原的活化效率。
2.4 TGm2A酶学性质分析
本研究利用阳离子交换柱成功纯化了来自野生型S.mobaraensis TGase和来自smY2022-TGm2A-2C的TGm2A(图4-a),并对纯化后的野生型TGase和TGm2A的最适温度、最适pH和半衰期进行了测定和比较。结果显示,TGm2A在60 ℃条件下处理60 min后,仍保留50%以上的酶活力,其60 ℃的半衰期达到120.36 min,是野生型TGase的100倍(图4-b)。此外,TGm2A的最适温度为60 ℃,比野生型TGase的最适温度高10 ℃(图4-c),并且纯化后的TGm2A和野生型TGase的相对酶活力分别为78.63 U/mg和24.52 U/mg。在pH 5~8,TGm2A和野生型TGase均保持较高的活力(图4-d)。上述结果表明,smY2022-TGm2A-2C表达的TGm2A具有良好的耐高温性能,明显优于野生型TGase。
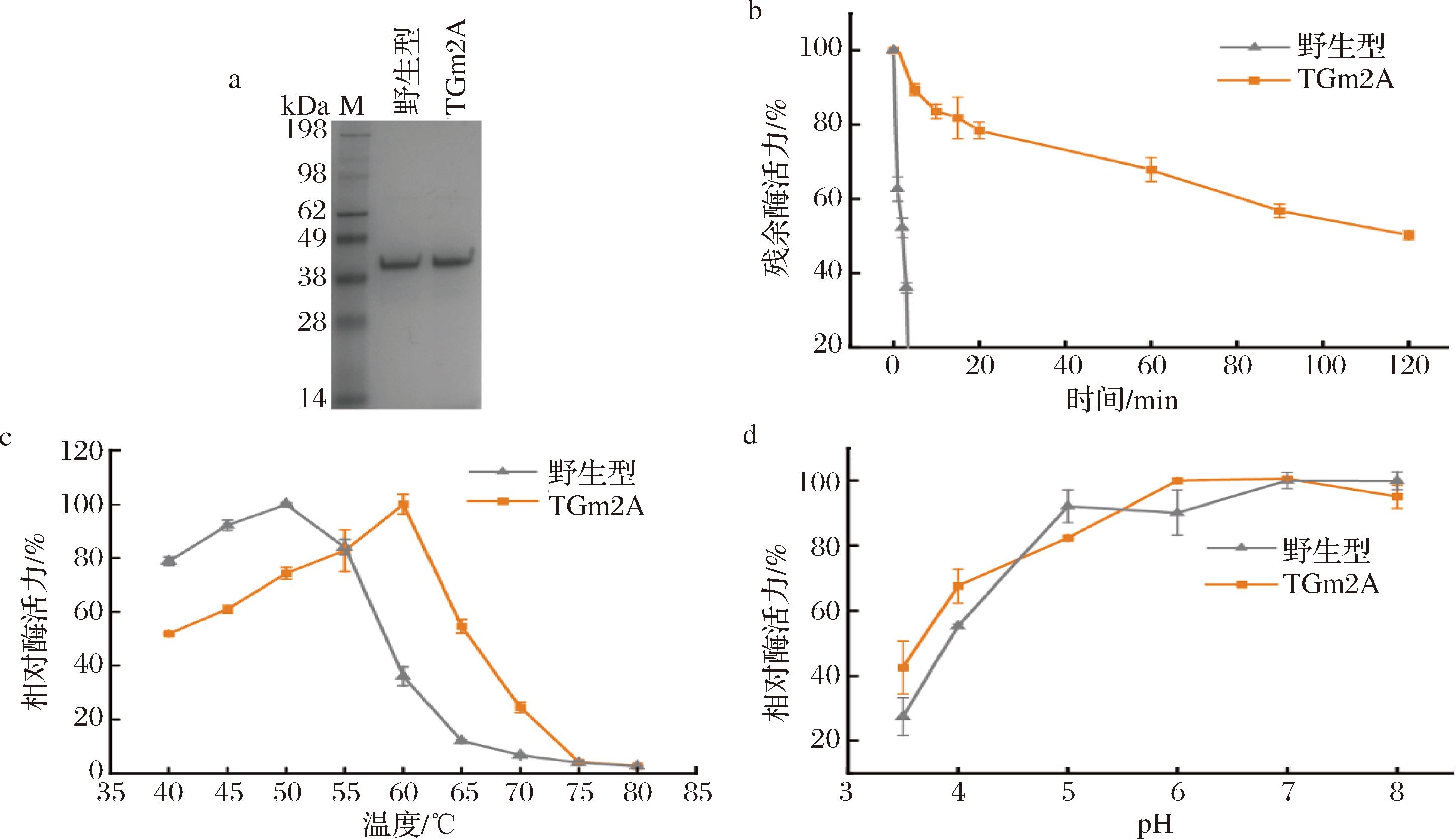
a-纯化酶SDS-PAGE分析;b-酶热稳定性分析;c-温度对酶活力的影响;d-pH对酶活力的影响
图4 TGm2A热稳定性及催化活性分析
Fig.4 The analysis on the thermal stability and catalytic activity of TGm2A
2.5 TGm2A高温条件下的蛋白交联能力分析
β-酪蛋白为测定TGase的蛋白质交联活性的常用蛋白[19]。为了比较TGm2A和野生型TGase在高温条件下的蛋白质交联潜力,将2种酶分别添加至β-酪蛋白溶液,在70 ℃下进行交联反应。通过SDS-PAGE分析β-酪蛋白交联反应过程。β-酪蛋白在加入TGm2A孵育5 min后条带开始明显变浅并且在蛋白胶加样口有大量蛋白质聚集,而加入野生型TGase后未发现交联现象(图5)。上述结果表明,TGm2A在高温条件下仍具备明显的蛋白交联活性,这将有助于其在牛肉凝胶和豆腐加工等高温环境中的应用。后续研究将采尺寸排阻色谱法来分析 TGm2A蛋白交联产物,以期进一步量化评估其蛋白交联性能。
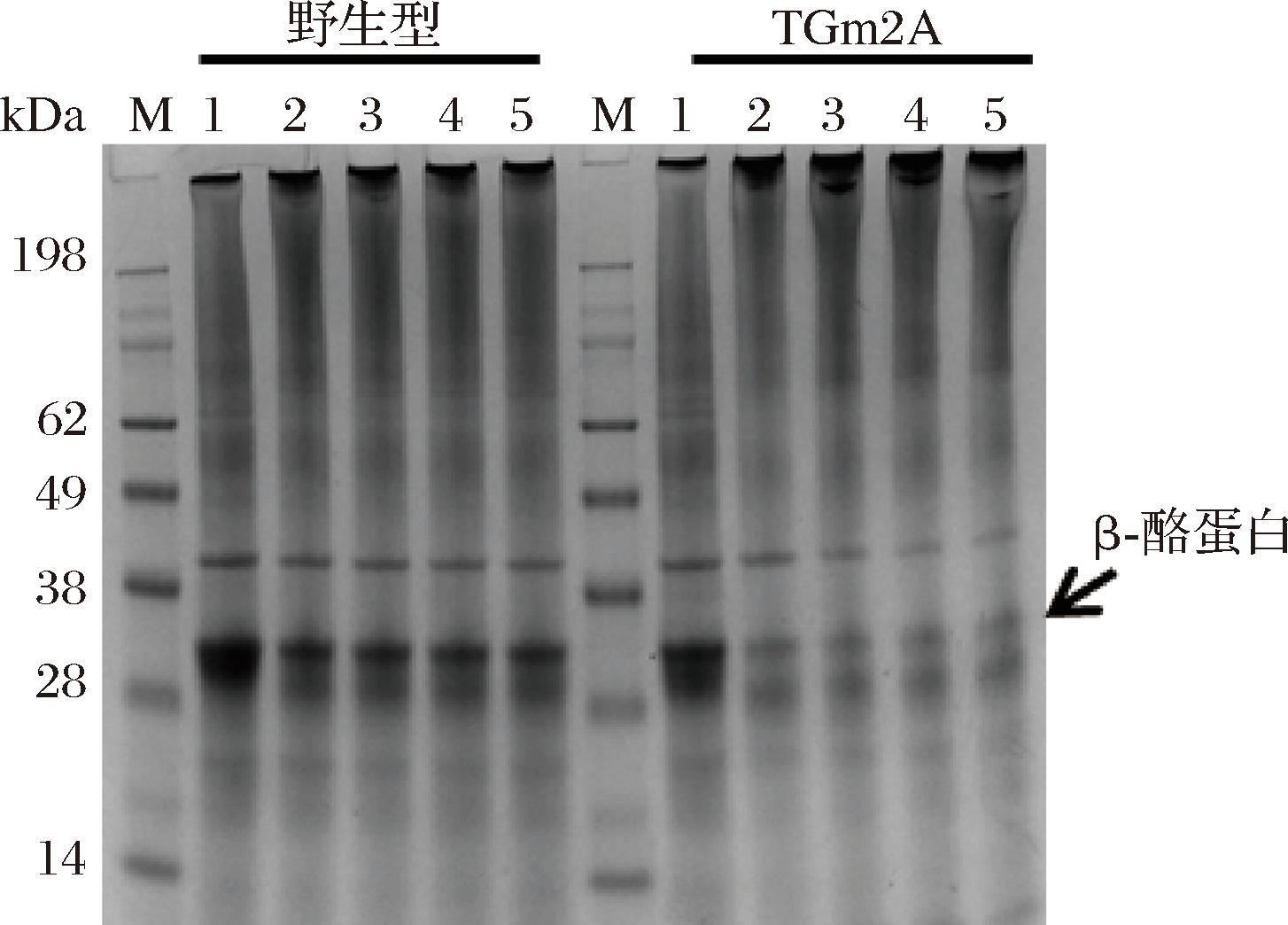
泳道1~5分别表示野生型TGase和TGm2A与酪蛋白在70 ℃反应0、5、10、20、40 min。
图5 SDS-PAGE分析在70 ℃的酶促蛋白质交联过程
Fig.5 SDS-PAGE analysis of the enzyme-mediated protein cross-linking at 70 ℃
3 结论
本研究通过启动子优化和基因拷贝数增加,显著提升了TGase在S.mobaraensis中的表达水平。启动子优化发现PsmY2022-2/gapdh串联启动子可使胞外TGase酶活力分别达到64.94 U/mL,显著优于其他启动子组合。进一步利用实现了TGm2A在S.mobaraensis双位点整合,构建的菌株smY2022-TGm2A-2C在发酵84 h后酶活力达到93.62 U/mL,成为目前报道的TGase产量最高的菌株。TGm2A在60 ℃条件下的半衰期长达120.36 min,是野生型的100倍,且最适温度为60 ℃,在pH 5~8保持较高活力。此外,TGm2A在70 ℃下对β-酪蛋白的交联能力显著优于野生型TGase,显示出优异的高温交联性能。这些结果不仅为TGase的工业化生产提供了高效的表达系统,还为其在高温食品加工等领域的应用奠定了基础,具有重要的科学和应用价值。
[1] SANTHI D,KALAIKANNAN A,MALAIRAJ P,et al.Application of microbial transglutaminase in meat foods:A review[J].Critical Reviews in Food Science and Nutrition 2017,57(10):2071-2076.
[2] AKBARI M,RAZAVI S H,KIELISZEK M.Recent advances in microbial transglutaminase biosynthesis and its application in the food industry[J].Trends in Food Science &Technology,2021,110:458-469.
[3] DUARTE L,MATTE C R,BIZARRO C V,et al.Review transglutaminases:Part Ⅱ-industrial applications in food,biotechnology,textiles and leather products[J].World Journal of Microbiology &Biotechnology,2019,36(1):11.
[4] NISHIOKA R,IIDA R,MINAMIHATA K,et al.Transglutaminase-mediated proximity labeling of a specific Lys residue in a native IgG antibody[J].Chemical Communications 2024,60(65):8545-8548.
[5] ![]() K,KNEZ Ž,LEITGEB M.Transglutaminase in foods and biotechnology[J].International Journal of Molecular Sciences,2023,24(15):12402.
K,KNEZ Ž,LEITGEB M.Transglutaminase in foods and biotechnology[J].International Journal of Molecular Sciences,2023,24(15):12402.
[6] DA SILVA FREITAS D,MERO A,PASUT G.Chemical and enzymatic site specific PEGylation of hGH[J].Bioconjugate Chemistry,2013,24(3):456-463.
[7] DONDERO M,FIGUEROA V,MORALES X,et al.Transglutaminase effects on gelation capacity of thermally induced beef protein gels[J].Food Chemistry,2006,99(3):546-554.
[8] LIU J,YANG S R,TANG R Y,et al.Enhanced tofu quality through calcium sulfate and transglutaminase treatment:Physicochemical properties and digestibility analysis[J].International Journal of Food Science and Technology,2024,59(10):7610-7618.
[9] BUETTNER K,HERTEL T C,PIETZSCH M.Increased thermostability of microbial transglutaminase by combination of several hot spots evolved by random and saturation mutagenesis[J].Amino Acids,2012,42(2-3):987-996.
[10] WANG X L,DU J H,ZHAO B C,et al.Significantly improving the thermostability and catalytic efficiency of Streptomyces mobaraenesis transglutaminase through combined rational design[J].Journal of Agricultural and Food Chemistry,2021,69(50):15268-15278.
[11] YANG P H,WANG X L,YE J C,et al.Enhanced thermostability and catalytic activity of Streptomyces mobaraenesis transglutaminase by rationally engineering its flexible regions[J].Journal of Agricultural and Food Chemistry,2023,71(16):6366-6375.
[12] NODA S,MIYAZAKI T,TANAKA T,et al.High-level production of mature active-form Streptomyces mobaraensis transglutaminase via pro-transglutaminase processing using Streptomyces lividans as a host[J].Biochemical Engineering Journal,2013,74:76-80.
[13] MA T G,LU J J,ZHU J,et al.The secretion of Streptomyces monbaraensis transglutaminase from Lactococcus lactis and immobilization on porous magnetic nanoparticles[J].Frontiers in Microbiology,2019,10:1675.
[14] WANG S T,YANG Z G,LI Z J,et al.Heterologous expression of recombinant transglutaminase in Bacillus subtilis SCK6 with optimized signal peptide and Codon,and its impact on gelatin properties[J].Journal of Microbiology and Biotechnology,2020,30(7):1082-1091.
[15] AQEEL S M,ABDULQADER A A,DU G C,et al.Integrated strategies for efficient production of Streptomyces mobaraensis transglutaminase in Komagataella phaffii[J].International Journal of Biological Macromolecules,2024,273:133113.
[16] ZOTZEL J,KELLER P,FUCHSBAUER H L.Transglutaminase from Streptomyces mobaraensis is activated by an endogenous metalloprotease[J].European Journal of Biochemistry,2003,270(15):3214-3222.
[17] JUETTNER N E,SCHMELZ S,ANDERL A,et al.The N-terminal peptide of the transglutaminase-activating metalloprotease inhibitor from Streptomyces mobaraensis accommodates both inhibition and glutamine cross-linking sites[J].The FEBS Journal,2020,287(4):708-720.
[18] YIN X Q,LI Y Y,ZHOU J W,et al.Enhanced production of transglutaminase in Streptomyces mobaraensis through random mutagenesis and site-directed genetic modification[J].Journal of Agricultural and Food Chemistry,2021,69(10):3144-3153.
[19] YE J C,YANG P H,ZHOU J W,et al.Efficient production of a thermostable mutant of transglutaminase by Streptomyces mobaraensis[J].Journal of Agricultural and Food Chemistry,2024,72(8):4207-4216.
[20] BAI C X,ZHANG Y,ZHAO X J,et al.Exploiting a precise design of universal synthetic modular regulatory elements to unlock the microbial natural products in Streptomyces[J].Proceedings of the National Academy of Sciences of the United States of America,2015,112(39):12181-12186.
[21] WANG Y,COBB R E,ZHAO H.High-efficiency genome editing of Streptomyces species by an engineered CRISPR/Cas system[J].Methods in Enzymology,2016,575:271-284.
[22] PASTERNACK R,DORSCH S,OTTERBACH J T,et al.Bacterial pro-transglutaminase from Streptoverticillium mobaraense:Purification,characterisation and sequence of the zymogen[J].European Journal of Biochemistry,1998,257(3):570-576.
[23] LIU S,WANG M,DU G C,et al.Improving the active expression of transglutaminase in Streptomyces lividans by promoter engineering and Codon optimization[J].BMC Biotechnology,2016,16(1):75.
[24] BIBB M J,JANSSEN G R,WARD J M.Cloning and analysis of the promoter region of the erythromycin resistance gene (ermE) of Streptomyces erythraeus[J].Gene,1985,38(1-3):215-226.
[25] MYRONOVSKYI M,LUZHETSKYY A.Native and engineered promoters in natural product discovery[J].Natural Product Reports,2016,33(8):1006-1019.
[26] SHAO Z Y,RAO G D,LI C,et al.Refactoring the silent spectinabilin gene cluster using a plug-and-play scaffold[J].ACS Synthetic Biology,2013,2(11):662-669.
[27] 叶佳才.耐热谷氨酰胺转氨酶在茂原链霉菌中的表达研究[D].无锡:江南大学,2024.YE J C.Expression of thermostable transglutaminase in Streptomyces mobaraensis[D].Wuxi:Jiangnan University,2024.
[28] YAO D B,HAN X D,GAO H H,et al.Enhanced extracellular production of raw starch-degrading α-amylase in Bacillus subtilis through expression regulatory element modification and fermentation optimization[J].Microbial Cell Factories,2023,22(1):118.
[29] LIU L Y,NING N Y,XU S M,et al.Double promoter and tandem gene strategy for efficiently expressing recombinant FGF21[J].Microbial Cell Factories,2024,23(1):171.
[30] WU Y J,FENG S,SUN Z A,et al.An outlook to sophisticated technologies and novel developments for metabolic regulation in the Saccharomyces cerevisiae expression system[J].Frontiers in Bioengineering and Biotechnology,2023,11:1249841.
[31] YADAV D,RANJAN B,MCHUNU N,et al.Enhancing the expression of recombinant small laccase in Pichia pastoris by a double promoter system and application in antibiotics degradation[J].Folia Microbiologica,2021,66(6):917-930.
[32] TAO H,ZHANG Y C,DENG Z X,et al.Strategies for enhancing the yield of the potent insecticide spinosad in Actinomycetes[J].Biotechnology Journal,2019,14(1):e1700769.
[33] SIOUD S,AIGLE B,KARRAY-REBAI I,et al.Integrative gene cloning and expression system for Streptomyces sp.US 24 and Streptomyces sp.TN 58 bioactive molecule producing strains[J].Journal of biomedicine &Biotechnology,2009(1):464986.