5-氨基乙酰丙酸(5-aminolevulinic acid,5-ALA)是一种非蛋白质氨基酸,广泛存在于植物、动物和微生物中,是血红素、叶绿素、维生素B12等四吡咯化合物生物合成的重要前体[1-2]。由于5-ALA具备良好的光动力学特性,并且具有高安全性(无残留和毒副作用)、良好的选择性、出色的渗透性,对动物无害,且能在环境中迅速降解等优点,使其在医药和农业等多个领域得到了广泛应用[3-5]。目前,工业上5-ALA的合成主要依赖化学合成法。然而,该方法存在步骤复杂、收率低、成本较高且对环境污染严重等问题,限制了其推广应用。近年来,随着生物技术的迅速发展,利用生物法合成5-ALA受到越来越多的关注。在生物体内,5-ALA的合成途径主要包括C4途径和C5途径[6]。C4途径以琥珀酰辅酶A和甘氨酸为底物,在5-氨基乙酰丙酸合酶(5-aminolevulinic acid synthase,ALAS)的作用下,利用5-磷酸吡哆醛为辅因子,一步催化生成5-ALA。相比之下,C5途径以谷氨酸为底物,经过谷氨酰tRNA合成酶、谷氨酰-tRNA-还原酶和谷氨酸-1-半醛氨基转移酶等多步酶促反应生成5-ALA,该过程依赖ATP、NADPH等辅因子,并与能量代谢、蛋白质合成和氧化还原状态紧密相关。由于C4途径只涉及一步反应,工艺优化和改造相对更为简便,因此成为研究重点。1996年,VAN DER WERF等[7]首次将类球红细菌的ALAS基因引入大肠杆菌(Escherichia coli),在外加前体物质的条件下,生成22 mmol/L的5-ALA,开启了异源5-ALA合成的研究。通过外源添加前体物质琥珀酸和甘氨酸,引入异源ALAS,是当前C4途径生物合成5-ALA的主流技术[8]。然而,C4途径也存在双底物添加带来的发酵工艺复杂性和生产成本增加等局限性。此外,甘氨酸对细胞具有毒害作用[2],这也为C4途径的改造带来了挑战。近年来,针对C4途径的研究不断取得突破。蒲苇等[9]通过敲除琥珀酸脱氢酶或琥珀酰CoA合成酶,成功建立了无需外源添加琥珀酸即可发酵生产5-ALA的重组E.coli体系,从而摆脱了现有技术对琥珀酸添加的依赖。此外,DING等[10]通过在利用C4途径的重组菌株中表达解除丝氨酸反馈抑制的serA基因,尝试加强丝氨酸到甘氨酸的代谢流量,实现甘氨酸的内源供给,并使5-ALA产量较对照组提升14%。ZOU等[11]在谷氨酸棒杆菌中采用类似策略,通过构建丝氨酸到甘氨酸的合成路径并强化glyA基因的表达,最终使5-ALA产量达到590 mg/L。REN等[12]基于逆向生物合成设计的碳骨架重构策略设计了从乙醛酸到甘氨酸的新型合成途径:通过引入异源乙醛酸转氨酶在胞内将乙醛酸转化为甘氨酸,强化aceA基因的表达并引入ALAS,最终5-ALA产量达到521 mg/L。同年,郑平等[13]也采用相似策略构建了高效、低成本的5-ALA生产菌株。
这些研究为改进C4途径、提升5-ALA生物合成效率提供了重要参考。虽然通过丝氨酸-甘氨酸代谢途径实现胞内甘氨酸供给已取得初步成果,但该途径通路长,且关键酶甘油醛-3-磷酸脱氢酶受到严格的反馈调控,导致代谢调控复杂,合成效率较低。因此,新的甘氨酸供给途径仍是目前研究的重点。而目前新型甘氨酸合成途径研究中菌株5-ALA产量仍然较低,不足以满足工业化需求。本研究在E.coli中引入异源谷氨酸乙醛酸氨基转移酶(glutamate aldehyde aminotransferase,GGAT)和ALAS,将谷氨酸转化为甘氨酸,并进一步与琥珀酰辅酶A合成5-ALA。并在此基础上,通过改造前体琥珀酸途径、5-ALA下游代谢途径及发酵优化等策略(图1),尝试构建更为高效的、无需外源添加甘氨酸的5-ALA代谢菌株。
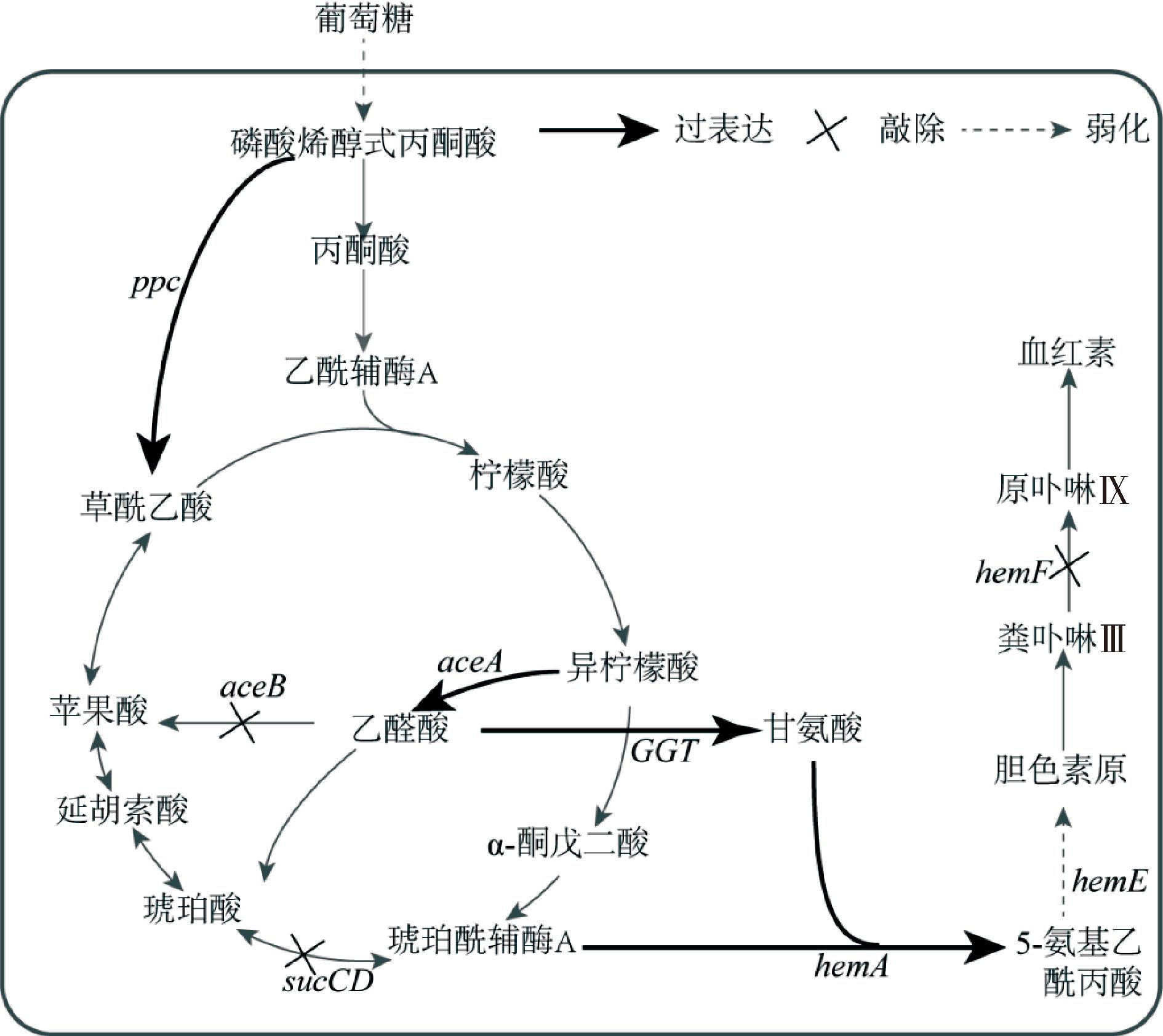
图1 C4途径5-ALA合成路径图及本研究主要策略
Fig.1 The C4 pathway for 5-ALA biosynthesis and key strategies in this study
注:ppc-编码磷酸烯醇式丙酮酸羧化酶基因;hemA-编码5-氨基乙酰丙酸合酶基因;sucCD-编码琥珀酰CoA合成酶基因;aceA-编码异柠檬酸裂解酶基因;aceB-编码苹果酸合酶基因;hemF-编码粪卟啉原脱羧酶基因。
1 材料与方法
1.1 材料与试剂
1.1.1 试剂
蛋白胨、酵母粉,Oxoid公司;各种无机盐,国药集团试剂有限公司;丹磺酰氯,上海麦克林生化科技股份有限公司;5-ALA,上海阿拉丁生化科技股份有限公司;质粒提取试剂盒、DNA产物纯化试剂盒、Phanta Flash Master Mix、ClonExpress Ultra One Step Cloning Kit V2,南京诺唯赞生物技术股份有限公司;GGAT酶联免疫分析试剂盒,江苏酶免实业有限公司。
1.1.2 培养基与缓冲液
LB(g/L):蛋白胨10,酵母粉5,氯化钠10。
2YT(g/L):蛋白胨12,酵母粉24,氯化钠5。
TB(g/L):蛋白胨12,酵母粉24,KH2PO4 2.313,K2HPO4 12.54。加入甘油 4 mL。
乳糖自诱导培养基(g/L):蛋白胨10,葡萄糖10,乳糖5,酵母粉5,25 mmol/L Na2HPO4,25 mmol/L KH2PO4,1 mmol/L MgSO4。
M9发酵培养基(g/L):Na2HPO4·12H2O 17.1,KH2PO4 3,NH4Cl 1 g/L,NaCl 0.5 g/L,酵母粉2,MgSO4 2 mmol/L,CaCl2 0.1 mmol/L,葡萄糖15,谷氨酸钠4,卡那霉素(Kanamycin,Kan)50 mg/L或氨苄青霉素(Ampicillin,Amp)100 mg/L,异丙基-β-D-硫代半乳糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG)终浓度为0.5 mmol/L。
1.1.3 菌株、质粒与引物
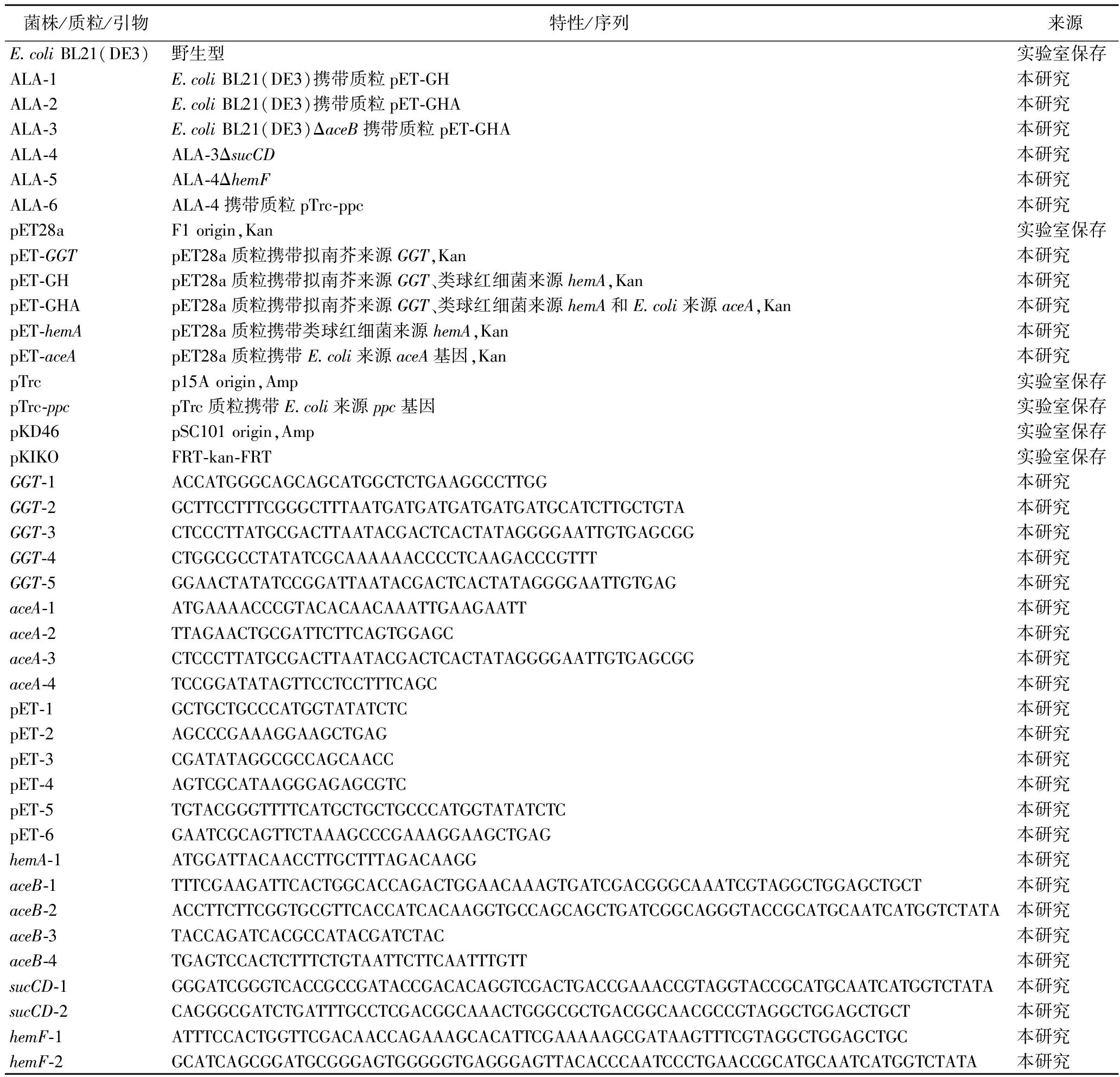
本研究所用菌株、质粒及引物如表1所示。
表1 本研究所用菌株、质粒及引物
Table 1 Strains,plasmids,and primers used in this study
菌株/质粒/引物特性/序列来源E.coli BL21(DE3)野生型实验室保存ALA-1E.coli BL21(DE3)携带质粒pET-GH本研究ALA-2E.coli BL21(DE3)携带质粒pET-GHA本研究ALA-3E.coli BL21(DE3)ΔaceB携带质粒pET-GHA本研究ALA-4ALA-3ΔsucCD本研究ALA-5ALA-4ΔhemF本研究ALA-6ALA-4携带质粒pTrc-ppc本研究pET28aF1 origin,Kan实验室保存pET-GGTpET28a质粒携带拟南芥来源GGT,Kan本研究pET-GHpET28a质粒携带拟南芥来源GGT、类球红细菌来源hemA,Kan本研究pET-GHApET28a质粒携带拟南芥来源GGT、类球红细菌来源hemA和E.coli来源aceA,Kan本研究pET-hemApET28a质粒携带类球红细菌来源hemA,Kan本研究pET-aceApET28a质粒携带E.coli来源aceA基因,Kan本研究pTrcp15A origin,Amp实验室保存pTrc-ppcpTrc质粒携带E.coli来源ppc基因实验室保存pKD46pSC101 origin,Amp实验室保存pKIKOFRT-kan-FRT实验室保存GGT-1ACCATGGGCAGCAGCATGGCTCTGAAGGCCTTGG本研究GGT-2GCTTCCTTTCGGGCTTTAATGATGATGATGATGATGCATCTTGCTGTA本研究GGT-3CTCCCTTATGCGACTTAATACGACTCACTATAGGGGAATTGTGAGCGG本研究GGT-4CTGGCGCCTATATCGCAAAAAACCCCTCAAGACCCGTTT本研究GGT-5GGAACTATATCCGGATTAATACGACTCACTATAGGGGAATTGTGAG本研究aceA-1ATGAAAACCCGTACACAACAAATTGAAGAATT本研究aceA-2TTAGAACTGCGATTCTTCAGTGGAGC本研究aceA-3CTCCCTTATGCGACTTAATACGACTCACTATAGGGGAATTGTGAGCGG本研究aceA-4TCCGGATATAGTTCCTCCTTTCAGC本研究pET-1GCTGCTGCCCATGGTATATCTC本研究pET-2AGCCCGAAAGGAAGCTGAG本研究pET-3CGATATAGGCGCCAGCAACC本研究pET-4AGTCGCATAAGGGAGAGCGTC本研究pET-5TGTACGGGTTTTCATGCTGCTGCCCATGGTATATCTC本研究pET-6GAATCGCAGTTCTAAAGCCCGAAAGGAAGCTGAG本研究hemA-1ATGGATTACAACCTTGCTTTAGACAAGG本研究aceB-1TTTCGAAGATTCACTGGCACCAGACTGGAACAAAGTGATCGACGGGCAAATCGTAGGCTGGAGCTGCT本研究aceB-2ACCTTCTTCGGTGCGTTCACCATCACAAGGTGCCAGCAGCTGATCGGCAGGGTACCGCATGCAATCATGGTCTATA本研究aceB-3TACCAGATCACGCCATACGATCTAC本研究aceB-4TGAGTCCACTCTTTCTGTAATTCTTCAATTTGTT本研究sucCD-1GGGATCGGGTCACCGCCGATACCGACACAGGTCGACTGACCGAAACCGTAGGTACCGCATGCAATCATGGTCTATA本研究sucCD-2CAGGGCGATCTGATTTGCCTCGACGGCAAACTGGGCGCTGACGGCAACGCCGTAGGCTGGAGCTGCT本研究hemF-1ATTTCCACTGGTTCGACAACCAGAAAGCACATTCGAAAAAGCGATAAGTTTCGTAGGCTGGAGCTGC本研究hemF-2GCATCAGCGGATGCGGGAGTGGGGGTGAGGGAGTTACACCCAATCCCTGAACCGCATGCAATCATGGTCTATA本研究
1.1.4 质粒与菌株构建
pET-GGT质粒构建:首先根据GGT基因序列以及pET28a质粒图谱分别设计引物GGT-1/GGT-2和pET-1/pET-2,具体序列如表1所示;以GGT基因片段为模板经PCR扩增后得到目的基因GGT片段,以pET28a质粒为模板经PCR后得到载体片段,将载体片段与目的片段回收纯化后同源重组。将同源重组得到的片段经热激法转化至E.coli JM109并涂布于含有Kan的LB固体培养基,于37 ℃下过夜培养。使用引物GGT-1/GGT-2对平板的单菌落进行菌落PCR验证,PCR鉴定阳性克隆并接种于含有Kan的液体LB中,过夜12 h后提取质粒测序,将正确的转化子保存。利用相同的方法构建其余质粒。
pET-GH质粒构建:以pET-hemA质粒为载体模板,设计引物pET-3/pET-4,以pET-GGT质粒为模板,设计引物GGT-3/GGT-4。使用以上质粒模板及引物分别进行PCR,得到相应的目的片段。经过胶回收、同源重组、转化后涂布在卡那抗性的平板上过夜培养。挑选阳性转化子接种于含有50 μg/mL卡那霉素的液体LB培养基中过夜培养,待12 h后提取质粒得到pET-GH。
pET-GHA质粒构建:根据异柠檬酸裂解酶基因序列设计引物aceA-1/aceA-2,根据pET28a质粒序列设计引物pET-5/pET-6,根据上述引物PCR构建质粒pET-aceA。以pET-aceA序列为模板设计引物aceA-3/aceA-4,以pET-GGT质粒为模板设计引物GGT-4/GGT-5,以pET-hemA质粒为模板设计引物pET-3/pET-4。分别使用以上引物及质粒按照前述方法构建质粒,质粒命名为pET-GHA。
Red同源重组敲除基因菌株构建方法以苹果酸合酶编码基因(aceB)敲除为例。根据苹果酸合酶基因序列设计引物aceB-1/aceB-2,以pKIKO质粒为模板进行PCR,将所得产物胶回收保存。将pKD46质粒转化至E.coli BL21(DE3)中,接种菌体于液体LB(100 μg/mL Amp)中,在30 ℃,200 r/min条件下过夜培养。转接种子液于相同抗性的2YT培养基中,并加入200 μL L-阿拉伯糖,在30 ℃,200 r/min条件下培养2 h至菌体OD600nm值达到0.5~0.8,4 ℃、4 000 r/min条件下离心10 min收集菌体弃上清液,然后分别用20 mL冰冷ddH2O清洗2次、40 mL冰冷10%(体积分数)甘油清洗3次,最后加入200 μL 10%甘油分装。向分装完毕的电转感受态中加入2 μL pKIKO片段,冰浴3 min后加入电转杯,设置电压2.5 kV 电转,电击后立即加入1 mL 2YT培养基,并放置在37 ℃摇床上培养1 h。后续结束后涂布在卡那霉素固体LB平板,在37 ℃恒温培养箱中过夜培养。挑取使用验证引物aceB-3/aceB-4对转化子及对照菌株菌落进行PCR,筛选正确转化子。将pCP20质粒转化至正确转化子中,消除卡那霉素抗性片段,最后将成功消除菌株在无抗LB平板上划线并培养至43 ℃下以消除pCP20质粒。
1.2 仪器与设备
Ultimate 3000高效液相色谱仪,美国ThermoFisher Scientific公司;V-5600PC紫外分光光度计,上海元析仪器有限公司;INFINITE E PLEX酶标仪,帝肯实验器材有限公司。
1.3 实验方法
1.3.1 GGAT活性检测方法
本研究表达的GGAT活性测定采用GGAT酶联免疫分析试剂盒检测。
1.3.2 5-ALA检测方法
200 μL稀释的发酵液加入100 μL乙酸钠缓冲液(pH 4.6),然后加入5 μL乙酰丙酮溶液,100 ℃水浴15 min,冷却至室温后加入等体积的Ehrlish’s试剂(42 mL冰醋酸,8 mL 70%高氯酸,1 g二甲氨基苯甲醛),显色10 min后测553 nm波长下的吸光度。
1.3.3 甘氨酸的检测方法[14]
柱前衍生:用移液枪分别吸取标准溶液和样品各1.0 mL于10 mL离心管中,分别加入5 g/L丹磺酰氯丙酮溶液1.0 mL,盖好后摇匀,于55 ℃下反应15 min取出,冷却至常温后,加入2.0 mL甲醇,摇匀、离心、取上清液过0.22 μm滤膜。
色谱柱:Diamonsil Plus C18-A(250 mm×4.6 mm,5 μm)。
流动相:V(醋酸钠缓冲液)∶V(乙腈)=75∶25;检测波长330 nm;流速1.0 mL/min;进样体积20 μL。
1.3.4 摇瓶发酵实验方法
将菌株接种LB液体培养基(根据需要添加100 mg/L Kan或50 mg/L Amp)中在37 ℃、200 r/min过夜培养,即为种子液。将种子液以1%接种量转接至50 mL M9发酵培养基(根据需要添加100 mg/L Kan或50 mg/L Amp),在37 ℃、200 r/min条件下培养2 h后加入0.5 mmol/L IPTG溶液,于25 ℃、200 r/min条件下发酵培养。
1.4 数据处理
本研究数据统计学分析采用Origin 2021软件完成。组间差异显著性通过双尾t检验进行定量评估。*表示P值介于0.01~0.05显著水平,**表示P值介于0.001~0.01显著水平,***表示P值<0.001显著水平。
2 结果与分析
2.1 GGAT的表达与酶活性验证
采用引物GGT-1/GGT-2对含有pET-GGT质粒的重组菌株进行PCR鉴定,成功检测到约1 500 bp的目的基因片段(图2),与GGT基因大小相符,表明质粒pET-GGT已成功构建。通过诱导重组菌株表达GGAT,并收集菌体进行超声破碎和离心,获得的上清液作为粗酶液进行下一步的分析。SDS-PAGE结果(图3)显示,与对照菌株相比,重组菌株在45~60 kDa出现一条明显的特异性条带,与GGAT的理论大小(约55 kDa)相符,表明拟南芥来源的GGAT酶能够在E.coli中正常表达。通过Ni-NTA重力柱对GGAT粗酶液进行纯化,SDS-PAGE分析显示(图4),随着洗脱液中咪唑浓度的增加,GGAT逐渐被洗脱:在100 mmol/L时仅有微量GGAT被洗脱,当浓度提升至200 mmol/L时,所有GGAT均被洗脱且未检测到其他蛋白杂质(图4)。纯化后的GGAT经超滤浓缩,最终蛋白质量浓度为1.999 mg/mL。为验证GGAT的活性,使用GGAT酶联免疫分析试剂盒进行测定。将试剂盒提供的GGAT标准品进行梯度稀释并按照说明书测定绘制标准曲线(图5),样品线性回归与预期浓度相关系数R2值为0.995 2以上,符合试剂盒使用标准(R2>0.95)。对纯化收集的GGAT样品进行测定,在OD450nm处测得结果为0.382 0,代入标准曲线可知GGAT样品酶活性为45.37 U/L。这表明拟南芥来源的GGAT在E.coli中得到了活性表达,为进一步构建代谢途径奠定了基础。
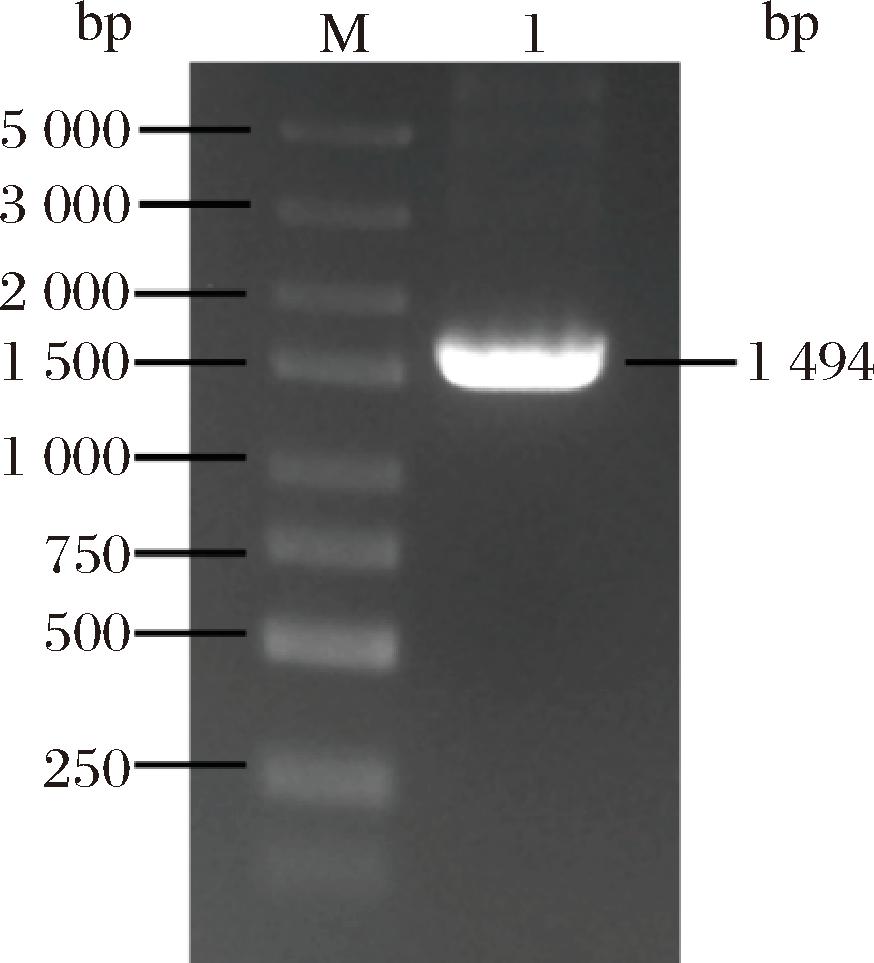
M-DNA Marker;泳道1-GGT片段。
图2 pET-GGT表达载体鉴定
Fig.2 Identification of pET GGT plasmid
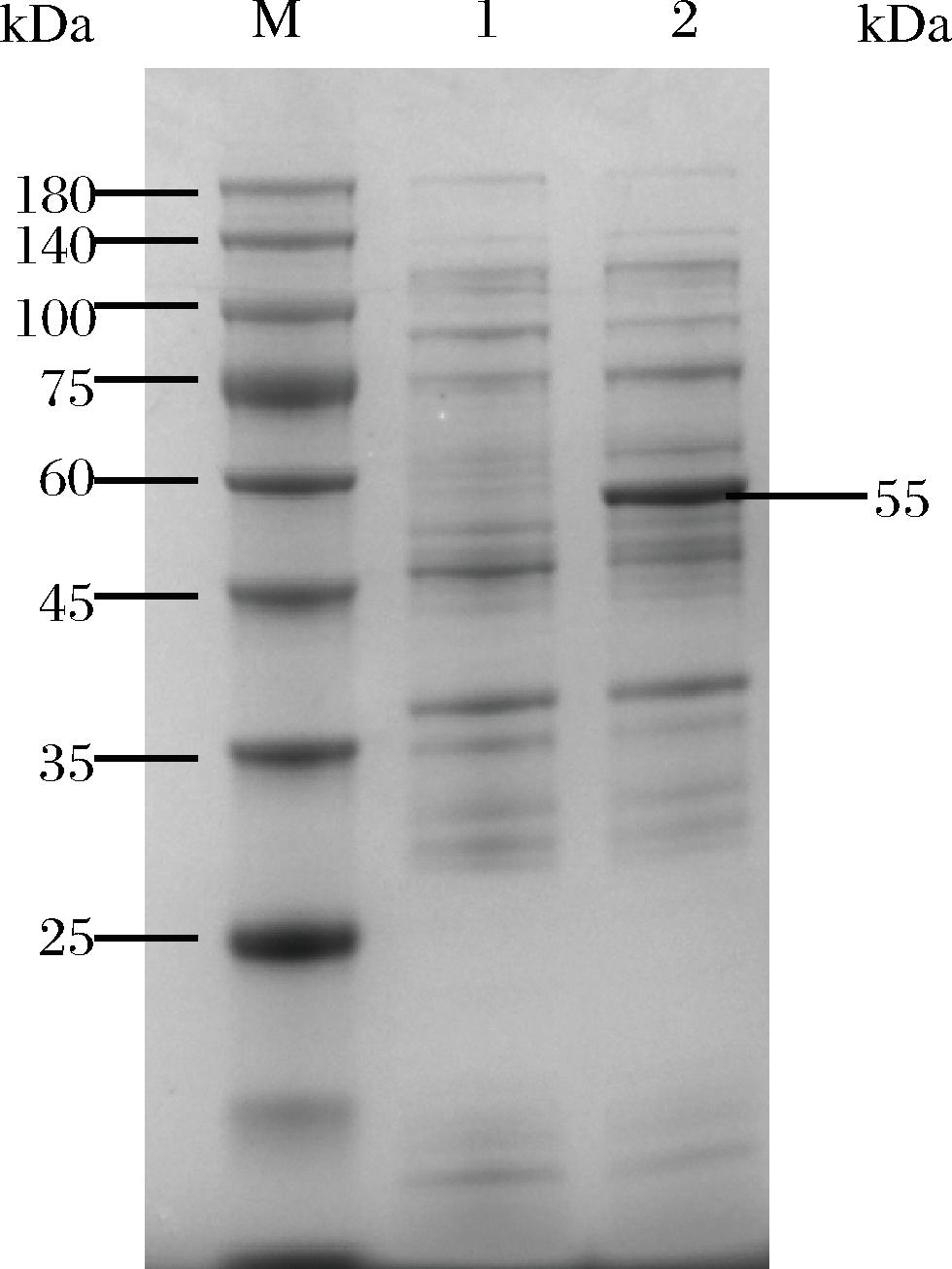
M-蛋白分子质量标准;泳道1-E.coli BL21(DE3)对照组;泳道2-包含pET-GGT质粒的重组菌株。
图3 GGAT表达验证图
Fig.3 Expression of the protein GGAT
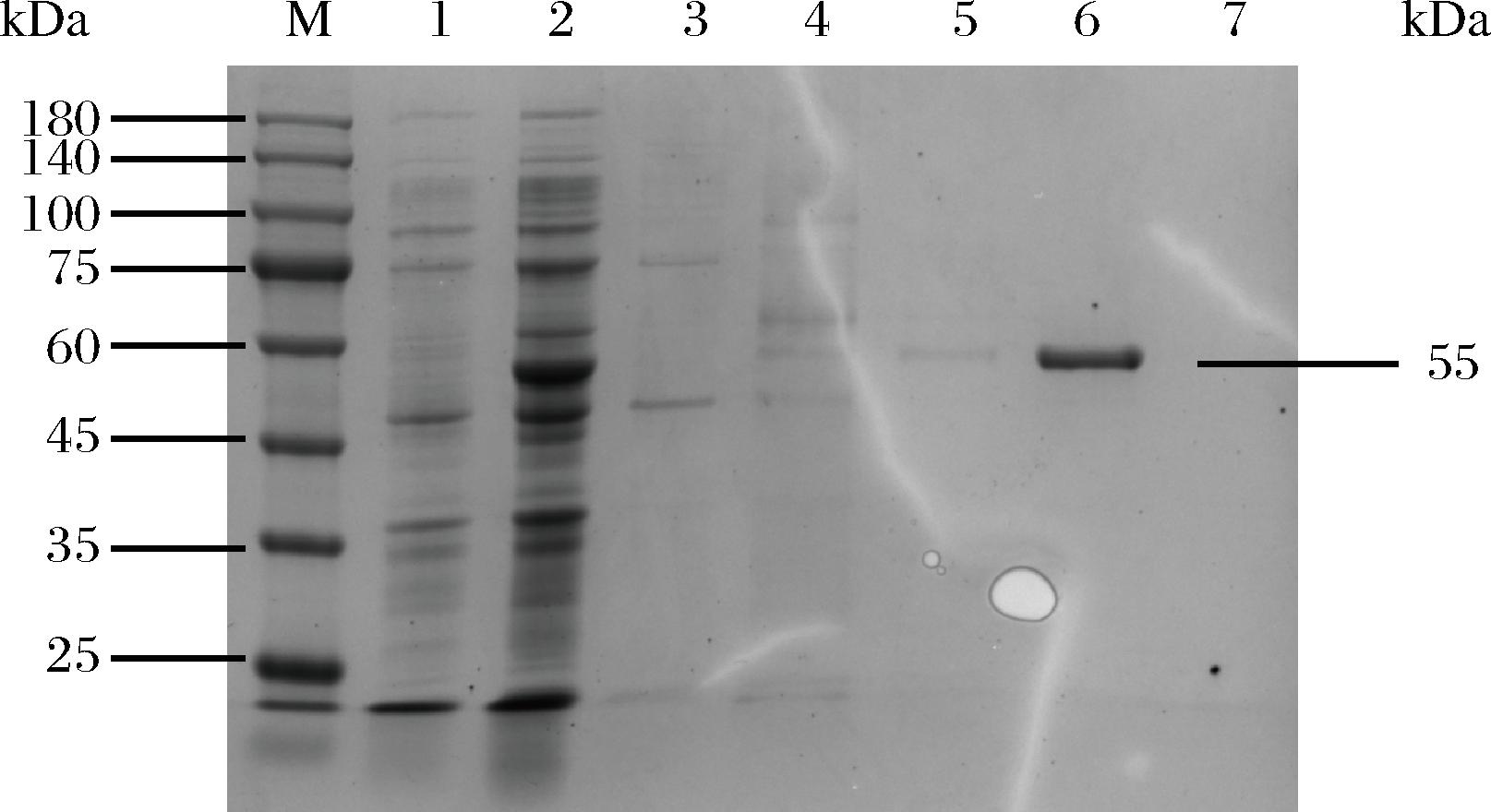
M-蛋白分子量标准;泳道1-E.coli BL21(DE3)对照组;泳道2-GGAT粗蛋白液;泳道3~7-20、50、100、200、500 mmol/L 洗脱液。
图4 GGAT纯化洗脱图
Fig.4 Purification elution diagram of GGAT
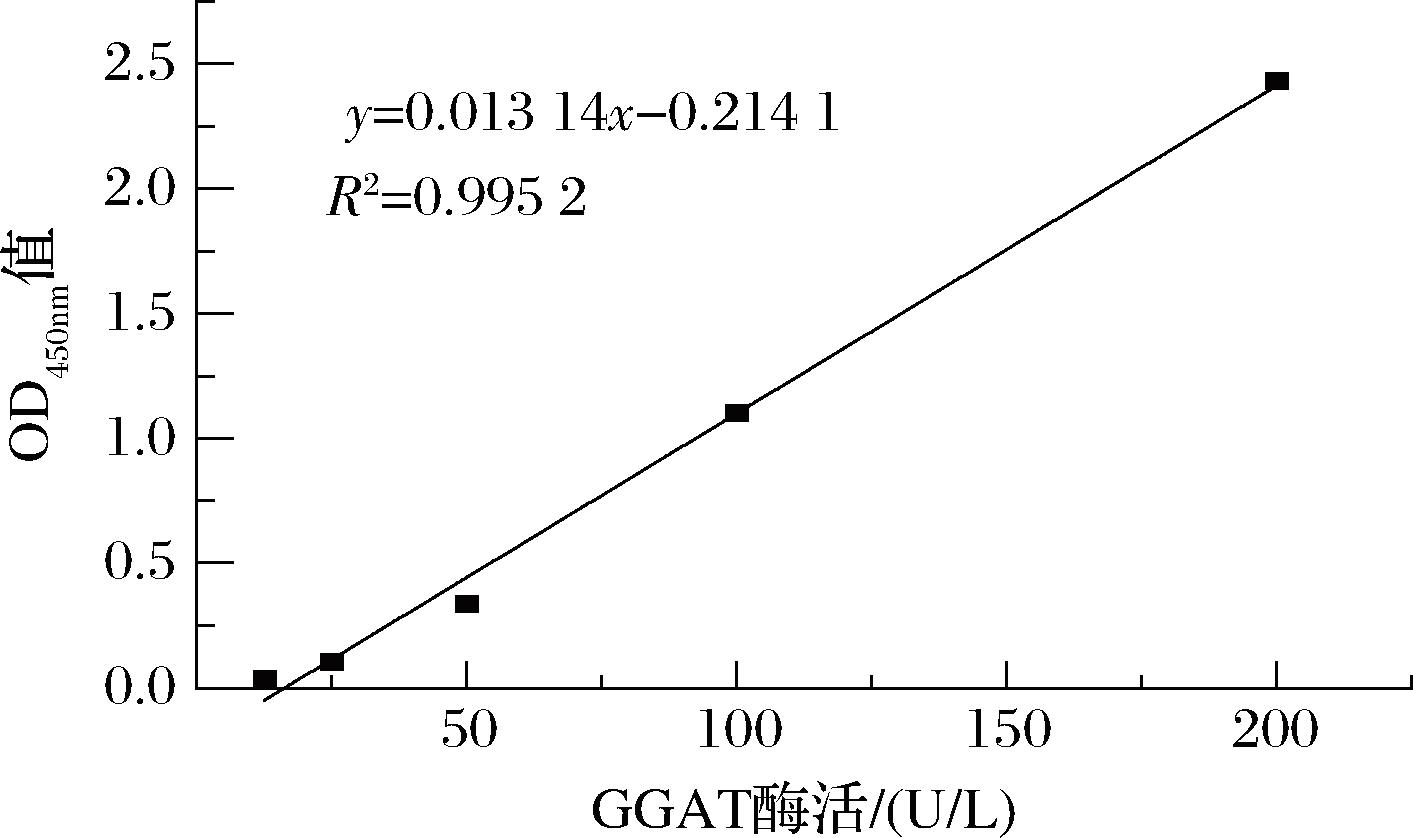
图5 GGAT活性标准曲线图
Fig.5 Standard curve for GGAT enzyme activity assay
2.2 非自然C4途径的构建
由于E.coli中缺乏C4途径合成5-ALA的关键酶ALAS,本研究将来源于荚膜红细菌(Rhodobacter capsulatus)的ALAS与GGAT构建至同一表达载体中,获得质粒pET-GH。通过引物GGT-1/hemA-1对含有质粒pET-GH的重组菌株进行PCR验证,结果显示(图6),成功扩增出长度约3 000 bp的条带,与目的基因大小(2 982 bp)相符,表明质粒pET-GH构建成功。将该质粒转化至E.coil BL21(DE3),获得重组菌ALA-1。在M9培养基中对菌株ALA-1进行发酵实验,结果如图7所示。在发酵0~20 h,菌株处于快速生长阶段,5-ALA的产量随菌株生物量的增加而增加,在21 h达到最高产量201.1 mg/L。这表明,通过异源表达ALAS和GGAT,构建的菌株ALA-1能够成功利用C4途径合成5-ALA,为进一步优化和提升产量奠定了基础。
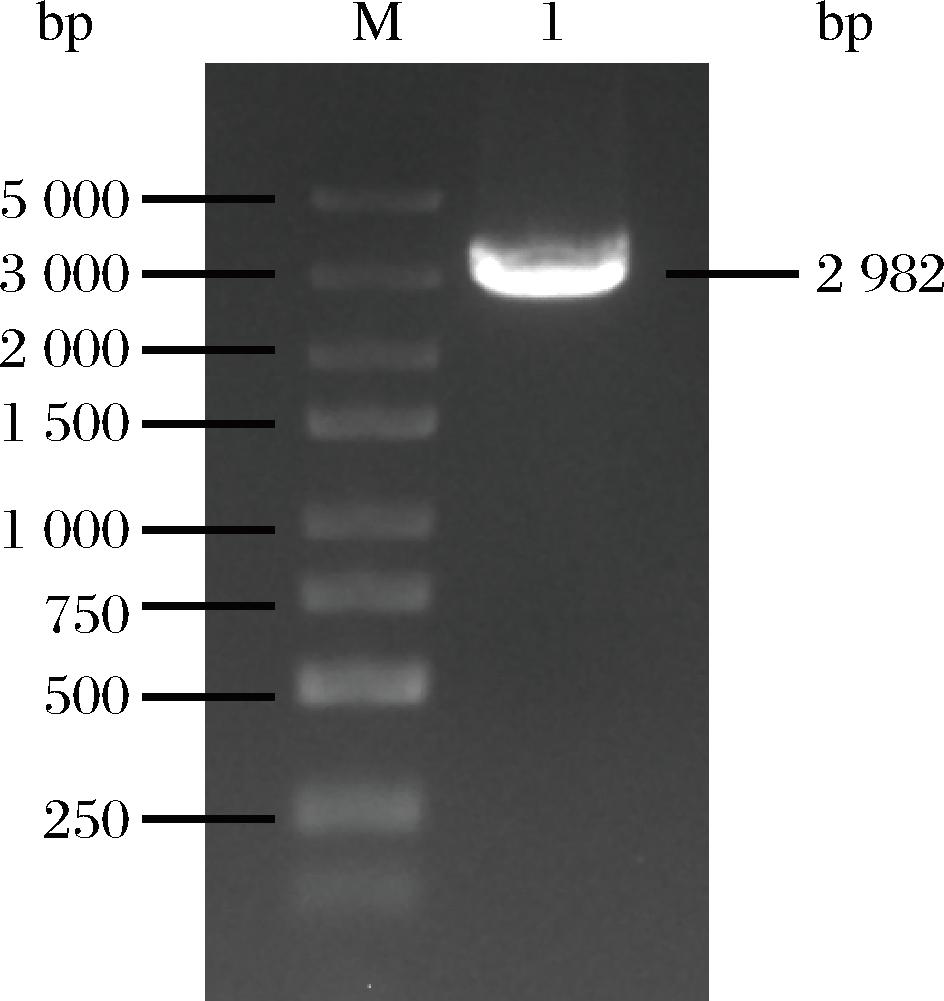
M-Marker;泳道1-pET-GH质粒。
图6 pET-GH质粒验证图
Fig.6 Identification of pET-GH plasmid
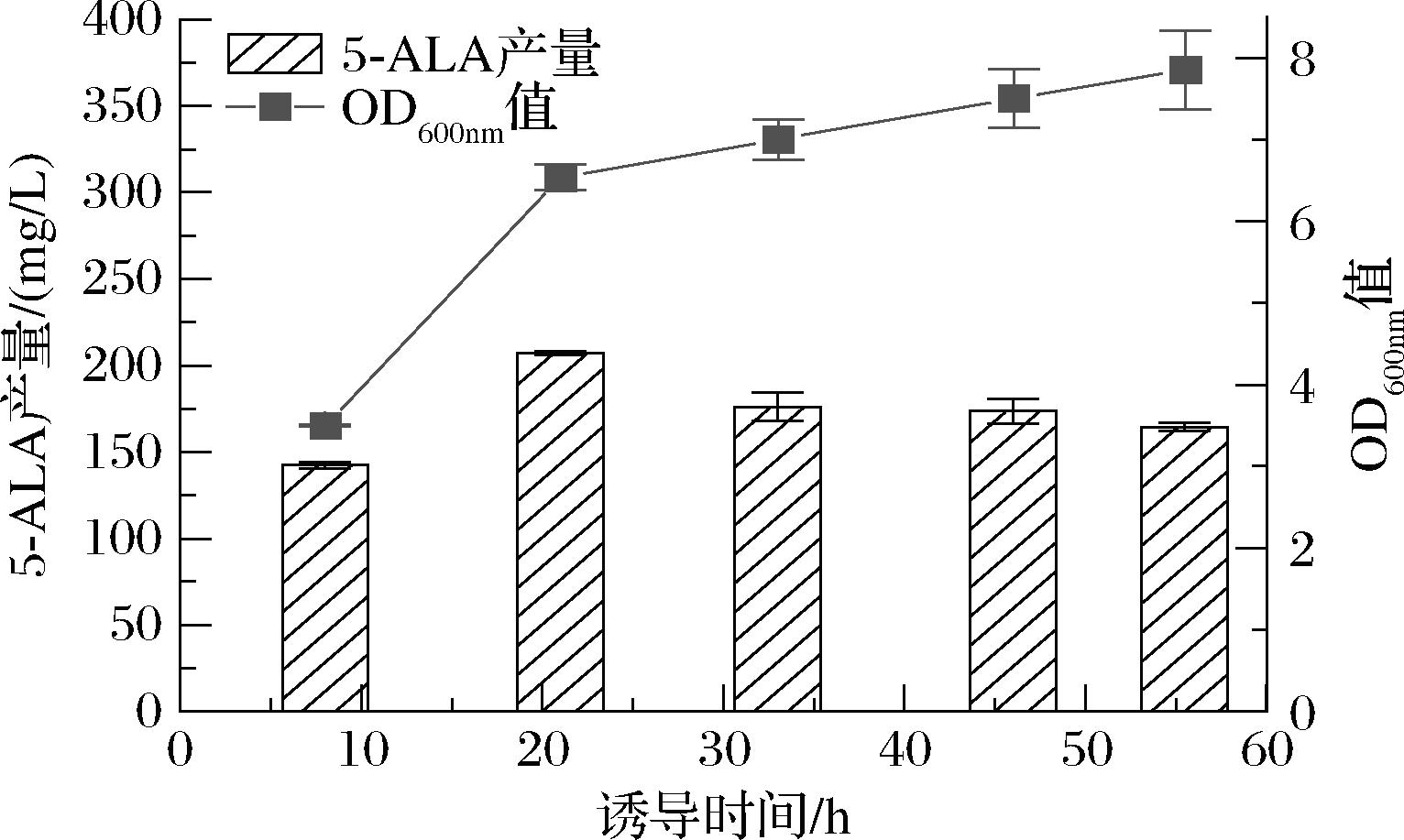
图7 ALA-1菌株发酵产5-ALA
Fig.7 ALA-1 strains ferments to produce 5-ALA
2.3 强化乙醛酸循环对合成5-ALA的影响
在E.coli中,由iclR基因编码的异柠檬酸裂解酶调节因子对乙醛酸途径的分流起关键作用。虽然在BL21菌株中,该基因突变使其调控能力降低,但乙醛酸通路的代谢流仍不足以提供足够的乙醛酸。因此,本研究通过过表达编码异柠檬酸裂解酶的aceA基因,以增加非自然C4途径重要节点乙醛酸的供应。通过将aceA基因、GGT、hemA基因共表达,构建了质粒pET-GHA。使用引物aceA-1/hemA-1对含有质粒pET-GHA的重组菌株进行菌落PCR鉴定,结果如图8所示,PCR扩增获得的条带长度为3 000~5 000 bp,与目的条带大小(4 490 bp)相符,表明质粒构建成功。随后,将重组质粒转化至E.coli BL21(DE3)中,并将该菌株命名为ALA-2。
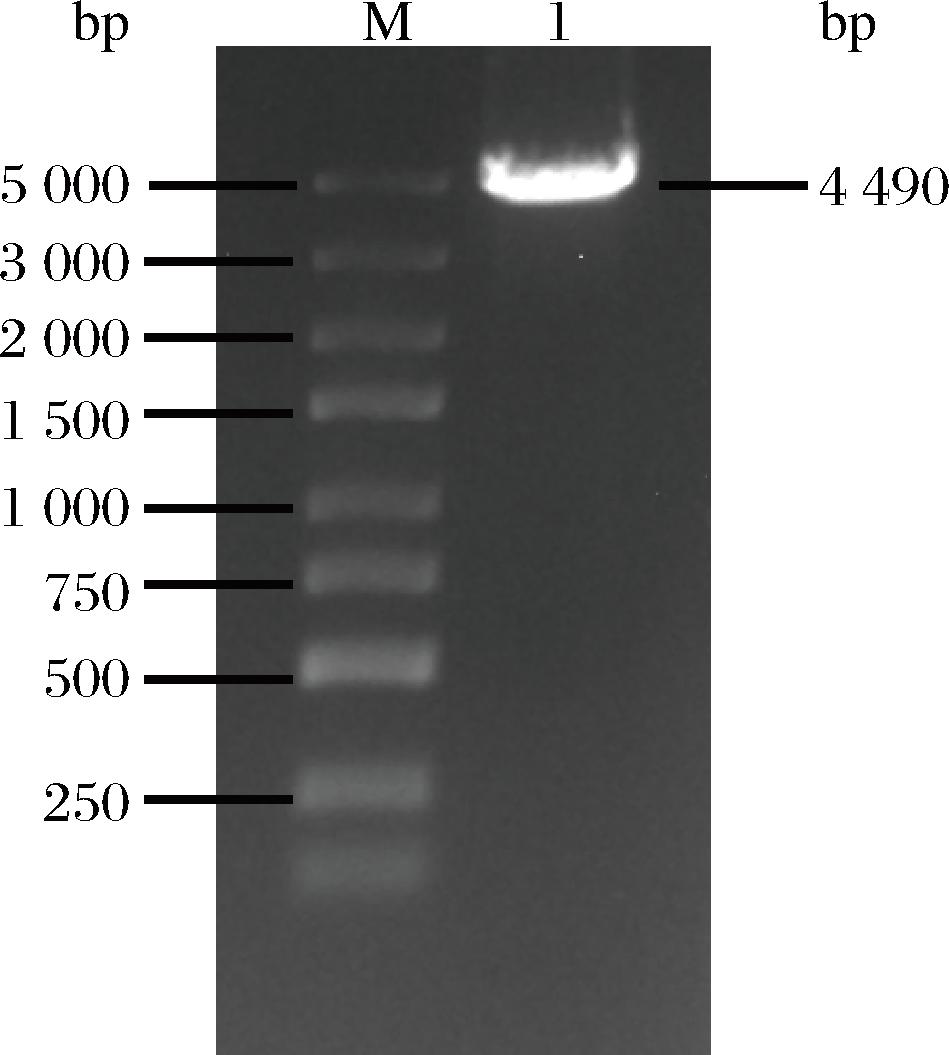
M-Marker;泳道1-pET-GHA质粒。
图8 pET-GHA质粒验证图
Fig.8 Identification of pET-GHA plasmid
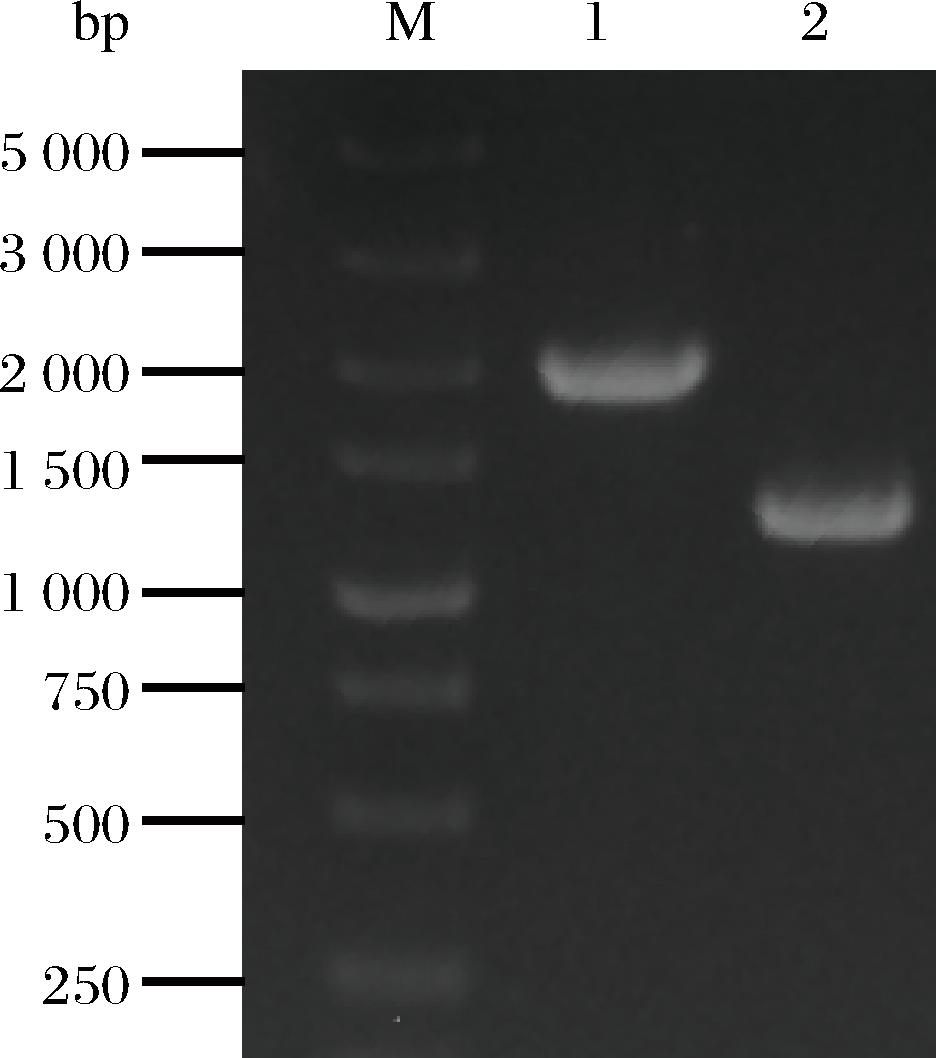
M-Marker;泳道1-E.coli BL21(DE3);泳道2-E.coli BL21(DE3)
图9 E.coli BL21(DE3)ΔaceB菌落PCR鉴定图谱
Fig.9 PCR identification map of E.coli BL21(DE3)ΔaceB
乙醛酸循环中的另一关键酶是苹果酸合酶(由aceB基因编码),催化乙酰CoA和乙醛酸生成苹果酸和CoA。敲除aceB基因可减少乙醛酸的下游代谢,从而促进5-ALA的积累。根据aceB基因序列设计引物aceB-1/aceB-2,采用Red同源重组法敲除E.coli BL21(DE3)菌株中aceB基因,并通过引物aceB-3/aceB-4进行菌落PCR验证,验证结果如图9所示,获得的条带大小分别为2 000 bp和1 000~1 500 bp,其大小分别与目的条带对照组2 000 bp、基因敲除组1 199 bp相符,表明aceB基因成功敲除。将质粒pET-GHA转化至aceB基因敲除菌株中,并命名重组菌株为ALA-3。为了验证乙醛酸循环途径的加强对5-ALA生产的影响,分别对菌株ALA-2和ALA-3进行摇瓶发酵。结果显示,与对照菌株ALA-1相比,过表达aceA提高了5-ALA的产量(图10),最高可达544.6 mg/L,较ALA-1显著提升1.7倍(P<0.001)。然而,过表达多个基因对菌体生长略有抑制作用,可能是由于细胞代谢负担加重。敲除aceB基因对菌株生长几乎没有影响,但对5-ALA的生产有一定促进作用,尽管差异并不显著,最高产量可达577.3 mg/L,进一步验证了通过调控乙醛酸循环途径可以有效提高5-ALA的生产效率。
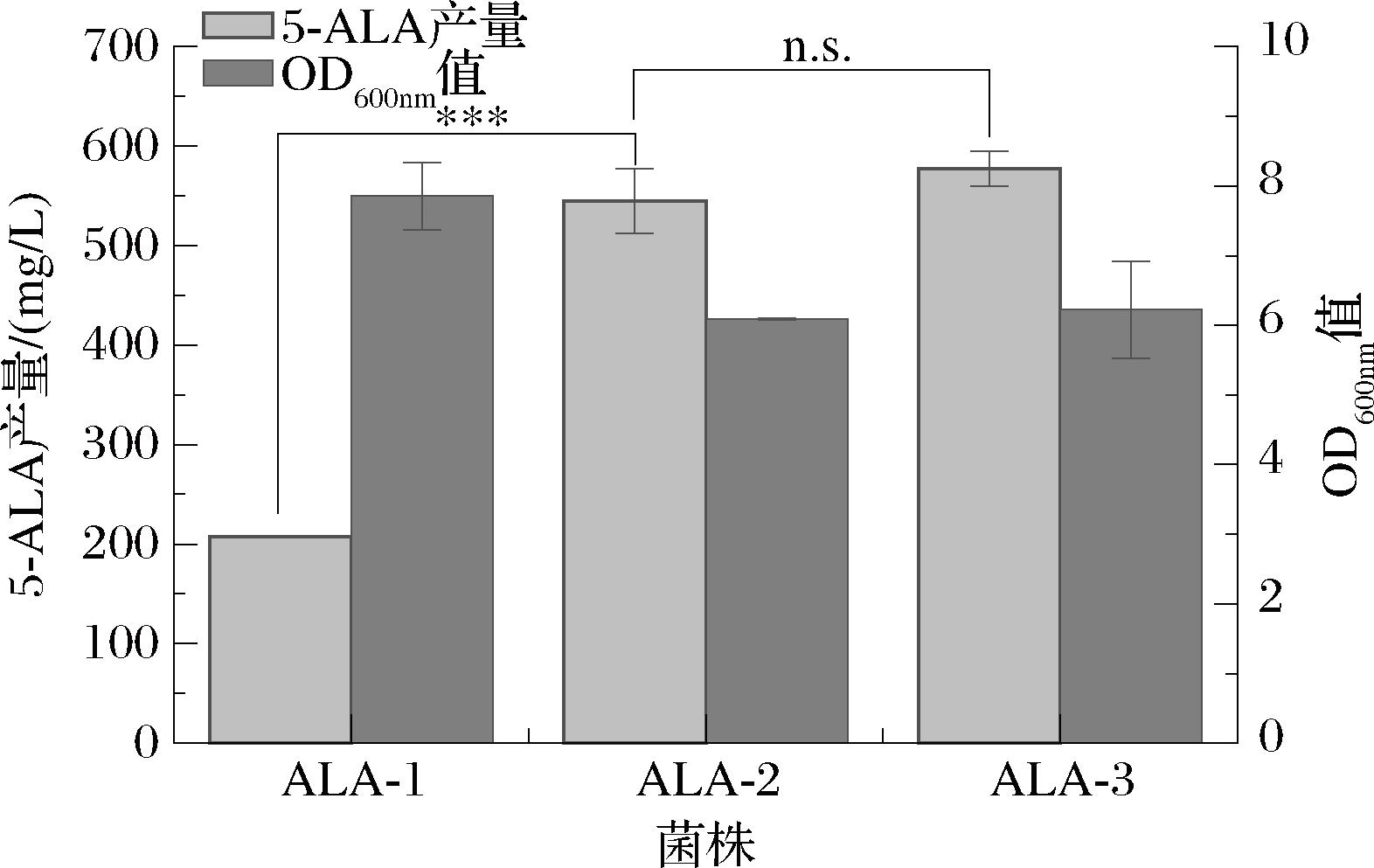
图10 过表达aceA及敲除aceB基因对5-ALA积累影响
Fig.10 Effects of overexpression of aceA and knockout of aceB gene on 5-ALA accumulation
注:***表示P值<0.001的显著水平,n.s.表示P值≥0.05即组间差异不显著。
2.4 琥珀酰CoA合成酶缺失对5-ALA积累的影响
琥珀酰CoA是5-ALA合成的关键前体之一,同时也是三羧酸循环的中间代谢产物。然而,在自然条件下,琥珀CoA几乎不会积累。琥珀CoA合成酶是催化琥珀酰CoA与琥珀酸转化的关键酶,sucCD基因的缺失可以阻断琥珀酰CoA向琥珀酸的循环代谢,促进琥珀酰CoA的胞内积累,为5-ALA的合成提供更多前体物质[15]。本研究根据sucCD基因序列设计引物sucCD-1/sucCD-2,在E.coli BL21(DE3)ΔaceB菌株的基础上,使用Red同源重组法进一步敲除sucCD 基因,并转化质粒pET-GHA至该双基因敲除菌株中,获得重组菌ALA-4。SucCD基因敲除验证图如图11所示,与对照菌株(条带长度为2 092 bp)相比,敲除sucCD基因后的菌株条带长度为1 090 bp,与预期结果一致,证明sucCD基因已成功敲除。将重组菌株ALA-4接种至M9培养基中进行发酵,研究sucCD基因的敲除对菌株生产和5-ALA生产的影响。发酵结果如图12所示,与ALA-3相比,ALA-4的生长速率有所下降,这可能是由于琥珀酰CoA的积累导致辅酶A在胞内过度消耗,造成辅酶A失衡,进而抑制了细胞的生长[15]。另外,sucCD基因的缺失提高了5-ALA 的产量,最高可达628.5 mg/L,与同批次ALA-3相比具有显著性差异(P<0.05),较ALA-3提高8.9%。该结果验证了琥珀酰CoA合成酶的缺失有助于5-ALA 的积累,为优化代谢工程菌株提供了思路。
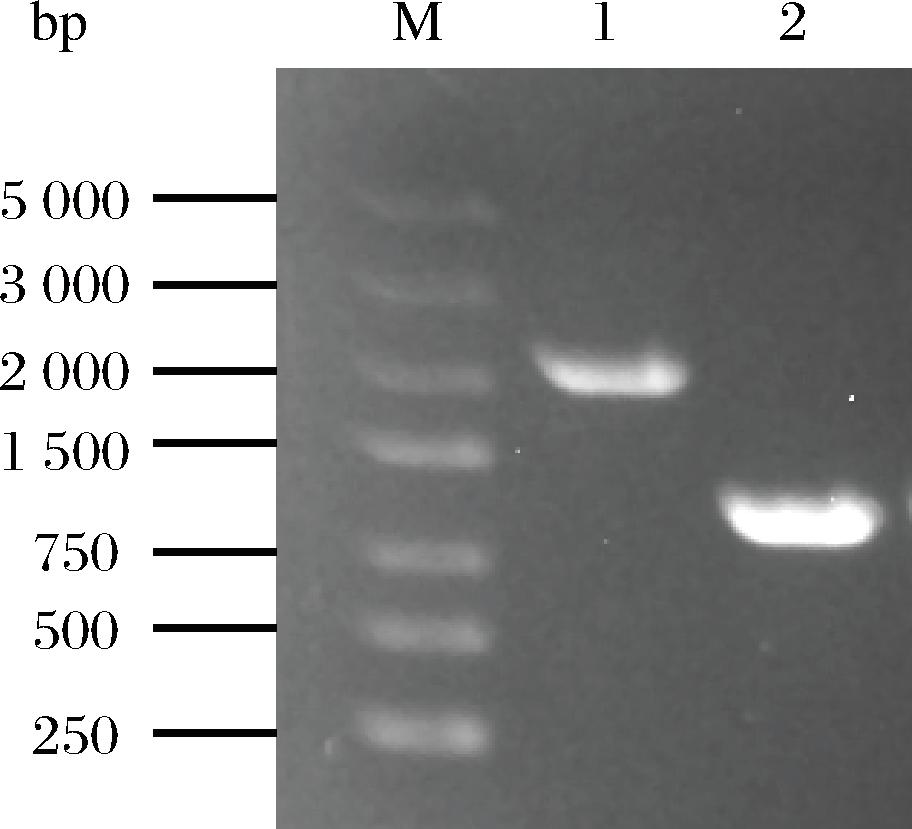
M-Marker;泳道1-E.coli BL21(DE3);泳道2-E.coli BL21(DE3)Δ aceBΔsucCD。
图11 E.coli BL21(DE3)ΔaceBΔsucCD菌落PCR鉴定图谱
Fig.11 PCR identification map of E.coli BL21(DE3)ΔaceBΔsucCD
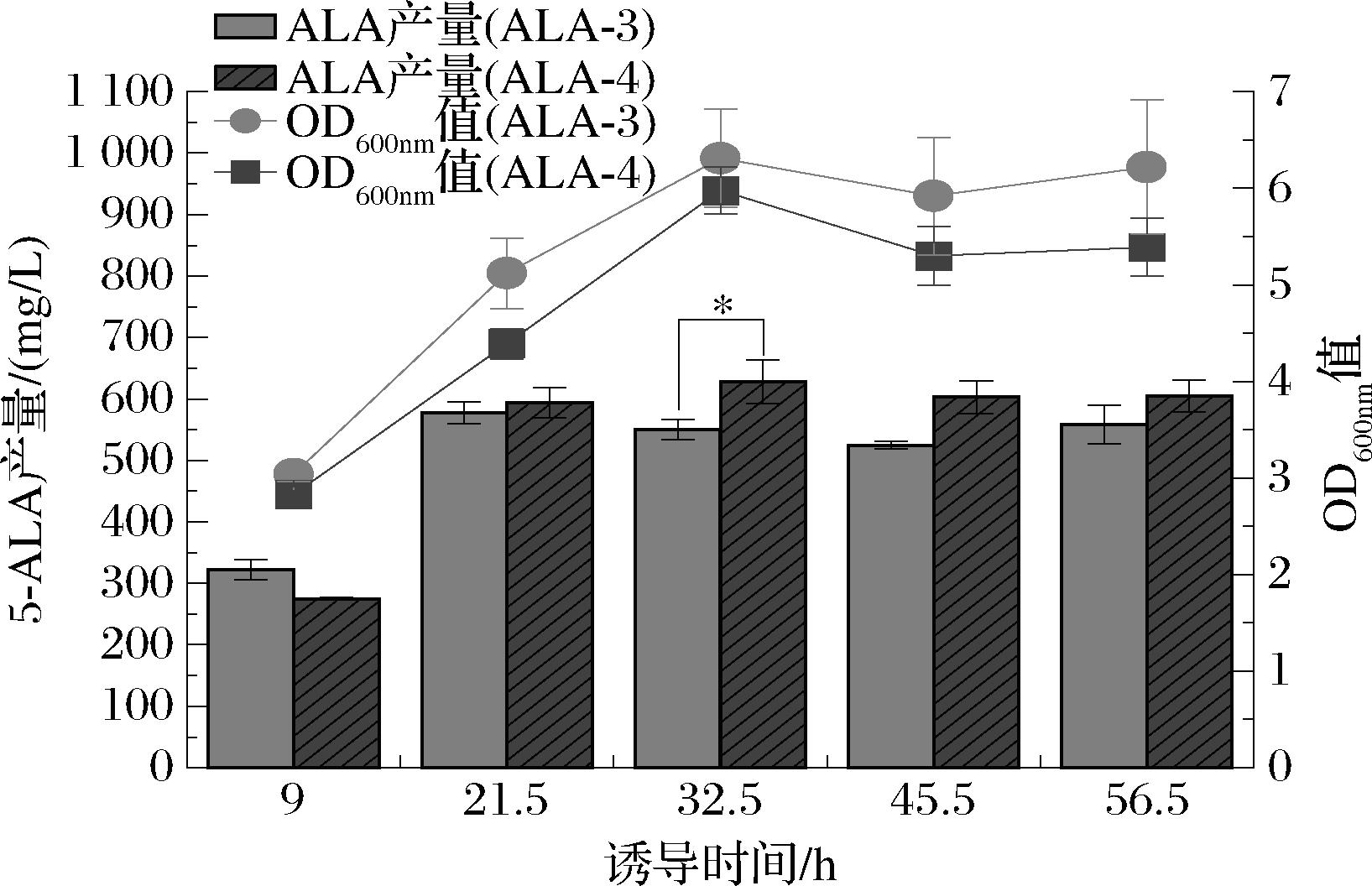
图12 敲除sucCD基因对ALA-3菌株生长和5-ALA合成的影响
Fig.12 Effect of knocking out the sucCD gene on the growth and 5-ALA synthesis of ALA-3 strain
注:*表示P值介于0.01~0.05的显著水平。
2.5 弱化下游代谢对5-ALA积累的影响
5-ALA在胞内经多步酶促反应可催化生成血红素[16],而血红素是细胞生长所必需的物质,因此,在代谢工程改造中,直接敲除hemB等关键基因完全阻断5-ALA的下游代谢会严重影响菌株的存活和生长,抑制hemB基因是目前研究常采用的策略。粪卟啉原脱羧酶(coproporphyrinogen decarboxylase,HEMF)在5-ALA的代谢途径中起关键作用,催化粪卟啉Ⅲ转化为原卟啉Ⅸ。有研究表明,HEMF的缺失可以有效减少5-ALA内源性损失,且不会影响细胞生长[17]。基于此,本研究在ALA-4菌株中对hemF基因进行了敲除,并转入C4途径质粒,构建了新的重组菌株ALA-5。使用引物对hemF基因的敲除进行验证(图13),结果显示,与对照菌株E.coli BL21(DE3)相比,ALA-5菌株的PCR产物条带较短,长度为326 bp,与预期相符,表明hemF基因被成功敲除。将ALA-4和ALA-5菌株分别接种至M9培养基中进行摇瓶发酵,结果表明(图14),ALA-5菌株在生物量和5-ALA产量上均有明显增高。5-ALA的产量最高可达672.5 mg/L,较同批次的ALA-4菌株(产量为554.8 mg/L)提升了21.2%。与现有研究相比,本研究选择了不同于代谢节点来弱化5-ALA下游代谢途径,验证了通过敲除hemF基因可以有效减少5-ALA的下游代谢消耗,从而进一步提升5-ALA的积累。这一策略为优化代谢工程菌株和提高5-ALA的工业生产水平提供了重要参考。
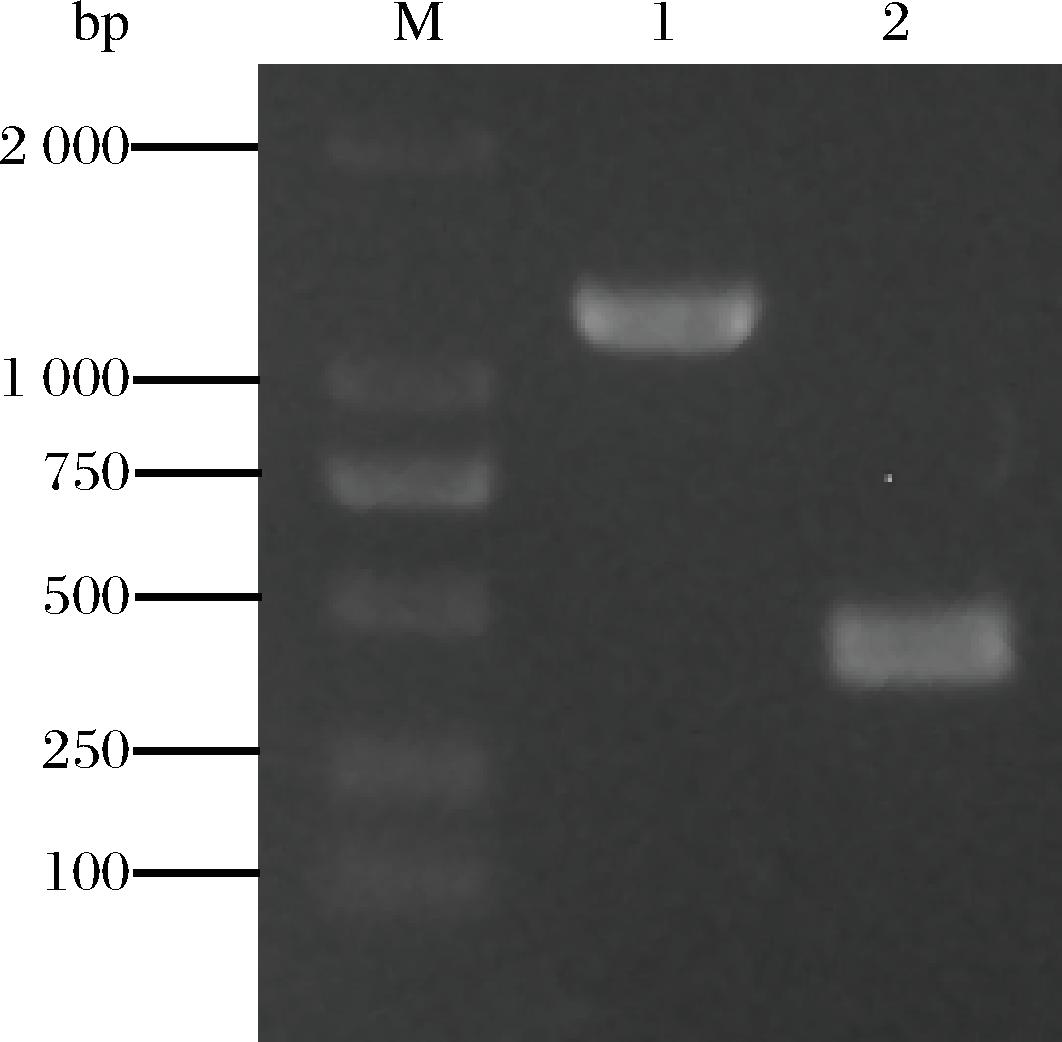
M-Marker;泳道1-E.coli BL21(DE3);泳道2-E.coli BL21(DE3) ΔaceBΔsucCDΔhemF。
图13 E.coli BL21(DE3)ΔaceBΔsucCDΔhemF菌落PCR鉴定图谱
Fig.13 PCR identification map of E.coli BL21(DE3)ΔaceBΔsucCDΔhemF
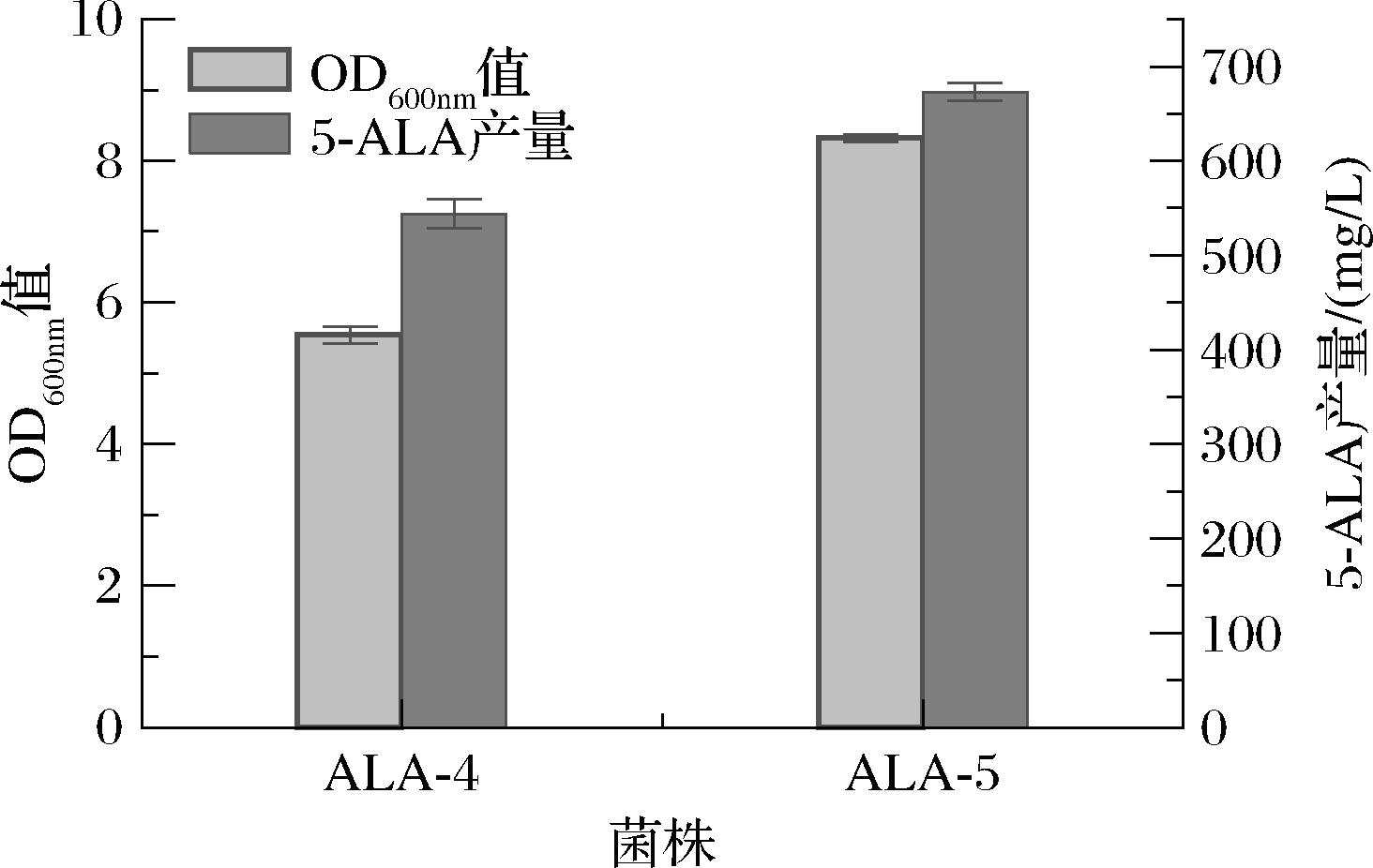
图14 ALA-5发酵5-ALA产量及生长情况
Fig.14 Fermentation yield and growth of 5-ALA by ALA-5 strain
2.6 强化草酰乙酸供应对5-ALA积累的影响
草酰乙酸是三羧酸循环的重要中间代谢产物,其主要来源之一是由磷酸烯醇式丙酮酸羧化酶(ppc基因编码)催化的回补途径。研究表明,ppc基因的过表达不仅能增加三羧酸循环中草酰乙酸的含量[18],还能改善E.coli在以葡萄糖为碳源时的生长情况[19],增加琥珀酸的合成效率[20]并减少副产物乙酸的分泌[21]。基于以上研究,本研究在ALA-5菌株的基础上,通过游离质粒pTrc过表达E.coli ppc基因,构建了重组菌株ALA-6。为减轻菌株因过表达多种外源蛋白而产生的诱导压力,将IPTG诱导浓度从0.5 mmol/L降至0.1 mmol/L。发酵结果(图15)显示,过表达ppc后的ALA-6菌株的5-ALA产量较ALA-5明显提升,最高可达1.74 g/L,较对照组的387.8 mg/L提高了3.4倍。这一结果表明,ppc基因的过表达对增加草酰乙酸的供给、优化碳代谢流向,以及提高5-ALA的积累具有积极作用。此策略展示了通过调控三羧酸循环重要代谢节点,增强代谢流的有效性,为进一步优化5-ALA的工业发酵生产奠定了基础。
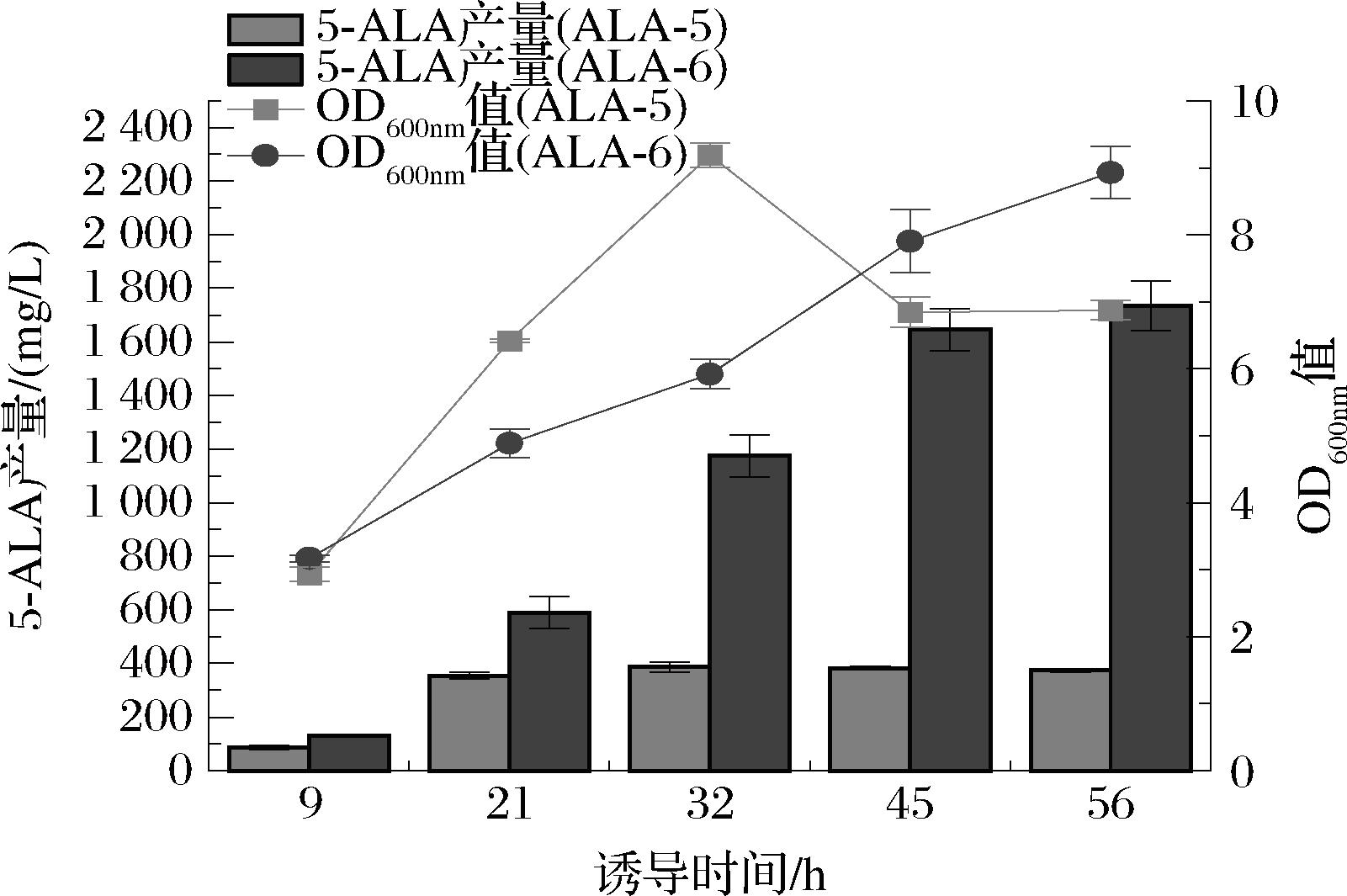
图15 ALA-6发酵产5-ALA产量及生长情况
Fig.15 Fermentation yield and growth of 5-ALA by ALA-6 strain
2.7 发酵条件优化
IPTG作为常用诱导剂,在重组蛋白表达中发挥着重要作用。其浓度的选择非常关键,如果诱导剂浓度过低,可能使重组蛋白表达不足,无法达到预期效果;而过高的浓度则可能对菌体产生毒性,抑制细菌的生长,反而影响重组蛋白的生产。在ALA-6菌株的发酵结果中,研究发现当诱导浓度降低时,ALA-5菌株产量反而降低,而ALA-6菌株产量却大幅提升。这表明,合适的IPTG浓度对5-ALA的生产至关重要。因此,本研究设置了不同浓度的IPTG(0.01、0.05、0.1、0.25 mmol/L)进行诱导,以确定最佳诱导浓度。实验结果表明,当IPTG浓度为0.1 mmol/L时,5-ALA产量达到最高。若诱导浓度低于0.1 mmol/L,由于诱导不足,重组蛋白的表达量无法满足需求,导致5-ALA产量极低;而当浓度为0.25 mmol/L时,由于过高的IPTG浓度抑制了细菌的生长,导致产量反而降低(图16)。除了IPTG浓度,发酵培养基的选择也对5-ALA的生产有重要影响。通过优化发酵培养基,研究发现含有丰富碳源和营养的乳糖自诱导培养基对5-ALA的生产更为有利,产量最高可达1.9 g/L。相比之下,虽然LB和2YT培养基也含有丰富的蛋白胨和酵母粉,但缺乏足够的碳源,未能为5-ALA的合成提供足够的前体物质,因此产量较低(图17)。综上所述,合适的IPTG浓度和优化的培养基能够显著提升5-ALA的产量,这为大规模生产5-ALA提供了重要的策略。
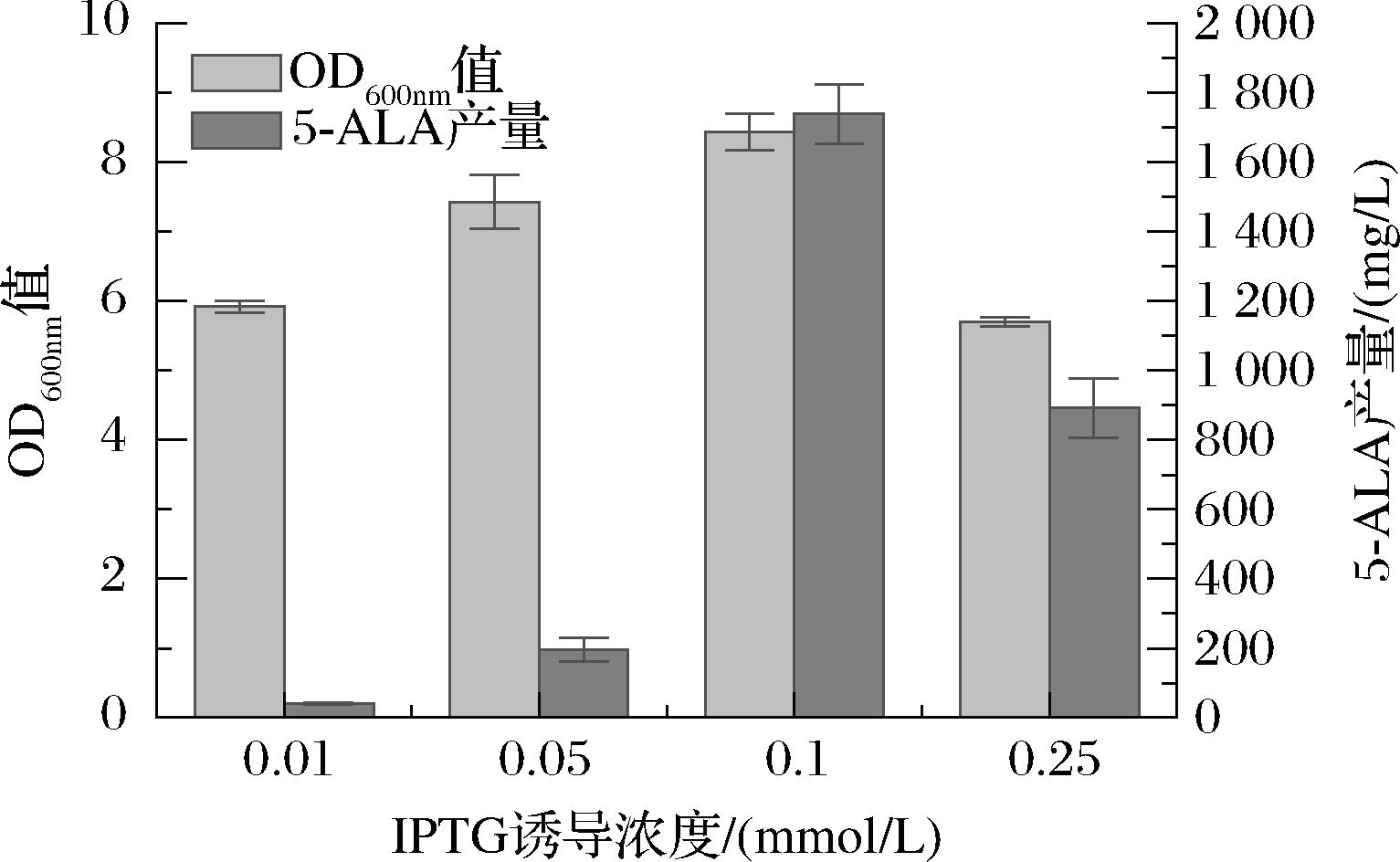
图16 IPTG诱导浓度优化
Fig.16 IPTG concentration optimization
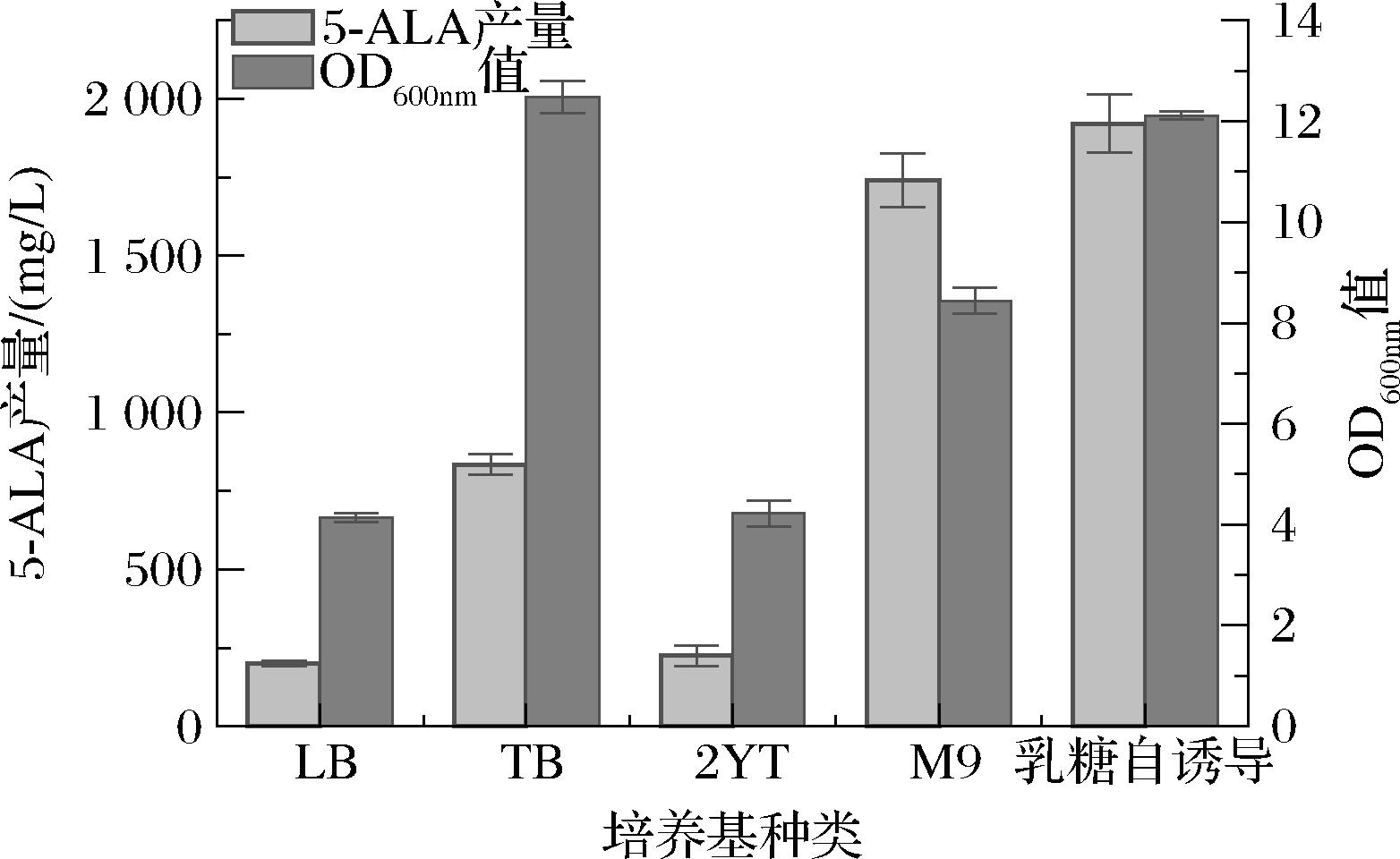
图17 发酵培养基优化
Fig.17 Optimization of fermentation medium
3 结论
本研究的主要目标是通过构建非自然C4途径来提高5-ALA的产量。首先,基于REN等[12]的研究,选取拟南芥来源的GGAT并在E.coli中进行表达和活性验证,构建一条无需添加甘氨酸的非自然C4途径用于生产5-ALA。在此基础上,进一步通过对关键酶的过表达和基因敲除策略进行代谢途径改造,其中包括:过表达异柠檬酸裂解酶、敲除苹果酸合酶,通过对乙醛酸循环途径改造提升前体物质甘氨酸的积累,敲除琥珀酰CoA合成酶来积累5-ALA另一前体物质琥珀酰CoA,使产量提升至628.5 mg/L。此外,通过抑制5-ALA下游代谢、补充草酰乙酸强化三羧酸循环、发酵优化等策略,最终摇瓶发酵得到1.9 g/L 5-ALA,显示出本研究代谢工程策略的有效性。
综上所述,本研究通过多重代谢途径改造和优化,成功提高了5-ALA的产量,为工业化生产提供了有价值的理论基础和技术支持。
[1] KANG Z,WANG Y,GU P F,et al.Engineering Escherichia coli for efficient production of 5-aminolevulinic acid from glucose[J].Metabolic Engineering,2011,13(5):492-498.
[2] NOH M H,LIM H G,PARK S,et al.Precise flux redistribution to glyoxylate cycle for 5-aminolevulinic acid production in Escherichia coli[J].Metabolic Engineering,2017,43:1-8.
[3] TAN S Y,CAO J,XIA X L,et al.Advances in 5-aminolevulinic acid priming to enhance plant tolerance to abiotic stress[J].International Journal of Molecular Sciences,2022,23(2):702.
[4] HANSEN R W,PEDERSEN C B,HALLE B,et al.Comparison of 5-aminolevulinic acid and sodium fluorescein for intraoperative tumor visualization in patients with high-grade gliomas:A single-center retrospective study[J].Journal of Neurosurgery,2019,133(5):1324-1331.
[5] BROEKX S,WEYNS F,DE VLEESCHOUWER S.5-Aminolevulinic acid for recurrent malignant gliomas:A systematic review[J].Clinical Neurology and Neurosurgery,2020,195:105913.
[6] CUI Z Y,ZHU Z W,ZHANG J H,et al.Efficient 5-aminolevulinic acid production through reconstructing the metabolic pathway in SDH-deficient Yarrowia lipolytica[J].Biochemical Engineering Journal,2021,174:108125.
[7] VAN DER WERF M J,ZEIKUS J G.5-Aminolevulinate production by Escherichia coli containing the Rhodobacter sphaeroides hemA gene[J].Applied and Environmental Microbiology,1996,62(10):3560-3566.
[8] 陈久洲,王钰,蒲伟,等.5-氨基乙酰丙酸生物合成技术的发展及展望[J].合成生物学,2021,2(6):1000-1016.CHEN J Z,WANG Y,PU W,et al.Advances and perspective on bioproduction of 5-aminolevulinic acid[J].Synthetic Biology Journal,2021,2(6):1000-1016.
[9] 蒲伟,陈久洲,孙村民,等.琥珀酸脱氢酶或琥珀酰辅酶A合成酶缺失促进大肠杆菌积累5-氨基乙酰丙酸[J].生物工程学报,2013,29(10):1494-1503.PU W,CHEN J Z,SUN C M,et al.Deficiency of succinic dehydrogenase or succinyl-CoA synthetase enhances the production of 5-aminolevulinic acid in recombinant Escherichia coli[J].Chinese Journal of Biotechnology,2013,29(10):1494-1503.
[10] DING W W,WENG H J,DU G C,et al.5-Aminolevulinic acid production from inexpensive glucose by engineering the C4 pathway in Escherichia coli[J].Journal of Industrial Microbiology &Biotechnology,2017,44(8):1127-1135.
[11] ZOU Y L,CHEN T,FENG L L,et al.Enhancement of 5-aminolevulinic acid production by metabolic engineering of the glycine biosynthesis pathway in Corynebacterium glutamicum[J].Biotechnology Letters,2017,39(9):1369-1374.
[12] REN J,ZHOU L B,WANG C,et al.An unnatural pathway for efficient 5-aminolevulinic acid biosynthesis with Glycine from glyoxylate based on retrobiosynthetic design[J].ACS Synthetic Biology,2018,7(12):2750-2757.
[13] 郑平,陈久洲,周文娟,等.5-氨基乙酰丙酸生产菌株及其构建方法和应用:中国CN201811076004.2[P].2022-09-09.ZHENG P,CHEN J Z,ZHOU W J,et al.5-Aminolevulinic acid-producing strain,construction method and applications:China,CN201811076004.2[P].2022-09-09.
[14] 赵志红,张逢秋,朱慧,等.柱前衍生高效液相色谱法测定乳制品中甘氨酸的含量[J].中国食品添加剂,2009(4):169-172.ZHAO Z H,ZHANG F Q,ZHU H,et al.Determination of glycin in dairy products by pre-column derivatization HPLC[J].China Food Additives,2009(4):169-172.
[15] GE F L,LI X K,GE Q R,et al.Modular control of multiple pathways of Corynebacterium glutamicum for 5-aminolevulinic acid production[J].AMB Express,2021,11(1):179.
[16] PU W,CHEN J Z,ZHOU Y Y,et al.Systems metabolic engineering of Escherichia coli for hyper-production of 5-aminolevulinic acid[J].Biotechnology for Biofuels and Bioproducts,2023,16(1):31.
[17] YE C C,YANG Y T,CHEN X,et al.Metabolic engineering of Escherichia coli BW25113 for the production of 5-aminolevulinic acid based on CRISPR/Cas9 mediated gene knockout and metabolic pathway modification[J].Journal of Biological Engineering,2022,16(1):26.
[18] CHEN J Z,WANG Y,GUO X,et al.Efficient bioproduction of 5-aminolevulinic acid,a promising biostimulant and nutrient,from renewable bioresources by engineered Corynebacterium glutamicum[J].Biotechnology for Biofuels,2020,13:41
[19] YANG Y T,ZOU Y H,CHEN X,et al.Metabolic engineering of Escherichia coli for the production of 5-aminolevulinic acid based on combined metabolic pathway modification and reporter-guided mutant selection (RGMS)[J].Biotechnology for Biofuels and Bioproducts,2024,17(1):82.
[20] MILLARD C S,CHAO Y P,LIAO J C,et al.Enhanced production of succinic acid by overexpression of phosphoenolpyruvate carboxylase in Escherichia coli[J].Applied and Environmental Microbiology,1996,62(5):1808-1810.
[21] FARMER W R,LIAO J C.Reduction of aerobic acetate production by Escherichia coli[J].Applied and Environmental Microbiology,1997,63(8):3205-3210.