肠道微生物群在代谢、免疫及疾病调控中起核心作用,肠道益生菌通过调控菌群稳态成为干预代谢性疾病(如肥胖、2型糖尿病)的新兴策略[1]。Akkermansia muciniphila(Akk)作为肠道黏液层优势菌[2],以宿主分泌的黏蛋白为食在肠道黏液层中生长,通过竞争性排斥在肠道中定植并保护肠道免受病原体的侵害[3],展现改善胰岛素抵抗、降低炎症及增强肿瘤免疫治疗的效果[4]。
随着益生菌菌株的不断开发和商业化,其安全性评价的重要性越发突显。近年来有研究指出,在病理状态下Akk的过度定植可能破坏黏液层动态平衡,使肠黏蛋白含量降低,降低黏液层厚度[5],其产生的琥珀酸也会上调病原菌毒力因子的表达,进一步加剧宿主感染[6]。其次,不同分离菌株对疾病干预效果差异显著,特定菌株可加重葡聚糖硫酸钠(dextran sulfate,DSS)小鼠结肠炎[7]。然而目前现有研究报道仅对Akk DSM 22959[8]、Akk ONE[9]和Akk PROBIO[10]等部分菌株通过基因毒性、急/亚慢性毒性测试等实验验证了其安全性。且Akk的一般特征、疾病疗效、抗生素耐药以及对宿主的毒性因菌株的不同而各异,故其临床应用仍需基于菌株级别的严格评估,从而确定安全性、剂量范围、副作用和益处,规避潜在风险,确保治疗的安全性和有效性[11]。
本研究系统评估Akk ATCC BAA835的益生特性与安全性:通过自聚集能力、表面疏水性及生物膜形成实验分析其肠道定植潜力;结合酸/胆盐耐受性及胃肠道模拟实验评估其肠道存活能力,并测定菌株抗氧化活性。同时,开展抗生素敏感性检测及急/亚急性毒性实验以明确其生物安全性,旨在阐明该菌株的益生潜力与风险,为其应用提供理论依据。
1 材料与方法
1.1 材料与试剂
Akk ATCC BAA835,宁波明舟生物科技有限公司;脑心浸液肉汤(brain heart infusion,BHI)培养基,青岛海博生物技术有限公司;胃蛋白酶1∶3 000,Biotopped/博奥拓达;胰酶,Sigma-Aldrich;1%质量分数结晶紫染色液,百泰克基因科技有限公司;二甲苯、正十六烷和正辛烷等,上海麦克林生化科技有限公司;抗生素药敏纸片,湖南比克曼实验器材有限公司;DPPH 自由基清除试剂盒、羟自由基测试盒、抑制或产生超氧阴离子自由基测试盒,南京建成生物工程研究所。
1.2 仪器与设备
Concept-M 400厌氧工作站,北京隆福佳生物科技有限公司;Infinite M Plex多功能微孔板检测器,上海帝肯贸易有限公司;DHP-9082电热恒温鼓风干燥箱,上海一恒科学仪器有限公司;FE20K精密pH计,上海梅特勒-托利多仪器有限公司;CF-1524R高速离心机,杭州佑宁仪器有限公司;JY 92-Ⅱ DN超声细胞破碎仪,宁波新芝生物科技有限公司。
1.3 菌株培养与生长曲线
Akk ATCC BAA835在BHI培养基中进行厌氧培养,厌氧箱的培养条件设定为90%氮气、5%二氧化碳、5%氢气,温度维持在37 ℃。菌株在经过2代的活化培养之后,将菌株以2%(体积分数)的接种量接种至培养基中。随后,每隔2 h吸取200 μL菌液,用于测定其在0、2、4、6、8、10、12、14、16、18、22 h等时间点时600 nm波长处的吸光度值。以时间为横坐标,以OD600值为纵坐标,绘制出菌株的生长曲线。
1.4 菌株益生特性评估
1.4.1 黏附特性
1.4.1.1 生物膜
将菌液用BHI培养基稀释至最终浓度为106 CFU/mL,转移至96孔板中,液体培养基作为阴性对照。37 ℃培养24 h,无菌PBS冲洗3次去除未黏附细胞,99%甲醇固定15 min,风干后每孔加入200 μL 10 mg/mL结晶紫染色,通过酶标仪测定在600 nm波长下光密度值。设定截止光密度(ODC)为阴性对照组平均OD值加上3个标准差,判定标准为:OD≤ODC为非生物膜产生者;ODC
1.4.1.2 自动聚集力
离心收集菌株,并利用PBS进行2次洗涤,以清除杂质,将Akk的浓度调整至OD600值为0.5(相当于1×109 CFU/mL),置于37 ℃的条件下进行孵育。分别于0、2、4、8、12、24 h测定上清液在600 nm处的光密度值。自动聚集率的计算公式(1)为[13]:
自动聚集率![]()
(1)
式中:At,在时间t时的吸光度值,A0,初始吸光度值。
1.4.1.3 表面疏水性
使用高速离心机在4 000 r/min下离心10 min收集对数生长末期的菌株,用PBS洗涤2次之后将细菌悬液的OD600值调整至0.5。向细菌悬液中分别加入等体积的二甲苯、十六烷或辛烷,并充分混合5 min。在37 ℃下孵育2、4、6、8 h后,测定水相在600 nm处的光密度值[14],按照公式(2)计算表面疏水性:
表面疏水率![]()
(2)
式中:Pt,在时间t时的吸光度值,P0,初始吸光度值。
1.4.2 抗氧化性
菌液在4 ℃、4 000 r/min的条件下离心10 min,收集上清液,并通过0.22 μm滤膜过滤,所得滤液即为无菌发酵液。菌体沉淀重悬于等体积的无菌生理盐水中,制得菌体混悬液。菌体沉淀经PBS洗涤3次后,调整浓度至109 CFU/mL,-20 ℃冻存,冻存后的菌体经解冻,使用细胞破碎仪在冰浴中超声破碎(150 W,超声5 s,间歇10 s,破碎20 min),此过程重复冻融超声破碎3次。最后,在4 ℃、12 000 r/min的条件下离心10 min,收集上清液,即得无细胞提取物[15]。
依据DPPH自由基清除能力试剂盒、抑制和产生超氧阴离子自由基测定试剂盒和羟自由基测定试剂盒的说明书,测定菌株发酵液、无细胞提取物和菌体混悬液的体外抗氧化指标。
1.4.3 对酸、胆盐和模拟胃肠液耐受性
溶液配制:不同酸性溶液:通过HCl溶液和NaOH溶液调节BHI培养基的pH值至2、3、4,高温灭菌。不同胆盐质量浓度溶液:配制含1、2、3 mg/mL胆盐的无菌BHI培养基。模拟胃液(simulated gastric fluid,SGF):按照3 mg/mL的质量浓度将胃蛋白酶溶解于含有5 mg/mL NaCl的无菌溶液中,并调节pH值至2.5。模拟肠液(simulated intestinal fluid,SIF):按照1 mg/mL的比例将胰蛋白酶溶解于5 mg/mL的无菌NaCl溶液中,并将pH值调节至8.0。
取0.1 mL菌液接种于0.9 mL上述不同条件的溶液中,在0、1、2、3 h进行稀释涂布,分别记录活菌数,用lg CFU/mL表示,根据公式(3)计算存活率:
存活率![]()
(3)
1.5 安全性评估
1.5.1 抗生素敏感性
采用圆盘扩散法对菌株对抗生素的敏感性进行了测定。实验中,将10种抗生素的药敏纸片紧密贴附于已均匀涂布菌株的固体琼脂平板上。将平板置于37 ℃的厌氧培养箱中培养24 h。培养结束后,测量形成的抑菌圈直径,根据美国临床和实验室标准协会将菌株对抗生素的敏感性划分为耐药(R)、敏感(S)或中间(I)这3个等级。所使用的10种抗生素包括:庆大霉素、氨苄青霉素、氯霉素、链霉素、克林霉素、四环素、卡那霉素、环丙沙星、万古霉素和红霉素。
1.5.2 动物毒性实验
1.5.2.1 实验动物
实验动物均采购自北京维通利华实验动物技术有限公司。饲养环境温度维持在20~25 ℃,相对湿度控制在(55±15)%,空气交换率为10~20 次/h,12 h昼夜循环的无特定病原菌(specific pathogen free,SPF)级别的动物房中,每只实验动物都能够自由地获取食物和水。所有程序均得到南开大学伦理委员会批准(批准号:2025-SYDWLL-000503)。
1.5.2.2 灌胃菌悬液制备
利用测定吸光度确定处于对数生长期末期和稳定期的菌株,OD600值为0.58±0.02。对该阶段的菌株通过平板稀释法进行了活菌计数,检测结果为9.4×108 CFU/mL。在4 ℃、4 000 r/min条件下,利用高速落地离心机收集菌株,无菌水清洗,制备不同浓度的菌悬液。
1.5.2.3 急性毒性实验
本实验遵循GB 15193.3—2014《食品安全国家标准 急性经口毒性试验》,选取SPF级SD大鼠(6~8 周龄,体质量180~220 g)30只(n=10/组,5只雄性,5只雌性),禁食12 h后按1×1011、1×1010 CFU/kg bw剂量经口灌胃受试菌株。灌胃后大鼠继续禁食3~4 h。给药后24 h内密切观察动物状态,无异常状况后,继续观察14 d。整个实验过程中,记录大鼠的死亡率、发病率、精神状态、毒性临床体征,每3 d检测大鼠体质量和摄食量。对所有的实验动物进行血常规和血清生化检测以及动物解剖检查。
1.5.2.4 亚急性毒性实验
亚急性毒性实验参照GB/T 23179—2008《饲料毒理学评价 亚急性毒性试验》,选择6~8周龄(体质量180~220 g)雌性和雄性大鼠40只,经过5~7 d的适应性饲养后,随机分配至4个实验组:对照组(无菌水10 mL/kg bw/d),低剂量组(1×108 CFU/kg bw/d),中剂量组(1×109 CFU/kg bw/d),高剂量组(1×1010 CFU/kg bw/d),每组包含10只大鼠,雄性和雌性各半,实验期间连续28 d对大鼠进行灌胃给药处理。
1.5.2.5 脏器系数
对所有实验动物的肝脏、脾脏、肾脏、胸腺、胰腺、雄鼠的睾丸、附睾以及雌鼠的子宫和卵巢等进行称重。通过以下公式(4)计算相对脏器质量,以标准化数据并消除个体质量差异的影响[16]:
脏器系数![]()
(4)
1.5.2.6 血常规和血清生化
对大鼠进行麻醉处理,采用眼眶取血法收集全血样本并分为2部分,一部分贮存于含EDTA-K2的抗凝管中,室温下24 h内使用全自动血细胞分析仪进行血液学参数的测定。另一部分经4 ℃低温离心(4 000×g,15 min)分离血清,使用全自动干式生化分析仪结合综合Ⅰ检测冻干试剂盒(微流控冻干化学法)进行血清生化检测。
1.5.2.7 组织病理学检测
动物实验结束取材后将组织浸泡在福尔马林溶液中,经二甲苯脱蜡、梯度乙醇脱水后通过苏木精和伊红(hematoxylin-eosin,HE)对细胞质和细胞核染色。最后经过脱水和透明化后封片,使用病理全景扫描仪对染色切片进行详细观察。
1.6 数据处理
数据以“平均值±标准差”表示(n≥3)。使用SPSS 25.0进行单因素方差分析。通过GraphPad Prism 9.5.0用于可视化绘图,显著性表示为:*P<0.05,**P<0.01,***P<0.001。
2 结果与分析
2.1 益生特性评估
2.1.1 生长曲线及黏附特性
Akk在BHI培养基中,于4 h进入对数生长期,并在14 h进入稳定期,吸光值稳定在约0.6左右(图1-a)。
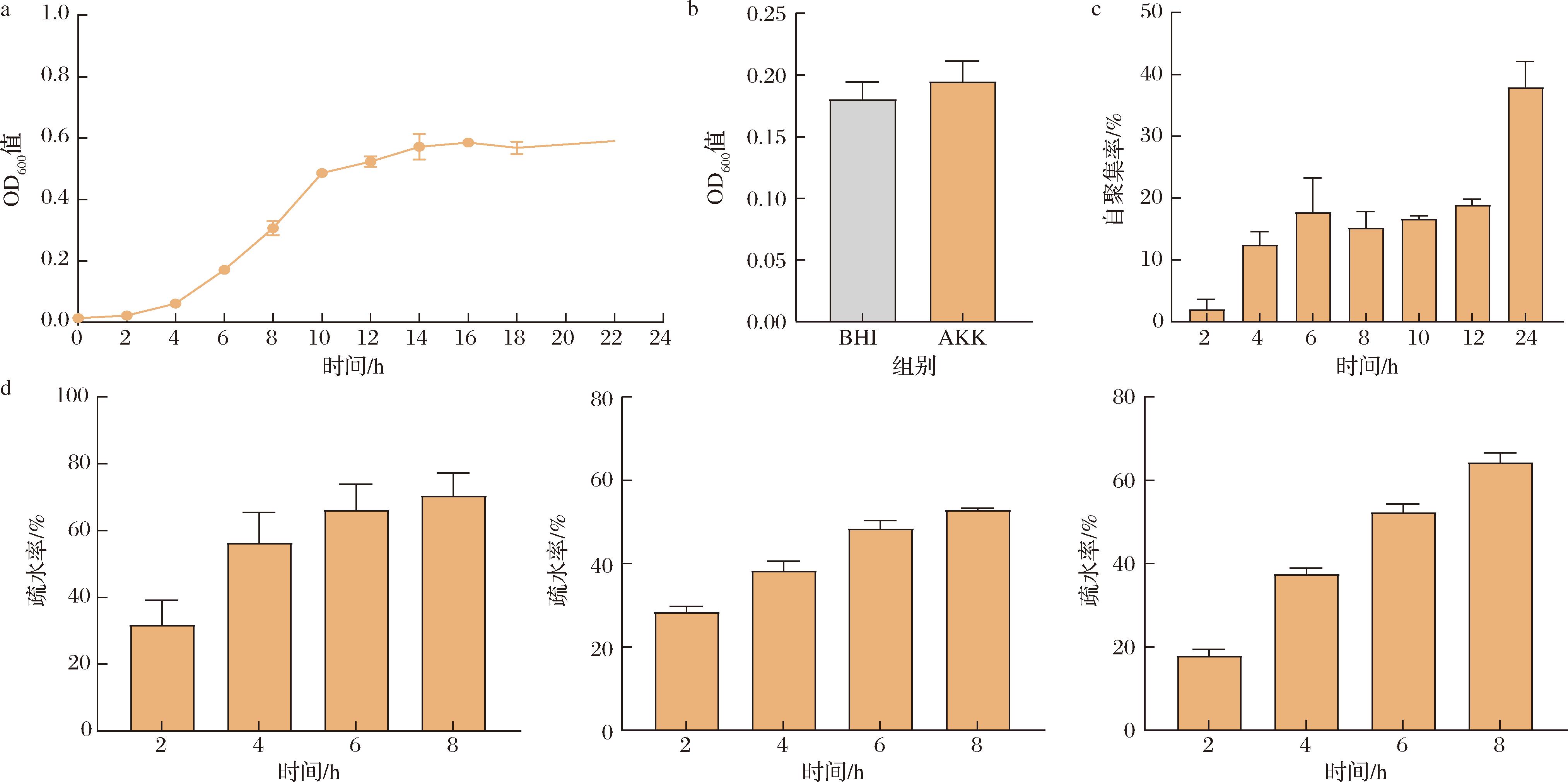
a-生长曲线;b-生物膜形成能力;c-自动聚集率;d-二甲苯、十六烷和辛烷的表面疏水率
图1 Akk ATCC BAA835的生长曲线和黏附特性
Fig.1 Growth curve and adhesion characteristics of Akk ATCC BAA835
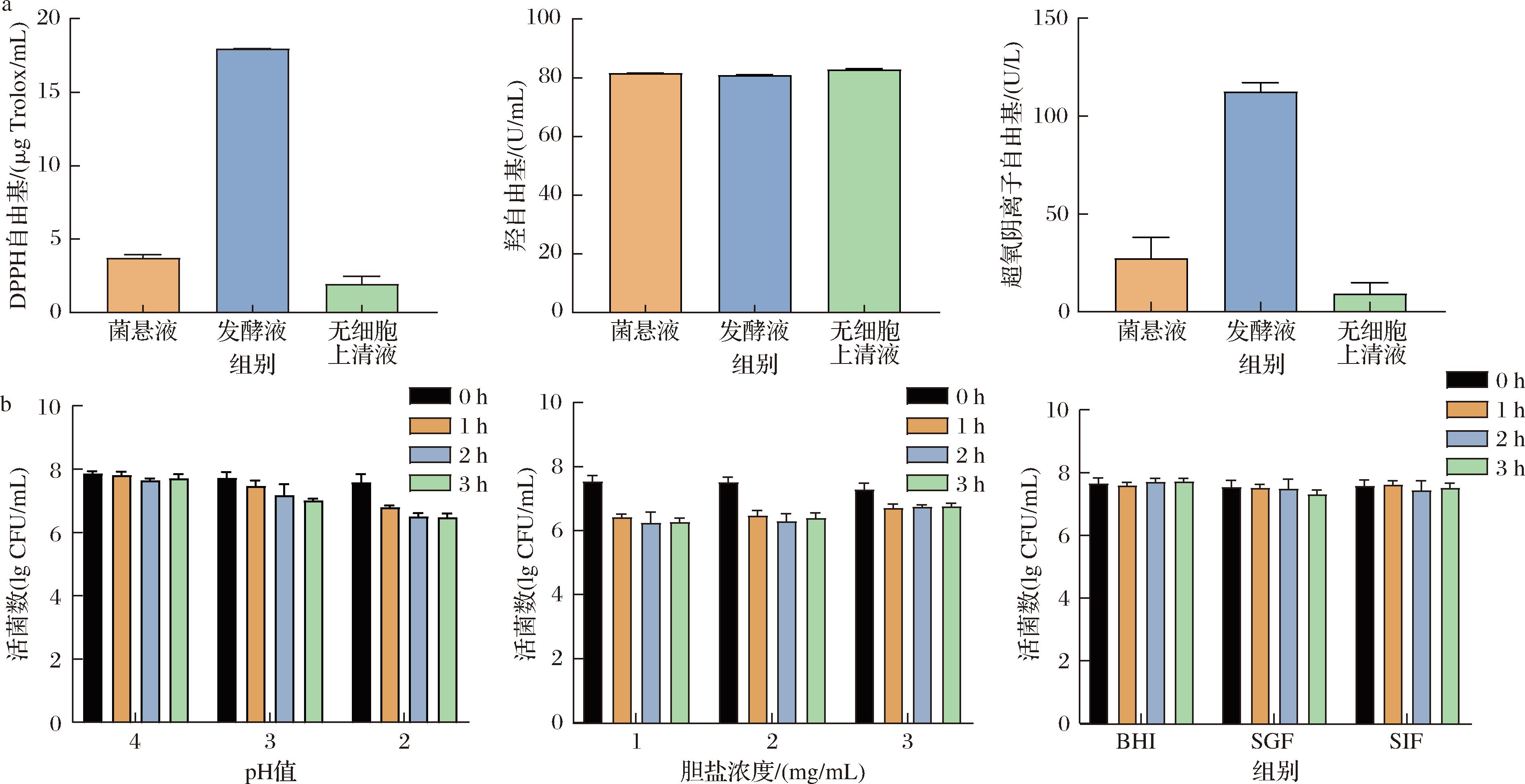
a-Akk菌悬液、发酵液和无细胞上清液的抗氧化能力;b-Akk在酸性、胆盐和模拟胃肠液中的活菌数
图2 Akk菌悬液、发酵液和无细胞上清液的抗氧化能力和在酸性、胆盐和模拟胃肠液中的活菌数
Fig.2 The antioxidant capacity and viable bacterial count in acidic,bile salt,and simulated gastrointestinal fluid of Akk bacterial suspension,fermentation broth,and cell-free supernatant
生物膜形成能力测试中,Akk的吸光值为0.194 7,小于阴性对照的ODC(0.221 2),表明其为非生物膜产生菌(图1-b),在实验测试条件下不具备生物膜形成能力。
细菌的自聚集能力可分为低、中和高,超过50%是高聚集能力,自动聚集率在30%~50%为具有中等聚集能力[17]。Akk的自聚集能力随时间延长呈逐渐增强趋势,在24 h时,Akk的自聚集能力达到37.97%,具备中等自聚集能力(图1-c)。
2.1.2 抗氧化能力
对Akk的发酵液、菌悬液和无细胞上清液这3种提取物溶液进行抗氧化性检测。如图2所示,菌株的菌悬液和无细胞上清液对DPPH自由基清除能力较低,均在5 μg Trolox/mL以下,而发酵液展现了突出的自由基清除能力(17.95 μg Trolox/mL),Akk ATCC BAA835的3种提取物溶液都展现了对较好的对羟自由基的清除能力,均在80 U/mL左右。对于超氧阴离子自由基的抑制效果,菌株的发酵液表现出良好的抑制能力,为112.34 U/L(图2-a)。
2.1.3 抗逆能力
Akk在各酸性pH值条件下,活菌数随着时间和pH值的降低呈现递减的趋势,3 h后在pH值=4的条件下,存活率为98.22%,在pH值=3的条件下,存活率为90.80%,在pH值=2的条件下,存活率仍可达到88.92%,表明该菌株具有较强的酸耐受机制,使其能够在酸性环境中保持较高的活性和生存能力。在胆盐的耐受性检测中,Akk在1 mg/mL胆盐质量浓度下3 h内,由7.53 lg CFU/mL降至6.26 lg CFU/mL(存活率83.13%);在2 mg/mL胆盐质量浓度下,由7.51 lg CFU/mL降至6.39 lg CFU/mL(存活率85.09%);在3 mg/mL胆盐质量浓度下3 h后仍可检测到6.76 lg CFU/mL的活菌数(存活率92.73%),在3种胆盐质量浓度条件下存活率均在80%以上。除了胆盐,小肠还含有胰酶和脂肪酶,它们也对细菌有潜在危害。Akk在SGF(由7.53 lg CFU/mL降至7.30 lg CFU/mL,存活率96.95%)和SIF(由7.57 lg CFU/mL降至7.50 lg CFU/mL,存活率99.21%)中的存活率均在95%以上(图2-b)。
2.2 安全性
2.2.1 抗生素敏感性
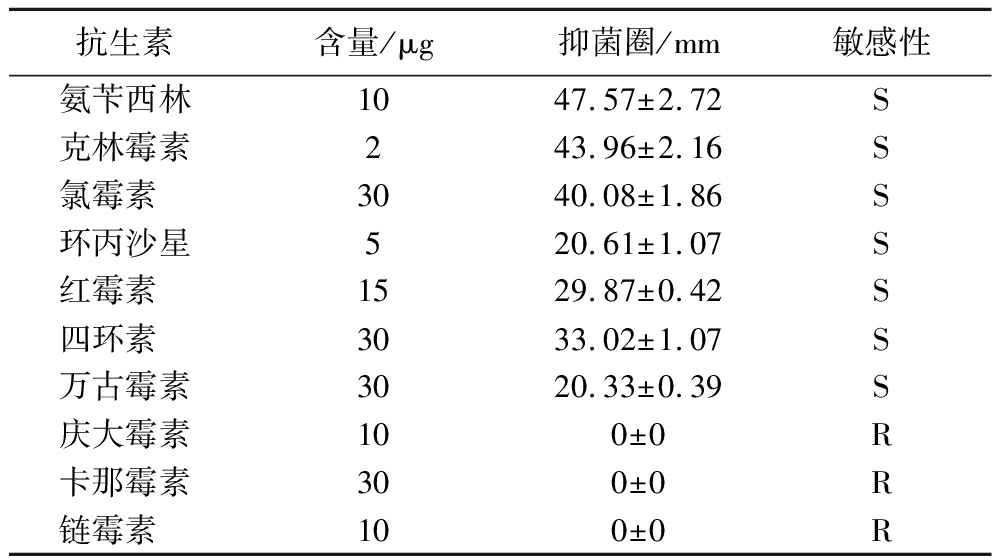
在本研究中通过药敏实验检测了Akk ATCC BAA835对于10种抗生素的敏感性(表1),结果表明菌株对氨基糖苷类抗生素具有耐受性(抑菌圈为0),如庆大霉素、卡那霉素、链霉素。对测试的其他抗生素如β-内酰胺类(青霉素)、林可酰胺类(克林霉素)、喹诺酮类(环丙沙星)等表现出敏感性。
表1 抗生素敏感性
Table 1 Results of antibiotics sensitivity
抗生素含量/μg抑菌圈/mm敏感性氨苄西林1047.57±2.72S克林霉素243.96±2.16S氯霉素 3040.08±1.86S环丙沙星520.61±1.07S红霉素 1529.87±0.42S四环素 3033.02±1.07S万古霉素3020.33±0.39S庆大霉素100±0R卡那霉素300±0R链霉素 100±0R
2.2.2 急性毒性实验
2.2.2.1 体质量和摄食
急性毒性暴露周期内,在本研究设定的给药剂量(1×1010、1×1011 CFU/kg bw)单次口服暴露14 d后,各实验组动物体质量增长及日均摄食量与空白对照组相比均无统计学差异(P>0.05,图3)。
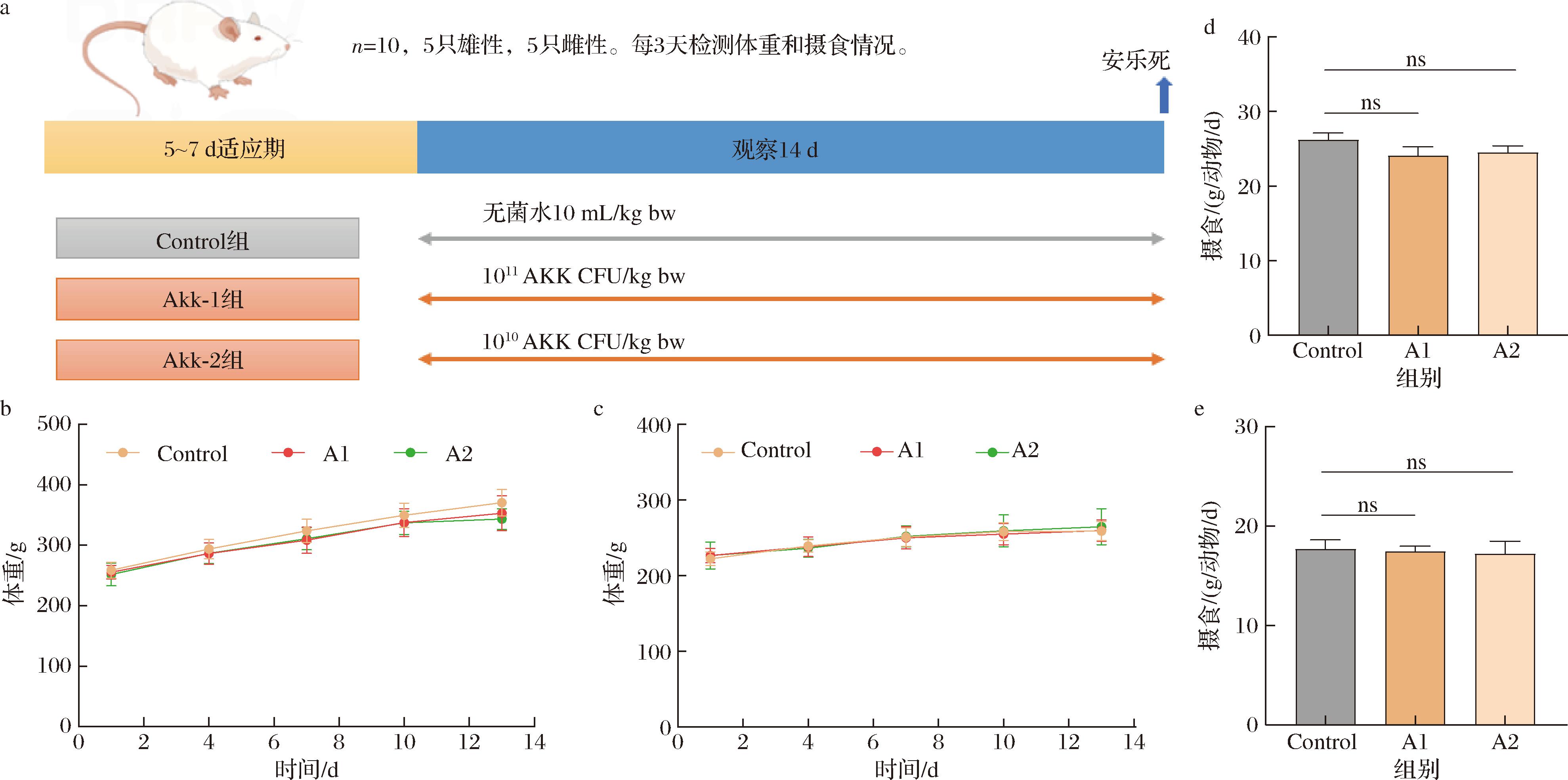
a-实验设计;b-雄性动物各组体质量;c-雌性动物各组体质量;d-雄性动物各组摄食;e-雌性动物各组摄食
图3 急性毒性实验
Fig.3 Acute toxicity test
注:ns表示不显著(下同)。
2.2.2.2 脏器系数
通过计算如肝、脾、肺、肾等主要脏器的脏器系数,2个实验组与对照组间均未呈现显著性差异(表2)。这一系统性评估结果提示,受试菌株在急性毒性实验条件下未引起实验动物重要器官的病理性改变或水肿等异常形态学变化。
表2 急性毒性实验脏器系数统计
Table 2 Organ coefficient of acute toxicity test
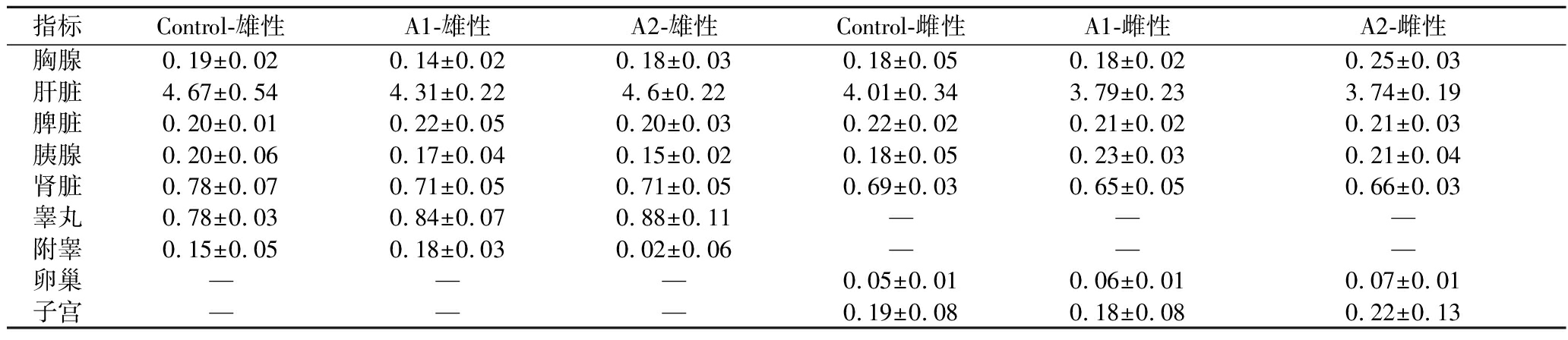
指标Control-雄性A1-雄性A2-雄性Control-雌性A1-雌性A2-雌性胸腺0.19±0.020.14±0.020.18±0.030.18±0.050.18±0.020.25±0.03肝脏4.67±0.544.31±0.224.6±0.224.01±0.343.79±0.233.74±0.19脾脏0.20±0.010.22±0.050.20±0.030.22±0.020.21±0.020.21±0.03胰腺0.20±0.060.17±0.040.15±0.020.18±0.050.23±0.030.21±0.04肾脏0.78±0.070.71±0.050.71±0.050.69±0.030.65±0.050.66±0.03睾丸0.78±0.030.84±0.070.88±0.11———附睾0.15±0.050.18±0.030.02±0.06———卵巢———0.05±0.010.06±0.010.07±0.01子宫———0.19±0.080.18±0.080.22±0.13
注:“—”表示无意义(下同)。
2.2.2.3 血常规
血常规检测结果显示(表3),各实验组血液学检测结果与对照组相比均无显著差异。
表3 急性毒性实验血液学参数
Table 3 Hematological parameters of acute toxicity test

指标Control-雄性A1-雄性A2-雄性Control-雌性A1-雌性A2-雌性WBC/(109/L)8.30±2.878.12±1.738.84±4.026.88±2.847.68±2.276.38±1.85Lymph/(109/L)6.64±2.226.76±1.447.18±3.235.50±2.456.06±1.815.38±1.69Mon/(109/L)0.20±0.120.16±0.050.20±0.120.18±0.040.20±0.070.14±0.05Gran/(109/L)1.46±0.721.20±0.391.46±0.721.20±0.371.42±0.580.86±0.23Lymph%/%79.80±4.4182.76±3.881.62±3.3579.12±3.0479.00±4.3783.32±5.48Mon%/%2.96±0.622.62±0.612.44±0.772.92±0.292.62±0.482.24±0.49Gran%/% 17.24±4.1014.62±3.3715.94±2.7017.96±2.9318.38±3.9414.44±5.14RBC/(1012/L)7.11±0.546.48±0.536.53±1.146.22±0.696.27±0.776.87±0.27HGB/(g/L)142.20±12.60128.20±11.52127.80±24.73118.40±14.15121.60±12.97132.20±4.55HCT/%44.96±3.2740.90±3.8239.68±7.1739.00±4.0038.26±3.7042.04±1.67MCV/fL63.34±1.0563.16±1.2360.86±1.6762.88±2.1361.26±2.0261.26±1.16MCH/pg19.94±0.6619.74±0.7119.48±0.6318.98±0.3719.36±0.8219.18±0.39MCHC/(g/L)315.40±12.4313.00±6.96321.20±7.40303.00±9.97317.40±10.09314.00±6.89RDW/%11.38±0.9111.30±0.4611.44±0.3310.48±0.9010.72±0.3810.48±0.27PLT/(109/L)1 032.60±466.081 026.60±272.28866.20±520.24942.25±265.13825.20±396.67829.00±365.95MPV/fL6.50±0.506.32±0.456.56±0.196.18±0.226.22±0.336.50±0.32PDW16.26±0.3416.06±0.1516.36±0.4116.03±0.1015.96±0.1716.06±0.15
注:单核细胞百分比,monocyte percentage,Mon%;中性粒细胞百分比,granulocyte percentage,Gran%;红细胞计数,red blood cell count,RBC;血红蛋白,hemoglobin,HGB;红细胞压积,erythrocyte pressure volume,HCT;平均红细胞体积,mean erythrocyte volume,MCV;平均红细胞血红蛋白含量,mean erythrocyte hemoglobin content,MCH;平均红细胞血红蛋白浓度,mean erythrocyte hemoglobin concentration,MCHC;红细胞分布宽度,coefficient of variation of red cell distribution width,RDW;血小板计数,platelet number,PLT;平均血小板体积,mean platelet volume,MPV;血小板分布宽度,platelet distribution width,PDW。
2.2.2.4 血清生化
如表4所示,雌性动物A1组胆固醇水平较对照组显著降低(P<0.05)。在雄性动物也观察到胆固醇水平降低趋势,但组间差异并未达到统计学显著水平(P>0.05)。
表4 急性毒性血清生化参数
Table 4 Acute toxicity serum biochemical parameters
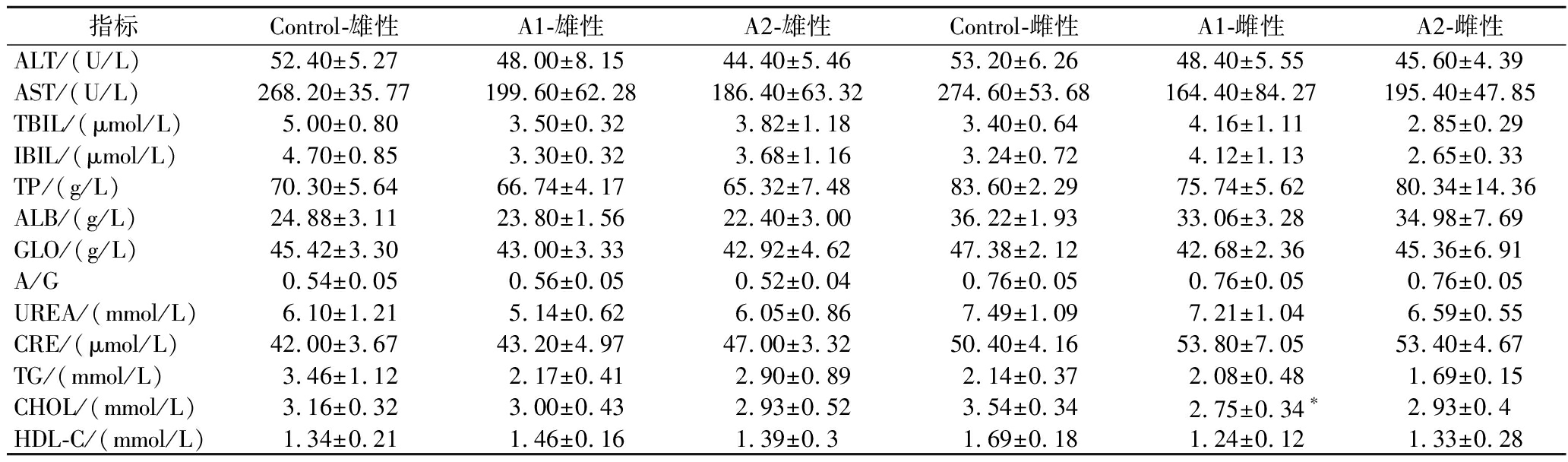
指标Control-雄性A1-雄性A2-雄性Control-雌性A1-雌性A2-雌性ALT/(U/L)52.40±5.2748.00±8.1544.40±5.4653.20±6.2648.40±5.5545.60±4.39AST/(U/L)268.20±35.77199.60±62.28186.40±63.32274.60±53.68164.40±84.27195.40±47.85TBIL/(μmol/L)5.00±0.803.50±0.323.82±1.183.40±0.644.16±1.112.85±0.29IBIL/(μmol/L)4.70±0.853.30±0.323.68±1.163.24±0.724.12±1.132.65±0.33TP/(g/L)70.30±5.6466.74±4.1765.32±7.4883.60±2.2975.74±5.6280.34±14.36ALB/(g/L)24.88±3.1123.80±1.5622.40±3.0036.22±1.9333.06±3.2834.98±7.69GLO/(g/L)45.42±3.3043.00±3.3342.92±4.6247.38±2.1242.68±2.3645.36±6.91A/G0.54±0.050.56±0.050.52±0.040.76±0.050.76±0.050.76±0.05UREA/(mmol/L)6.10±1.215.14±0.626.05±0.867.49±1.097.21±1.046.59±0.55CRE/(μmol/L)42.00±3.6743.20±4.9747.00±3.3250.40±4.1653.80±7.0553.40±4.67TG/(mmol/L)3.46±1.122.17±0.412.90±0.892.14±0.372.08±0.481.69±0.15CHOL/(mmol/L)3.16±0.323.00±0.432.93±0.523.54±0.342.75±0.34∗2.93±0.4HDL-C/(mmol/L)1.34±0.211.46±0.161.39±0.31.69±0.181.24±0.121.33±0.28
注:丙氨酸氨基转移酶,aminotransferase,ALT;天冬氨酸转氨酶,spartate aminotransferase,AST;总胆红素,total bilirubin,TBIL;间接胆红素,indirect bilirubin,IBIL;总蛋白,total protein,TP;白蛋白,albumin,ALB;球蛋白,globulin,GLO;白球比,A/G;尿素,urea,UREA;肌酐,creatinine,CRE;甘油三酯,triglycerides,TG;胆固醇,cholesterol,CHOL;高密度脂蛋白胆固醇,high-density lipoprotein cholesterol,HDL-C;*表示P<0.05(下同)。
2.2.3 亚急性毒性
2.2.3.1 质量和摄食
如图4所示,各剂量组个体质量与对照组相比均无显著差异,这表明Akk在3种剂量浓度下不影响动物的个体质量和进食状态,对实验动物的基础代谢平衡和摄食行为无可观测的生物学影响。
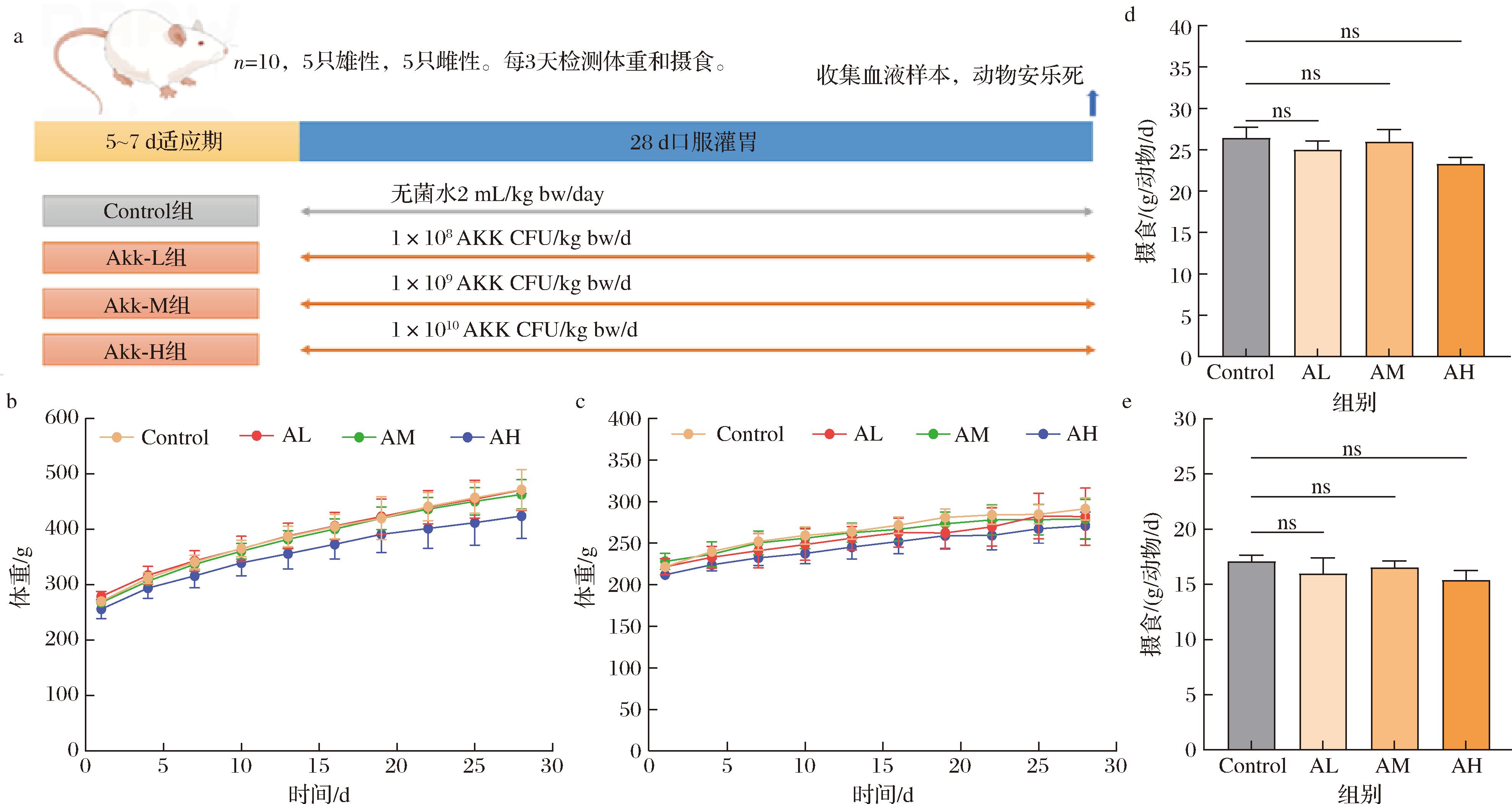
a-实验设计;b-雄性动物各组体质量;c-雌性动物各组体质量;d-雄性动物各组摄食;e-雌性动物各组摄食
图4 亚急性毒性实验
Fig.4 Subacute toxicity
2.2.3.2 血常规
血常规检测显示(表5)雌性动物的3个剂量组红细胞分布宽度变异系数均显著下降(P<0.05),但3组间未见统计学差异,其他血液学参数与对照组无显著性异常。
表5 亚急性毒性血液学参数
Table 5 Hematological parameters of subacute toxicity
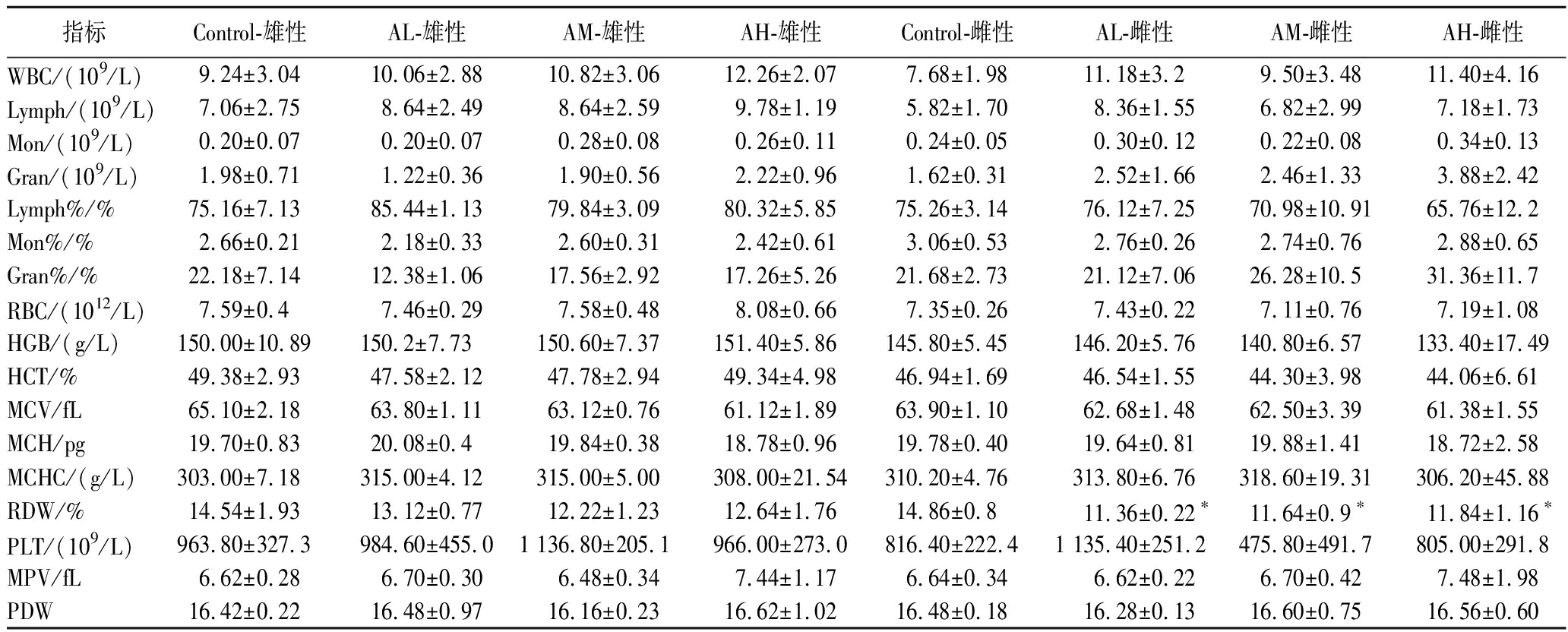
指标Control-雄性AL-雄性AM-雄性AH-雄性Control-雌性AL-雌性AM-雌性AH-雌性WBC/(109/L)9.24±3.0410.06±2.8810.82±3.0612.26±2.077.68±1.9811.18±3.29.50±3.4811.40±4.16Lymph/(109/L)7.06±2.758.64±2.498.64±2.599.78±1.195.82±1.708.36±1.556.82±2.997.18±1.73Mon/(109/L)0.20±0.070.20±0.070.28±0.080.26±0.110.24±0.050.30±0.120.22±0.080.34±0.13Gran/(109/L)1.98±0.711.22±0.361.90±0.562.22±0.961.62±0.312.52±1.662.46±1.333.88±2.42Lymph%/%75.16±7.1385.44±1.1379.84±3.0980.32±5.8575.26±3.1476.12±7.2570.98±10.9165.76±12.2Mon%/%2.66±0.212.18±0.332.60±0.312.42±0.613.06±0.532.76±0.262.74±0.762.88±0.65Gran%/%22.18±7.1412.38±1.0617.56±2.9217.26±5.2621.68±2.7321.12±7.0626.28±10.531.36±11.7RBC/(1012/L)7.59±0.47.46±0.297.58±0.488.08±0.667.35±0.267.43±0.227.11±0.767.19±1.08HGB/(g/L)150.00±10.89150.2±7.73150.60±7.37151.40±5.86145.80±5.45146.20±5.76140.80±6.57133.40±17.49HCT/%49.38±2.9347.58±2.1247.78±2.9449.34±4.9846.94±1.6946.54±1.5544.30±3.9844.06±6.61MCV/fL65.10±2.1863.80±1.1163.12±0.7661.12±1.8963.90±1.1062.68±1.4862.50±3.3961.38±1.55MCH/pg19.70±0.8320.08±0.419.84±0.3818.78±0.9619.78±0.4019.64±0.8119.88±1.4118.72±2.58MCHC/(g/L)303.00±7.18315.00±4.12315.00±5.00308.00±21.54310.20±4.76313.80±6.76318.60±19.31306.20±45.88RDW/%14.54±1.9313.12±0.7712.22±1.2312.64±1.7614.86±0.8 11.36±0.22∗11.64±0.9∗11.84±1.16∗PLT/(109/L)963.80±327.3984.60±455.01 136.80±205.1966.00±273.0816.40±222.41 135.40±251.2475.80±491.7805.00±291.8MPV/fL6.62±0.286.70±0.306.48±0.347.44±1.176.64±0.346.62±0.226.70±0.427.48±1.98PDW16.42±0.2216.48±0.9716.16±0.2316.62±1.0216.48±0.1816.28±0.1316.60±0.7516.56±0.60
红细胞分布宽度变异系数是一种常规全血细胞计数参数,用于评估循环中红细胞大小的异质性[18],健康SD大鼠的红细胞分布宽度正常范围为11.0%~15.5%,本研究中各组动物的平均值均处于正常生理范围内。红细胞分布宽度变异系数的下降提示Akk对红细胞系统具有调节作用,可在一定程度上恢复生理功能,减少炎症反应。
2.2.3.3 血清生化
如表6所示,在雌性大鼠中,检测到AM、AH组天门冬氨酸氨基转移酶水平与对照组相比出现不同程度的降低(P<0.05)。谷氨酸氨基转移酶和天门冬氨酸氨基转移酶是参与肝脏糖异生的转氨酶,当肝细胞膜受损时,这2种酶会溢出至血液循环,使其血清水平升高[19]。谷氨酸氨基转移酶长期被视为肝损伤的传统血清标志物,现有研究多聚焦于其病理性升高的诊断价值,而血清谷氨酸氨基转移酶水平下降缺乏特异性临床指向[20]。
表6 亚急性毒性血清生化参数
Table 6 Subacute toxicity serum biochemical parameters
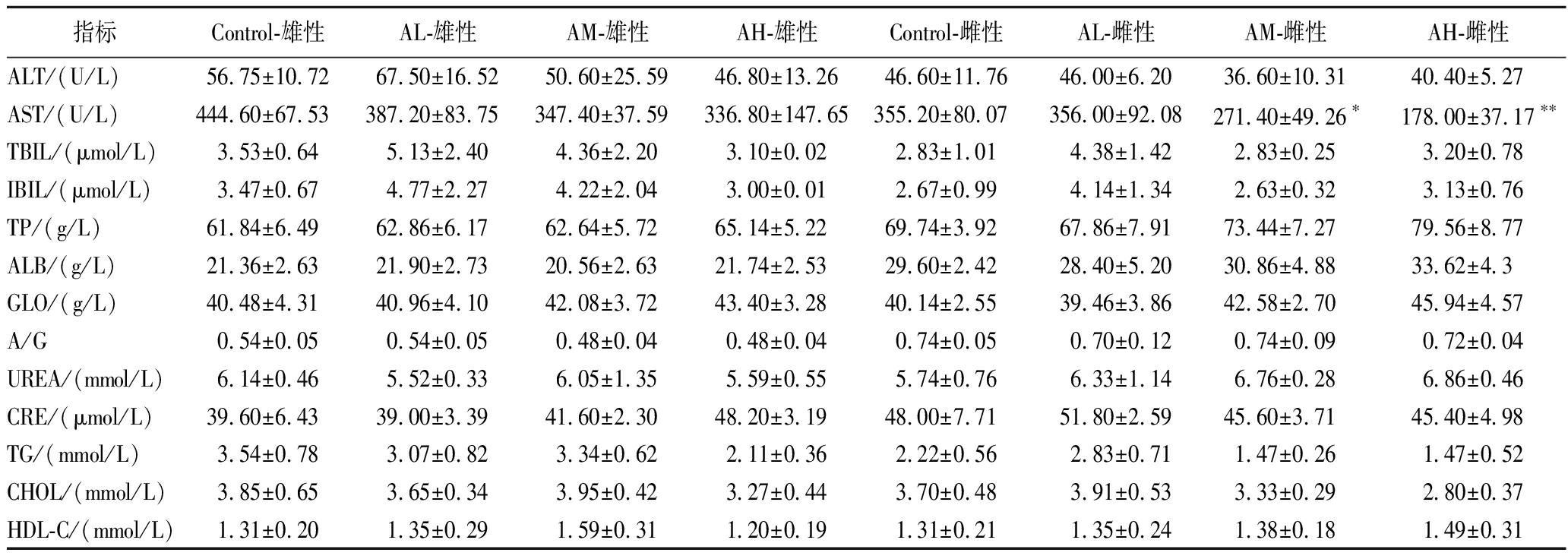
指标Control-雄性AL-雄性AM-雄性AH-雄性Control-雌性AL-雌性AM-雌性AH-雌性ALT/(U/L)56.75±10.7267.50±16.5250.60±25.5946.80±13.2646.60±11.7646.00±6.2036.60±10.3140.40±5.27AST/(U/L)444.60±67.53387.20±83.75347.40±37.59336.80±147.65355.20±80.07356.00±92.08271.40±49.26∗178.00±37.17∗∗TBIL/(μmol/L)3.53±0.645.13±2.404.36±2.203.10±0.022.83±1.014.38±1.422.83±0.253.20±0.78IBIL/(μmol/L)3.47±0.674.77±2.274.22±2.043.00±0.012.67±0.994.14±1.342.63±0.323.13±0.76TP/(g/L)61.84±6.4962.86±6.1762.64±5.7265.14±5.2269.74±3.9267.86±7.9173.44±7.2779.56±8.77ALB/(g/L)21.36±2.6321.90±2.7320.56±2.6321.74±2.5329.60±2.4228.40±5.2030.86±4.8833.62±4.3GLO/(g/L)40.48±4.3140.96±4.1042.08±3.7243.40±3.2840.14±2.5539.46±3.8642.58±2.7045.94±4.57A/G0.54±0.050.54±0.050.48±0.040.48±0.040.74±0.050.70±0.120.74±0.090.72±0.04UREA/(mmol/L)6.14±0.465.52±0.336.05±1.355.59±0.555.74±0.766.33±1.146.76±0.286.86±0.46CRE/(μmol/L)39.60±6.4339.00±3.3941.60±2.3048.20±3.1948.00±7.7151.80±2.5945.60±3.7145.40±4.98TG/(mmol/L)3.54±0.783.07±0.823.34±0.622.11±0.362.22±0.562.83±0.711.47±0.261.47±0.52CHOL/(mmol/L)3.85±0.653.65±0.343.95±0.423.27±0.443.70±0.483.91±0.533.33±0.292.80±0.37HDL-C/(mmol/L)1.31±0.201.35±0.291.59±0.311.20±0.191.31±0.211.35±0.241.38±0.181.49±0.31
注:**表示P<0.01。
2.2.3.4 脏器系数
如表7所示,脏器系数结果显示雌性动物的AH组肾脏脏器系数(0.72±0.05)显著大于对照组(0.63±0.03)。传统毒理学认为,脏器系数的异常反映了器官的异常,脏器系数增加表明实验动物的器官充血、水肿、肥大等变化,脏器系数降低表明实验动物器官可能萎缩、退化等变化[21]。但也有研究提出,脏器指数变化或表征器官的功能代偿与生理适应[22],脏器质量的变化是否具有毒理学意义应与组织形态学和病理学结果相结合。
表7 亚急性毒性脏器系数
Table 7 Subacute toxicity organ coefficient
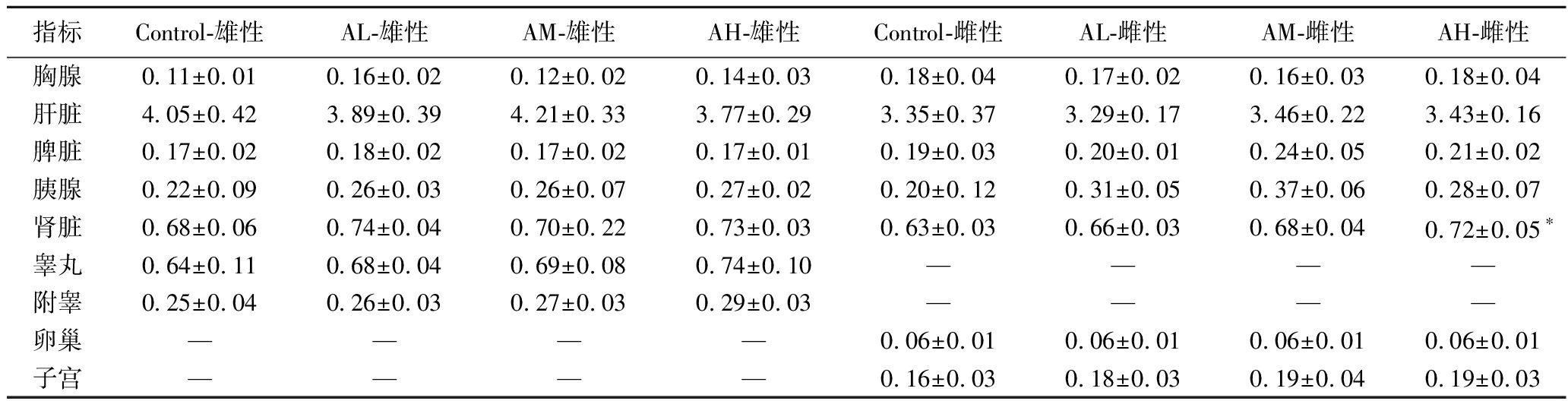
指标Control-雄性AL-雄性AM-雄性AH-雄性Control-雌性AL-雌性AM-雌性AH-雌性胸腺0.11±0.010.16±0.020.12±0.020.14±0.030.18±0.040.17±0.020.16±0.030.18±0.04肝脏4.05±0.423.89±0.394.21±0.333.77±0.293.35±0.373.29±0.173.46±0.223.43±0.16脾脏0.17±0.020.18±0.020.17±0.020.17±0.010.19±0.030.20±0.010.24±0.050.21±0.02胰腺0.22±0.090.26±0.030.26±0.070.27±0.020.20±0.120.31±0.050.37±0.060.28±0.07肾脏0.68±0.060.74±0.040.70±0.220.73±0.030.63±0.030.66±0.030.68±0.040.72±0.05∗睾丸0.64±0.110.68±0.040.69±0.080.74±0.10————附睾0.25±0.040.26±0.030.27±0.030.29±0.03————卵巢————0.06±0.010.06±0.010.06±0.010.06±0.01子宫————0.16±0.030.18±0.030.19±0.040.19±0.03
2.2.3.5 组织病理学
对高剂量组和对照组动物的肝脏、脾脏、肾脏、胸腺、胰腺、结肠、雄鼠的睾丸和附睾以及雌鼠的子宫和卵巢进行了HE染色,结果显示检测的脏器组织形态结构良好,未见毒性作用(图5)。
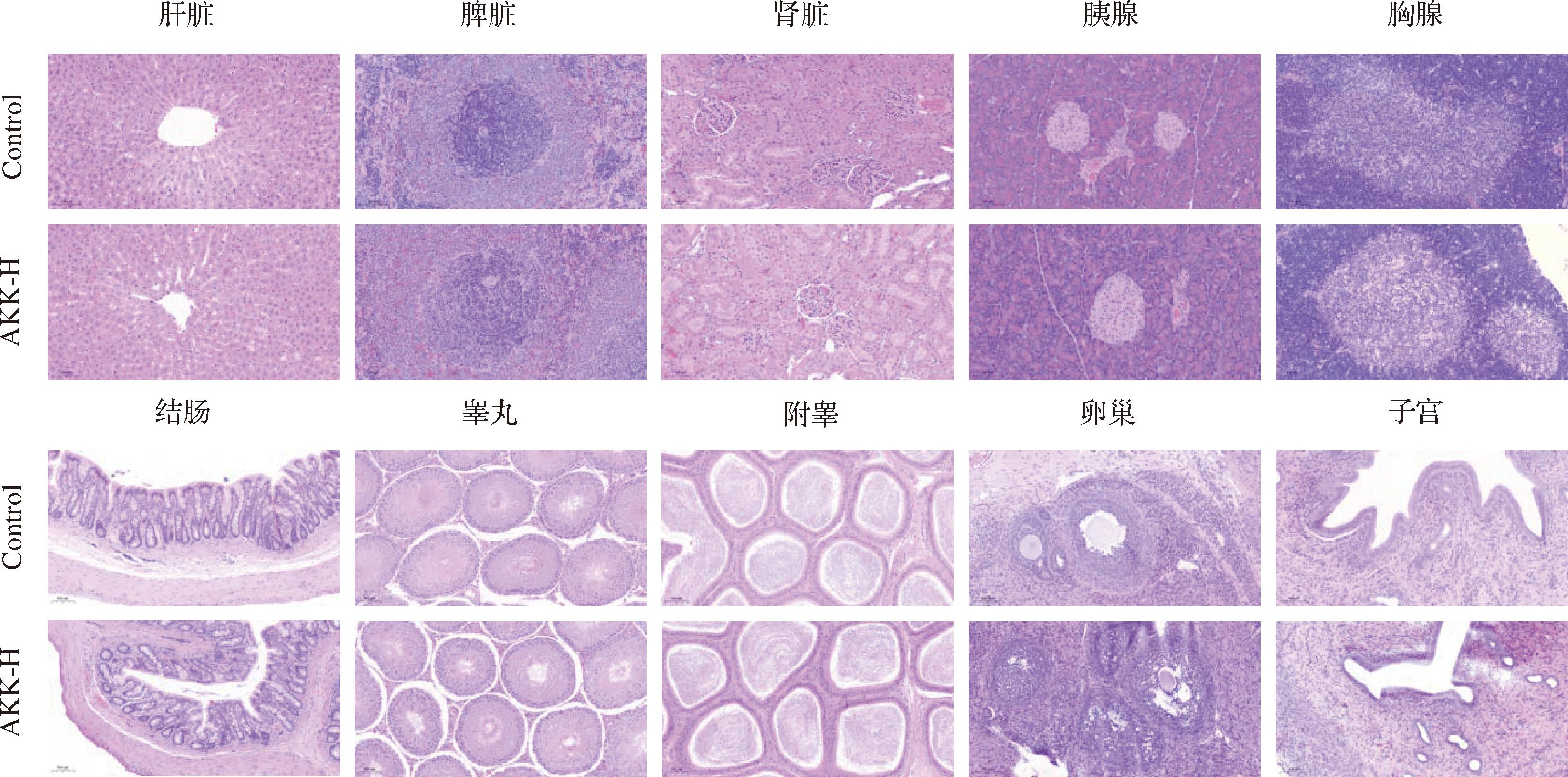
图5 对照组和高剂量组的组织病理学结果
Fig.5 Histopathological results of control group and high dose group
3 结论与讨论
在本研究中对Akk ATCC BAA835的黏附特性、抗氧化性、耐受性和安全性进行了全面的评估。在厌氧培养条件下,Akk在14 h进入稳定期,吸光度(OD600)稳定在0.6左右。为非生物膜产生者,在24 h的自动聚集率达到37.97%,为中等聚集能力。Akk在3种有机溶剂中的疏水作用表现较好,8 h疏水作用均超过50%,其中在二甲苯中为70.42%。但与其他菌株相比,黏附特性表现较弱,Akk DSM 22959、Akk PROBIO和Akk ONE这3株菌在二甲苯中的疏水性在60 min便可达到30%以上,24 h聚集力均在50%以上[8-10]。抗氧化实验表明,Akk发酵液对DPPH自由基和超氧阴离子自由基的清除能力显著优于菌悬液及无细胞上清液,清除率分别达到了17.95 μg Trolox/mL和112.34 U/L。耐受性实验结果显示,菌株在极端酸性和胆盐条件下的耐受性良好,在SGF和SIF中的存活率均高于95%,相比于Akk PROBIO在SGF和SIF中暴露2 h后的存活率分别为84%和82%,展现出更加优异的消化道环境适应能力。
急性毒性实验显示,动物在单次口服1×1010、1×1011 CFU/kg bw菌液后,没有发现动物死亡或行为异常,血常规和血清生化参数与灌胃同等体积无菌水的对照组无统计学差异,值得注意的是,在1×1011 CFU/kg bw组发现胆固醇水平出现一定降低。进一步的亚急性毒性检测结果显示,菌株在1×108~1×1010 CFU/kg bw/d这3种剂量下连续口服28 d后,实验动物的质量、摄食与对照组一致,血常规检测显示在灌胃Akk后,RDW值显著下降,提示菌株对红细胞生理状态的改善。血清生化检测中,雌性动物AST水平与对照组相比出现显著降低,但其降低并非指示毒性作用。杨立峰等[23]对150只健康雌性SD大鼠脏器系数进行检测,结果显示其平均值为0.674±0.041,95%参考值范围0.595~0.754。本研究中脏器系数分析显示雌性动物高剂量组的肾脏质量较对照组而言出现轻微升高(0.72±0.05),但其仍处于健康范围内,且结合本研究所检测的血清生化中肾脏功能指标(尿素、肌酐)以及组织病理学检测均未显示异常变化,因此判定指数的变化为动物的正常生理波动并非毒性作用。
综上研究表明,Akk ATCC BAA835展现出良好的益生特性和生物安全性,研究结果为Akk的后续应用提供了重要的安全性依据。
[1] CANI P D,DEPOMMIER C,DERRIEN M,et al.Akkermansia muciniphila:Paradigm for next-generation beneficial microorganisms[J].Nature Reviews Gastroenterology &Hepatology,2022,19(10):625-637.
[2] PLOVIER H,EVERARD A,DRUART C,et al.A purified membrane protein from Akkermansia muciniphila or the pasteurized bacterium improves metabolism in obese and diabetic mice[J].Nature Medicine,2017,23(1):107-113.
[3] LIU Q,LU W W,TIAN F W,et al.Akkermansia muciniphila exerts strain-specific effects on DSS-induced ulcerative colitis in mice[J].Frontiers in Cellular and Infection Microbiology,2021,11:698914.
[4] ZHAI Q X,FENG S S,ARJAN N,et al.A next generation probiotic,Akkermansia muciniphila[J].Critical Reviews in Food Science and Nutrition,2019,59(19):3227-3236.
[5] QU S,ZHENG Y H,HUANG Y C,et al.Excessive consumption of mucin by over-colonized Akkermansia muciniphila promotes intestinal barrier damage during malignant intestinal environment[J].Frontiers in Microbiology,2023,14:1111911.
[6] WANG W Y,LI N,XU H K,et al.ILC3 s regulate the gut microbiota via host intestinal galactosylation to limit pathogen infection in mice[J].Nature Microbiology,2025,10(3):654-666.
[7] XIE K H,CAI W D,LI L J,et al.Probiotic administration aggravates dextran sulfate sodium salt-induced inflammation and intestinal epithelium disruption in weaned pig[J].Animal Microbiome,2025,7(1):8.
[8] COZZOLINO A,VERGALITO F,TREMONTE P,et al.Preliminary evaluation of the safety and probiotic potential of Akkermansia muciniphila DSM 22959 in comparison with Lactobacillus rhamnosus GG[J].Microorganisms,2020,8(2):189.
[9] LV N,WANG C P,ZHOU H T,et al.Genome-and toxicology-based safety assessment of probiotic Akkermansia muciniphila ONE isolated from humans[J].Foods,2024,13(13):1979.
[10] MA X,TIAN M,YU X P,et al.Characterization and preliminary safety evaluation of Akkermansia muciniphila PROBIO[J].Foods,2024,13(3):442.
[11] LI L F,LI M C,CHEN Y H,et al.Function and therapeutic prospects of next-generation probiotic Akkermansia muciniphila in infectious diseases[J].Frontiers in Microbiology,2024,15:1354447.
[12] ZHANG C,MA K J,NIE K,et al.Assessment of the safety and probiotic properties of Roseburia intestinalis:A potential “Next Generation Probiotic”[J].Frontiers in Microbiology,2022,13:973046.
[13] ALIZADEH BEHBAHANI B,JOOYANDEH H,HOJJATI M,et al.Evaluation of probiotic,safety,and anti-pathogenic properties of Levilactobacillus brevis HL6,and its potential application as bio-preservatives in peach juice[J].LWT,2024,191:115601.
[14] TARIQUE M,ABDALLA A,MASAD R,et al.Potential probiotics and postbiotic characteristics including immunomodulatory effects of lactic acid bacteria isolated from traditional yogurt-like products[J].LWT,2022,159:113207.
[15] 周闯,宋俊雅,叶菁,等.1株马乳酒样乳杆菌的分离鉴定及益生特性研究[J].中国畜牧兽医,2023,50(7):2974-2986.ZHOU C,SONG J Y,YE J,et al.Isolation,identification and probiotic properties of a strain of Lactobacillus kefiranofaciens[J].China Animal Husbandry &Veterinary Medicine,2023,50(7):2974-2986.
[16] LI Y J,ZHUANG Y L,TIAN W H,et al.In vivo acute and subacute toxicities of phenolic extract from rambutan (Nephelium lappaceum) peels by oral administration[J].Food Chemistry,2020,320:126618.
[17] MONTORO B P,BENOMAR N,LAVILLA LERMA L,et al.Fermented alore a table olives as a source of potential probiotic Lactobacillus pentosus strains[J].Frontiers in Microbiology,2016,7:1583.
a table olives as a source of potential probiotic Lactobacillus pentosus strains[J].Frontiers in Microbiology,2016,7:1583.
[18] YANG K,PAN Y,YAN B,et al.Red blood cell distribution width-standard deviation but not red blood cell distribution width-coefficient of variation as a potential index for the diagnosis of iron-deficiency Anemia in mid-pregnancy women[J].Open Life Sciences,2021,16(1):1213-1218.
[19] AGRAWAL S,DHIMAN R K,LIMDI J K.Evaluation of abnormal liver function tests[J].Postgraduate Medical Journal,2016,92(1086):223-234.
[20] TAMBER S S,BANSAL P,SHARMA S,et al.Biomarkers of liver diseases[J].Molecular Biology Reports,2023,50(9):7815-7823.
[21] DONG Z,XING S Y,ZHANG J Y,et al.14-day repeated intraperitoneal toxicity test of ivermectin microemulsion injection in wistar rats[J].Frontiers in Veterinary Science,2020,7:598313.
[22] SUN S A,LI B,WU M M,et al.Effect of dietary supplemental vitamin C and betaine on the growth performance,humoral immunity,immune organ index,and antioxidant status of broilers under heat stress[J].Tropical Animal Health and Production,2023,55(2):96.
[23] 杨立峰,黄燕倩,莫怡飞,等.医疗器械亚慢性毒性试验SD大鼠生理指标历史对照参考值范围的建立[J].中国医疗器械信息,2024,30(9):23-26.YANG L F,HUANG Y Q,MO Y F et al.Establishment of historical reference values for physiological indexes of SD rats in subchronic toxicity test of medical devices[J].China Medical Device Information,2024,30(9):23-26.