贻贝(Mytilus spp.)因高营养价值被誉为“海中鸡蛋”,其蛋白质含量高,脂肪含量低,且富含必需氨基酸、多不饱和脂肪酸及硒、锌等微量元素[1]。然而,贻贝收获期集中,通常在3~4个月内集中捕捞,加之其水分含量高达75%~80%,捕捞后易腐败变质,导致保鲜周期短、流通半径受限。目前市售贻贝制品(如生腌、烟熏等)虽可短期贮藏,但因含水量较高,难以有效抑制微生物增殖,产品保质期普遍不足15 d,严重制约了规模化加工与跨区域销售。相比之下,干制贻贝通过脱水显著降低水分活度,抑制微生物增殖与酶活性,可实现长期贮藏。该工艺不仅能突破季节性供应限制,减少资源浪费,还可最大限度保留贻贝的蛋白质、微量元素等营养成分,同时赋予产品独特风味。目前贻贝干制加工最常用的方法是热风或热泵干燥,但该方法存在干燥时间长、能耗高的缺点,由此导致在长时间干燥过程中发生多种品质裂变,如褐变、脂氧化等。开发新型贻贝干制加工方法,提高其干燥速率,缩短干燥时间,缓解长时间干燥过程中发生的品质裂变反应,这对节能、提高产品品质都有重要意义。
冷等离子体(cold plasma,CP)是一种通过高能电场电离气体产生的正负离子组成的离子化气体状物质,其体系温度接近室温,包含带电粒子、活性氧/氮基团(reactive oxygen species/reactive nitrogen species,ROS/RNS)、紫外辐射等多种物理/化学作用因子[2]。已有研究表明,CP作为一种前处理方法在食品加工中显示出显著效果,包括减菌、促进生物活性物质提取、提升腌制品品质及食用油氢化预处理等[3]。在水产品加工中,CP对鱼、虾、贝等水产原料具有很好的减菌、保持品质和延长货架期的作用[4]。CP在食品加工中的应用机制主要依赖于其产生的ROS/RNS、带电粒子、紫外辐射、电场等化学或物理因子,这些因子能够导致微生物细胞的死亡,或引起食品原料的氧化和物理修饰[5]。自2019年以来,研究人员发现,CP预处理可显著提高多种植物源食品的干燥效率,提高多酚、黄酮等生物活性物质的保留率[6-7]。近期的研究观察到CP预处理能显著加速贻贝肉的热泵干燥速率。具体而言,按照本文条件处理,贻贝肉干燥至15%水分所需时间从19.06 h缩短至11.69 h,降低了热加工引发的不良变化,进而显著提高干制品质。然而,CP协同干燥对干制贻贝的贮藏品质的影响尚不明确。
鉴于此,本研究以厚壳贻贝(Mytilus coruscus)为原料,系统研究了冷等离子体协同处理对热泵干制贻贝在不同温度(-18、4、25 ℃)下贮藏品质的影响。通过监测菌落总数、挥发性盐基氮(total volatile basic nitrogen,TVB-N)、pH值、复水率、硫代巴比妥酸值(thiobarbituric acid reactive substance,TBARS)及羰基含量等关键指标,结合零级/一级动力学模型与Arrhenius方程构建货架期预测模型。本研究结果可为CP技术在水产品干制加工中的应用提供理论依据与指导。
1 材料与方法
1.1 材料与试剂
新鲜贻贝,浙江省湖州市德清县秋山水产市场,并于25 min内运送至实验室。贻贝在沸水中热烫15 s,手工取出完整贻贝肉。使用电子天平筛选(15±1.0) g的贻贝肉,用于后续实验。将贻贝肉均匀平铺于不锈钢网沥水。
平板计数琼脂(plate count agar,PCA)、硫代巴比妥酸(thiobarbituric acid,TBA)、轻质氧化镁、硼酸、磷酸钠、氯化钠、三氯乙酸(trichloroacetic acid,TCA)、无水乙醇、甲基红、溴甲酚绿、2,4-二硝基苯肼(2,4-dinitrophenylhydrazine,DNPH)、盐酸、乙酸乙酯、盐酸胍,以上试剂均为分析纯,购自国药化学试剂有限公司(中国上海)。
1.2 仪器与设备
CTP-2000KP冷等离子体设备,南京苏曼等离子体有限公司;GWOE-3HP热泵干燥设备,杭州艾门特科技有限公司;K9840凯氏定氮仪,海能未来技术集团股份有限公司;PTY-124/223电子天平,华智(福建)电子技术有限公司;HX-4拍打式均质器,上海沪析实业有限公司;Spark 20M酶标仪,瑞士帝肯实验器材有限公司;PD500-TP均质机,格林普利玛有限公司;HWS-160恒温培养箱,宁波科技园区新江南仪器有限公司;YC-725L低温冰箱,中科美菱低温科技股份有限公司;D2400真空包装机,温州卓腾包装机械有限公司;HH-4恒温水浴锅,常州金坛良友仪器有限公司;FE28 pH计,梅特勒-托利多仪器有限公司;CHT210R离心机,湖南湘仪实验室仪器开发有限公司。
1.3 实验方法
1.3.1 贻贝的CP-热泵干燥联合处理
取1.1节贻贝肉置于热泵干燥装置中,设定干燥温度为60 ℃,湿度为15%,此条件下先干燥2 h,以脱除表面水分。之后,进行冷等离子体处理,射流口到样品的距离为3 cm,工作气体为空气,处理时间为3 min,处理电压为10 kV,频率为10 kHz。处理完成后,将贻贝置于热泵装置继续进行干燥。以不经CP处理,直接进行热泵干燥的样品作为对照,二者分别记为CP-热泵制品和热泵制品。根据前期研究建立的Logarithmic干燥模型,CP-热泵制品和热泵制品干燥至水分含量15%所需的干燥时间分别为11.69、19.06 h。干燥结束后CP-热泵制品与热泵制品水分含量分别为(15.18±0.21)%和(15.01±0.22)%。该实验所用的CP参数是经预实验筛选得出的。
1.3.2 贮藏实验
将制备的干制贻贝冷却至室温后,装入真空袋中密封保存。分别放进-18 ℃低温冰箱、4 ℃恒温培养箱和25 ℃的恒温培养箱中进行贮藏,恒温培养箱湿度设置为80%。-18、4 ℃贮藏每隔15 d取一次样品,25 ℃贮藏每隔5 d取一次样品,进行指标测定,每个指标重复测定3次,结果取平均值。
1.3.3 菌落总数测定
将10 g样品加入90 mL 0.85%(体积分数)无菌生理盐水中,然后使用拍打式均质器匀浆3 min。随后,使用无菌生理盐水以10倍的增量进行梯度稀释。取1 mL稀释样品转移到PCA培养基平板上,然后在30 ℃恒温箱下孵育72 h以进行菌落计数,结果以lg CFU/g计。
1.3.4 TVB-N含量测定
根据GB 5009.228—2016《食品安全国家标准 食品中挥发性盐基氮的测定》中所述的自动凯氏定氮法,并稍作修改。先将贻贝样品破碎再称取5 g碎肉于离心管中,加入50 mL去离子水振荡,摇匀,使样品分散均匀。室温孵育30 min后,以8 000 r/min离心10 min,取上清液,倒入蒸馏管中,加入1 g轻质氧化镁,立刻连接自动凯氏定氮仪蒸馏管上,按仪器操作开始测定。同时,添加30 mL 20 g/L的硼酸溶液,加入10滴显色指示剂(1 g/L甲基红乙醇溶液与1 g/L溴甲酚绿乙醇溶液按体积比1∶5混合)于锥形瓶中,收集蒸馏液。最后,以0.01 mol/L盐酸标准溶液滴定,终点颜色呈紫红色。不加样品的测试管为仪器空白,每组样品重复3次,结果取平均值,TVB-N含量的计算如公式(1)所示:
(1)
式中:X为样品中挥发性盐基氮的含量,mg/100 g;V1为样品滴定消耗盐酸标准溶液的体积,mL;V2为空白滴定消耗盐酸标准溶液的体积,mL;C为盐酸标准溶液的浓度,mol/L;14为滴定1.0 mL 1.00 mol/L盐酸标准滴定溶液相当的氮的质量,g/mol;100为计算结果的换算系数;m为称取样品质量,g。
1.3.5 pH值测定
根据GB 5009.237—2016《食品安全国家标准 食品pH值的测定》,样品pH值由pH计的电极探针测定。
1.3.6 复水率测定
将取出的样品称重,记录质量为M0。然后将每个样品单独放入自封袋中,以料液比1∶100(g∶mL)加入去离子水。将密封袋浸入20 ℃的恒温水浴锅中6 h。充分复水后,将样品从自封袋中取出,并使用吸水纸轻轻吸取表面明水,不可挤压,然后进行称重,记录质量为M1。每组3个平行,结果取平均值。复水率的计算如公式(2)所示:
复水率![]()
(2)
式中:M1为样品复水后的质量,g;M0为样品复水前的质量,g。
1.3.7 TBARS测定
TBARS测定依据NING等[8]描述的方法,并稍作修改。首先,取5 g破碎后的样品加入100 mL离心管中,加入20 mL去离子水和25 mL 15%(体积分数,下同)TCA溶液混合。使用均质机对样品进行均质匀浆,孵育30 min。随后,在8 000 r/min离心10 min。将上清液转移至50 mL试管中,补加15% TCA 至刻度线,摇匀,吸取5 mL加到25 mL试管中。向每个试管中加入5 mL 0.02 mol/L的TBA溶液。之后,在沸水浴中加热30 min,形成粉红色物质。结束后,在流水下冷却。以去离子水代替样品做空白对照,在532 nm波长测其吸光度。TBARS表示为mg/kg样品。
1.3.8 总羰基含量测定
参照KANG等[9]描述的方法,稍作修改。取1 g破碎后的样品置于离心管中,加入10 mL 0.02 mol/L磷酸钠缓冲液(含0.6 mol/L NaCl,pH 7.2),并使用均质机均质30 s,以获得1∶10(g∶mL)的匀浆液。取0.5 mL匀浆液,加入到离心管中。之后,加入0.5 mL 10% TCA溶液,使蛋白质沉淀。然后,以8 000 r/min离心5 min,弃上清液。将不同离心管中收集到的沉淀分成2部分,一份加入1 mL 2 mol/L HCl作为对照,用于与DNPH对比分析;另一份加入1 mL 0.01 mol/L的DNPH(溶于2 mol/L HCl),用于评估羰基含量。所有样品在黑暗条件下孵育1 h,之后向样品中加入1 mL 20% TCA,再以8 000 r/min离心5 min得到沉淀。用1 mL V(乙酸乙酯)∶V(乙醇溶液)=1∶1洗涤沉淀,重复洗涤3次以充分洗去未反应的DNPH。随后,将所得沉淀溶解在1 mL磷酸钠缓冲液(含6 mol/L盐酸胍,pH值为7.2),并置于35 ℃水浴中,直至沉淀完全溶解。以8 000 r/min离心5 min,收集上清液。使用酶标仪在370 nm波长处测量吸光度,并利用22 000 L/(mol·cm)的摩尔吸光系数计算羰基含量。以每毫克蛋白质中含有的纳摩尔数蛋白(nmol/mg protein)表示。
1.3.9 货架期预测模型的建立
1.3.9.1 化学动力学方程
贮藏过程中的食品质量劣化,通常使用零级和一级动力学来表征。将干制贻贝贮藏期间测得的TVB-N、菌落总数和TBARS的测试值代入方程中求得反应速率k值,决定系数R2,用于评估零级和一级动力学模型。零级和一级动力学方程如公式(3)和公式(4)所示:
零级:A=A0+kt
(3)
一级:lnA=ln A0+kt
(4)
式中:A为样品贮藏第t天时观测的指标值,A0为样品贮藏0 d时观测的指标值,k是反应速率常数,t是贮藏时间,d。
1.3.9.2 Arrhenius方程
Arrhenius方程常用于温度对食品指标变化的影响分析,其中k与T的关系尤为重要,如方程(5)所示:
(5)
式中:k为在温度T下的反应速率常数;k0是频率因子;Ea是反应活化能,kJ/mol;R是理想气体常数,8.314 4 J/mol K;T是绝对温度,K。
1.3.9.3 货架期预测
温度对反应速率(k)的影响(根据Arrhenius方程确定)可通过动力学模型纳入货架期计算方程中,从而得出如公式(6)和公式(7)所示的预测模型[10]:
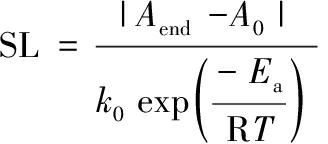
(6)
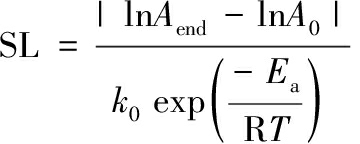
(7)
式中:SL为保存期预测值;Aend为贮藏结束时的指标观测值;A0为贮藏开始时的指标观测值。
1.4 数据处理与分析
试验数据均采用Excel和Origin 2024软件进行分析处理和图形绘制。采用IBM SPSS Statistics 25软件进行显著相关性分析。其中,采用单因素分析(one-way analysis of variance,ANOVA)进行差异性分析处理(P<0.05)。
2 结果与分析
2.1 CP协同处理对干制贻贝在贮藏期间菌落总数变化的影响
菌落总数是表征食品腐败程度的关键指标。CP-热泵制品与单一热泵制品在不同贮藏温度下菌落总数的变化如图1所示。其中,单一热泵组的初始菌落总数为4.364 lg CFU/g,而CP-热泵组仅为3.991 lg CFU/g。这表明CP协同处理可有效杀灭贻贝中微生物,这是由于CP所具有的较强的杀菌能力所致[11]。但由于CP在生物组织中的作用深度受限[12],其无法完全灭活内脏及消化腺等深层组织的微生物。
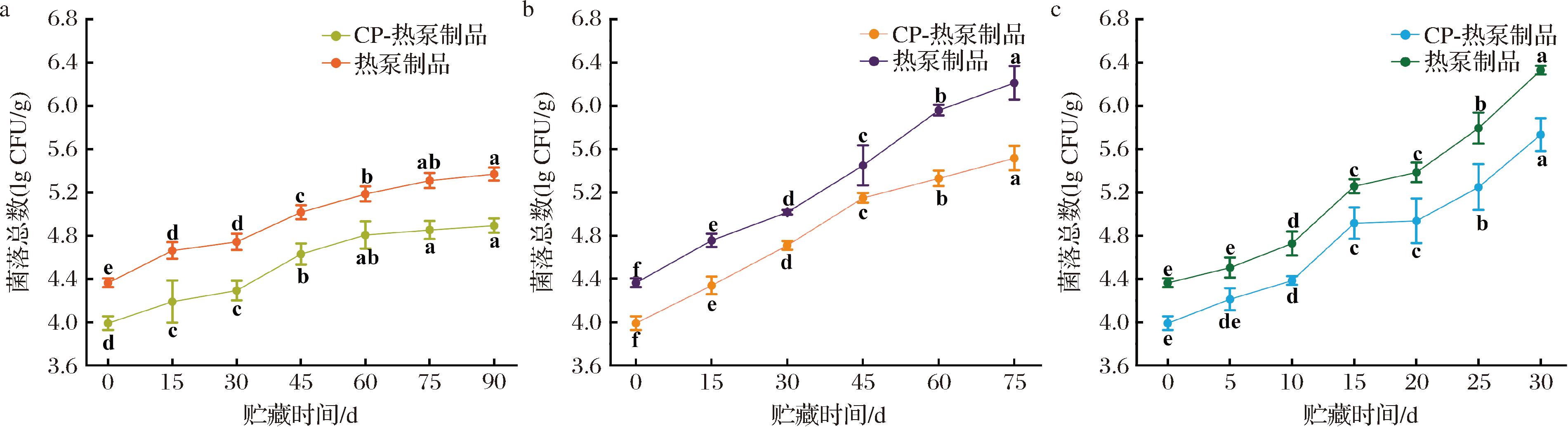
a--18 ℃;b-4 ℃;c-25 ℃
图1 CP协同处理对热泵干制贻贝在不同贮藏温度下菌落总数变化的影响
Fig.1 Effect of CP treatment on the change of total bacterial count of heat-pump dried mussels at different storage temperatures
注:不同小写字母表示组内显著差异(P<0.05)(下同)。
在整个贮藏期间,CP-热泵组与单一热泵组的菌落总数均随着贮藏时间的延长而增加,但CP-热泵组始终显著低于单一热泵组,这与CAI等[13]报道的研究结果一致。例如,在4 ℃条件下,贮藏15、45、75 d后,单一热泵组菌落总数分别增加至4.757 lg CFU/g、5.450 lg CFU/g和6.213 lg CFU/g(P<0.05),CP-热泵组菌落总数分别为4.340 lg CFU/g、5.150 lg CFU/g和5.517 lg CFU/g(P<0.05),分别低于前者0.417 lg CFU/g、0.300 lg CFU/g和0.696 lg CFU/g。在-18 ℃和25 ℃贮藏条件下,也得到了类似的结果。如,-18 ℃贮藏90 d后,单一热泵组和CP-热泵组菌落总数分别为4.893 lg CFU/g和5.370 lg CFU/g,后者比前者少了0.477 lg CFU/g;25 ℃贮藏30 d后,单一热泵组和CP-热泵组菌落总数分别为5.734 lg CFU/g和6.331 lg CFU/g,后者比前者少了0.597 lg CFU/g。这表明CP处理不仅能有效减少干制贻贝的初始菌落数,还能有效抑制贮藏期间微生物增殖,对延长货架期具有积极影响。
2.2 CP协同处理对干制贻贝在贮藏期间TVB-N变化的影响
TVB-N常被用于评价水产品鲜度,其含量变化是由于内源酶和微生物的作用使蛋白质分解而产生氨以及胺类等碱性含氮物质。CP-热泵组与单一热泵组在不同贮藏温度下TVB-N的变化如图2所示。CP-热泵组初始TVB-N值为13.103 mg/100 g,较对照组(15.960 mg/100 g)降低2.857 mg/100 g。这一结果说明CP处理可减少TVB-N等碱性氮类物质,可能的原因是CP处理时产生了某些酸性物质与其发生反应,从而降低其含量。OEHMIGEN等[14]报道,空气CP处理会产生多种氮氧化物,后者进一步与水反应生成硝酸根、亚硝酸根等物质,并导致pH降低。这些酸性物质可能是导致干制贻贝TVB-N降低的原因。
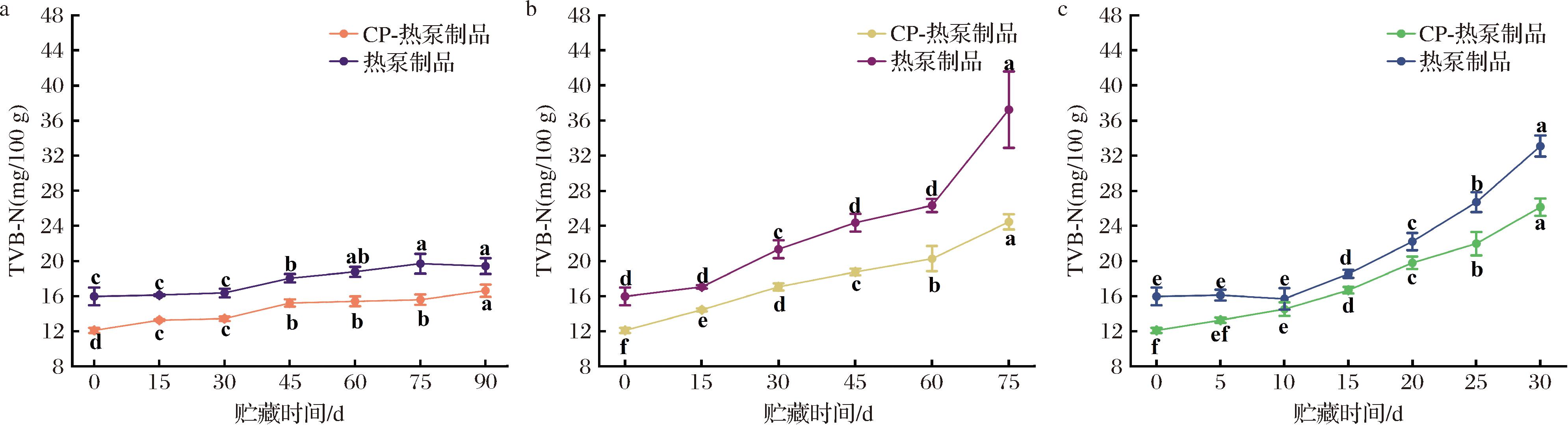
a--18 ℃;b-4 ℃;c-25 ℃
图2 CP协同处理对热泵干制贻贝在不同贮藏温度下TVB-N变化的影响
Fig.2 Effect of CP treatment on the change of TVB-N of heat-pump dried mussels at different storage temperatures
在整个贮藏期间,CP-热泵组与单一热泵组均随着贮藏时间的延长,TVB-N值逐渐增加,但前者始终低于后者。例如,在4 ℃条件下,贮藏15、45、75 d后,单一热泵组TVB-N值分别为17.043、24.360、37.240 mg/100 g(P<0.05),而CP-热泵组分别为14.430、18.740、24.447 mg/100 g(P<0.05),分别低于前者2.613、5.62、12.793 mg/100 g,这与ZOUELM等[15]的研究结果一致。在-18、25 ℃贮藏条件下,也得到了类似的结果。如,-18 ℃贮藏90 d后,单一热泵组和CP-热泵组TVB-N值分别为19.413、16.613 mg/100 g,后者比前者少了2.800 mg/100 g;25 ℃贮藏30 d后,单一热泵组和CP-热泵组TVB-N值分别为33.087、26.133 mg/100 g,后者比前者少了6.954 mg/100 g。CP-热泵组TVB-N值更低的原因除了上述CP产生的酸性物质与TVB-N类物质反应以外,还可能是由于CP处理通过减少初始菌落数和抑制内源酶活性,从而抑制了TVB-N的生成。这一结果表明,CP系统处理能显著提高贻贝干制品在贮藏期间的新鲜度。
2.3 CP协同处理对干制贻贝在贮藏期间pH变化的影响
CP-热泵组和单一热泵组样品在不同贮藏温度下pH的变化如图3所示。CP-热泵组样品初始pH 6.22,较单一热泵组(pH 6.27)低了0.05,这同样是由于CP产生的酸性物质所致。有研究显示,CP处理产生的氮氧化物与食品表面或食品基质中的水反应,进而降低食品的pH值[16]。在贮藏期间,随着贮藏时间的延长,2组样品的pH值增加,这可能是由于微生物代谢产生碱性化合物所致,而CP-热泵组始终低于单一热泵组。在4 ℃条件下,贮藏15、45、75 d后,单一热泵组pH值分别为6.35、6.51和6.84(P<0.05),CP-热泵组分别为6.28、6.38和6.61(P<0.05),分别低于前者0.07、0.13和0.23。而在-18 ℃ 和25 ℃贮藏条件下,也得到了类似的结果。如,-18 ℃贮藏90 d后,单一热泵组和CP-热泵组分别为6.47和6.41,后者比前者少了0.06;25 ℃贮藏30 d后,单一热泵组和CP-热泵组分别为6.91和6.71,后者比前者少了0.20。贮藏期间,CP-热泵组pH增加缓慢的原因可能正是由于CP协同处理减少了样品中的菌落总数,进而减少了碱性物质生成所致。
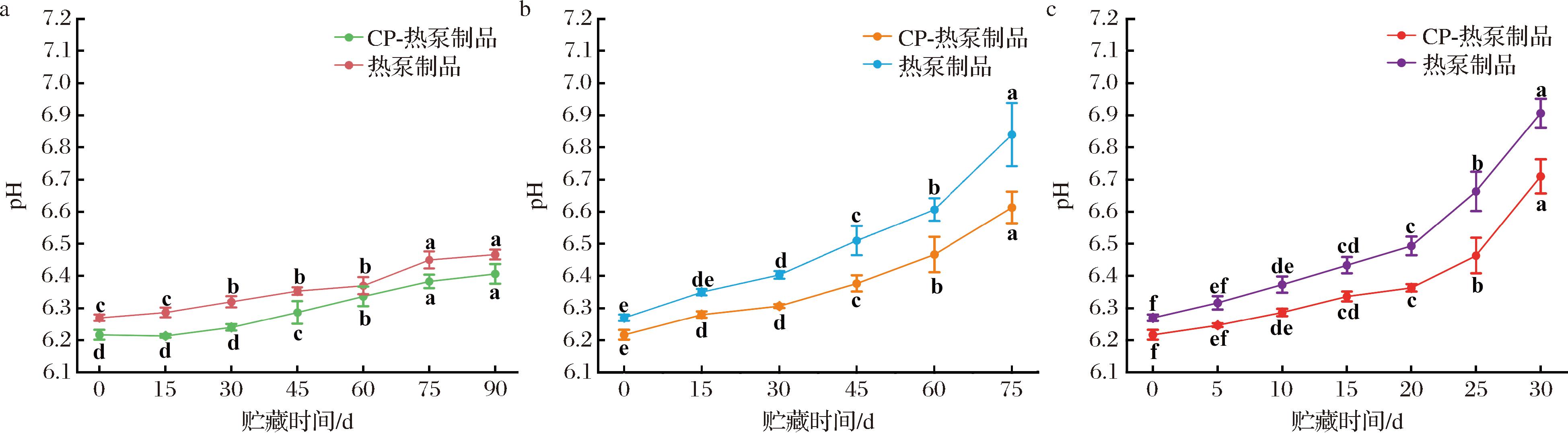
a--18 ℃;b-4 ℃;c-25 ℃
图3 CP协同处理对热泵干制贻贝在不同贮藏温度下pH变化的影响
Fig.3 Effect of CP treatment on the change of pH of heat-pump dried mussels at different storage temperatures
2.4 CP协同处理对干制贻贝在贮藏期间复水率变化的影响
复水率是评价干制品品质的关键指标。CP-热泵组与单一热泵组样品在贮藏期间复水率的变化情况如图4所示。在贮藏0 d时,CP-热泵组复水率达1.873,较单一热泵组的1.513显著提高了0.360,表明CP处理能显著提高干制贻贝的复水率。这可能是由于CP处理在贻贝表面产生微孔,从而加速了水分的渗透所致[17]。SHEN等[18]研究也显示,CP处理能诱导鱼干产品肌纤维断裂收缩,增加微孔结构,从而提高复水率。在整个贮藏期间,CP-热泵组与单一热泵组均随着贮藏时间的延长,样品复水率出现了波动。在不同贮藏温度下显示,单一热泵组在-18、25 ℃ 下并未发生显著变化(P<0.05)。而CP-热泵组复水率的变化则更为明显。例如,在4 ℃条件下,贮藏15、45、75 d后,单一热泵组复水率分别为1.456、1.427和1.470(P<0.05),CP-热泵组复水率分别为1.727、1.617和1.603(P<0.05),较比前者高了0.271、0.19和0.133,但与初始时相比CP-热泵组贻贝复水率有所降低。在25 ℃条件下也出现了类似的结果,当贮藏5、15、30 d后复水率分别为1.828、1.749、1.665,与初始时比降低了0.024、0.103和0.187。CP-热泵组在贮藏期间复水率的降低可能与蛋白质氧化变性程度有关,导致亲水性下降和结构致密化,降低了水分子与蛋白质的结合能力并阻碍水分的渗透吸收[19]。
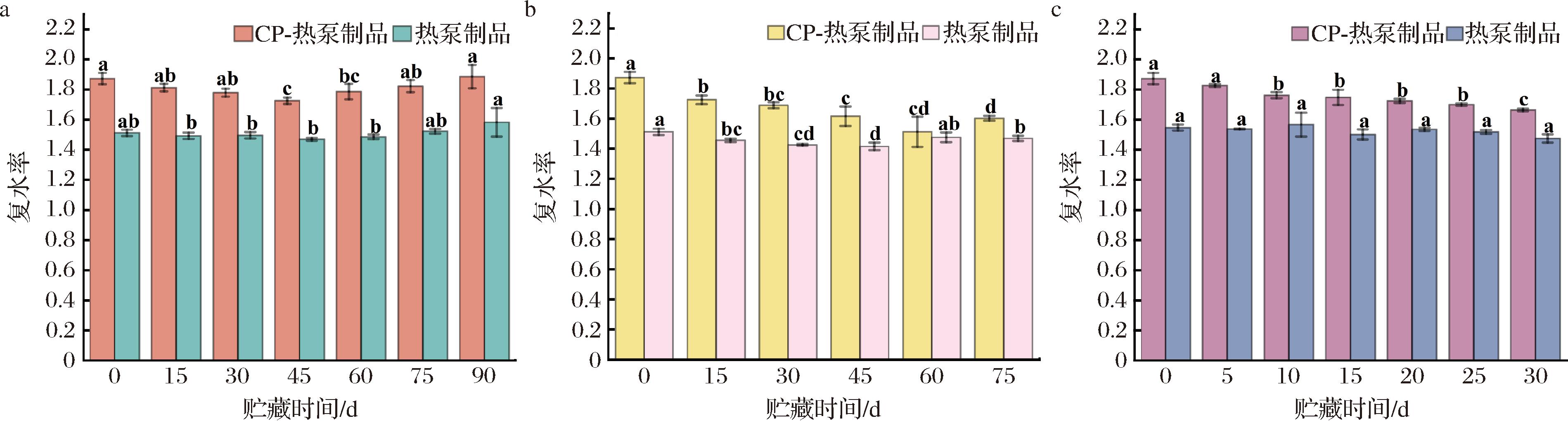
a--18 ℃;b-4 ℃;c-25 ℃
图4 冷等离子体协同处理对热泵干制贻贝在不同贮藏温度下复水率变化的影响
Fig.4 Effect of CP treatment on the change of rehydration ratio of heat-pump dried mussels at different storage temperatures
2.5 CP协同处理对干制贻贝在贮藏期间TBARS变化的影响
TBARS是肉品食品最常用的脂质氧化指标。CP-热泵组与单一热泵组样品在贮藏期间TBARS的变化如图5所示。在贮藏初始阶段(0 d),CP-热泵组TBARS值为2.30 mg/kg,相比较热泵组的3.43 mg/kg,降低了1.13 mg/kg。这是由于CP处理有效缩短了贻贝的热泵干燥时间,进而减少了干燥过程中的脂质氧化程度。HU等[20]研究发现,牡蛎在热风干燥过程TBARS的含量随干燥时间的延长而增加,说明干燥过程中贝类脂质会发生明显氧化。本文CP协同处理使得热泵干燥时间由19.06 h缩短至11.69 h,因此也就抑制了在此期间发生的脂质氧化。
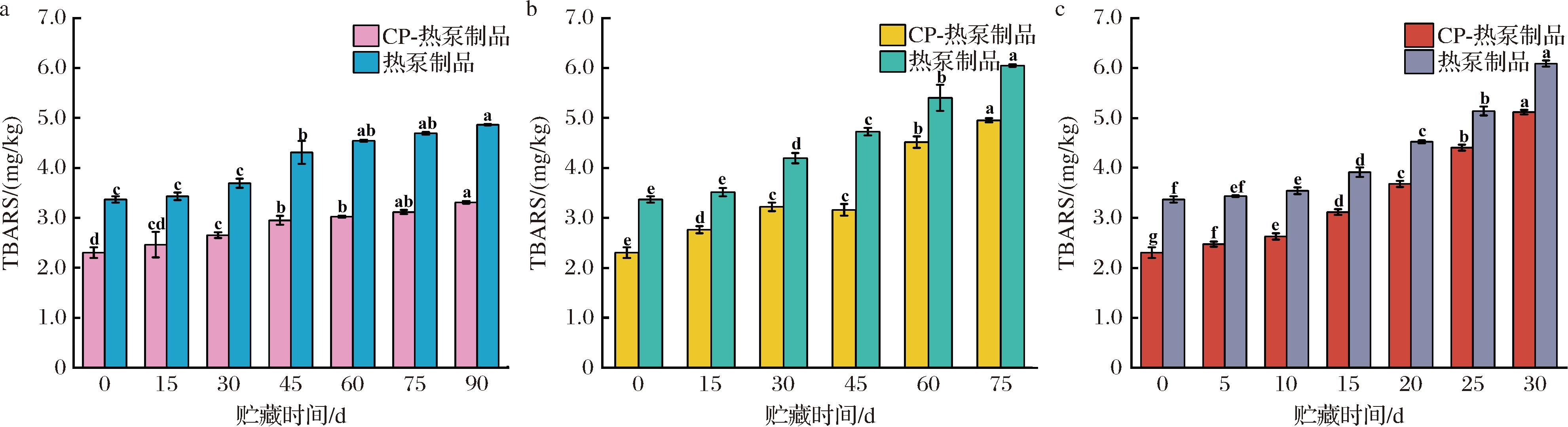
a--18 ℃;b-4 ℃;c-25 ℃
图5 CP协同处理对热泵干制贻贝在不同贮藏温度下TBARS变化的影响
Fig.5 Effect of CP treatment on the change of TBARS of heat-pump dried mussels at different storage temperatures
在贮藏期间,CP-热泵组TBARS值也始终低于单一热泵组。例如,在4 ℃条件下,贮藏15、45、75 d后,单一热泵组TBARS值分别为3.517、4.727、6.050 mg/kg(P<0.05),CP-热泵组分别为2.763、3.160、4.953 mg/kg(P<0.05),分别低于前者0.754、1.567、1.097 mg/kg。而在-18 ℃和25 ℃贮藏条件下,也得到了类似的结果。如-18 ℃贮藏90 d后,单一热泵组和CP-热泵组TBARS值分别为4.867、3.310 mg/kg,后者比前者少了1.557 mg/kg;25 ℃贮藏30 d后,单一热泵组和CP-热泵组TBARS值分别为6.090、5.117 mg/kg,后者比前者少0.973 mg/kg。在贮藏期间脂质发生复杂的自由基链式反应,产生醛、酮等小分子物质,其氧化程度与光、温度或酶等因素有关。因此,为有效维持样品品质,避免其因脂质氧化而降低质量与营养价值,合理选择贮藏条件尤为关键。
2.6 CP协同处理对干制贻贝在贮藏期间羰基含量变化的影响
羰基含量是评估蛋白质氧化程度的重要指标。它是在氧化胁迫条件下,蛋白质分子中侧链氨基酸残基被氧化修饰形成。研究显示,CP-热泵组的初始羰基含量为5.811 nmol/mg protein,显著高于单一热泵组(3.947 nmol/mg protein)(图6)。这是因为CP处理产生的ROS、RNS诱导了蛋白质的氧化[21]。WANG等[22]的研究也发现,介质阻挡放电冷等离子体处理会诱导猪肉蛋白氧化,降游离巯基含量。此外,CHEN等[23]研究也发现,大气冷等离子体处理3~5 min 会导致红虾肌原纤维蛋白过度氧化,影响其结构稳定性[23]。另外,CP处理产生的蚀刻效应使得ROS/RNS及自由基作用于更多组织中的蛋白质分子并使其暴露,而在随后的干燥及贮藏过程中,暴露的蛋白质分子与空气中氧气的接触增加,进而使得蛋白质氧化程度加深。
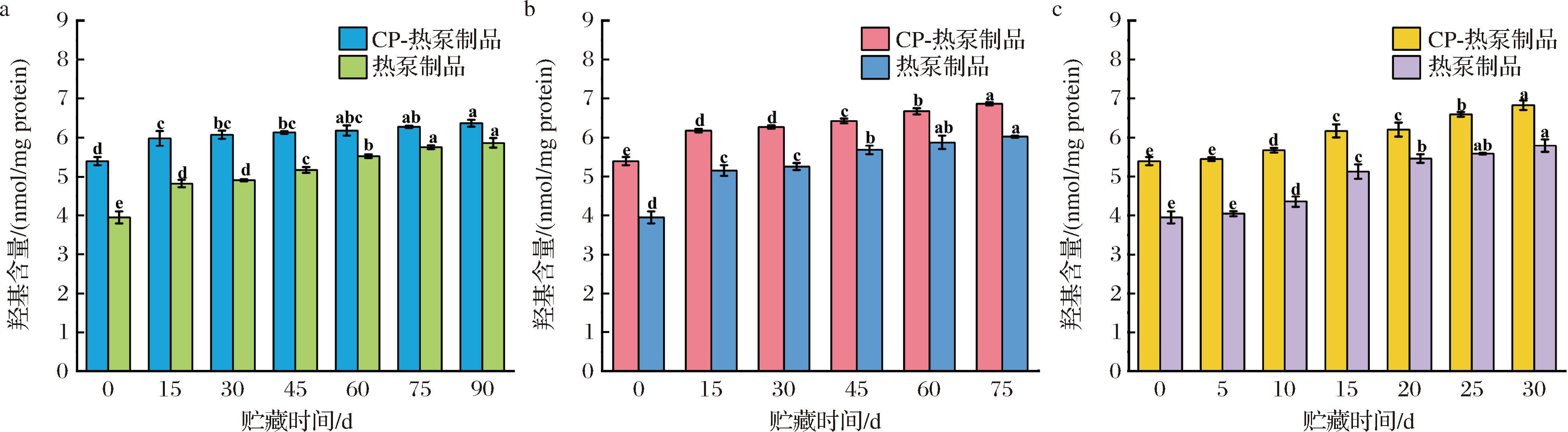
a--18 ℃;b-4 ℃;c-25 ℃
图6 CP协同处理对热泵干制贻贝在不同贮藏温度下羰基含量变化的影响
Fig.6 Effect of CP treatment on the change of carbonyl content of heat-pump dried mussels at different storage temperatures
在贮藏期间,CP-热泵组羰基含量值仍高于单一热泵组。例如,在4 ℃条件下,贮藏15、45、75 d后,单一热泵组羰基含量分别为5.150、5.677、6.02 nmol/mg protein,CP-热泵组分别为6.180、6.423、6.80 nmol/mg protein,分别高于前者1.030、0.746、0.780 nmol/mg protein。而在-18 ℃和25 ℃贮藏条件下,也得到了类似的结果。如-18 ℃贮藏90 d后,单一热泵组和CP-热泵组羰基含量分别为5.860、6.367 nmol/mg protein,后者比前者高了0.567 nmol/mg protein;25 ℃贮藏30 d后,单一热泵组和CP-热泵组羰基含量分别为5.790、6.823 nmol/mg protein,后者比前者高了1.033 nmol/mg protein。贮藏过程中蛋白质的氧化还受到微生物、酶活力及脂质过氧化产物的影响。贮藏温度越高,蛋白质氧化越显著,羰基含量增长越明显。因此,后续研究中,可联合应用低温贮藏及添加抗氧化剂等措施以减缓蛋白质氧化。
2.7 干制贻贝货架期模型的建立
2.7.1 质量指标的拟合分析
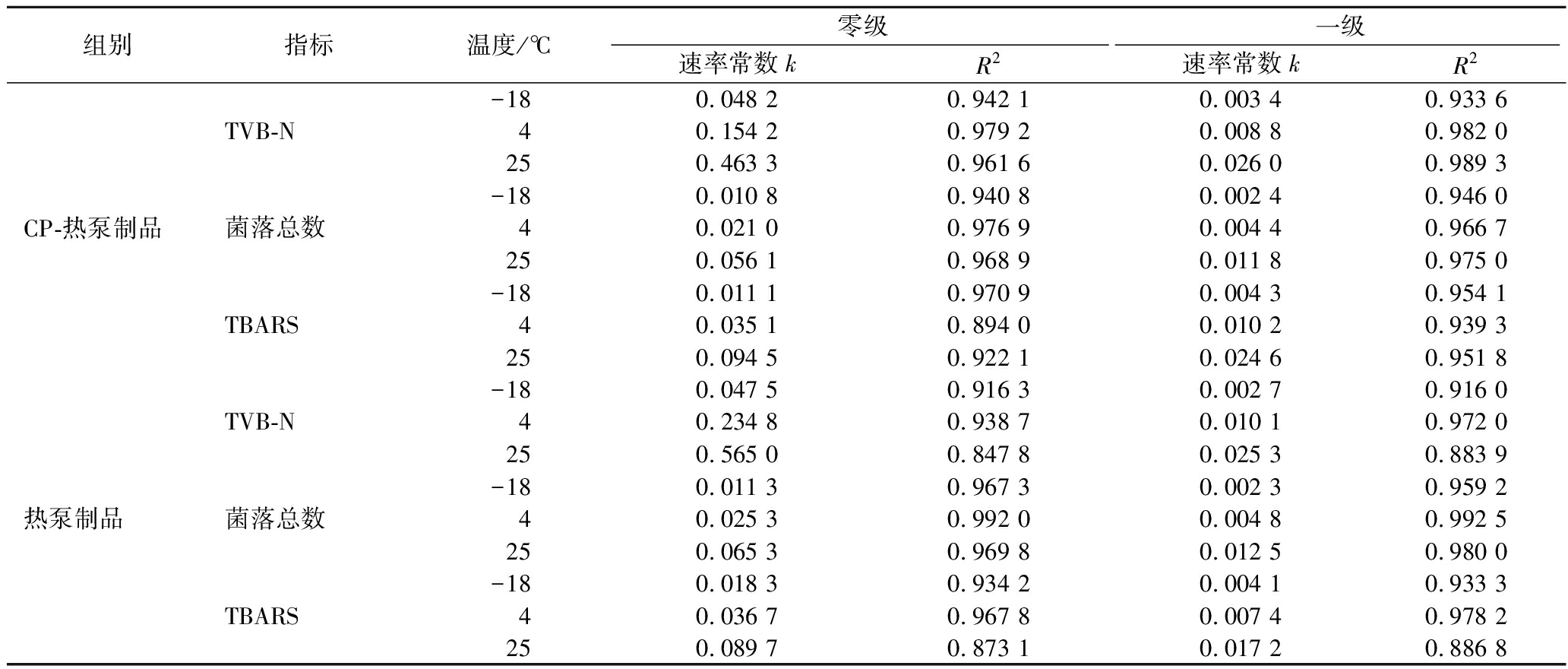
在食品加工、贮存和运输过程中,大多数干制水产品的质量变化都遵循零级或一级反应动力学模型[24]。CP-热泵组和热单一热泵组样品在不同贮藏温度下TVB-N、菌落总数和TBARS指标的模型参数如表1所示。R2值越大,代表拟合度越好。由表1可知,只有少数实验组R2值小于0.90,但平均值均大于0.90,表明模型方程的拟合性良好。其中,菌落总数组无论是零级或一级方程,R2平均值都大于TVB-N和TBARS组。另外,3组指标中,绝大部分数据均表现出一级方程R2大于零级方程R2值,表明一级方程比零级方程表现出更好的拟合性。因此,菌落总数更适合用于预测干制贻贝的贮藏货架期,选取一级方程用于计算。
表1 不同贮藏温度下CP-热泵组和单一热泵组贻贝品质变化的反应动力学模型拟合及决定系数R2
Table 1 Fitting of reaction kinetic models and determination coefficient R2 of quality changes in mussels at different storage temperatures
组别指标温度/℃零级一级速率常数kR2速率常数kR2CP-热泵制品-180.048 20.942 10.003 40.933 6TVB-N40.154 20.979 20.008 80.982 0250.463 30.961 60.026 00.989 3-180.010 80.940 80.002 40.946 0菌落总数40.021 00.976 90.004 40.966 7250.056 10.968 90.011 80.975 0-180.011 10.970 90.004 30.954 1TBARS40.035 10.894 00.010 20.939 3250.094 50.922 10.024 60.951 8热泵制品-180.047 50.916 30.002 70.916 0TVB-N40.234 80.938 70.010 10.972 0250.565 00.847 80.025 30.883 9-180.011 30.967 30.002 30.959 2菌落总数40.025 30.992 00.004 80.992 5250.065 30.969 80.012 50.980 0-180.018 30.934 20.004 10.933 3TBARS40.036 70.967 80.007 40.978 2250.089 70.873 10.017 20.886 8
2.7.2 温度对反应速率的影响
通常情况下,反应速率常数k与温度的关联性可根据Arrhenius方程进行分析,得到CP-热泵组和单一热泵组菌落总数的反应速率ln k与1/T呈良好的线性关系,R2值分别为0.924 8、0.964 6,均大于0.90,表明拟合度高,精度好。2组ln k与1/T的线性方程及参数,如公式(8)、公式(9)所示:
CP-热泵组:![]()
(8)
单一热泵组:![]()
(9)
2.7.3 货架期预测
活化能Ea是化学反应启动所需要的能量值,CP-热泵组和单一热泵组的Ea分别为23.160、24.70 kJ/mol,位于食品相关的化学反应活化能范围之内[25](10~150 kJ/mol),表面本研究中计算得到的活化能是合理的。将计算得到的Ea代入到公式(7),得到SL菌落总数方程如公式(10)、公式(11)所示:
CP-热泵组: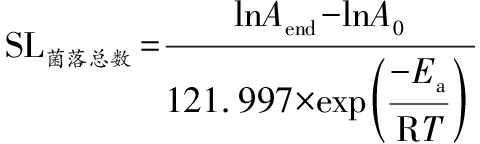
(10)
单一热泵组: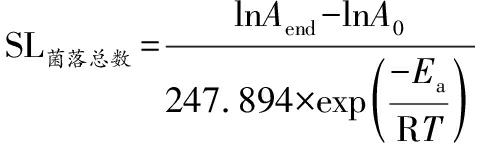
(11)
通过计算得到预测值(d),Aend限值6 lg CFU/g(食品安全限值),计算结果如表2所示。在-18、4、25 ℃ 贮藏温度下,CP-热泵组比单一热泵组货架期分别延长了54.43、26.35、14.30 d,表明CP协同处理能有效提高干制产品的货架期。
表2 预测的货架期结果
Table 2 Predicted shelf-life results

组别温度/℃预测值/dCP-热泵制品-18201.16484.562541.66热泵制品 -18146.73458.212527.36
3 结论
本研究系统探究了CP协同处理对热泵干制贻贝在-18、4、25 ℃贮藏温度下品质变化的影响,并构建货架期预测模型。监测菌落总数、TVB-N、TBARS、蛋白质羰基含量等关键指标发现,CP协同处理可显著降低初始微生物负载,抑制贮藏期TVB-N增加,有效延缓脂质氧化,还能提升复水率。但是,研究也显示,CP协同处理会加剧蛋白质氧化。基于Arrhenius理论的模型显示,在-18、4、25 ℃下,CP协同处理分别延长干制贻贝货架期54.43、26.35、14.30 d,显著提高其贮藏稳定性,减少品质劣变损失。本研究成果为基于CP协同处理的水产品干制加工新方法提供理论依据与技术指导。未来的研究应侧重于探索CP处理工艺参数与蛋白质氧化水平之间的动态调控机制,并利用天然抗氧化剂复配技术协同抑制氧化损伤。同时,需要验证该技术在不同水产品(如牡蛎、鱼类)中的普适性及其工业化应用潜力,以推动其在多样化水产品加工中的规模化应用。
[1] CHERIFI H,CHEBIL AJJABI L,SADOK S.Nutritional value of the Tunisian mussel Mytilus galloprovincialis with a special emphasis on lipid quality[J].Food Chemistry,2018,268:307-314.
[2] GOMEZ E,RANI D A,CHEESEMAN C R,et al.Thermal plasma technology for the treatment of wastes:A critical review[J].Journal of Hazardous Materials,2009,161(2-3):614-626.
[3] ![]() BEZERRA J,LAM
BEZERRA J,LAM RO C V,SANCHES E A,et al.Cold plasma as a pre-treatment for processing improvement in food:A review[J].Food Research International,2023,167:112663.
RO C V,SANCHES E A,et al.Cold plasma as a pre-treatment for processing improvement in food:A review[J].Food Research International,2023,167:112663.
[4] RATHOD N B,RANVEER R C,BHAGWAT P K,et al.Cold plasma for the preservation of aquatic food products:An overview[J].Comprehensive Reviews in Food Science and Food Safety,2021,20(5):4407-4425.
[5] DHARINI M,JASPIN S,MAHENDRAN R.Cold plasma reactive species:Generation,properties,and interaction with food biomolecules[J].Food Chemistry,2023,405:134746.
[6] ZHANG X L,ZHONG C S,MUJUMDAR A S,et al.Cold plasma pretreatment enhances drying kinetics and quality attributes of chili pepper (Capsicum annuum L.)[J].Journal of Food Engineering,2019,241:51-57.
[7] KARIM N,SHISHIR M R I,BAO T,et al.Effect of cold plasma pretreated hot-air drying on the physicochemical characteristics,nutritional values and antioxidant activity of shiitake mushroom[J].Journal of the Science of Food and Agriculture,2021,101(15):6271-6280.
[8] NING H Q,WANG Z S,LI Y Q,et al.Effects of glycinin basic polypeptide on the textural and physicochemical properties of Scomberomorus niphonius surimi[J].LWT,2019,114:108328.
[9] KANG D C,ZOU Y H,CHENG Y P,et al.Effects of power ultrasound on oxidation and structure of beef proteins during curing processing[J].Ultrasonics Sonochemistry,2016,33:47-53.
[10] XING W M,LIU W L,LI H M,et al.Development of predictive models for shelf-life of sweet cherry under different storage temperatures[J].LWT,2025,217:117442.
[11] MISRA N N,JO C.Applications of cold plasma technology for microbiological safety in meat industry[J].Trends in Food Science &Technology,2017,64:74-86.
[12] NIE L,YANG Y,DUAN J,et al.Effect of tissue thickness and liquid composition on the penetration of long-lifetime reactive oxygen and nitrogen species (RONS) generated by a plasma jet[J].Journal of Physics D:Applied Physics,2018,51(34):345204.
[13] CAI Z C,WANG J M,LIU C C,et al.Effects of high voltage atmospheric cold plasma treatment on the number of microorganisms and the quality of Trachinotus ovatus during refrigerator storage[J].Foods,2022,11(17):2706.
[14] OEHMIGEN K,H HNEL M,BRANDENBURG R,et al.The role of acidification for antimicrobial activity of atmospheric pressure plasma in liquids[J].Plasma Processes and Polymers,2010,7(3-4):250-257.
HNEL M,BRANDENBURG R,et al.The role of acidification for antimicrobial activity of atmospheric pressure plasma in liquids[J].Plasma Processes and Polymers,2010,7(3-4):250-257.
[15] ZOUELM F,ABHARI K,HOSSEINI H,et al.The effects of cold plasma application on quality and chemical spoilage of Pacific white shrimp (Litopenaeus vannamei) during refrigerated storage[J].Journal of Aquatic Food Product Technology,2019,28(6):624-636.
[16] PANKAJ S K,WAN Z F,KEENER K M.Effects of cold plasma on food quality:A review[J].Foods,2018,7(1):4.
[17] BAO T,HAO X,SHISHIR M R I S,et al.Cold plasma:An emerging pretreatment technology for the drying of jujube slices[J].Food Chemistry,2021,337:127783.
[18] SHEN Z W,LUAN A N,YI S X,et al.Moderate protein degradation and lipid oxidation induced by cold plasma and its effect on the quality of dried fish products[J].Journal of Food Composition and Analysis,2023,123:105636.
[19] NAWAZ A,IRSHAD S,KHAN I A,et al.Protein oxidation in muscle-based products:Effects on physicochemical properties,quality concerns,and challenges to food industry[J].Food Research International,2022,157:111322.
[20] HU Y Y,ZENG X B,JIANG K Y,et al.Effect of non-enzymatic browning on oysters during hot air-drying process:Color and chemical changes and insights into mechanisms[J].Food Chemistry,2024,454:139758.
[21] OLATUNDE O O,HEWAGE A,DISSANAYAKE T,et al.Cold atmospheric plasma-induced protein modification:Novel nonthermal processing technology to improve protein quality,functionality,and allergenicity reduction[J].Comprehensive Reviews in Food Science and Food Safety,2023,22(3):2197-2234.
[22] WANG X T,WANG J,WANG Z B,et al.Impact of dielectric barrier discharge cold plasma on the lipid oxidation,color stability,and protein structures of myoglobin-added washed pork muscle[J].Frontiers in Nutrition,2023,10:1137457.
[23] CHEN Y Y,PENG S W,HU J J,et al.Excellent quality acquisition of myofibrillar protein in red shrimp (Solenocera crassicornis) based on regulating the oxidation degree of atmospheric cold plasma treatment[J].Journal of the Science of Food and Agriculture,2025,105(4):2712-2721.
[24] YIN C,WANG J,QIAN J,et al.Quality changes of rainbow trout stored under different packaging conditions and mathematical modeling for predicting the shelf life[J].Food Packaging and Shelf Life,2022,32:100824.
[25] LABUZA T P.Application of chemical kinetics to deterioration of foods[J].Journal of Chemical Education,1984,61(4):348.