随着现代社会发展和生活节奏的加快,疲劳已成为生活中常见的健康问题,体力疲劳、心理疲劳、脑力疲劳和病理疲劳频繁出现在大众视野中[1],疲劳不仅影响了人们对生活获得感与满足感,而且降低了工作效率,危害身体健康,疲劳状态下,机体可出现注意力不集中、身体倦怠、情绪低落等临床症状[2]。同时,研究表明,疲劳的发生会增加多发性硬化症、脑出血、神经衰弱等症状发病几率,长期疲劳更会降低机体免疫力,导致外界病原体更容易入侵机体,从而引起疾病[3-4]。传统中医中认为,五加科人参属植物人参(Panax ginseng C.A.Meyer)具有强大的补气功效,有着安神和增强智力等功效[5]。现代药理学研究表明,人参皂苷是其人参的主要活性成分[6],并且其被认为是人参抗疲劳的主要成分之一[7],目前的研究结果表明人参皂苷Rg1(ginsenoside Rg1,Rg1)、人参皂苷Rg3(ginsenoside Rg3,Rg3)、人参皂苷Ro(ginsenoside Ro,Ro)、人参皂苷Rb1(ginsenoside Rb1,Rb1)具有抗疲劳作用[8]。
网络药理学作为新兴的技术,已用于众多领域,其中在中药复杂成分药效研究中,已逐渐显现出独特的优势,它以网络的形式整体、系统地研究药效成分多靶点、多途径调控,以揭示药物发挥治疗作用相关机制,降低了新药的研发成分和新药的研究时间[9]。近年来,网络药理学也逐渐应用于抗疲劳药效机制预测研究。张楠等[10]利用网络药理学及分子对接技术研究发现,天麻相关药效成分通过STAT3、PIK3CA、PIK3CB、PIK3CD、ESR1、PIK3R1靶点发挥抗疲劳作用;刘秋容等[11]利用网络药理学预测出其成分主要通过磷脂酰肌醇3′-激酶(phosphatidylinositol 3′-kinase,PI3K)-Akt 等信号通路起抗疲劳作用。人参沙棘复合物(ginseng sea buckthorn complex,GSC)利用了沙棘果酸对人参提取物(ginseng extract,GE)进行酸转化,转化后人参皂苷种类及含量未知并且该转化产物抗疲劳作用机制仍待探索。因此,该研究拟采用超高效液相色谱-四极杆飞行时间串联质谱技术(ultra performance liquid chromatography-quadrupole time-of-flight tandem mass spectrometry,UPLC-QTOF-MS)阐明GE和GSC中人参皂苷成分及相对含量,并进行网络药理学、分子对接技术和动物实验研究,探索其潜在抗疲劳作用机制。
1 材料与方法
1.1 材料与试剂
1.1.1 实验动物
8周龄C57BL/6小鼠63只[SPF级,雌性,体重(20±2) g,生产许可证号编号:SCXK(粤)2022-0002],购买于广东省医学实验动物中心。饲养于完美(广东)日用品有限公司,环境温度为(22±2) ℃,湿度(50±10)%,24 h内进行昼夜更替。适应性喂养1周后进行实验。该研究动物实验已获得完美(广东)日用品有限公司动物伦理委员会批准(批准文号:WM-GD-PZDW024)。
1.1.2 受试品与试剂
GE(人参总皂苷含量大于1%),广东青云山药业有限公司;GSC,完美(广东)日用品有限公司生命健康科技研究院,由GE加入至沙棘果汁中加热进行人参皂苷转化,喷雾干燥后制得;糖原检测试剂盒,南京建成生物工程有限公司;尿素检测试剂盒,Mindray公司;乳酸试纸,SensLab公司。
1.2 仪器与设备
MS250DU电子天平,METTLER TOLEDO公司;JM-16D-28/45超声波清洗机,深圳市洁盟清洗设备有限公司;G2高分辨四级杆飞行时间串联液质联用仪,Waters公司;BS-240VET全自动生化仪、Mindray;Synergy H1酶联免疫分析仪,BioTek公司;Lactate Scout 4便携式乳酸测定仪,SensLab公司;NextSeq 2000基因测序仪,Illumina公司。
1.3 实验方法
1.3.1 GSC及GE成分鉴定与含量检测
1.3.1.1 供试品准备
精密称取GE、GSC约0.5 g,放入25.00 mL容量瓶中,加体积分数70%甲醇至容量瓶总体积2/3,超声波清洗机超声60 min,取出并放冷,继续加入70%甲醇定容后充分摇匀,用滤膜过滤得到续滤液进行检测。各样品另取300 μL上清液混合成QC样品,在序列的前中后各进样一针检测。
1.3.1.2 色谱条件
流动相A:体积分数0.1%甲酸水,流动相B:体积分数0.1%甲酸乙腈,梯度洗脱(0~22 min,5%~100% B;22~26 min,100% B;26~26.1 min,100%~5% B;26.1~30 min,5% B)。色谱柱为L100-15(Waters),ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 μm),流速0.3 mL/min,柱温30 ℃,进样量1 μL。
1.3.1.3 质谱条件
离子源采用负离子扫描模式,毛细管电压2.5 kV。离子源温度120 ℃,锥孔电压40 kV,其气流速50 L/h。脱溶剂气温度250 ℃,其气流速为600 L/h。以0.5 s的扫描频率扫描范围50~1 300 m/z。扫描时低电压6 V,高能碰撞电压20~40 V。
1.3.2 基于网络药理学和分子对接的GSC抗疲劳机制预测
1.3.2.1 数据库与软件
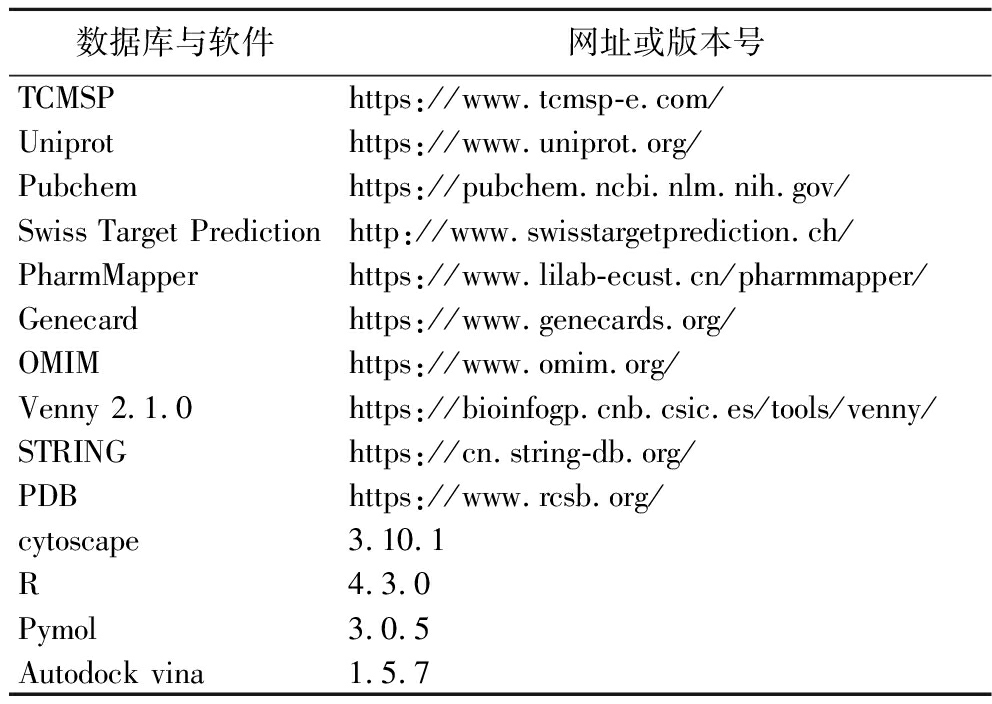
基于网络药理学及分子对接技术预测GSC抗疲劳机制时所使用的数据库及软件如表1所示。
表1 数据库与软件
Table 1 Database and software
数据库与软件网址或版本号TCMSPhttps://www.tcmsp-e.com/Uniprothttps://www.uniprot.org/Pubchemhttps://pubchem.ncbi.nlm.nih.gov/Swiss Target Predictionhttp://www.swisstargetprediction.ch/PharmMapperhttps://www.lilab-ecust.cn/pharmmapper/Genecardhttps://www.genecards.org/OMIMhttps://www.omim.org/Venny 2.1.0https://bioinfogp.cnb.csic.es/tools/venny/STRINGhttps://cn.string-db.org/PDBhttps://www.rcsb.org/cytoscape3.10.1R4.3.0Pymol3.0.5Autodock vina1.5.7
1.3.2.2 GSC作用靶点收集及筛选
利用UPLC-QTOF-MS鉴定出GSC中人参皂苷种类及相对含量后,利用TCMSP数据库检索到这些人参皂苷后,利用Mol ID获取其对应的蛋白质靶点信息,在Uniprot数据库查询得到基因名并收集。
将鉴定出的人参皂苷在Pubchem数据库中收集SMILES号,将其导入到Swiss Target Prediction数据库中进行预测人参皂苷的潜在活性靶点,以Probability>0为条件筛选靶点。并利用Pubchem数据库中人参皂苷2D结构数据在PharmMapper数据库预测作用靶点,以Norm Fit>0.3为条件筛选靶点。将以上数据库中结果汇总并删除重复值,得到GSC潜在活性靶点。
1.3.2.3 疲劳靶点收集与筛选
通过在Genecard与OMIM数据库中使用“fatigue”和“anti fatigue”作为关键词进行搜索,以获取相关靶点。从Genecard数据库筛选出相关性分数≥5的靶点,并将OMIM与Genecard数据库的靶点结果合并去重,获得疲劳疾病的靶点。
1.3.2.4 GSC-抗疲劳交集靶点筛选
将GSC潜在活性靶点与疲劳靶点导入Venny 2.1.0中,获得两者的交集靶点。
1.3.2.5 GSC-成分-靶点网络图构建及关键成分筛选
将GSC中成分、作用靶点及疲劳靶点信息进行数据整理,将数据导入至cytoscape中进行可视化处理,构建出GSC-成分-靶点网络图。利用cytoscape中cytohubba插件进行网络分析,筛选出评分前5的活性成分。
1.3.2.6 交集靶点PPI网络图构建与关键靶点筛选
输入GSC抗疲劳潜在活性靶点与疲劳靶点的共有靶点至STRING网站中,选定物种为人源,设定相互作用阈值为0.9,获取蛋白质相互作用(protein-protein interaction,PPI)网络数据。利用cytoscape软件中cytohubba插件进行网络分析,并选取富集得分最高的前10个结果作为核心靶点。
1.3.2.7 交集靶点GO、KEGG富集分析
利用 “ClusterProfiler”工具包,在R语言中对GSC活性靶点和疲劳靶点的共同靶点进行GO和KEGG富集分析。设定筛选标准为P<0.05,并在R语言中进行结果输出和结果的可视化展示。
1.3.2.8 GSC关键成分与关键靶点分子对接
在PDB网站上下载筛选出的GSC关键靶点蛋白质结构,同时在pubchem网站上下载GSC关键成分结构,在Pymol对蛋白质结构进行去除水分子及小分子配体处理后,在Autodock vina进行分子对接,并使用Pymol可视化结果。
1.3.3 GSC对小鼠的抗疲劳作用
1.3.3.1 实验分组及给药
将63只C57BL/6小鼠分为空白对照组(Cont)、人参提取物组(GE)、人参沙棘复合物组(GSC),每组各21只,GSC组按0.9 g/kg给药灌胃;GE组按0.15 g/kg给药灌胃;Cont组给予同体积生理盐水,每天定时定量给药1次,每次灌胃0.1 mL/10 g,连续给药30 d。将每组21只小鼠分为3批,每批7只。
1.3.3.2 负重力竭游泳实验
将第1批小鼠尾部捆绑相当于体重10%铅皮的小鼠放入深度至少30 cm、水温控制在(30±1.0) ℃的游泳池内游泳。从游泳开始到小鼠的口鼻沉入水面超过8 s,表示小鼠达到负重游泳的疲劳极限,记录此时时间即为小鼠的负重力竭游泳时间。
1.3.3.3 非负重游泳实验
将第2批小鼠在(30±1.0) ℃的水温中无负重游泳90 min,休息60 min,随后采集其血液、肌肉和肝脏样本。
1.3.3.4 小鼠血乳酸检测及乳酸曲线下面积计算
将第3批小鼠在(30±1.0) ℃的水温中无负重游泳,持续10 min。在游泳前、游泳后0 min以及游泳后休息20 min分别采集血液样本,并利用乳酸仪进行乳酸含量的测定。随后,根据所得数据计算出血乳酸曲线下面积。计算方法如公式(1)所示:
S=5×(A1+3A2+2A3)
(1)
式中:S,血乳酸曲线下面积,mmol/L;A1,游泳前血乳酸值,mmol/L;A2,游泳后0 min的血乳酸值,mmol/L;A3,游泳后休息20 min的血乳酸值,mmol/L。
1.3.3.5 尿素检测
将收集的第2批小鼠血液静置4 h,以3 000 r/min转速进行离心,离心15 min后得到血清样本,利用全自动生化仪进行尿素含量检测。
1.3.3.6 肝糖原及肌糖原检测
将收集的第2批小鼠肌肉及肝脏,按料液比1∶9(g∶mL)加入PBS,同时加入研磨珠利用研磨仪进行冷冻研磨得到匀浆,以3 000 r/min转速进行冷冻离心,离心20 min 后收集上清液,按照试剂盒说明进行检测肝糖原及肌糖原浓度。
1.3.3.7 小鼠肠道菌群宏基因组检测
第1批小鼠处死后,立即获取其结肠粪便保存于无菌无酶管中并立即放置液氮冻存。开始检测时,首先从样本中提取总DNA,进行PCR扩增。纯化扩增产物后测定含量,均一化处理后建库。文库通过质量检查后,在Illumina NextSeq2000平台进行测序。获得测序结果后,对结果数据进行质量控制、筛选及组装,获得结果后,进行基因预测、基因定量和群落多样性分析。
1.4 数据处理
采用GraphPad Prism 8.0软件进行统计处理,结果表述为“平均值±标准差”,多组间比较采用单因素方差分析,P<0.05视为差异具有统计学意义。
2 结果与分析
2.1 GSC成分鉴定与含量检测结果
利用UNIFI软件对UPLC-QTOF-MS结果进行定性与半定量分析,以自建标准品数据库与检测数据进行精确质量数、二级质谱图和保留时间的综合比对来定性未知物;以提取离子流图的峰面积进行半定量。
如电子版增强出版附图1、附表1、附表2(https://doi.org/10.13995/j.cnki.11-1802/ts.042870,下同)所示,经过归纳整理,鉴定出GSC中含有17种人参皂苷,GE中含有23种人参皂苷。经过沙棘果酸转化后,GSC相比于原料GE,稀有人参皂苷如人参皂苷Rg5(ginsenoside Rg5,Rg5)、人参皂苷Rh2(ginsenoside Rh2,Rh2)、人参皂苷C-K(ginsenoside compound K,C-K)、20(R)-人参皂苷Rg2[20(R)-ginsenoside Rg2,20(R)-Rg2]、20(S)-人参皂苷Rg2[20(S)-ginsenoside Rg2,20(S)-Rg2]、人参皂苷F3(ginsenoside F3,F3)、人参皂苷Rg6(ginsenoside Rg6,Rg6)、20(R)-人参皂苷Rg3[20(R)-ginsenoside Rg3,20(R)-Rg3]、20(S)-人参皂苷Rg3[20(S)-ginsenoside Rg3,20(S)-Rg3]、人参皂苷Rk1(ginsenoside Rk1,Rk1)的相对含量得到提升。
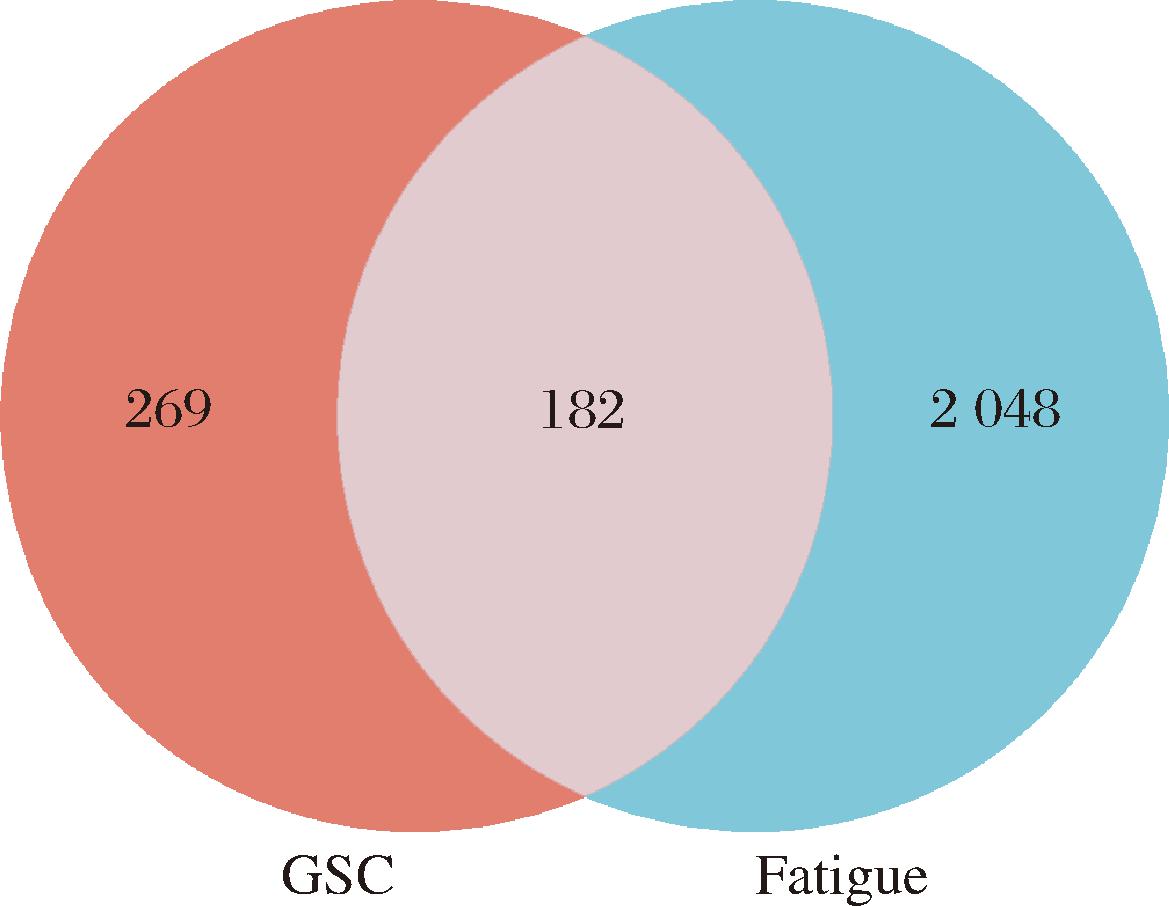
图1 GSC-Fatigue交集靶点图
Fig.1 GSC-Fatigue intersection target map
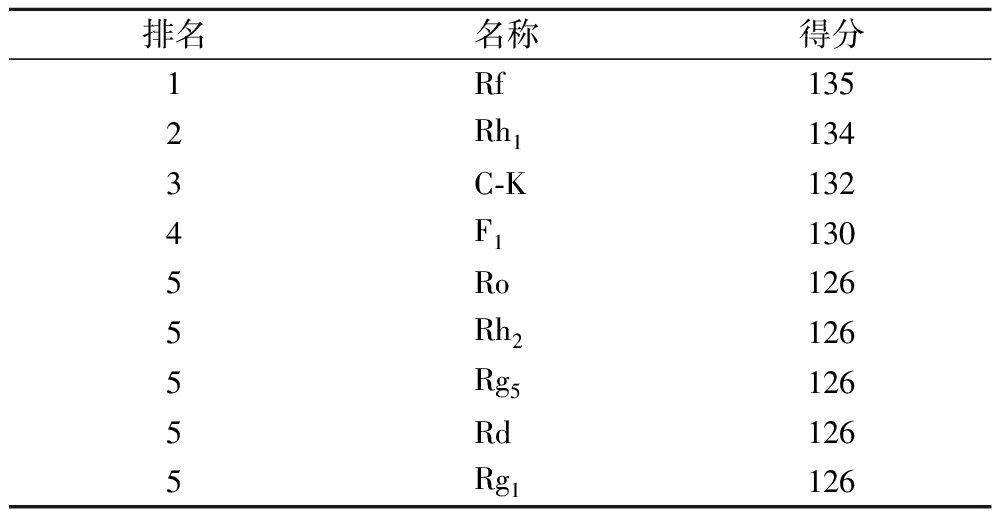
表2 核心成分评分表
Table 2 Core component rating scale
排名名称得分1Rf1352Rh11343C-K1324F11305Ro1265Rh21265Rg51265Rd1265Rg1126
2.2 GSC活性靶点
利用UPLC-QTOF-MS检测出的17种人参皂苷成分,通过TCMSP数据库获得活性靶点8个;通过pharmmapper预测活性靶点383个,通过Swiss TargetPrediction预测的潜在靶点共101个。通过去除重复基因并汇总后,共得到潜在活性靶点451个。
2.3 GSC潜在抗疲劳活性靶点
通过GeneCards和OMIM数据库共获得2 230个疲劳疾病靶点。通过Venny将GSC活性靶点与疲劳靶点进行交集,得到共同靶点182个,如图1所示。
2.4 GSC-成分-靶点网络图与核心成分
收集GSC-疲劳的共同靶点及其对应的人参皂苷成分信息,利用Cytoscape软件绘制出GSC-成分-靶点网络图,如附图2所示,GSC中人参皂苷成分与抗疲劳相关靶点关系密切。通过插件cytohubba筛选核心成分,如表2所示,获得评分前5的核心成分分别是人参皂苷Rf(ginsenoside Rf,Rf)、人参皂苷Rh1(ginsenoside Rh1,Rh1)、人参皂苷F1(ginsenoside F1,F1)、人参皂苷Rd(ginsenoside Rd,Rd)、Rh2、Rg1、Ro、C-K、Rg5。
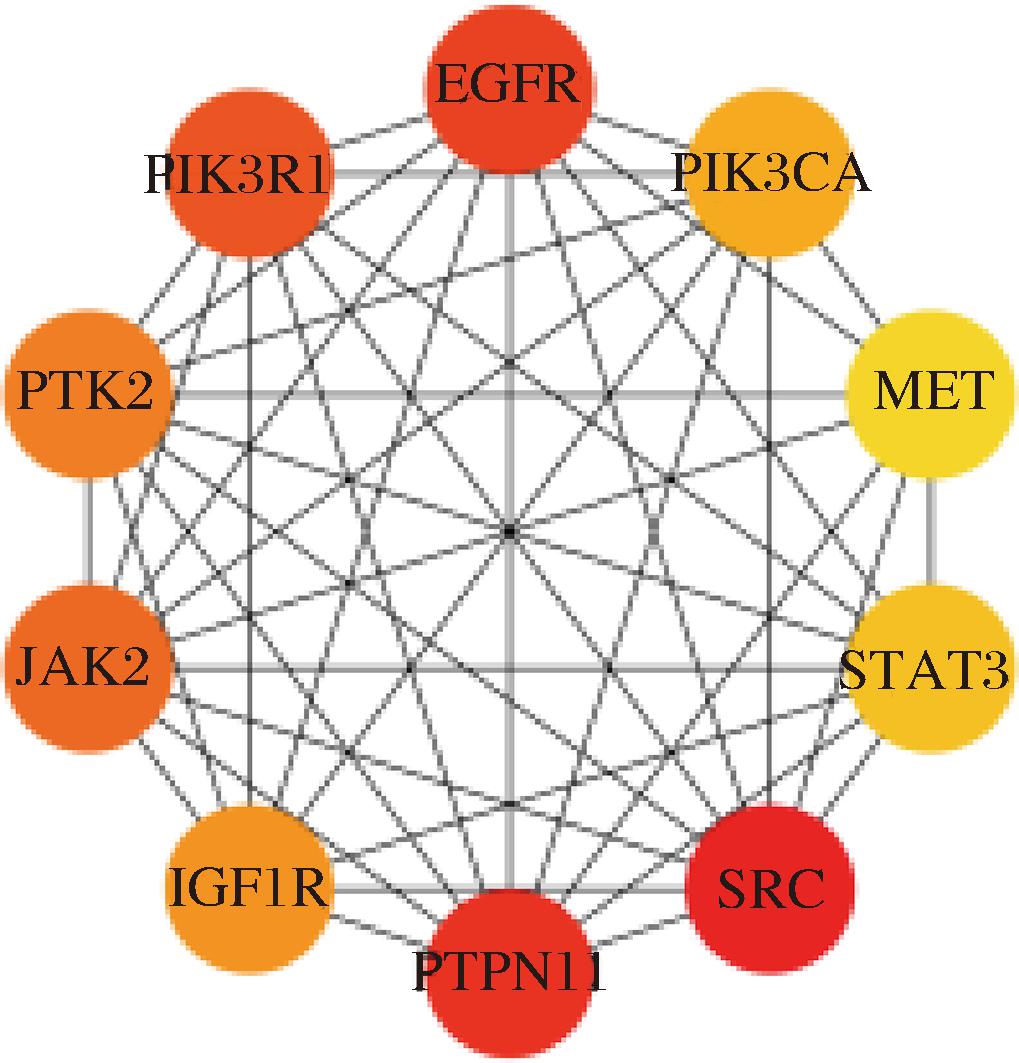
图2 GSC缓解疲劳核心靶点图
Fig.2 Map of the core targets of GSC for fatigue relief
注:颜色越深代表评分越高。
2.5 PPI网络图与关键靶点
将GSC-疲劳的共同靶点导入到STRING数据库,得到共同靶点PPI网络图,如附图3所示。同时获得蛋白互作信息,得到182个靶点的454个互作信息,将信息导入至cytoscape软件进行分析。如图2、表3所示,筛选到评分前10的关键靶点为SRC、PTPN11、EGFR、PIK3R1、JAK2、PTK2、IGF1R、PIK3CA、STAT3、MET。
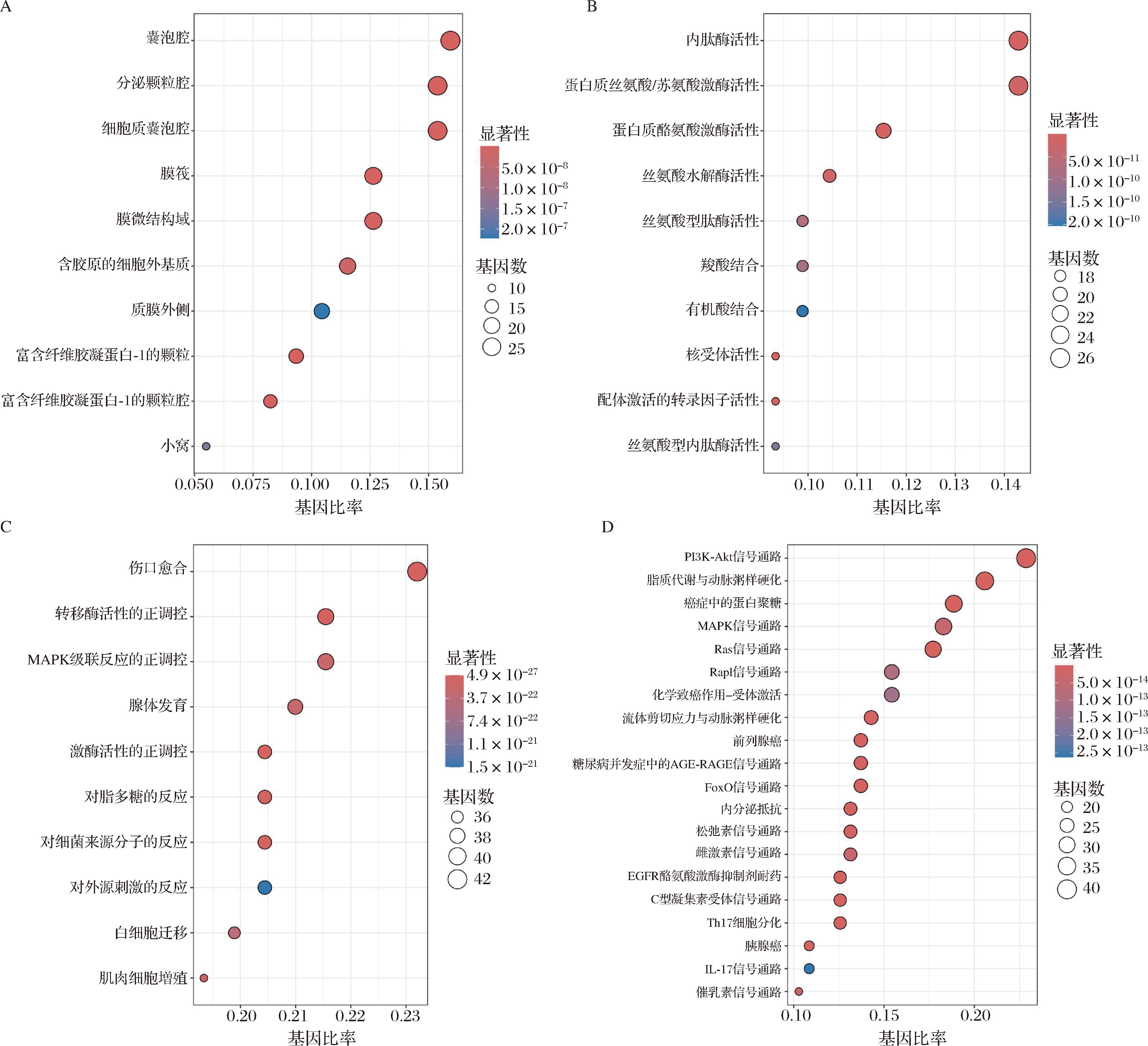
A-GO细胞组成;B-GO分子功能;C-GO生物过程;D-KEGG通路
图3 GSC-疲劳交集靶点富集分析
Fig.3 Enrichment analysis of GSC-Fatigue intersection targets
表3 核心靶点评分
Table 3 Core target score
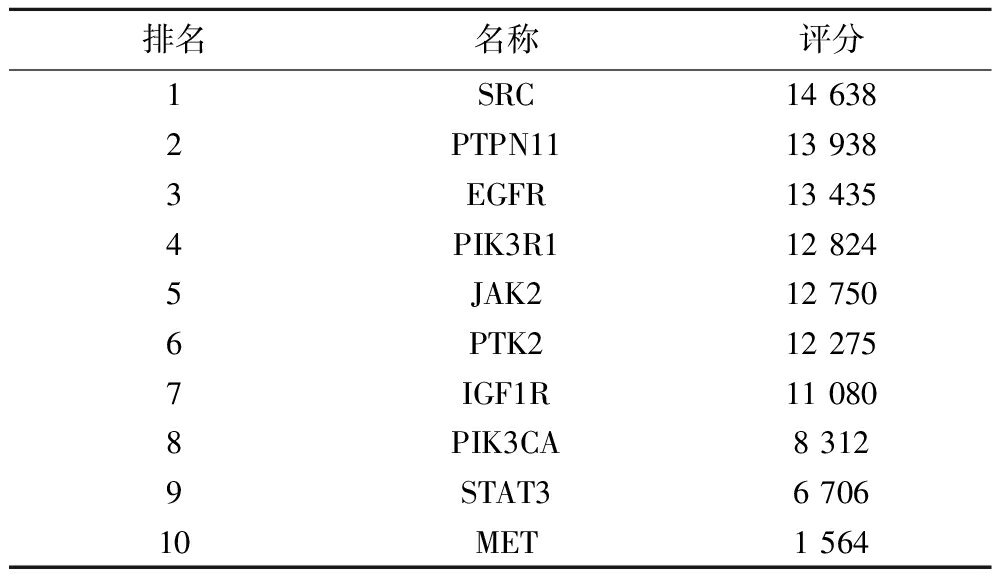
排名名称评分1SRC14 6382PTPN1113 9383EGFR13 4354PIK3R112 8245JAK212 7506PTK212 2757IGF1R11 0808PIK3CA8 3129STAT36 70610MET1 564
2.6 GO、KEGG富集分析结果
采用R语言对182个GSC-疲劳的共同靶点进行GO、KEGG富集分析。其中,GO富集分析中细胞组分(cellular component,CC)富集出352个条目;分子功能(molecular function,MF)富集出352个条目和生物过程(biological processes,BP)富集出5 590个条目,将得分前10结果进行可视化,如图3-A~图3-C所示。细胞组分主要涉及囊泡腔、分泌颗粒腔、细胞质囊泡内腔,其中囊泡腔与细胞质囊泡内腔参与细胞内物质的运输,包括代谢产物和能量分子[12-13],疲劳状态下,细胞能量需求增加,代谢废物积累。囊泡运输功能受损可能导致代谢物清除效率降低[14],进一步加重疲劳感。
对共同靶点进行KEGG通路富集,得到268条信号通路,将得分前20结果进行可视化,如图3-D所示。
GSC抗疲劳主要通路富集在PI3K-Akt等信号通路。PI3K-Akt信号通路作为抗疲劳中重要信号转导通路,可调控细胞的能量代谢,在疲劳发生时,机体能量需求增加。该通路能促进葡萄糖转运蛋白转位至细胞膜,增强细胞对葡萄糖的摄取,为细胞提供能量[15]。PI3K-Akt信号通路还参与调节糖原合成和糖异生过程,维持血糖水平稳定[16]。此外,PI3K-Akt信号通路Akt通过抑制FoxO转录因子,可减少自噬相关基因表达,影响受损细胞器和蛋白质的清除[17]。另外,丝裂原活化蛋白激酶级联反应(mitogen-activated protein kinase cascade,MAPK)信号通路也在机体适应外界环境改变及体内氧化抗氧化平衡系统中发挥着重要作用[11]。这些线索进一步表明,GSC可能通过调节PI3K-Akt、MAPK等信号通路改善能量代谢、代谢废物清除和氧化应激状态,起到抗疲劳作用。
2.7 GSC关键成分与关键靶点分子对接
进一步研究GSC关键成分与关键靶点结合情况,选取GSC抗疲劳得分前5的9种核心成分与核心靶点SRC、PTPN11、EGFR、PIK3R1、JAK2、PTK2、IGF1R、PIK3CA、STAT3和MET分别进行分子对接,得出90组对接结果,如图4所示,关键成分与关键靶点分子对接结合能均小于-7.00 kcal/mol,一般认为,结合能低于-7.00 kcal/mol时,活性成分与靶点有强烈的对接活性[18]。由此可进一步推测GSC具有良好抗疲劳作用。其中GSC中所含关键皂苷与PI3K-Akt信号通路上PIK3CA、PIK3R1、EGFR靶点结合能较低,说明GSC关键成分可能有较好的调节PI3K-Akt信号通路特性。将对接结合能最小的8个对接模型进行可视化展示,如图5所示。关键成分与关键靶点在结合过程中形成了多个氢键,其中Rf与PIK3CA结合形成4个氢键;Ro与PTK2结合形成8个氢键;Ro与PIK3CA结合形成5个氢键;Ro与EGFR结合形成8个氢键;Rh2与PIK3R1结合形成3个氢键;Rh2与EGFR结合形成2个氢键;Rg5与PIK3CA结合形成4个氢键;Rg5与EGFR结合形成4个氢键。表明GSC中核心成分与抗疲劳核心靶点之间具有良好的结合性能。
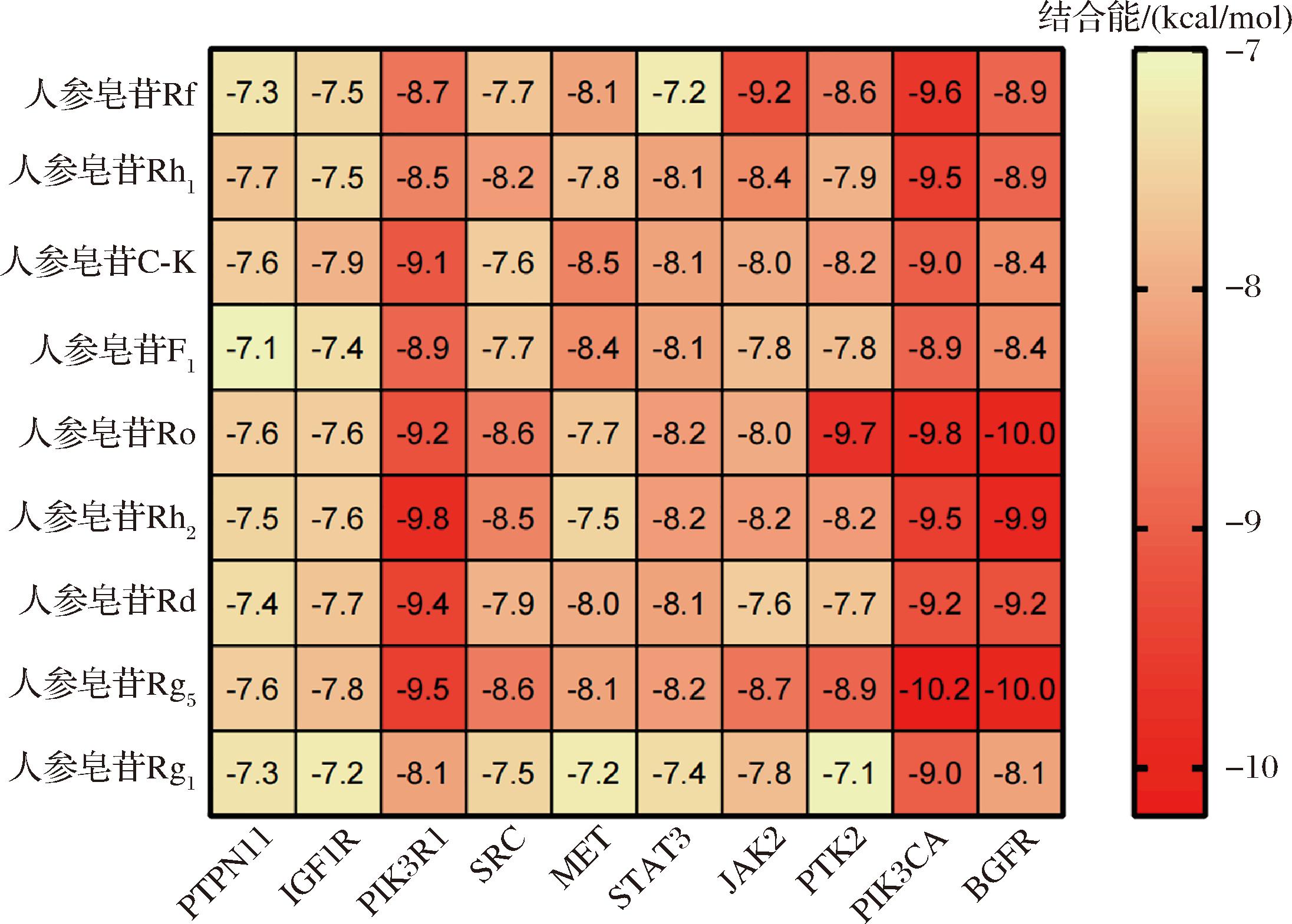
图4 分子对接结合能热图
Fig.4 Thermogram of molecular docking binding energy
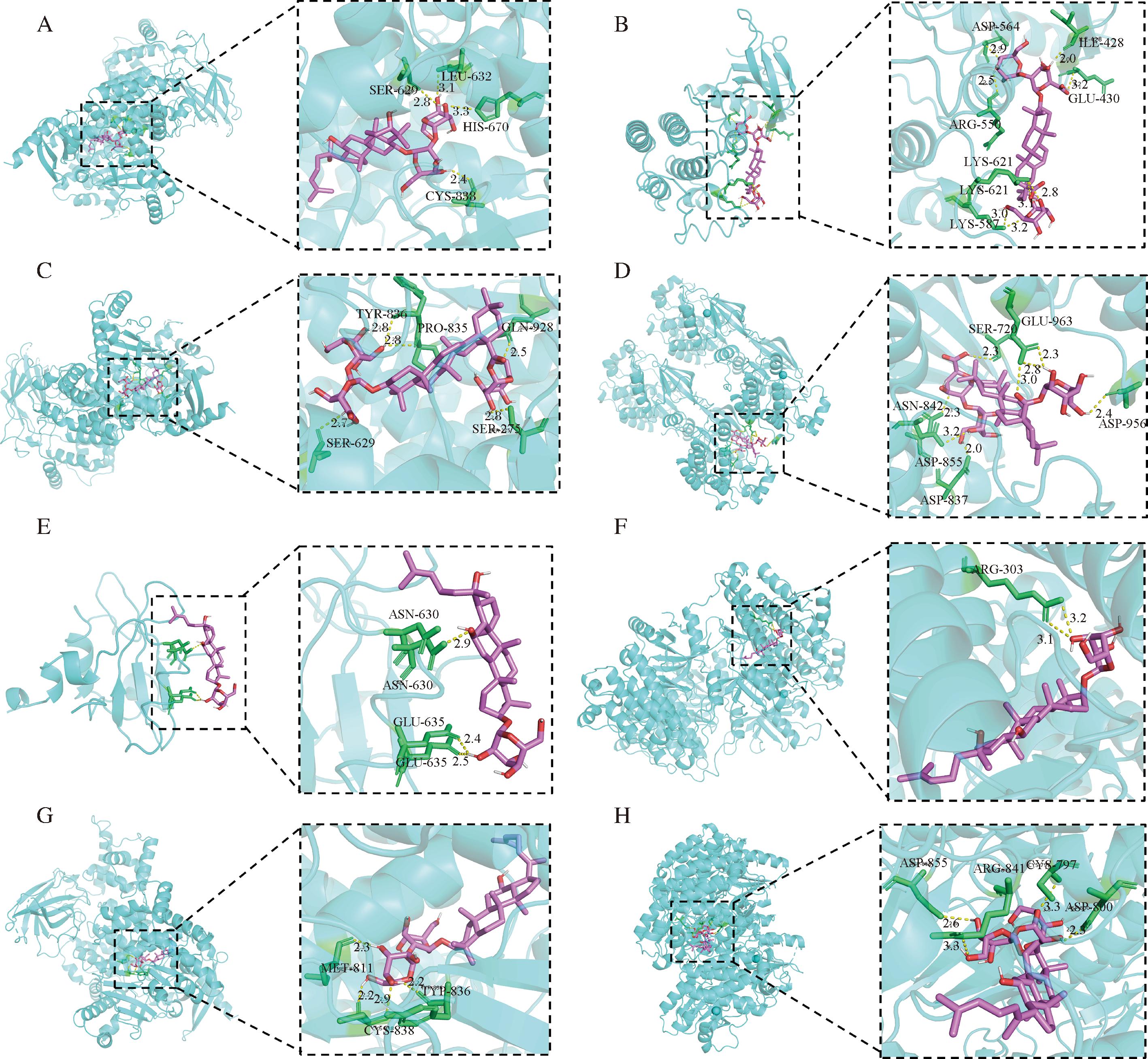
A-Rf-PIK3CA;B-Ro-PTK2;C-Ro-PIK3CA;D-Ro-EGFR;E-Rh2-PIK3R1;F-Rh2-EGFR;G-Rg5-PIK3CA;H-Rg5-EGFR
图5 分子对接结果图
Fig.5 Molecular docking results map
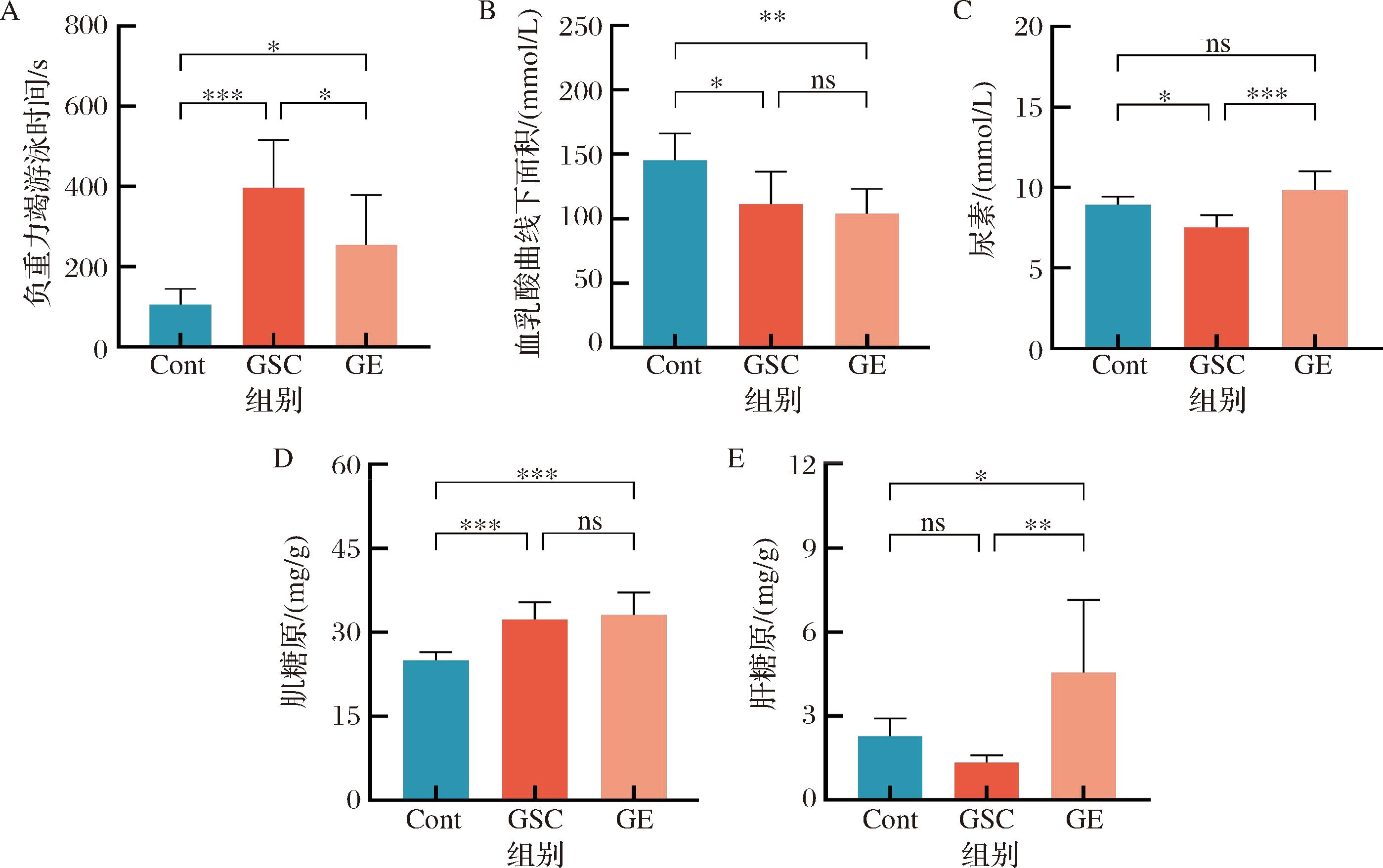
A-负重力竭游泳时间;B-血乳酸曲线下面积;C-尿素;D-肝糖原;E-肌糖原
图6 GSC对疲劳小鼠影响
Fig.6 Effects of GSC on fatigued mice
注:ns表示不显著,*表示P<0.05;**表示P<0.01;***表示P<0.001(下同)。
2.8 GSC对小鼠负重力竭游泳及非负重游泳影响
为了进一步探究GSC是否通过网络药理学预测结果对疲劳能量代谢及代谢废物清除产生作用,对小鼠进行非负重游泳及负重游泳实验,如图6-A所示,结果表明,GSC组、GE组与Cont相比,小鼠负重游泳时间分别延长275.52%(P<0.001)、141.08%(P<0.05),并且相比于GE组,GSC组延长小鼠负重游泳时间55.77%(P<0.05)。
在能量代谢及代谢物清除指标上,如图6-B~图6-E所示,与Cont相比,GSC组能降低23.43%(P<0.05)血乳酸曲线下面积和15.83%(P<0.05)尿素水平,显著增加29.25%(P<0.001)肌糖原水平;GE组能降低28.59%(P<0.01)血乳酸曲线下面积,增加98.95%(P<0.05)肝糖原和32.46%(P<0.001)肌糖原水平。与GE组相比,GSC组血清尿素水平降低了23.73%(P<0.001)。
2.9 GSC对负重力竭游泳小鼠肠道菌群影响
为了进一步探究GSC是否通过改善肠道菌群组成,进而调节能量代谢和代谢清除过程,最终提升小鼠的运动表现,本文对小鼠粪便菌群进行了宏基因组测序。结果表明,在alpha多样性上,各组Shannon指数、Simpson指数均无显著性差异,反映各组间肠道菌群多样性相近,如图7-A、图7-B所示。通过PCoA评估肠道菌群beta多样性,结果也表明,3组小鼠粪便肠道菌群结构相似,如图7-C所示。以上研究表明,GSC对运动小鼠肠道菌群多样性及整体结构影响较小。
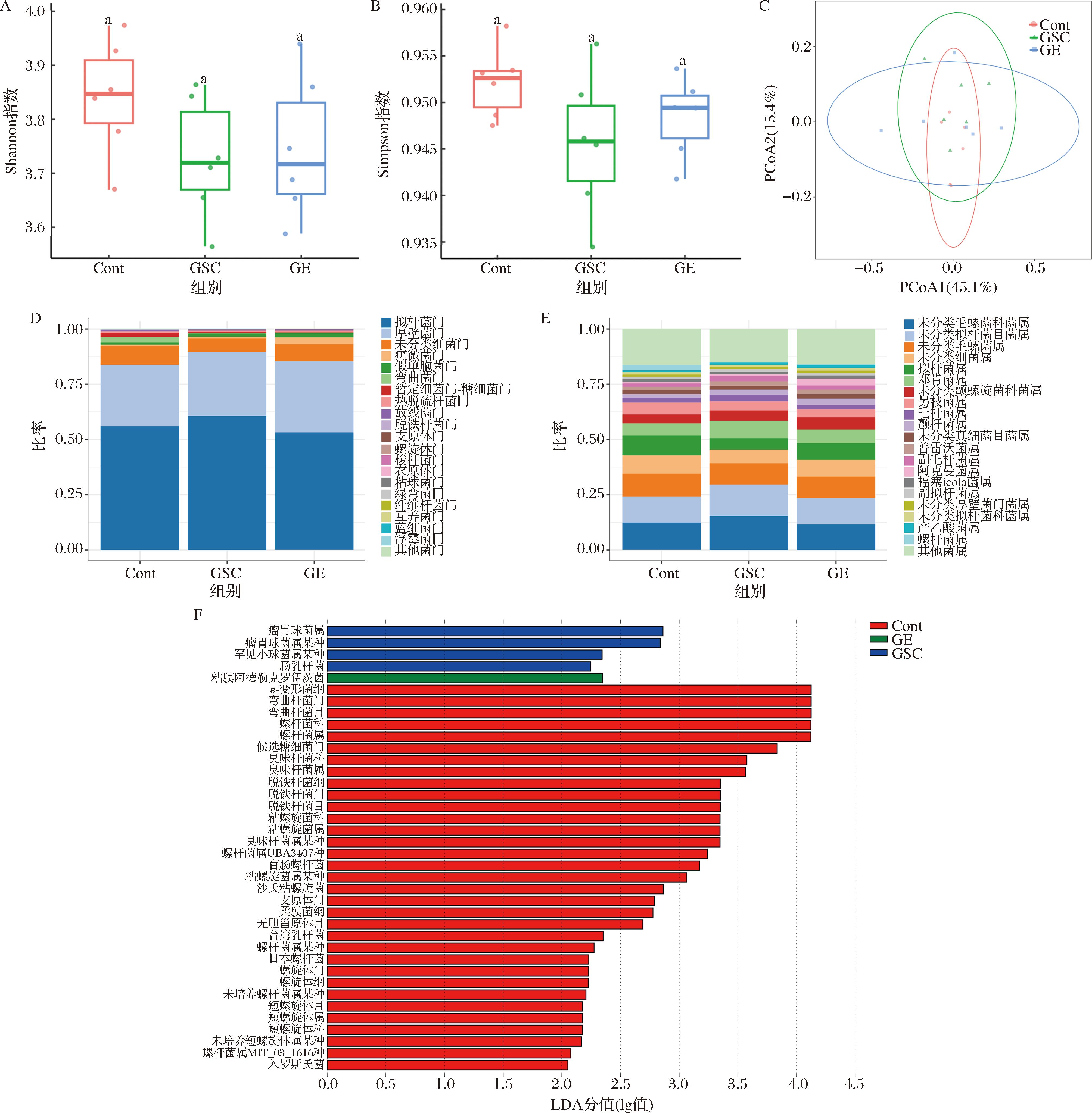
A-Shannon指数;B-Simpson指数;C-主坐标分析;D-门水平组成;E-属水平组成;F-LDA
图7 GSC对疲劳小鼠肠道菌群影响
Fig.7 Effects of GSC on the intestinal flora of fatigued mice
进一步在门、种不同水平研究GSC对肠道菌群影响。在门水平上,拟杆菌门与厚壁菌门为生物群落中主要微生物,在经过GSC处理后,拟杆菌门与厚壁菌门相对丰度上升,结果表明GSC增加了2种菌门的比例,且拟杆菌门增加相对丰度大于厚壁菌门,如图7-D所示。在属水平上,与Cont相比,GSC处理后提高了未分类毛螺菌科菌属、未分类拟杆菌目菌属、邓肯菌属、未分类颤螺旋菌科菌属、毛杆菌属、颤杆菌属、副毛杆菌属的相对丰度,降低了拟杆菌属、阿克曼菌属、螺杆菌属的相对丰度,如图7-E所示。结合线性判别分析(linear discriminant analysis,LDA),进一步探究GSC组与Cont组之间的差异菌种,瘤胃球菌属某种、肠乳杆菌、罕见小球菌属某种属于3组样品中GSC组的优势菌种,粘膜阿德勒克罗伊茨菌属于3组样品中GE组的优势菌种,结果如图7-F所示。
3 结论与讨论
人参具有显著的抗疲劳功效,可延长运动时间,增强体力,提高机体耐力,缓解运动后疲劳,促进体力恢复,是一种天然有效的抗疲劳药食两用原料。然而因为人参其培育难度大,一般健康产品中只能用5年以下的人参,其人参稀有皂苷含量较少,而人参稀有皂苷是人参抗疲劳功效的核心功效成分。本研究通过将人参和沙棘汁进行复配,利用沙棘汁的有机酸将人参皂苷进行转化,以期获得更多稀有人参皂苷。本研究首先运用了UPLC-QTOF-MS技术鉴定分析GSC及其原料GE中人参皂苷成分。其中GE中鉴定出23种人参皂苷,GSC共鉴定出17种人参皂苷,在17种人参皂苷中,稀有皂苷含量得到提升。已有研究表明,稀有皂苷生物利用度更高,生物活性更强[19-20]。分子对接结果中,GSC中含量提升的稀有皂苷Rh2、Rg5与筛选出关键靶点结合特性良好,提示稀有皂苷Rh2、Rg5可能为具有良好的抗疲劳作用成分。因此,对GSC下一步的研究可针对这些稀有人参皂苷抗疲劳作用进行进一步探究。
疲劳的病因和致病机制复杂,目前认为其致病机制与能量供应、代谢调整、氧化应激、炎症、中枢神经活动及激素分泌均有关系[21]。在网络药理学中,评分前10关键靶点与PI3K-Akt信号通路密切相关,PI3K-Akt信号通路作为抗疲劳中重要信号转导通路,可调节细胞糖类及脂质代谢改善机体能量代谢及激活下游Nrf-2抵抗氧化应激改善运动表现[22-23]。在HU等[24]研究中,姜黄素可通过激活PI3K/Akt/AMPK/mTOR信号通路和增加肌糖原含量及减少乳酸积累减轻运动疲劳;ZHANG等[25]研究发现,人参可通过PI3K/Akt/mTOR信号通路减少乳酸及尿素氮积累改善大鼠慢性疲劳。这些线索进一步表明GSC可能通过改善能量代谢与代谢废物清除起到抗疲劳作用。
为进一步验证GSC是否通过优化能量代谢、促进代谢废物清除发挥抗疲劳作用,本文开展了相关动物实验。在抗疲劳小鼠实验里,GSC组显著延长了小鼠的负重游泳时间,相比于GE组,延长时间更为显著。高强度的运动会导致乳酸和尿素的积累,代谢废物会对内环境产生干扰,血氨水平过高会对脑细胞造成神经毒性[26-27],GSC可能通过以上途径改善了小鼠的运动表现且效果优于GE。肌糖原在运动与疲劳中起着关键作用,餐后摄取的葡萄糖80%以上通过肌肉消耗[28]。在高强度运动中,碳水化合物的氧化,尤其是肌肉糖原的氧化占主导地位[29]。在运动早期,肌糖原的分解及甘油三酯脂肪酸氧化最为强烈,随着葡萄糖摄取的增加,肝糖原糖原及糖异生增强[30-31]。因此肌糖原浓度的维持对于提高运动表现至关重要。GSC可能通过激活PI3K-Akt信号通路促进肌肉中糖原合成[32],进而为运动过程提供能量,改善小鼠运动表现。
随着近年来对疲劳机制研究的不断深入,越来越多文献表明肠道菌群可通过影响骨骼肌、骨骼健康和减少肠道中乳酸生成及吸收来提高运动表现[33-35]。有研究表明,拟杆菌门的增加有助于分解膳食纤维及淀粉释放能量[36],且与炎症因子TNF-α、IL-6水平呈现负相关[37]。瘤胃球菌属已被证明是丁酸主要生产者,可进行多糖、纤维降解,与能量代谢密切相关[38]。乳杆菌属为耐力运动员的主要肠道益生菌[39],可促进抑炎因子表达,抑制肠道有害细菌生长,保护肠道黏膜屏障和免疫系统功能[40],并且能促进蛋白质的利用,增加支链氨基酸含量,从而抑制疲劳的发生发展[41]。此外,癌症相关疲劳发生时,罕见小球菌属相对丰度出现下降[42],罕见小球菌属可促进丁酸盐产生,有助于减少肠道炎症和氧化应激[43]。丁酸盐在肠道扮演重要角色,一方面其可被结肠吸收用于产生能量,另一方面可对肠道整体环境、黏膜屏障及炎症、氧化应激状态产生影响[44]。另外有研究表明,丁酸盐可通过激活ERK/MAPK通路促进C2C12成肌细胞增殖[45]。GSC可能通过调节上述菌群丰度,促进丁酸产生,进而进一步激活体内中MAPK信号通路,最终对抗疲劳产生积极影响。在本研究中,GSC的干预可以促进瘤胃球菌属、瘤胃球菌属某种、肠乳杆菌、罕见小球菌属某种丰度的增加,而这些菌株有助于改善能量代谢与肠道健康,提高运动耐力,进一步表明GSC对改善疲劳能量代谢产生了积极影响。
该研究证实了GSC具备抗疲劳作用,并且通过一系列实验明确了GSC对能量代谢及代谢废物清除存在显著影响,符合前期网络药理学预测结果。然而,不可忽视的是,GSC抗疲劳的具体机制仍未完全明晰,这限制了研究者对其作用本质的深入理解与应用拓展。因此,后续的机制探索应紧密围绕网络药理学富集结果PI3K-Akt、MAPK等信号通路展开,精准挖掘GSC在这些通路中的关键作用节点,力求全面揭示GSC抗疲劳的深层机制。
综上所述,本研究通过UPLC-QTOF-MS检测分析技术、分子对接技术及动物实验探究了GSC改善疲劳的作用及潜在机制。人参经过沙棘转化后提高了20(S)-Rg2等10种稀有皂苷的含量,通过进一步的网络药理学预测结果表明,GSC可能通过关键皂苷成分Rf、Ro、Rh2、Rg5与关键靶点PIK3CA、EGFR、SRC、PIK3R1、JAK2结合,进而激活PI3K-AKT、MAPK等信号通路起抗疲劳作用。在进一步动物实验中,网络药理学中预测的GSC抗疲劳活性进一步得到证实,GSC促进了代谢废物清除及能量物质的供应,显示出良好的抗疲劳作用。另一方面,GSC影响了小鼠的肠道菌群,改变了拟杆菌门和厚壁菌门相对丰度,并增加了瘤胃球菌属、肠乳杆菌、罕见小球菌等肠道有益菌丰度,GSC改善小鼠疲劳的功效可能源于其对肠道菌群的改变。以上结果均表明,GSC是一种具有广阔前景的抗疲劳转化物,对GSC抗疲劳机制进一步研究,可为GSC的进一步开发和应用提供实验依据。
[1] 吴名草,王晶,沈旭丹,等.人参葛根植物饮料对小鼠体力疲劳的缓解作用研究[J].粮油食品科技,2022,30(5):212-218.WU M C,WANG J,SHEN X D,et al.Research on relieving effect of botanical beverage with ginseng extract and pueraria extract on physical fatigue in mice[J].Science and Technology of Cereals,Oils and Foods,2022,30(5):212-218.
[2] CALDWELL J A,CALDWELL J L,THOMPSON L A,et al.Fatigue and its management in the workplace[J].Neuroscience &Biobehavioral Reviews,2019,96:272-289.
[3] 徐艺园,王凯,王佳音,等.疲劳产生相关机制研究进展[J].科学技术创新,2019(23):50-51.XU Y Y,WANG K,WANG J Y,et al.Research progress on related mechanisms of fatigue[J].Scientific and Technological Innovation,2019(23):50-51.
[4] 曹晶晶,杨卫杰,曹轶.刺梨多糖的抗氧化和抗疲劳研究[J].中国中医基础医学杂志,2018,24(4):474-476; 481.CAO J J,YANG W J,CAO Y.Anti-fatigue and antioxidant activity of the polysaccharides isolated from Rosa roxburghii tratt.F.normalis rehd.et wils[J].Chinese Journal of Basic Medicine in Traditional Chinese Medicine,2018,24(4):474-476; 481.
[5] 陈虹宇,曹洋,杨华平.林下山参与栽培人参的应用价值剖析[J].中医药导报,2019,25(6):67-68; 81.CHEN H Y,CAO Y,YANG H P.Analysis on the application value of ginseng cultivation under forest mountain[J].Guiding Journal of Traditional Chinese Medicine and Pharmacy,2019,25(6):67-68; 81.
[6] 李贵明,李燕.人参皂苷药理作用研究现状[J].中国临床药理学杂志,2020,36(8):1024-1027.LI G M,LI Y.Research status of pharmacological effects of ginsenosides[J].The Chinese Journal of Clinical Pharmacology,2020,36(8):1024-1027.
[7] 郑怡菲,李涛,赵余庆.人参有效成分抗疲劳作用机制的研究进展[J].药物评价研究,2023,46(11):2496-2504.ZHENG Y F,LI T,ZHAO Y Q.Research progress of anti-fatigue mechanism of active components of ginseng[J].Drug Evaluation Research,2023,46(11):2496-2504.
[8] 王学芳,任红贤,封颖璐.人参皂苷单体的抗疲劳作用研究进展[J].解放军医药杂志,2019,31(12):114-116.WANG X F,REN H X,FENG Y L.Research progress on anti-fatigue effect of ginsenoside monomer[J].Medical &Pharmaceutical Journal of Chinese PLA,2019,31(12):114-116.
[9] HOPKINS A L.Network pharmacology[J].Nature Biotechnology,2007,25(10):1110-1111.
[10] 张楠,杨帆,马仲帅,等.基于网络药理学探究滇黄精抗疲劳作用及其机制[J].云南农业大学学报(自然科学),2024,39(1):101-110.ZHANG N,YANG F,MA Z S,et al.Antifatigue effect and mechanism of Polygonatum kingianum based on network pharmacology[J].Journal of Yunnan Agricultural University (Natural Science),2024,39(1):101-110.
[11] 刘秋容,许先梅,许震,等.基于UPLC-Q-TOF-MS技术和网络药理学人参黄精杏麦饮化学成分群的抗疲劳作用研究[J].沈阳药科大学学报,2024,41(8):1097-1108.LIU Q R,XU X M,XU Z,et al.Study on the anti-fatigue effect of the chemical constituents of Ginseng Huangjing Xing Mai Yin based on UPLC-Q-TOF-MS technology and network pharmacology[J].Journal of Shenyang Pharmaceutical University,2024,41(8):1097-1108.
[12] ESTÉVEZ-SOUTO V,DA SILVA- LVAREZ S,COLLADO M.The role of extracellular vesicles in cellular senescence[J].The FEBS Journal,2023,290(5):1203-1211.
LVAREZ S,COLLADO M.The role of extracellular vesicles in cellular senescence[J].The FEBS Journal,2023,290(5):1203-1211.
[13] GÖRAN RONQUIST K.Extracellular vesicles and energy metabolism[J].Clinica Chimica Acta,2019,488:116-121.
[14] GILOTEAUX L,O′NEAL A,CASTRO-MARRERO J,et al.Cytokine profiling of extracellular vesicles isolated from plasma in myalgic encephalomyelitis/chronic fatigue syndrome:A pilot study[J].Journal of Translational Medicine,2020,18(1):387.
[15] ZHU S M,SUN F,LI W J,et al.Apelin stimulates glucose uptake through the PI3K/Akt pathway and improves insulin resistance in 3T3-L1 adipocytes[J].Molecular and Cellular Biochemistry,2011,353(1):305-313.
[16] LIU T Y,SHI C X,GAO R,et al.Irisin inhibits hepatic gluconeogenesis and increases glycogen synthesis via the PI3K/Akt pathway in type 2 diabetic mice and hepatocytes[J].Clinical Science,2015,129(10):839-850.
[17] MANNING B D,TOKER A.AKT/PKB signaling:Navigating the network[J].Cell,2017,169(3):381-405.
[18] 石崯力,王旭,盛沛,等.运用数据挖掘和网络药理学探讨糖尿病认知功能障碍中医用药规律和作用机制[J].天然产物研究与开发,2021,33(7):1223-1235.SHI Y L,WANG X,SHENG P,et al.Prescription rules and mechanism of core drugs in the treatment of diabetic cognitive dysfunction based on data mining and network pharmacology[J].Natural Product Research and Development,2021,33(7):1223-1235.
[19] 郭佳龙,刘畅,王瑶,等.稀有人参皂苷的应用基础与开发利用研究进展[J].中国中药杂志,2024,49(2):304-314.GUO J L,LIU C,WANG Y,et al.Research progress on development and utilization of minor ginsenosides[J].China Journal of Chinese Materia Medica,2024,49(2):304-314.
[20] 袁松竹,王斌,周旋,等.稀有人参皂苷生物转化的研究进展[J].食品工业科技,2023,44(12):480-489.YUAN S Z,WANG B,ZHOU X,et al.Research progress on biotransformation of rare ginsenoside[J].Science and Technology of Food Industry,2023,44(12):480-489.
[21] LI Y H,LI J J,XU F Q,et al.Gut microbiota as a potential target for developing anti-fatigue foods[J].Critical Reviews in Food Science and Nutrition,2023,63(18):3065-3080.
[22] CHEN Y Y,GAO T H,BAI J,et al.Ren-Shen-Bu-Qi decoction alleviates exercise fatigue through activating PI3K/AKT/Nrf2 pathway in mice[J].Chinese Medicine,2024,19(1):154.
[23] ZHUANG C L,MAO X Y,LIU S,et al.Ginsenoside Rb1 improves postoperative fatigue syndrome by reducing skeletal muscle oxidative stress through activation of the PI3K/Akt/Nrf2 pathway in aged rats[J].European Journal of Pharmacology,2014,740:480-487.
[24] HU M H,HAN M X,ZHANG H,et al.Curcumin (CUMINUP60®) mitigates exercise fatigue through regulating PI3K/Akt/AMPK/mTOR pathway in mice[J].Aging,2023,15(6):2308-2320.
[25] ZHANG G L,LU B F,WANG E H,et al.Panax ginseng improves physical recovery and energy utilization on chronic fatigue in rats through the PI3K/AKT/mTOR signalling pathway[J].Pharmaceutical Biology,2023,61(1):316-323.
[26] ZHAO R Y,WU R M,JIN J J,et al.Signaling pathways regulated by natural active ingredients in the fight against exercise fatigue-a review[J].Frontiers in Pharmacology,2023,14:1269878.
[27] GOUGH L A,SPARKS S A,MCNAUGHTON L R,et al.A critical review of citrulline malate supplementation and exercise performance[J].European Journal of Applied Physiology,2021,121(12):3283-3295.
[28] MERZ K E,THURMOND D C.Role of skeletal muscle in insulin resistance and glucose uptake[J].Comprehensive Physiology,2020,10(3):785-809.
[29] HARGREAVES M,SPRIET L L.Skeletal muscle energy metabolism during exercise[J].Nature Metabolism,2020,2(9):817-828.
[30] SYLOW L,KLEINERT M,RICHTER E A,et al.Exercise-stimulated glucose uptake:Regulation and implications for glycaemic control[J].Nature Reviews Endocrinology,2017,13(3):133-148.
[31] RICHTER E A,HARGREAVES M.Exercise,GLUT4,and skeletal muscle glucose uptake[J].Physiological Reviews,2013,93(3):993-1017.
[32] GOLDAR S,KHANIANI M S,DERAKHSHAN S M,et al.Molecular mechanisms of apoptosis and roles in cancer development and treatment[J].Asian Pacific Journal of Cancer Prevention,2015,16(6):2129-2144.
[33] CLAUSS M,GÉRARD P,MOSCA A,et al.Interplay between exercise and gut microbiome in the context of human health and performance[J].Frontiers in Nutrition,2021,8:637010.
[34] TAKAHASHI K,TERASHIMA H,KOHNO K,et al.A stand-alone synbiotic treatment for the prevention of D-lactic acidosis in short bowel syndrome[J].International Surgery,2013,98(2):110-113.
[35] LIU Z D,WU Y J,LIU T H,et al.Serotonin regulation in a rat model of exercise-induced chronic fatigue[J].Neuroscience,2017,349:27-34.
[36] STOJANOV S,BERLEC A, TRUKELJ B.The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J].Microorganisms,2020,8(11):1715.
TRUKELJ B.The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J].Microorganisms,2020,8(11):1715.
[37] 刘昊,张晋芳,李玥,等.蓝靛果多酚调控肠道健康缓解小鼠低温运动疲劳研究[J].食品科技,2024,49(8):79-88.LIU H,ZHANG J F,LI Y,et al.Effect of Lonicera caerulea berry polyphenols on regulate intestinal health and relief exercise fatigue of mice in low temperature[J].Food Science and Technology.2024,49(8):79-88.
[38] XING Y Y,XU Y Q,JIN X,et al.Optimization extraction and characterization of Artemisia ordosica polysaccharide and its beneficial effects on antioxidant function and gut microbiota in rats[J].RSC Advances,2020,10(44):26151-26164.
[39] CHEN Y M,WEI L,CHIU Y S,et al.Lactobacillus plantarum TWK10 supplementation improves exercise performance and increases muscle mass in mice[J].Nutrients,2016,8(4):205.
[40] LIU W,CROTT J W,LYU L,et al.Diet and genetically-induced obesity produces alterations in the microbiome,inflammation and Wnt pathway in the intestine of apc(+/1638 N) mice:Comparisons and contrasts[J].Journal of Cancer,2016,7(13):1780-1790.
[41] J GER R,MOHR A E,PUGH J N.Recent advances in clinical probiotic research for sport[J].Current Opinion in Clinical Nutrition and Metabolic Care,2020,23(6):428-436.
GER R,MOHR A E,PUGH J N.Recent advances in clinical probiotic research for sport[J].Current Opinion in Clinical Nutrition and Metabolic Care,2020,23(6):428-436.
[42] XIAO C H,FEDIRKO V,BEITLER J,et al.The role of the gut microbiome in cancer-related fatigue:Pilot study on epigenetic mechanisms[J].Supportive Care in Cancer,2021,29(6):3173-3182.
[43] SABATER C,IGLESIAS-GUTIÉRREZ E,RUIZ L,et al.Next-generation sequencing of the athletic gut microbiota:A systematic review[J].Microbiome Research Reports,2023,2(1):5.
[44] SINGH V,LEE G D,SON H W,et al.Butyrate producers,“The Sentinel of Gut”:Their intestinal significance with and beyond butyrate,and prospective use as microbial therapeutics[J].Frontiers in Microbiology,2022,13:1103836.
[45] GUAN L,CAO Z Y,PAN Z Y,et al.Butyrate promotes C2C12 myoblast proliferation by activating ERK/MAPK pathway[J].Molecular Omics,2023,19(7):552-559.