杨梅(Myrica rubra)是我国南方特色水果,果实口感酸甜,富含酚酸、糖类等营养物质[1]。杨梅采摘期集中在高温多雨的夏季,极易发生腐败变质,货架期短[2]。为了延长杨梅货架期,满足多样化的消费需求,目前市场上已开发出杨梅汁、杨梅酒等众多产品。然而杨梅果渣作为此类产品的加工副产物却被大量废弃。杨梅果渣中含有丰富的糖类、多酚和膳食纤维等活性成分,具有抗氧化、降血糖、降血脂、免疫调节、改善肠道菌群等多种营养功效[3-4]。丢弃杨梅果渣不仅导致营养价值利用不足,还会造成经济损失和环境负担。
铁皮石斛(Dendrobium officinale)是我国传统名贵中药材,其药用部分一般为茎,富含多糖、黄酮类、生物碱、植物甾醇等功能活性物质,具有极高的药用和经济价值[5]。然而占铁皮石斛生物总量35%~45%的铁皮石斛叶却常作为加工副产物被直接丢弃,造成了大量的资源浪费[6]。已有研究表明,铁皮石斛叶中的功能活性成分种类与茎基本一致,其中叶多糖含量大致为茎的50%,而黄酮、多酚类和氨基酸含量则高于茎[7]。因此,铁皮石斛叶同样具有很高的应用价值。
反向传播(backpropagation,BP)神经网络是一种基于误差反向传播算法训练的多层前馈神经网络,是目前应用最广泛的人工神经网络模型[8]。BP神经网络能够学习和处理复杂的非线性关系,具备比传统的响应面法更广泛的预测范围和更高的预测精度[9-10]。龚敏慧等[11]以多糖为指标,采用BP神经网络模型结合响应面法,优化了复合乳酸菌发酵蓝莓汁工艺。CHEN等[12]利用BP神经网络构建了米糠货架期的预测模型。YANG等[13]利用BP和径向基函数神经网络实现了对816个双菌和三菌共发酵产物中蒽醌含量的预测。
铁皮石斛叶味涩,食用口感欠佳,限制了其资源化利用。将杨梅果渣与铁皮石斛叶复配,利用酶解法酶解多糖以促进多糖溶出,减小多糖的分子质量,可以增加人体对杨梅果渣和铁皮石斛叶中多糖的吸收利用率,并改善风味和口感。结合冻干工艺制备混合冻干粉,不仅能够有效利用加工副产物,还能提高产品的营养和经济价值。因此,本研究以杨梅果渣和铁皮石斛叶为原料,建立BP神经网络模型并通过遗传算法(genetic algorithm,GA)优化确定多糖酶解的最佳工艺条件,制备了富含多糖的杨梅果渣和铁皮石斛叶混合冻干粉,并对其体外抗氧化和降血糖活性进行研究,为促进杨梅果渣和铁皮石斛叶的资源化利用,提高杨梅和铁皮石斛产业的经济效益提供科学依据。
1 材料与方法
1.1 材料与试剂
杨梅,浙江省余姚市,品种为荸荠种;铁皮石斛叶,浙江寿仙谷医药股份有限公司;果胶酶、纤维素酶,河南万邦化工科技有限公司;α-葡萄糖苷酶、α-淀粉酶,上海源叶生物科技有限公司;其他试剂均为分析纯。
1.2 仪器与设备
KS-520搅拌机,广州市祈和电器有限公司;DZG-6050型真空干燥箱,上海森信实验仪器有限公司;FreeZone真空冷冻干燥机,美国LABCONCO公司;R214旋转蒸发仪,上海申生科技有限公司;XMTD-8222水浴锅,上海精宏实验设备有限公司;ReadMax 1900型光吸收全波长酶标仪,上海闪谱生物科技有限公司。
1.3 实验方法
1.3.1 样品前处理
新鲜杨梅清水洗净后去核,榨汁,留下果渣;铁皮石斛叶清水漂洗,沥干水分。将杨梅果渣和铁皮石斛叶放于60 ℃中真空干燥。使用搅拌机将干燥后的杨梅果渣和铁皮石斛叶粉碎并过80目筛。
1.3.2 杨梅果渣/铁皮石斛叶混合冻干粉酶解制备工艺
将杨梅果渣粉和铁皮石斛叶粉按质量比1∶1混合,称取5 g混合粉于烧杯中,按照一定料液比(g∶mL)加入纯净水,加入一定量的复合酶,在一定温度下酶解一定时间,酶解结束后过滤溶液,滤液90 ℃水浴20 min灭酶。随后使用旋转蒸发仪浓缩滤液,最后将浓缩液冷冻干燥,得到杨梅果渣/铁皮石斛叶混合冻干粉。
1.3.3 多糖得率测定
参考陈阳等[14]的方法,计算不同酶解条件下的多糖得率。配制质量浓度分别为0.1、0.08、0.06、0.04、0.02和0 mg/mL的葡萄糖标准溶液,取标准溶液和适当稀释后的酶解滤液各1 mL,加入1 mL 50 g/L苯酚和5 mL浓硫酸,混匀后沸水浴20 min,在波长490 nm处测定吸光值,根据葡萄糖标准曲线计算多糖得率。
1.3.4 单因素试验设计
分别固定复合酶添加量3%(质量分数),料液比1∶100 (g∶mL),复合酶(果胶酶与纤维素酶)质量配比1∶1,酶解时间1.5 h,酶解温度60 ℃,考察复合酶添加量(1%、2%、3%、4%、5%,质量分数),料液比(1∶50、1∶100、1∶150、1∶200、1∶250,g∶mL),复合酶配比(果胶酶与纤维素酶,3∶1、2∶1、1∶1、1∶2、1∶3,质量比),酶解时间(0.5、1.0、1.5、2.0、2.5 h)以及酶解温度(50、55、60、65、70 ℃)5个单因素对多糖得率的影响。
1.3.5 响应面法试验设计
基于单因素试验结果,筛选出复合酶添加量(A)、料液比(B)、酶解时间(C)、酶解温度(D)为自变量,以多糖得率为响应值,设计3水平4因素响应面优化试验。
表1 响应面试验水平与因素设计
Table 1 Levels and factors design in response surface methodology experiments

水平因素A(酶添加量)/%B(料液比)(g∶mL)C(酶解时间)/hD(酶解温度)/℃-131∶500.555041∶1001.060151∶1501.565
1.3.6 GA-BP神经网络模型设计
基于响应面试验结果,使用MATLAB平台编写BP神经网络模型,对多糖得率进行预测。该模型由输入层、隐藏层和输出层组成,输入层设计4个神经元:复合酶添加量(X1),料液比(X2),酶解时间(X3),酶解温度(X4);输出层设计1个神经元:多糖得率(Y)。使用sig函数作为隐藏层传递函数,纯线性函数作为输出层传递函数。将响应面试验得到的29组样本数据随机排序后用于训练模型,其中30%用于验证和测试。应用均方误差(mean squared error,MSE)和相关系数R评估模型的准确性。通过遗传算法预测最佳工艺条件,并进行3次验证实验。
1.3.7 体外抗氧化活性测定
参考LIU等[15]的方法测定DPPH自由基清除能力。取杨梅果渣/铁皮石斛叶混合冻干粉水溶液100 μL,加入100 μL 0.1 mmol/L的DPPH溶液,室温下避光反应30 min,于517 nm处测定吸光值。按照公式(1)计算DPPH自由基清除率:
DPPH自由基清除率![]()
(1)
式中:I0,无水乙醇代替样本的吸光度;I1,样本吸光度;I2,无水乙醇代替DPPH溶液的吸光度。
参考尤洁等[16]的方法测定ABTS阳离子自由基清除能力。取杨梅果渣/铁皮石斛叶混合冻干粉水溶液100 μL,加入100 μL ABTS反应液,室温下避光反应30 min,于734 nm处测定吸光值。按照公式(2)计算ABTS阳离子自由基清除率:
ABTS阳离子自由基清除率![]()
(2)
式中:I0,无水乙醇代替样本的吸光度;I1,样本吸光度;I2,无水乙醇代替ABTS溶液的吸光度。
1.3.8 体外降血糖活性测定
参考HU等[17]的方法测定α-葡萄糖苷酶抑制率。取杨梅果渣/铁皮石斛叶混合冻干粉水溶液100 μL,加入100 μL α-葡萄糖苷酶溶液,于37 ℃反应10 min。向溶液中加入100 μL 10 mmol/L的对硝基苯-β-D-半乳糖苷溶液混匀,于37 ℃下继续反应30 min,随后加入400 μL 0.1 mol/L的Na2CO3溶液,混匀后于405 nm处测定吸光值。按照公式(3)计算α-葡萄糖苷酶抑制率:
α-葡萄糖苷酶抑制率![]()
(3)
式中:I0,蒸馏水代替样本的吸光度;I1,样本吸光度;I2,蒸馏水代替α-葡萄糖苷酶溶液的吸光度。
参考张琪婧等[18]的方法测定α-淀粉酶抑制率。将100 μL杨梅果渣/铁皮石斛叶混合冻干粉水溶液与100 μL α-淀粉酶溶液混合,于37 ℃下反应10 min。加入100 μL 10 g/L淀粉溶液继续反应10 min,随后加入100 μL 3,5-二硝基水杨酸溶液并用蒸馏水定容至1 mL,沸水浴10 min,冷却至室温后于540 nm处测定吸光值。按照公式(4)计算α-淀粉酶抑制率:
α-淀粉酶抑制率![]()
(4)
式中:I0,蒸馏水代替样本的吸光度;I1,样本吸光度;I2,蒸馏水代替α-淀粉酶溶液的吸光度。
1.4 数据处理
每组实验重复3次,采用DesignExpert 10.0软件进行响应面试验设计与分析。采用SPSS 26.0软件进行显著性分析,采用Origin 2021软件作图。采用MATLAB软件构建神经网络模型。
2 结果与分析
2.1 单因素试验结果
2.1.1 酶添加量对多糖得率的影响
由图1-a可知,杨梅果渣/铁皮石斛叶混合冻干粉多糖得率最高时复合酶添加量为4%。而复合酶添加量为5%时,多糖得有所下降。这可能是因为复合酶用量过高时,酶与底物的定向反应反而被阻碍,抑制了酶的催化效果,导致多糖得率下降[19]。
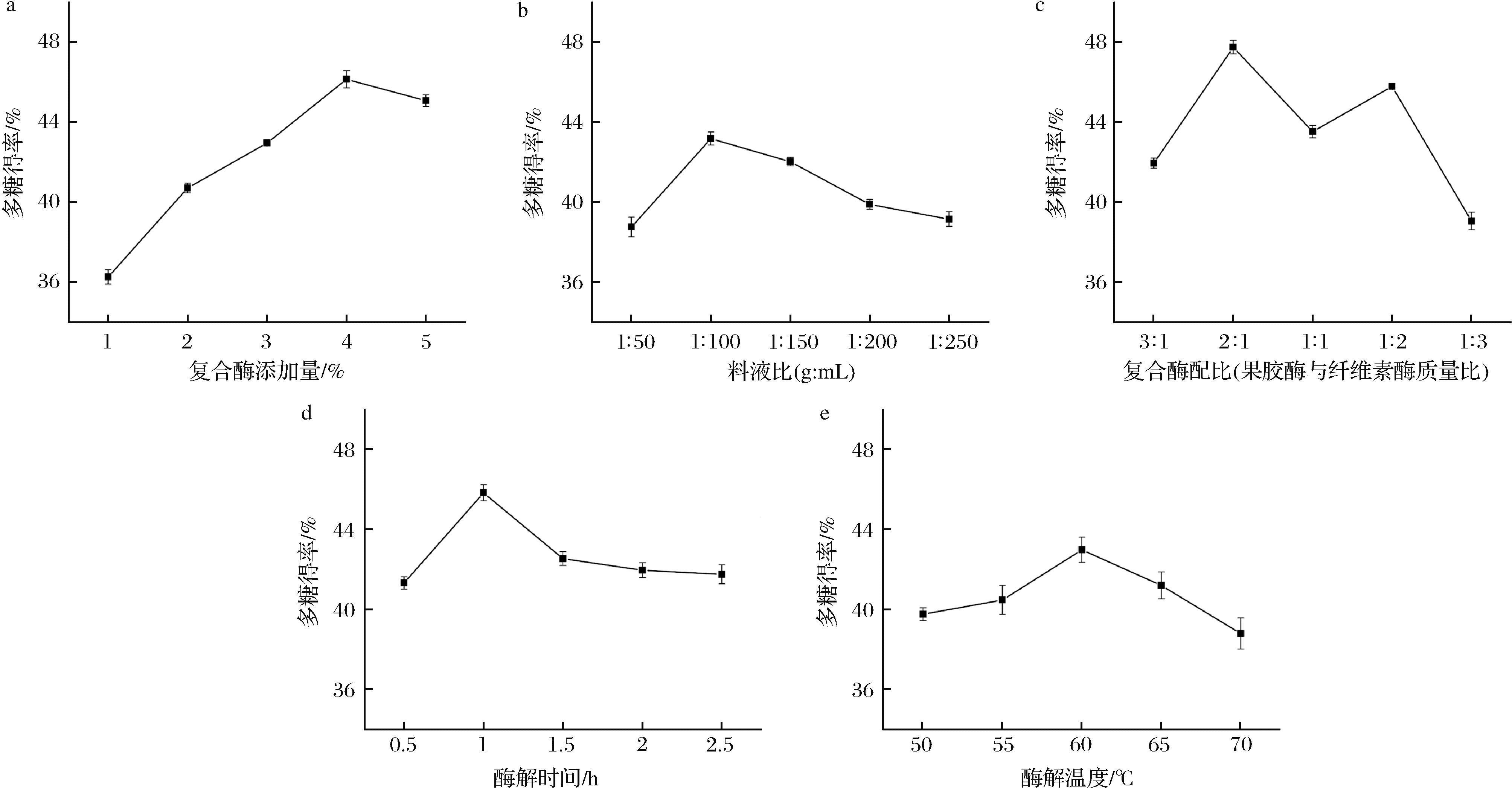
a-复合酶添加量;b-料液比;c-复合酶配比;d-酶解时间;e-酶解温度
图1 各单因素对多糖得率的影响
Fig.1 Effects of individual factors on polysaccharide yield
2.1.2 料液比对多糖得率的影响
由图1-b可知,料液比为1∶100(g∶mL)时,多糖得率最高。当溶剂用量继续增大时,多糖得率呈下降趋势,这可能是由于溶剂用量过高,其他杂质的溶出阻碍了多糖的酶解,多糖得率下降。
2.1.3 复合酶配比对多糖得率的影响
由图1-c可知,当复合酶配比(果胶酶与纤维素酶质量比)为2∶1时,多糖得率最高。纤维素酶能够切割β-1,4糖苷键,从而降解纤维素,促进细胞裂解[20-21]。果胶酶能够分解细胞壁中的果胶,破坏细胞结构,释放多糖成分[22]。因此后续试验中选择的最佳复合酶配比(果胶酶与纤维素酶质量比)为2∶1。
2.1.4 酶解时间对多糖得率的影响
由图1-d可知,酶解时间为1 h时获得最大多糖得率。此后随着酶解时间的延长,多糖得率呈下降趋势,这可能是由于过长的热作用时间导致部分多糖被分解,使得多糖得率降低[23]。
2.1.5 酶解温度对多糖得率的影响
由图1-e可知,酶解温度为50~70 ℃时,多糖得率先上升后下降,在60 ℃时达到最大值。这是由于在50~60 ℃时,纤维素酶和果胶酶活性随着温度的升高而增大,当温度超过60 ℃时,酶的空间构象发生变化,酶活性降低,导致多糖得率下降[24]。结果表明最佳酶解温度在60 ℃左右。
2.2 响应面法试验结果
2.2.1 回归方程方差分析
根据单因素试验结果,将复合酶配比(果胶酶与纤维素酶质量比)固定为2∶1,响应面优化试验结果如表2所示。对试验数据进行拟合得到响应面模型的回归方程:Y=50.01+1.60A+1.19B+0.46C+0.50D-0.35AB-0.94AC-0.12AD-0.75BC+0.16BD-0.69CD-2.46A2-3.73B2-3.06C2-2.84D2。
表2 响应面试验结果
Table 2 Response surface test results
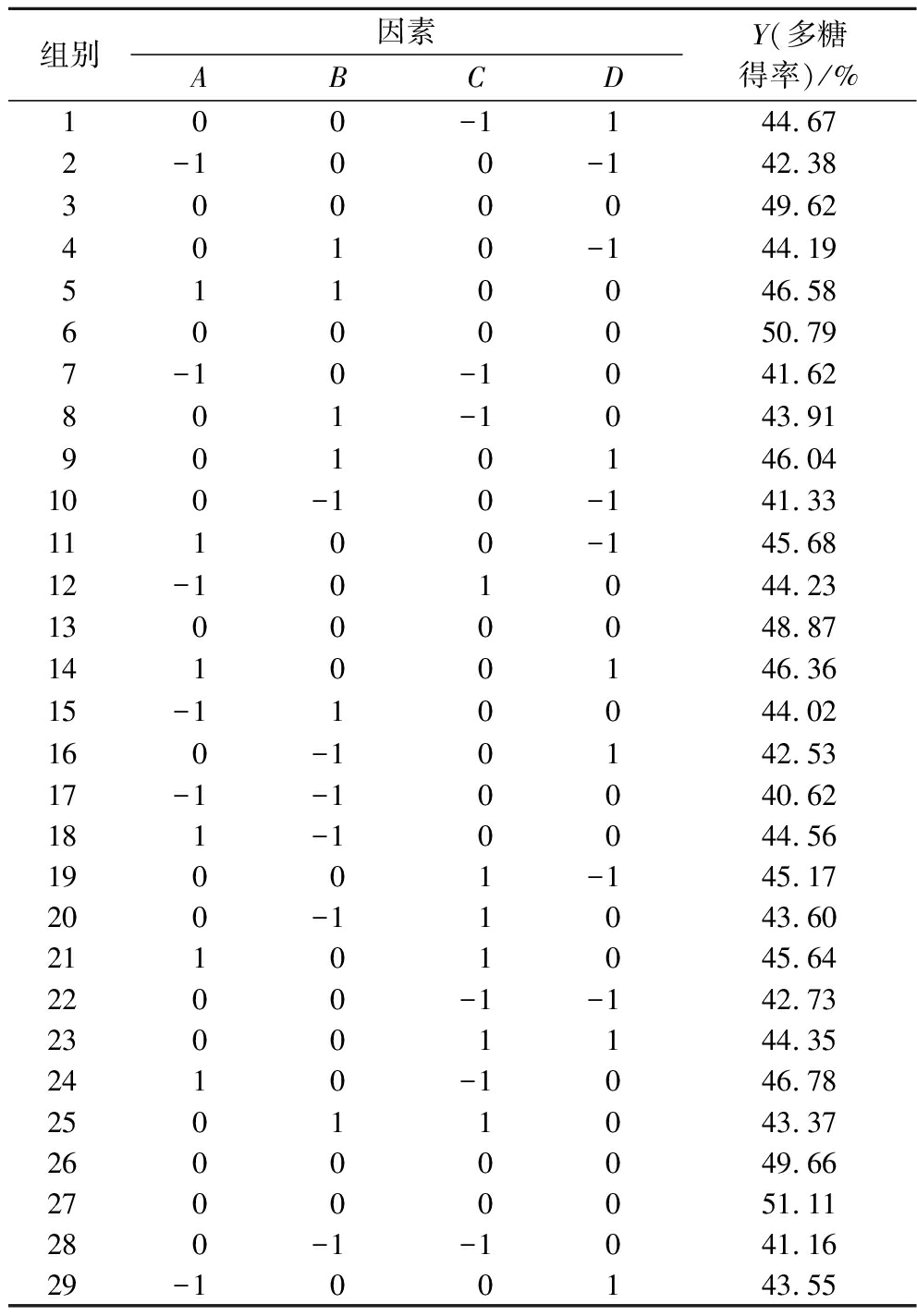
组别因素ABCDY(多糖得率)/%100-1144.672-100-142.383000049.624010-144.195110046.586000050.797-10-1041.62801-1043.919010146.04100-10-141.3311100-145.6812-101044.2313000048.8714100146.3615-110044.02160-10142.5317-1-10040.62181-10044.5619001-145.17200-11043.6021101045.642200-1-142.7323001144.352410-1046.7825011043.3726000049.6627000051.11280-1-1041.1629-100143.55
表3为回归模型的方差分析和显著性检验结果。模型P<0.000 1,失拟项P>0.05,表明响应面回归模型对试验结果的拟合程度高。根据F值大小,各单因素对多糖得率的影响程度为:复合酶添加量>料液比>酶解温度>酶解时间。其中复合酶添加量和料液比对多糖得率的影响极显著(P<0.01)。
表3 响应面试验方差分析表
Table 3 Response surface test variance analysis table
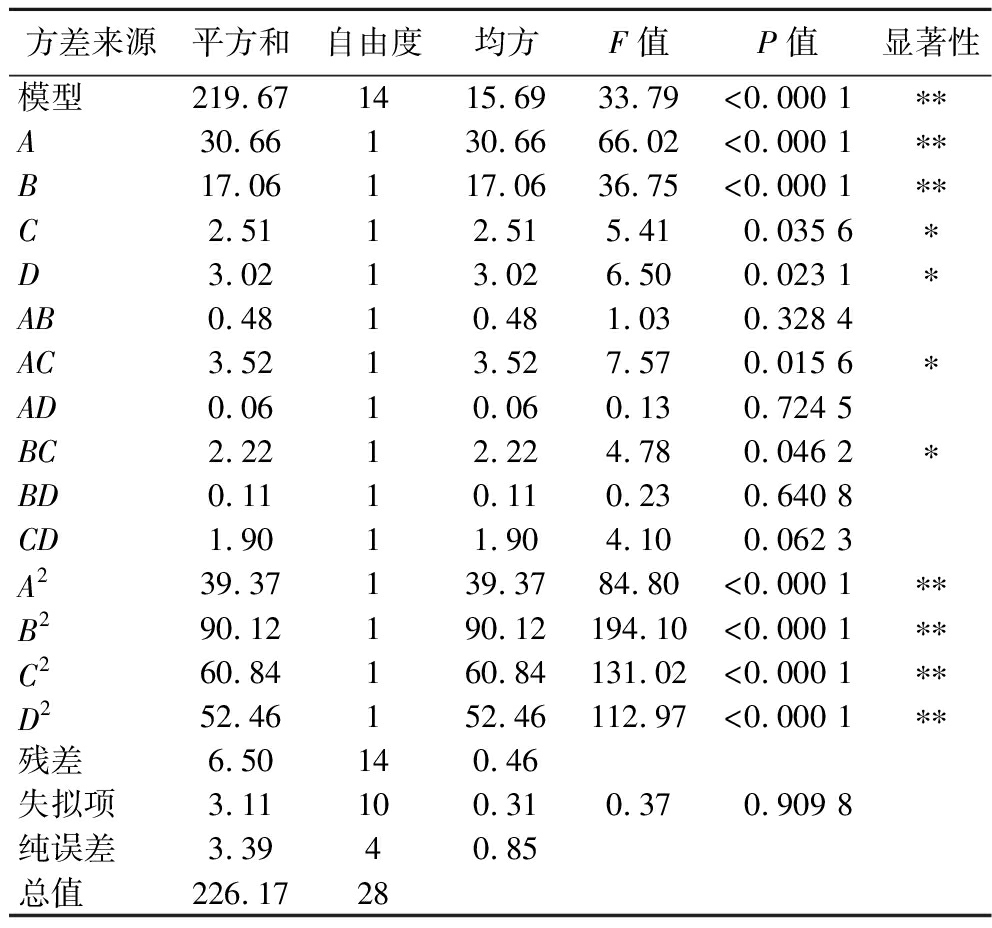
方差来源平方和自由度均方F值P值显著性模型219.671415.6933.79<0.000 1∗∗A30.66130.6666.02<0.000 1∗∗B17.06117.0636.75<0.000 1∗∗C2.5112.515.410.035 6∗D3.0213.026.500.023 1∗AB0.4810.481.030.328 4AC3.5213.527.570.015 6∗AD0.0610.060.130.724 5BC2.2212.224.780.046 2∗BD0.1110.110.230.640 8CD1.9011.904.100.062 3A239.37139.3784.80<0.000 1∗∗B290.12190.12194.10<0.000 1∗∗C260.84160.84131.02<0.000 1∗∗D252.46152.46112.97<0.000 1∗∗残差6.50140.46失拟项3.11100.310.370.909 8纯误差3.3940.85总值226.1728
注:![]() 表示有显著差异(P<0.05);**表示有极显著差异(P<0.01)。
表示有显著差异(P<0.05);**表示有极显著差异(P<0.01)。
2.2.2 响应曲面图分析
由表3可知,交互项AC和BC即复合酶添加量与酶解时间、料液比与酶解时间之间的交互作用对多糖得率的影响显著(P<0.05)。其响应面图如图2所示。2个交互作用的3D曲面图坡度均较陡,表明其对多糖得率的影响程度高。
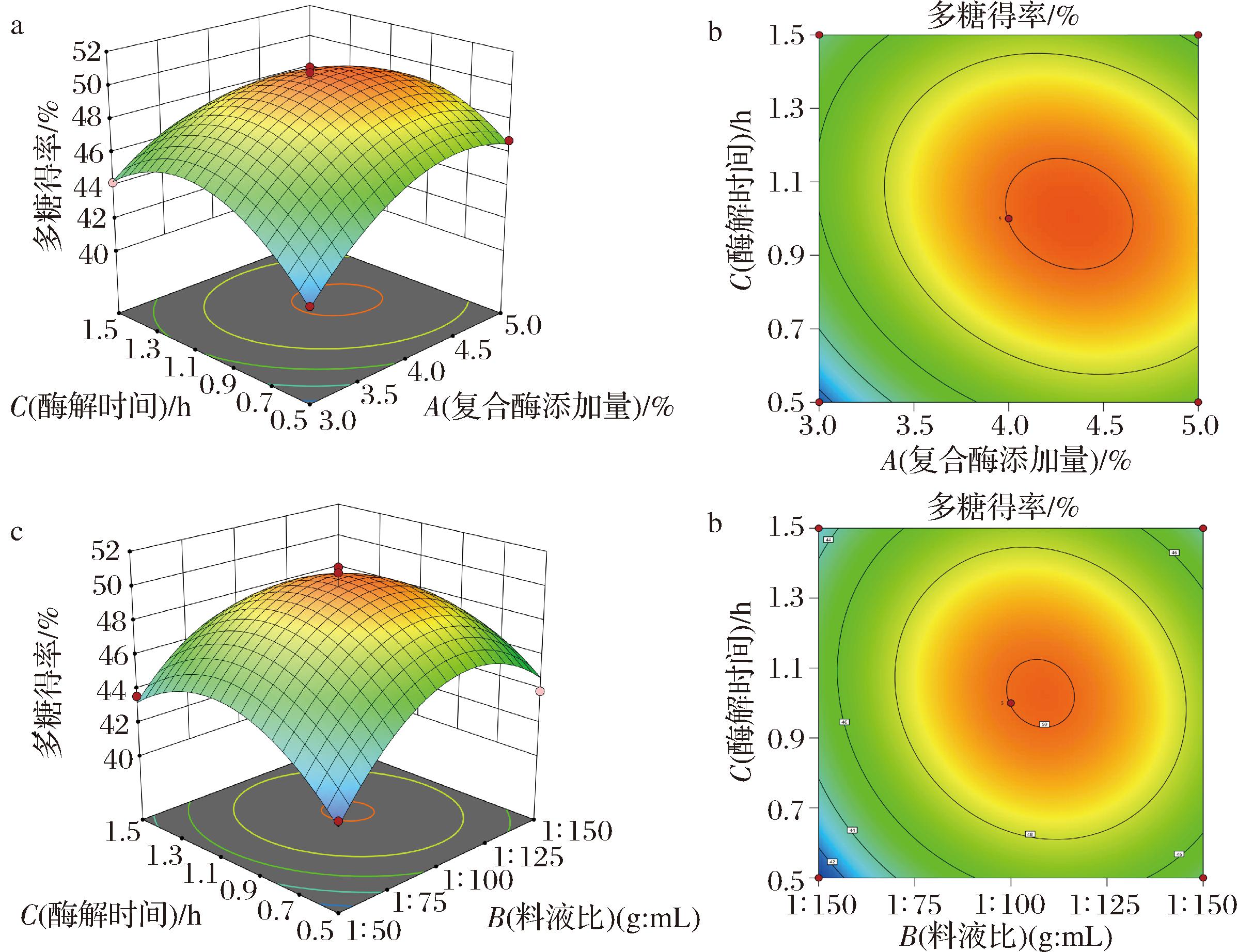
a-复合酶添加量与酶解时间之间交互作用的响应曲面图;b-复合酶添加量与酶解时间之间交互作用的等高线图;c-料液比与酶解时间之间交互作用的响应曲面图;d-料液比与酶解时间之间交互作用的等高线图
图2 因素间交互作用对多糖得率的影响
Fig.2 Effects of interfactor interactions on polysaccharide yield
图2-a、图2-b为料液比1∶100(g∶mL)、酶解温度60 ℃时复合酶添加量与酶解时间的交互作用。当料液比较高时,增加复合酶用量能够有效提高酶与底物的接触量,进而提升多糖得率。而当溶剂量继续增加,非多糖杂质溶出量增多,即使提高酶用量也难以克服溶剂阻力,导致多糖得率出现下降趋势。
图2-c、图2-d为复合酶添加量4%、酶解温度60 ℃ 时,料液比与酶解时间的交互作用。当酶解时间小于1 h时,增加溶剂用量和酶解时间可以提高多糖得率。而当时间继续延长,多糖得率随溶剂用量和时间的增加而下降。这可能是由于热作用时间延长导致部分多糖分解,此时料液比与酶解时间产生负面的交互作用。
2.3 GA-BP神经网络预测结果
2.3.1 神经网络模型的建立
将响应面试验获得的29组试验结果用于BP神经网络模型的训练。为了得到更加精确的预测结果,使用遗传算法对BP神经网络模型进行优化[25]。构建的BP神经网络结构如图3所示,以复合酶添加量、料液比、酶解时间和酶解温度这4个变量作为输入参数,隐藏层包括5个神经元,以多糖得率作为输出参数。设计训练次数为60 000,训练目标最小误差0.000 01。该模型的均方误差、平均绝对误差(mean absolute error,MAE)、均方根误差(root mean square error,RMSE)分别为0.15、0.17、0.39,表明模型具有较高的预测准确性。如图4-a所示,在训练次数高于200次后,训练性能的MSE趋于稳定并接近于0,在第336次迭代后达到最佳训练性能,此时MSE为0.004 3,表明模型具有较高的稳定性。如图4-b所示,训练数据R值为0.992 5,表明模型拟合效果好,仿真能力强。如图4-c所示,BP预测值与真实值基本吻合,表明模型对多糖得率的预测精度高。图4-d和图4-e分别为预测值与真实值的误差百分比和误差直方图,可知大部分测试样本的误差趋近于零误差线,表明模型预测误差小,对多糖得率的预测值可靠。图4-f展示了真实值和预测值之间的线性拟合关系,可知R2=0.983 3,高于响应面模型的0.971 3,表明该BP神经网络模型具有比响应面模型更可靠的预测能力。
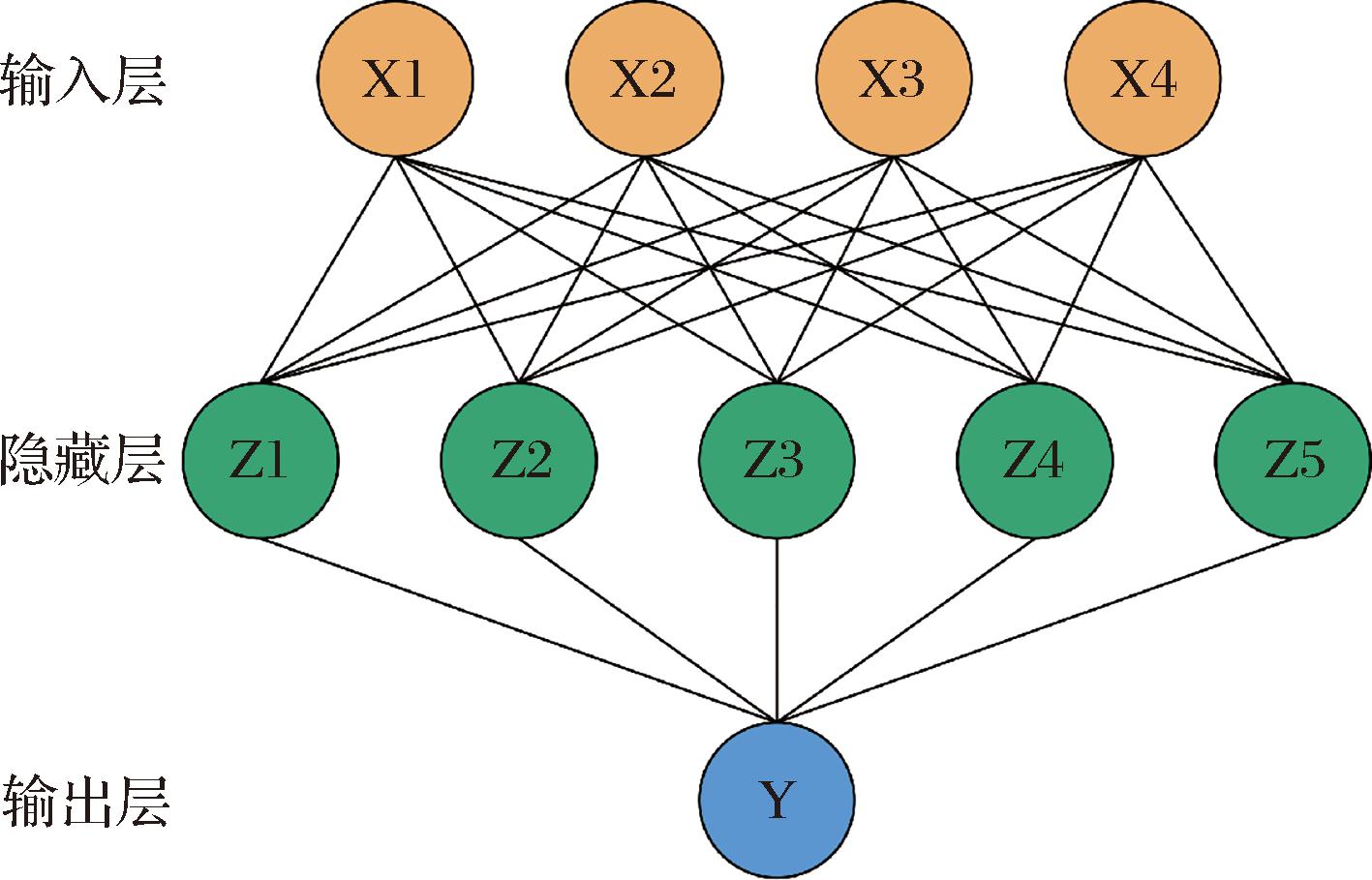
图3 BP神经网络结构示意图
Fig.3 The structure schematic diagram of BP neural network
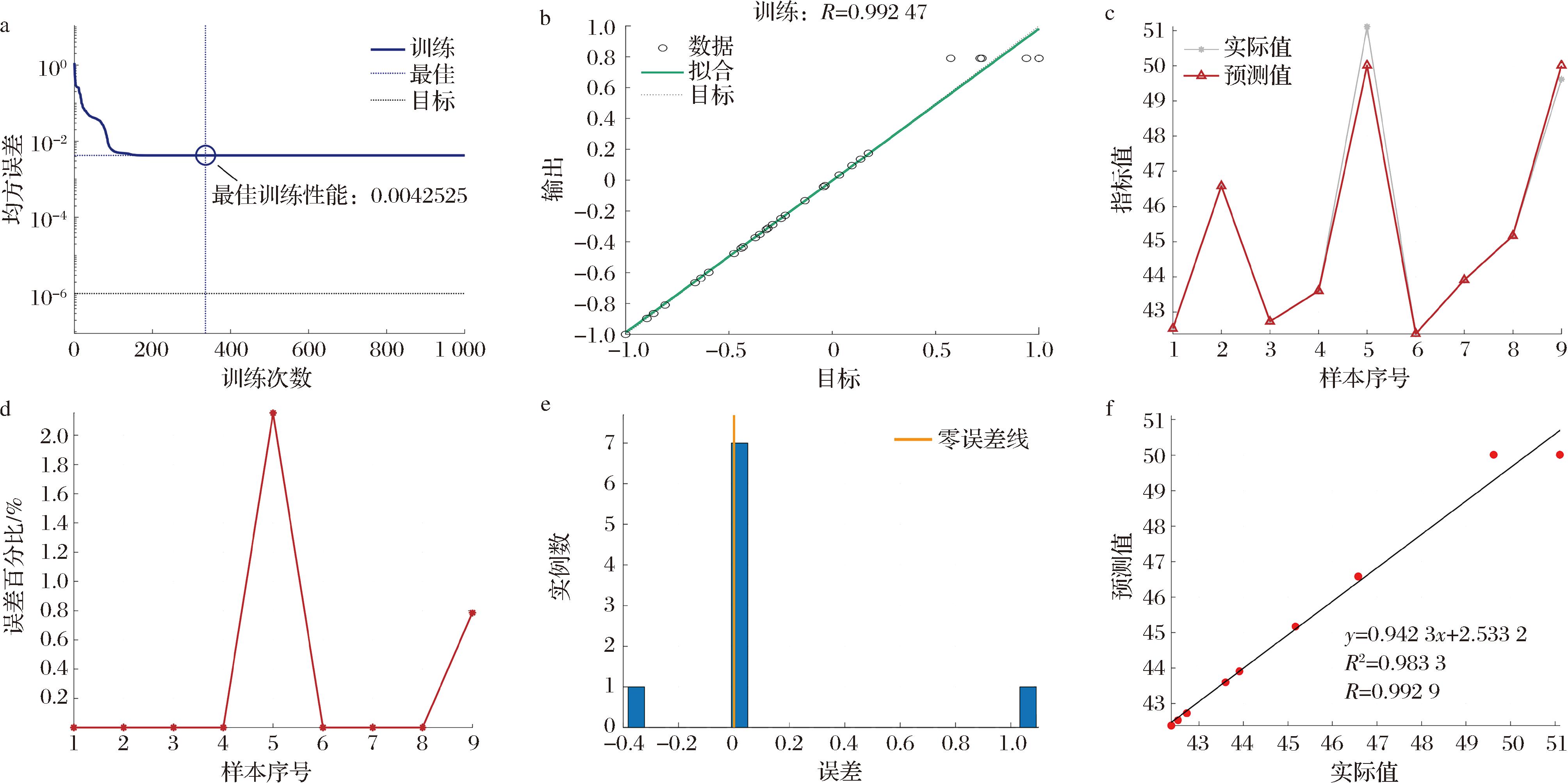
a-训练次数与均方误差关系;b-训练集回归分析;c-预测值与真实值对比;d-测试样本的误差百分比;e-测试样本的误差直方图;f-预测值与真实值的线性回归分析
图4 BP神经网络模型训练结果
Fig.4 Training results of BP neural network model
注:b图中输出=0.98×目标-0.002 5。
2.3.2 寻优预测结果
使用遗传算法确定多糖酶解最佳工艺。设计最大迭代次数50,种群个体数200。图5为适应度值随迭代次数变化的趋势图。在第15次迭代后,平均适应度接近于最佳适应度并趋于稳定。根据迭代寻优结果得到预测的最佳酶解工艺:复合酶添加量4.42%,料液比1∶111.7(g∶mL),酶解时间1.11 h,酶解温度59.71 ℃,该条件下多糖得率理论值为50.50%。结合实际调整多糖酶解最佳工艺条件为:复合酶添加量4.4%,料液比1∶112(g∶mL),酶解时间1.1 h,酶解温度60 ℃。在该条件下进行验证实验,得到多糖实际得率为(51.42±0.29)%,与预测值基本一致,证明所建立的GA-BP网络明模型可用于杨梅果渣与铁皮石斛叶的多糖酶解工艺优化中。
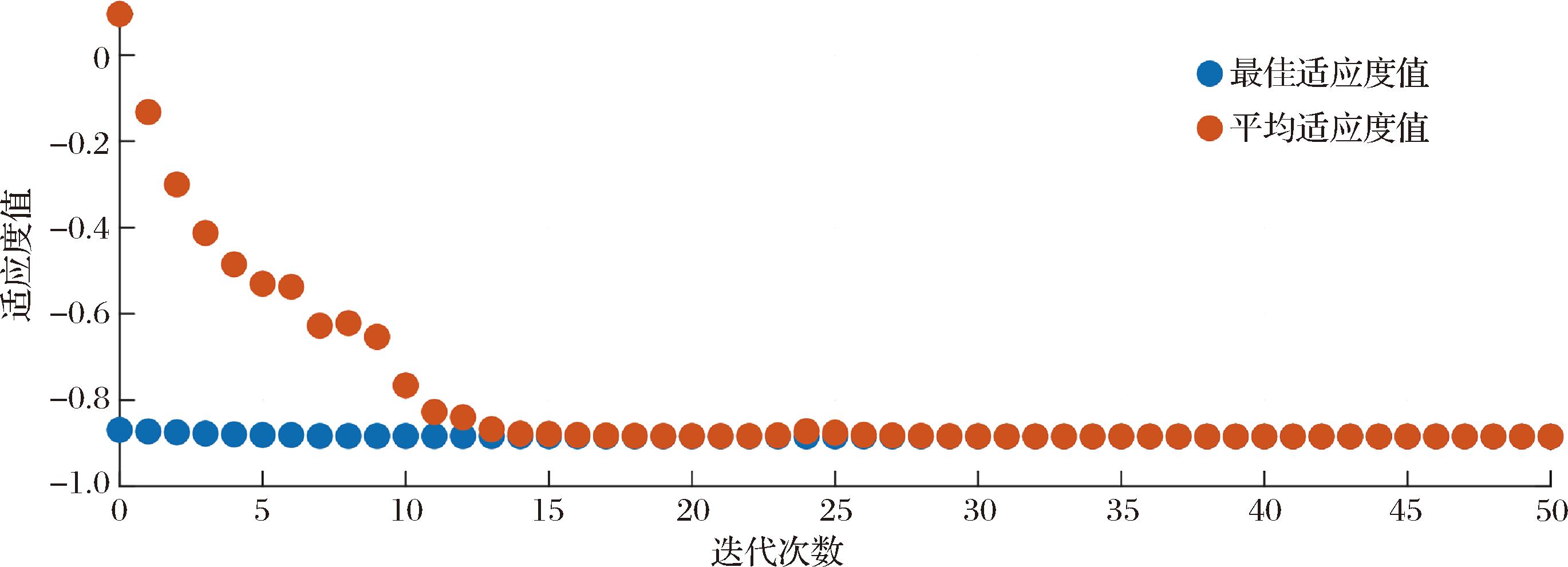
图5 GA迭代寻优结果
Fig.5 GA iterative optimization results
2.4 杨梅果渣/铁皮石斛叶混合冻干粉体外抗氧化能力
植物多糖含有大量的羟基等还原基团,可以与自由基结合,阻断自由基链式反应[26]。研究表明,相比高分子质量多糖紧凑的空间结构,低分子质量多糖因为暴露了更多的还原基团而具有更高的抗氧化活性[27-28]。此外,杨梅果渣和铁皮石斛叶中丰富的酚类和黄酮类活性成分同样具备较强的抗氧化活性[29-30]。因此,本研究考察了混合冻干粉的体外抗氧化能力。如图6所示,杨梅果渣/铁皮石斛叶混合冻干粉水溶液对DPPH自由基和ABTS阳离子自由基的清除能力随着质量浓度的增大而逐渐增强。当水溶液质量浓度为10 mg/mL时,其对DPPH自由基和ABTS阳离子自由基的清除率分别达(58.31±0.78)%和(61.77±2.21)%,表明杨梅果渣/铁皮石斛叶混合冻干粉具有良好的抗氧化能力。
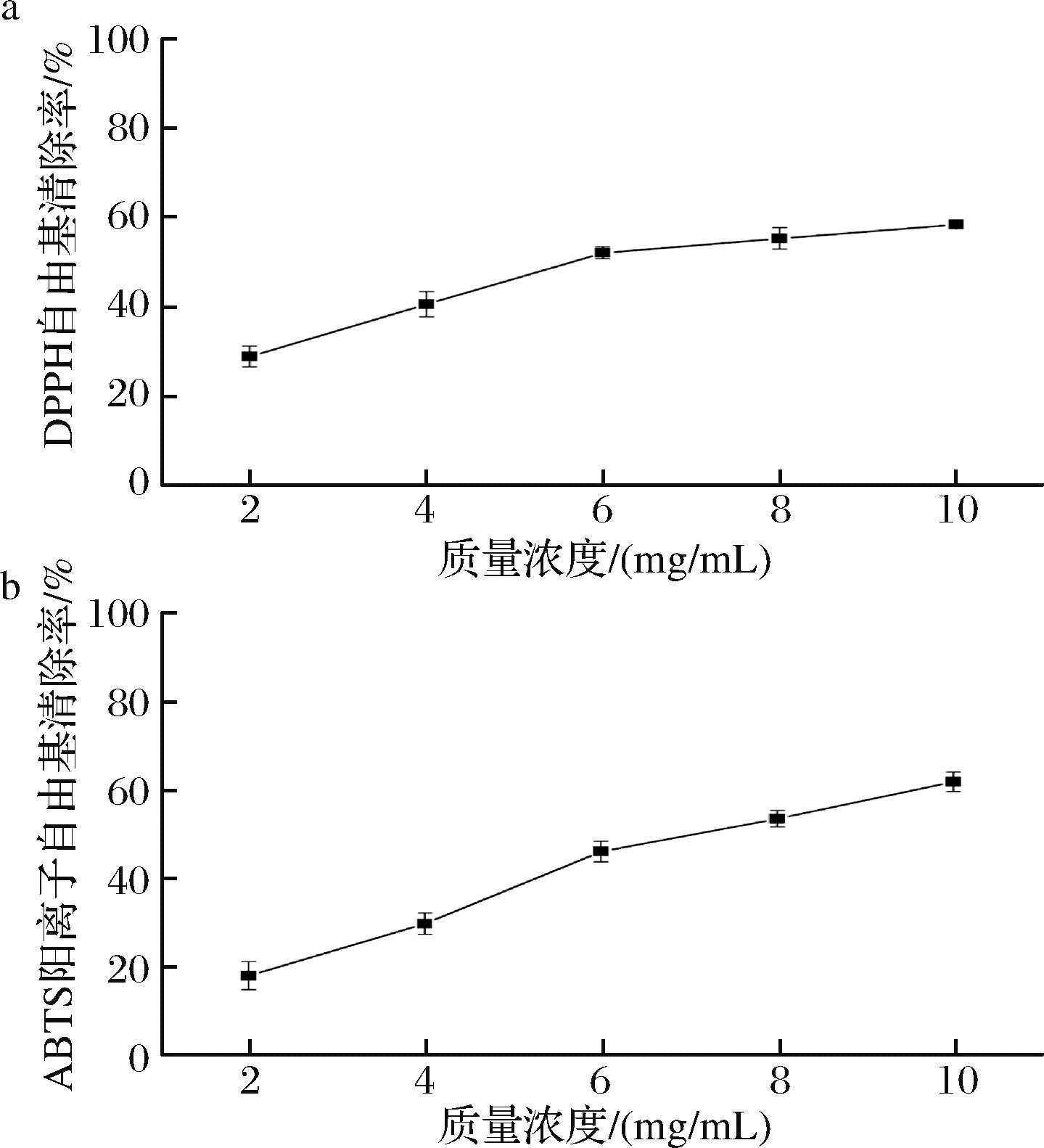
a-DPPH自由基清除活性;b-ABTS阳离子自由基清除活性
图6 杨梅果渣/铁皮石斛叶混合冻干粉的体外抗氧化活性
Fig.6 In vitro antioxidant activity of M.rubra pomace/D.officinale leaf
2.5 杨梅果渣/铁皮石斛叶混合冻干粉体外降血糖作用
α-葡萄糖苷酶和α-淀粉酶在参与机体消化碳水化合物过程起着重要作用[17]。已有研究表明,多糖、酚类、黄酮类和膳食纤维等活性物质可以抑制这2种酶的活性,从而延缓葡萄糖吸收,发挥降血糖功效[31-34]。因此,本研究还考察了混合冻干粉的体外降血糖能力。如图7所示,混合冻干粉水溶液对α-葡萄糖苷酶和α-淀粉酶表现出了显著的抑制能力。当水溶液质量浓度为10 mg/mL时,其对α-葡萄糖苷酶和α-淀粉酶的抑制率分别达(65.89±1.22)%和(68.21±1.49)%,表明杨梅果渣/铁皮石斛叶混合冻干粉具有较强的降血糖效果。
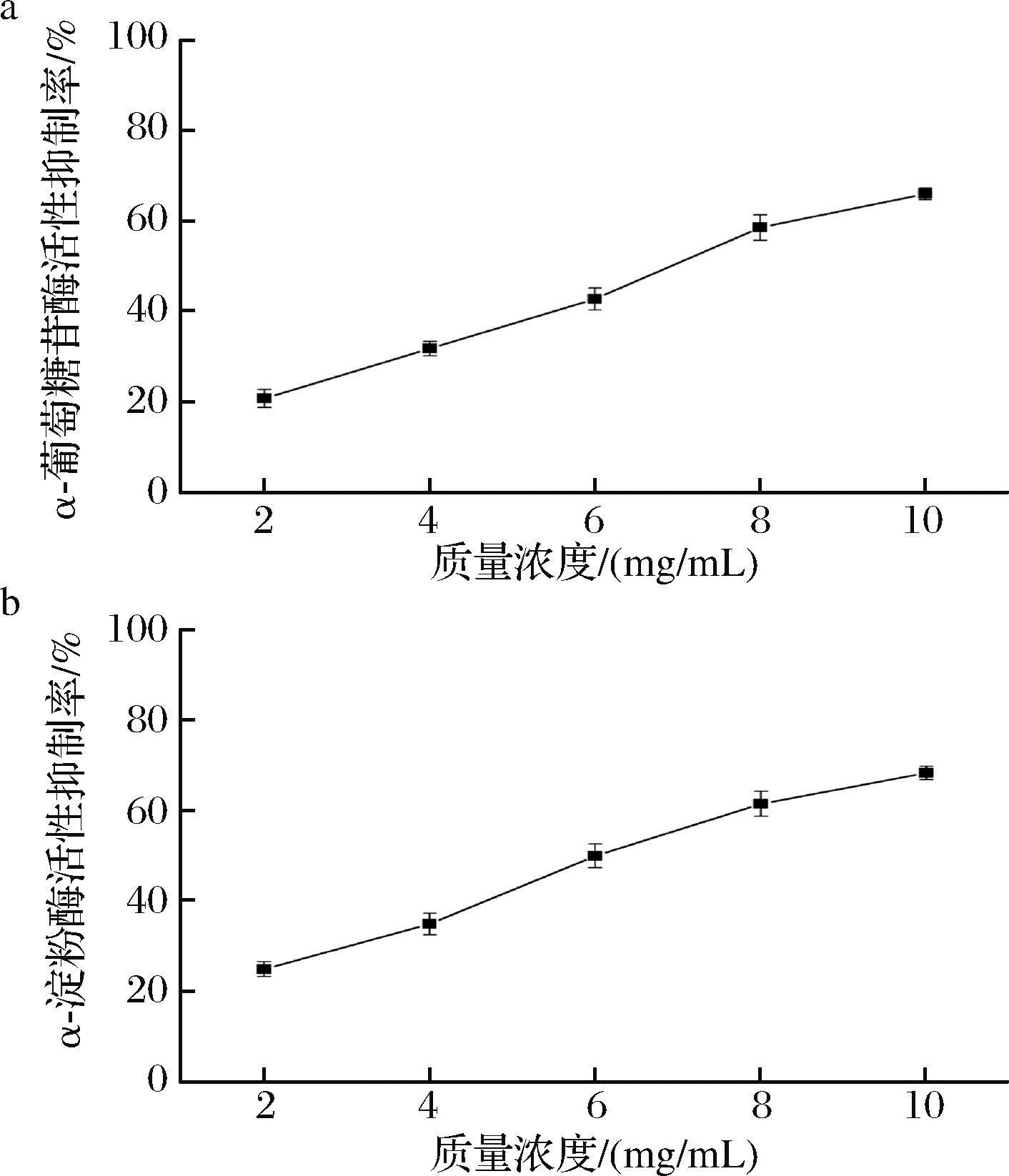
a-α-葡萄糖苷酶活性抑制能力;b-α-淀粉酶活性抑制能力
图7 杨梅果渣/铁皮石斛叶混合冻干粉的体外降血糖活性
Fig.7 In vitro hypoglycemic activity of M.rubra pomace/D.officinale leaf
3 结论
本研究通过响应面试验结合GA-BP神经网络模型,对杨梅果渣和铁皮石斛叶的多糖酶解工艺进行优化,制备了富含多糖的杨梅果渣/铁皮石斛叶混合冻干粉。GA-BP神经网络模型预测得到的最优工艺条件为复合酶添加量4.4%(质量分数),果胶酶与纤维素酶质量配比为2∶1,料液比1∶112(g∶mL),酶解时间1.1 h,酶解温度60 ℃。研究建立的BP神经网络模型具有良好的预测性,优化后的酶解工艺稳定可靠,验证实验得到多糖实际得率(51.42±0.29)%,与预测值相当。制备的杨梅果渣/铁皮石斛叶混合冻干粉对DPPH自由基和ABTS阳离子自由基表现出良好的清除能力,同时对α-葡萄糖苷酶和α-淀粉酶具有较好的抑制活性,表明杨梅果渣/铁皮石斛叶混合冻干粉具有较强的体外抗氧化和降血糖能力。综上所述,实验结果为杨梅果渣和铁皮石斛叶的资源化利用和工业化生产提供了参考依据。
[1] ZHANG S W,YU Z P,SUN L,et al.An overview of the nutritional value,health properties,and future challenges of Chinese bayberry[J].PeerJ,2022,10:e13070.
[2] 杨涵,李雪,王立芹,等.杨梅采后保鲜研究进展[J].浙江大学学报(农业与生命科学版),2023,49(2):200-212.YANG H,LI X,WANG L Q,et al.Research progress on postharvest preservation of Chinese bayberry fruit[J].Journal of Zhejiang University (Agriculture &Life Sciences),2023,49(2):200-212.
[3] ZHANG Z L,RUAN Q,SUN X M,et al.Optimization of enzymolysis modification conditions of dietary fiber from bayberry pomace and its structural characteristics and physicochemical and functional properties[J].Molecules,2024,29(14):3415.
[4] ZHU Y Y,LYU J M,GU Y,et al.Polysaccharides of Chinese bayberry pomace wine:Structural characteristics,antioxidant activity and influence on the bayberry wine[J].Food Bioscience,2022,50:102025.
[5] 黄晓君,汪志强,聂少平.铁皮石斛的功能活性研究及产业化现状[J].中国食品学报,2023,23(11):1-12.HUANG X J,WANG Z Q,NIE S P.Functional activity research and industrialization status of Dendrobium officinale[J].Journal of Chinese Institute of Food Science and Technology,2023,23(11):1-12.
[6] 林雨晴,陆胜民,周万怡,等.铁皮石斛叶多糖结构及其益生性质初探[J].浙江农业学报,2022,34(11):2504-2511.LIN Y Q,LU S M,ZHOU W Y,et al.Preliminary investigation about structure and probiotic properties of polysaccharides from Dendrobium officinale leaves[J].Acta Agriculturae Zhejiangensis,2022,34(11):2504-2511.
[7] 严静,蔡易熹,陈燕兰,等.铁皮石斛茎、叶、花的活性成分及综合利用研究进展[J].食品与发酵工业,2021,47(17):299-306.YAN J,CAI Y X,CHEN Y L,et al.Research progress in active components and comprehensive utilization of stems,leaves and flowers of Dendrobium officinale[J].Food and Fermentation Industries,2021,47(17):299-306.
[8] 王申申,张超,王艳梅.基于GA-BP神经网络优化北五味子籽油微胶囊制备工艺[J].食品研究与开发,2024,45(23):117-125.WANG S S,ZHANG C,WANG Y M.Study on the preparation and properties of Schisandra chinensis seed oil microcapsules based on GA-BP neural network[J].Food Research and Development,2024,45(23):117-125.
[9] 孙嘉,郑远荣,刘振民,等.基于反向传播神经网络和遗传算法的新鲜Halloumi奶酪生产工艺优化[J].食品与发酵工业,2024,50(1):133-143.SUN J,ZHENG Y R,LIU Z M,et al.Production process optimization of fresh Halloumi cheese based on BP neural network and genetic algorithm[J].Food and Fermentation Industries,2024,50(1):133-143.
[10] 代帅帅,吴伟杰,牛犇,等.机器学习在食品贮藏品质预测中的应用[J].中国食品学报,2023,23(12):337-348.DAI S S,WU W J,NIU B,et al.Application of machine learning on food storage quality prediction[J].Journal of Chinese Institute of Food Science and Technology,2023,23(12):337-348.
[11] 龚敏慧,单成俊,李双健,等.基于响应面法和人工神经网络优化复合乳酸菌发酵蓝莓汁产胞外多糖工艺[J].食品工业科技,2023,44(17):242-250.GONG M H,SHAN C J,LI S J,et al.Optimization of exocytopolysaccharide production from fermented blueberry juice by complex lactic acid bacteria based on response surface method and artificial neural network[J].Science and Technology of Food Industry,2023,44(17):242-250.
[12] CHEN C,WANG X S,JING P,et al.Kinetic analysis and back propagation neural network model for shelf-life estimation of stabilized rice bran[J].Journal of Food Engineering,2024,380:112168.
[13] YANG J,HUANG Y,XU H Y,et al.Optimization of fungi co-fermentation for improving anthraquinone contents and antioxidant activity using artificial neural networks[J].Food Chemistry,2020,313:126138.
[14] 陈阳,潘凯进,石万银,等.超声波结合酶法提取葛仙米多糖工艺优化及其在酒体中的抗疲劳活性[J].食品科技,2024,49(8):200-209.CHEN Y,PAN K J,SHI W Y,et al.Optimization of ultrasonic and enzymatic extraction process of polysaccharides from Nostoc sphaeroides Küte and its anti-fatigue activity in wine body[J].Food Science and Technology,2024,49(8):200-209.
[15] LIU L,XIANG H X,SHEN H M,et al.Effects of low phosphorus stress on the main active ingredients and antioxidant activities of Dendrobium officinale[J].Industrial Crops and Products,2021,173:114095.
[16] 尤洁,谢茹胜,吴伟斌.松针红薯糯米酒发酵工艺优化及抗氧化活性分析[J].食品工业科技,2025,46(4):185-193.YOU J,XIE R S,WU W B.Optimization of the fermentation process for pine-needle sweet-potato glutinous rice wine and analysis of its antioxidant activity[J].Science and Technology of Food Industry,2025,46(4):185-193.
[17] HU X,XIE J,BAI Y Y,et al.Extraction,in vitro hypoglycaemic activity and active ingredient analysis of polyphenols from walnut green husk[J].Journal of Functional Foods,2024,122:106508.
[18] 张琪婧,耿振甲,李敏,等.覆盆子总黄酮的酶辅助闪式提取及其抗氧化、降血糖和降血脂活性分析[J].粮食与油脂,2025,38(1):115-120;126.ZHANG Q J,GENG Z J,LI M,et al.Enzyme-assisted flash extraction of total flavonoids from raspberry and analysis of its antioxidant,hypoglycemic,and hypolipidemic activities[J].Cereals &Oils,2025,38(1):115-120;126.
[19] 颜凤,张家萍,崔亚雪,等.西洋参汁酶解法制备工艺研究[J].食品科技,2024,49(11):98-106.YAN F,ZHANG J P,CUI Y X,et al.Enzymatic hydrolysis preparation process of American ginseng juice[J].Food Science and Technology,2024,49(11):98-106.
[20] ZHANG H,WU J H,ZHANG M J,et al.Systematic optimization of cellulases production and extraction by Sporotrichum thermophile mutant strain TH3-9 and application in enzymatic hydrolysis of corn stover[J].Environmental Technology &Innovation,2024,36:103868.
[21] LI S C,ZHENG Y,LI M L,et al.Quantitative analyses of major enzyme activities in postharvest fruit[J].Future Postharvest and Food,2024,1(2):213-221.
[22] CHEN R Z,TAN L,JIN C G,et al.Extraction,isolation,characterization and antioxidant activity of polysaccharides from Astragalus membranaceus[J].Industrial Crops and Products,2015,77:434-443.
[23] CHENG Z Y,SONG H Y,YANG Y J,et al.Optimization of microwave-assisted enzymatic extraction of polysaccharides from the fruit of Schisandra chinensis Baill[J].International Journal of Biological Macromolecules,2015,76:161-168.
[24] DURHAM E K,SASTRY S K.Moderate electric field treatment enhances enzymatic hydrolysis of cellulose at below-optimal temperatures[J].Enzyme and Microbial Technology,2020,142:109678.
[25] 杨银爱,牛犇,陈慧芝,等.基于GA-BP神经网络和遗传算法优化雪梨莲子银耳羹工艺与风味[J].核农学报,2023,37(12):2395-2407.YANG Y A,NIU B,CHEN H Z,et al.Optimization of processing conditions and flavor of snow pear,Lotus seed and Tremella soup based on GA-BP neural network and genetic algorithm[J].Journal of Nuclear Agricultural Sciences,2023,37(12):2395-2407.
[26] LAI C H,HUO C Y,XU J,et al.Critical review on the research of chemical structure,bioactivities,and mechanism of actions of Dendrobium officinale polysaccharide[J].International Journal of Biological Macromolecules,2024,263:130315.
[27] ZHA X Q,WANG J H,YANG X F,et al.Antioxidant properties of polysaccharide fractions with different molecular mass extracted with hot-water from rice bran[J].Carbohydrate Polymers,2009,78(3):570-575.
[28] SALEHI M,RASHIDINEJAD A.Multifaceted roles of plant-derived bioactive polysaccharides:A review of their biological functions,delivery,bioavailability,and applications within the food and pharmaceutical sectors[J].International Journal of Biological Macromolecules,2025,290:138855.
[29] ZHANG Y,ZHANG L H,LIU J J,et al.Dendrobium officinale leaves as a new antioxidant source[J].Journal of Functional Foods,2017,37:400-415.
[30] ZHU Y Y,WANG M T,ZHU J J,et al.Protective effects of Chinese bayberry pomace wine against oxidative stress on Drosophila melanogaster[J].Food Research International,2024,194:114885.
[31] XU Z X,ZHENG Z H,CAI G L,et al.Improving the hypoglycemic activity of phenolic extracts from Dendrobium officinale leaves using the solid-state fermentation of edible fungi[J].Food Bioscience,2024,58:103828.
[32] SUN C D,LIU Y L,ZHAN L H,et al.Anti-diabetic effects of natural antioxidants from fruits[J].Trends in Food Science &Technology,2021,117:3-14.
[33] ZHANG X N,HUANG H Z,ZHAO X Y,et al.Effects of flavonoids-rich Chinese bayberry (Myrica rubra Sieb.et Zucc.) pulp extracts on glucose consumption in human HepG2 cells[J].Journal of Functional Foods,2015,14:144-153.
[34] ZHANG Y Q,WANG H X,CHEN H J,et al.The crucial evaluation indexes and relative measurement methods of edible value for fresh fruits and vegetables:A review[J].Future Postharvest and Food,2024,1(2):222-236.