油茶(Camellia oleifera Abel)是山茶科(Theaceae)山茶属(Camellia)的多年生植物,原产于中国,主要分布于长江流域和中国南方14省(区)[1-2]。油茶作为一种重要的木本油料树种[3],在我国有2 300多年栽培历史。目前,中国油茶种植面积占世界的95%以上,形成了千亿级的产业规模。除了茶油,果壳和饼粕是油茶产业的主要副产品,每年有超过1 000万t作为燃料或肥料被粗放地利用[4]。前人研究表明,油茶在生长发育过程中会积累丰富的代谢产物,黄酮和脂肪酸等代谢产物在油茶果中大量积累[5];其中类黄酮化合物是一种在植物界中广泛存在的代谢产物,具有抗氧化、抗癌、抗肿瘤、保护心脏等活性[6]。作为油茶产业的重要副产品,果壳和饼粕中存在大量类黄酮物质,对其进行高值化利用是相关领域的研究热点。
网络药理学基于系统生物学、药理学和现代计算机技术,通过构建生物网络揭示药物与疾病之间的复杂关系,具有“多基因、多靶点”的特点[7],代谢组学则通过高通量技术分析生物样本中的代谢产物,能够系统挖掘药用植物的化学成分差异[8];网络药理学和代谢组学的交叉应用为药用植物活性成分的研究提供了强有力的技术支撑,也为深入挖掘油茶药用价值提供了可能。2025年,我国油茶种植面积将达到600万公顷,但其开发利用水平仍较为有限[9]。油茶果为油茶生产的主要收获形式,由种仁、种壳和果壳构成,其中富含不饱和脂肪酸、黄酮、多酚和维生素E等多种活性成分,这些成分赋予了其抗氧化、抗炎、抗菌和促进消化等功效[9-13]。本研究拟在广泛靶向代谢组分析油茶果不同组织代谢物构成基础上,结合网络药理学和分子对接等技术,探索油茶果类黄酮组分抗心血管疾病的作用机制,为油茶副产品的高值化利用提供科学依据。
1 材料与方法
1.1 材料与试剂
油茶‘长林40号’,湖北省林科院黄梅基地;细胞培养试剂、药物和溶剂,上海柏辰生物科技有限公司;HepG2细胞系,上海富恒生物科技有限公司;槲皮素(质量分数99.01%),上海Selleck公司;总甘油三酯(triglycerides,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)和低密度脂蛋白胆固醇(low density lipoprotein cholesterin,LDL-C)检测试剂盒,武汉伊莱瑞特生物科技有限公司;RNA纯化试剂盒和qRT-PCR相关试剂盒,南京诺唯赞生物科技股份有限公司;实验中使用的所有化学试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
研磨仪(MM400,Retsch),37 ℃、5% CO2细胞培养箱。
1.3 实验方法
1.3.1 油茶果的代谢组分析
油茶品种‘长林40号’待果实自然成熟后采集,分别收集种仁(seed kernel,SK)、种壳(seed shell,SS)和果壳(fruit shell,FS)于冻干机(Scienta-100F)中真空冷冻干燥,利用研磨仪(MM400,Retsch)研磨(30 Hz) 1.5 min至粉末状,分别称取50 mg样品粉末,加入1 200 μL-20 ℃预冷的70%(体积分数)甲醇水内标提取液,每30 min旋涡1次,每次持续30 s,共旋涡6次;12 000 r/min离心3 min,吸取上清液,用微孔滤膜过滤样品并保存于进样瓶中,用于超高效液相色谱串联质谱(ultra performance liquid chromatography tandem mass spectrometry,UPLS-MS/MS)分析,每个组织设置3个重复。数据采集基于UPLS-MS/MS进行。本研究委托武汉迈特维尔生物科技有限公司进行,基于该公司自建数据库进行物质定性分析,基于三重四级杆质谱的多反应监测模式进行定量分析。
1.3.2 网络药理学分析
1.3.2.1 类黄酮核心成分预测及作用靶点筛选
基于代谢组学鉴定获得的油茶果类黄酮组分,通过PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)查询其分子式和分子结构;再利用Swiss Target Prediction数据库检索其潜在作用靶点(http://swiss target prediction.ch/),删除重复项,即得到油茶果类黄酮的作用靶点。将成分靶点、活性成分以及药物类黄酮导入到cytoscape 3.10.3软件中,进行网络分析。
1.3.2.2 心血管类疾病相关靶点预测
以“冠心病、高血压、冠状动脉粥样硬化性心脏病、心肌梗死”为关键词,在GeneCards数据库(http://www.genecards.org/)中进行查询,删除重复值,获得疾病靶点。将类黄酮组分的作用靶点与心血管类疾病靶点导入微生信平台(http://www.bioinformatics.com.cn/)获得交集靶点。
1.3.2.3 蛋白质-蛋白质相互作用(protein-protein interaction,PPI)构建
将交集靶点上传至String(https://string-db.org/),选择研究物种为“Homo sapiens”,设置置信度为0.9,导出蛋白互作关系文件。通过cytoscape 3.10.3软件绘制PPI,利用软件中的Network analyzer功能分析计算互作关系的连通度(Degree),以Degree值排行前5的靶点筛选为关键作用靶点,并根据连通度值调节所有节点大小和颜色深浅,利用蛋白质互作的结合率评分高低调节边的粗细。
1.3.2.4 GO和KEGG富集分析
基于DAVID生物信息学数据库(https://davidbioinformatics.nih.gov/)对核心靶基因进行系统分析。通过GO富集分析,从生物学过程(biological process,BP)、细胞组分(cell components,CC)及分子功能(molecular function,MF)3个维度解析靶基因功能特征。随后采用KEGG通路富集分析,重点揭示靶基因参与的生物通路及其调控网络。
1.3.2.5 分子对接及分子动力学模拟
通过PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)获得核心成分的mol2格式文件,将文件导入AutoDock Tools 1.5.6软件中进行配体预处理,包括氢原子添加、电荷计算和旋转键检测等操作,最后保存为pdbqt格式文件。从RCSB PDB数据库(http://www.rcsb.org/)获取目标蛋白的三维晶体结构,使用PyMOL2.3.0软件进行结构优化,包括去除结晶水分子、分离原始配体等操作,确保蛋白结构的完整性和准确性。进一步利用GROMACS2020.3软件包、amber99SB力场和SPC水模型进行分子动力学模拟分析。采用最陡下降法进行最大步数(50 000 000步)的能量最小化(energy minimization,EM)利用正则系统和等温等压系统平衡体系,在常温常压下进行100 ns的均方根偏差(root mean square error,RMSD)、原子位置的均方根波动(root mean square fluctuation,RMSF)、回转半径(Rg)和氢键(H-bond)进行分析。
1.3.2.6 扩展基因功能富集及潜在治疗靶标数据库创建
在GeneMANIA数据库中分别导入1.4筛选的核心靶点,获得各个核心靶点的20个功能相关基因,进一步整合,创建基于GeneMANIA的扩展数据库。
1.3.2.7 细胞实验验证
HepG2细胞系接入添加了15%(体积分数)胎牛血清(fetal bovine serum,FBS)的DMEM培养基,置于37 ℃、5% CO2细胞培养箱中培养。用胰蛋白酶消化细胞,并以每孔6×10 h的细胞密度接种于12孔板过夜培养。将细胞随机分为:对照组,正常培养细胞;模型组,油酸处理24 h;阳性对照组,辛伐他汀处理24 h;实验组,预测的类黄酮核心组分低、中、高剂量组(40、80、120 μg/mL)处理24 h。参照试剂盒说明书,对各组细胞的TG、TC、HDL-C和LDL-C水平进行评估。
1.3.2.8 核心靶点的差异性表达分析及real-time PCR验证
采用Gene Expression Omnibus(GEO)数据库对油茶果核心类黄酮组分干预心血管类疾病前 5名核心基因进行差异表达分析。然后借助ggpubr软件包绘制心血管类疾病患者和正常人核心靶基因的 mRNA表达的箱形图,并选取有显著性差异表达的靶点基因进行real-time PCR验证。简要步骤为,使用RNA纯化试剂盒提取并纯化细胞RNA,依据说明书进行逆转录。采用SYBR Green法通过定量PCR测定基因表达水平,即50 ℃下激活尿嘧啶-DNA糖基化酶15 min,然后85 ℃变性2 s,再经历至少40个PCR循环的三阶段扩增过程。以GAPDH为内参基因,测定目的基因表达水平,并使用2-ΔΔCt法进行定量。引物序列详见表1。
表1 引物序列
Table 1 primer sequences
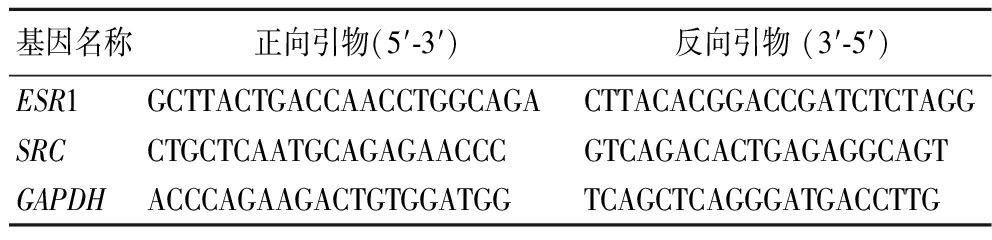
基因名称正向引物(5′-3′)反向引物 (3′-5′)ESR1GCTTACTGACCAACCTGGCAGACTTACACGGACCGATCTCTAGGSRCCTGCTCAATGCAGAGAACCCGTCAGACACTGAGAGGCAGTGAPDHACCCAGAAGACTGTGGATGGTCAGCTCAGGGATGACCTTG
1.3.2.9 药物相似性评价和安全性评价
使用ADMET lab3.0在线工具(https://admetlab3.scbdd.com/)和Pro Tox3.0数据库(https://tox.charite.de/protox3/),评估油茶果类黄酮活性成分的毒理参数,预测活性成分在各个器官中的毒性特征以及药物的吸收与分布情况。最终筛选出对肝脏、肾脏等器官毒性较小的化合物,以确定具有应用前景的类黄酮组分。
2 结果与分析
2.1 ‘长林40号’油茶果代谢物分类及主成分分析
油茶果代谢组分析共鉴定获得1 728个代谢物,其中黄酮类代谢物373种,占总代谢物的21.59%(图1-A)。主成分分析(principal component analysis,PCA)结果表明,种仁、种壳和果壳之间存在显著差异,但组内没有显著差异,说明本次实验的稳定性较好(图1-B),可进行后续的差异代谢物筛选和分析。
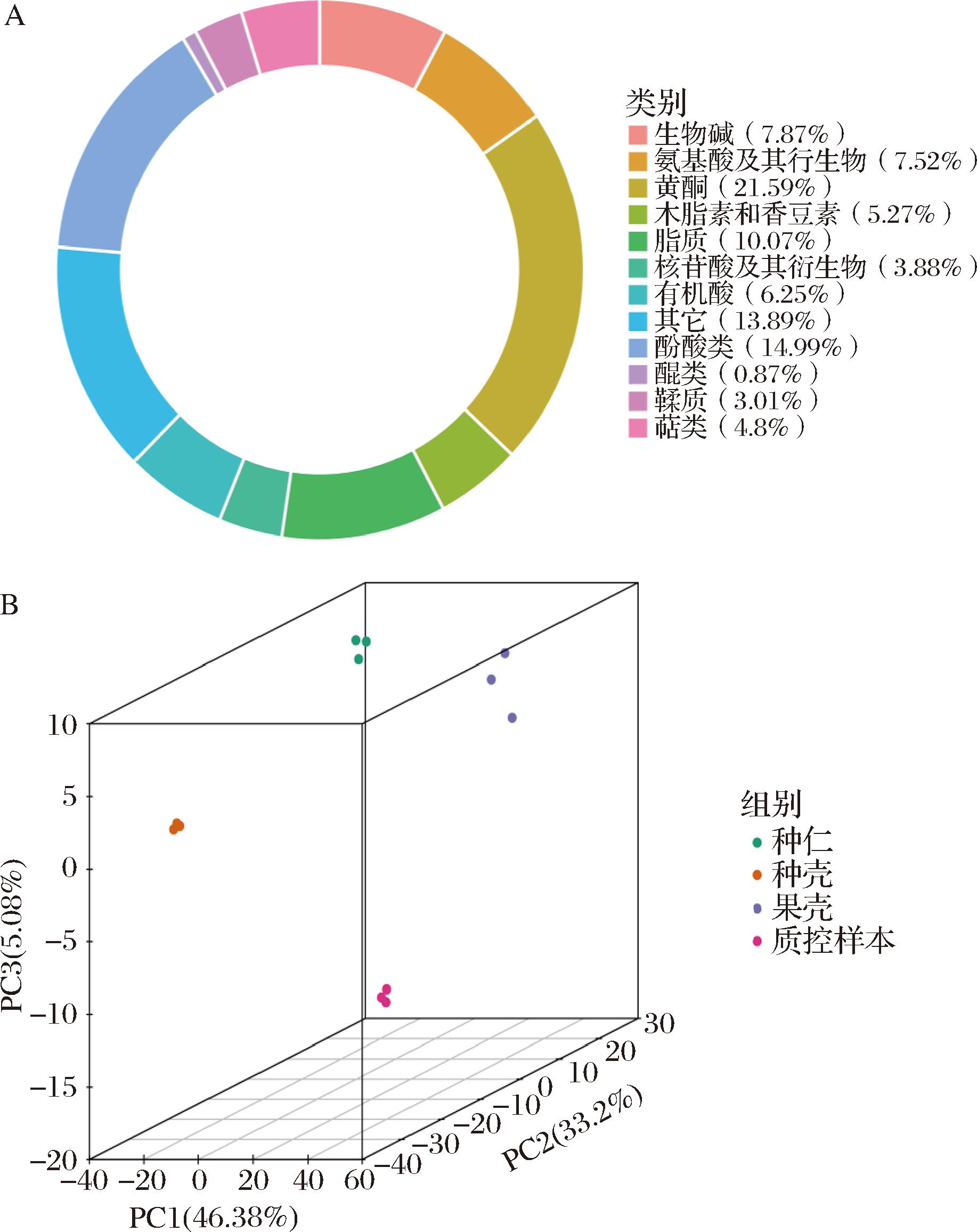
A-代谢物的分类;B-三维主成分分析
图1 油茶果代谢物鉴定
Fig.1 Identification of metabolites in Camellia oleifera fruit
2.2 ‘长林40号’油茶果类黄酮构成及核心成分预测
果壳、种壳和种仁中的黄酮含量表现出显著差异(电子版增强出版附图1,https://doi.org/10.13995/j.cnki.11-1802/ts.042956,下同);数量也表现出一定差异,其中三者共有代谢物种类336种,占所有黄酮种类的90.08%;种壳/种仁、种壳/果壳和种仁/果壳的差异黄酮物质数量分别为30、24、20种,果壳特有黄酮物质1种(附图2)。将373种类黄酮组分输入Swiss Target Prediction数据库中,以Probability值≥0.9为标准进行筛选,删除重复值,共得到46个有效成分和132个成分靶点。通过cytoscape3.10.3软件创建了一个由178个节点组成的“药物-成分-靶点”网络图(附图3)。其中红色节点表示药物成分靶点,共131个;蓝色节点表示药物成分,共46个;中间黄色部分表示类黄酮。该网络图反映了药物中各种成分与相关靶点之间的相互作用关系。根据化学成分与作用靶点之间的连通性,Degree值较大的功效类黄酮组分按从高到低排序依次为:槲皮素、7,3′,4′,5′-四羟基黄酮、木犀草素、白杨黄素、5,7,3′,4′,5′-五羟基黄酮、山奈酚。
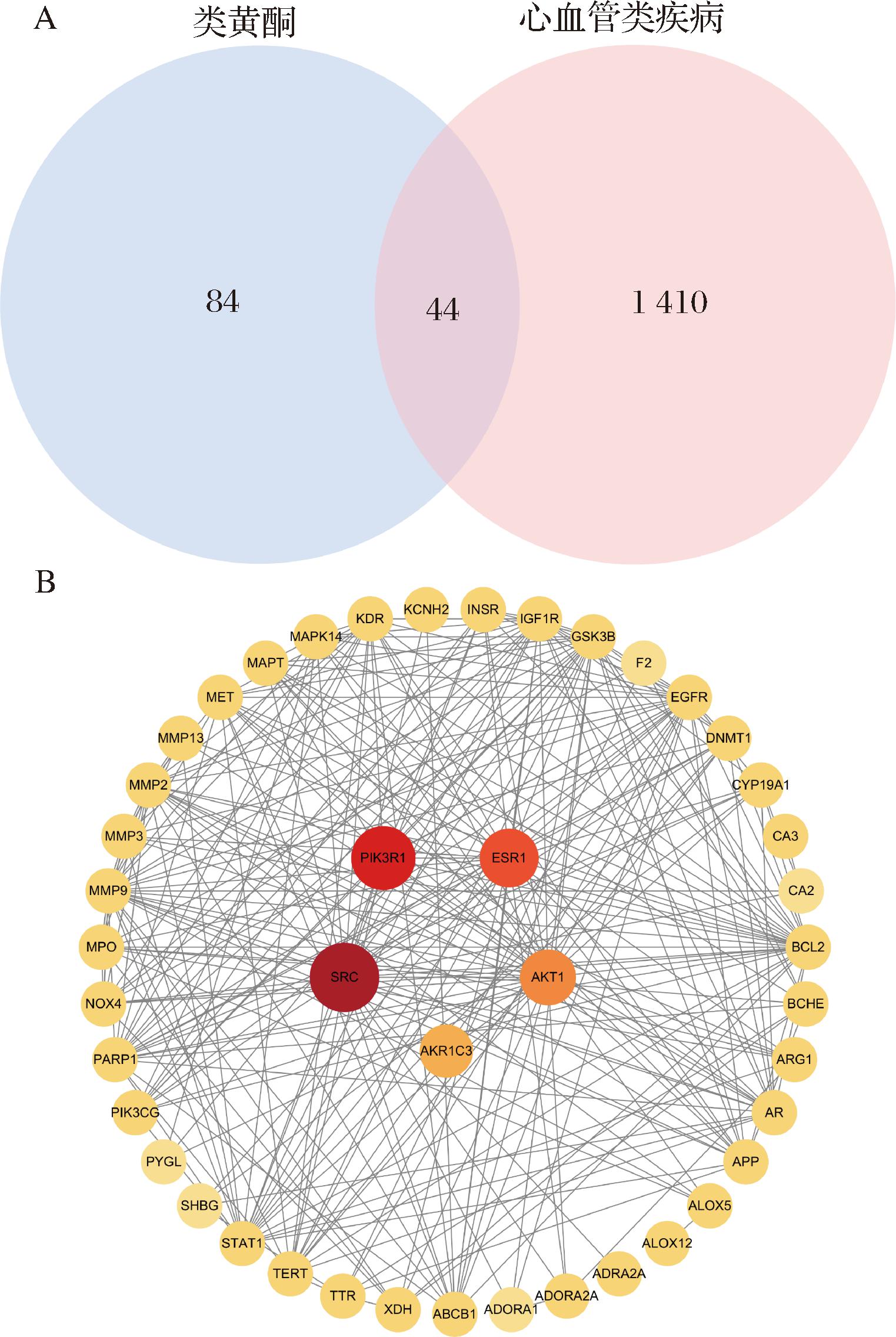
A-成分靶点与疾病靶点交集Venn图;B-交集靶点PPI网络图
图2 成分靶点与疾病靶点交集Venn图、交集靶点PPI网络图
Fig.2 Venn diagram of intersection of component targets and disease targets and intersection targets PPI network diagram
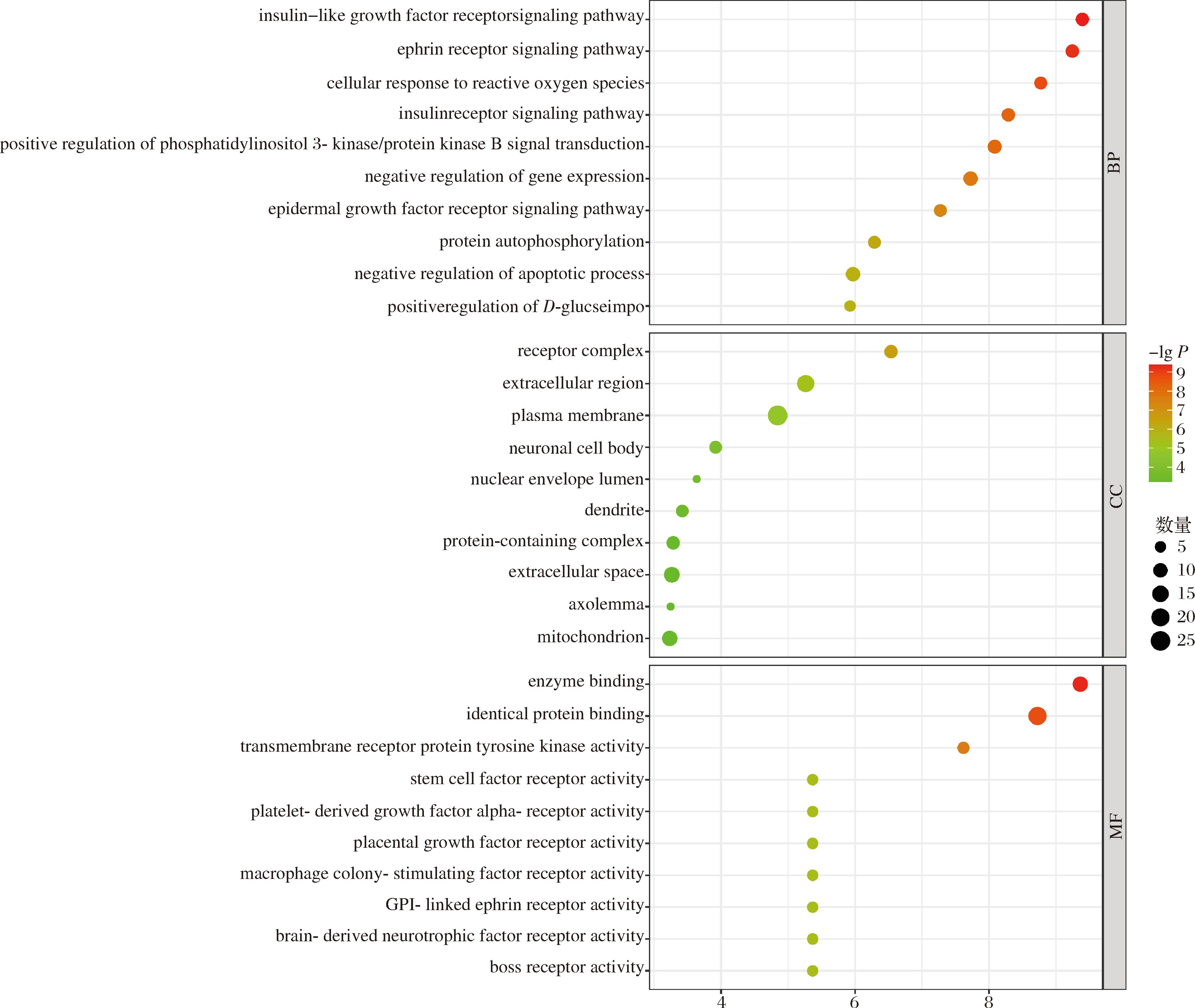
图3 类黄酮组分关键作用靶点GO功能富集
Fig.3 Functional enrichment of GO at the key targets of flavonoid component
2.3 心血管疾病相关靶点预测及PPI网络构建
通过GeneCards数据库筛选疾病的相关靶点,剔除重复后共收集到1 453个心血管类疾病靶点。利用Venn工具筛选出油茶果相关靶点与心血管类疾病靶点之间的44个共同靶点,作为油茶果类黄酮组分干预心血管疾病作用的潜在靶点(图2-A)。利用STRING数据库,采用44个潜在靶点构建PPI网络,如图2-B所示。该PPI网络包含44个节点和276条边,平均连通度为3.833。基于化学成分与作用靶点之间的连通性,排名前5的基因被认为是参与油茶果干预心血管类疾病的枢纽基因,分别为SRC、PIK3R1、ESR1、AKT1和AKR1C3。
2.4 GO和KEGG富集分析
通过GO功能富集分析对44个交集靶点进行系统研究,以揭示类黄酮化合物在心血管疾病中的潜在作用机制。结果显示,得到的GO功能富集条目359条。其中,BP显著富集237个条目,主要涉及胰岛素样生长因子受体信号通路、肝配蛋白受体信号通路调控、活性氧应激响应机制及胰岛素受体信号转导等;CC共获得40个显著条目,主要分布于受体复合体、细胞外基质、质膜结构域及神经元胞体等;MF显著富集82个条目,主要涉及酶结合活性、同源蛋白互作能力、跨膜受体酪氨酸激酶活性及GPI锚定肝配蛋白受体功能等(图3)。得到KEGG通路21条,关键通路包括AP-1信号转导通路、动脉粥样硬化脂质代谢通路、MAPK级联反应通路、PI3K-Akt生存信号通路、催乳素信号网络及ErbB受体信号系统等。这些结果提示类黄酮化合物可能通过多靶点协同作用调控心血管类疾病的发生发展。基于微生信平台构建了桑基气泡图(图4)。
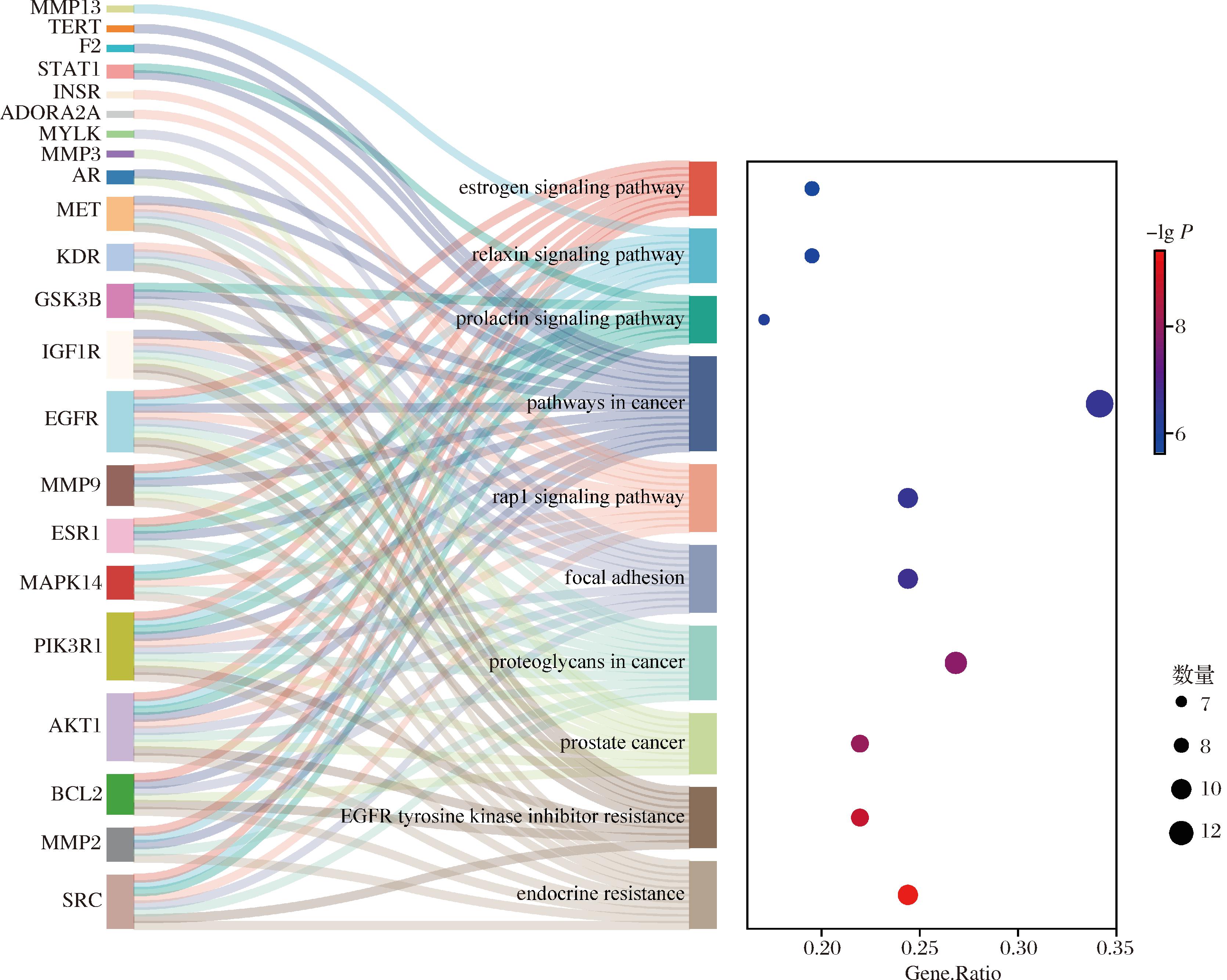
图4 类黄酮组分关键作用靶点KEGG桑基气泡图
Fig.4 KEGG bubble diagram of key targets of flavonoid component
2.5 分子对接与分子动力学模拟
选取核心靶点ESR1、SRC、PIK3R1、AKT1、AKR1C3与槲皮素、7,3′,4′,5′-四羟基黄酮、木犀草素、白杨黄素、5,7,3′,4′,5′-五羟基黄酮、山奈酚进行分子对接(图5)。结果显示,核心成分与核心靶点蛋白均有良好的结合作用(结合能<-5 kcal/mol),其中槲皮素与AKR1C3、木犀草素与PIK3R1的结合自由能均低于-7.0 kcal/mol,表明两者之间存在较强的结合亲和力和特异性相互作用(图5),提示槲皮素和木犀草素可能是油茶果类黄酮组分发挥抗心血管疾病的关键组分。进一步通过分子动力学模拟分析,结果显示槲皮素与AKR1C3复合物的RMSD和Rg值波动范围较小(RMSD<0.2 nm,Rg变化幅度<5%),表明复合物的形成未引起受体蛋白构象的显著改变,体系整体稳定性较高。相比之下,木犀草素与PIK3R1、7,3′,4′,5′-四羟基黄酮与PIK3R1复合物的RMSD和Rg值波动较大(RMSD>0.3 nm,Rg变化幅度>10%),提示这些活性成分的结合可能诱导靶蛋白发生显著的构象重排,进而影响其生物学功能(附图4)。综上,油茶果中槲皮素与靶点蛋白结合能力较强且复合物较为稳定,将通过后续的细胞实验进一步评估其降血脂活性,考察其作为抗心血管疾病的关键类黄酮组分的应用潜力。
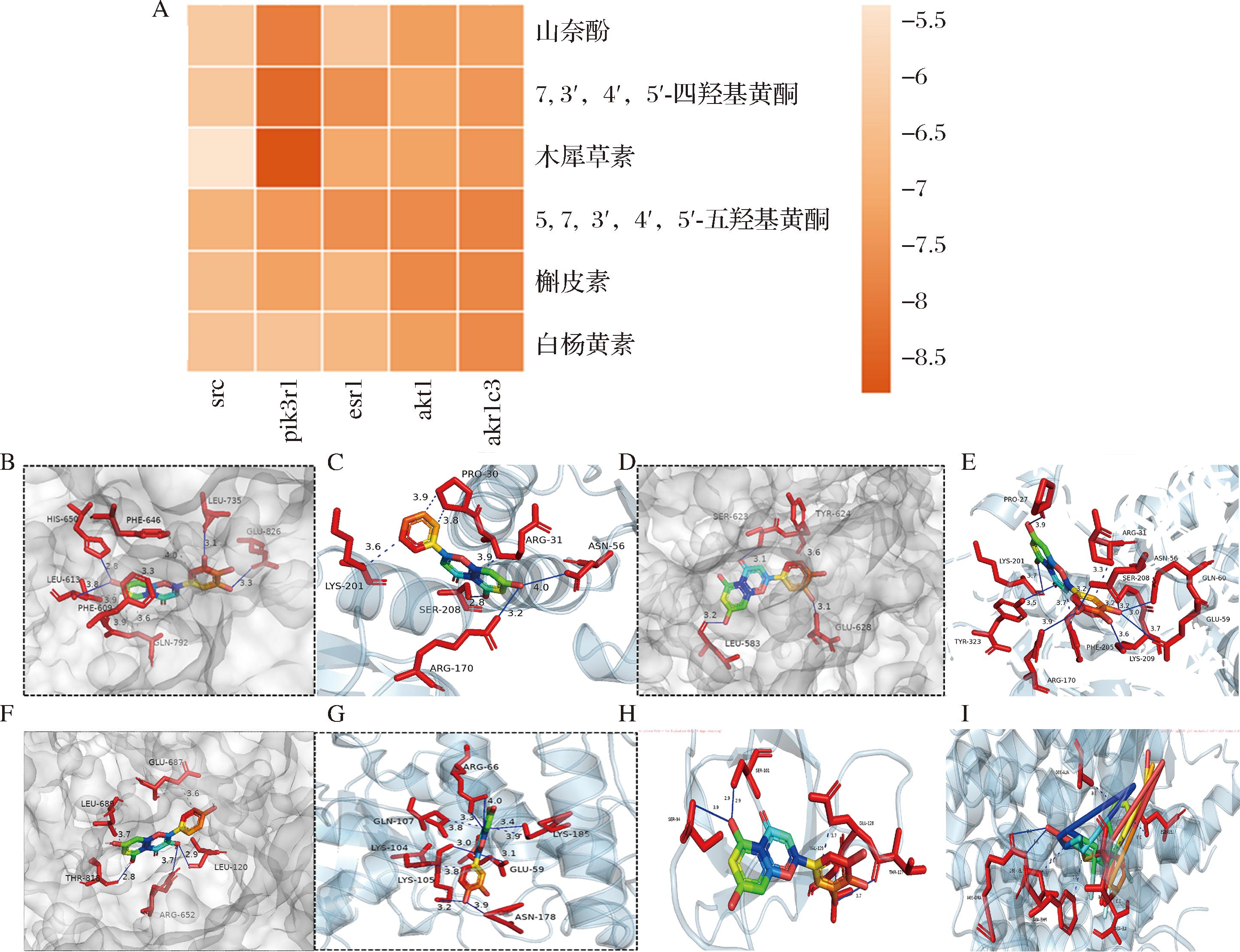
A-展示对接结合能的热图;B~I-核心成分的分子对接 (B:7,3′,4′,5′-四羟基黄酮-PIK3R1;C-白杨黄素-AKR1C3;D-木犀草素-PIK3R1;E-5,7,3′,4′,5′-五羟基黄酮-AKR1C3;F-山奈酚-PIK3R1;G-槲皮素-AKR1C3;H:5,7,3′,4′,5′-五羟基黄酮-SRC;I:7,3′,4′,5′-四羟基黄酮-ESR1
图5 主要成分与核心靶点的分子对接分析
Fig.5 Molecular docking analysis of key compounds binding to key targets
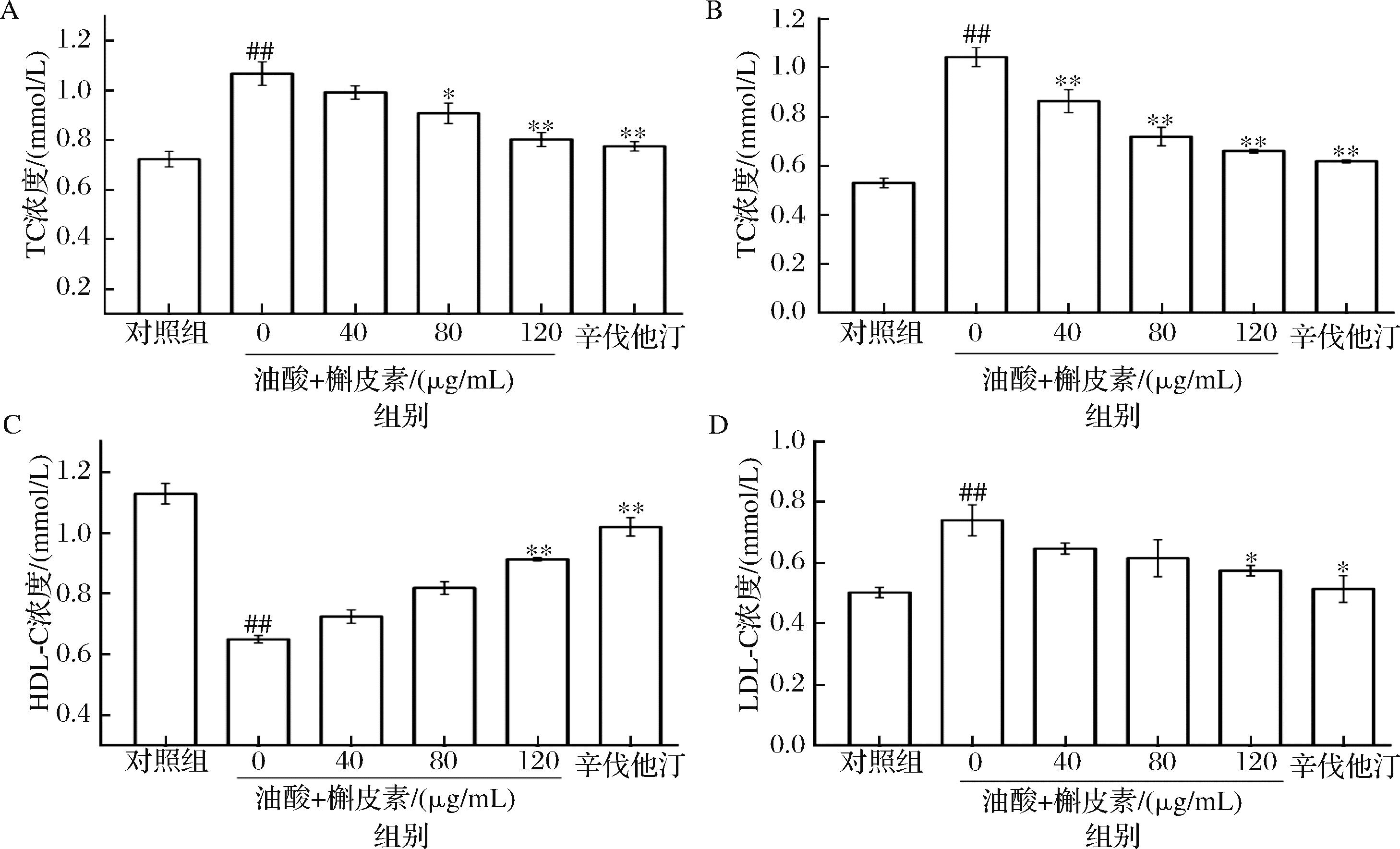
A-TC;B-TG;C-HDL-C;D-LDL-C
图6 类黄酮核心组分槲皮素对HepG2细胞中TC、TG、HDL-C和LDL-C水平的影响
Fig.6 The effect of total flavonoid extract from COF on the levels of TC,TG,HDL-C,and LDL-C in HepG2 cells
注:与对照组相比,## P<0.01;与模型组相比,*P<0.05,**P<0.01(下同)。
2.6 扩展基因及功能富集
基于GeneMANIA数据库去重后,得到91个扩展基因,并对其进行GO和KEGG富集分析。BP结果显示,类黄酮干预心血管类疾病的关键过程包括胰岛素受体信号通路、柔红霉素代谢过程、细胞凋亡过程的负调控、胰岛素样生长因子受体信号传导等。CC中类黄酮干预心血管类疾病,主要涉及细胞质、核质、RNA聚合酶Ⅰ复合物、RNA聚合酶Ⅲ复合物等组分。此外,MF与类黄酮组分蛋白受体的信号传导密切相关,如醛糖还原酶(NADPH)活性、RNA聚合酶Ⅱ活性、蛋白酪氨酸激酶活性、SH2结构域结合等(附图5)。KEGG结果显示扩展基因多富集于ErbB、PI3K-Akt等信号通路(附图5)。以上验证了2.3节结果分析的可靠性,进一步强调了PI3K-Akt信号通路对于类黄酮干预心血管类疾病的重要性。
2.7 预测的核心类黄酮组分降血脂活性评价
综合考量网络药理学分析、分子对接及分子动力学模拟实验结果,选取油茶果抗心血管疾病的关键类黄酮组分槲皮素进行细胞实验。高油酸诱导的高脂HepG2细胞模型广泛用于高脂血症和肝脂肪变性的体外研究。
与对照组相比,油酸刺激显著升高了实验组细胞的TC、TG和LDL-C水平(P<0.001),并显著降低了HDL-C水平(P<0.001)。与模型组相比,槲皮素处理组显著减少了细胞内胆固醇的积累,且呈现出一定的剂量依赖性(图6-A)。此外,在降低甘油三酯方面,槲皮素高浓度组也比低浓度组表现更优(图6-B)。与此同时,120 μg/mL槲皮素处理组的HDL-C水平显著高于模型组(P<0.001)(图6-C),且其LDL-C水平也呈现显著差异(P<0.05)(图6-D)。核心类黄酮组分槲皮素在降低脂质积累方面效果显著,作为一种抗心血管类疾病潜力较大的类黄酮物质,在生物医药和功能性食品领域具有较好的应用前景。
2.8 核心基因的表达差异分析和初步验证
为了验证网络药理学分析筛选出的前5名核心靶点在心血管类疾病患者和正常人的表达情况(图7),通过对GEO数据库中心血管类疾病患者的基因表达谱的数据集(GSE5406)进行分析发现,与健康人群相比,ESR1和SRC在患者中显著上调,其余核心靶点则无明显差异。提示这些差异基因的表达可能与油茶果核心类黄酮组分发挥治疗心血管类疾病作用密切相关。为了进一步验证GEO数据库中筛选出的具有统计学差异的核心靶点,通过RT-PCR验证上述筛选靶点的mRNA表达情况。与对照组相比,HepG2细胞经过油酸刺激后ESR1和SRC的mRNA 水平明显升高,使用槲皮素处理后能显著逆转ESR1和SRC表达的上调,提示槲皮素可能通过ESR1和SRC 2个核心靶点来发挥治疗心血管类疾病的作用。
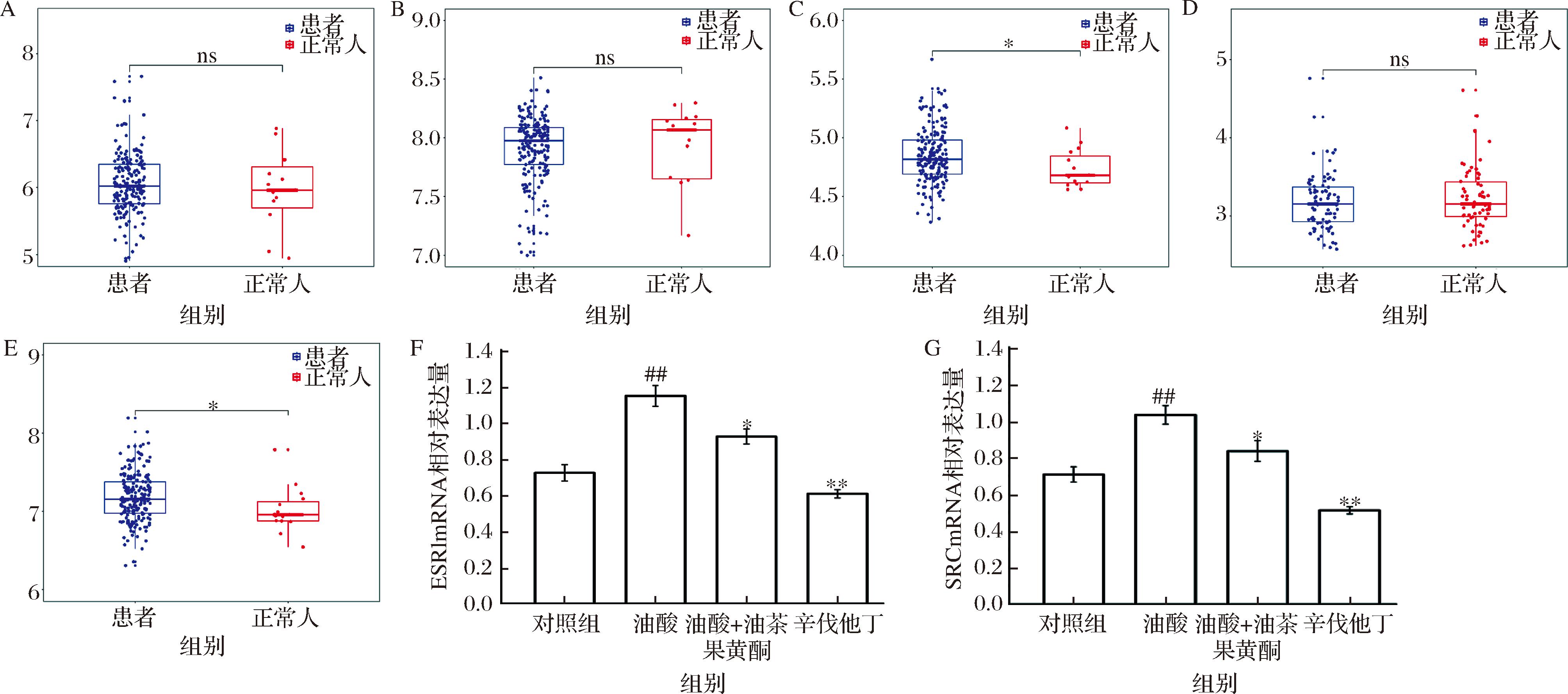
A-AKR1C3;B-AKT1;C-ESR1;D-PIK3R1;E-SRC;F-ESR1;G-SRC
图7 GSE5406数据集中正常和心血管类疾病患者核心靶点基因的mRNA表达及通过RT-PCR检测的不同组细胞中核心靶点基因的相对mRNA表达水平
Fig.7 The mRNA expression of core target genes in normal individuals and patients with cardiovascular diseases in the GSE5406 dataset and the relative mRNA expression levels of the core target genes in different groups of cells detected by RT-PCR
2.9 安全性评估
ADMET3.0和Pro Tox3.0的预测结果(图8)显示,槲皮素、7,3′,4′,5′-四羟基黄酮和木犀草素均不会引起肾毒性以及神经毒性,但可能引起轻微的肝毒性,其毒性程度在可控范围内,进一步验证了预测的类黄酮关键成分的安全性。
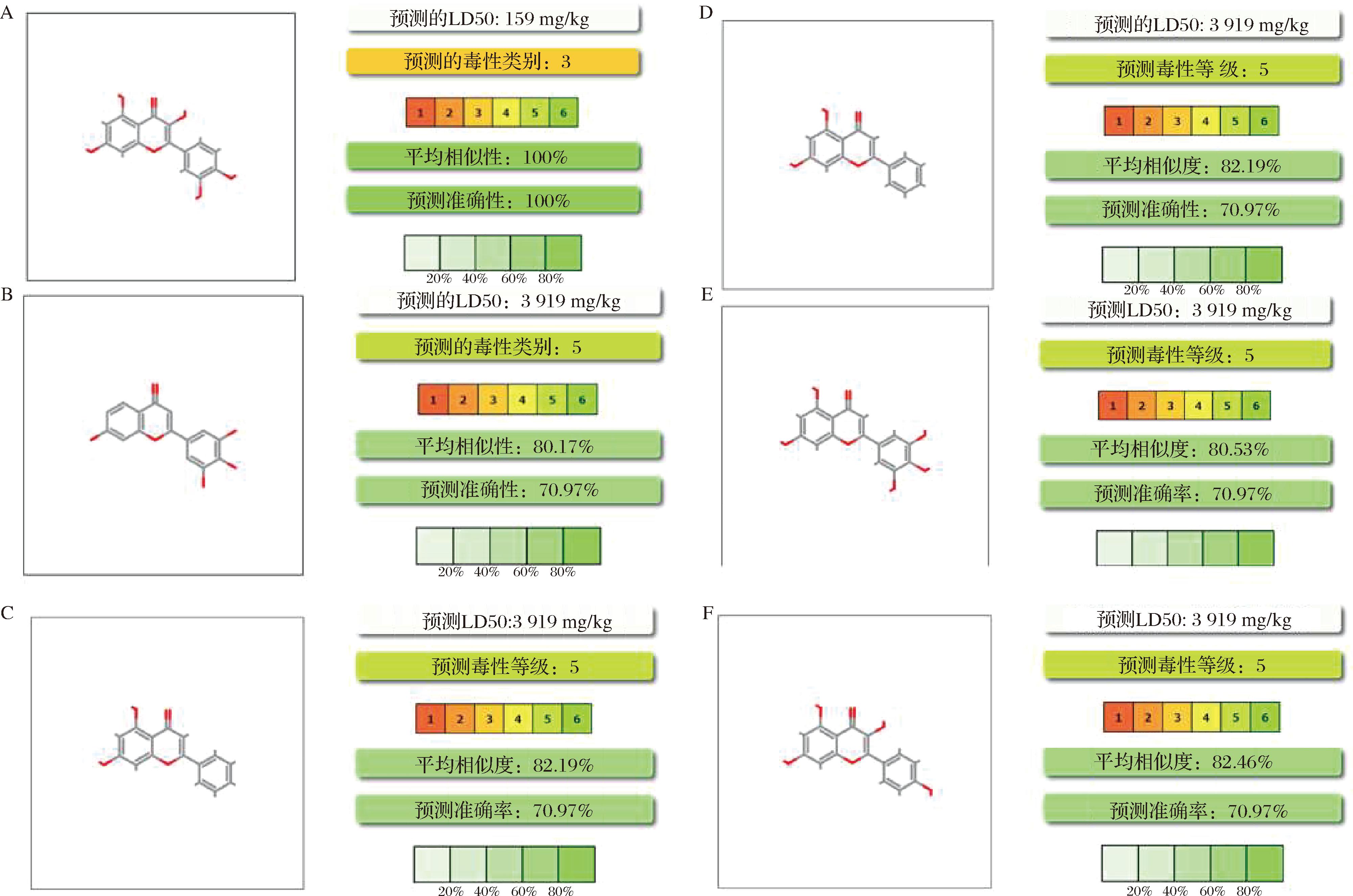
A-槲皮素;B-7,3′,4′,5′-四羟基黄酮;C-木犀草素;D-白杨黄素;E-5,7,3′,4′,5′-五羟基黄酮;F-山柰酚
图8 毒性等级评估
Fig.8 Toxicity level assessment
3 讨论和结论
全球心血管疾病负担持续上升,预计2050年心血管死亡人数将达到3 560万[14]。目前,临床用于治疗心血管疾病的药物主要有他汀类药物、β-受体阻滞剂、ACE抑制剂/AIIRAs、抗血小板药物等[15],副作用和治疗依从性有限等问题影响了药物治疗的效果。天然植物提取物如油茶果中类黄酮化合物的抗氧化、抗癌、抗肿瘤、保护心脏等多种活性,有望成为干预心血管类疾病的手段[16]。临床研究表明,HDL-C水平的高低可独立预测动脉粥样硬化的风险[17],降低LDL-C浓度能够降低心血管疾病的发病率和死亡率[18]。本研究表明,油茶果中主要抗心血管疾病的核心黄酮组分有6种,其中槲皮素、木犀草素已被证实对心血管类疾病有治疗作用。槲皮素具有抗氧化、抗炎和降低血脂等作用,可以降低动脉粥样硬化大鼠体内丙二醛的含量,减少细胞的脂质成分受到的氧化损伤[19],对动脉粥样硬化患者干预治疗研究中发现,补充槲皮素后,患者血液中的炎症标志物水平有所下降[20],提示槲皮素在心血管类疾病发生发展中起重要的调节作用。本研究的细胞实验也表明,槲皮素能显著地调节高脂HepG2细胞的LDL-C和HDL-C水平,对心血管疾病表现出较好的治疗潜力。此外,补充木犀草素可以显著降低血压并改善血管内皮功能[21],还可以调节免疫细胞的功能,增强机体的抗炎能力[22]。
血管内皮细胞内SRC活性在高血压、动脉粥样硬化这类常见心血管疾病的发生中频繁异常升高,致使内皮型一氧化氮合酶磷酸化位点改变,酶活性降低,NO合成随之减少,最终引发血管舒张功能障碍[23]。本研究发现,油茶果类黄酮能够显著减少油酸诱导HepG2细胞的脂质积累,与心血管疾病患者的基因表达结果一致,即病患体内SRC表达异常升高。油茶果核心类黄酮组分槲皮素处理HepG2细胞后,显著降低了SRC表达的上调,提示SRC对于未来心血管疾病的新药开发具有重要的意义。还有研究发现,ESR1与心血管类疾病的发生和发展密切相关,全基因组关联研究发现,特定ESR1基因位点与心血管疾病易感性紧密相连,携带相关等位基因者发病概率更高[24]。核心基因表达分析结果显示,心血管疾病患者体内ESR1的表达明显高于正常人,而相对于模型组,槲皮素干预组的ESR1基因表达水平显著降低,为心血管疾病治疗提供了新视角。
此外,有研究表明,在动脉粥样硬化斑块的发展过程中,AP1信号通路可以调节细胞外基质(extracellular matrix,ECM)的合成[25]。此外,MAPK信号通路在血管新生过程中发挥关键作用。在心肌梗死发生后,梗死心肌周围区域会启动血管新生的过程以改善心肌血供[26]。另一项研究发现,在新生小鼠心脏损伤模型中,通过激活 PI3K-Akt信号通路,可以刺激心肌细胞重新进入细胞周期并增殖,这对于心脏再生和修复受损心脏组织具有潜在的应用价值[27]。催乳素可以降低血管平滑肌细胞内的钙离子浓度,使平滑肌细胞舒张,这有助于降低血管紧张度,对高血压等心血管疾病的治疗有潜在意义[28]。本研究中的KEGG通路富集分析显示,类黄酮与心血管类疾病主要靶向AP1信号通路、脂质与动脉粥样硬化、MAPK信号通路、PI3K-Akt信号通路、催乳素信号通路、ErbB信号通路等信号通路,进一步表明以上信号通路在心血管类疾病的发生发展中发挥重要作用,为利用类黄酮治疗心血管疾病提供了理论基础。
4 结论
本研究结合网络药理学、分子对接和分子动力学模拟技术,构建了“类黄酮-活性成分-靶点”网络和PPI网络,以确定油茶果类黄酮的核心活性成分和作用靶点,并探讨其治疗心血管类疾病的潜在作用机制。初步研究表明,油茶果类黄酮在抗心血管类疾病机制可能是通过PI3K-Akt等信号通路实现,通过评估枢纽基因表达水平,探讨了核心靶点与疾病的关联性,ADMET3.0和Pro Tox3.0分析显示核心类黄酮组分槲皮素、7,3′,4′,5′-四羟基黄酮和木犀草素均无肾毒性和神经毒性,为油茶果类黄酮的安全应用提供了依据。在后续研究中,课题组将继续围绕核心类黄酮组分槲皮素,结合动物实验及临床实验,系统验证油茶果功效类黄酮组分抗心血管疾病的药用价值及作用机制。此外,课题组还将基于代谢组学结合网络药理学鉴定的油茶果活性成分,开展系统的遗传育种研究,为开发药用价值种质资源提供了新的思路。
[1] YE H L,CHEN Z G,JIA T T,et al.Response of different organic mulch treatments on yield and quality of Camellia oleifera[J].Agricultural Water Management,2021,245:106654.
[2] VIEIRA E F,PINHO O,FERREIRA I M P L V O,et al.Chayote (Sechium edule):A review of nutritional composition,bioactivities and potential applications[J].Food Chemistry,2019,275:557-568.
[3] XIN T,HUANG W J,DE RIEK J,et al.Genetic diversity,population structure,and traditional culture of Camellia reticulata[J].Ecology and Evolution,2017,7(21):8915-8926.
[4] WANG T Y,LIU J J,LUO X L,et al.Functional metabolomics innovates therapeutic discovery of traditional Chinese medicine derived functional compounds[J].Pharmacology &Therapeutics,2021,224:107824.
[5] YE Z C,YU J,YAN W P,et al.Integrative iTRAQ-based proteomic and transcriptomic analysis reveals the accumulation patterns of key metabolites associated with oil quality during seed ripening of Camellia oleifera[J].Horticulture Research,2021,8(1):157.
[6] CALIS Z,MOGULKOC R,BALTACI A K.The roles of flavonols/flavonoids in neurodegeneration and neuroinflammation[J].Mini-Reviews in Medicinal Chemistry,2020,20(15):1475-1488.
[7] 张军军,白育庭,邵开元,等.网络药理学的应用研究与发展[J].比较化学,2019,3(2):11-15.ZHANG J J,BAI Y T,SHAO K Y,et al.Application research and development of network pharmacology[J].Journal of Comparative Chemistry,2019,3(2):11-15.
[8] 胡媛,吴蓓,易达,等.基于广泛靶向代谢组学技术与高通量测序技术探究广陈皮陈化机制[J].天然产物研究与开发,2022,34(4):553-562.HU Y,WU B,YI D,et al.Integration of high throughput sequencing and widely targeted metabolomics reveals the aging mechanism of Pericarpium Citri Reticulatae ‘Chachiensis’[J].Natural Product Research and Development,2022,34(4):553-562.
[9] 游美红.油茶资源现状及其多元利用模式探索:以江西省宜春市袁州区为例[J].安徽农业科学,2024,52(14):76-79.YOU M H.Current status of Camellia oleifera resources and exploration of diversified utilization model:Taking Yuanzhou district,Yichun city,Jiangxi province as an example[J].Journal of Anhui Agricultural Sciences,2024,52(14):76-79.
[10] 柯城.茶油主要营养物质组成和保健功能[J].现代食品,2019,25(13):105-108.KE C.Main nutrient composition and health function of tea oil[J].Modern Food,2019,25(13):105-108.
[11] GUO L N,GUO Y T,WU P,et al.Camellia oil lowering blood pressure in spontaneously hypertension rats[J].Journal of Functional Foods,2020,70:103915.
[12] LEI X H,LIU Q,CAO Z Y,et al.Camellia oil (Camellia oleifera Abel.) attenuates CCl4-induced liver fibrosis via suppressing hepatocyte apoptosis in mice[J].Food &Function,2020,11(5):4582-4590.
[13] ZHANG T,QIU F C,CHEN L,et al.Identification and in vitro anti-inflammatory activity of different forms of phenolic compounds in Camellia oleifera oil[J].Food Chemistry,2021,344(49):128660.
[14] CHONG B,JAYABASKARAN J,KUEH M T W,et al.The global burden of cardiovascular diseases over the next 30 years:Predictions from the past 30 years[J].Journal of the American College of Cardiology,2024,83(13):1996.
[15] 孙运奇,黄志强,庞志勇,等.牡丹籽粕总黄酮提取工艺优化及降血脂功能研究[J].中国食品添加剂,2023,34(12):59-67.SUN Y Q,HUANG Z Q,PANG Z Y,et al.Optimization of extraction technology of total flavonoids from peony seed meal and its hypolipidemic function[J].China Food Additives,2023,34(12):59-67.
[16] XU H,YU S L,LIN C X,et al.Roles of flavonoids in ischemic heart disease:Cardioprotective effects and mechanisms against myocardial ischemia and reperfusion injury[J].Phytomedicine,2024,126:155409.
[17] CASULA M,COLPANI O,XIE S N,et al.HDL in atherosclerotic cardiovascular disease:In search of a role[J].Cells.2021,10(8):1869.
[18] ESTEBAN-SAL N M,GUIM
N M,GUIM N-BARDESI A,DE LA VIUDA-UNZUETA J M,et al.Analytical and clinical evaluation of two homogeneous assays for LDL-cholesterol in hyperlipidemic patients[J].Clinical Chemistry,2000,46(8):1121-1131.
N-BARDESI A,DE LA VIUDA-UNZUETA J M,et al.Analytical and clinical evaluation of two homogeneous assays for LDL-cholesterol in hyperlipidemic patients[J].Clinical Chemistry,2000,46(8):1121-1131.
[19] 张才科,白静,余慧,等.槲皮素体外抗氧化及对小鼠血脂代谢作用的研究[J].天然产物研究与开发,2012,24(5):663-667.ZHANG C K,BAI J,YU H,et al.Effect of quercetin on serum lipid metabolism of mice and its antioxidant activity in vitro[J].Natural Product Research and Development,2012,24(5):663-667.
[20] 向露,杨丽娜,肖琳.槲皮素改善动脉粥样硬化作用机制研究进展[J].中国药理学通报,2024,40(6):1007-1013.XIANG L,YANG L N,XIAO L.Research progress on anti-atherosclerotic effect of quercetin[J].Chinese Pharmacological Bulletin,2024,40(6):1007-1013.
[21] JI L,SU S S,XIN M Y,et al.Luteolin ameliorates hypoxia-induced pulmonary hypertension via regulating HIF-2α-Arg-NO axis and PI3K-AKT-ENOS-NO signaling pathway[J].Phytomedicine,2022,104:154329.
[22] SURAI P F,SURAI A,EARLE-PAYNE K.Silymarin and inflammation:Food for thoughts[J].Antioxidants,2024,13(1):98.
[23] KIM M P,PARK S I,KOPETZ S,et al.SRC family kinases as mediators of endothelial permeability:Effects on inflammation and metastasis[J].Cell and Tissue Research,2009,335(1):249-259.
[24] ARAGAM K G,JIANG T,GOEL A,et al.Discovery and systematic characterization of risk variants and genes for coronary artery disease in over a million participants[J].Nature Genetics,2022,54(12):1803-1815.
[25] MEIJER C A,LE HAEN P A A,VAN DIJK R A,et al.Activator protein-1 (AP-1) signalling in human atherosclerosis:Results of a systematic evaluation and intervention study[J].Clinical Science,2012,122(9):421-428.
[26] LODDENKEMPER R,SCHABERG T.Robert Koch und sein Kampf Gegen die tuberkulose[J].Pneumologie,2010,64(5):311-315.
[27] 唐莹,刘金东.PI3K-Akt信号通路与心肌保护[J].医学综述,2009,15(10):1470-1473.TANG Y,LIU J D.PI3K-Akt signaling pathway and myocardial protection[J].Medical Recapitulate,2009,15(10):1470-1473.
[28] 黄浪浪.基于数据挖掘的刘中勇教授治疗原发性高血压经验研究[D].南昌:江西中医药大学,2019.HUANG L L.Professor Liu Zhongyong’s experience in treating essential hypertension based on data mining[D].Nanchang:Jiangxi University of Chinese Medicine,2019.