油桃因其口味独特、色泽鲜艳、营养成分丰富而受到人们的喜爱。作为桃属中的佼佼者,油桃不仅满足了人们对健康饮食的需求,也推动了相关产业链的蓬勃发展,展现了极高的经济价值。然而,油桃在采收后的保鲜难题一直是影响其产业持续发展的关键。特别是在冷藏条件下,油桃易受冷害影响,表现为果实硬度下降、色泽变暗、风味丧失及腐烂加剧等,这些现象不仅严重影响了油桃的商品价值,而且增加了贮藏和运输的成本[1]。因此,探索有效的保鲜技术,以减轻油桃冷害,延长其保鲜期和货架期,成为当前油桃产业急待解决的重要课题。
茉莉酸甲酯(methyl jasmonate,MeJA),作为一种天然的植物生长调节剂,近年来在水果保鲜领域展现出广阔的应用前景[2]。已有研究表明,MeJA能够显著增强果实抵御冷害的能力。如GLOWACZ等[3]的研究表明,MeJA可通过改变脂肪酸含量与组成,降低脂氧合酶(lipoxygenase,LOX)基因表达量并削弱LOX活性,最终增强梨的抗冷性。杨文慧[4]研究发现MeJA可提升香蕉果实抗氧化酶活性,增强果实清除活性氧的能力,减轻细胞膜损伤,缓解冷害。然而,在油桃保鲜中的具体应用及其与冷害的关系仍需深入研究。
乙烯吸收剂(ethylene absorbent,EA),能够去除果实所释放出的乙烯,进而对果实的成熟以及衰老进程起到延缓作用。乙烯为植物体内重要的气态信号分子,在果实成熟和衰老的过程中扮演着至关重要的角色。已有研究表明,EA在蓝莓[5]、葡萄[6]、猕猴桃[7]保鲜中均表现出显著效果。但其在油桃保鲜中的应用及其与MeJA的协同作用尚未得到充分研究。
课题组前期研究发现MeJA与EA复合处理可延缓桃果冷害的发生(未发表),为进一步明确MeJA与EA复合处理对桃果冷害的调节机制。本研究以‘曙光’油桃为试材,通过对贮藏期油桃品质、生理以及苯丙烷代谢相关指标进行测定,旨在探索一种安全、高效的油桃采后保鲜方法,从而有助于延长油桃的保鲜期和货架期,提高商品价值,还能为其他易冷害水果的保鲜提供借鉴和参考。
1 材料与方法
1.1 材料与试剂
‘曙光’油桃,采自运城市平陆县,于采收当日将油桃果实转运至实验室进行分拣。标准为果实色泽均匀、个体大小相仿,成熟度一致,且外观无病虫害侵蚀与机械损伤痕迹。
实验用聚乙烯(polyethylene,PE)保鲜袋和EA均由山西省农业科学院农产品贮藏保鲜研究所提供,EA每袋10 g,KMnO4纯度10%。
茉莉酸甲酯、无水醋酸钠、愈创木酚、邻苯二酚、聚乙二醇6000(分析纯),美国Sigma公司;冰醋酸、浓盐酸、硼酸、甲醇、L-苯丙氨酸、石英砂(分析纯),天津市清华津英有限公司;丙酮、乙醇、磷酸氢二钠、磷酸二氢钠(分析纯),上海阿拉丁股份有限公司。
1.2 仪器与设备
TA-XT plus质构仪,上海仪电科学仪器股份有限公司;F-900便携式呼吸测定仪,美国贝克曼库尔特有限公司;GC-14A型气相色谱仪,日本岛津公司;PAL-1手持测定仪、SP-2500紫外分光光度计,上海优尼克仪器有限公司;HC-2518R冷冻离心机,德国SIGMA公司。
1.3 实验方法
1.3.1 采后处理
将油桃随机分成4组,分别为对照组(CK)、EA、MeJA、MeJA+EA处理组,每组用果30 kg,每组设定3个重复。
CK组:不做任何处理,用PE保鲜袋扎口密封放置于(0±1) ℃的低温环境中贮藏。
EA组:放入2袋乙烯吸收剂,用PE保鲜袋扎口密封放置于(0±1) ℃的低温环境中贮藏。
MeJA组:将油桃置于50 μmol/L MeJA的密闭PE帐环境中,室温熏蒸处理24 h后通风换气60 min,随后装入0.02 mm厚度的PE保鲜袋内在(0±1) ℃的低温环境中贮藏。
MeJA+EA处理组:将油桃置于50 μmol/L的茉莉酸甲酯密闭PE帐环境中,室温熏蒸处理24 h后通风换气60 min,而后将其放置于装有2袋乙烯吸收剂的PE保鲜袋中。
1.3.2 样品制备
在(0±1) ℃,湿度控制在90%~95%的低温环境中贮藏。贮藏期间,每隔7 d随机抽取3个油桃果实作为样本进行相关指标测定,具体包括桃果实的硬度、出汁率以及可溶性固形物等;同时,取适量桃果肉切碎并充分搅拌混匀,用于测定其相关酶活性。为保障实验数据的科学性与严谨性,整套实验流程设置3次生物学重复实验。
1.3.3 冷害指数的测定
根据WANG等[8]的方法。冷害指数的计算如公式(1)所示:
冷害指数![]()
(1)
1.3.4 硬度、出汁率和可溶性固形物的测定
硬度的测定:每组处理随机选择3个果实,利用TA-XT plus质构仪在果实赤道线对称位置去掉直径约为3 cm果皮的果肉上进行测定。取平均值为测定结果。单位为N。
出汁率的测定:参照刘雪平等[9]的方法测定,利用直径6 mm的打孔器具,对每一个去皮后的桃果实进行钻取,获取长约5 cm的果肉柱。随后将其置于已预先称重(m1)且内置吸水纸的离心管内,并立即记录该组合的总质量(m2)。接着,在1 500×g的条件下离心处理10 min,取出果肉后再次称重(m3)。重复3次。出汁率的计算如公式(2)所示:
出汁率![]()
(2)
可溶性固形物的测定:使用PAL-1手持测定仪测定,以%表示。
1.3.5 褐变指数和多酚氧化酶(polyphenoloxidase,PPO)活性的测定
根据WANG等[8]的方法。褐变指数的的计算如公式(3)所示:
褐变指数![]()
(3)
PPO活性参照曹建康等[10]的方法测定,在470 nm处测定吸光值。单位为U/g。
1.3.6 呼吸速率和乙烯释放率的测定
每组取8个油桃,放入3 L的玻璃样品瓶中,密封保持120 min后,使用果蔬呼吸速率测定仪测定油桃的呼吸速率,呼吸释放率单位为mg/(kg·h)。每组取8个油桃,放入3 L的玻璃样品瓶中,密封保持120 min后,吸取1 mL气体,采用气相色谱仪测定油桃的乙烯释放率,乙烯释放率单位为μL/(kg·h)。
1.3.7 苯丙烷代谢相关酶活性及其代谢产物的测定
苯丙氨酸解氨酶(phenylalanine ammonia-lyase,PAL)、肉桂酸4-羟化酶(cinnamate-4-hydroxylase,C4H)、4-香豆酸辅酶A连接酶(4-coumarate coA ligase,4CL)活性的测定方法分别参照曹建康等[10]、董柏余等[11]和李冰茹等[12]的方法。依次在290、340、333 nm处测定吸光值,单位均为U/g。
总酚、类黄酮含量的测定参照曹建康等[10]的方法,依次在280、325 nm处测定吸光值,单位为mg/g。
木质素含量的测定参照董柏余等[11]方法,在280 nm处测定吸光值,单位为mg/g。
1.4 数据统计与分析
各指标均做3次重复。利用Excel 2019进行数据处理分析,计算平均值、标准差;利用Origin 2021软件作图;利用SPSS Statistics 21软件进行单因素方差分析和最小显著性差异法比较不同处理间的差异显著性。
2 结果与分析
2.1 MeJA结合EA处理对油桃果实冷害指数的影响
油桃的冷害症状表现为果体出现水渍状斑点。如图1和图2所示,在贮藏第14天时,对照组油桃果实冷害症状显现,果体表面出现水渍状斑点,处理组均未出现冷害症状,说明EA、MeJA、MeJA+EA处理均能缓解冷害。随着贮藏时间的延长,经EA和MeJA处理的油桃果实在第21天时出现冷害症状,MeJA+EA处理组未出现。贮藏49 d时,EA、MeJA、MeJA+EA处理组冷害指数分别为13.67%、11.12%、5.98%,与对照组相比(38.89%),EA、MeJA、MeJA+EA处理组分别降低了25.22%、27.77%、32.91%,冷害抑制效果显著(P<0.05),其中MeJA+EA处理组效果最佳。
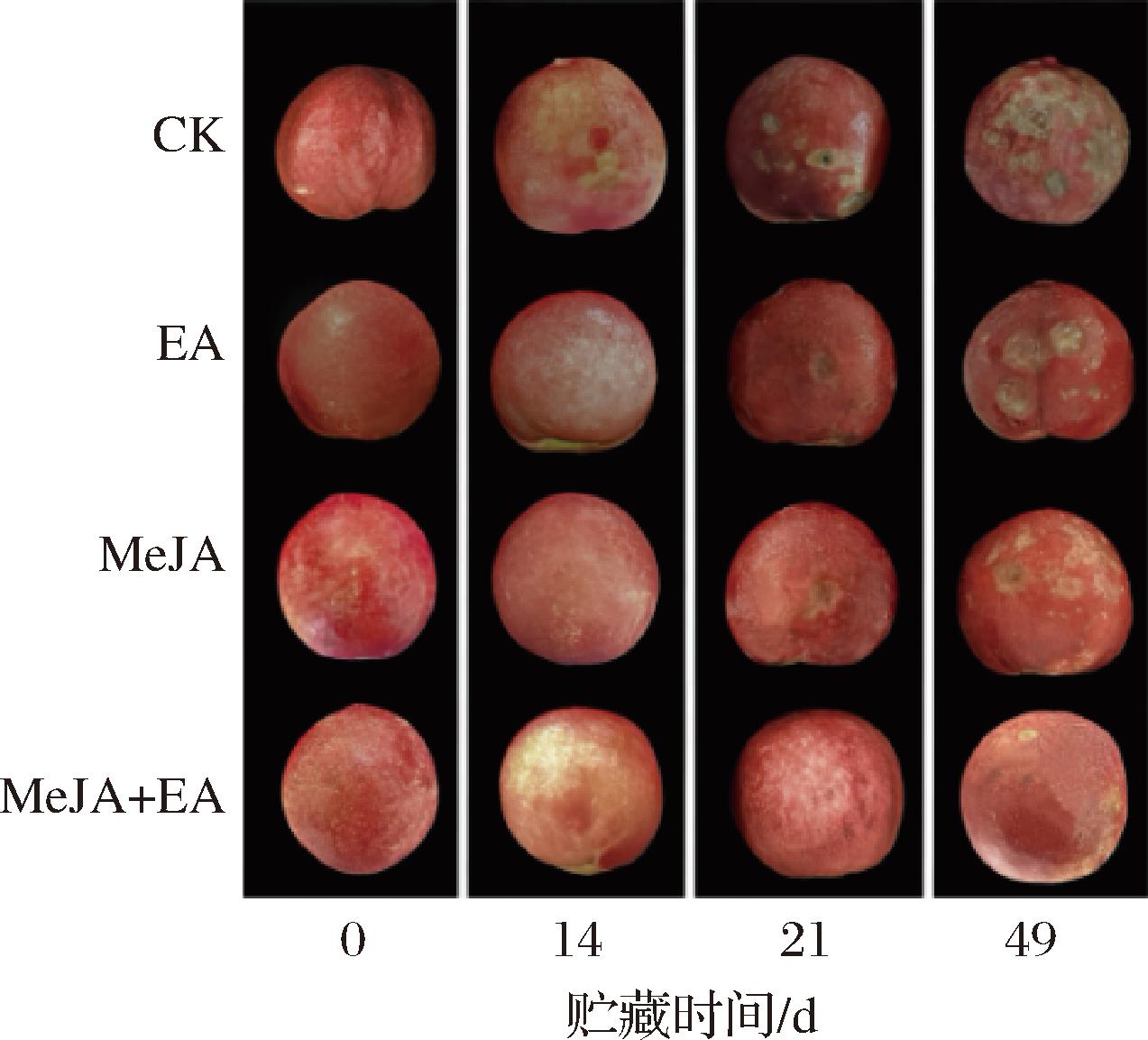
图1 EA、MeJA单独及复合处理对冷藏油桃果实外观的影响
Fig.1 Effect of EA,MeJA alone and combined treatment on the appearance of refrigerated nectarine fruit
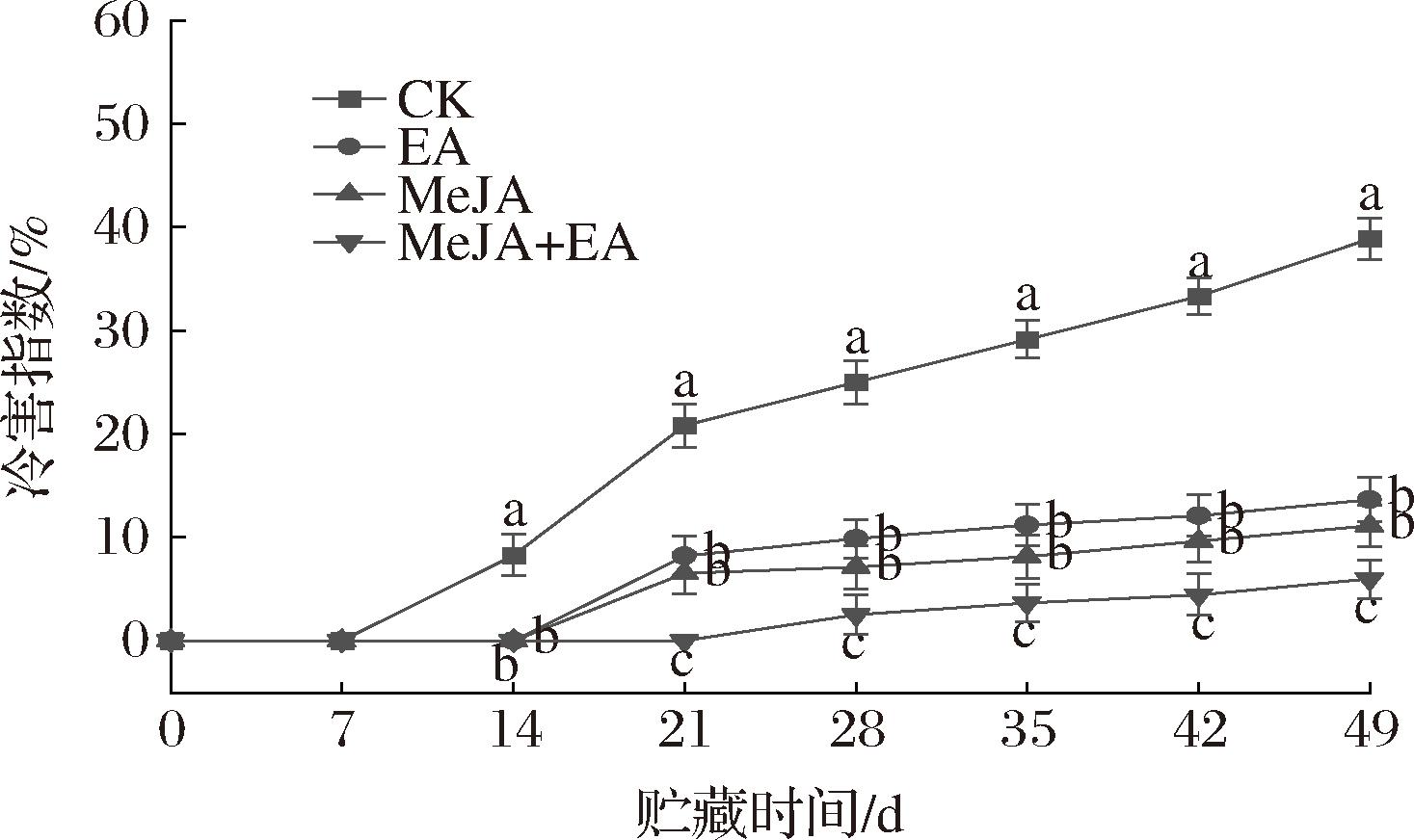
图2 EA、MeJA单独及复合处理对冷藏油桃果实冷害指数的影响
Fig.2 Effect of EA,MeJA alone and combined treatment on cold damage index of refrigerated nectarine fruit
注:不同字母表示同一时间不同处理有显著性差异(P<0.05),下同。
2.2 MeJA结合EA处理对油桃果实硬度、出汁率和可溶性固形物的影响
硬度是油桃果实品质的关键指标。如图3-A所示,在整个贮藏阶段,各组处理下的油桃果实硬度均呈逐步降低态势。贮藏期内,对照组油桃果实硬度的下降速度较快。相较对照组,经处理的油桃果实硬度下降速度有所减缓。贮藏49 d后,EA、MeJA、MeJA+EA处理组的硬度分别为3.89、4.22、5.81 N,MeJA+EA复合处理优于前2种处理,其果实硬度显著(P<0.05)高于对照组。以上结果表明复合处理最能够有效延缓油桃果实硬度的下降速度。
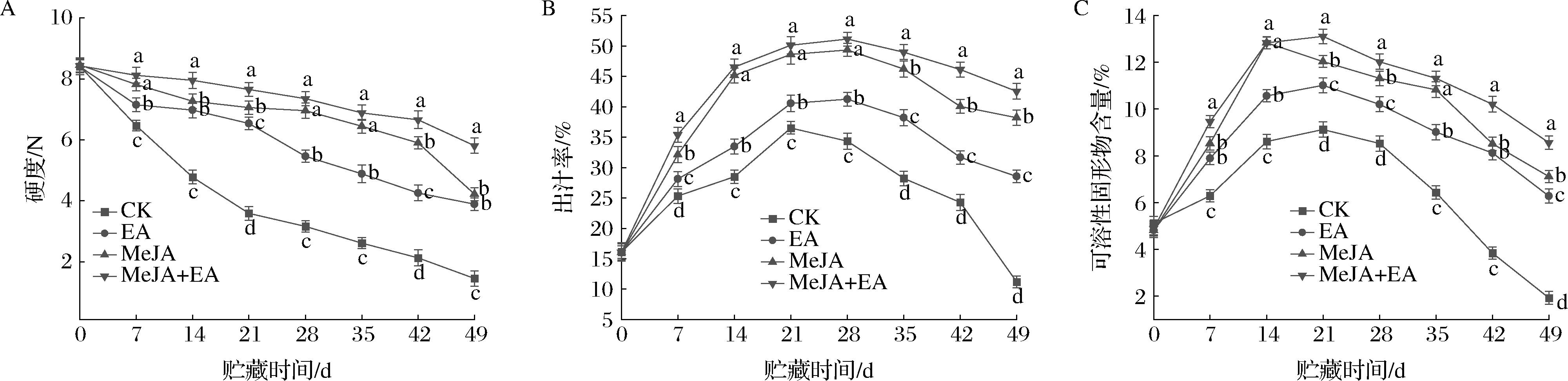
A-硬度;B-出汁率;C-可溶性固形物含量
图3 EA、MeJA单独及复合处理对冷藏油桃果实硬度、出汁率和可溶性固形物含量的影响
Fig.3 Effect of EA,MeJA alone and combined treatment on fruit hardness,juice yield,and soluble solid
出汁率可以有效反映果实内部结构以及质地的变化。如图3-B所示,对照组油桃果实在第21天时达到峰值,处理组油桃果实的出汁率高峰推迟到了第28天,至第49天时,EA、MeJA、MeJA+EA处理组出汁率分别为28.56%、38.22%、42.55%,其中MeJA+EA处理组出汁率最高。
可溶性固形物含量是评价油桃的贮藏效果的关键指标之一。如图3-C所示,CK、EA、MeJA、MeJA+EA组油桃果实的可溶性固形物含量在贮藏期均先上升后下降的趋势。49 d时,经EA、MeJA、MeJA+EA处理的油桃果实可溶性固形物含量分别为6.28%、7.11%、8.56%,其中MeJA+EA复合处理组的油桃可溶性固形物含量最高,与对照组(1.92%)相比差异显著(P<0.05)。这一结果表明,MeJA+EA复合处理能够有效维持油桃在贮藏过程中的可溶性固形物水平,进而有助于保持果实的口感。
2.3 MeJA结合EA处理对油桃果实褐变指数和PPO活性的影响
褐变是油桃果实发生冷害的典型症状。如图4和图5-A所示,在贮藏初期,CK、EA、MeJA、MeJA+EA组均未出现明显的褐变症状。但随着贮藏时间的延长,褐变程度持续增加,褐变指数呈现出不断上升的变化趋势。进入贮藏后期,对照组的褐变程度急剧加剧,至第49天时褐变指数已达到83.33%。第49天时,EA、MeJA、MeJA+EA处理组油桃果实褐变指数分别为62.5%、54.17%、20.83%,相比对照组差异显著(P<0.05),其中MeJA+EA处理组褐变指数最低。
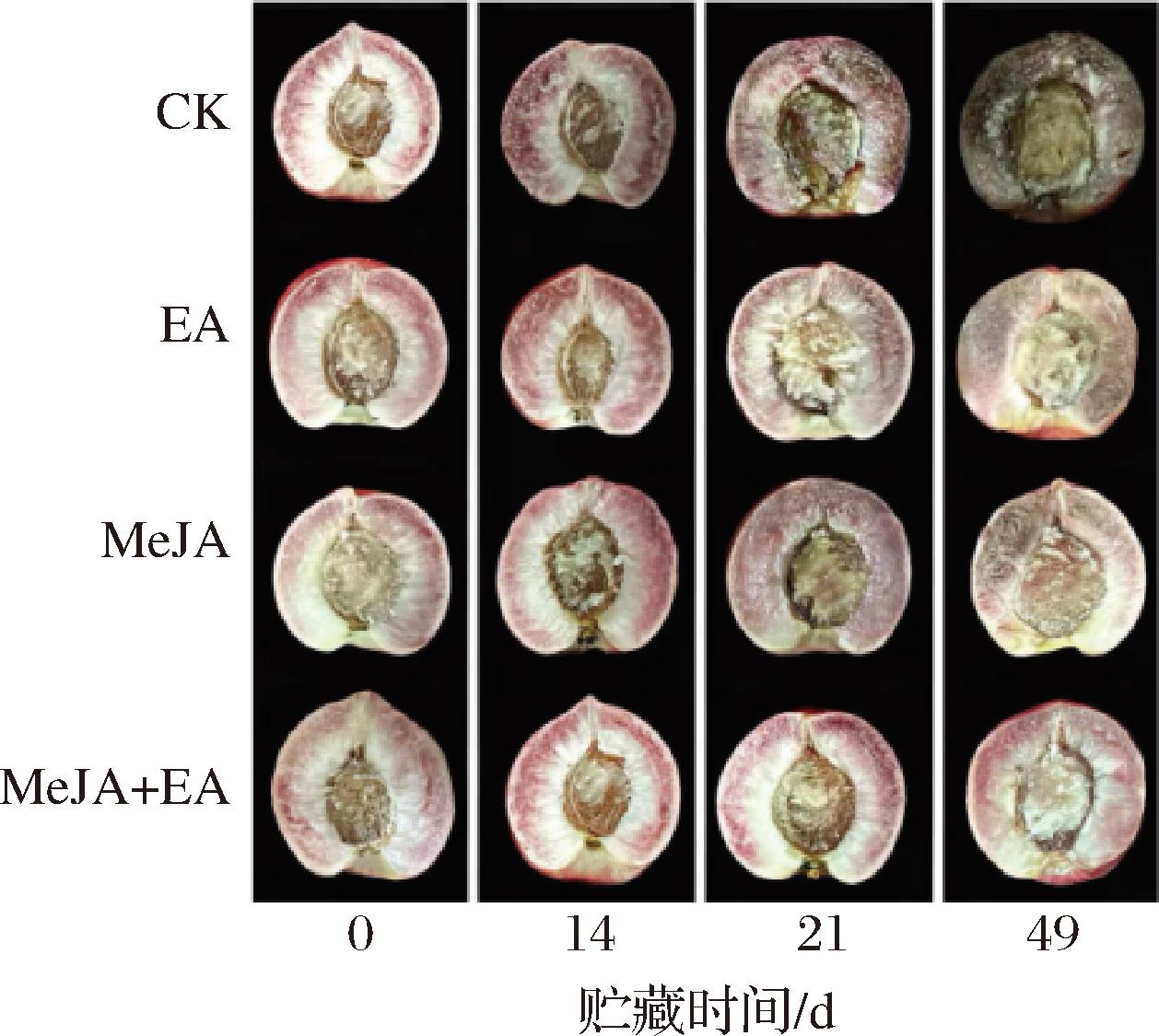
图4 EA、MeJA单独及复合处理对冷藏油桃果肉的影响
Fig.4 Effect of EA,MeJA alone and combined treatment on the pulp of refrigerated nectarine
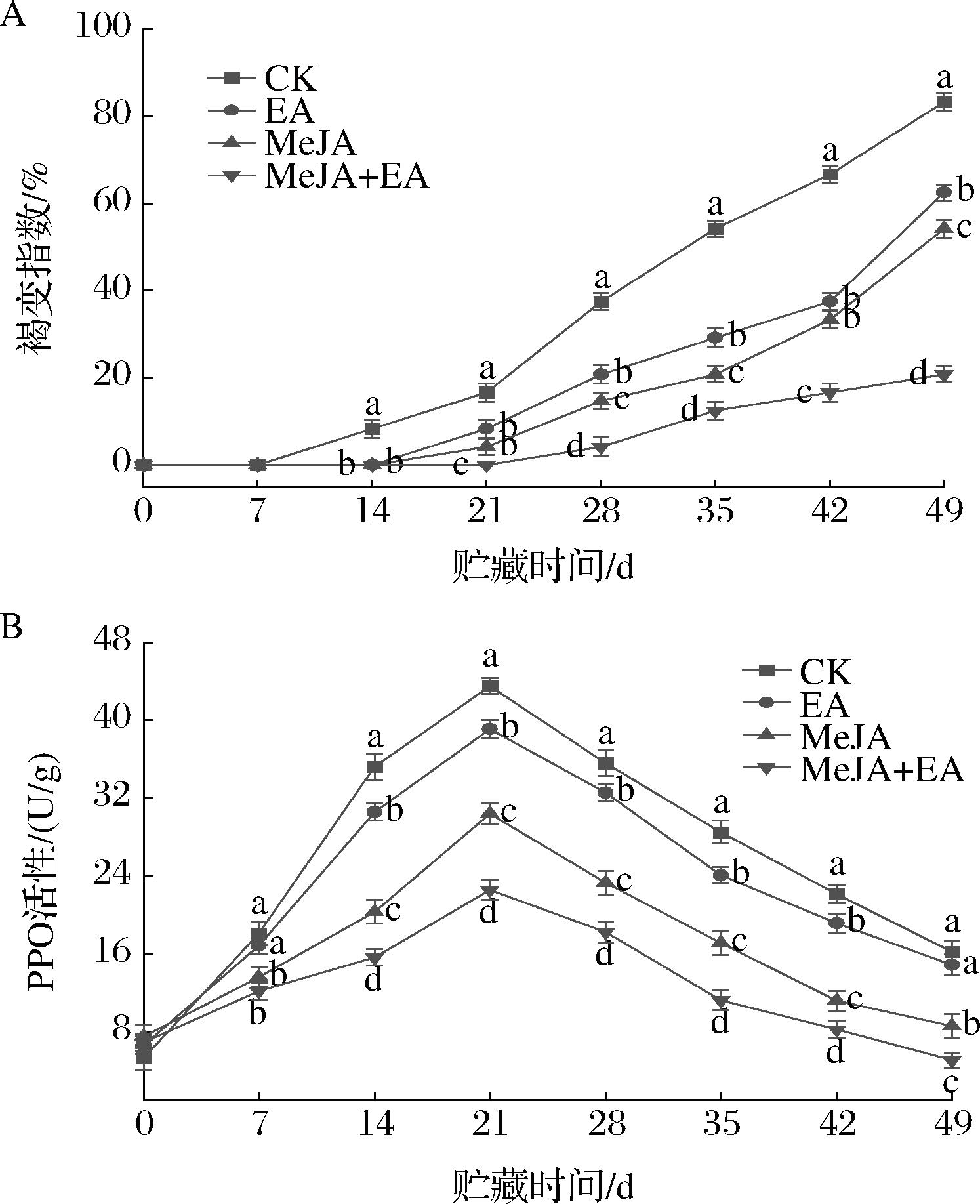
A-褐变指数;B-PPO
图5 EA、MeJA单独及复合处理对冷藏油桃果实褐变指数和PPO活性的影响
Fig.5 Effect of EA,MeJA alone and combined treatment on browning index and PPO activity of refrigerated nectarine fruit
PPO可以促进油桃果实中的酚类物质向褐色物质转化。如图5-B所示,对照组和处理组油桃果实的PPO活性先上升后下降,第21天活性最高,CK、EA、MeJA、MeJA+EA组PPO活性分别为42.31、39.11、30.42、22.56 U/g。EA、MeJA、MeJA+EA处理组酶活性比对照组分别降低7.56%、28.10%、46.68%。贮藏后期,处理组相比对照组仍保持较低的活性,其中MeJA+EA处理组活性最低。
2.4 MeJA结合EA处理对油桃果实呼吸速率和乙烯释放速率的影响
呼吸速率与乙烯释放率能够反映果实受冷害的程度以及果实在冷害条件下的生理状态变化。如图6 所示,CK、EA、MeJA、MeJA+EA组油桃果实在贮藏期间的呼吸速率和乙烯释放率均表现出先增后减的趋势特征,并伴随有明显的释放高峰。未经处理的油桃果实,其呼吸速率与乙烯释放率的最高值均集中出现在第21天。经处理的油桃果实,呼吸速率峰值延迟到了第28天和第35天。进入贮藏后期,处理组与对照组之间差异显著(P<0.05)。MeJA+EA复合处理的抑制效果最为显著。
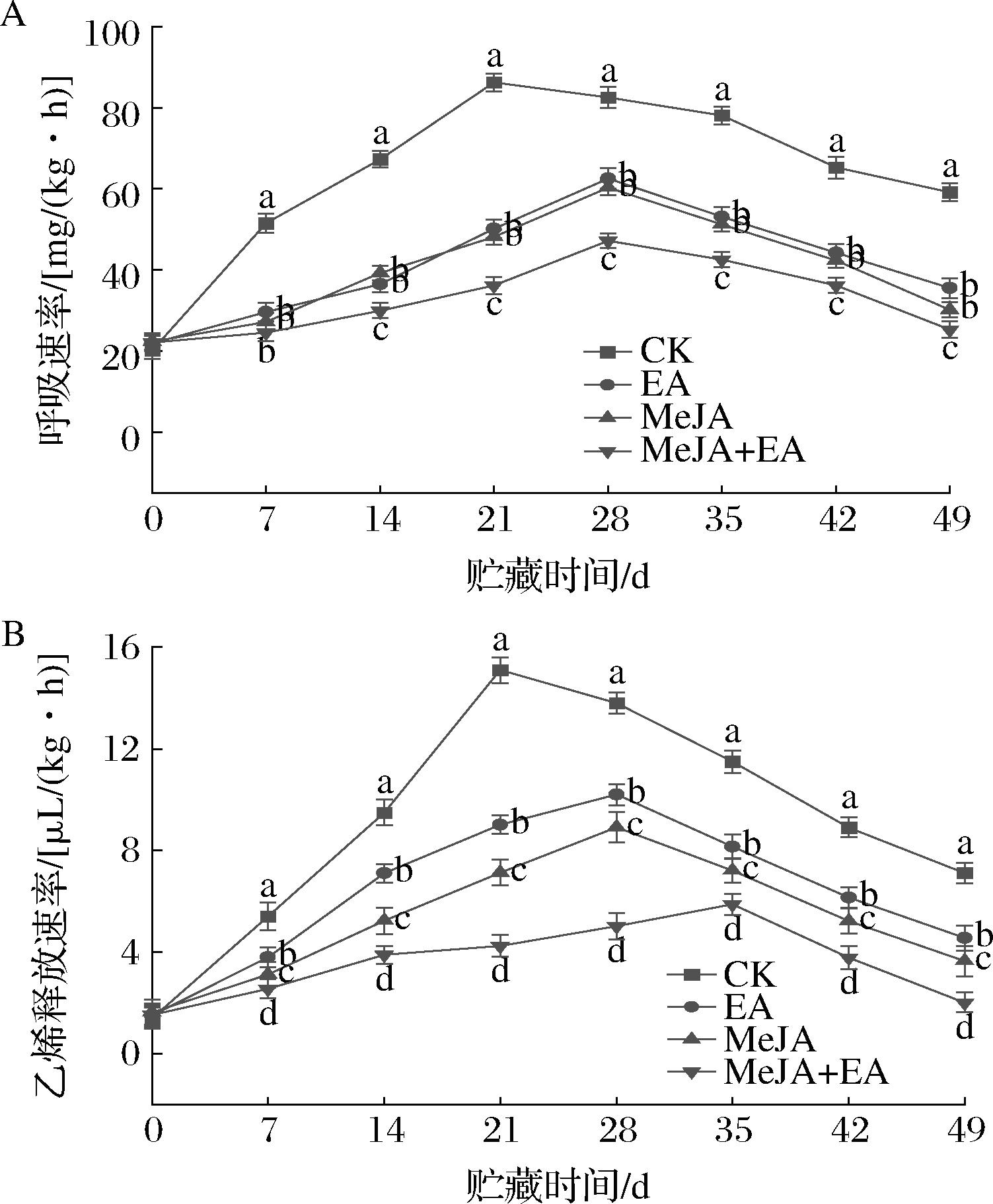
A-呼吸速率;B-乙烯释放率
图6 EA、MeJA单独及复合处理对冷藏油桃果实呼吸速率和乙烯释放率的影响
Fig.6 Effects of EA,MeJA alone and combined treatment on the respiration rate and ethylene release rate of refrigerated nectarine fruit
2.5 MeJA结合EA处理对油桃果实苯丙烷代谢相关酶活性及其代谢产物的影响
PAL、C4H、4CL是催化苯丙氨酸生成总酚、类黄酮和木质素的关键酶。如图7-A所示,CK、EA、MeJA、MeJA+EA组油桃果实的PAL活性在贮藏21 d时出现峰值,分别为7.03、9.21、10.91、11.22 U/g,EA、MeJA、MeJA+EA处理组分别比对照组提高了31.01%、55.20%、59.60%。随后各组PAL活性逐渐降低,处理组比对照组下降速度慢,在贮藏末期仍保持着较高水平活性,其中MeJA+EA处理组活性最高。
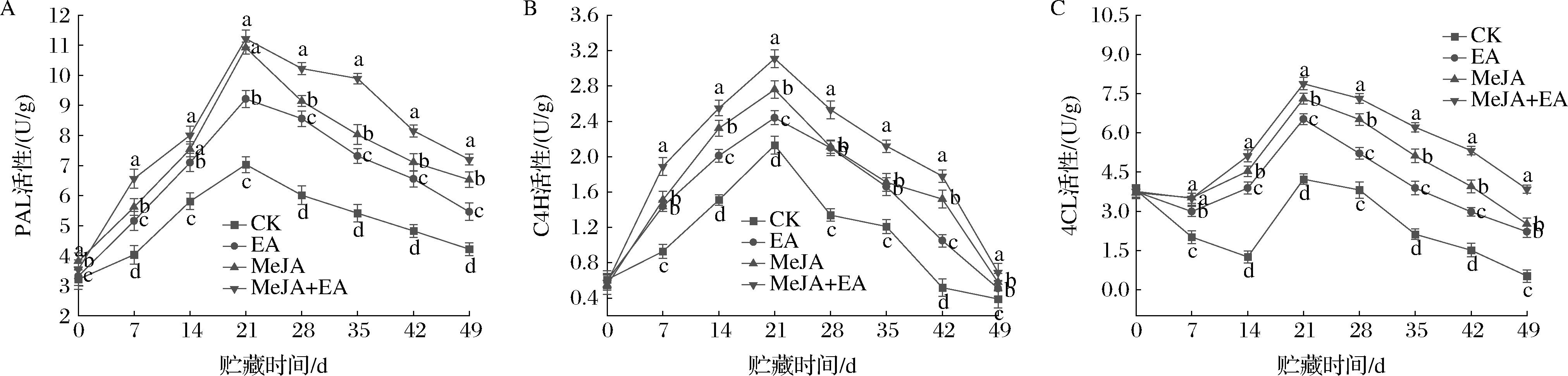
A-PAL;B-C4H;C-4CL
图7 EA、MeJA单独及复合处理对冷藏油桃果实PAL活性、C4H活性和4CL活性的影响
Fig.7 Effect of EA,MeJA alone and combined treatment on PAL activity,C4H activity,and 4CL activity in refrigerated nectarine fruit
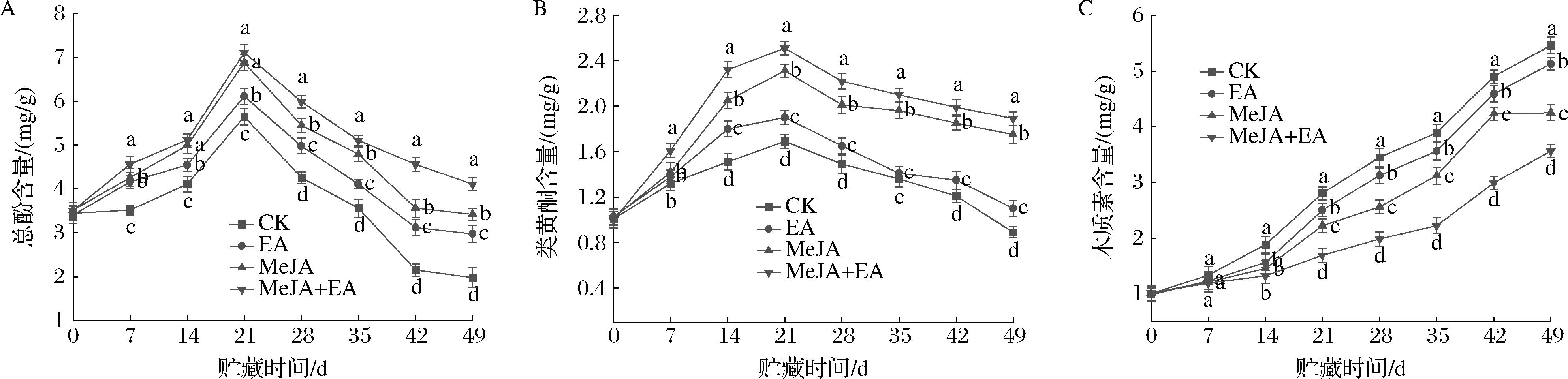
A-总酚;B-类黄酮;C-木质素
图8 EA、MeJA单独及复合处理对冷藏油桃果实总酚、类黄酮和木质素的影响
Fig.8 Effects of EA,MeJA alone and combined treatments on total phenol,flavonoids,and lignin in fruits of refrigerated nectarine
如图7-B所示,C4H活性高峰与PAL相同,均出现在21 d。21~49 d,C4H的活性都显著高于对照组(P<0.05)。第49天,CK、EA、MeJA、MeJA+EA组酶活性分别为0.39、0.51、0.58、0.69 U/g,EA、MeJA、MeJA+EA处理组分别比对照组提高了30.77%、48.72%、76.92%,其中MeJA+EA复合处理效果最佳。
如图7-C所示,对照组和各处理组的油桃果实的4CL活性在贮藏前期出现小幅度下降,而后4CL活性急剧上升,在21 d时达到峰值,CK、EA、MeJA、MeJA+EA组酶活性分别为4.23、6.52、7.31、7.88 U/g,EA、MeJA、MeJA+EA处理组相比对照组分别提高了54.14%、72.81%、86.29%。随后各组酶活性逐渐下降,至49 d,相比其他3组,MeJA+EA处理组活性最高。
总酚、类黄酮在油桃冷害过程中可以通过增强细胞膜稳定性、抗氧化防御、调节信号转导途径等机制,提高油桃果实抗性。如图8-A和图8-B所示,对照组和处理组油桃果实的总酚和类黄酮含量均呈现先增后减的变化趋势。经处理的油桃果实,含量得到显著提升(P<0.05),且其变化趋势相较于对照组更为平稳。MeJA+EA复合处理下,桃果实的总酚和类黄酮含量达到最高水平。这一结果表明,MeJA和EA处理都能够有效延缓油桃贮藏期间类黄酮和总酚含量的下降,而MeJA+EA复合处理效果最佳。
如图8-C所示,随着贮藏时间的延长,木质素含量不断升高,但在贮藏初期,对照组与处理组之间的木质素含量差异并不明显。随着贮藏时间的延长,各处理组之间的差异逐渐变得显著(P<0.05)。到第49天,CK、EA、MeJA、MeJA+EA组木质素含量分别为5.46、5.13、4.25、3.56 mg/g,EA、MeJA、MeJA+EA处理组比对照组分别降低了6.04%、22.16%、34.80%,其中MeJA+EA复合处理效果最佳。
2.6 MeJA结合EA处理对油桃果实冷害的相关性分析
为进一步明确MeJA+EA处理对油桃冷害的影响,对油桃的各项生理指标进行了相关性分析。如图9 所示,硬度与呼吸速率、乙烯释放率、冷害指数、呈显著负相关(P<0.05),说明呼吸和乙烯释放越旺盛、冷害指数越高,硬度越容易下降。冷害指数与呼吸速率、乙烯释放率呈显著正相关(P<0.05),说明呼吸和乙烯释放增强会加剧冷害。褐变指数与PPO活性呈显著正相关(P<0.05),说明PPO活性越高,褐变指数越高。PAL、C4H、4CL相互之间及与总酚、类黄酮呈显著正相关(P<0.05),符合苯丙烷代谢途径生成这些物质的规律,说明该代谢途径的激活会促进抗氧化和结构物质合成,增强果实抗逆性。
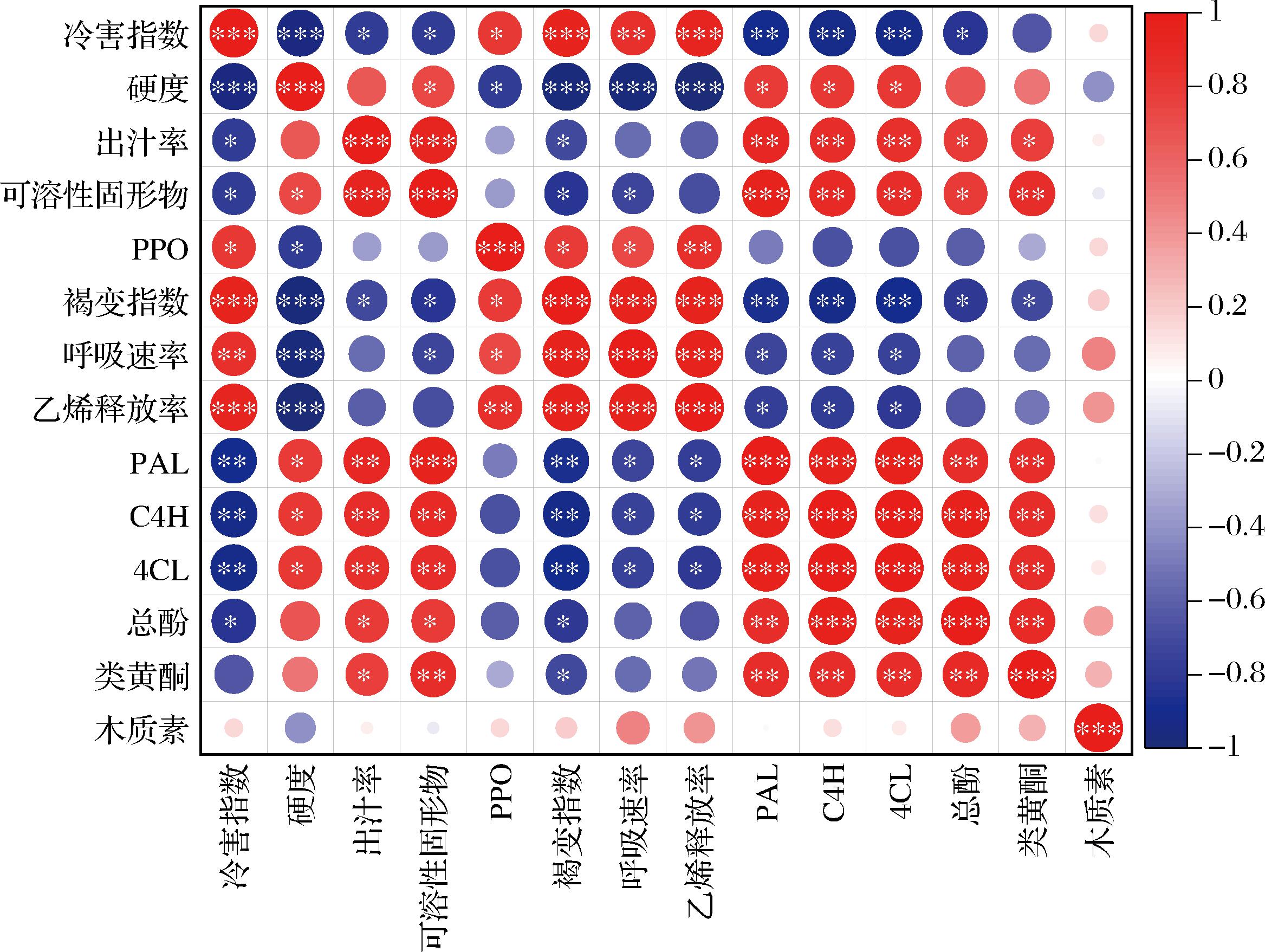
图9 MeJA结合EA处理对油桃果实冷害的相关性分析
Fig.9 Correlation analysis of MeJA combined with EA treatment
注:*P≤0.05、**P≤0.01、***P≤0.001。
3 讨论
油桃富含多种营养成分,口感鲜美、香气馥郁,因而备受消费者青睐。然而,作为冷敏型水果,油桃在不当的低温或长期冷藏条件下容易发生软化、絮败等现象,导致风味丧失,影响其品质[13]。硬度、出汁率、可溶性固形物直接反映了油桃果实的口感品质,是其重要的贮藏指标。诸多研究表明,MeJA和EA处理可以提高果实的抗冷性,减轻果实冷害的发生,延长贮藏期[14-16]。本实验结果同样表明EA、MeJA、MeJA+EA处理组均延缓了桃果实贮藏期间硬度的下降,提高了出汁率和可溶性固形物含量,降低了冷害指数。其中MeJA+EA处理组效果最佳。
油桃果实冷害的一个显著症状是褐变,这主要是由于酚类物质发生一系列酶促反应生成醌,最终导致褐变。在酶促反应里,PPO是起到关键作用的酶。尤其是低温条件下果肉褐变现象的加剧与PPO活性的大幅上升密切相关[17]。在本研究中,4种处理后的油桃果实PPO活性规律为:CK>EA>MeJA>MeJA+EA,褐变指数规律为:CK>EA>MeJA>MeJA+EA。这一结果与袁芳等[18]的研究结果一致,即通过调节PPO活性水平可以降低果肉褐变程度。而MeJA+EA复合处理组相比单一的EA、MeJA处理效果更好,PPO活性受到显著抑制(P<0.05)。
在果蔬采后代谢进程中,呼吸作用占据主导地位,它会持续消耗果实自身储存的有机物质,进而对果实的色泽、口感、质地等品质特性产生显著影响[19]。特别是对于冷敏性果实而言,一旦遭遇不适宜的低温环境,其呼吸速率往往会出现异常攀升的情况,而这一现象极有可能与果实冷害的发生、发展紧密相关[20]。在本研究中,EA、MeJA、MeJA+EA处理组油桃果实的呼吸速率和乙烯释放率均受到显著抑制(P<0.05)。相较于对照组呼吸速率分别降低了39.85%、48.94%、57.23%,乙烯释放率分别降低了35.77%、48.60%、71.69%。结果表明,不同处理方式均对呼吸速率及乙烯释放率起到抑制作用,进而有效延缓了果实品质恶化,减缓冷害发展进程。其中MeJA+EA处理组效果最好,推测可能是因为EA减少乙烯刺激,从而影响乙烯参与冷害信号的转导[21]和细胞壁的代谢[22],MeJA促使防御反应发生,进而增强了果实细胞壁的稳定性。二者协同强化果实防御,更好地抑制了呼吸。
苯丙烷代谢是植物抵御逆境胁迫的重要途径。苯丙烷代谢的激活通常导致下游产物的分化:一方面,PAL催化苯丙氨酸脱氨生成肉桂酸,经C4H和4CL作用进入木质素合成途径[23];另一方面,代谢流也可转向酚酸和类黄酮等抗氧化物质的合成[24]。本研究中,经EA、MeJA、MeJA+EA处理过的油桃果实PAL、C4H和4CL的活性显著高于对照组,其中以MeJA+EA复合处理效果最佳,MeJA+EA复合处理促进苯丙烷代谢途径中代谢产物总酚、类黄酮的大量积累,延缓了木质素含量的上升,最终提升了油桃抵抗冷害的能力。这一结论与SAGHARYAN等[25]关于“MeJA促进酚类合成”的结果相一致。
4 结论
本研究结果表明,在贮藏过程中,不同处理的油桃果实品质指标和相关酶活性指标相比对照组变化趋势具有差异,主要表现为延缓了果肉软化、呼吸高峰和冷害现象的发生,提高了果实可溶性固形物的含量,使油桃保持很好的风味。而各处理中,MeJA+EA复合处理组对油桃贮藏期间冷害的抑制及果实外观品质的保持效果最佳。此外,MeJA+EA复合处理对苯丙烷代谢途径中PAL、C4H、4CL活性诱导能力最强,同时显著抑制PPO活性,促进了桃果实内部总酚、类黄酮的累积,延缓了木质素含量的上升,从而提升了油桃抵抗冷害的能力。由此可见,MeJA+EA复合处理可显著减轻桃果在49 d低温贮藏期内冷害的发生,提升油桃果实的贮藏品质,且操作便捷,处理量大,在实际生产中应用前景广阔,因此本研究可为油桃采后贮藏保鲜提供一定的技术参考。
[1] 刘雪平,张永涛,刘凌霄,等.桃保鲜技术与加工工艺研究进展[J].粮食与油脂,2023,36(5):19-23.LIU X P,ZHANG Y T,LIU L X,et al.Research progress on preservation technology and processing technology of peach[J].Cereals &Oils,2023,36(5):19-23.
[2] 唐伟杰,张潆支,张良,等.不同浓度茉莉酸甲酯处理对“金冠”苹果保鲜效果的影响[J].包装与食品机械,2024,42(1):12-18.TANG W J,ZHANG Y Z,ZHANG L,et al.Effects of different concentrations of methyl jasmonate treatment on preservation of“Jinguan”apple fruit[J].Packaging and Food Machinery,2024,42(1):12-18.
[3] GLOWACZ M,BILL M,TINYANE P P,et al.Maintaining postharvest quality of cold stored ‘Hass’ avocados by altering the fatty acids content and composition with the use of natural volatile compounds-methyl jasmonate and methyl salicylate[J].Journal of the Science of Food and Agriculture,2017,97(15):5186-5193.
[4] 杨文慧.五种外源物质处理对采后香蕉果实冷害控制效果的研究[D].南宁:广西大学,2021.YANG W H.Study on the effect of five kinds of exogenous substances on the control of chilling injury of postharvest bananas[D].Nanning:Guangxi University,2021.
[5] 李亚敏.乙烯吸收剂处理可有效改善蓝莓果实的储存效果[J].基因组学与应用生物学,2019,38(12):5574-5580.LI Y M.Ethylene absorbent can effectively improve the storage effect of blueberry fruit[J].Genomics and Applied Biology,2019,38(12):5574-5580.
[6] 王胜永.1-MCP、乙烯吸收剂双控对“阳光玫瑰”葡萄货架品质的影响[J].食品研究与开发,2022,43(7):236.WANG S Y.Effect of 1-MCP and ethylene absorbent on the shelf quality of “Sunshine Rose” grape[J].Food Research and Development,2022,43(7):236.
[7] 张鹏,陈曦冉,贾晓昱,等.1-MCP结合乙烯吸收剂对软枣猕猴桃贮藏品质的影响[J].包装工程,2022,43(21):17-24.ZHANG P,CHEN X R,JIA X Y,et al.Effects of 1-MCP combined with ethylene absorbent on storage quality of Actinidia arguta[J].Packaging Engineering,2022,43(21):17-24.
[8] WANG J W,ZHOU X,ZHOU Q,et al.Low temperature conditioning alleviates peel browning by modulating energy and lipid metabolisms of ‘Nanguo’ pears during shelf life after cold storage[J].Postharvest Biology and Technology,2017,131:10-15.
[9] 刘雪平,张永涛,崔晓梅,等.不同桃品种的品质及加工特性评价分析[J].保鲜与加工,2023,23(6):34-40.LIU X P,ZHANG Y T,CUI X M,et al.Evaluation and analysis of qualities and processing characteristics of different peach varieties[J].Storage and Process,2023,23(6):34-40.
[10] 曹建康,姜微波,赵玉梅.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社,2007.CAO J K,JIANG W B,ZHAO Y M.Biological and Biochemical Experiments of Fruits and Vegetable[M].Beijing:China Light Industry Press,2007.
[11] 董柏余,汤洪敏,姚秋萍,等.采后水杨酸处理对金刺梨果实活性氧和苯丙烷代谢的影响[J].食品工业科技,2021,42(17):308-315.DONG B Y,TANG H M,YAO Q P,et al.Effects of salicylic acid treatment on reactive oxygen species metabolism and phenylpropanoid pathway in Rosa sterilis[J].Science and Technology of Food Industry,2021,42(17):308-315.
[12] 李冰茹,李美琪,李皎琪,等.冷激预处理减轻鲜切火龙果褐变的作用及机理[J].食品科学,2023,44(13):97-104.LI B R,LI M Q,LI J Q,et al.Alleviating effect and mechanism of cold shock pretreatment on browning of fresh-cut pitaya fruit[J].Food Science,2023,44(13):97-104.
[13] 李京春.1-Pent CP结合自发气调对油桃采后生理及保鲜效果的影响[D].淄博:山东理工大学,2023.LI J C.Effects of 1-Pent CP combined with modified atmosphere on postharvest physiology and preservation of nectarine[D].Zibo:Shandong University of Technology,2023.
[14] 杨晓涵.外源茉莉酸甲酯抑制不同溶质桃果实采后冷害的作用机制研究[D].杭州:浙江工商大学,2022.YANG X H.Exogenous methyl jasmonate inhibits chilling injury of peach fruit with different flesh types during postharvest[D].Hangzhou:Zhejiang Gongshang University,2022.
[15] DUAN W Y,YANG C,CAO X M,et al.Transcriptome and DNA methylome analysis reveal new insights into methyl jasmonate-alleviated chilling injury of peach fruit after cold storage[J].Postharvest Biology and Technology,2022,189:111915.
[16] 刘佰霖,王文辉,马风丽,等.自发气调包装和乙烯吸收剂对‘玉露香’梨果实品质及耐贮性的影响[J].果树学报,2019,36(7):911-921.LIU B L,WANG W H,MA F L,et al.Effect of modified atmosphere packaging and ethylene absorbents on postharvest fruit quality and storage performance of‘Yuluxiang’pear[J].Journal of Fruit Science,2019,36(7):911-921.
[17] 陈维宁,李旋,王文月,等.桃酶促褐变机理与调控技术研究进展[J].食品科学,2024,45(7):290-298.CHEN W N,LI X,WANG W Y,et al.Research progress on the mechanism and regulation of enzymatic browning in peach fruit[J].Food Science,2024,45(7):290-298.
[18] 袁芳,邱诗铭,李丽.不同保鲜剂复合处理对鲜切芒果活性氧代谢、细胞膜透性和褐变的影响[J].食品科学,2020,41(3):218-223.YUAN F,QIU S M,LI L.Effect of composite preservatives on active oxygen metabolism,cell membrane permeability and browning of fresh-cut mango[J].Food Science,2020,41(3):218-223.
[19] 宋聪慧,郭水欢,史小强,等.褪黑素调控果蔬采后保鲜研究进展[J].食品科学,2023,44(3):228-236.SONG C H,GUO S H,SHI X Q,et al.Research progress on the regulatory effect of melatonin on postharvest preservation of fruits and vegetables[J].Food Science,2023,44(3):228-236.
[20] GHASEMNEZHAD M,MARSH K,SHILTON R,et al.Effect of hot water treatments on chilling injury and heat damage in ‘Satsuma’ mandarins:Antioxidant enzymes and vacuolar ATPase,and pyrophosphatase[J].Postharvest Biology and Technology,2008,48(3):364-371.
[21] LUO M L,SUN H J,GE W Y,et al.Effect of Glycine betaine treatment on aroma production of ‘Nanguo’ pears after long-term cold storage-possible involvement of ethylene synthesis and signal transduction pathways[J].Food and Bioprocess Technology,2022,15(6):1327-1342.
[22] NASCIMENTO V L,PEREIRA A M,SIQUEIRA J A,et al.Exogenous ethylene reduces growth via alterations in central metabolism and cell wall composition in tomato (Solanum lycopersicum)[J].Journal of Plant Physiology,2021,263:153460.
[23] SHEN X Y,LIU Y,ZENG Y,et al.Hydrogen sulfide alleviates the chilling-induced lignification in loquat fruit by regulating shikimate,phenylpropanoid and cell wall metabolisms[J].Postharvest Biology and Technology,2024,214:113012.
[24] 汪开拓,郑永华,唐文才,等.茉莉酸甲酯处理对采后葡萄果实酚酸合成和抗氧化活性的影响及其机理研究[J].食品科学,2013,34(6):260-265.WANG K T,ZHENG Y H,TANG W C,et al.Effect of methyl jasmonate treatment on synthesis and antioxidant activity of phenolic acids in grape berries and corresponding mechanisms[J].Food Science,2013,34(6):260-265.
[25] SAGHARYAN M,SHARIFI M,SAMARI E.Methyl jasmonate redirects the dynamics of carbohydrates and amino acids toward the lignans accumulation in Linum album cells[J].Plant Physiology and Biochemistry,2023,198:107677.