草菇(Volvariella volvacea)又名包脚菇、稻草菇,是一种生长在热带和亚热带地区的担子菌类[1]。草菇味道鲜美,含有丰富的多糖、蛋白质、不饱和脂肪酸等营养成分,具有降血压、降胆固醇、预防癌症等功效[2-3],深受消费者的喜爱。和其他主要栽培食用菌相比,草菇的生物学效率偏低;平菇的生物学效率可达200%左右,双孢蘑菇、香菇的生物学效率也可达65%~100%,而草菇的生物学效率仅为10%~40%[4]。朱巍巍[5]对糙皮侧耳菌丝进行连续继代培养,发现活性氧(reactive oxygen species,ROS)的积累会导致子实体产量降低。怀美玉等[6]研究发现继代培养蛹虫草退化菌株菌丝内的ROS含量升高,子实体产量降低。ROS属于生物体有氧代谢的副产物之一,主要包括超氧阴离子![]() 和H2O2等,ROS的过度积累会造成生物体生长发育受阻,导致食用菌子实体产量降低。
和H2O2等,ROS的过度积累会造成生物体生长发育受阻,导致食用菌子实体产量降低。
作为生物体抗氧化胁迫酶促反应系统的成员之一,谷胱甘肽过氧化物酶(glutathione peroxidase,GPX)是一类以还原型谷胱甘肽(glutathione,GSH)或硫氧还蛋白(thioredoxin,Trx)为电子供体,催化H2O2、有机氢过氧化物或脂质过氧化物还原成H2O或相应醇类的同工酶的总称[7]。GPX参与调节细胞周期、细胞信号转导等一系列重要的生物学过程[8],广泛存在动物、植物、真菌等生物体内。GPX是生物体内重要的ROS清除剂,保护细胞免受氧化胁迫[9]。ZHAO等[10]发现在草菇无性继代退化过程中,GPX酶活力显著下降。XIONG等[11]通过过表达gpx基因使退化的蛹虫草重新长出了子实体。
本研究通过在草菇商业栽培菌种V110中过表达gpx基因,对比草菇原种及转化子的抗氧化性能、ROS含量、基质降解酶活力、生产性状等指标,探讨gpx基因过表达对草菇ROS清除能力和生产性状的影响。
1 材料与方法
1.1 材料与试剂
草菇V110,广东揭阳锐一食用菌;草菇gpx基因过表达转化子(OE-V3、OE-V4、OE-V16、OE-V21),由课题组前期实验所获得。引物合成,北京擎科生物科技有限公司。
马铃薯葡萄糖琼脂培养基(potato dextrose agar,PDA)(g/L):马铃薯20,葡萄糖2,琼脂粉2[12]。液体发酵培养基(g/L):粉碎的棉籽壳1.0,酵母抽提物0.5,KH2PO4 0.06,MgSO4 0.05。种子培养基(质量分数):棉籽壳88%,麸皮10%,石灰2%,含水量75%,pH 8~9。栽培培养基(质量分数):废棉97%,石灰3%,含水量约70%,pH 9~10。
无水葡萄糖、琼脂粉、无水乙醇、磷酸二氢钾、硫酸镁、亚硫酸钠、二硝基水杨酸、羧甲基纤维素钠、微晶纤维素、水杨苷、丙二酸钠、木聚糖、酒石酸钾钠、酵母抽提物、2,2′-联氮双-3-乙基苯并噻唑啉-6-磺酸,上海源叶生物科技有限公司;棉籽壳、废棉、麸皮、石灰,广东锐一食用菌栽培基地;氢氧化钾、氢氧化钠,国药集团化学试剂有限公司;氯化硝基四氮唑蓝(nitrotetrazolium blue chloride,NBT),合肥博美生物科技有限公司;SYBR Green混合液,天根生化技术有限公司;商业试剂盒,北京索莱宝科技有限公司。
1.2 仪器与设备
SW-CJ-IFD超净工作台,苏州安泰空气技术有限公司;LDZX-50KBs立式蒸汽灭菌锅,上海申安医疗器械厂;FA1204B电子天平,上海佑科仪器仪表有限公司;HWS-26恒温水浴锅、THZ-98A恒温振荡器、LRH-150电热恒温培养箱,上海一恒科学仪器有限公司;S-1000型PCR仪、ChemiDoc-XRS紫外凝胶成像系统,美国Bio-red;Bio-Spec-nano超微量分光光度计、Bio-Spec-nano紫外可见分光光度计,日本岛津公司;DYY-6D电泳仪,北京六一公司;ZTKX-CG-1500智能食用菌出菇箱,北京智态康兴生物科技有限公司。
1.3 实验方法
1.3.1 抗氧化酶基因表达量测定
参照草菇基因组序列(http://jgi.doe.gov),利用Primer Premier 5.0软件进行引物设计。以内体SPRY结构域蛋白基因(endosomal SPRY domain protein gene,SPRYp)为内参基因,采用SYBR Green混合液进行实时荧光定量PCR (real-time quantitative polymerase chain reaction,RT-qPCR)检测目的基因gpx及超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)和谷胱甘肽还原酶(glutathione reductase,GR)的编码基因Cu/Zn-sod、Mn-sod1、Mn-sod2、cat1、cat2及gr的相对表达量,引物序列如表1所示。参考王文沛等[13]的方法,进行RT-qPCR扩增,使用2-△△Ct方法计算基因的相对表达量。
表1 用于RT-qPCR的引物
Table 1 Primers used for RT-qPCR

基因正向序列 (5′-3′)反向序列 (5′-3′)Cu/Zn-sodATGCGTTGCGCAACATTCGTCGCTGAGCTGGTGTACGTCCAATGACACCAMn-sod1CAGGGTTCTGGATGGGGCTAATGGGGATGTGGGTGAGGMn-sod2CACAAAGACCGCTGCTATCTAGTAACGACCTCTAGCTTGCcat1GCCGCATCGCCATTCTTGCTTCACCCATACCCAACTcat2CCTTGCCCACTTTGACCGTTGCCCTGACCTTCTTGCgrGCTGTCGTAGGTGCTGGGTAGGGTCAAATCGCCTCAAAgpxTCGGAGGTGAATGGGAACTTGATCCTCGTCAGACCCATASPRYpCATTGCTTGTTCTACTGCCACCTTCAAACCCACCCTC
1.3.2 抗氧化能力、ROS含量的测定
将草菇菌丝块接种在PDA培养基中培养3 d,收集菌丝,使用商业试剂盒检测CAT、SOD、GR和GPX活力,GSH、氧化型谷胱甘肽![]() 和H2O2的含量。
和H2O2的含量。
1.3.3 NBT染色
参照WANG等[14]的方法,取直径1 cm的菌丝块接种于PDA平板中心,将灭菌好的载玻片斜插入培养基中,30 ℃培养至菌丝占据载玻片约1/2处时,取出载玻片。将20 μL 0.3 mmol/L NBT溶液滴到载玻片的菌丝密集处,室温反应15 min,放于光学显微镜下观察菌丝颜色。
1.3.4 基质降解酶活力的测定
将活化好的菌株接种于液体发酵培养基中,在33 ℃、180 r/min的条件下摇床培养8 d后,取适量上清液在4 ℃、1 000 r/min下进行离心10 min,吸取上清液即为粗酶液。
β-葡萄糖苷酶(β-glucosidase activity,BGL)活力的测定参照ZHAO等[15]的方法,滤纸酶(filter paper enzyme,FPA)、内切葡聚糖酶(endoglucanase,EG)、外切葡聚糖酶(celloBioHydrolase,CBH)、漆酶(laccase,Lac)、锰过氧化物酶(manganese peroxidase,MnP)活力的测定参照ZHAO等[16]的方法,木聚糖酶(xylanase,Xyl)和半纤维素酶(hemicellulase,HMC)活力的测定参照DOS SANTOS等[17]的方法。
1.3.5 氧化胁迫实验
参照YANG等[18]的方法,将草菇接种于添加8 mmol/L H2O2的PDA平板上,30 ℃培养6 d,记录菌落形态,并采用十字交叉法测定菌丝生长速度。
1.3.6 栽培实验
将草菇菌株统一活化后,接种于种子培养基上,30 ℃培养;当菌丝长满后,将其接种到装有栽培培养基的栽培框(40 cm×20 cm×10 cm)中,置于出菇箱中进行培养;待菌丝长满栽培培养基表面,喷出菇水,打开照明灯和加湿器,使温度保持在33 ℃,湿度保持在90%左右。在栽培过程中测定以下指标。
原基形成时间(d):从接种到第1个原基出现的时间。
生产周期(d):从接种开始到收获第1个蛋形阶段所需的时间周期。
平均单菇重(g):生长至蛋形期时,从每个栽培框随机摘取5个,分别称重后,取平均值。
生物学效率按公式(1)计算:
生物学效率![]()
(1)
1.4 数据处理
所有实验均进行3次重复,取平均值,采用Origin 2021软件作图、IBM SPSS Statistics27软件进行显著性分析。
2 结果与分析
2.1 gpx基因过表达对草菇抗氧化酶活力及其基因相对表达量的影响
对抗氧化酶活力及编码基因表达量进行测定,结果如图1所示。GPX酶活力及gpx基因表达量均显著提高(P<0.05);与V110相比,OE-V3、OE-V4、OE-V16和OE-V21的GPX酶活力分别提高了16.63%、70.42%、88.51%和83.62%,gpx基因相对表达量分别提高了32.68%、73.26%、97.09%和92.13%。OE-V3、OE-V4、OE-V16和OE-V21的CAT酶活力分别较V110提高了13.92%、43.41%、61.81%和58.00%,OE-V16、OE-V21的cat1、cat2基因表达量较V110提高幅度最大。OE-V3、OE-V4、OE-V16和OE-V21的SOD酶活力分别较V110提高了19.04%、45.69%、61.61%和56.26%,OE-V16、OE-V21菌株的Mn-sod2、Cu/Zn-sod基因表达量较V110提高幅度最大,4个过表达gpx菌株的Mn-sod1的基因相对表达量和V110相比,差异均不显著(P>0.05)。OE-V3、OE-V4、OE-V16和OE-V21的GR酶活力分别较V110提高了19.53%、71.07%、88.97%和83.73%,OE-V16、OE-V21菌株的gr基因表达量较V110提高幅度最大。4个过表达gpx菌株的抗氧化酶活力变化趋势与抗氧化酶基因的相对表达量变化趋势基本一致。
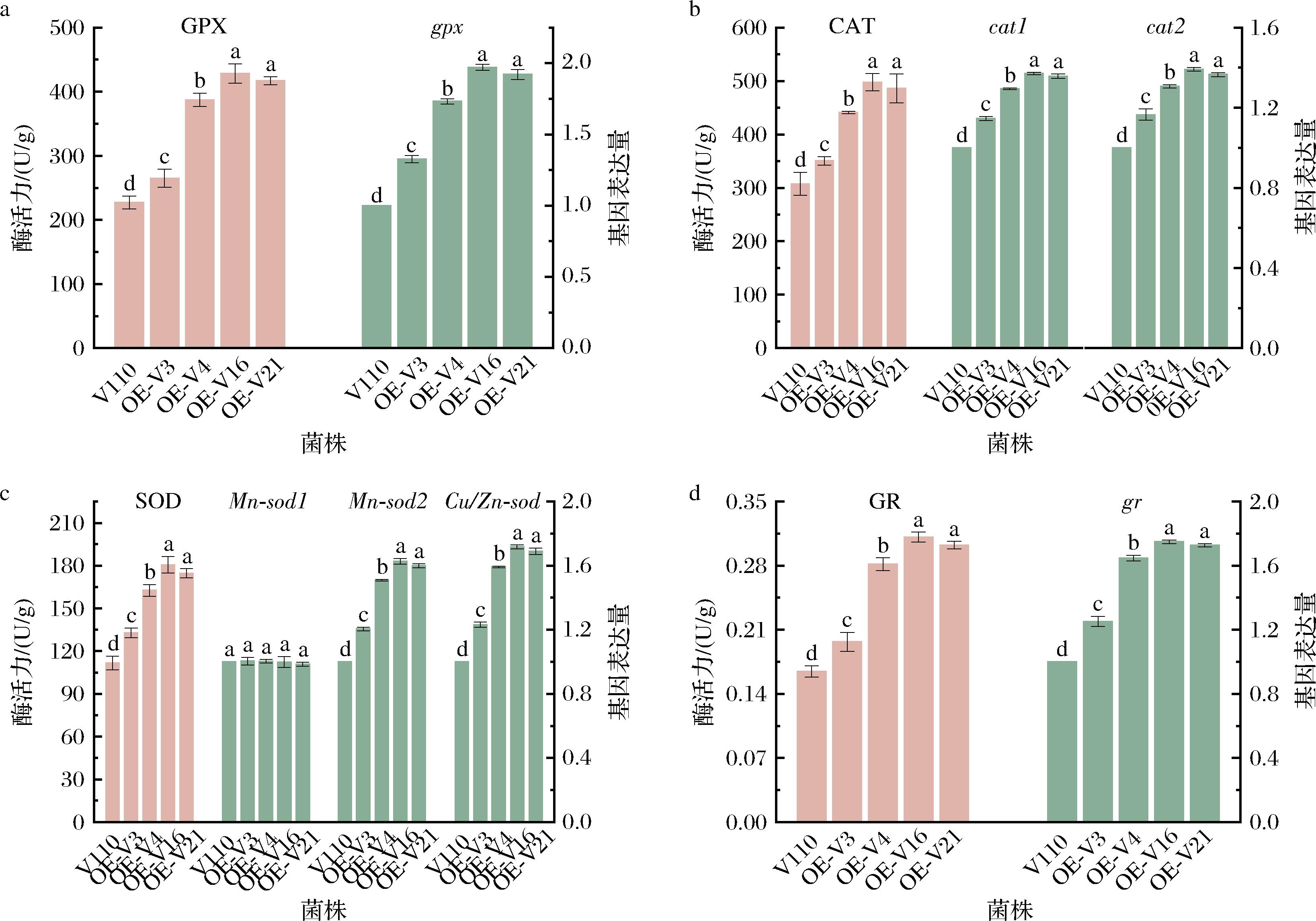
a-GPX酶活力和gpx基因表达量;b-CAT酶活力和cat1、cat2基因表达量;c-SOD酶活力和Mn-sod1、Mn-sod2、Cu/Zn-sod基因表达量;d-GR酶活力和gr基因表达量
图1 草菇菌株抗氧化酶活力和基因相对表达量
Fig.1 Antioxidant enzyme activity and relative gene expression levels in V.volvacea strains
注:不同小写字母代表同一组内有显著性差异(P<0.05)(下同)。
2.2 gpx基因过表达对草菇GSH和GSSG含量的影响
对草菇菌株的GSH和GSSG含量进行测定。结果如图2所示。4个过表达gpx基因草菇菌株的GSH、GSSG含量均显著高于V110(P<0.05)。OE-V16、OE-V21、OE-V4和OE-V3的GSH含量比V110分别升高了46.96%、42.55%、34.57%和16.69%;GSSG含量比V110分别升高了26.68%、24.76%、21.11%和11.59%。此外,OE-V4、OE-V16和OE-V21的GSH/GSSG值均较V110显著升高,OE-V16的GSH/GSSG值达到最高。这些结果表明,gpx基因相对表达量的提高可以提高草菇菌株中GSH和GSSG的含量。
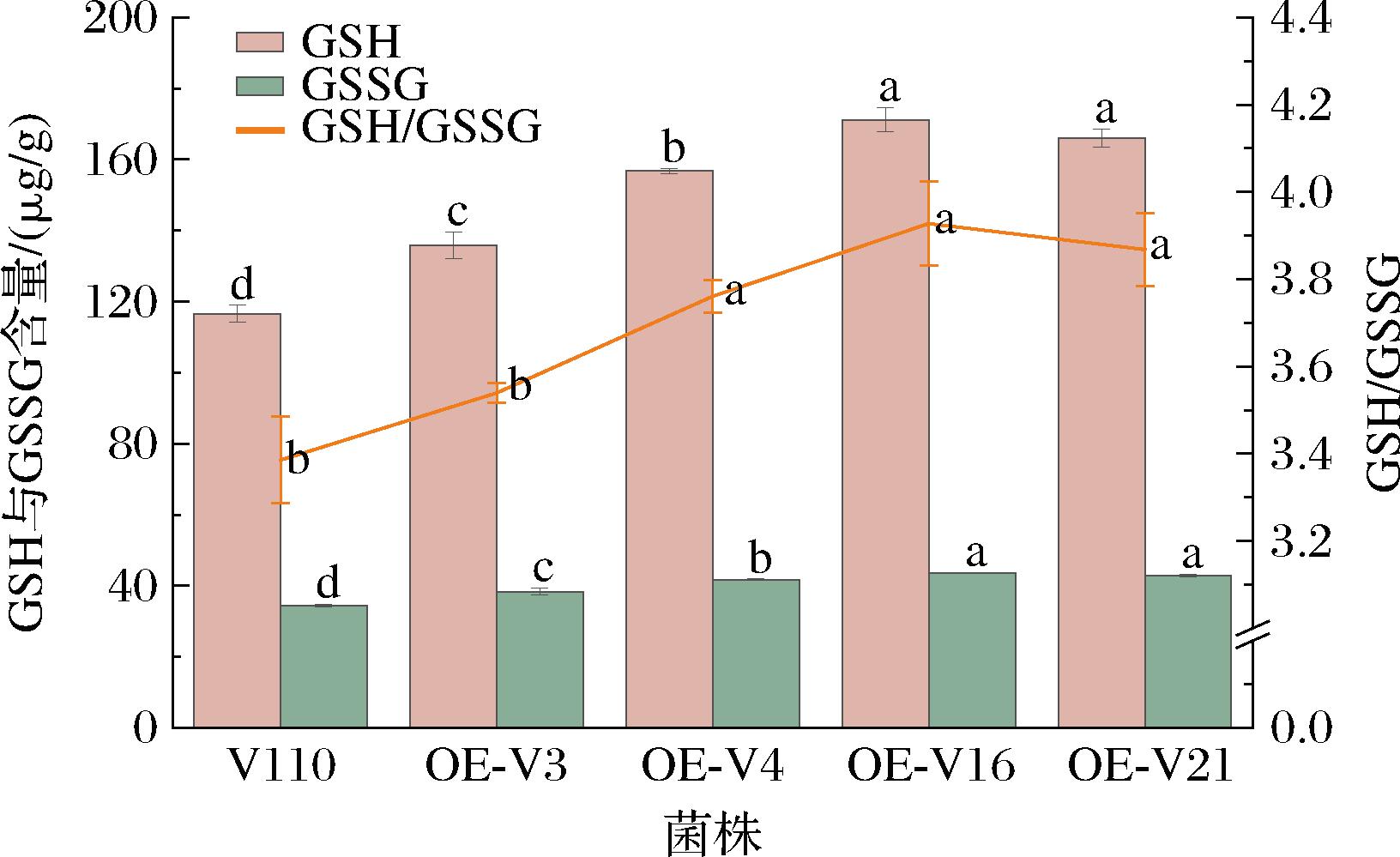
图2 草菇菌株的GSH、GSSG含量
Fig.2 The content of GSH and GSSG in V.volvacea strains
2.3 gpx基因过表达对草菇ROS含量的影响
通过NBT染色实验测定草菇的ROS含量,颜色越深说明菌丝内ROS含量越高[19]。由图3-a可知,相同的染色时间内,V110的颜色呈现深蓝色,OE-V3、OE-V4呈现浅蓝色,OE-V16、OE-V21的菌丝颜色最浅,表明过表达gpx基因可以显著降低菌株的ROS积累。
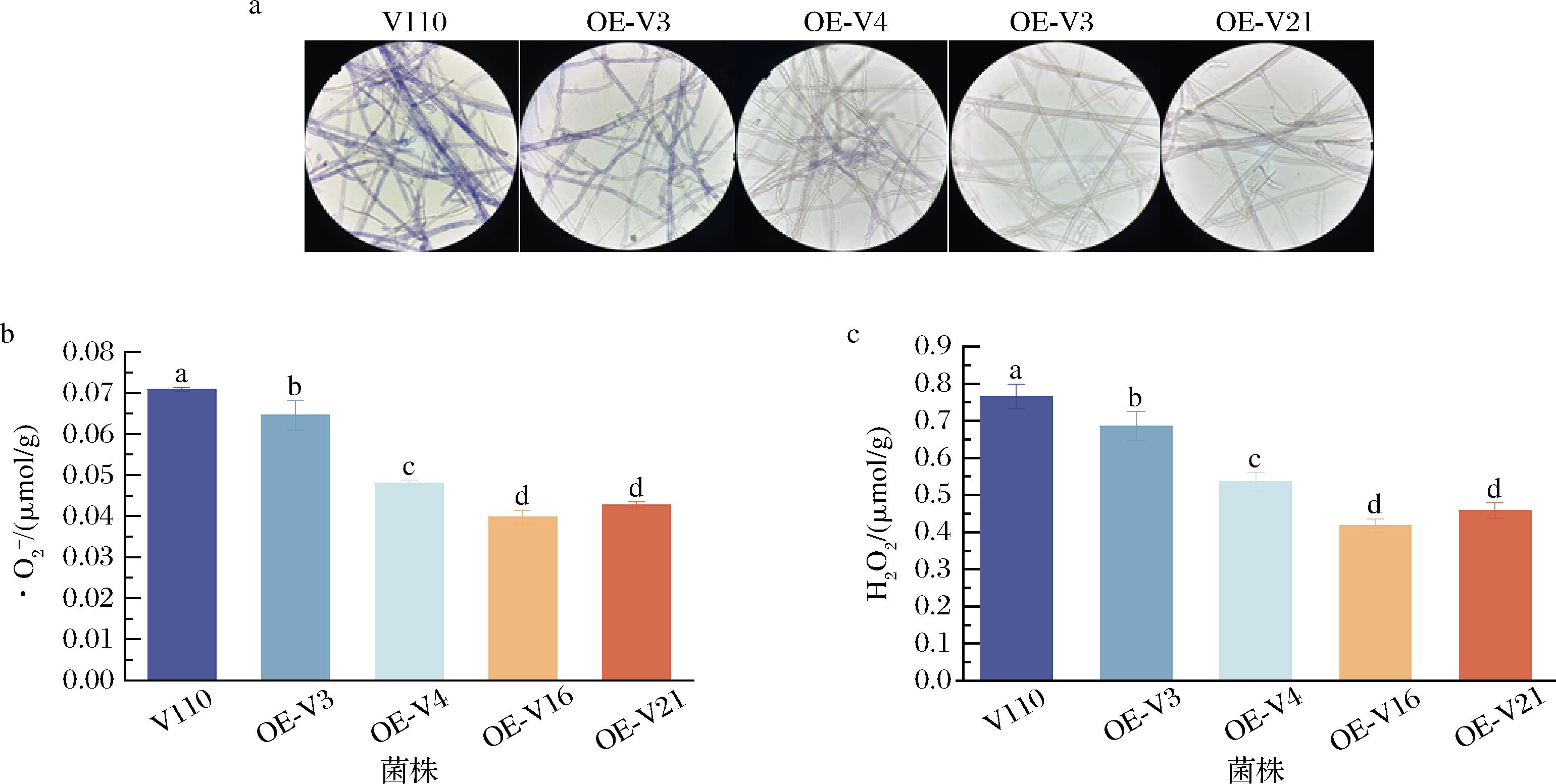
a-NBT染色;![]() 含量;c-H2O2含量
含量;c-H2O2含量
图3 草菇菌株的ROS含量
Fig.3 The content of ROS in V.volvacea strains
对草菇菌株中ROS的主要组分![]() 和H2O2的含量进行测定。4个过表达gpx基因菌株的
和H2O2的含量进行测定。4个过表达gpx基因菌株的![]() 和H2O2的含量均显著低于V110(P<0.05)。与V110相比,OE-V3、OE-V4、OE-V16、OE-V21菌株的
和H2O2的含量均显著低于V110(P<0.05)。与V110相比,OE-V3、OE-V4、OE-V16、OE-V21菌株的![]() 的含量分别降低了8.89%、32.22%、43.89%、39.72%,H2O2的含量分别降低了10.43%、30.06%、45.40%、40.18%。这些结果表明,提高gpx基因的表达量可以有效降低草菇菌株中ROS的含量。
的含量分别降低了8.89%、32.22%、43.89%、39.72%,H2O2的含量分别降低了10.43%、30.06%、45.40%、40.18%。这些结果表明,提高gpx基因的表达量可以有效降低草菇菌株中ROS的含量。
2.4 gpx基因过表达对草菇基质降解酶活力的影响
对草菇菌株的基质降解酶活力进行测定,结果如图4所示。纤维素降解相关酶活力测定结果表明:与V110相比,4个过表达菌株的FPA、EG、CBH活力均显著提高(P<0.05),BGL没有显著性差异(P>0.05)。OE-V16和OE-V21菌株的FPA、EG、CBH活力提高幅度最大,OE-V3菌株的提高幅度最低。木质素降解相关酶活力测定结果表明:4个过表达菌株的Lac、MnP活力均显著提高(P<0.05),与V110相比,OE-V16和OE-V21菌株的Lac、MnP活力提高幅度最大;OE-V3菌株提高幅度最低。半纤维素降解相关酶活力测定结果表明:4个过表达菌株的HMC、Xyl活力较V110均无显著差异(P>0.05)。这些结果表明,gpx基因的过表达可以提高部分基质降解酶的活力,促进草菇的生长和发育。
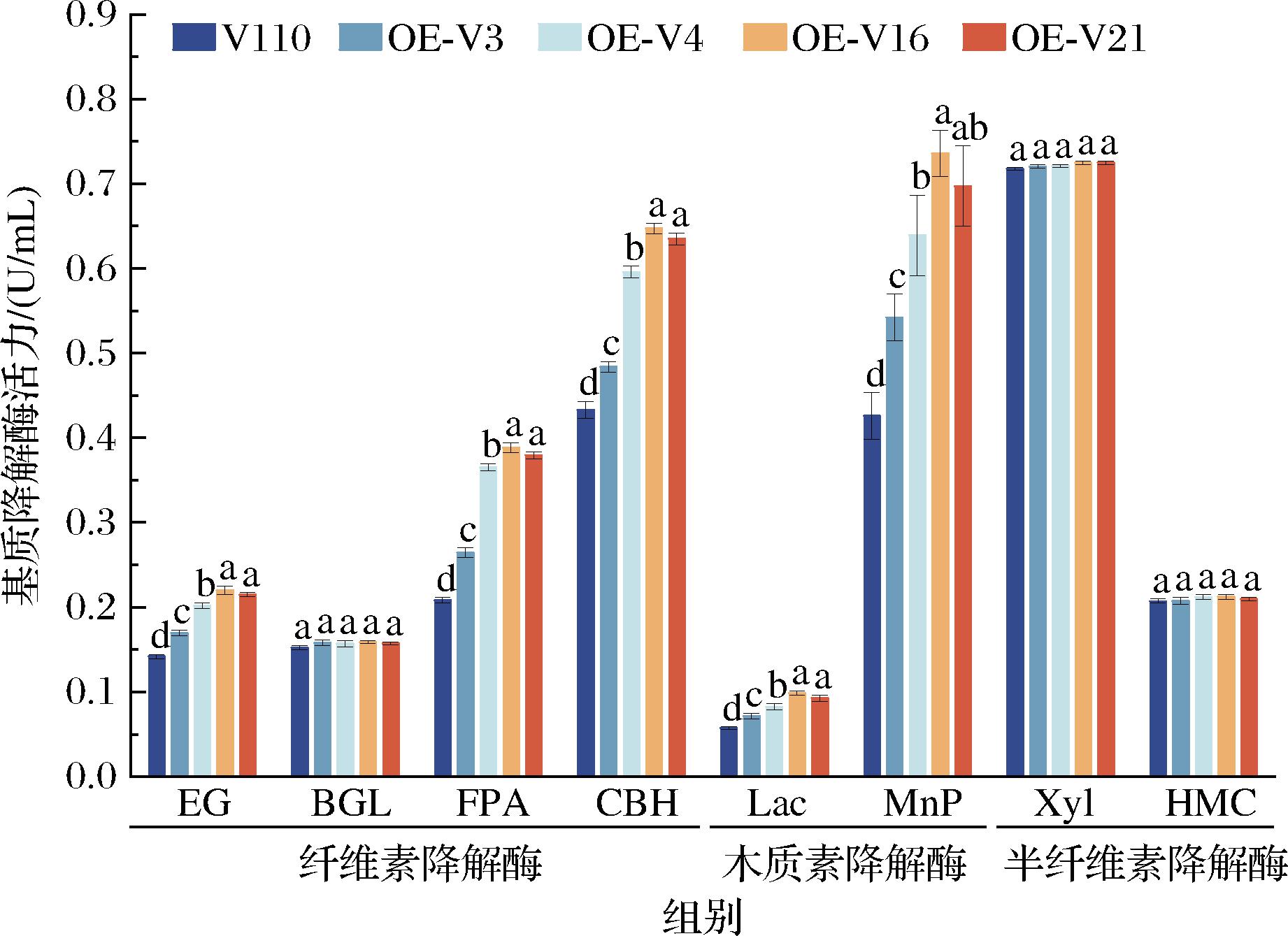
图4 草菇菌株的基质降解酶活力
Fig.4 The matrix degradation enzyme activity of V.volvacea strains
2.5 gpx基因过表达对H2O2胁迫下草菇菌丝生长的影响
在PDA培养基中添加H2O2,对草菇菌丝生长进行测定。在不添加H2O2的培养基中,草菇菌株气生菌丝浓密;在8 mmol/L H2O2胁迫的条件下,所有菌株的生长均受到了一定的抑制,过表达gpx基因菌株表现出更强的抗逆性(图5-a)。
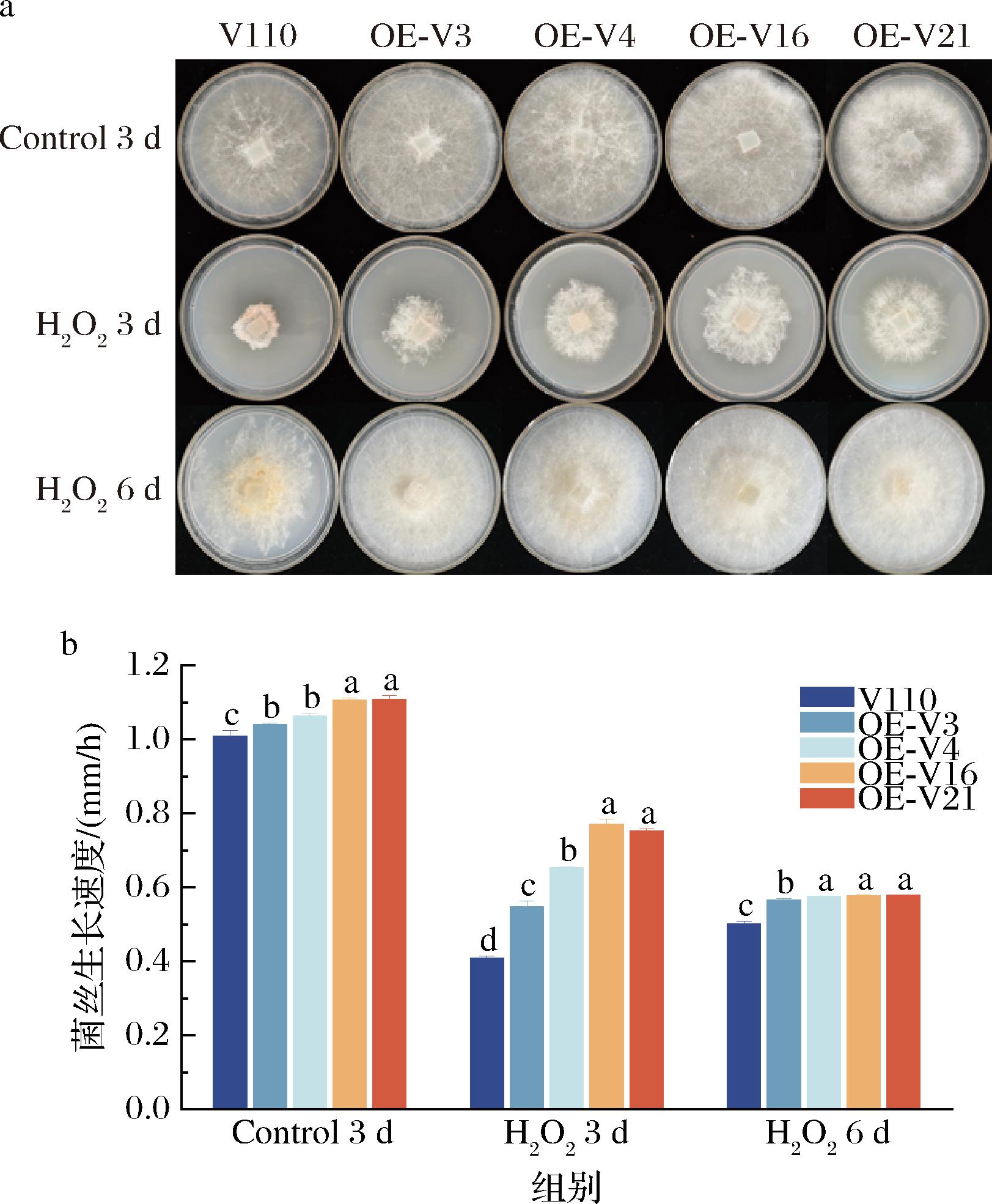
a-菌丝生长;b-菌丝生长速度
图5 草菇菌株在H2O2胁迫下的生长
Fig.5 Growth of V.volvacea strains under H2O2 stress
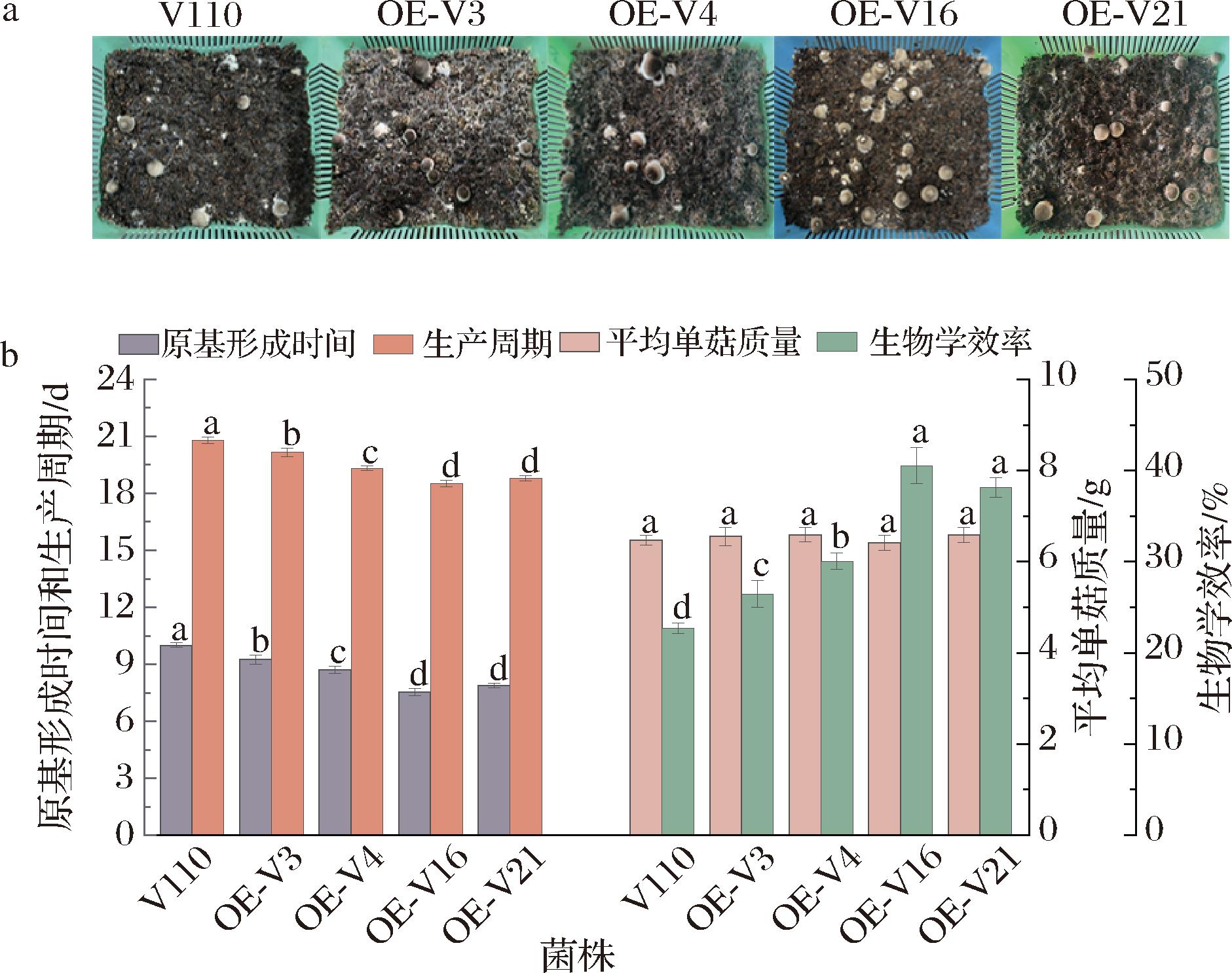
a-栽培实验;b-原基形成时间、平均单菇质量、生产周期和生物学效率
图6 草菇菌株的栽培变化
Fig.6 Cultivation changes of V.volvacea strains
对菌丝生长速度进行测定,结果如图5-b所示。在不添加H2O2的培养基中,与V110相比,OE-V3、OE-V4、OE-V16、OE-V21的第3天菌丝生长速度分别提高了3.02%、5.36%、9.69%和9.78%。在H2O2胁迫条件下,在第3天和第6天时,gpx过表达菌株的菌丝生长速度均高于V110,第3天时,OE-V16和OE-V21菌株的生长速度最快,分别为0.77 mm/h和0.75 mm/h,比V110分别提高了88.36%和83.82%。第6天时,OE-V3、OE-V4、OE-V16、OE-V21菌丝生长速度分别比V110提高了12.81%、14.68%、15.16%和15.42%。这些结果表明提高gpx基因表达量有助于抵抗H2O2介导的氧化应激。
2.6 gpx基因过表达对草菇生产性状的影响
草菇菌株栽培实验结果如图6所示。所有菌株均能长出子实体,与V110相比,过表达菌株的子实体数量呈不同程度的增加,且OE-V16子实体数量最多。对草菇菌株的农艺学性状进行测定,结果表明:相比于V110,过表达菌株OE-V3、OE-V4、OE-V16和OE-V21的原基形成时间和生产周期显著缩短,生物效率显著提高(P<0.05),OE-V16和OE-V21的原基形成时间分别为7.5、7.9 d,生产周期分别为19.29、19.58 d,生物学效率分别为40.56%和35.40%,过表达菌株的平均单菇重较V110没有显著性差异(P>0.05)。这些结果表明gpx基因的过表达对草菇的生产性状有影响。
2.7 相关性分析
对草菇的ROS清除能力和生产性状相关指标进行相关性分析,结果如图7所示,GPX、CAT、SOD、GR的酶活力与GSH、GSSG含量及EG、FPA、CBH、Lac、MnP酶活力呈显著正相关,与![]() 呈显著负相关(P<0.05),EG、FPA、CBH、Lac、MnP酶活力与原基形成时间、生产周期呈显著负相关,与生物学效率呈显著正相关(P<0.05)。
呈显著负相关(P<0.05),EG、FPA、CBH、Lac、MnP酶活力与原基形成时间、生产周期呈显著负相关,与生物学效率呈显著正相关(P<0.05)。
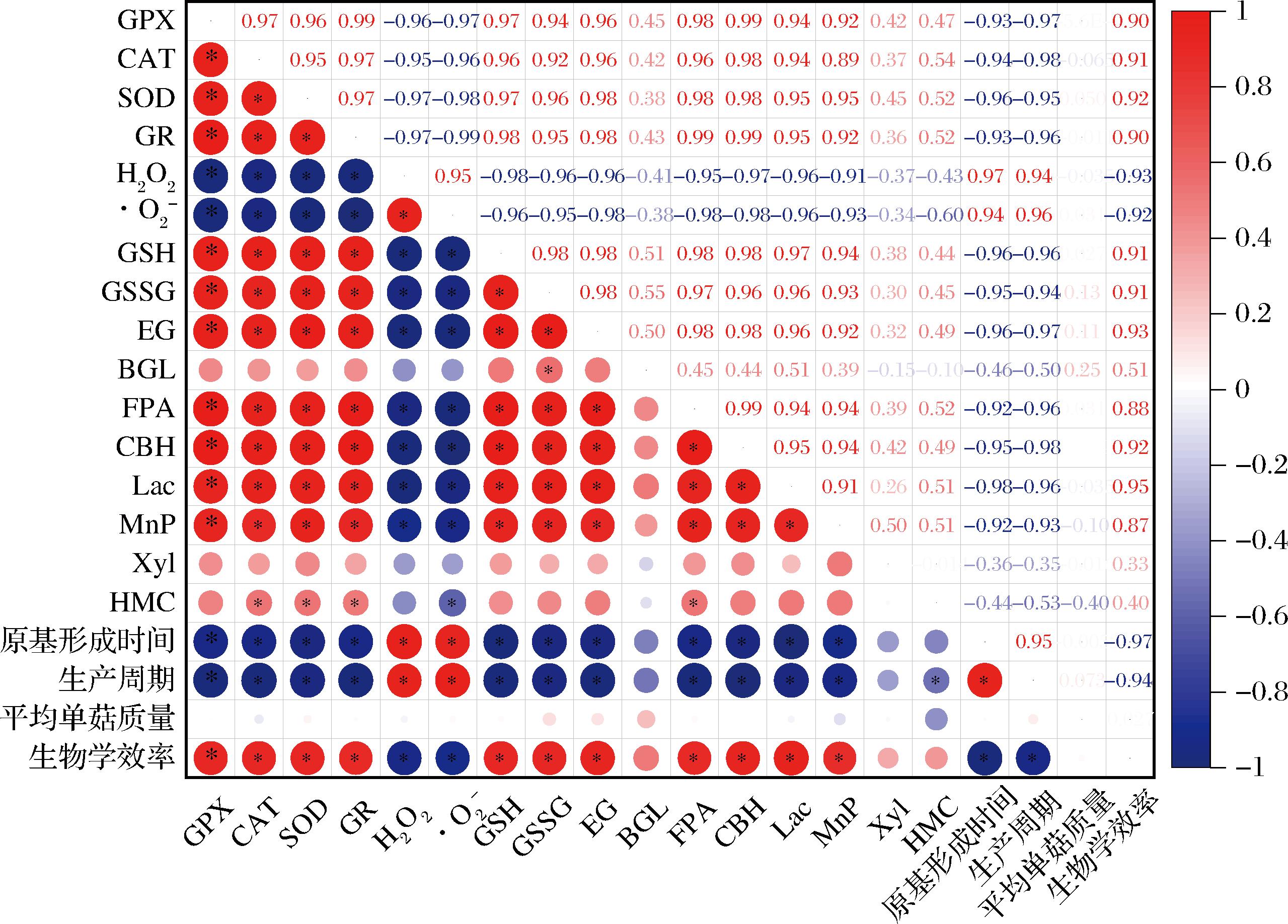
图7 相关性分析
Fig.7 Correlation analysis
3 讨论
我国是草菇生产大国,年产量超过35万t,占世界总产量的70%~80%[20]。与平菇、双孢蘑菇等大宗食用菌相比,草菇生物学效率低的问题严重制约着草菇产业的规模化发展[21]。选育优良高产的菌种是提高草菇产量、扩大产业规模的关键因素之一。目前常见的食用菌育种方法包括单孢分离、诱变育种、原生质体融合等方法[22-23]。传统的育种方法耗时长,工作量大,育种方向性不强。近些年,随着分子生物学的发展,草菇全基因组测序工作的完成,使草菇功能基因的研究越来越受到关注,基因工程育种技术也迅速发展起来。ZHAO等[24]利用PEG介导原生质体转化法将福寿螺的多功能纤维素酶基因(mfc)转入草菇,显著提高了草菇的子实体产量。钟海英等[25]利用RNA干扰法(RNA interference method,RNAi)沉默了生长素合成基因(YUCCA8),显著提高了香菇的菌丝生长速度。本研究表明,通过过表达gpx基因有效提高了草菇的菌丝生长速度、缩短生产周期、增加了子实体产量,表明基因工程育种是一种食用菌优良菌种选育的有效方法。
作为抗氧化酶家族的重要成员,GPX的转录水平和酶活性直接影响真菌的生长发育及应对生物胁迫的能力。LI等[26]发现gpx基因沉默使灵芝中的ROS含量升高,菌丝生长受到抑制。ZHANG等[27]发现gpx缺失会导致真姬菇丧失生成子实体的能力。GPX分解ROS的方法是通过消耗GSH将H2O2转化为无毒的H2O和GSSG,GSSG在GR的作用下以NADPH作为电子供体,快速还原为GSH,在此过程中维持一定的GSH/GSSG水平[28-29]。GSH/GSSG水平可以保证谷胱甘肽循环及抗坏血酸-谷胱甘肽循环的正常运转,防止细胞遭受氧化应激的损伤。KIM等[30]通过在白色念珠菌中添加柚皮苷导致GSH/GSSG水平的失衡,使线粒体产生极端氧化应激,造成菌体凋亡。AYER等[31]发现,在酿酒酵母中,线粒体功能障碍耦合降低了GSH/GSSG比率。本研究发现,gpx基因过表达显著提高了GSH/GSSG值,而且伴随着gpx转录水平的提升和GPX酶活力的增强,过表达菌株中的SOD、CAT、GR等抗氧化酶的活力均得到了提升,这可能是由于GPX降低了菌体内的ROS含量造成的。H2O2氧化胁迫实验也进一步印证了这一结果。
草菇是一种典型的草腐菌,常用废棉、稻草及棉籽壳等富含纤维素、半纤维素和木质素的物质作为栽培基质。这些基质在草菇分泌的酶作用下分解为小分子物质,以供其生长、发育和繁殖所需[32]。半纤维素通过共价键和氢键与木质素分子紧密相连,将纤维素包裹在其中,当木质素被分解后,化学键断裂,纤维素暴露出来,被进一步酶解[33]。在本研究中,gpx基因表达量与FPA、EG、CBH、Lac、MnP酶活力呈正相关。ZHU等[34]发现过表达cat2后,草菇的抗氧化酶活力增加,ROS含量降低,基质降解酶活力和生物学效率也显著提高。GUPTA等[35]发现灵芝的生长、生物量等的变化与漆酶产量呈正相关。胡延如等[36]发现添加一定浓度的磷酸氢二铵可以提高糙皮侧耳的基质降解酶活力,加快其菌丝生长速率。在本研究中,gpx过表达提高了草菇的FPA、EG、CBH、Lac、MnP酶活力。这可能是因为gpx基因过表达显著上调了抗氧化酶相关基因表达量和酶活力,进而增强了草菇菌株的抗氧化能力,降低了ROS含量,使得菌丝活力增强,菌丝分解基质中大分子物质的能力也随之增强。
ROS是需氧型生物在新陈代谢进程中的代谢产物,参与许多细胞分化与发育过程,比如菌丝生长、细胞信号传递、次生代谢物合成等[37]。同时,ROS水平也影响食用菌原基形成[38]和子实体发育[39]。WANG等[40]向草菇培养基中外源添加MnSO4后,有效降低了草菇体内H2O2和![]() 含量,提高了生物学效率;WANG等[41]在草菇中沉默gpx基因,显著提高了细胞内H2O2和
含量,提高了生物学效率;WANG等[41]在草菇中沉默gpx基因,显著提高了细胞内H2O2和![]() 含量,使得gpx沉默菌株不能长出子实体。本研究在商业化草菇菌株V110中过表达gpx基因,使得转化子ROS含量降低,生产周期缩短,生物学效率提高。相关性分析表明,抗氧化酶活力与基质降解酶活力、生物学效率呈显著正相关。说明草菇体内的ROS含量显著影响着其生产性状,具体的调控机制有待于进一步研究。
含量,使得gpx沉默菌株不能长出子实体。本研究在商业化草菇菌株V110中过表达gpx基因,使得转化子ROS含量降低,生产周期缩短,生物学效率提高。相关性分析表明,抗氧化酶活力与基质降解酶活力、生物学效率呈显著正相关。说明草菇体内的ROS含量显著影响着其生产性状,具体的调控机制有待于进一步研究。
草菇是大规模人工栽培的食用菌,菌种质量直接关系到草菇的经济效益,因此草菇的遗传育种工作在产业发展中占据核心地位。在本研究中,gpx在草菇菌株中过表达后,相关抗氧化基因表达上调,抗氧化酶活性提高,ROS积累显著减少,菌丝抵御氧化胁迫的能力增强,部分基质降解酶活力升高;进而促进了草菇菌丝的生长,提高了草菇的生物学效率(图8)。本研究为草菇及其他食用菌在基因工程育种和提高生物学效率提供了一种新的策略。
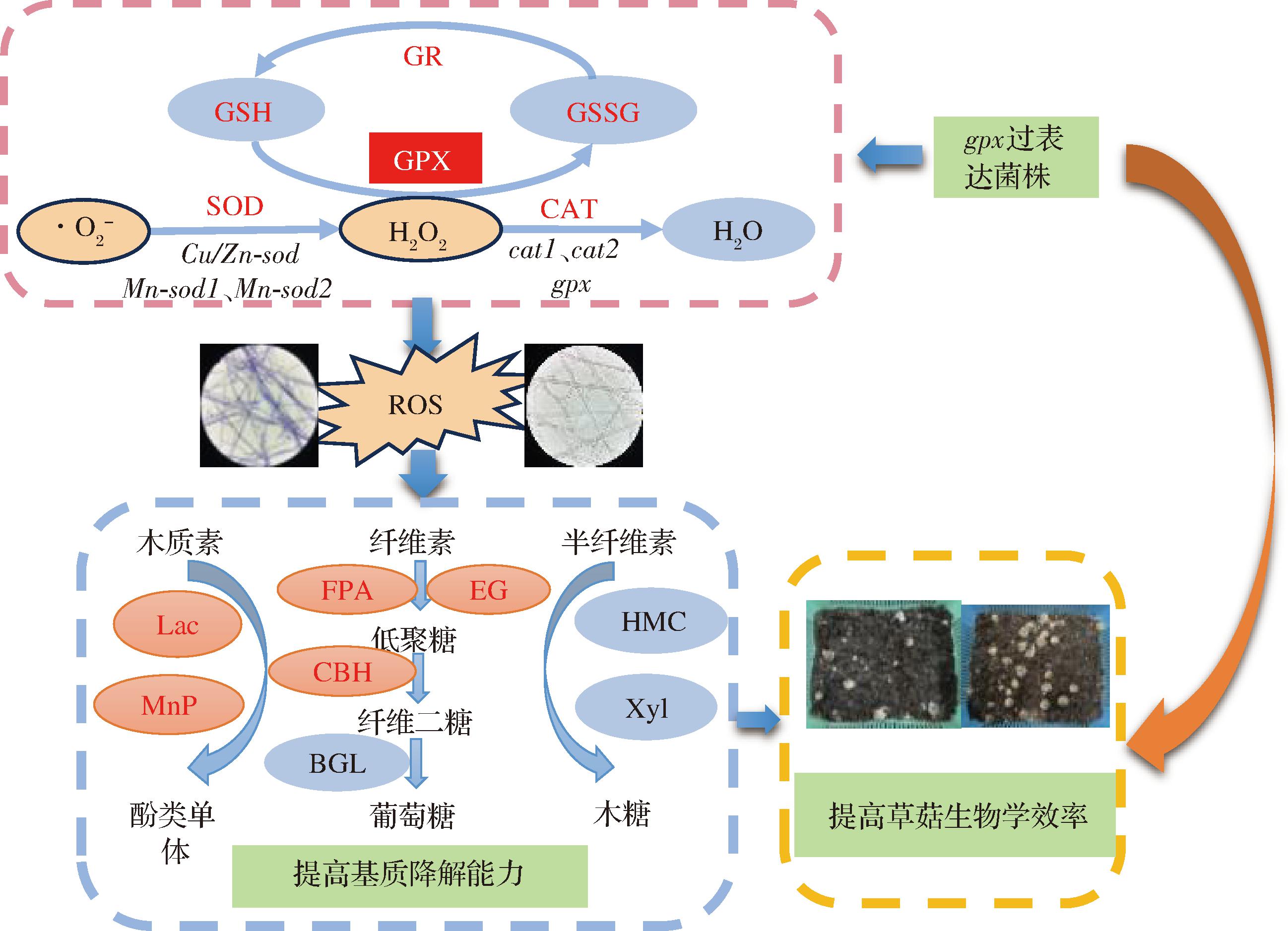
图8 gpx过表达对草菇抗氧化性能和生产能力的影响
Fig.8 Effects of gpx overexpression on antioxidant performance and production capacity of V.volvacea
4 结论
本研究以草菇原始菌株V110及其过表达gpx基因菌株OE-V3、OE-V4、OE-V16和OE-V21为实验材料,对草菇的抗氧化性能、ROS含量、基质降解酶活力和生产性状进行测定。结果表明:4个转化子的Cu/Zn-sod、Mn-sod2、cat1、cat2、gr、gpx的基因相对表达量及SOD、CAT、GR、GPX酶活力均显著提高,Mnsod1基因的相对表达量变化不显著;GSH、GSSG含量及GSH/GSSG值均显著高于V110,ROS含量低于V110;纤维素降解相关酶、木质素降解相关酶活力显著提高,半纤维素降解相关酶活力差异不显著;gpx基因过表达提高了草菇在H2O2胁迫下的菌丝生长速度;栽培实验表明,4个转化子的生产周期缩短、生物学效率显著提高,平均单菇重差异不显著。本研究表明gpx基因过表达是提高草菇生物学效率的一种有效策略。
[1] LI H B,HE Z X,JIANG Y Z,et al.Bioconversion of bamboo shoot shells through the cultivation of the edible mushrooms Volvariella volvacea[J].Ecotoxicology,2021,30(7):1476-1486.
[2] 戴玉成,杨祝良.中国药用真菌名录及部分名称的修订[J].菌物学报,2008,27(6):801-824.DAI Y C,YANG Z L.A revised checklist of medicinal fungi in China[J].Mycosystema,2008,27(6):801-824.
[3] KISHIDA E,KINOSHITA C,SANE Y,et al.Structures and antitumor activities of polysaccharides isolated from Mycelium of Volvariella volvacea[J].Bioscience,Biotechnology,and Biochemistry,1992,56(8):1308-1309.
[4] 丁少军,宋美静,池杏微,等.不同碳源条件下草菇内切型纤维素酶基因(eg1)转录表达的分析[J].应用与环境生物学报,2005,11(4):419-422.DING S J,SONG M J,CHI X W,et al.Transcriptional analysis of eg1 expression of Volvariella volvacea growth and development in media with different carbon sources[J].Chinese Journal of Applied and Environmental Biology,2005,11(4):419-422.
[5] 朱巍巍.糙皮侧耳继代培养稳定性及子实体分化调控研究[D].大连:大连理工大学,2020.ZHU W W,Subculture stability of Pleurotus ostretus and regulation of fruiting body differentiation[D].Dalian:Dalian University of Technology,2020.
[6] 怀美玉,刘晴,徐方旭,等.蛹虫草菌株退化特征及鉴别方法[J].菌物学报,2022,41(11):1819-1830.HUAI M Y,LIU Q,XU F X,et al.Characteristics and identification of Cordyceps militaris strain degeneration[J].Mycosystema,2022,41(11):1819-1830.
[7] MARGIS R,DUNAND C,TEIXEIRA F K,et al.Glutathione peroxidase family-an evolutionary overview[J].The FEBS Journal,2008,275(15):3959-3970.
[8] AKTAR K,KAFI A,DAHIYA R.Association of Gpx1 fluctuation in cell cycle progression[J].In Vitro Cellular &Developmental Biology-Animal,2019,55(2):94-103.
[9] AHWACH S M,THOMAS M,ONSTEAD-HAAS L,et al.The glutathione mimic ebselen inhibits oxidative stress but not endoplasmic reticulum stress in endothelial cells[J].Life Sciences,2015,134:9-15.
[10] ZHAO F Y,WANG Q L,AN X M,et al.Oxidative damage from repeated tissue isolation for subculturing causes degeneration in Volvariella volvacea[J].Frontiers in Microbiology,2023,14:1210496.
[11] XIONG C H,XIA Y L,ZHENG P,et al.Increasing oxidative stress tolerance and subculturing stability of Cordyceps militaris by overexpression of a glutathione peroxidase gene[J].Applied Microbiology and Biotechnology,2013,97(5):2009-2015.
[12] 赵光辉,陈剑,郑铃,等.草菇菌株比较试验[J].食用菌,2016,38(5):25-26.ZHAO G H,CHEN J,ZHENG L,et al.Volvariella volvacea strain comparison test[J].Edible Fungi,2016,38(5):25-26.
[13] 王文沛,谭强飞,程志虹,等.草菇不同菌株RT-qPCR参考基因筛选[J].菌物学报,2022,41(5):749-758.WANG W P,TAN Q F,CHENG Z H,et al.Selection of optimal RT-qPCR reference genes for examining different strains of Volvariella volvacea[J].Mycosystema,2022,41(5):749-758.
[14] WANG M Y,XU H,LIU C J,et al.Peroxisome proliferator FpPEX11 is involved in the development and pathogenicity in Fusarium pseudograminearum[J].International Journal of Molecular Sciences,2022,23(20):12184.
[15] ZHAO Y,LIU S J,ZHA L,et al.Influence of cellulase gene expression and cellulolytic activity on cellulose utilization in different Volvariella volvacea strains[J].Scientia Horticulturae,2020,261:108956.
[16] ZHAO F Y,LIU X X,CHEN C,et al.Successive mycelial subculturing decreased lignocellulase activity and increased ROS accumulation in Volvariella volvacea[J].Frontiers in Microbiology,2022,13:997485.
[17] DOS SANTOS T C,DOS SANTOS REIS N,SILVA T P,et al.Production,optimisation and partial characterisation of enzymes from filamentous fungi using dried forage cactus pear as substrate[J].Waste and Biomass Valorization,2018,9(4):571-579.
[18] YANG Y Y,XIE B,JING Z H,et al.Flammulina filiformis pkac gene complementing in Neurospora crassa mutant reveals its function in mycelial growth and abiotic stress response[J].Life,2022,12(9):1336.
[19] 张勇,田小霞,郑明利,等.过表达长穗偃麦草EeHKT1;4基因增强拟南芥抗旱耐盐性分析[J].草业学报,2022,31(8):188-198.ZHANG Y,TIAN X X,ZHENG M L,et al.Analysis of drought and salt resistance of EeHKT1;4 gene from Elytrigia elongata in Arabidopsis[J].Acta Prataculturae Sinica,2022,31(8):188-198.
[20] BAO D P,GONG M,ZHENG H J,et al.Sequencing and comparative analysis of the straw mushroom (Volvariella volvacea) genome[J].PLoS One,2013,8(3):e58294.
[21] 谷凤举,赖亮民,杜敏如,等.航天诱变处理对草菇生物学特性的影响[J].北方园艺,2022(17):112-120.GU F J,LAI L M,DU M R,et al.Effects of space mutagenesis on biological characteristics of Volvariella volvacea[J].Northern Horticulture,2022(17):112-120.
[22] 刘昆昂,刘萌,张根伟,等.金针菇遗传育种研究进展[J].江苏农业科学,2019,47(14):18-22.LIU K A,LIU M,ZHANG G W,et al.Research progress on genetic breeding of Flammulina velutipes[J].Jiangsu Agricultural Sciences,2019,47(14):18-22.
[23] 宋冬灵,曾宪贤,吕杰,等.金针菇遗传育种研究进展[J].种子,2007,26(5):52-54.SONG D L,ZENG X X,LYU J,et al.Progress of study on genetic and breeding of Flammulina Velutipes[J].Seed,2007,26(5):52-54.
[24] ZHAO F Y,LIN J F,ZENG X L,et al.Improvement in fruiting body yield by introduction of the Ampullaria crossean multi-functional cellulase gene into Volvariella volvacea[J].Bioresource Technology,2010,101(16):6482-6486.
[25] 钟海英,罗义,龚钰华,等.RNAi法分析香菇YUCCA8基因的功能[J].食用菌学报,2021,28(3):11-18.ZHONG H Y,LUO Y,GONG Y H,et al.Functional analysis of indole-3-pyruvate monooxygenase gene YUCCA8 involved in heat resistance of Lentinula edodes by RNAi[J].Acta Edulis Fungi,2021,28(3):11-18.
[26] LI C Y,SHI L,CHEN D D,et al.Functional analysis of the role of glutathione peroxidase (GPx) in the ROS signaling pathway,hyphal branching and the regulation of ganoderic acid biosynthesis in Ganoderma lucidum[J].Fungal Genetics and Biology,2015,82:168-180.
[27] ZHANG J J,HAO H B,WU X L,et al.The functions of glutathione peroxidase in ROS homeostasis and fruiting body development in Hypsizygus marmoreus[J].Applied Microbiology and Biotechnology,2020,104(24):10555-10570.
[28] LIU T,SUN L,ZHANG Y B,et al.Imbalanced GSH/ROS and sequential cell death[J].Journal of Biochemical and Molecular Toxicology,2022,36(1):e22942.
[29] PANDAY S,TALREJA R,KAVDIA M.The role of glutathione and glutathione peroxidase in regulating cellular level of reactive oxygen and nitrogen species[J].Microvascular Research,2020,131:104010.
[30] KIM H,GUN L.Naringin-generated ROS promotes mitochondria-mediated apoptosis in Candida albicans[J].IUBMB Life,2021,73(7):953-967.
[31] AYER A,GOURLAY C W,DAWES I W.Cellular redox homeostasis,reactive oxygen species and replicative ageing in Saccharomyces cerevisiae[J].FEMS Yeast Research,2014,14(1):60-72.
[32] 程志虹,王文沛,谭强飞,等.外源甘露醇复壮草菇退化菌株的研究[J].食品与发酵工业,2022,48(11):30-35.CHENG Z H,WANG W P,TAN Q F,et al.Degraded strains of Volvariella volvacea rejuvenated by exogenous mannitol[J].Food and Fermentation Industries,2022,48(11):30-35.
[33] ZHANG S T,XIAO J L,WANG G,et al.Enzymatic hydrolysis of lignin by ligninolytic enzymes and analysis of the hydrolyzed lignin products[J].Bioresource Technology,2020,304:122975.
[34] ZHU J N,WANG W P,SUN W H,et al.Overexpression of cat2 restores antioxidant properties and production traits in degenerated strains of Volvariella volvacea[J].Free Radical Biology and Medicine,2024,215:94-105.
[35] GUPTA A,JANA A K.Effects of wheat straw solid contents in fermentation media on utilization of soluble/insoluble nutrient,fungal growth and laccase production[J].3 Biotech,2018,8(1):35.
[36] 胡延如,柴茜茜,董浩哲,等.磷酸氢二铵对糙皮侧耳菌丝生长及基质降解酶活性的影响[J].菌物学报,2022,41(4):658-667.HU Y R,CHAI Q Q,DONG H Z,et al.Effects of different concentrations of ammonium phosphate on mycelial growth and enzyme activities related to substrate degradation of Pleurotus ostreatus[J].Mycosystema,2022,41(4):658-667.
[37] KHAN M,ALI S,AL AZZAWI T N I,et al.The key roles of ROS and RNS as a signaling molecule in plant-microbe interactions[J].Antioxidants,2023,12(2):268.
[38] DIAMANTOPOULOU P,PAPANIKOLAOU S,KATSAROU E,et al.Mushroom polysaccharides and lipids synthesized in liquid agitated and static cultures.Part II:Study of Volvariella volvacea[J].Applied Biochemistry and Biotechnology,2012,167(7):1890-1906.
[39] MAGAE Y,AKAHANE K,NAKAMURA K,et al.Simple colorimetric method for detecting degenerate strains of the cultivated basidiomycete Flammulina velutipes (Enokitake)[J].Applied and Environmental Microbiology,2005,71(10):6388-6389.
[40] WANG Q L,WANG W P,WANG Y H,et al.Exogenous MnSO4 improves productivity of degenerated Volvariella volvacea by regulating antioxidant activity[J].Journal of Fungi,2024,10(12):825.
[41] WANG W P,TAN Q F,WANG Q L,et al.Glutathione peroxidase gene regulates substrate development and prevents strain aging in Volvariella volvacea[J].International Journal of Biological Macromolecules,2025,289:138835.