在食品行业中,β-葡萄糖苷酶(β-glucosidases,BGL)能够有效水解苦杏仁苷、异黄酮等糖苷类化合物,释放出具有独特功能的单体成分,可以有效改善食品风味[1];在医药行业中,可将大分子糖苷大豆异黄酮、人参皂苷分解为小分子活性成分,提高其在人体内的吸收和利用效率,将植物中的白藜芦醇苷水解为高药用价值的白藜芦醇,用于药用活性化合物的制备[2];更为重要的是,BGL是分解纤维素的关键限速酶,对提高纤维素的糖化率、推进新一代工业发酵用碳源-秸秆糖的产业化进程具有重要作用。黑曲霉(Aspergillus niger)是BGL的主要生产者[3],使用生物技术提升黑曲霉的产酶性能,将有助于推进BGL在食品、医药、生物能源和生物化工等领域中的广泛应用。
高效原生质体的制备、转化、再生是建立非模式黑曲霉遗传转化体系与基因编辑技术的关键,但不同来源的黑曲霉在这些方面存在显著差异。ZHENG等[4]制备黑曲霉CBS513.88的原生质体所使用的是单一的溶壁酶,LIU等[5]报道制备黑曲霉N1原生质体时,又需要附加溶菌酶、蜗牛酶、几丁质酶才能获得大量原生质体;本团队以自主筛选出的具有较强BGL生产能力的野生黑曲霉An-1为对象,研究发现使用常规的聚乙二醇(polyethylene glycol,PEG)-原生质体转化方法,无法将操作质粒引入到该菌株中。因此,建立针对非模式黑曲霉菌株An-1稳定的遗传转化体系至关重要。与此同时,随着基因编辑技术的快速发展,利用分子生物学手段选育高产木聚糖酶、海藻糖酶和BGL等酶制剂的黑曲霉菌株成为研究热点。例如,LI等[6]利用基因组编辑将xynA定点整合表达在黑曲霉AG11的基因组上,使木聚糖酶活力提高到1 460 U/mL;DONG等[7]在黑曲霉HL-1通过多拷贝表达TreM,相应转化子的海藻糖酶活力最高可达1 943.06 U/mL;CAI等[8]在黑曲霉ZJUBE-1中利用强启动子Pgpd分别过表达了同源的BGL1和BGL2,纯酶的比酶活力为20 U/mg;WANG等[9]在黑曲霉ATCC 20611中利用其自身启动子PfopA过表达了bglA基因,使酶活力达到17.84 U/mL。本团队自主筛选高产BGL酶活力的黑曲霉菌株An-1,通过测序发现该菌株含有11条BGL相关基因[10],但关键BGL基因筛选和高效过表达的相关研究尚未见报道。
为了有效改造黑曲霉An-1,提升其产BGL活力,本研究拟通过优化原生质体的制备条件与再生方法,建立稳定的非模式黑曲霉An-1遗传转化体系;以表达红色荧光蛋白作为报告基因,建立BGL表达盒,筛选出野生黑曲霉An-1的关键BGL基因;构建非模式黑曲霉An-1基因编辑体系,并期望实现关键BGL基因的高效表达,为分子改造非模式黑曲霉An-1、实现BGL的高效生产奠定了科学基础。
1 材料与方法
1.1 材料
1.1.1 菌种
本研究的黑曲霉菌株An-1为实验室筛选,保存于中国典型培养物保藏中心,保藏编号为CCTCC NO:M2024768;大肠杆菌DH5α,南京诺唯赞生物科技有限公司;pFC332质粒,湖南丰晖生物科技有限公司;pUC-sgRNA和puc-mCherry,南京金唯智生物科技有限公司;引物由上海生工生物工程有限公司合成,序列见表1。
表1 本研究所用引物
Table 1 Primers used in this study
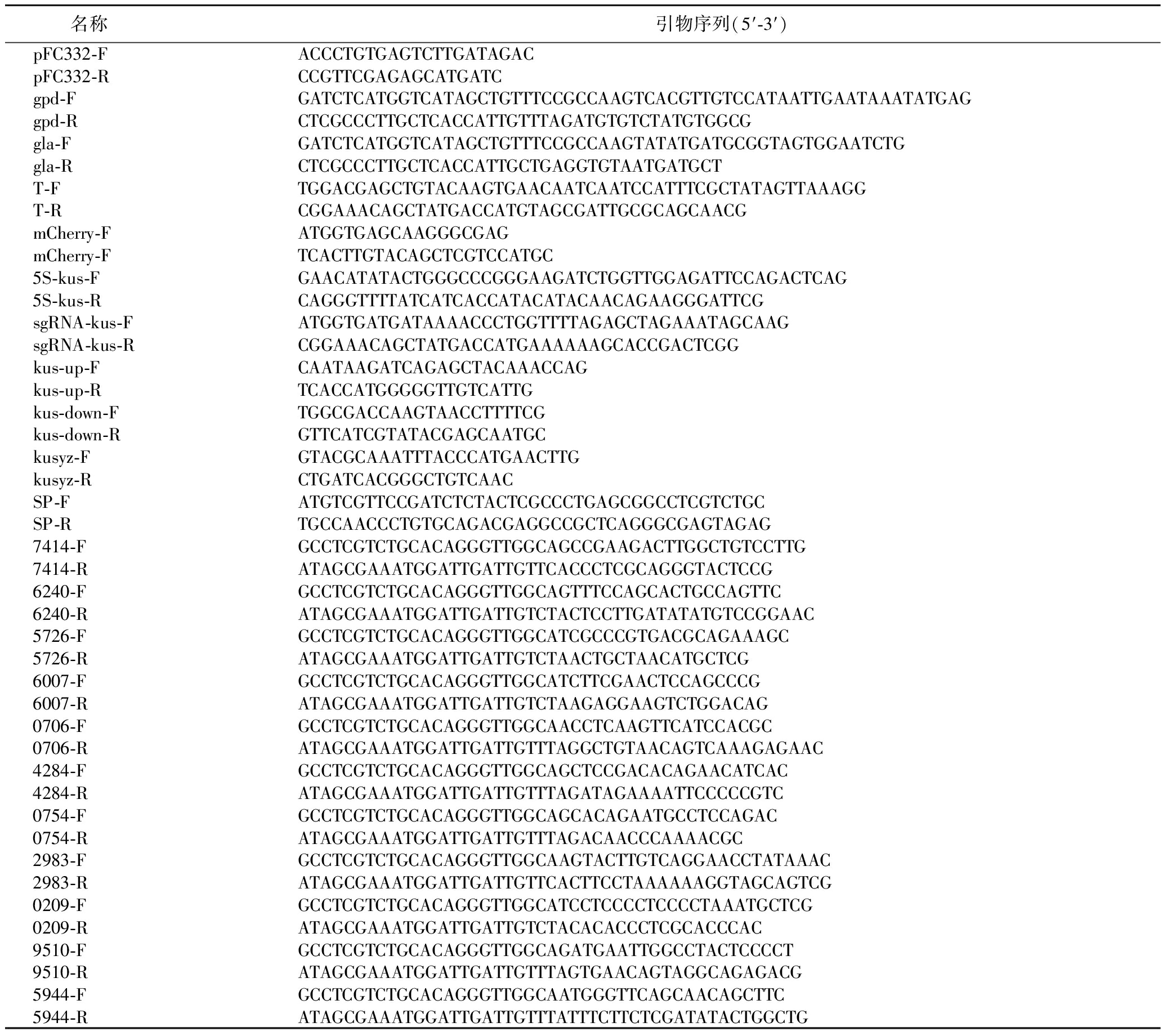
名称 引物序列(5′-3′)pFC332-FACCCTGTGAGTCTTGATAGACpFC332-RCCGTTCGAGAGCATGATCgpd-FGATCTCATGGTCATAGCTGTTTCCGCCAAGTCACGTTGTCCATAATTGAATAAATATGAGgpd-RCTCGCCCTTGCTCACCATTGTTTAGATGTGTCTATGTGGCGgla-FGATCTCATGGTCATAGCTGTTTCCGCCAAGTATATGATGCGGTAGTGGAATCTGgla-RCTCGCCCTTGCTCACCATTGCTGAGGTGTAATGATGCTT-FTGGACGAGCTGTACAAGTGAACAATCAATCCATTTCGCTATAGTTAAAGGT-RCGGAAACAGCTATGACCATGTAGCGATTGCGCAGCAACGmCherry-FATGGTGAGCAAGGGCGAGmCherry-FTCACTTGTACAGCTCGTCCATGC5S-kus-FGAACATATACTGGGCCCGGGAAGATCTGGTTGGAGATTCCAGACTCAG5S-kus-RCAGGGTTTTATCATCACCATACATACAACAGAAGGGATTCGsgRNA-kus-FATGGTGATGATAAAACCCTGGTTTTAGAGCTAGAAATAGCAAGsgRNA-kus-RCGGAAACAGCTATGACCATGAAAAAAGCACCGACTCGGkus-up-FCAATAAGATCAGAGCTACAAACCAGkus-up-RTCACCATGGGGGTTGTCATTGkus-down-FTGGCGACCAAGTAACCTTTTCGkus-down-RGTTCATCGTATACGAGCAATGCkusyz-FGTACGCAAATTTACCCATGAACTTGkusyz-RCTGATCACGGGCTGTCAACSP-FATGTCGTTCCGATCTCTACTCGCCCTGAGCGGCCTCGTCTGCSP-RTGCCAACCCTGTGCAGACGAGGCCGCTCAGGGCGAGTAGAG7414-FGCCTCGTCTGCACAGGGTTGGCAGCCGAAGACTTGGCTGTCCTTG7414-RATAGCGAAATGGATTGATTGTTCACCCTCGCAGGGTACTCCG6240-FGCCTCGTCTGCACAGGGTTGGCAGTTTCCAGCACTGCCAGTTC6240-RATAGCGAAATGGATTGATTGTCTACTCCTTGATATATGTCCGGAAC5726-FGCCTCGTCTGCACAGGGTTGGCATCGCCCGTGACGCAGAAAGC5726-RATAGCGAAATGGATTGATTGTCTAACTGCTAACATGCTCG6007-FGCCTCGTCTGCACAGGGTTGGCATCTTCGAACTCCAGCCCG6007-RATAGCGAAATGGATTGATTGTCTAAGAGGAAGTCTGGACAG0706-FGCCTCGTCTGCACAGGGTTGGCAACCTCAAGTTCATCCACGC0706-RATAGCGAAATGGATTGATTGTTTAGGCTGTAACAGTCAAAGAGAAC4284-FGCCTCGTCTGCACAGGGTTGGCAGCTCCGACACAGAACATCAC4284-RATAGCGAAATGGATTGATTGTTTAGATAGAAAATTCCCCCGTC0754-FGCCTCGTCTGCACAGGGTTGGCAGCACAGAATGCCTCCAGAC0754-RATAGCGAAATGGATTGATTGTTTAGACAACCCAAAACGC2983-FGCCTCGTCTGCACAGGGTTGGCAAGTACTTGTCAGGAACCTATAAAC2983-RATAGCGAAATGGATTGATTGTTCACTTCCTAAAAAAGGTAGCAGTCG0209-FGCCTCGTCTGCACAGGGTTGGCATCCTCCCCTCCCCTAAATGCTCG0209-RATAGCGAAATGGATTGATTGTCTACACACCCTCGCACCCAC9510-FGCCTCGTCTGCACAGGGTTGGCAGATGAATTGGCCTACTCCCCT9510-RATAGCGAAATGGATTGATTGTTTAGTGAACAGTAGGCAGAGACG5944-FGCCTCGTCTGCACAGGGTTGGCAATGGGTTCAGCAACAGCTTC5944-RATAGCGAAATGGATTGATTGTTTATTTCTTCTCGATATACTGGCTG
1.1.2 试剂
限制性内切核酸酶BglⅡ,北京NEB公司;质粒提取试剂盒、PCR产物纯化试剂盒、2×Rapid Taq Master Mix、2×Phanta Max Master Mix (Dye Plus)、DL5000 DNA Marker、Ultra Gel Red (10 000×),南京诺唯赞公司;琼脂糖凝胶,上海生工生物工程有限公司;50×(Tris-acetate-EDTA),碧云天生物公司;无缝克隆试剂盒,上海都友生物公司;基因组提取试剂盒、潮霉素、溶壁酶、蜗牛酶和溶菌酶,北京索莱宝有限公司;纤维素酶,麦克林有限公司。
TC(Tris calcium)缓冲溶液:5.5 g/L CaCl2,1.2 g/L Tris,定容到1 L。
STC(sorbitol Tris calcium)缓冲溶液:242.3 g D-山梨醇,TC缓冲液定容到1 L。
50%(质量分数)PEG缓冲溶液:5 g PEG-6000,TC缓冲液定容到10 mL。
1.1.3 培养基
PDA培养基(g/L):200马铃薯,20葡萄糖。用于转化子筛选时加入潮霉素B,终质量浓度为300 μg/mL。
CD(chemically defined)高渗固态培养基(g/L):3 NaNO3,2 KCl,0.5 MgSO4·7H2O,1 K2HPO4·3H2O,0.01 FeSO4·7H2O,342 蔗糖,pH 5.5。上层、下层培养基分别加入10 g/L、20 g/L琼脂粉。
生长培养基(g/L):6酵母浸粉,3蛋白胨,20葡萄糖,0.5 KH2PO4,0.5 (NH4)2SO4,1 MgSO4·7H2O。
LB培养基(g/L):10 NaCl,10蛋白胨,5酵母浸粉,自然pH。
1.2 仪器与设备
ZQLY-180V生化培养箱、ZQZY-78BV恒温培养摇床,上海知楚仪器有限公司;MX-307高速冷冻离心机,日本TOMY有限公司;AZY1603149紫外可见分光光度计,日本岛津有限公司;PSH-3E雷磁精密pH计,上海图新电子科技有限公司;ICX41-EX31-OD4000UHW10荧光倒置显微镜,宁波舜宇仪器有限公司。
1.3 实验方法
1.3.1 黑曲霉菌丝体的培养
将黑曲霉接种于PDA固体平板上,28 ℃倒置培养4 d,用0.9%(质量分数)NaCl溶液制作孢子悬液。
液体培养菌丝体:利用血球计数板计数,取约1×107个孢子接种量接种于生长培养基,28 ℃、200 r/min振荡培养16~18 h,经无菌滤袋过滤、生理盐水洗涤,获得菌丝体。
固体培养菌丝体:取100 μL黑曲霉孢子悬液均匀涂布在铺有玻璃纸铺在PDA培养基平板上,于28 ℃培养箱培养16~18 h,此时菌丝体附着于玻璃纸上。
1.3.2 高效稳定的非模式黑曲霉菌株An-1遗传操作体系的构建
1.3.2.1 原生质体的制备及条件优化
称取0.25 g摇瓶培养的菌丝体,分别加入10 mL的单一裂解酶(2%溶壁酶,质量分数)和复合酶液(1%纤维素酶+0.5%蜗牛酶+0.25%溶菌酶,质量分数),于37 ℃酶解2 h,记录酶解液中的菌体形态变化,并取适量酶解液置于显微镜下,观察原生质体的释放情况,探究不同酶解液对制备黑曲霉原生质体的影响。
采用上述方法,使用10 mL的复合酶液处理摇瓶培养所获菌丝体。对于固体平板所培养的菌丝体,使用无菌镊子将附有菌丝体的玻璃纸,置于含有10 mL复合酶液的无菌培养皿中酶解处理2 h。取适量酶解液置于显微镜下,观察原生质体的释放情况,探究不同菌丝体对制备黑曲霉原生质体的影响。
将固体培养菌丝置于10 mL复合酶液中,分别处理1.5、2.0、2.5、3.0 h,取适量酶解液置于显微镜下,观察原生质体的释放情况,探究酶解时间对制备黑曲霉原生质体的影响。
菌丝体在经过酶解处理后,使用尼龙布过滤酶解液,从菌丝体中分离出原生质体,滤液经5 000 r/min,离心10 min,获得沉淀,并使用STC缓冲溶液洗涤2次后进行悬浮,得到用于转化的原生质体。
1.3.2.2 PEG介导的原生质体转化
取100 μL原生质体,加入3 μg质粒,混合均匀,冰浴20 min。加等体积的50%(质量分数)PEG缓冲溶液,混合均匀后,置于25 ℃下,孵育20 min。
1.3.2.3 原生质体的固体与液体再生
原生质体的固体再生:在转化体系中,加入4 mL CD上层软琼脂培养基,混合均匀后,铺板于含300 μg/mL潮霉素的CD下层培养基上,28 ℃培养3~5 d,观察转化子的生长情况。
原生质体的液体再生:在转化体系中,加入2 mL的STC缓冲液,混合均匀,置于28 ℃静置孵育4 h后,5 000 r/min,离心10 min,弃上清液,使用残留液体悬浮菌体沉淀,均匀涂布于含300 μg/mL潮霉素的CD培养基上,28 ℃培养3~5 d,观察转化子的生长情况。
1.3.2.4 菌丝破碎方法、转化子的筛选及验证方法优化
待抗生素CD平板上长出单菌落后,挑取转化子接种于含有300 μg/mL潮霉素的PDA固体平板上,28 ℃培养2~3 d,分离并筛选出抗性转化子。挑取菌丝,分别采用以下方法破菌,使用pFC332-F/R进行菌丝PCR验证。
热处理破菌:挑取适量菌丝于50 μL的TE缓冲液中,混匀后95 ℃加热10 min,裂解液于12 000 r/min离心10 min后,取2 μL上清液作模板。
超声破菌:挑取适量菌丝于50 μL的Tris-EDTA(TE)缓冲液中,混匀后置于超声清洗仪中处理10 min,裂解液离心后,取上清液作模板。
热处理+超声组合破菌:按上述方法先热处理10 min,接着置于超声下处理10 min,裂解液离心后,取上清液作模板。
碱裂解破菌:挑取适量菌丝于含有45 μL 2 mol/L NaOH溶液的离心管中,混匀后95 ℃加热10 min,待冷却后加入5 μL 2 mol/L Tris-HCl溶液,裂解液离心后,取上清液作模板。
1.3.3 高效的非模式黑曲霉菌株An-1基因编辑体系的构建与BGL关键基因的过表达、筛选
1.3.3.1 红色荧光蛋白和黑曲霉An-01的11条BGL的表达
以黑曲霉An-1基因组为模版,分别以gpd-F/R、gla-F/R和T-F/R为引物,扩增启动子Pgpd、启动子Pgla和终止子Tgla片段。以puc-mCherry质粒为模板,mCherry-F/R为引物,扩增红色荧光蛋白mCherry片段,对PCR产物进行纯化回收。经融合PCR,分别组装Pgpd-mCherry-Tgla与Pgla-mCherry-Tgla荧光表达盒。使用BglⅡ酶切处理pFC332质粒,经无缝克隆,将Pgpd-mCherry-Tgla与Pgla-mCherry-Tgla荧光表达盒整合至pFC332线性化载体。挑取多个转化子,使用pFC332-F与T-R进行菌液PCR验证,经琼脂糖凝胶电泳,将片段大小正确的表达质粒,送至生工生物公司测序检测。将构建成功的红色荧光表达质粒,按上述方法进行原生质体转化,导入至黑曲霉中,经筛选、验证得到黑曲霉红色荧光蛋白表达菌株。进一步使用荧光倒置显微镜,在绿色荧光激发下,观察黑曲霉转化子菌丝中的荧光强度,用于判断基因的过表达强度。
按照红色荧光蛋白表达载体的构建方法,经融合PCR组装完成各个BGL基因过表达盒子Pgpd-SP-bgl-Tgla,再整合至pFC332载体上,将所构建的载体转化至黑曲霉中An-1中,实现各个BGL在黑曲霉中的过表达。
1.3.3.2 CRISPR-Cas9靶向质粒及供体片段的构建
使用CHOPCHOP(http://chopchop.cbu.uib.no/)在线设计kusA基因的靶位点,将靶位点设计进5S-kus-R和sgRNA-kus-F中。以黑曲霉基因组为模板,5S-kus-F/R扩增携带靶位点的5S rRNA启动子片段,以puc-sgRNA质粒为模版,sgRNA-kus-F/R为引物扩增携带靶位点的sgRNA,PCR产物进行纯化回收。5S rRNA和sgRNA片段按1∶1的摩尔比进行融合PCR扩增,获得5S rRNA-kusA-sgRNA表达盒。使用BglⅡ酶切处理pFC332质粒,经无缝克隆,将5S rRNA-kusA-sgRNA表达盒整合至pFC332线性化载体。挑取多个转化子,使用pFC332-F/R进行菌液PCR验证,经琼脂糖凝胶电泳,将片段大小正确的Cas9与sgRNA共表达质粒pFC332-Cas9-sgRNA,送至生工生物公司测序检测。对于敲除供体片段的构建,以黑曲霉基因组为模板,kus-up-F/R和kus-down-F/R为引物,扩增靶位点附近的kusA基因上下游片段。经融合PCR,以kus-up-F和kus-down-R为引物将上下游片段融合为供体片段。将PCR产物通过醋酸钠-乙醇沉淀法纯化回收。
按照上述方法,分别构建用于敲除与过表达HQM9510的靶向质粒与供体片段。
1.3.3.3 基因编辑菌株的构建、BGL基因的过表达及筛选
采用上述的原生质体转化方法,100 μL转化体系中加入3 μg pFC332-Cas9-sgRNA质粒和3 μg供体片段,转化体系在液体再生后,均匀涂布于含300 μg/mL潮霉素的CD培养基上,28 ℃培养3~5 d。
待转化子长出后,在抗性PDA平板上进行分离筛选,并使用kusyz-F/R进行菌丝PCR,根据电泳条带大小,初步判断黑曲霉An-1的kusA基因是否发生敲除,再进一步测序检验菌株的正确性。
按照上述方法,分别构建HQM9510的敲除与过表达的菌株。
1.3.4 黑曲霉菌株的发酵与酶活测定
将黑曲霉接种于PDA固体平板上,28 ℃倒置培养4 d,用0.9%(质量分数)NaCl溶液制作孢子悬液。利用血球计数板计数,取约1×107个孢子接种量接种于生长培养基,30 ℃、200 r/min振荡培养4 d。取适量发酵液,12 000 r/min离心10 min后取上清液进行酶活力测定。以纤维二糖和p-硝基苯酚-α-D-吡喃葡萄糖苷2种底物测定BGL活力。
2 结果与分析
2.1 五种不同条件对非模式黑曲霉An-1原生质体转化的影响
2.1.1 不同酶解液对制备黑曲霉An-1原生质体的影响
酶解作用下菌丝体的细胞壁被破坏,使原生质体释放。溶壁酶能够水解细胞壁葡聚糖的糖苷键,对大多数真菌都有较好的脱壁效果,例如,ZHENG等[4]使用单一溶壁酶处理黑曲霉菌丝体后,获得了大量原生质体用于PEG介导的转化。纤维素酶、蜗牛酶、溶菌酶等均能水解细胞壁组分的糖苷键,LIU等[5]将这些酶按一定比例混合后,处理高产淀粉的黑曲霉,所制备的原生质体数量能达到105~106个/mL。DONG等[7]在构建高效表达海藻糖酶的工程黑曲霉时,制备原生质体时所使用的也是以纤维素酶为主的混合酶。因此,本研究系统比较了单一溶壁酶和混合酶在制备产BGL黑曲霉原生质体的效率。
黑曲霉菌丝体酶解流程如图1-A所示。将液体培养所获得的菌丝体,按照1.3.2.1节的方法,使用不同类型的酶液进行处理。如图1-B和图1-C所示,单一溶壁酶处理2 h后,菌丝球保持较完整状态,酶解液较透亮,而在混合酶液(1%纤维素+0.5%蜗牛酶+0.25%溶菌酶)的作用下,菌丝球分散开,酶解液比较浑浊。酶解液的镜检分析如图1-D和图1-E所示,菌丝球经单一溶壁酶处理后,视野比较干净,仅存在少量菌丝,未出现原生质体。然而,在混合酶的酶解液中,能观察到大量分散的菌丝和少量原生质体的存在。以上结果表明,混合酶液在制备黑曲霉An-1的原生质体时具有良好的酶解脱壁效果。

A-黑曲霉菌丝体酶解流程;B-溶壁酶处理黑曲霉菌丝;C-复合酶处理黑曲霉菌丝;D-溶壁酶处理黑曲霉菌丝镜检;E-复合酶处理黑曲霉菌丝镜检
图1 不同酶解液制备黑曲霉An-1的原生质体
Fig.1 Preparation of protoplasts using different enzymatic hydrolysates
2.1.2 菌丝培养方式对制备黑曲霉An-1原生质体的影响
以上研究发现,液体摇瓶培养的菌球所制备原生质体的数量极少,且大多附着在菌丝上(图1-D),使用过滤的方式难以将菌丝体和原生质体进行有效地分离,残留的大量菌丝会干扰转化效率。赵君[11]通过优化黑曲霉液体培养时间、改进培养基配方,减少了菌球形成,使原生质体悬液浓度从1×104 个/mL提升至4×105 个/mL。
本研究前期尝试优化液体培养方式,获得相对分散的菌丝体,结果并没有获得理想的酶解材料。LI等[12]和QIAN等[13]在制备草酸青霉与里氏木霉的原生质体时,使用的酶解材料是附着在玻璃纸上的菌丝体。对于高产的糖化酶工业黑曲霉菌株,LIU等[5]使用固体培养菌丝体制备的原生质体浓度最高达到1.7×107 个/mL。因此,本部分探究了固体培养菌丝的酶解脱壁效果。
按照1.3.2.1节方法使用固体培养菌丝进行酶解处理,镜检视野中原生质体从菌丝体中释放到酶解液中,与液体培养菌丝体的酶解液相比,数量有了明显提升,且体积较大(图2)。在黑曲霉菌丝长度方面,固体培养比液体培养的较短,菌丝虽然相互缠绕,但不存在抱团现象,其相对分散的菌丝状态增加了与酶液的接触,有利于菌丝体的充分酶解。以上结果表明,固体培养菌丝在制备黑曲霉An-1的原生质体时具有良好效果。
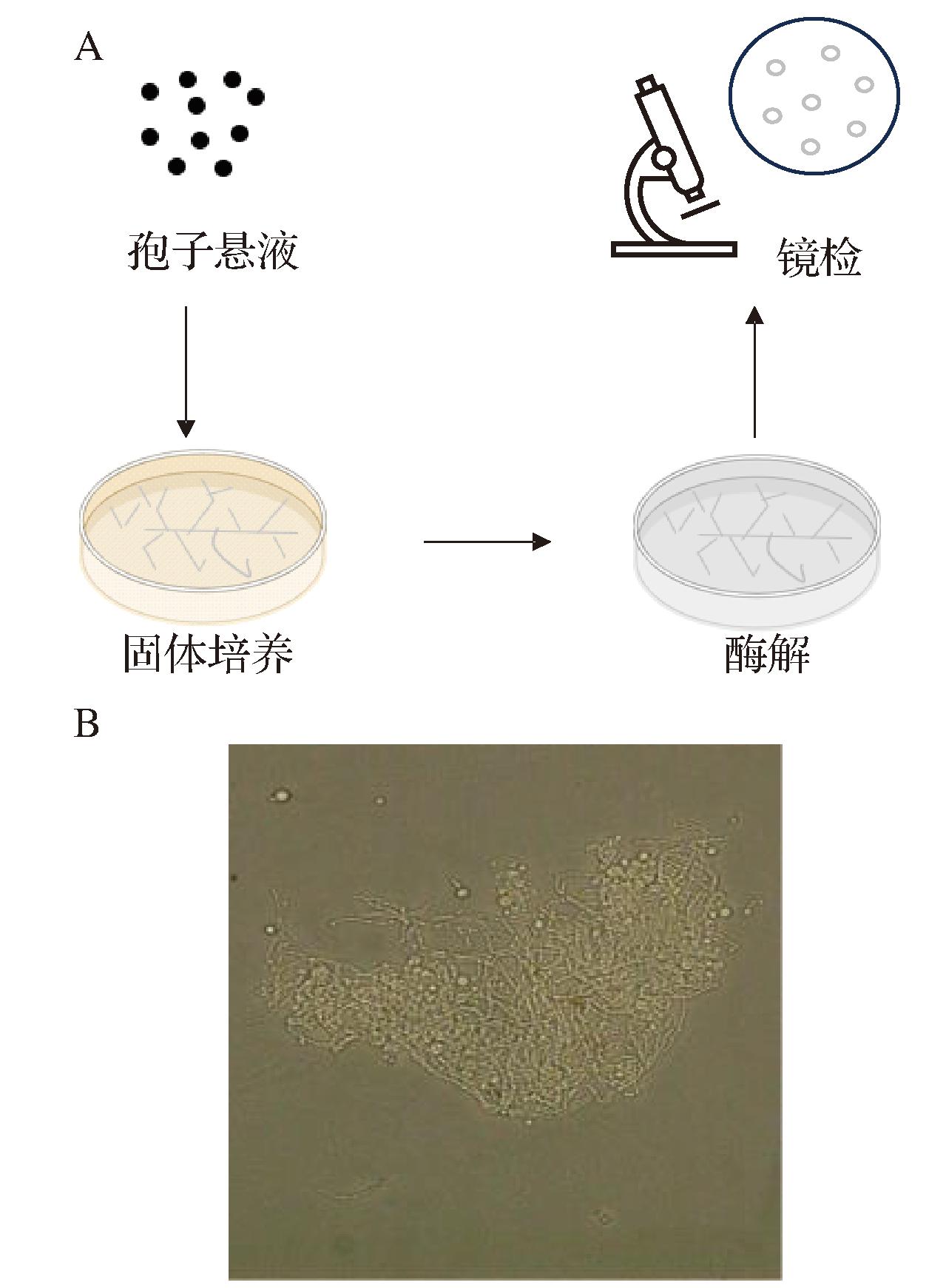
A-黑曲霉菌丝体酶解流程;B-固体培养黑曲霉菌丝镜检
图2 固体培养的菌丝酶解效果
Fig.2 Enzymatic hydrolysis of solid cultured mycelium
2.1.3 酶解时间对制备黑曲霉原生质体An-1的影响
菌丝酶解时间过短,大量的原生质体还未得到释放,充分地酶解有利于提升原生质体的制备效率,然而,过度地酶解处理会破坏原生质体的完整状态,因此,按照1.3.2.1节方法对酶解时间进行了研究。将固体培养的菌丝用混合酶液,分别酶解不同时间后进行镜检,结果如图3所示,酶解处理1.5 h,视野中约有14颗原生质体;酶解2.0 h后,原生质体数量增长至23颗;酶解处理2.5~3.0 h,原生质体的数量出现下降,不足10颗。从以上结果可知,原生质体的数量随酶解时间的延长先增加后减少,对于黑曲霉An-1,最佳酶解时间为2.0 h。朱思远[14]在优化黑曲霉CICC2169原生质体的制备条件时,发现最佳的酶解处理为2.5 h。赵君[11]在酶解处理黑曲霉CBS 513.88时,发现原生质体的最佳酶解时间为1.5 h。由此可见,不同黑曲霉菌株的酶解处理时间存在一定差异。具体见图3。
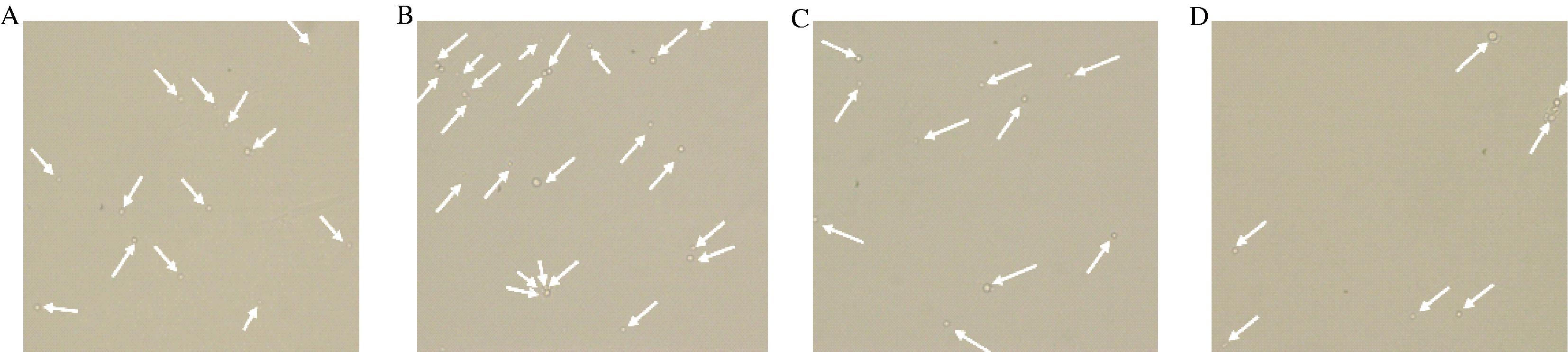
A-酶解1.5 h;B-酶解2.0 h;C-酶解2.5 h;D-酶解3.0 h
图3 酶解时间对制备黑曲霉An-1原生质体的影响
Fig.3 Effect of treatment time on the preparation of A.niger An-1 protoplasts
2.1.4 再生方式对PEG介导黑曲霉An-1原生质体转化效率的影响
原生质体需要在适宜的条件下再生出细胞壁,才能回复正常的生长,因此,原生质体的再生对于黑曲霉的转化起到了关键作用。通常来说,在黑曲霉等丝状真菌进行原生质体再生时多采用双层平板法,原生质体在无抗的高渗固体培养基中完成再生[4-5,7]。本研究在使用该方法时发现,双层平板上长出致密的黑曲霉菌落,但是这些菌落无法生长于抗性PDA,因此,使用双层平板进行黑曲霉An-1进行固体再生,存在大量假阳性现象(图4-A)。
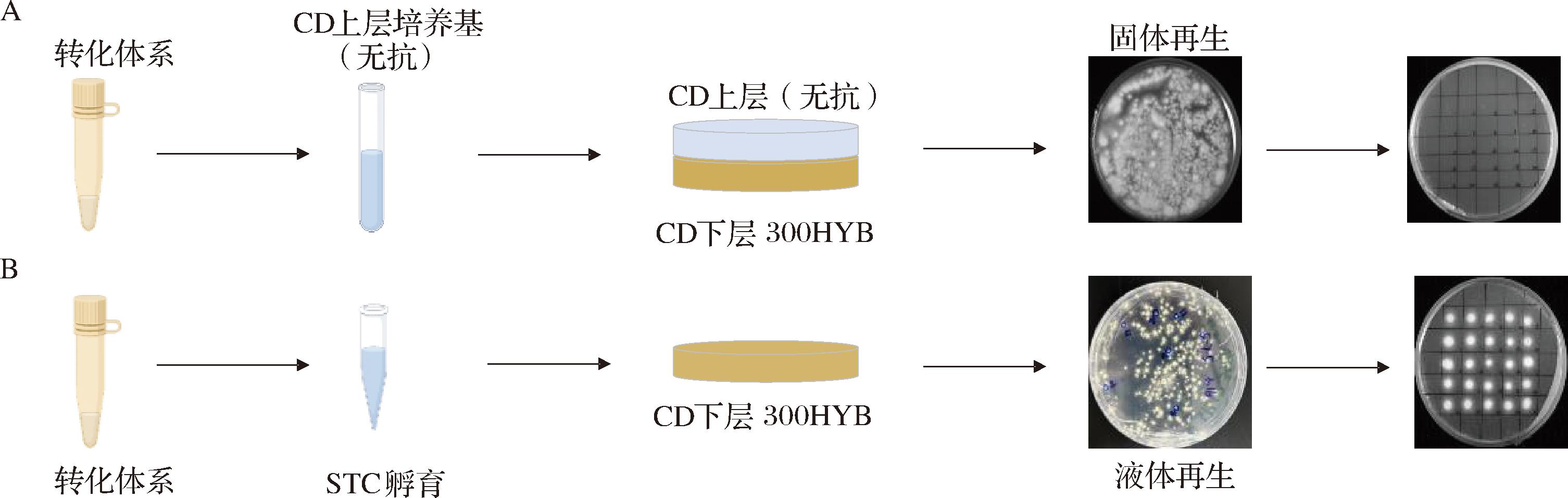
A-原生质体的固体再生;B-原生质体的液体再生
图4 原生质体再生方式对转化效果的影响
Fig.4 The influence of solid or liquid regeneration of protoplasts on transformation efficiency
黑曲霉SJ1和ATCC12846在PEG介导完转化后,直接涂布于抗性PDA上进行转化子的筛选[15]。黑曲霉AG11采用的是将转化液直接转移至抗性高渗固体平板,进行再生培养[8]。为了使黑曲霉An-1的原生质体得到较好的再生,本研究按照1.3.2.2节和1.3.2.3节的方法将转化体系在STC缓冲液中进行孵育后,再在抗性高渗固体平板进行筛选。结果如图4-B所示,使用液体再生的方法成功获得了具有抗性的黑曲霉转化子,一个转化体系能获得100个左右的转化子。随机挑取的转化子转接于抗性平板上,均表现出良好抗性,不存在假阳性菌株。
2.1.5 菌丝破菌方式对黑曲霉An-1转化子鉴定和筛选的影响
黑曲霉菌丝的细胞壁结构致密,破菌成功率会影响转化子验证的正确性。因此,本研究进一步优化了菌丝破壁方式,以提高黑曲霉An-1转化子的验证效率。张晓娟等[16]利使用微波处理置于10×TE缓冲液中的黑曲霉菌丝,裂解上清液直接用于PCR扩增,然而微波炉处理极易造成裂解液的喷溅。赵杰宏等[17]使用高温水浴、超声的方式处理丝状真菌,裂解液上清液均能作为DNA模板用于PCR扩增。罗中钦等[18]使用氢氧化钠悬浮菌丝并进行加热处理,快速制备的丝状真菌的模板DNA用于转化子的快速筛选。结合以上研究,本部分按照1.3.2.4节的方法比较了高温水浴、超声处理、高温水浴和超声组合处理以及碱裂解4种方式,对黑曲霉An-1检测效率的影响。结果如图5-A所示,以上方法中,高温水浴处理的检测效率低于10%,而碱裂解法的检测效率最高为97%,另外2种方式的检测效率较低,约为20%和50%。以上结果说明,碱裂解法实现了菌体的高效裂解,适用于黑曲霉An-1转化子的快速鉴定和大量筛选。
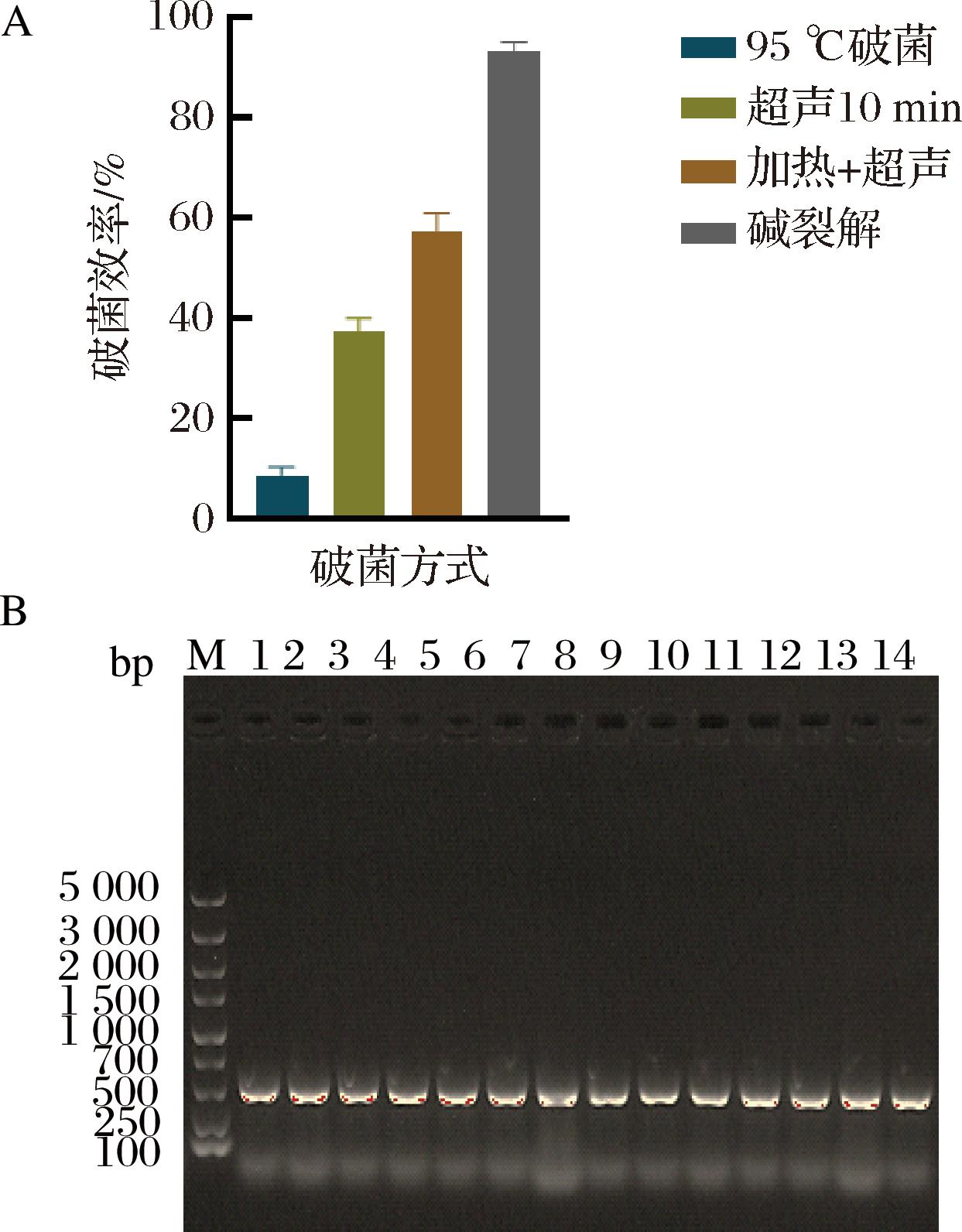
M表示Marker(下同),泳道1~14为黑曲霉An-1转化子。A-不同破菌方式的检测效率;B-碱裂解的菌丝PCR凝胶电泳
图5 菌丝破壁方式对转化子验证的影响
Fig.5 Effect of cell wall-breaking methods on transformant validation
2.2 非模式黑曲霉An-1基因编辑体系的构建与11条BGL的表达
2.2.1 红色荧光蛋白报告基因及11条BGL基因在黑曲霉An-01中的过表达与筛选
本研究按照1.3.3.1节的方法通过构建红色荧光表达盒子,检测以上遗传转化体系是否适用于蛋白表达。启动子Pgpd和Pgla分别是黑曲霉中的强组成型与诱导型启动子[19],将两者分别用于驱动红色荧光蛋白的表达,通过融合PCR,构建Pgpd-RED-Tgla与Pgla-RED-Tgla的表达盒子,再整合于黑曲霉的游离表达质粒pFC332上,并把重组质粒导入至黑曲霉An-1的原生质体中(图6-A)。抗性转化子Pgpd-RED和Pgla-RED中存在相应的红色荧光蛋白表达盒。荧光观察结果显示,转化子Pgpd-RED和Pgla-RED均能成功地激发出红色荧光,而出发菌株An-1未检测到荧光信号,说明启动子Pgpd和Pgla能够驱动蛋白在黑曲霉An-1中的表达(图6-B~图6-C)。其中,转化子Pgla-RED的荧光强度要低于Pgpd-RED,可能是由于诱导型启动子Pgla未处于适宜的诱导条件。
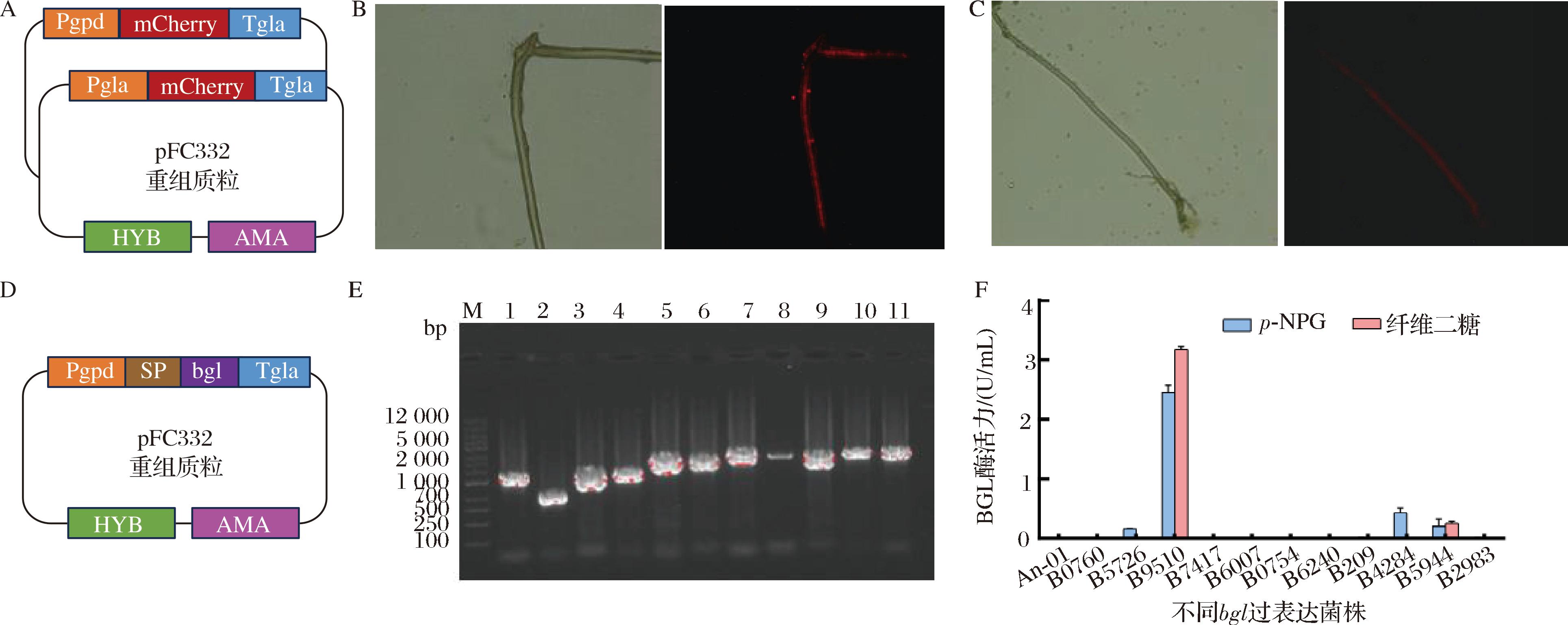
E图中泳道1~11为11条BGL编码基因,相关信息见表2。A-红色荧光蛋白表达盒子的构建;B-Pgpd-RED菌丝显微成像;C-Pgla-RED菌丝显微成像;D-不同BGL表达盒子的构建;E-不同BGL基因的凝胶电泳图;F-不同BGL表达菌株的酶活力测定
图6 黑曲霉An-1中红色荧光蛋白与不同bgl基因的表达
Fig.6 Expression of red fluorescent protein and different bgl genes in A.niger An-1
本团队前期对黑曲霉An-1进行全基因测序,和NCBI黑曲霉基因序列比对分析,发现黑曲霉An-1存在11条BGL编码基因,相关信息见表2。采用1.3.3.3节的方法,构建过表达菌株(图6-D和图6-E),检测酶活力变化以筛选关键BGL基因。发酵结果如图6-E所示,其中HQM5726和HQM4284以对硝基苯基-α-D-吡喃葡萄糖苷(p-nitrophenyl-α-D-glucopyranoside,p-NPG)为底物能够检测出酶活力,分别为0.17、0.43 U/mL。HQM5944在p-NPG与纤维二糖为底物时,均能检测出酶活力,分别为0.21、0.26 U/mL。相比之下,HQM9510的酶活力水平最高,以p-NPG与纤维二糖为底物的酶活力分别为2.46、3.18 U/mL。综上,推断HQM9510是黑曲霉An-1的关键BGL编码基因。
表2 黑曲霉An-1中的β-葡萄糖苷酶相关信息
Table 2 β-glucosidase related information in A.niger An-1
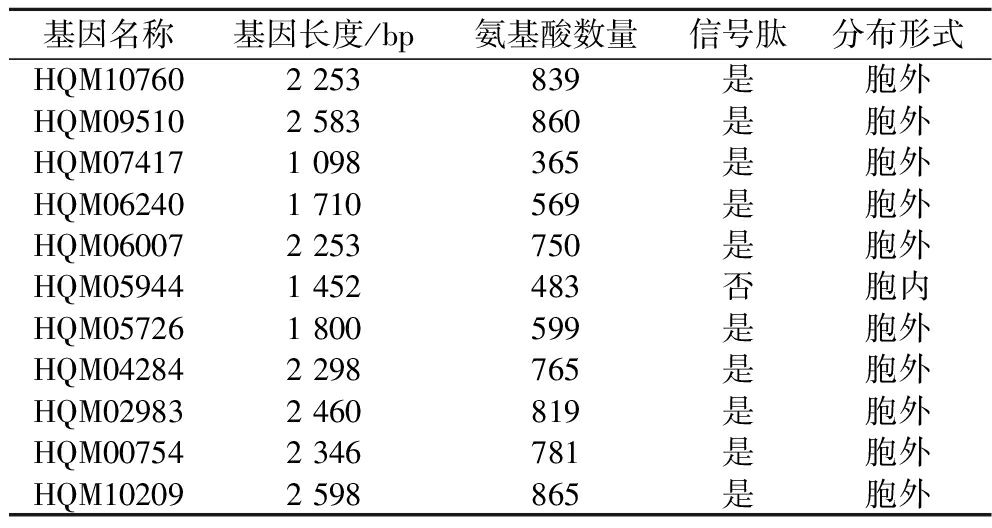
基因名称基因长度/bp氨基酸数量信号肽分布形式HQM107602 253839是胞外HQM095102 583860是胞外HQM074171 098365是胞外HQM062401 710569是胞外HQM060072 253750是胞外HQM059441 452483否胞内HQM057261 800599是胞外HQM042842 298765是胞外HQM029832 460819是胞外HQM007542 346781是胞外HQM102092 598865是胞外
2.2.2 非模式黑曲霉中An-1基因编辑体系的建立
基于以上黑曲霉An-1中遗传转化体系的建立和内源蛋白的成功表达,验证CRISPR-Cas9基因组编辑技术在黑曲霉An-1中的可行性。黑曲霉kusA基因的敲除能够提高同源重组的概率,在此选择该基因为敲除靶标。pFC332质粒广泛用于黑曲霉的基因编辑[20-21],本研究选取该质粒为操作工具,按照1.3.3.2节和1.3.3.3节方法建立黑曲霉An-1的基因编辑方法。
如图7-A所示,首先构建5S rRNA-target-sgRNA表达盒,然后将其整合至pFC332质粒中,实现Cas9和靶向sgRNA的共表达。在此,选取kusA基因的上下游500 bp序列融合形成1 kb的供体片段。图7-B显示,靶向质粒与供体片段已成功构建。
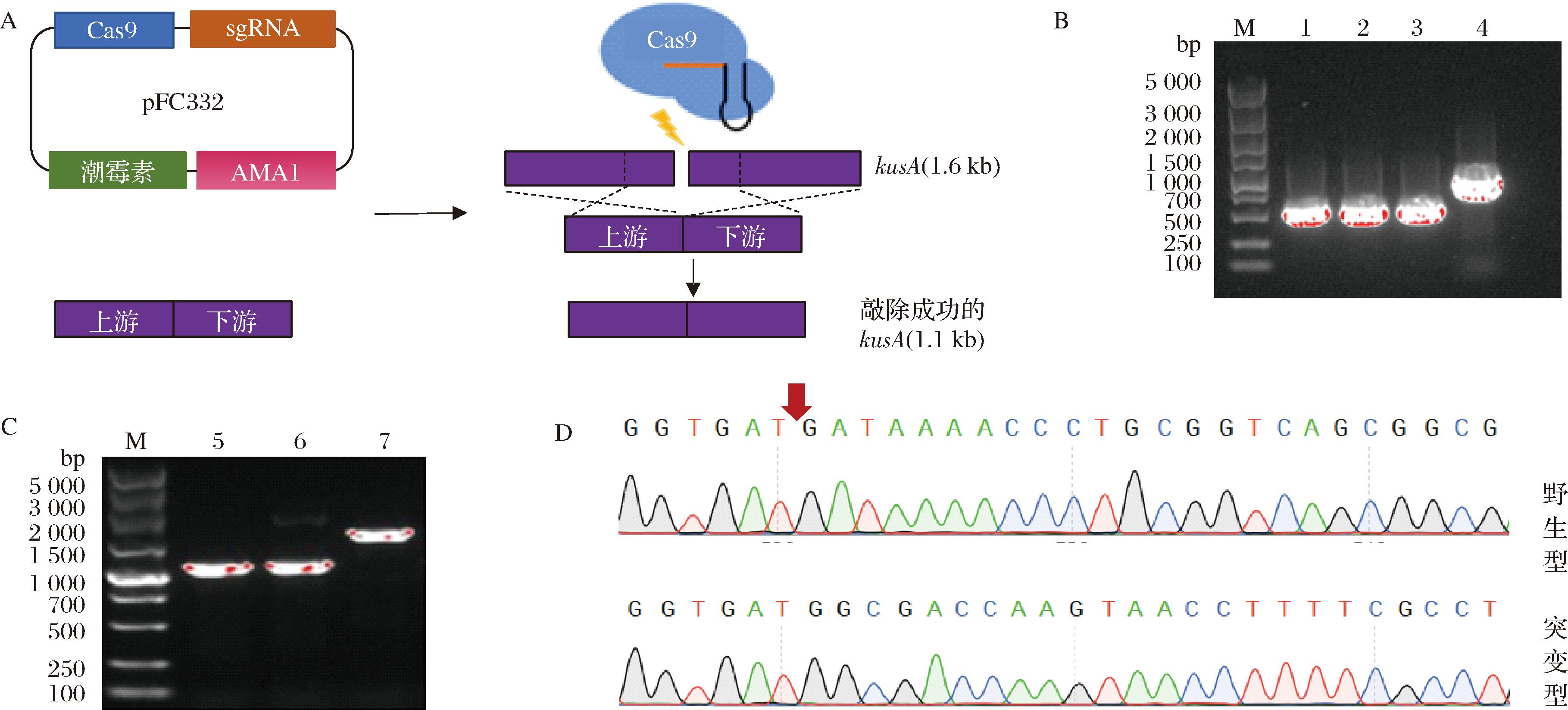
泳道1~3为5S rRNA-target-sgRNA表达盒,泳道4为供体片段,泳道5~6为敲除菌株,泳道7为对照菌株。A-5S rRNA-target-sgRNA及供体片段构建及kusA的敲除示意图;B-5S rRNA-target-sgRNA及供体片段的核酸凝胶验证;C-黑曲霉敲除菌株的菌丝PCR;D-敲除菌株的DNA测序
图7 利用CRISPR-Cas9技术敲除黑曲霉An-1中的kusA基因
Fig.7 Knockout of kusA gene in A.niger An-1 through CRISPR-Cas9 technology
通过PEG-原生质体转化法,将靶向质粒与敲除供体共同转化至黑曲霉An-1中,随后把在潮霉素抗性CD高渗固体培养基上的转化子进行传代,转接于抗性的PDA平板上。待转化子长出后挑取菌丝,利用碱裂解法破菌,采用kusyz-F/R引物对转化子进行PCR检测,结果显示,未敲除成功的条带长度为1.6 kb,而敲除kusA基因的条带长度仅有1.1 kb(图7-C)。经测序确认,kusA基因被成功敲除,基因编辑体系构建成功(图7-D)。
2.2.3 非模式黑曲霉BGL的关键基因An-1 HQM9510的敲除及过表达
HQM9510基因通过鉴定,全长2 583 bp,蛋白分子质量为93.3 kDa,属于GH3家族。使用以上的CRISPR-Cas9基因组编辑技术,对HQM9510基因分别进行敲除和过表达(图8-A和图8-D),经转化子验证D9510与O9510构建成功(图8-B和图8-E)。酶活力比对发现,敲除菌株D9510的p-NPG酶活力出现明显下降,而纤维二糖酶活力几乎检测不到,而过表达菌株O9510的酶活力水平提升明显,以p-NPG与纤维二糖为底物的酶活力分别为12.88、17.10 U/mL,比游离表达菌株B9510酶活力分别提高4.2倍和4.4倍,由此确定了HQM9510为黑曲霉BGL关键基因,并得到过表达HQM9510基因的黑曲霉工程菌株O9510。
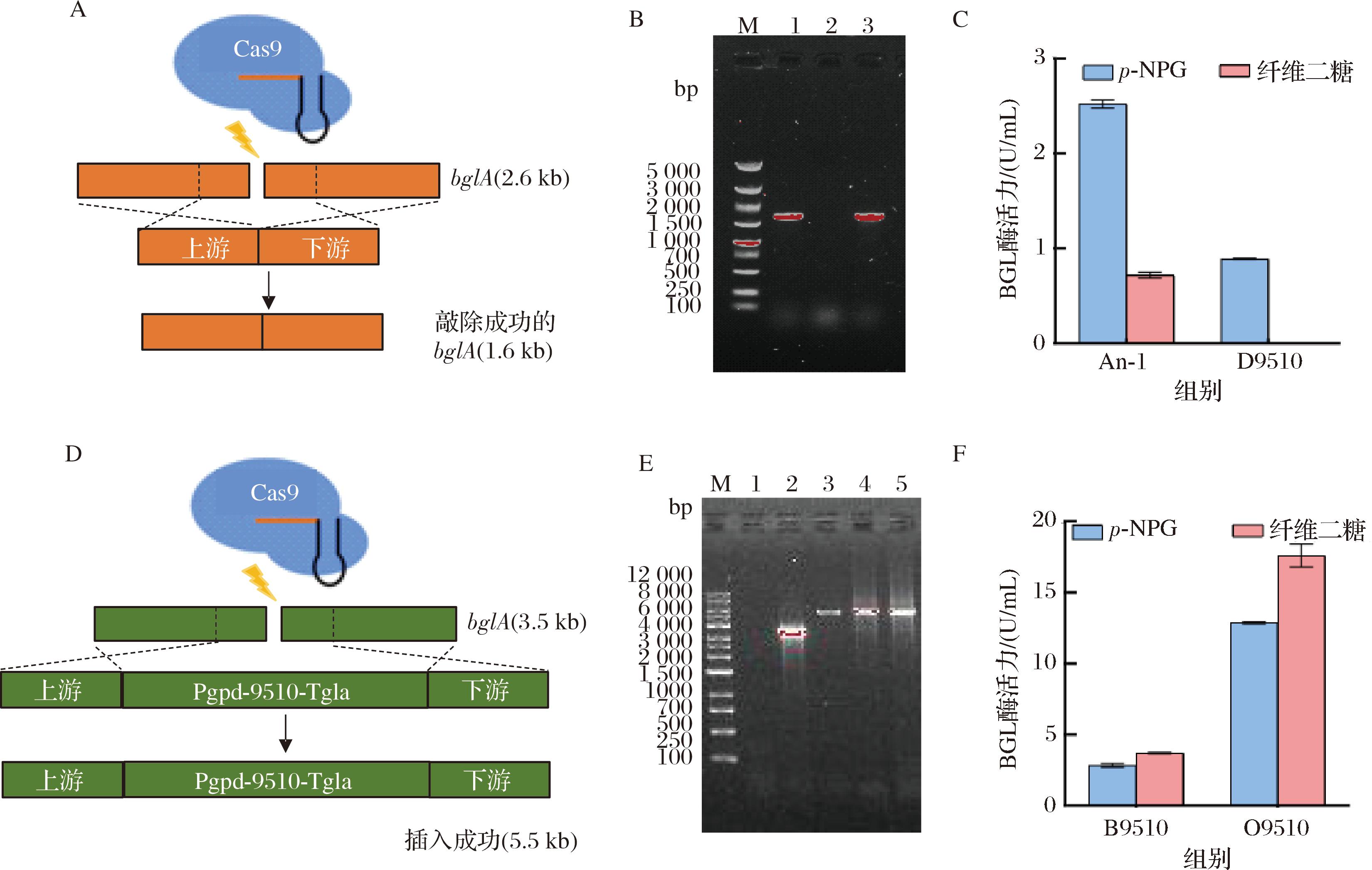
B图中泳道1为敲出成功转化子验证条带,泳道2为未破菌成功条带,泳道3为敲出成功转化子验证条带;E图中泳道1为未破菌成功条带,泳道2为转化子未编辑条带,泳道3~泳道5为过表达HQM9510编辑转化子验证条带。A-HQM9510基因敲除示意图;B-敲除菌株的菌丝PCR;C-HQM9510基因敲除对酶活力的影响;D-HQM9510基因过表达示意图;E-过表达菌株的菌丝PCR;F-HQM9510基因过表达对酶活力的影响
图8 黑曲霉An-1中关键BGL基因HQM9510的敲除及过表达
Fig.8 Knockout and overexpression of key BGL gene HQM9510 in A.niger An-1
3 讨论与结论
黑曲霉广泛使用的转化方法是PEG介导的原生质体转化,原理是去除掉部分细胞壁,在PEG与Ca2+作用下,改变细胞膜的流动性,从而有利于细胞对外源DNA的吸收,在此过程中原生质体的制备、再生是转化成功的关键点。本研究发现所得到的黑曲霉An-1菌丝体呈坚实的球状,难以酶解释放原生质体。相比之下,固体培养的方式能够获得分散的菌丝,有利于酶解过程。因此,分散的菌丝体是丝状真菌制备原生质体的理想材料[13]。市面上有多种制备原生质体的酶制剂,例如默克公司的单一溶壁酶Lysing Enzyme,价格过于昂贵,使用不同比例的混合酶成为平价替代品,但混合酶的酶解不充分,原生质体未能有效释放,而且长时间的酶解处理会破坏原生质体的完整状态。因此,丝状真菌原生质体的酶解效率、酶解液浓度和酶解时间密切相关[18]。固体再生是一种传统技术手段,但是该过程过于复杂和繁琐,而液体再生的方式省时省力,几乎没有假阳性转化子的出现,所以,本研究选用液体再生构建后续的工程菌株。
黑曲霉多条BGL编码基因的存在,给解析该酶的表达调控机制带来了难度,因此有必要对关键BGL基因分析鉴定。经同源或异源过表达以及酶学性质研究,发现BglA具有胞外酶学特征[9],Bgl1B在胞内发挥了转糖苷和降解活性,4条编码基因是没有功能的假基因[22],其他编码基因对黑曲霉酶活力产生何种影响有待进一步研究。PANG等[23]在证明Cel3 J是里氏木霉的关键BGL时所采取的是构建β-葡萄糖苷酶单敲除菌株的手段,而本研究鉴定黑曲霉分解纤维二糖的关键BGL基因采用的是逐个过表达的方式,更为简便、高效。通过对11条BGL的酶活力比较,发现HQM9510(BglA)是关键BGL,基因敲除与过表达实验则进一步验证了该酶在BGL表达中的重要作用,同时在里氏木霉、草酸青霉中也存在异源表达该基因提升BGL酶活力[24-25]。同时,所构建的黑曲霉工程菌株O9150展示出良好的BGL生产潜力,后续研究将采用优化表达元件、多拷贝整合的方式进一步提升黑曲霉中BGL的酶活力,为更好地解决纤维素糖的关键酶源奠定基础。
本研究形成主要结论如下:
a)以自主筛选的产BGL黑曲霉An-1为研究对象,优化了原生质体的制备条件和再生方法,实现了该菌株的高效遗传转化,建立了稳定的非模式黑曲霉An-1的遗传转化体系。所确定的PEG-原生质体转化方法为:将玻璃纸上的幼嫩菌丝,使用1%纤维素+0.5%蜗牛酶+0.25%溶菌酶(均为质量分数)处理2 h,收集原生质体,转化体系中加入3 μg以上的质粒,使用终质量分数为25%的PEG-6000于25 ℃下孵育20 min,将转化体系置于2 mL的STC缓冲液中于28 ℃下孵育4 h后,直接涂布于抗性的高渗固体培养基上进行筛选。菌丝破壁方式的改进,极大提升了转化子进行菌丝PCR的验证效率。转化子的快速验证方法为:挑取适量转化子菌丝置于2 mol/L NaOH溶液中于95 ℃处理10 min 后,加入2 mol/L Tris-HCl溶液进行中和,裂解液上清直接作为PCR模板使用。
b)建立了稳定的非模式黑曲霉An-1的基因编辑体系,并成功应用于BGL的过表达。研究表明启动子Pgpd和Pgla驱动了红色荧光蛋白在黑曲霉An-1的表达,证实了黑曲霉An-1作为蛋白表达宿主的可行性。采用共表达sgRNA与Cas9、线性化供体片段的方式,黑曲霉An-1可有效进行基因组编辑。基于以上遗传转化和基因编辑体系,明确了HQM9510是黑曲霉An-1的关键BGL,获得了过表达HQM9510基因的黑曲霉工程菌株O9510,以纤维二糖和p-NPG为底物的酶活力分别提升至12.88 U/mL和17.10 U/mL,比游离表达菌株B9510酶活力分别提高4.2倍和4.4倍。
本研究为分子改造非模式黑曲霉An-1,实现BGL的高效生产奠定了科学基础。
[1] PARK M,JEONG M K,KIM M,et al.Modification of isoflavone profiles in a fermented soy food with almond powder[J].Journal of Food Science,2012,77(1):C128-C134.
[2] KANNAN P,SHAFREEN M M,ACHUDHAN A B,et al.A review on applications of β-glucosidase in food,brewery,pharmaceutical and cosmetic industries[J].Carbohydrate Research,2023,530:108855.
[3] FITZPATRICK J,KRICKA W,JAMES T C,et al.Expression of three Trichoderma reesei cellulase genes in Saccharomyces pastorianus for the development of a two-step process of hydrolysis and fermentation of cellulose[J].Journal of Applied Microbiology,2014,117(1):96-108.
[4] ZHENG X M,CAIRNS T,ZHENG P,et al.Protocol for gene characterization in Aspergillus niger using 5S rRNA-CRISPR-Cas9-mediated Tet-on inducible promoter exchange[J].STAR Protocols,2022,3(4):101838.
[5] LIU D D,LIU Q,GUO W Z,et al.Development of genetic tools in glucoamylase-hyperproducing industrial Aspergillus niger strains[J].Biology,2022,11(10):1396.
[6] LI Y Y,LI C,MUHAMMAD AQEEL S,et al.Enhanced expression of xylanase in Aspergillus niger enabling a two-step enzymatic pathway for extracting β-glucan from oat bran[J].Bioresource Technology,2023,377:128962.
[7] DONG L B,YU D,LIN X T,et al.Improving expression of thermostable trehalase from Myceliophthora sepedonium in Aspergillus niger mediated by the CRISPR/Cas9 tool and its purification,characterization[J].Protein Expression and Purification,2020,165:105482.
[8] CAI L N,XU S N,LU T,et al.Directed expression of halophilic and acidophilic β-glucosidases by introducing homologous constitutive expression cassettes in marine Aspergillus niger[J].Journal of Biotechnology,2019,292:12-22.
[9] WANG L,XIE Y J,CHANG J J,et al.A novel sucrose-inducible expression system and its application for production of biomass-degrading enzymes in Aspergillus niger[J].Biotechnology for Biofuels.2023,16(23):1-20.
[10] 龚大春,马东旭,王昕,等.一种高产BGL黑曲霉菌及其构建方法与应用:中国,CN 202510036900X[P].2025-01-09.GONG D C,MA D X,WANG X,et al.A high-yield BGL Aspergillus niger strain,its construction method and application:China,CN 202510036900X[P].2025-01-09.
[11] 赵君.黑曲霉胞β-葡萄糖苷酶的鉴定及其在纤维素降解酶系合成调控中的作用[D].郑州:河南农业大学,2021.ZHAO J.Identification of intracellular β-glucosidase from Aspergillus niger and its role in the synthesis and regulation of cellulolytic enzyme system[D].Zhengzhou:Henan Agricultural University,2021.
[12] LI Z H,YAO G S,WU R M,et al.Synergistic and dose-controlled regulation of cellulase gene expression in Penicillium oxalicum[J].PLoS Genetics,2015,11(9):e1005509.
[13] QIAN Y C,ZHONG L X,GAO J,et al.Production of highly efficient cellulase mixtures by genetically exploiting the potentials of Trichoderma reesei endogenous cellulases for hydrolysis of corncob residues[J].Microbial Cell Factories,2017,16(1):207-223.
[14] 朱思远.无抗黑曲霉表达系统构建及脂肪酶的表达[D].无锡:江南大学,2019.ZHU S Y.Construction of non-resistant Aspergillus niger expression system and expression of lipase[D].Wuxi:Jiangnan University,2019.
[15] 应汉杰,张涛,陈勇,等.一株重组黑曲霉基因工程菌及构建方法和应用:中国,CN202110095568.6[P].2020-07-31.YING H J,ZHANG T,CHEN Y,et al.A recombinant Aspergillus niger genetically engineered strain,construction method and application:China,CN202110095568.6[P].2020-07-31.
[16] 张晓娟,刘松青,夏珊,等.一种用于PCR扩增的丝状真菌DNA快速提取方法:中国,CN201510918551.0[P].2016-02-10.ZHANG X J,LIU S Q,XIA S,et al.A rapid extraction method for filamentous fungal DNA for PCR amplification:China,CN201510918551.0[P].2016-02-10.
[17] 赵杰宏,桂艳玲,韩洁,等.一种丝状真菌快速PCR模板的简易制备方法:中国,CN202110031221.5[P].2021-05-18.ZHAO J H,GUI Y L,HAN J,et al.A simple method for preparing a rapid PCR template for filamentous fungi:China,CN202110031221.5[P].2021-05-18.
[18] 罗中钦,程琳,张茜,等.丝状真菌PCR模板DNA的快速制备方法[J].生物技术通报,2015(9):79-83.LUO Z Q,CHENG L,ZHANG X,et al.A rapid method of preparing DNA template of filamentous fungi for PCR amplification[J].Biotechnology Bulletin,2015(9):79-83.
[19] KLUGE J,TERFEHR D,KÜCK U.Inducible promoters and functional genomic approaches for the genetic engineering of filamentous fungi[J].Applied Microbiology and Biotechnology,2018,102(15):6357-6372.
[20] ZHENG X M,ZHENG P,ZHANG K,et al.5S rRNA Promoter for guide RNA expression enabled highly efficient CRISPR/Cas9 genome editing in Aspergillus niger[J].ACS Synthetic Biology,2019,8(7):1568-1574.
[21] DONG L B,LIN X T,YU D,et al.High-level expression of highly active and thermostable trehalase from Myceliophthora thermophila in Aspergillus niger by using the CRISPR/Cas9 tool and its application in ethanol fermentation[J].Journal of Industrial Microbiology &Biotechnology,2020,47(1):133-144.
[22] ZHAO J,SHI D C,YANG S,et al.Identification of an intracellular β-glucosidase in Aspergillus niger with transglycosylation activity[J].Applied Microbiology Biotechnology,2020,104(19):8367-8380.
[23] PANG A P,WANG H Y,LUO Y S,et al.Investigating the cellular functions of β-glucosidases for synthesis of lignocellulose-degrading enzymes in Trichoderma reesei[J].Engineering Microbiology,2023,3(4):100105.
[24] GAO J,QIAN Y C,WANG Y F,et al.Production of the versatile cellulase for cellulose bioconversion and cellulase inducer synthesis by genetic improvement of Trichoderma reesei[J].Biotechnology for Biofuels,2017,10:272.
[25] 阚钦标.草酸青霉β-葡萄糖苷酶的过表达及纤维素酶新调控位点的筛选[D].济南:山东大学,2016.KAN Q B.Penicillium oxalate Kan QB.Overexpression of β-glucosidase of Penicillium oxalate and screening of new regulatory sites for cellulase[D].Jinan:Shandong University,2016.