母乳是新生儿最理想的天然营养源,其成分精准满足婴儿的生长发育需求,其中母乳低聚糖(human milk oligosaccharides,HMOs)是母乳中的重要组成成分[1-2]。母乳寡糖主要包括岩藻糖基化寡糖、唾液酸化寡糖和中性核心结构寡糖。其中,3′-唾液酸乳糖(3′-sialyllactose,3′-SL)是由乳糖通过α-2,3-糖苷键连接唾液酸[N-乙酰神经氨酸(N-acetylneuraminic acid,Neu5Ac)]而形成的三糖,具有促进婴儿肠道益生菌(如双歧杆菌)生长、抑制病原体(如肺炎链球菌、空肠弯曲杆菌等)黏附和帮助于幼儿的认知发育等功能[3-6]。
目前,3′-SL的生产方法主要包括生物提取法、酶法合成、化学合成和微生物发酵,微生物发酵法具有高效可控、生产成本低和环境友好的特点,因此已成为理想的3′-SL合成方式[7-8]。天然的微生物宿主中并不具有3′-SL的合成途径,需要在菌株中异源表达3′-SL合成途径的相关酶[9-10]。异源合成途径通常与微生物宿主自身的源代谢网络适配性较差,导致目标产物的合成效率较低[11]。因此,需要重构微生物宿主的代谢网络,使更多地代谢通量流向3′-SL的合成途径,提高3′-SL的合成效率。早期研究者主要通过阻断竞争代谢支路来提升产物积累,PRIEM等[12]开创性地对大肠杆菌(Escherichia coli)JM107进行代谢改造,通过补料发酵在2 L发酵罐中添加Neu5Ac使3′-SL产量达到2.6 g/L,其0.12 g/(L·h)的生产强度揭示了该产物的工业化潜力。随着代谢工程技术的进步,研究者开始探索多元产物的协同合成,GUO等[13]发现一种具有双重反式Neu5Ac活性的重组巴氏杆菌唾液酸转移酶,在E.coli BL21中成功实现3′-SL(1.7 g/L)和6′-SL(2.1 g/L)的同步生物合成。近年来,整合基因组编辑与质粒工程技术取得突破性进展,ZHANG等[14]开发了新型“质粒-染色体”双轨表达策略,通过利用诱导型质粒强化neuC[编码尿苷二磷酸-N-乙酰葡糖胺(uridine diphosphate-N-acetylglucosamine,UDP-GlcNAc)差向异构酶]、neuB(编码N-乙酰神经氨酸合酶)、neuA(编码CMP-Neu5Ac合酶)表达,同时将末端酶基因Vs16(编码α-2,3-唾液酸转移酶)稳定整合于基因组,在5 L规模发酵中的3′-SL产量达到23.1 g/L,标志着3′-SL制备技术进入新阶段。然而,现有研究为强化3′-SL合成途径的代谢流,通常会使用质粒过表达途径关键酶,易导致生产稳定性差,并且会使用诱导型启动子调控关键酶的表达,导致发酵过程中需要额外添加诱导剂,增加了生产成本。
本研究通过在大肠杆菌中整合3′-SL合成基因neuC、neuB、neuA、Vs16/nst(编码α-2,3-唾液酸转移酶),优化基因表达、阻断乳糖分解代谢途径、强化前体供应,构建了无质粒且无需诱导剂的工程菌株,最终使3′-SL在摇瓶和3 L发酵罐中产量分别提升至3.02、14.85 g/L,为实现工业化生产奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
本研究使用的菌株和质粒见表1。
表1 本研究使用的菌株和质粒
Table 1 Strains and plasmids employed in this study
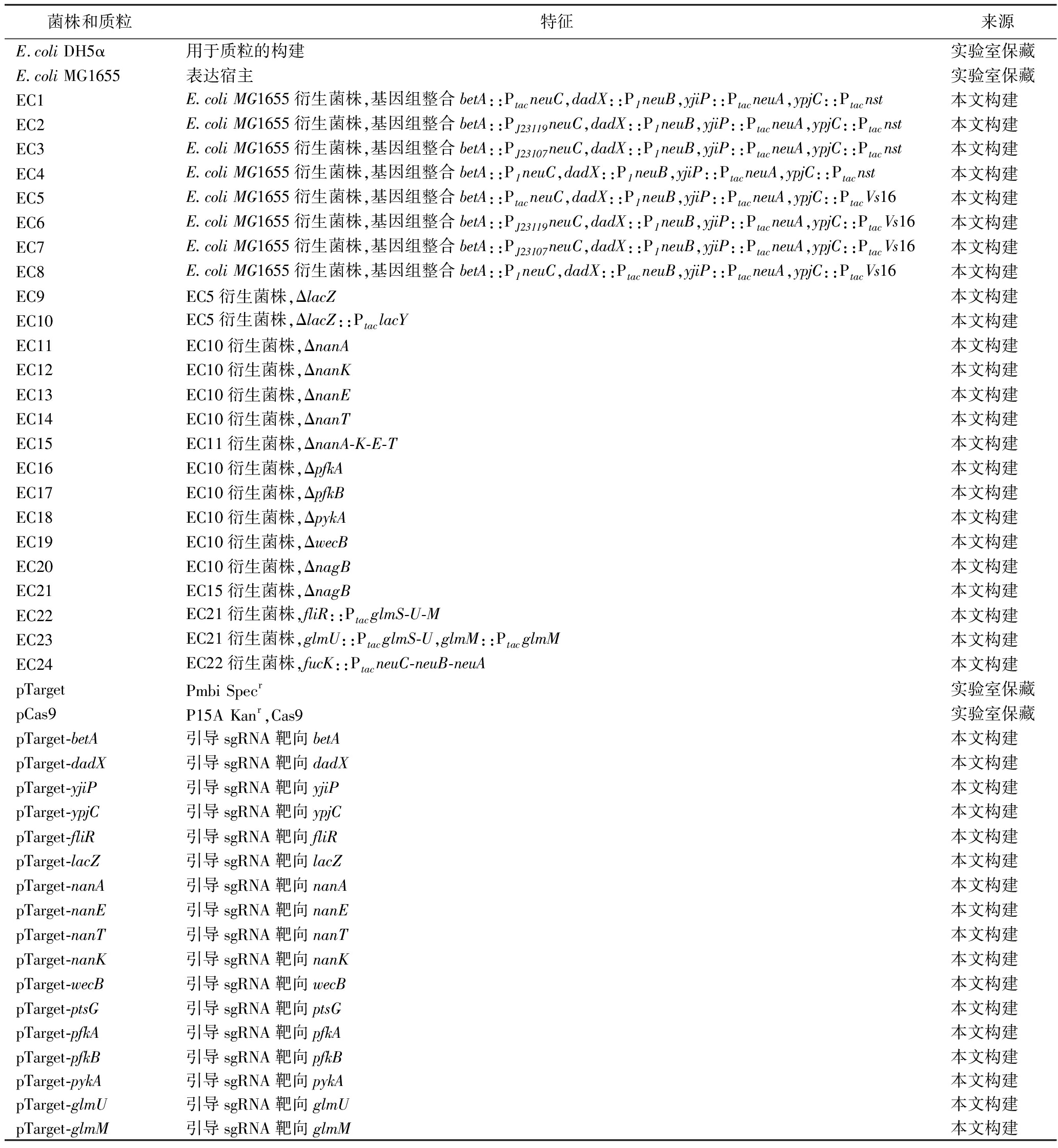
菌株和质粒特征来源E.coli DH5α用于质粒的构建实验室保藏E.coli MG1655表达宿主实验室保藏EC1E.coli MG1655衍生菌株,基因组整合betA::PtacneuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::Ptacnst本文构建EC2E.coli MG1655衍生菌株,基因组整合betA::PJ23119neuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::Ptacnst本文构建EC3E.coli MG1655衍生菌株,基因组整合betA::PJ23107neuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::Ptacnst本文构建EC4E.coli MG1655衍生菌株,基因组整合betA::P1neuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::Ptacnst本文构建EC5E.coli MG1655衍生菌株,基因组整合betA::PtacneuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::PtacVs16本文构建EC6E.coli MG1655衍生菌株,基因组整合betA::PJ23119neuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::PtacVs16本文构建EC7E.coli MG1655衍生菌株,基因组整合betA::PJ23107neuC,dadX::P1neuB,yjiP::PtacneuA,ypjC::PtacVs16本文构建EC8E.coli MG1655衍生菌株,基因组整合betA::P1neuC,dadX::PtacneuB,yjiP::PtacneuA,ypjC::PtacVs16本文构建EC9EC5衍生菌株,ΔlacZ本文构建EC10EC5衍生菌株,ΔlacZ::PtaclacY本文构建EC11EC10衍生菌株,ΔnanA本文构建EC12EC10衍生菌株,ΔnanK本文构建EC13EC10衍生菌株,ΔnanE本文构建EC14EC10衍生菌株,ΔnanT本文构建EC15EC11衍生菌株,ΔnanA-K-E-T本文构建EC16EC10衍生菌株,ΔpfkA本文构建EC17EC10衍生菌株,ΔpfkB本文构建EC18EC10衍生菌株,ΔpykA本文构建EC19EC10衍生菌株,ΔwecB本文构建EC20EC10衍生菌株,ΔnagB本文构建EC21EC15衍生菌株,ΔnagB本文构建EC22EC21衍生菌株,fliR::PtacglmS-U-M本文构建EC23EC21衍生菌株,glmU::PtacglmS-U,glmM::PtacglmM本文构建EC24EC22衍生菌株,fucK::PtacneuC-neuB-neuA本文构建pTargetPmbi Specr实验室保藏pCas9P15A Kanr,Cas9实验室保藏pTarget-betA引导sgRNA靶向betA本文构建pTarget-dadX引导sgRNA靶向dadX本文构建pTarget-yjiP引导sgRNA靶向yjiP本文构建pTarget-ypjC引导sgRNA靶向ypjC本文构建pTarget-fliR引导sgRNA靶向fliR本文构建pTarget-lacZ引导sgRNA靶向lacZ本文构建pTarget-nanA引导sgRNA靶向nanA本文构建pTarget-nanE引导sgRNA靶向nanE本文构建pTarget-nanT引导sgRNA靶向nanT本文构建pTarget-nanK引导sgRNA靶向nanK本文构建pTarget-wecB引导sgRNA靶向wecB本文构建pTarget-ptsG引导sgRNA靶向ptsG本文构建pTarget-pfkA引导sgRNA靶向pfkA本文构建pTarget-pfkB引导sgRNA靶向pfkB本文构建pTarget-pykA引导sgRNA靶向pykA本文构建pTarget-glmU引导sgRNA靶向glmU本文构建pTarget-glmM引导sgRNA靶向glmM本文构建
1.1.2 培养基与培养条件
LB液体培养基(g/L):氯化钠10.00,酵母提取物5.00,胰蛋白胨10.00;LB固体培养基(g/L):在液体培养基基础上添加琼脂粉20,121 ℃灭菌15 min。
摇瓶与发酵罐培养基(g/L):酵母提取物5.00,胰蛋白胨2.00,甘油20.00,磷酸二氢钾2.31,磷酸氢二钾12.54,乳糖10.00(单独过滤灭菌),121 ℃灭菌15 min。
摇瓶培养:摇瓶加入20 mL培养基经121 ℃灭菌15 min后接种0.2 mL种子液,摇床220 r/min、30 ℃条件下发酵72 h。
发酵罐培养:在3 L罐体中装入1 L培养基,经121 ℃灭菌15 min后接种30 mL种子液,在30 ℃环境中维持40%溶氧度持续培养,通过发酵控制系统调控pH,使用50%稀释的氨水来控制发酵罐的实时pH值维持在6.8~7.0。发酵期间以5 mL/h流速流加300 g/L质量浓度乳糖使其终质量浓度维持在8~10 g/L,并于发酵12 h后开始以每4 h流加20 g的甘油进行分批补料,确保甘油质量浓度基本保持5 g/L以下。
1.1.3 试剂
甲醇与乙腈(色谱纯),美国TEDIA公司;3′-唾液酸乳糖标准品,上海西格玛奥德里奇贸易有限公司;Rapid Taq Master Mix,南京诺唯赞生物有限公司;PrimeSTARTM Max DNA Polymerase和DNA Marker,宝生物工程(大连)有限公司;质粒提取、感受态制备试剂盒、琼脂糖、硫酸卡那霉素、壮观霉素,生工生物工程(上海)股份有限公司;酵母提取物、胰蛋白胨,安琪酵母股份有限公司;乳糖、磷酸二氢钾、磷酸氢二钾、甘油,国药集团。
1.2 实验方法
1.2.1 底盘菌株与质粒的构建
本实验使用CRISPR/Cas9系统对菌株进行基因编辑,此编辑系统由2个质粒pCas9和pTarget组成。通过将pCas9质粒化转到E.coli MG1655中。同时电转入同源臂片段和pTarget质粒,即可敲除基因和整合基因的目的。例如:在野生型菌株betA基因座整合neuC基因,需要将制备好的pTarget质粒(插入含有betA靶序列的sgRNA表达载体)和同源臂片段(利用融合PCR技术将上下同源臂和neuC基因融合成一个片段)按比例(1 000 ng∶2 000 ng)电击转化进感受态细胞中,验证基因编辑正确后消除pCas9和pTarget质粒后即完成整合。本研究在构建含不同启动子的基因表达菌株过程中,首先在上游同源臂与目的基因的连接处预先设计启动子同源区,通过PCR扩增获得上游同源臂、下游同源臂及目的基因3个独立片段,然后利用融合PCR技术将三者连接为含特定启动子的完整片段。随后应用上述基因编辑系统,通过同源重组将该片段精准整合至目标基因座,最终获得整合4种不同启动子的neuC基因工程菌株。关于内源启动子的更换,其中EC23菌株的构建基于EC21菌株进行改造,通过定向敲除目标基因的原始启动子区域,并以带有Ptac组成型强启动子片段通过同源重组实现置换。
pTarget质粒构建的核心操作在于靶序列区域的替换,每次只需基于CHOPCHOP在线工具设计20 bp特异性靶序列,并合成对应的PCR引物对。利用高保真DNA聚合酶扩增质粒载体,经琼脂糖凝胶电泳验证后获取线性化骨架片段。将PCR产物直接转化至E.coli DH5α感受态细胞,在含壮观霉素的LB固体培养基上进行培养。经过16~18 h恒温培养后,随机选取3~5个单菌落进行Sanger测序(金唯智生物技术公司),将序列比对确认正确的菌株进行扩增培养,提取质粒用于后续基因编辑实验。
1.2.2 基因序列与引物合成
基因neuC、neuB、nst[来自脑膜炎奈瑟菌(Neisseria meningitidis)]、neuA[来自空肠弯曲菌(Campylobacter jejuni)]、Vs16[来自弧菌属JT-FAJ-16(Vibrio sp.JT-FAJ-16)]以及实验所使用的引物均由苏州金唯智生物科技有限公司进行合成。
构建质粒和同源臂片段所使用引物见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.042855,下同)。
1.2.3 感受态细胞制备和转化
化学转化采用TAKARA高效制备感受态细胞试剂盒规范制备感受态细胞放-80 ℃冻存。转化时先将装有化转感受态的EP管进行冰浴解冻,加入连接产物混合后先冰浴静置30 min,再经42 ℃水浴90 s处理后37 ℃复苏培养40~60 min,将菌液离心(4 ℃,5 000 r/min)富集后涂布在含相关抗性的LB固体平板上,置于37 ℃培养箱中培养12~16 h。
电转化实验需先在30 ℃培养50 mL菌体(OD600值为0.5~0.7),冰浴30 min后离心(4 ℃,5 000 r/min)收集菌体,再依次用水和10%(质量分数)甘油洗涤处理后分装冻存备用。实验中使用的pTarget质粒需经过基因编辑构建与测序验证,同源模板则通过2轮PCR扩增制备。将质粒与模板按1 000 ng∶2 000 ng混合加入感受态细胞后实施电击转化,经过30 ℃复苏培养2.5 h后涂布于卡那和壮观霉素双抗性平板,最终通过菌落PCR和基因测序对基因编辑效果进行验证,然后挑取菌落在加入0.1%(质量分数)异丙基-β-D-硫代半乳糖者的LB培养基中,30 ℃过夜培养消除pTarget质粒,挑取消除成功的菌落在无抗LB培养基42 ℃过夜培养消除pCas9后即完成整合。
1.2.4 LC-MS检测方法
取1 mL发酵液离心10 min(4 ℃,12 000 r/min),用乙腈萃取上清液2 min,再离心10 min(4 ℃,12 000 r/min)取上清液作为样品检测。
采用ACQUITY Premier UPLC液相色谱系统对样品进行定性分析,色谱柱为ACQUITY BEH Amide(2.1 mm×150 mm,1.7 μm),流动相为10 mmol/L甲酸铵水溶液-乙腈体系,色谱柱柱温40 ℃,流速0.3 mL/min。质谱检测使用电喷雾电离源(electrospray ionization,ESI),在多反应监测模式下设置参数[毛细管电压2.5 kV,离子源温度120 ℃,脱溶剂气温度550 ℃(流速1 100 L/h),锥孔气流速250 L/h],监测母离子632.3 m/z及其特征子离子290.2和408.0 m/z。
1.2.5 HPLC检测方法
取1 mL发酵液样本,于12 000 r/min离心力下进行10 min离心分离。收集上清液经0.22 μm孔径水性微孔滤膜过滤后,转移至液相色谱专用进样瓶。采用配备UV检测器(210 nm)的Agilent 1260高效液相色谱系统,使用Hungpu XBT Amide(4.6 mm×150 mm,3.5 μm)色谱柱进行3′-SL定量分析。流动相组成为V(乙腈)∶V(10 mmol/L甲酸铵)=70∶30,流速恒定1 mL/min,柱温箱设定为60 ℃,进样体积5 μL。
细胞内3′-SL检测操作流程如下:首先将发酵液样品OD600值稀释到5左右,取1 mL在12 000 r/min离心10 min收集菌体,弃上清液后加入等体积超纯水重悬菌体,重复离心-重悬洗涤步骤2次。随后将洗涤后的菌体置于冰水浴超声破碎仪中(全程维持低温),设定功率300 W、工作2 s/间歇4 s的工作参数,破碎20 min至溶液澄清。最后将破碎液于12 000 r/min离心10 min,取上清液经0.22 μm滤膜过滤后装入液相进样瓶检测(最终检测结果需要乘以稀释倍数得到实际产物浓度)。
2 结果与分析
2.1 3′-SL合成途径构建
本研究在E.coli MG1655的基因组整合了neuC、neuB、neuA、Vs16/nst 4个外源基因构建了3′-SL从头合成途径(图1)。
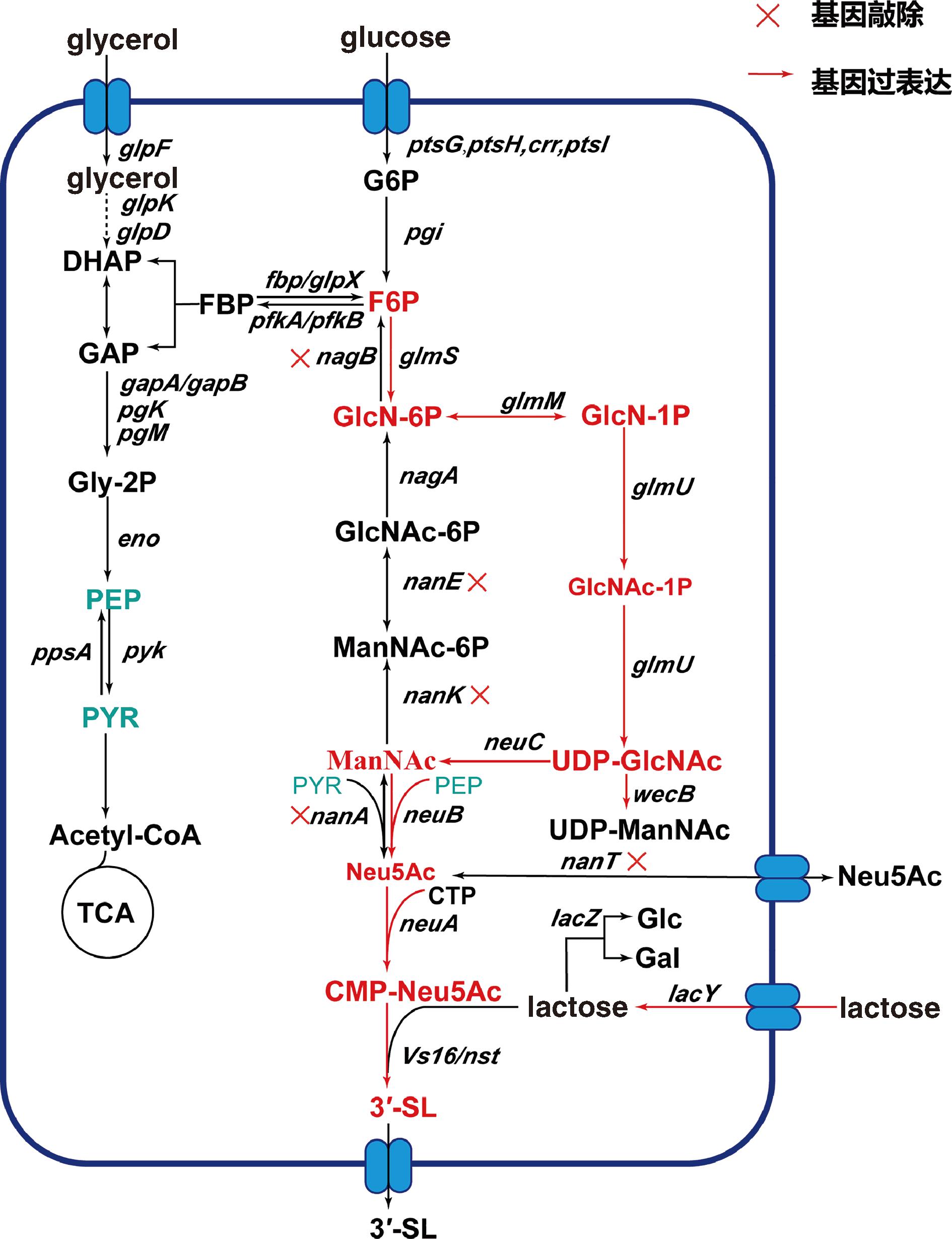
图1 3′-SL合成途径
Fig.1 The 3′-SL synthesis pathway
注:glycerol:甘油;glucose:葡萄糖;DHAP:二羟丙酮磷酸(dihydroxyacetone phosphate);GAP:甘油醛-3-磷酸(glyceraldehyde-3-phosphate);Gly-2P:甘油-2-磷酸(glycerol-2-phosphate);PEP:磷酸烯醇式丙酮酸(phosphoenolpyruvate);PYR:丙酮酸(pyruvate);acetyl-CoA:乙酰辅酶A(acetyl coenzyme A);G6P:葡萄糖-6-磷酸(glucose-6-phosphate);F6P:果糖-6-磷酸(fructose-6-phosphate);GlcN-6P:葡糖胺-6-磷酸(glucosamine-6-phosphate);GlcN-1P:葡糖胺-1-磷酸(glucosamine-1-phosphate);GlcNAc-6P:N-乙酰葡糖胺-6-磷酸(N-acetylglucosamine-6-phosphate);ManNAc-6P:N-乙酰甘露糖胺-6-磷酸(N-acetylmannosamine-6-phosphate);ManNAc:N-乙酰甘露糖胺(N-acetylmannosamine);CMP-Neu5Ac:胞苷单磷酸-N-乙酰神经氨酸(cytidine-monophosphate-Neu5Ac);Glc:葡萄糖(glucose);Gal:半乳糖(galactose);lactose:乳糖;UDP-ManNAc:尿苷二磷酸-N-乙酰甘露糖胺(uridine diphosphate-N-acetylmannosamine);CTP:胞苷三磷酸(cytidine triphosphate);TCA:三羧酸循环(tricarboxylic acid cycle);glpF:编码甘油转运蛋白;glpK:编码甘油激酶;glpD:编码甘油-3-磷酸脱氢酶;gapA/gapB:编码甘油醛-3-磷酸脱氢酶;pgK:编码磷酸甘油酸激酶;pgM:编码磷酸甘油酸变位酶;eno:编码烯醇化酶;ppsA:编码磷酸烯醇式丙酮酸合成酶;pyk:编码丙酮酸激酶;ptsG,ptsH,crr,ptsI:编码磷酸转移酶系统组分;pgi:编码磷酸葡萄糖异构酶;fbp/glpX:编码果糖-1,6-二磷酸酶;pfkA/pfkB:编码磷酸果糖激酶;nagB:编码氨基葡萄糖-6-磷酸异构酶/脱氢酶;glmS:编码葡糖胺-6-磷酸合成酶;glmM:编码葡糖胺-6-磷酸变位酶;glmU:编码葡糖胺-1-磷酸乙酰转移酶/尿苷酰转移酶;nagA:编码N-乙酰葡糖胺-6-磷酸脱乙酰酶;nanE:编码N-乙酰甘露糖胺-6-磷酸异构酶;nanK:编码N-乙酰甘露糖胺激酶;nanA:编码N-乙酰神经氨酸醛缩酶;nanT:编码N-乙酰神经氨酸转运蛋白;lacZ:编码β-半乳糖苷酶;lacY:编码乳糖通透酶;wecB:编码乙酰转移酶。
菌株EC1发酵结果表明(图2),3′-SL标品与发酵样品的出峰时间一致,且质谱检测中的碎片分子质量也一致,证明在E.coli MG1655中合成3′-SL。
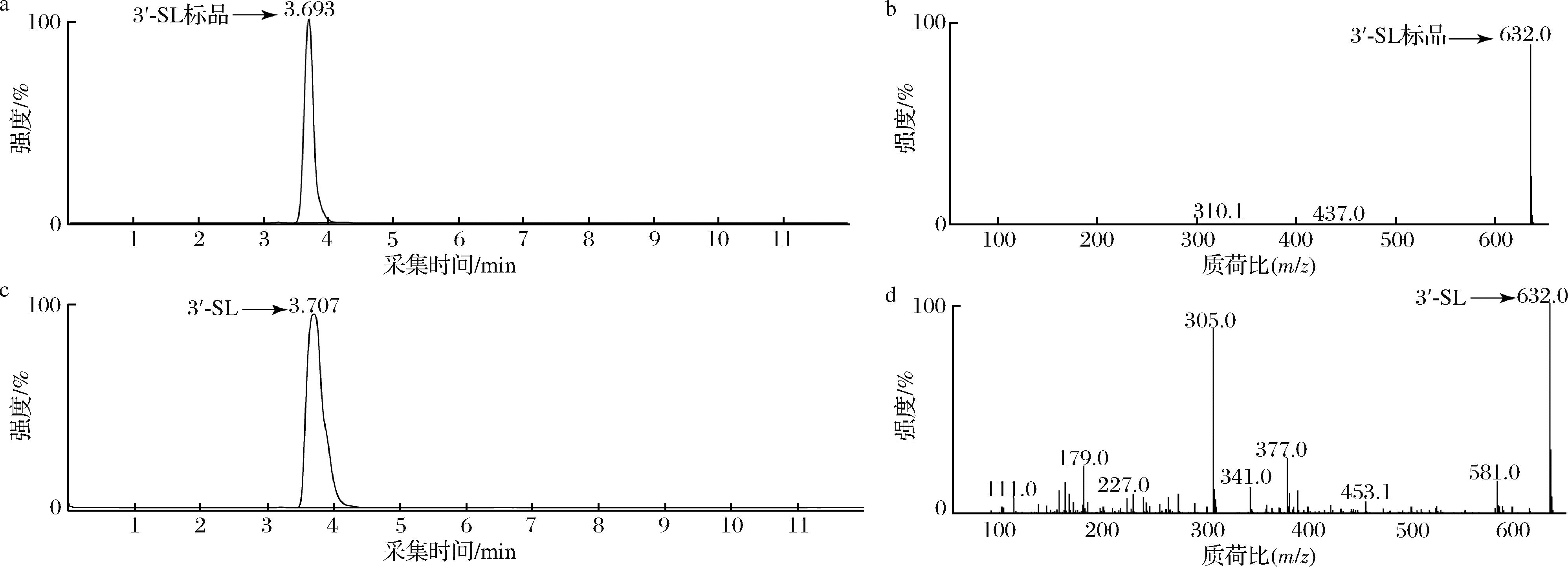
a-3′-SL标准品的LC谱图;b-3′-SL标准品LC峰在3.7 min处的ESI-MS谱图;c-菌株EC1摇瓶培养物的LC谱图;d-菌株EC1摇瓶培养物LC峰在3.7 min处的ESI-MS谱图
图2 基于LC/MS鉴定细胞中合成的3′-SL
Fig.2 LC/MS-based identification of 3′-SL synthesized intracellularly
如图3-a所示,在E.coli MG1655基因组整合组成型启动子P1控制的neuC与neuB基因以及启动子Ptac控制neuA和nst基因得到了菌株EC4,然而发酵结果显示其3′-SL产量较低(14.53 mg/L)且未检测到前体ManNAc,这可能是neuC表达强度过低所导致[15]。为解决该问题,在固定其他3个外源基因表达强度的前提下,通过替换不同组成型启动子来调控neuC的表达强度。结果显示使用组成型强启动子Ptac表达neuC的工程菌株EC1产量达到83.70 mg/L的产物质量浓度,显著高于使用PJ23119、PJ23107、P1启动子的EC2、EC3和EC4,这表明neuC基因表达强度对3′-SL的合成起关键调控作用(图3-b)。
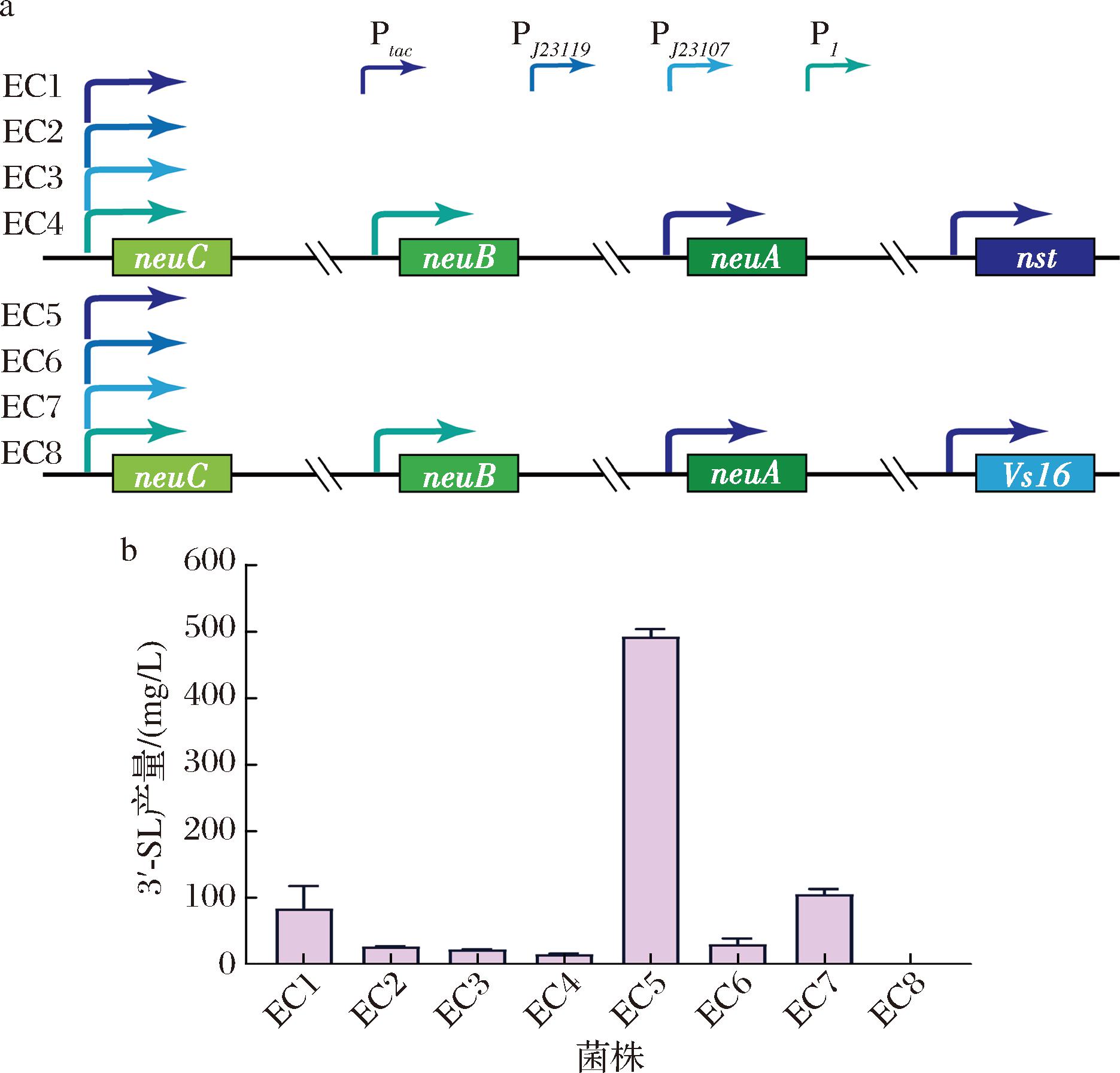
a-初始菌株构建示意图;b-初始菌株产量图
图3 大肠杆菌中3′-SL合成途径的构建
Fig.3 Engineering the 3′-SL biosynthesis pathway in Escherichia coli
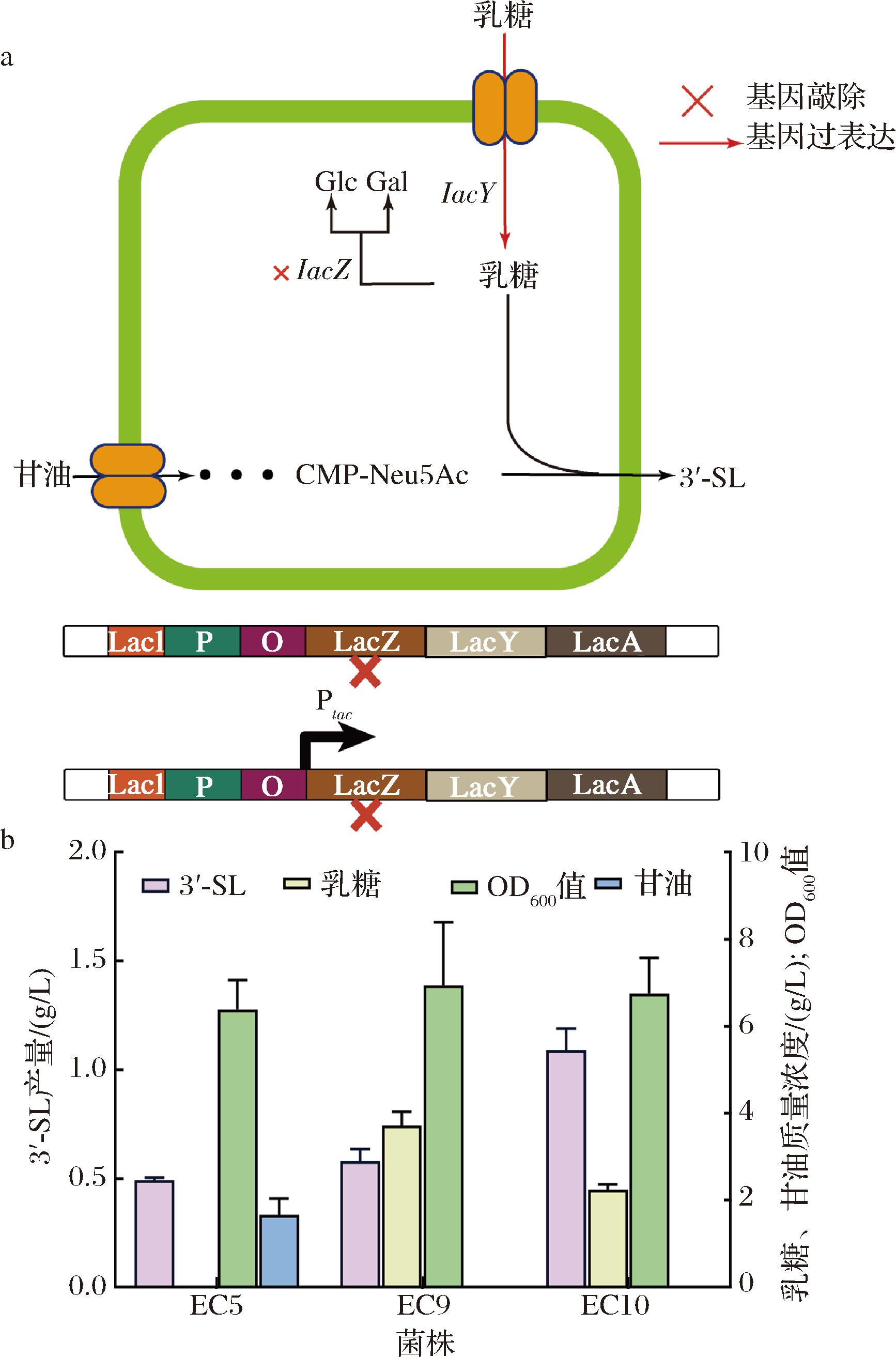
a-乳糖操纵子调控示意图;b-敲除lacZ和强化表达lacY对菌株的影响
图4 乳糖转运系统改造
Fig.4 Lactose transport system modification
在此基础上,对2种不同来源的α-2,3-唾液酸转移酶Nst(N.meningitidis)与Vs16(Vibrio sp.JT-FAJ-16)进行了对比。数据结果显示,采用Vs16的EC5菌株3′-SL产量达到492.51 mg/L,较采用Nst的EC1菌株提升了4.9倍(图2-b)。在Nst菌株体系中,EC2和EC3的产量分别为26.29和21.89 mg/L;而采用Vs16系统的对应菌株EC6(29.81 mg/L)和EC7(105.58 mg/L)均呈现更高产量。
值得注意的是,虽然EC6的neuC启动子PJ23119强度高于EC7,但其产量却低于EC7,这表明基因表达强度与产物产量并非简单正相关,可能更多取决于基因表达水平与宿主代谢网络的适配性。上述结果表明,相较于Nst,Vs16在3′-SL合成过程中具有更高的适配性和催化效率,展现出显著的性能优势。
2.2 乳糖分解/转运系统改造
本研究通过代谢工程策略对工程菌株的乳糖代谢途径进行系统改造,以提升3′-SL的生物合成效率(图4-a)。首先敲除β-半乳糖苷酶编码基因lacZ,该酶会分解乳糖造成底物供应不足。如图4-b所示,对照菌株EC5因lacZ基因的表达,胞内胞外均未检测到乳糖积累,而敲除lacZ基因的菌株EC9胞内外乳糖积累量显著提升,3′-SL的产量达到了0.58 g/L,较对照菌株EC5提升显著(P<0.05),这表明阻断细胞对乳糖的分解代谢可以有效促进3′-SL的合成。
为进一步优化乳糖利用效率,在lacZ敲除菌株EC9基础上强化表达了乳糖通透酶编码基因lacY获得菌株EC10。通过对EC10菌株摇瓶发酵液进行检测,乳糖质量浓度从3.7 g/L降低到2.24 g/L,这可能是因lacY的高表达增加乳糖向胞内转运,增加细胞内乳糖的供应使3′-SL产量最终提升至1.09 g/L,该双重改造菌株EC10展现出协同效应(图4-b),本研究较FIERFORT等[16]报道的lacZ单敲除菌株(0.43 g/L)显著提高0.66 g/L(相对提升153%)。对比EC9与EC10菌株的转化效率差异:前者虽然阻断分解途径,但由于lacY天然表达水平限制,乳糖转运速率成为新的限速步骤。该现象突显代谢工程中代谢流平衡调控的重要性——单纯阻断分解途径虽能积累中间产物,但必须同步强化底物转运能力才能实现代谢网络的整体优化。在理想情况下,1 mol乳糖与1 mol CMP-唾液酸(CMP-Neu5 Ac)反应可生成1 mol 3′-SL,但实际产率受酶活性限制导致转化效率差异(如NeuB、NeuA、NeuC等催化酶效能不同)、底物供应不足(乳糖、CMP-Neu5 Ac等)及副反应损耗(乳糖分解与中间产物代谢分流)的多重制约,EC10菌株消耗1 mol乳糖仅产生0.076 mol 3′-SL,所以后续的高产菌株开发需协调分解代谢抑制与转运/合成模块。
2.3 优化3′-SL合成途径
在改善菌株乳糖供应不足的问题后,本研究进一步采用系统代谢工程策略,对工程菌株EC10的3′-SL合成途径进行了多层次优化,包括强化前体供应、调控碳通量平衡以及过表达关键基因。首先基于底盘菌株EC10,通过分别敲除N-乙酰神经氨酸(Neu5 Ac)分解通路关键基因nanA(编码N-神经氨酸醛缩酶)、nanK(编码N-乙酰甘露糖胺激酶)、nanE(编码N-乙酰甘露糖胺-6-磷酸差向异构酶)及唾液酸转运蛋白编码基因nanT,获得菌株EC11~EC14,发现上述基因的单敲除均可以使产量提升至1.11~1.37 g/L,而组合敲除nanA-K-E-T基因簇构建的EC15菌株产量达1.94 g/L(较EC10提升77.98%,P<0.01),说明通过阻断Neu5Ac的分解代谢并促进胞内积累可以提高3′-SL产量(图5)。
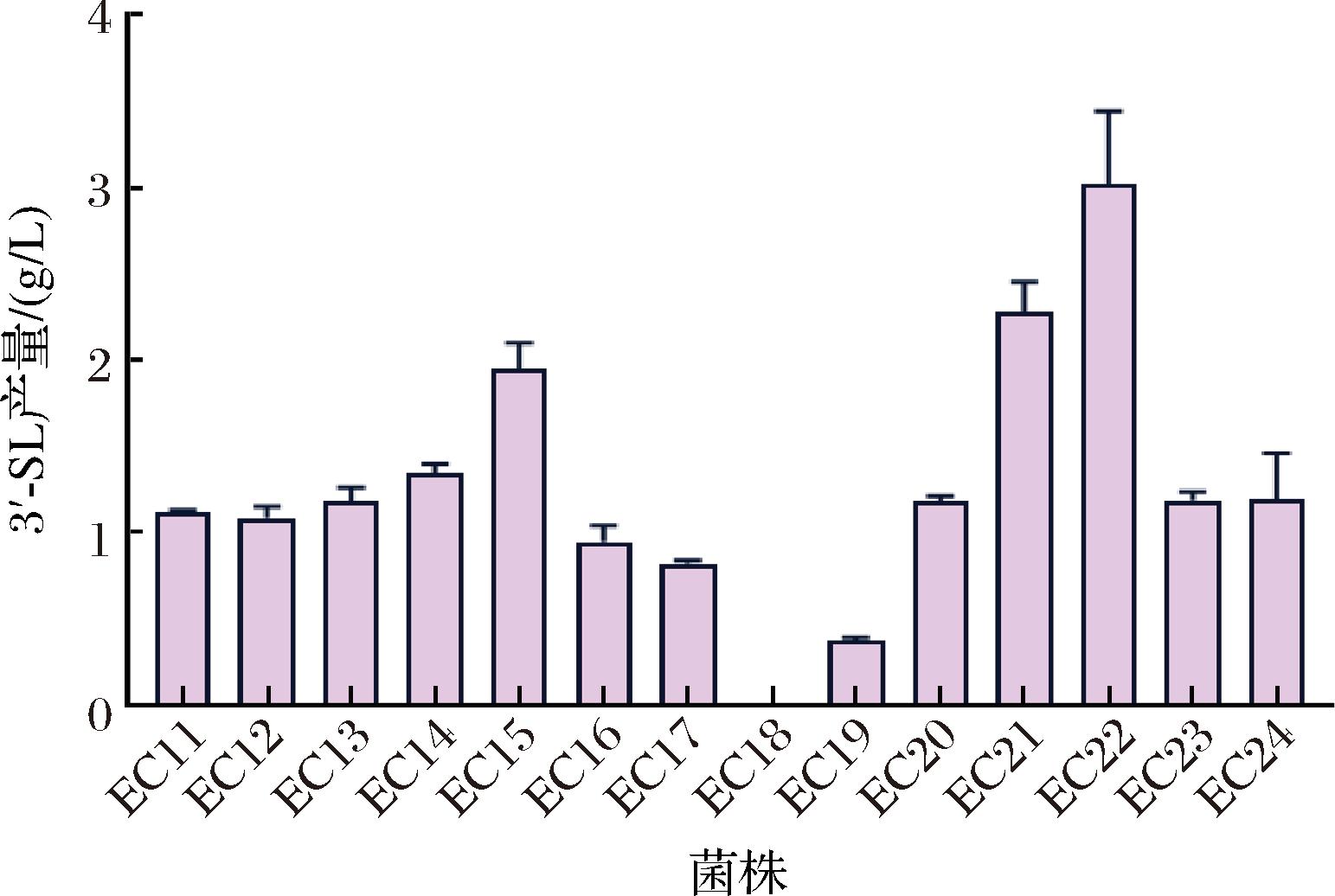
图5 优化关键基因的表达和限制竞争途径调控3′-SL的合成
Fig.5 Optimizing the expression of key genes and rate-limiting enzymes and suppression of competing metabolic pathways to regulate 3′-SL biosynthesis
为了平衡中心碳代谢对细胞生长和3′-SL合成的竞争关系,因此通过在EC10的基础上敲除pfkA/pfkB(6-磷酸果糖激酶A/B,6-phosphofructokinase A/B)阻断果糖-6-磷酸(fructose-6-phosphate,F6P)向果糖-1,6-二磷酸(fructose-1,6-diphosphate,FBP)转化,以增加F6P的积累,结果菌株EC16和EC17的3′-SL的产量分别降低至0.94和0.82 g/L,作为糖酵解的“开关”,pfkA和pfkB的活性直接影响细胞中ATP的生成速率,尤其pfkA突变可能影响碳源利用效率,从而影响生长和生产性能[17]。前体网络优化中,PEP是合成Neu5Ac的重要底物,为了增加其供应,在EC10菌株的基础上敲除PEP的分解途径基因pykA(编码丙酮酸激酶Ⅰ)获得菌株EC18,对其进行摇瓶发酵,结果显示未检测到3′-SL,这可能是由于PEP的代谢干扰导致ATP失衡与途径抑制,本研究的产量下降趋势与LYU等[18]关于敲除pykA产量下降的研究结论相吻合。通过敲除wecB基因(编码UDP-N-乙酰氨基葡萄糖2-异构酶)阻断了UDP-GlcNAc分解路径。作为细胞壁结构成分和ManNAc生物合成前体,UDP-GlcNAc代谢通量的改变可能会激活细菌的应激调控机制,促使能量代谢向维持基础生理活动偏移而非产物合成,最终导致工程菌EC18的产量降低至0.37 g/L。此外,通过敲除nagB基因(编码氨基葡萄糖-6-磷酸脱氨酶)成功阻断了GlcN-6-P分解途径,使工程菌EC20的产量提升至1.18 g/L;基于nagB敲除的正向效果,在已完成唾液酸分解途径优化的EC15菌株(产量1.94 g/L)基础上实施组合敲除策略,构建的EC21工程菌通过协同优化使碳通量高效汇聚至目标产物,最终产量提升至2.28 g/L(图5)。
在EC21基础上,对关键基因表达进行强化,直接过表达glmS(编码6-磷酸氨基葡萄糖合成酶)、glmU(编码葡萄糖胺-1-磷酸乙酰转移酶)和glmM(编码磷酸葡萄糖胺变位酶)的EC22菌株产量达3.02 g/L(提升32.46%),显著优于启动子替换策略的EC23(1.18 g/L),而外源基因neuC、neuB和neuA的过表达导致EC24产量下降至1.85 g/L,推测因组成型表达引发代谢压力。研究发现,竞争途径敲除与前体调控协同可有效提升产量,但需平衡碳通量重定向与能量稳态,外源基因表达需优化调控元件以减轻代谢负担,后续将通过动态调控与工艺优化进一步提升合成效率。综合实验数据分析表明,EC22菌株表现出优于其他菌株的产物合成效率,因此被用于后续发酵工艺优化研究。
2.4 3′-SL在3 L生物反应器的放大生产
为了证明3′-SL菌株EC22的大规模生产潜力,本研究在3 L生物反应器中进行了间歇补料发酵(图6)。菌株EC22在培养28 h后快速生产3′-SL,108 h达到最高值,胞内加胞外的产量为14.85 g/L,比摇瓶培养增加了5倍,3′-SL的总生产强度为0.13 g/(L·h)。分析结果发现胞内3′-SL的累积量最高达到3.66 g/L,已有文献报道可以表达scrY,增加产物向胞外转运,说明3′-SL的生产效率仍有提高的空间,应进一步减少细胞内3′-SL在细胞内的积累,提高生产效率[18]。3 L生物反应器放大验证表明,本研究构建的无质粒且组成型表达关键基因的3′-SL合成菌株无需外源诱导即可实现菌体生长与产物合成的同步化。通过调控代谢通量平衡策略,成功维持菌株高效生产,使工程菌株在放大生产过程中展现出稳定的高效合成能力。
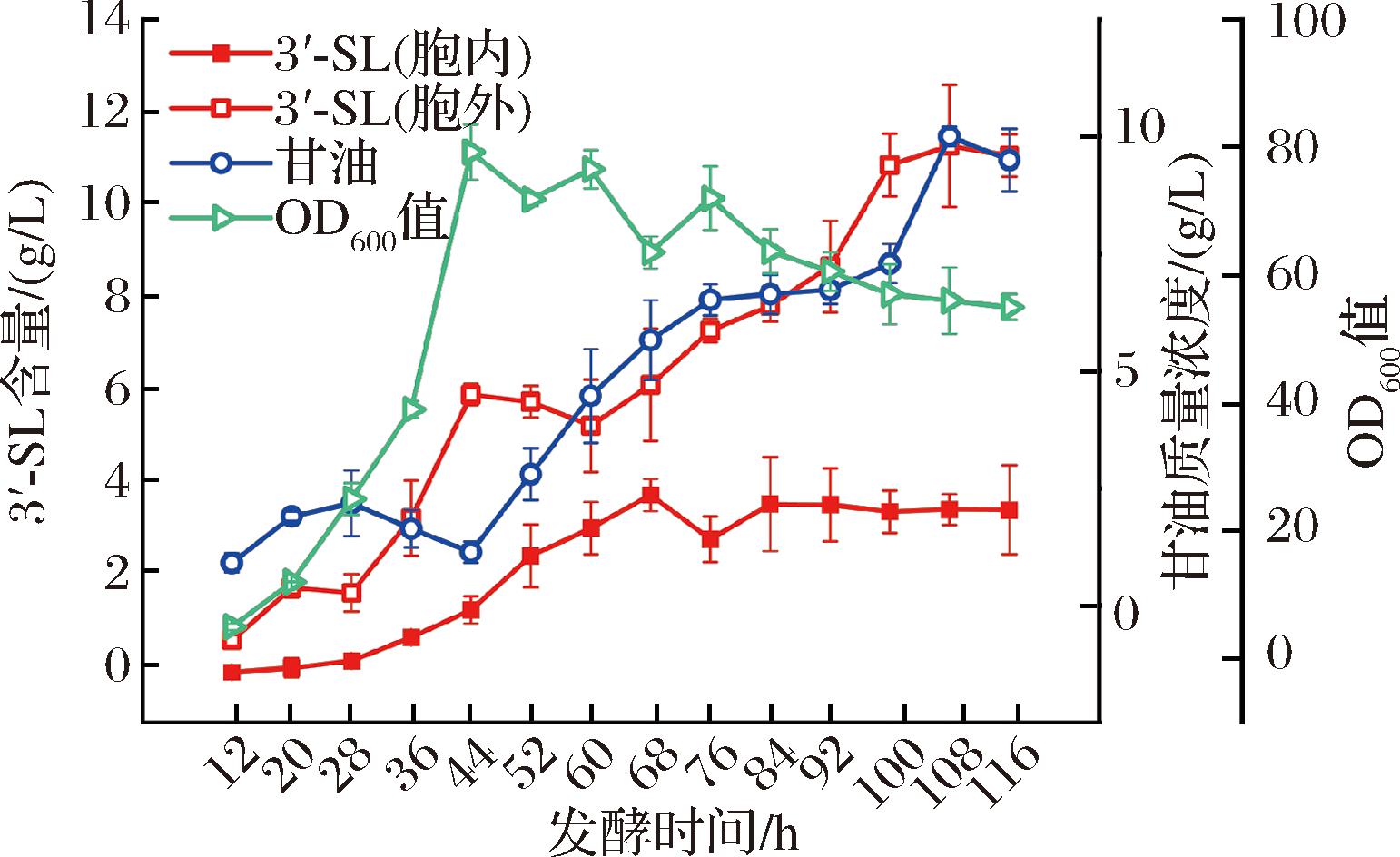
图6 3 L发酵罐补料分批发酵
Fig.6 Fed-batch fermentation in a 3-L bioreactor
3 结论
本研究以E.coli MG1655为底盘细胞,通过整合neuC、neuB、neuA和Vs16/nst基因构建了无质粒、无需诱导剂的3′-SL从头合成途径,相较于传统混菌耦合发酵[19],本研究所采用的单一菌株从头合成策略避免了添加更多的底物,简化了发酵步骤且降低底物成本。针对代谢瓶颈展开系统性优化:通过调控neuC基因表达平衡代谢流、敲除lacZ基因阻断乳糖分解代谢、过表达lacY强化乳糖转运效率,使3′-SL产量提升至1.09 g/L;进一步通过敲除nanA-K-E-T基因簇和nagB基因解除前体供应限制后,目标产物产量提升至1.94 g/L,与ZHANG等[14]研究中采用质粒表达并敲除lacZ、nanA及nanK基因的菌株EZAK1产量(1.99 g/L)仅相差0.05 g/L;最终过表达glmS-U-M后在摇瓶中实现3.02 g/L产量,并在3 L发酵罐中达到14.85 g/L[生产强度0.13 g/(L·h)]。值得注意的是,本研究通过基因组整合替代组成型启动子,相较于传统质粒依赖与诱导表达系统,本研究所采用的基因组整合策略避免了质粒丢失风险,同时消除了抗生素对发酵过程的干扰,为3′-SL工业化生产提供了高效稳定的微生物细胞工厂。然而,分泌效率瓶颈与代谢负荷累积问题表明,未来需整合合成生物学工具(如动态代谢开关、群体感应系统)实现代谢通量的时空精准调控,推动研究成果向工业化应用转化[20-22]。
[1] ZHANG Q W,LIU Z M,XIA H Z,et al.Engineered Bacillus subtilis for the de novo production of 2′-fucosyllactose[J].Microbial Cell Factories,2022,21(1):110.
[2] OOZEER R,VAN LIMPT K,LUDWIG T,et al.Intestinal microbiology in early life:Specific prebiotics can have similar functionalities as human-milk oligosaccharides[J].The American Journal of Clinical Nutrition,2013,98(2):561S-571S.
[3] KUNZ C.Historical aspects of human milk oligosaccharides[J].Advances in Nutrition,2012,3(3):430S-439S.
[4] RUIZ-PALACIOS G M,CERVANTES L E,RAMOS P,et al.Campylobacter jejuni binds intestinal H(O) antigen (Fucα1,2Galβ1,4GlcNAc),and fucosyloligosaccharides of human milk inhibit its binding and infection[J].Journal of Biological Chemistry,2003,278(16):14112-14120.
[5] ANDERSSON B,PORRAS O,HANSON L A,et al.Inhibition of attachment of Streptococcus pneumoniae and Haemophilus influenzae by human milk and receptor oligosaccharides[J].The Journal of Infectious Diseases,1986,153(2):232-237.
[6] ASAKUMA S,AKAHORI M,KIMURA K,et al.Sialyl oligosaccharides of human colostrum:Changes in concentration during the first three days of lactation[J].Bioscience,Biotechnology,and Biochemistry,2007,71(6):1447-1451.
[7] PÉREZ-ESCALANTE E,ALATORRE-SANTAMAR A S,CASTA
A S,CASTA EDA-OVANDO A,et al.Human milk oligosaccharides as bioactive compounds in infant formula:Recent advances and trends in synthetic methods[J].Critical Reviews in Food Science and Nutrition,2022,62(1):181-214.
EDA-OVANDO A,et al.Human milk oligosaccharides as bioactive compounds in infant formula:Recent advances and trends in synthetic methods[J].Critical Reviews in Food Science and Nutrition,2022,62(1):181-214.
[8] WALSH C,LANE J A,VAN SINDEREN D,et al.From lab bench to formulated ingredient:Characterization,production,and commercialization of human milk oligosaccharides[J].Journal of Functional Foods,2020,72:104052.
[9] KENDALL S K.Encyclopedia of life sciences[J].The Charleston Advisor,2012,13(3):19-21.
[10] BLOUNT Z D.The unexhausted potential of E.coli[J].eLife,2015,4:e05826.
[11] KEASLING J D.Manufacturing molecules through metabolic engineering[J].Science,2010,330(6009):1355-1358.
[12] PRIEM B,GILBERT M,WAKARCHUK W W,et al.A new fermentation process allows large-scale production of human milk oligosaccharides by metabolically engineered bacteria[J].Glycobiology,2002,12(4):235-240.
[13] GUO Y,JERS C,MEYER A S,et al.A Pasteurella multocida sialyltransferase displaying dual trans-sialidase activities for production of 3′-sialyl and 6′-sialyl glycans[J].Journal of Biotechnology,2014,170:60-67.
[14] ZHANG J M,ZHU Y Y,ZHANG W L,et al.Efficient production of a functional human milk oligosaccharide 3′-sialyllactose in genetically engineered Escherichia coli[J].ACS Synthetic Biology,2022,11(8):2837-2845.
[15] LIU C,LYU X Q,LI J H,et al.Metabolic engineering of Escherichia coli for increased bioproduction of N-acetylneuraminic acid[J].Journal of Agricultural and Food Chemistry,2022,70(50):15859-15868.
[16] FIERFORT N,SAMAIN E.Genetic engineering of Escherichia coli for the economical production of sialylated oligosaccharides[J].Journal of Biotechnology,2008,134(3-4):261-265.
[17] HOLLINSHEAD W D,RODRIGUEZ S,MARTIN H G,et al.Examining Escherichia coli glycolytic pathways,catabolite repression,and metabolite channeling using Δ pfk mutants[J].Biotechnology for Biofuels,2016,9(1):212.
[18] LYU X Y,CHEN X S,LIU Y F,et al.Efficient production of 3′-sialyllactose using Escherichia coli[J].Journal of Agricultural and Food Chemistry,2024,72(49):27314-27325.
[19] ENDO T,KOIZUMI S,TABATA K,et al.Large-scale production of CMP-NeuAc and sialylated oligosaccharides through bacterial coupling[J].Applied Microbiology and Biotechnology,2000,53(3):257-261.
[20] MIRSALAMI S M,MIRSALAMI M.Advances in genetically engineered microorganisms:Transforming food production through precision fermentation and synthetic biology[J].Future Foods,2025,11:100601.
[21] NIU T F,LIU Y F,LI J H,et al.Engineering a glucosamine-6-phosphate responsive glmS ribozyme switch enables dynamic control of metabolic flux in Bacillus subtilis for overproduction of N-acetylglucosamine[J].ACS Synthetic Biology,2018,7(10):2423-2435.
[22] GU P F,MA Q Q,ZHAO S,et al.Application of quorum sensing system in microbial synthesis of valuable chemicals:A mini-review[J].World Journal of Microbiology and Biotechnology,2022,38(11):192.