汤是我国居民日常饮食中不可或缺的一部分,炖汤过程食材会发生一系列生物化学反应,原料的营养成分及结构也会相应发生变化[1]。牛骨白汤是将牛骨通过破碎并熬煮,继而提取、汤油分离、风味调配和骨汤浓缩,最后进行调和乳化而制作出来的高汤类半固态复合调味料[2]。牛骨白汤不仅可以增加食物的香味和口感,而且含有丰富的胶原蛋白、维生素和钙质等营养成分,有补气、活血和健脾开胃等功效[3]。因此,在食品行业应用广泛,例如餐饮行业通过对牛骨白汤进行稀释,用于火锅、麻辣烫和汤面等的汤底制备。然而这类产品在食品行业实际应用过程中由于煮制温度的不同出现了聚集、破乳、分层等不稳定的现象,导致消费者的感官体验受到影响。目前,关于牛骨白汤的研究集中在调味配方及工艺的改善,而忽略了其应用过程中煮制带来的影响。为了解决这一问题,本实验以牛骨白汤为原料,探究其在不同温度下乳化体系稳定性的差异。
影响乳化体系稳定性的因素较多,包括乳液浓度、油体积分数、pH值、离子强度、加工方式以及酶解程度等[4-5]。餐饮行业中经常用不同温度(60~100 ℃)炖煮高汤,而加热温度对汤的稳定性有一定的影响,可能会使乳液不稳定,随着温度升高,乳液液滴的沉降和团聚速率逐渐增大,导致乳液体系不稳定[6]。近些年大部分研究集中在温度、时间这2个协同因素对乳液稳定性的影响。朱秀清等[7]分析了热处理对汉麻乳稳定性的影响,发现在65 ℃时,汉麻乳乳化稳定性最强。高飞等[8]研究发现70 ℃热处理时,金枪鱼蛋白乳液的各项指标整体优于其他组,且贮藏28 d未出现分层情况,乳液的稳定性显著提高。DYBOWSKA等[9]证明了乳清蛋白分散体或乳液热处理对水包油乳液稳定性有一定的影响,发现60 ℃加热的蛋白质乳液稳定性较差,70 ℃处理对乳液稳定性影响较小,70 ℃以上温度对乳液稳定性影响最明显。这些报道为研究牛骨白汤体系提供了参考,由于煮制温度和时间等参数的差异,会影响牛骨白汤的乳化稳定性。
目前,温度对牛骨白汤煮制过程中乳化体系稳定性差异研究鲜有报道,因此本文以牛骨白汤为研究对象,通过测定不同温度热处理(60、80、100 ℃)下牛骨白汤乳化活性(emulsifying activity index,EAI)、乳化稳定性(emulsification activity index,ESI)、黏度、zeta电位、粒径、表面疏水性和荧光光谱等指标,研究煮制温度对牛骨白汤乳化体系稳定性的影响,为牛骨白汤实际生产应用提供一定的理论参考。
1 材料与方法
1.1 材料与试剂
牛骨白汤,青岛汇泽食品配料有限公司;十二烷基硫酸钠(sodium dodecyl sulfate,SDS),天津华盛有限公司;PBS,爱必信生物科技有限公司;溴酚蓝,百克赛斯生物科技有限公司。所有试剂均为分析纯。
1.2 仪器与设备
Nikon ECLIPSE BOi光学显微镜,日本尼康公司;UV-759CRT 紫外分光光度计、HHCC-45121型恒温水浴锅,青岛聚创世纪环保科技有限公司;FL-4600荧光分光光度计,日本日立公司;Zatatronix 939SZ多角度纳米粒度仪,上海澳普特科技有限公司;TMNDJ-5S天马数显黏度计,天津天马衡基仪器有限公司。
1.3 实验方法
1.3.1 牛骨白汤的制备
操作要点:将浓缩牛骨白汤用蒸馏水冲调,静置备用。分别在60、80、100 ℃加热牛骨白汤,对照组置于常温下(25 ℃)。
1.3.2 EAI、ESI的测定
参考HU等[10]的方法并稍作修改进行EAI和ESI的测定。样品和SDS溶液(0.1%,体积分数)以1∶100稀释混匀,在波长500 nm处测量初始吸光度值A0,10 min后的吸光度值为A10。EAI和ESI计算分别如公式(1)和公式(2)所示:
(1)
(2)
式中:N为稀释倍数;φ为油相分数,%;c为蛋白质质量浓度,mg/mL;Δt为时间间隔。
1.3.3 黏度的测定
黏度的测定参照郝梦等[11]的方法并稍作修改,数字黏度计选用4号转子,60×g转速,取50 mL样进行测定,时间为60 s。
1.3.4 粒径和Zeta 电位的测定
牛骨白汤的粒径和电位的测定参照CHEN等[12]的方法稍作修改。取牛骨白汤将其稀释250倍,以蒸馏水为分散介质,用纳米粒度仪测量其液滴粒径分布及Zeta电位。
1.3.5 表面疏水性的测定
牛骨白汤表面疏水性的测定参考高飞等[8]的方法测定并稍加修改。1 mL样品中加入200 μL溴酚蓝(1 g/L),混匀后离心。上清液稀释10倍后测定其吸光度(波长595 nm)。表面疏水性计算如公式(3)所示:
表面疏水性![]()
(3)
式中:A1表示空白样品的吸光度,A2表示样品的吸光度。
1.3.6 荧光光谱的采集
参照HE等[13]的方法并稍作修改,用10 mol/L PBS(pH 7.0)将样品稀释至1.0 mg/mL。测定参数为:激发波长为290 nm,发射波长为400~700 nm,狭缝宽度都为5 nm。
1.4 数据处理及分析
每组平行测定3次及以上,表示为“平均值±标准差”。采用SPSS 26.0进行单因素方差分析(P<0.05为差异显著),利用Origin 2021绘图。
2 结果与分析
2.1 不同煮制温度对牛骨白汤乳化活性和乳化稳定性的影响
为了比较不同煮制温度对牛骨白汤乳化性和乳化稳定性的影响,测量了牛骨白汤的EAI和ESI。EAI反映了蛋白质形成乳化体系的能力[14]。由图1可知,煮制温度对牛骨白汤的EAI影响显著(P<0.05)。对照组EAI为9.18 m2/g,不同煮制温度(60、80、100 ℃)下,EAI随着煮制温度升高和时间的延长,呈先上升后下降的趋势(P<0.05),特别当煮制温度为80 ℃时,EAI与对照组相比有所增加,在煮制温度为80 ℃,3 h时达到最大值10.51 m2/g。但在煮制温度为60 ℃和80 ℃时,EAI与对照组相比有所下降。这与MA等[15]研究报道的结果一致。分析其原因可能是在煮制温度为80 ℃时,界面处的蛋白质吸附量增多,暴露出更多疏水基团覆盖在油滴表面,蛋白质二级结构展开,增强了蛋白质之间的疏水相互作用[16],使EAI最佳。然而当温度超过一定范围时,蛋白空间结构遭到破坏[17],从而加剧了絮凝和聚集现象,EAI随之降低。
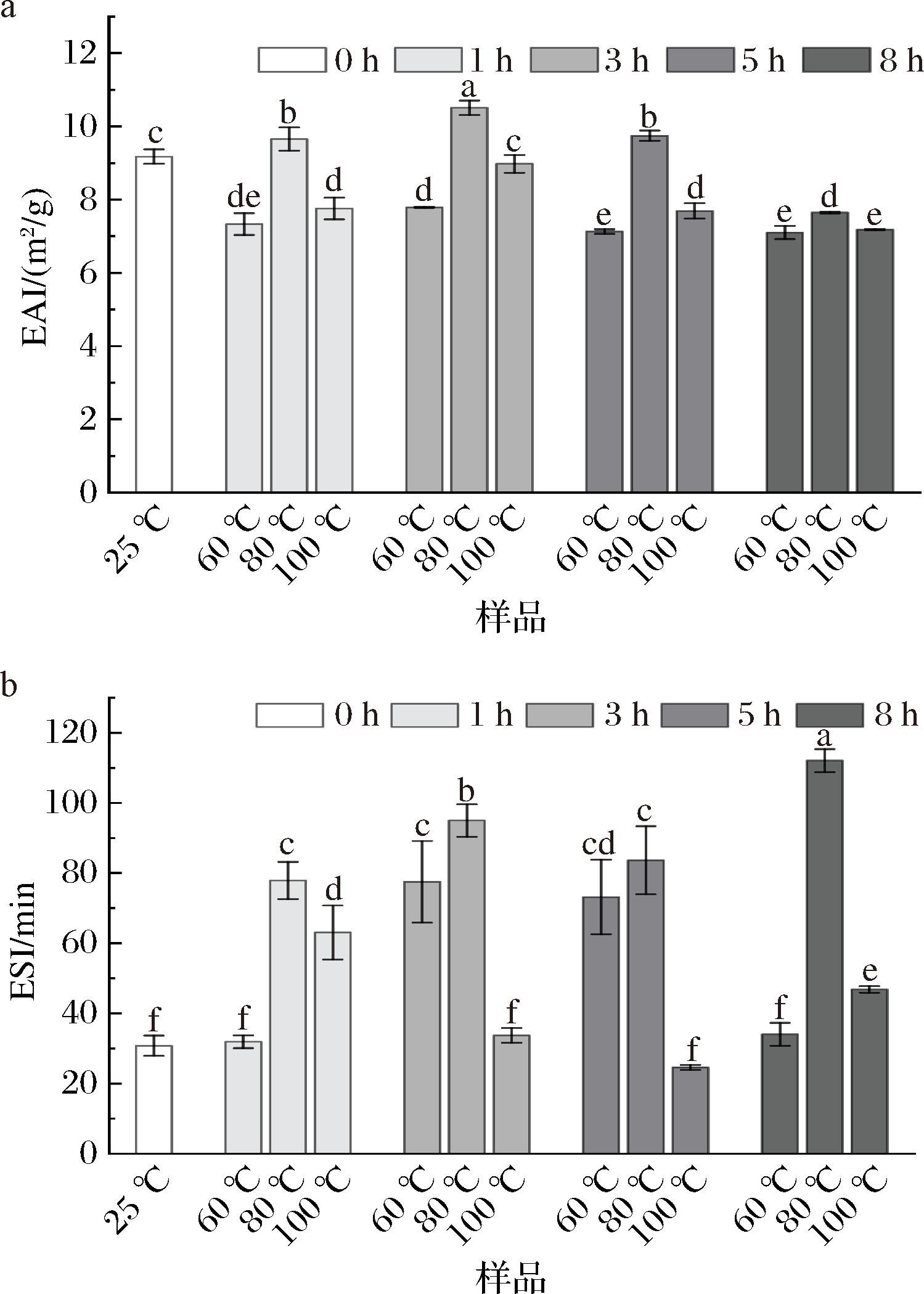
a-EAI;b-ESI
图1 不同煮制温度对牛骨白汤EAI和ESI的影响
Fig.1 Effect of different cooking temperatures on emulsification and emulsification stability of bovine bone white soup
注:上标字母完全不同表示差异显著(P<0.05)(下同)。
ESI表征了乳化体系的稳定能力[14]。由图1可知,随着煮制温度的升高,ESI呈现先上升后下降的趋势。煮制过程中ESI会增加,对照组的牛骨白汤ESI为30.76 min,在煮制温度为80 ℃,8 h时达到最大值112.06 min,但随着温度的进一步升高,ESI逐渐下降。在煮制温度为100 ℃、煮制5 h时,ESI最低,为24.58 min。分析其原因可能是在60~100 ℃,随着温度的升高,降低了液滴碰撞和聚集的可能性,同时增加了与油-水界面接触的几率[18],从而提高了ESI;然而随着煮制温度的进一步升高,会加速液滴的运动,容易引发聚集或絮凝,导致乳化体系失稳。
总而言之,煮制温度80 ℃有利于EAI和ESI的提高,但温度过高或处理时间过长则会导致EAI降低。综合考虑,为保持牛骨白汤良好的EAI和ESI,煮制过程中应避免过高的温度。
2.2 不同煮制温度对牛骨白汤黏度的影响
黏度可以反映牛骨白汤中液体流动性,黏度越大乳液越稳定[11]。不同温度和煮制时间下牛骨白汤的黏度结果如图2所示,在同一时间不同煮制温度下,随着煮制温度的升高,乳液的黏度呈现先增大后减小的趋势。对照组的黏度为2.42 Pa·s,在煮制温度为80 ℃,3 h时达到最大值2.65 Pa·s,这是因为煮制温度为80 ℃时乳液粒径减小,液滴间的相互作用力增强,导致液滴间的摩擦力增大,从而使黏度增加;而当煮制温度进一步升高到100 ℃时黏度反而减小,这可能是部分蛋白高级结构在高温煮制过程中发生了折叠,也可能是原来位于蛋白分子内部的某些疏水基团暴露[19],油滴聚集或絮凝现象增多,导致黏度减小,高飞等[8]通过对金枪鱼蛋白乳液进行不同温度的(30~90 ℃)热处理,发现经70 ℃加热30 min后金枪鱼蛋白乳液黏度最大,这与本研究结果一致。随着煮制时间的延长,黏度减小,可能是由于煮制时间过长导致乳液的平均粒径增大,蛋白质与油滴间的疏水相互作用减弱,蛋白质结构趋于无序,从而导致黏度下降。综上,80 ℃的煮制温度有助于提高牛骨白汤的黏度。
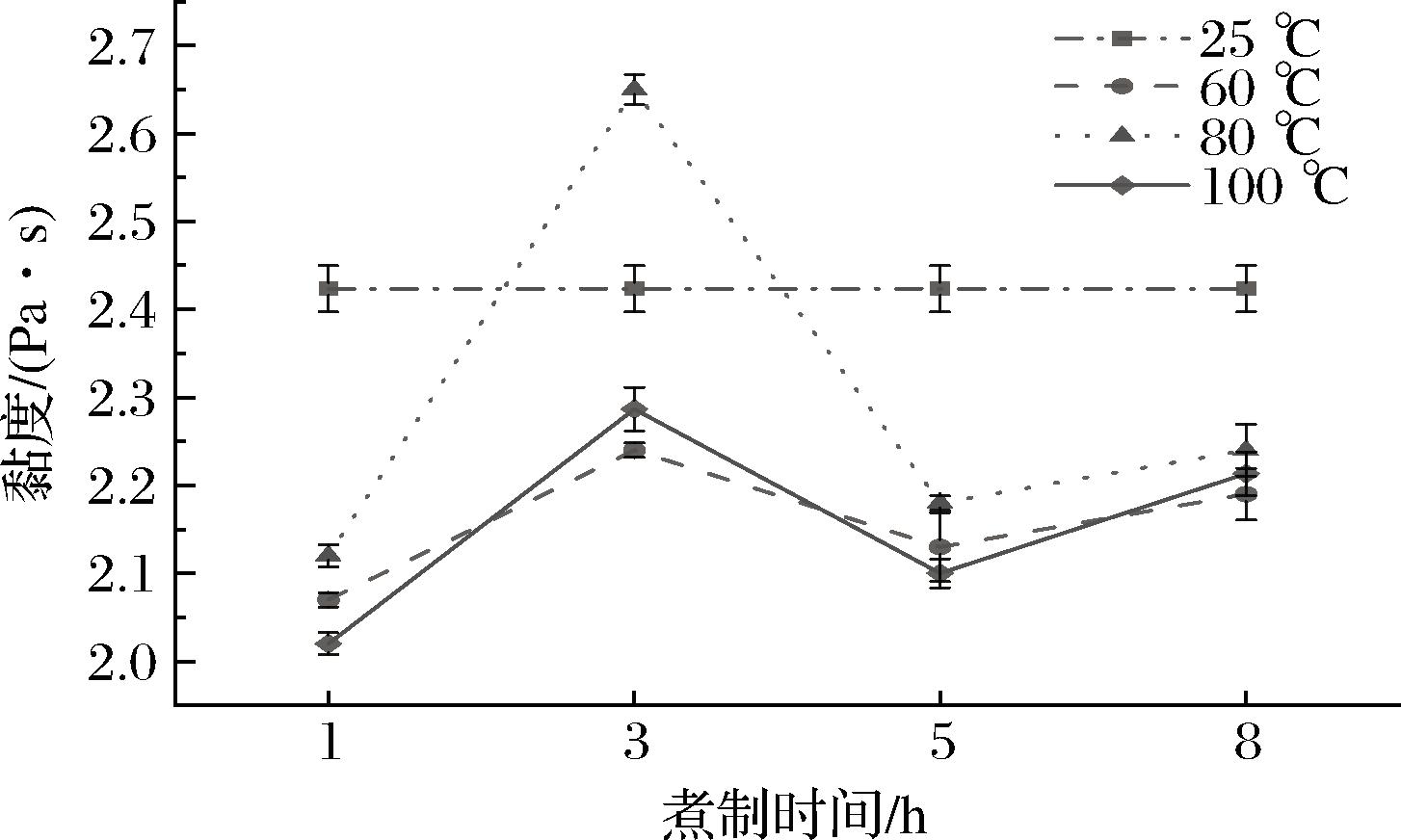
图2 不同煮制温度对牛骨白汤粘黏度的影响
Fig.2 Effect of different cooking temperatures on the viscosity of bovine bone white soup
2.3 不同煮制温度对牛骨白汤粒径的影响
液滴颗粒粒径的大小可用于评价乳液乳化能力,乳化体系越稳定,液滴粒径越小[20]。由图3和图4可知,在不同煮制温度下,随着煮制温度的升高,乳液粒径呈现先减小后增大的趋势(P<0.05)。对照组的平均粒径大小为468.4 nm,当煮制温度为80 ℃,煮制3 h时牛骨白汤的平均粒径最小,为422.5 nm,较对照组降低了45.9 nm,这表明,在一定煮制温度范围内,蛋白分子在界面展开了重排,增强了蛋白分子的疏水作用,使液滴保持更长时间的分散,煮制时间越长平均粒径越大。80 ℃下煮制的牛骨白汤乳液平均粒径最小,可能是加热过程使更多的蛋白分子包裹着油滴颗粒,暴露了原本被掩藏的非极性基团,增加了与油-水界面的接触,导致颗粒不易结聚或絮凝,同时,加热过程也提高了乳液黏度,导致液滴颗粒的聚集受阻[21],乳液稳定性增强。煮制温度超过80 ℃时,乳液的平均粒径增大,这可能是因为在达到一定的温度后,蛋白质形成了可溶性聚集体,其空间位阻效应不利于形成稳定的油-水界面[22],导致油滴之间发生聚集,粒径随之增大。综上所述,煮制温度为80 ℃时,牛骨白汤乳液粒径最小,证明其稳定性最好。这与CHEN等[12]研究的热处理对乳清分离蛋白稳定水包油(oil in water,O/W)乳液的物理稳定性、界面组成及蛋白-脂质共氧化的影响结果一致。
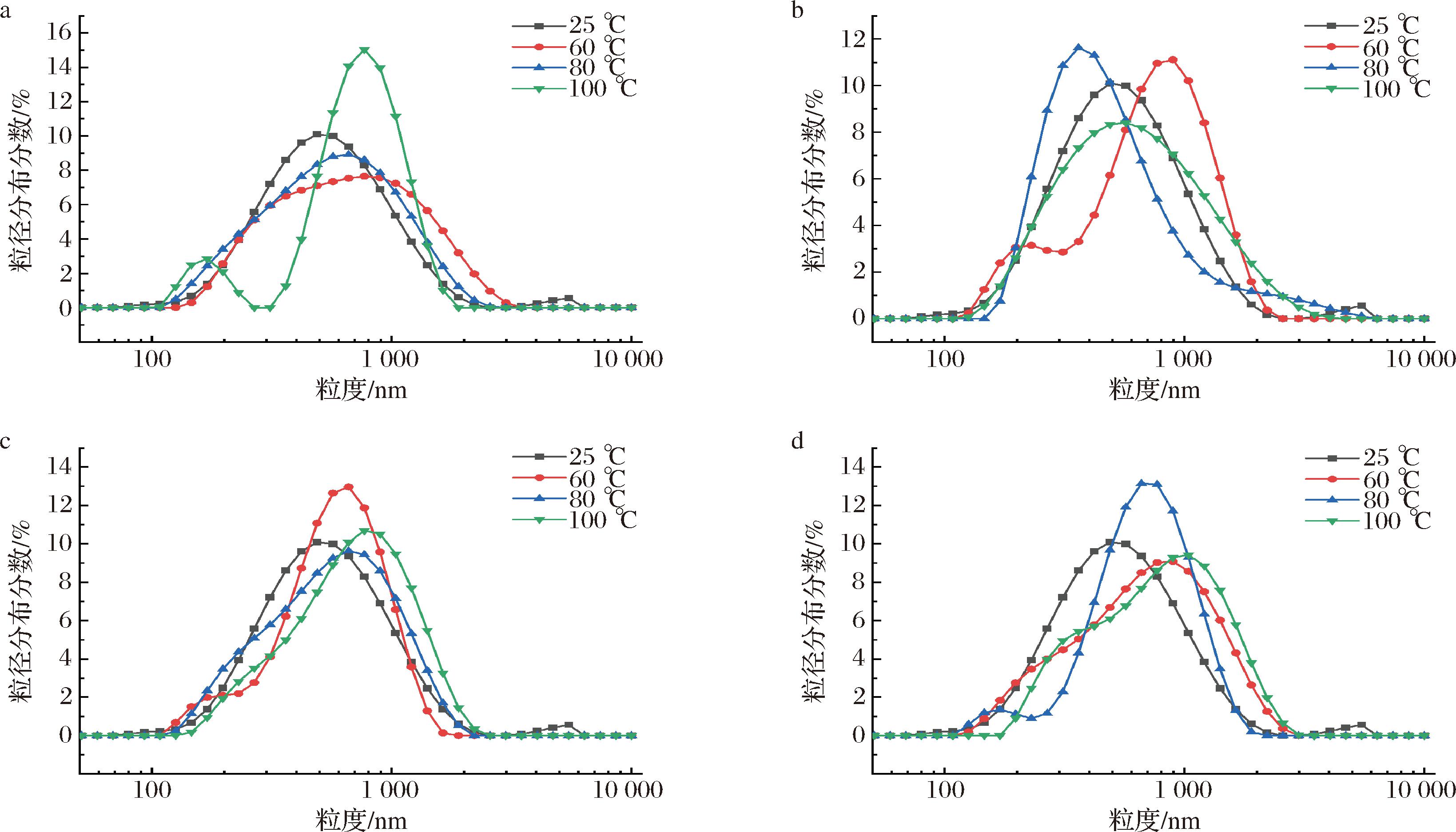
a-1 h;b-3 h;c-5 h;d-8 h
图3 不同煮制温度对牛骨白汤粒径分布的影响
Fig.3 Effect of different cooking temperatures on particle size distribution of bovine bone white soup
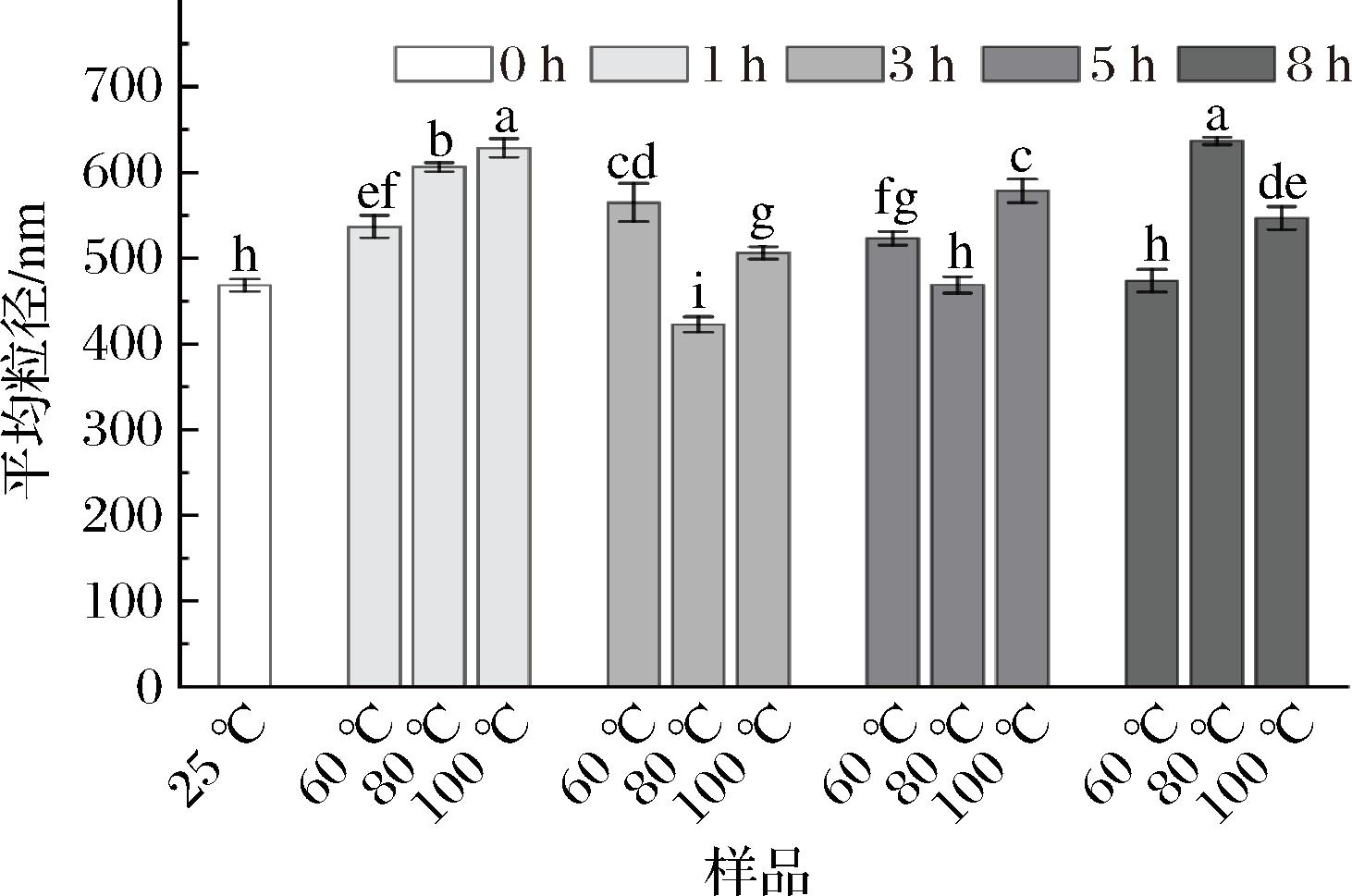
图4 不同煮制温度对牛骨白汤平均粒径的影响
Fig.4 Effect of different cooking temperatures on average particle size of bovine bone white soup
2.4 不同煮制温度对牛骨白汤Zeta电位的影响
Zeta电位可以表征乳液中颗粒表面的电荷量,与乳液液滴间的相互排斥或吸引有关[23]。Zeta电位的绝对值越大,说明乳滴分散性好,很少产生聚集,体系越趋于稳定[24]。由表1可知,在不同煮制温度(60、80、100 ℃)下,随着煮制温度的升高,牛骨白汤的Zeta电位绝对值增大,在温度为80 ℃煮制3 h时的Zeta电位绝对值达到最大,为18.70 mV(P<0.05),分析其原因可能是因为加热过程导致氨基酸残基和带电基团暴露到蛋白质分子表面,使得蛋白质结构发生无规则的卷曲,改变了蛋白质分子构象,增加了表面负电荷的数量,进而增强了静电斥力,抑制了液滴的聚集[25],使乳液体系更加稳定。ZHAO等[26]的研究报道与本研究结果一致,该研究发现谷蛋白在100 ℃加热60 min后,表面电位绝对值显著增大,说明带负电氨基酸基团的暴露能够增强蛋白质分子柔性,使乳液趋于稳定。然而,当煮制温度继续升高时,乳液表面电位绝对值却降低,分析其原因可能是高温导致更多带正电荷的基团暴露,减弱了液滴间的静电排斥作用[27],从而加剧乳液絮凝现象的产生。
表1 不同煮制温度对牛骨白汤Zeta电位的影响
Table 1 Effect of different cooking temperatures on Zeta potential of bovine bone white soup
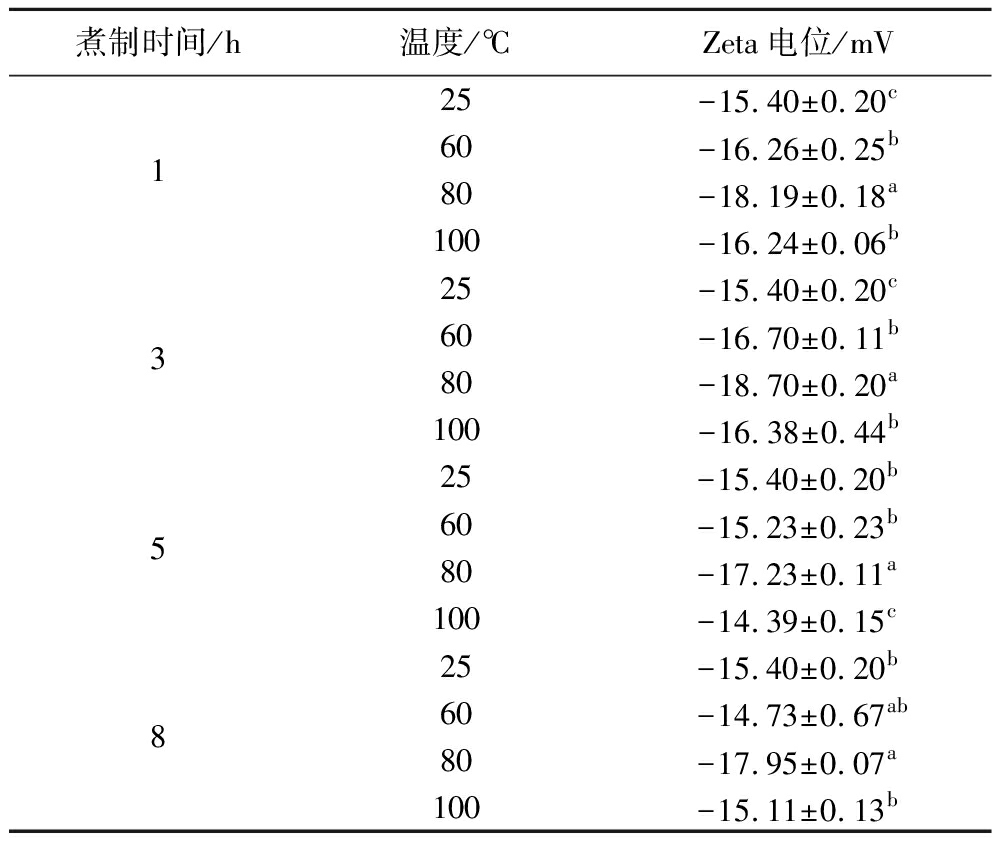
煮制时间/h温度/℃Zeta电位/mV125-15.40±0.20c60-16.26±0.25b80-18.19±0.18a100-16.24±0.06b325-15.40±0.20c60-16.70±0.11b80-18.70±0.20a100-16.38±0.44b525-15.40±0.20b60-15.23±0.23b80-17.23±0.11a100-14.39±0.15c825-15.40±0.20b60-14.73±0.67ab80-17.95±0.07a100-15.11±0.13b
注:在同一煮制时间下,同列均值上标字母完全不同表示差异显著(P<0.05)。
2.5 不同煮制温度对牛骨白汤表面疏水性的影响
表面疏水性表征暴露在蛋白质表面的疏水基团,反映了蛋白质分子的聚集倾向[15]。不同煮制温度下牛骨白汤表面疏水性变化如图5所示。对照组的表面疏水系数为29.34 μg,煮制过后牛骨白汤的表面疏水性均高于对照组。在煮制温度由60 ℃升至80 ℃的过程中,牛骨白汤的表面疏水性呈现上升趋势(P<0.05),这可能是由于在适当的煮制温度下,蛋白质分子内部的疏水基团暴露,发生去折叠现象,增加了表面疏水性[10]。煮制温度继续升高至100 ℃时,牛骨白汤的表面疏水性下降,此现象归因于过高温度煮制导致蛋白质变性,表现为热力学不稳定性[28],削弱了蛋白质之间的疏水相互作用[29],形成更大的聚集体,掩盖了疏水区域,进而导致表面疏水性降低。这与MA等[30]的研究结果相似,当预热温度从70 ℃升高到80 ℃时,鳕鱼蛋白表面疏水性显著增加,当温度进一步升高到100 ℃时,表面疏水性降低。因此,较高的表面疏水性有助于提高蛋白分子的表面活性,有利于提高乳液体系的稳定性。
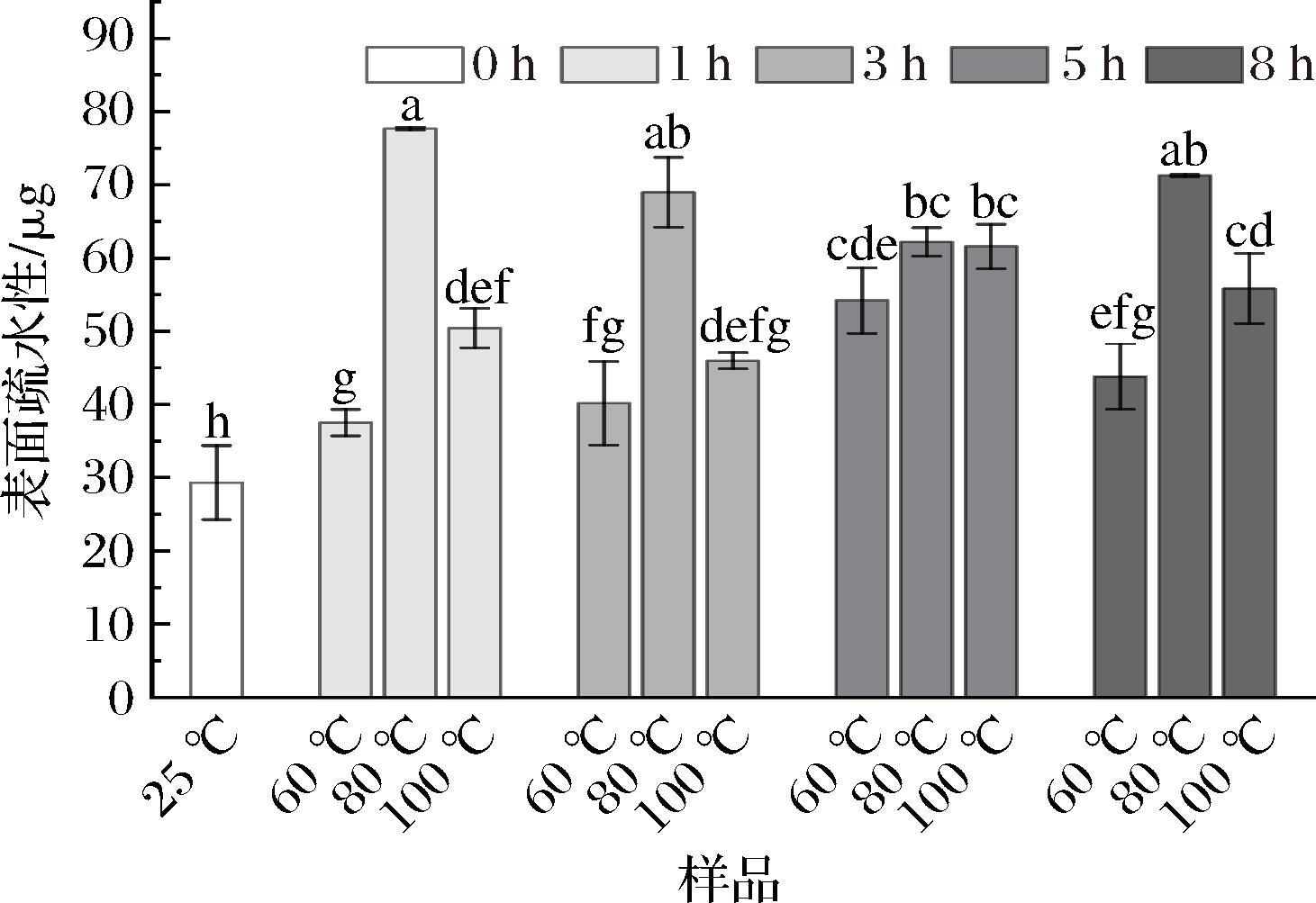
图5 不同煮制温度对牛骨白汤表面疏水性的影响
Fig.5 Effect of different cooking temperatures on surface hydrophobicity of bovine bone white soup
2.6 不同煮制温度对牛骨白汤氨基酸微环境的影响
荧光光谱分为2种:内源荧光光谱和外源荧光光谱,内源荧光团是天然存在于样品中的,而外源荧光团则是被引入用于标记特定的分子或结合,以便研究人员可以追踪所研究系统的特定属性[31]。本研究通过内源荧光研究不同煮制温度对牛骨白汤的影响,荧光光谱主要反映芳香族氨基酸微环境极性的变化[32]。如图6所示,牛骨白汤在468 nm处有强烈的荧光发射峰,随着煮制温度的升高,牛骨白汤的最大吸收波长发生了轻微红移(468~470 nm),往长波长方向移动,同时荧光强度逐渐升高。通过内源性荧光光谱峰的最大值变化能推测蛋白质中生色基团的疏水性变化情况。此现象说明随着温度的提高,牛骨白汤的色氨酸残基趋向于亲水性的微环境。色氨酸残基趋向于亲水性的微环境的主要与蛋白质的氧化和交联有关,波长红移表明色氨酸暴露在极性环境中[17],由于高温加热使蛋白质的结构展开,蛋白质结构变得松散[33-34],加热到一定程度会导致蛋白质出现不同程度的聚集[35],从而降低蛋白质在界面上的有效吸附浓度和吸附能力,不利于提高其乳化特性,因而导致牛骨白汤乳化稳定性下降。LI等[25]研究了热处理对大豆分离蛋白制备的水包油乳液物理稳定性和脂质-蛋白质共氧化的影响,与本研究结果一致。
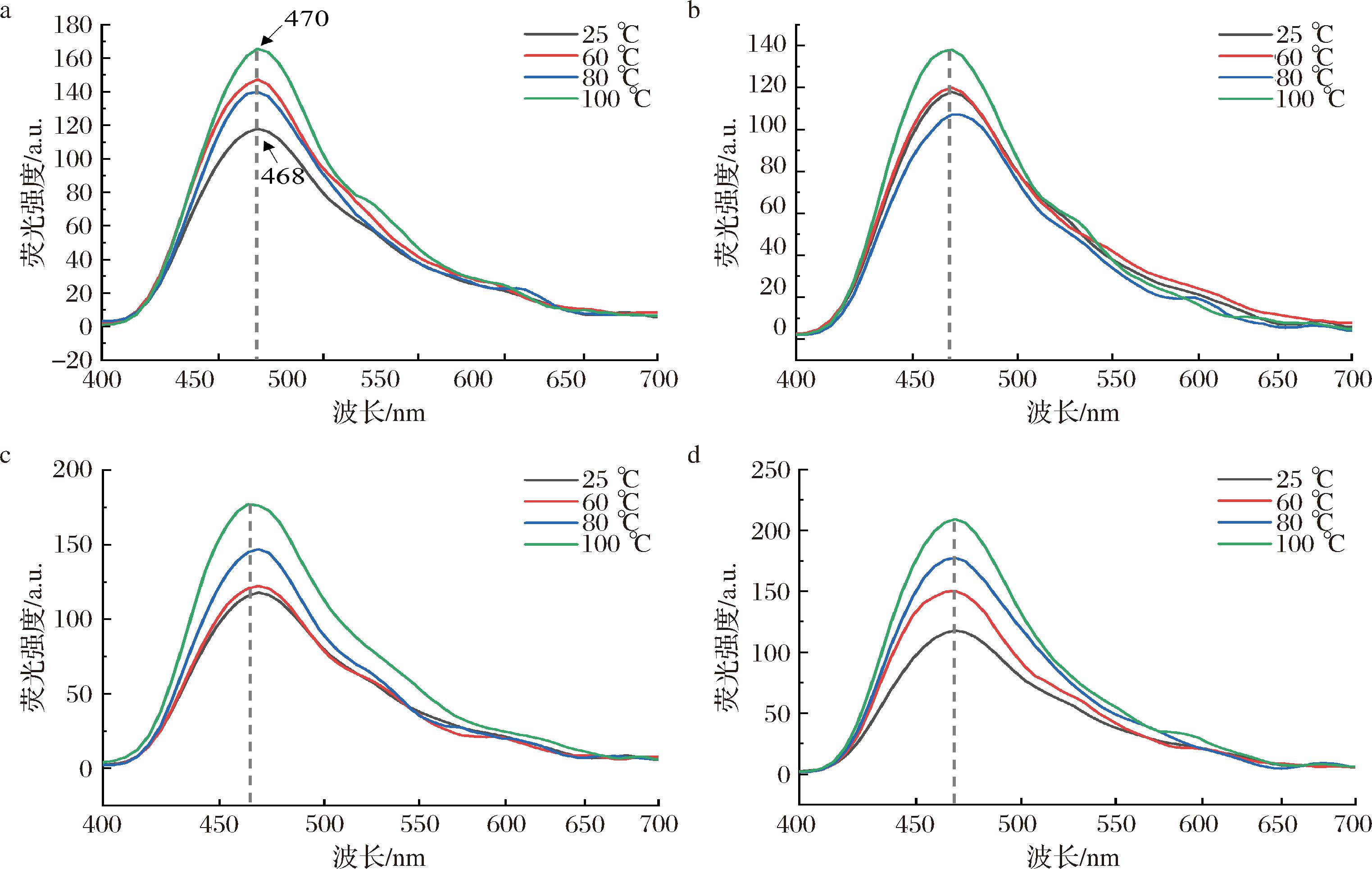
a-1 h;b-3 h;c-5 h;d-8 h
图6 不同煮制温度对牛骨白汤荧光光谱的影响
Fig.5 Effect of different cooking temperatures on the fluorescence spectrum of bovine bone white soup
3 结论
牛骨白汤作为食品工业中广泛应用的乳化类产品,其乳化体系的稳定性尤为重要。本文主要研究了温度对牛骨白汤煮制过程中乳化体系稳定性的影响,结果表明,80 ℃煮制温度下牛骨白汤的乳化稳定性最佳。当煮制温度从60 ℃上升至80 ℃时,牛骨白汤中疏水性氨基酸暴露,静电斥力增强,液滴聚集得到抑制,进而乳液粒径减小,因此提高了牛骨白汤的乳化稳定性(煮制温度为80 ℃时乳化活性为10.51 m2/g,乳化稳定性为112.06 min);然而,当煮制温度升高至100 ℃时,牛骨白汤的乳化活性、乳化稳定性、Zeta电位绝对值和表面疏水性等均呈下降趋势,同时乳液颗粒粒径增大,这是由于过高温度破坏了蛋白质的结构,加剧乳液蛋白液滴聚集,导致乳液稳定性下降。总体而言,煮制温度为80 ℃牛骨白汤乳液的各项指标整体优于60 ℃和100 ℃。在其他条件保持一致的情况下,选择80 ℃煮制牛骨白汤可保持其乳化体系稳定性最佳,对牛骨白汤的合理利用加工具有指导意义。本文中牛骨白汤体系较为复杂,并且长时间的高温煮制导致乳液不稳定的不确定因素较多,因此在今后的研究中还需要深入探讨。
[1] MA C W,TIAN X J,LI Y S,et al.Using high-temperature cooking for different times for bone soup:Physicochemical properties,protein oxidation and nutritional value[J].Journal of Food Composition and Analysis,2023,122:105467.
[2] ZHANG L L,CAO X X,ZHU B Q,et al.Enhancing saltiness perception in bone broth:The additive effect of oil and optimization of sodium-reduction formula for consumer acceptability[J].Journal of the Science of Food and Agriculture,2024,104(10):6108-6117.
[3] GUAN H N,FENG C M,TIAN Y L,et al.Effect of fat addition on the characteristics and interfacial behavior of chicken white soup emulsion from chicken skeleton[J].Food Chemistry:X,2024,21:101163.
[4] 王君文,韩旭,李田甜,等.乳化剂稳定乳液的机理及应用研究进展[J].食品科学,2020,41(21):303-310.WANG J W,HAN X,LI T T,et al.Mechanism and application of emulsifiers for stabilizing emulsions:A review[J].Food Science,2020,41(21):303-310.
[5] 刘立鹏,方晓敏,姜鑫,等.发芽处理对玉米醇溶蛋白结构、热特性及乳化特性的影响[J].中国食品学报,2024,24(7):252-260.LIU L P,FANG X M,JIANG X,et al.Effect of germinating treatment on structure,thermal and emulsifying properties of zein[J].Journal of Chinese Institute of Food Science and Technology,2024,24(7):252-260.
[6] XU W,NING Y L,WU S P,et al.Heat stability promoted Pickering emulsions stabilized by glidian/sodium caseinate nanoparticles and konjac glucomannan[J].LWT,2023,182:114847.
[7] 朱秀清,王子玥,李美莹,等.热处理对汉麻乳稳定性的影响及蛋白结构表征[J].食品科学,2021,42(7):68-73.ZHU X Q,WANG Z Y,LI M Y,et al.Effect of heat treatment on the stability of hemp seed milk and characterization of protein structure[J].Food Science,2021,42(7):68-73.
[8] 高飞,余海霞,张小军,等.热处理对金枪鱼蛋白乳液稳定性的影响[J].食品工业科技,2024,45(11):86-92.GAO F,YU H X,ZHANG X J,et al.Effect of heat treatment on the stability of the tuna protein emulsion[J].Science and Technology of Food Industry,2024,45(11):86-92.
[9] DYBOWSKA B E,KRUPA‐KOZAK U.Stability of oil‐in‐water emulsions as influenced by thermal treatment of whey protein dispersions or emulsions[J].International Journal of Dairy Technology,2020,73(3):513-520.
[10] HU J Y,YU B,YUAN C,et al.Influence of heat treatment before and/or after high-pressure homogenization on the structure and emulsification properties of soybean protein isolate[J].International Journal of Biological Macromolecules,2023,253:127411.
[11] 郝梦,毛书灿,周志,等.热处理和蛋白浓度对肌原纤维蛋白乳液的稳定性和流变特性的影响[J].食品工业科技,2022,43(23):56-63.HAO M,MAO S C,ZHOU Z,et al.Effect of heat treatment and protein concentration on the stability and rheological properties of myofibrillar protein emulsion[J].Science and Technology of Food Industry,2022,43(23):56-63.
[12] CHEN J X,HE J J,ZHAO Z H,et al.Effect of heat treatment on the physical stability,interfacial composition and protein-lipid co-oxidation of whey protein isolate-stabilised O/W emulsions[J].Food Research International,2023,172:113126.
[13] HE X F,WANG B,ZHAO B T,et al.Effect of hydrothermal treatment on the structure and functional properties of quinoa protein isolate[J].Foods,2022,11(19):2954.
[14] YAN X H,LIANG S B,PENG T,et al.Influence of phenolic compounds on physicochemical and functional properties of protein isolate from Cinnamomum camphora seed kernel[J].Food Hydrocolloids,2020,102:105612.
[15] MA J R,PAN C,HE R R,et al.Physicochemical properties and oil-water interfacial behavior of subcritical water-treated coconut (Cocos nucifera L.) globulins[J].Food Hydrocolloids,2024,152:109897.
[16] CAO M M,ZHANG X C,ZHU Y Q,et al.Enhancing the physicochemical performance of myofibrillar gels using Pickering emulsion fillers:Rheology,microstructure and stability[J].Food Hydrocolloids,2022,128:107606.
[17] 王振国,高育哲,时家峰,等.挤压温度对大豆分离蛋白与原花青素复合物结构和功能特性的影响[J].农业工程学报,2022,38(21):279-286.WANG Z G,GAO Y Z,SHI J F,et al.Effects of extrusion temperature on the functional and structural properties of soybean protein isolate and proanthocyanidin complex[J].Transactions of the Chinese Society of Agricultural Engineering,2022,38(21):279-286.
[18] 邵家起,邓乾春,李康昱,等.双蛋白天然共生颗粒Pickering纳米乳液的稳定性分析[J].食品工业科技,2024,45(21):74-84.SHAO J Q,DENG Q C,LI K Y,et al.Stability analysis of Pickering nanoemulsion covered by dual-protein natural symbiotic particles[J].Science and Technology of Food Industry,2024,45(21):74-84.
[19] SETIOWATI A D,WIJAYA W,VAN DER MEEREN P.Whey protein-polysaccharide conjugates obtained via dry heat treatment to improve the heat stability of whey protein stabilized emulsions[J].Trends in Food Science &Technology,2020,98:150-161.
[20] LI D F,WU Y N,YIN H R,et al.Panax Notoginseng polysaccharide stabilized gel-like Pickering emulsions:Stability and mechanism[J].International Journal of Biological Macromolecules,2023,249:125893.
[21] LIN D Q,LU W,KELLY A L,et al.Interactions of vegetable proteins with other polymers:Structure-function relationships and applications in the food industry[J].Trends in Food Science &Technology,2017,68:130-144.
[22] 王美月,布冠好,常永锋,等.蛋白多肽美拉德反应物稳定乳液的研究进展[J].食品科学,2024,45(3):227-234.WANG M Y,BU G H,CHANG Y F,et al.Research progress on emulsions stabilized by Maillard reaction products from protein-derived peptides[J].Food Science,2024,45(3):227-234.
[23] WU S Z,MENG Z M,YUE Z Y,et al.Effects of addition of Clitocybe squamulose on nutrients and formation of micro-nanoparticles in Chinese three-yellow chicken soup[J].LWT,2024,191:115593.
[24] FU J N,LI S B,XU M Z,et al.Changes in physicochemical properties and formation process of colloidal nanoparticles (CNPs) during the lamb soup stewing[J].Food Chemistry,2024,442:138290.
[25] LI Q Y,ZHENG J B,GE G,et al.Impact of heating treatments on physical stability and lipid-protein co-oxidation in oil-in-water emulsion prepared with soy protein isolates[J].Food Hydrocolloids,2020,100:105167.
[26] ZHAO M,XIONG W F,CHEN B X,et al.Enhancing the solubility and foam ability of rice glutelin by heat treatment at pH12:Insight into protein structure[J].Food Hydrocolloids,2020,103:105626.
[27] TIAN Y,ZHAO X X,WANG Z G,et al.Structural characteristics and stability analysis of coconut oil body and its application for loading β-carotene[J].Food Chemistry,2024,446:138818.
[28] SHEN L,TANG C H.Microfluidization as a potential technique to modify surface properties of soy protein isolate[J].Food Research International,2012,48(1):108-118.
[29] TAO X,CAI Y J,LIU T X,et al.Effects of pretreatments on the structure and functional properties of okara protein[J].Food Hydrocolloids,2019,90:394-402.
[30] MA W C,WANG J M,WU D,et al.Effects of preheat treatment on the physicochemical and interfacial properties of cod proteins and its relation to the stability of subsequent emulsions[J].Food Hydrocolloids,2021,112:106338.
[31] 郭晨晨,耿宏庆,徐毅,等.琥珀酰化改性对猪肝蛋白乳化特性的影响与机理研究[J].食品与发酵工业,2024,50(12):202-208.GUO C C,GENG H Q,XU Y,et al.Effect and mechanism of succinylation modification on emulsification characteristics of porcine liver protein[J].Food and Fermentation Industries,2024,50(12):202-208.
[32] HUANG M Y,XU Y J,CHEN X,et al.Improved emulsifying properties of water-soluble myofibrillar proteins at acidic pH conditions:Emphasizing pH-regulated electrostatic interactions with chitosan[J].International Journal of Biological Macromolecules,2024,257:128557.
[33] AHMED I,LV L t,LIN H,et al.Effect of tyrosinase-aided crosslinking on the IgE binding potential and conformational structure of shrimp (Metapenaeus ensis) tropomyosin[J].Food Chemistry,2018,248:287-295.
[34] GONG B W,MAO S L,LI X K,et al.Mineral oil emulsion species and concentration prediction using multi-output neural network based on fluorescence spectra in the solar-blind UV band[J].Analytical Methods:Advancing Methods and Applications,2024,16(13):1836-1845.
[35] 刁静静,陶阳,国慧,等.加热温度对牡荆素-绿豆蛋白互作物结构和功能性的影响[J].中国食品学报,2023,23(8):197-207.DIAO J J,TAO Y,GUO H,et al.Effect of heating temperature on the structural and functional characteristics of vitexin-mung bean protein[J].Journal of Chinese Institute of Food Science and Technology,2023,23(8):197-207.