油桃(Prunus persica var.nectarina)果香独特且营养丰富,是国内外水果市场中最受欢迎的果品之一[1]。由于油桃采后呼吸旺盛极易品质劣变,因此常采用低温保鲜技术以减缓油桃的成熟保持其商品价值。但长时间的低温贮藏容易使桃果蔗糖代谢、能量代谢紊乱,降低了桃果贮期品质。因此,寻找一种操作方便且能有效调节桃果贮期生理代谢的保鲜技术,对于提高桃果耐贮性极为重要。
油桃采后主要的可溶性糖为蔗糖、葡萄糖和果糖,其中蔗糖含量最高。蔗糖代谢是果蔬采后重要的糖代谢途径,与果蔬贮藏期细胞膜完整性、抗氧化性以及渗透压的调节密切相关[2]。转化酶、蔗糖合酶,蔗糖磷酸合酶是调控蔗糖代谢的关键酶,其中蔗糖转化酶根据反应最佳pH,分为中性转化酶和酸性转化酶。研究表明,长期低温贮藏会使桃果中性转化酶、酸性转化酶等蔗糖降解酶活性上升,加速蔗糖降解,导致桃果果肉褐变,而采用1-甲基环丙烯(1-methylcyclopropene,1-MCP)、热风和茉莉酸甲酯等方式处理桃果均可提高蔗糖合成酶的活性,延缓蔗糖含量的下降,有效维持桃果贮期品质[3-4]。此外,蔗糖分解为葡萄糖、果糖后又可经过糖酵解途径分别生成丙酮酸、果糖-6-磷酸,随后经过三羧酸循环释放能量。因此,蔗糖代谢不仅与能量代谢联系密切,而且影响油桃贮藏品质。
油桃采后品质劣变与能量代谢密切相关,当果蔬衰老或处于逆境胁迫时,线粒体更容易受到损伤,导致ATP合成减少,扰乱细胞功能,造成细胞损伤或凋亡[5],而线粒体作为细胞能量代谢的主要场所,内含参与能量代谢的关键酶,包括琥珀酸脱氢酶(succinate dehydrogenase,SDH)、细胞色素氧化酶(cytochrome c oxidase,CCO)、氢-腺苷三磷酸酶(hydrogen-adenosine triphosphatase,H+-ATPase)与钙-腺苷三磷酸酶(hydrogen-adenosine triphosphatase,Ca2+-ATPase)等。当能量代谢相关酶活性下降时会使线粒体产能减弱,缺乏足够的能量来维持细胞代谢容易诱发果蔬软化、营养流失、褐变等问题,严重影响其感官品质,诱导果蔬提高SDH、CCO、H+-ATPase和Ca2+-ATPase活性,可有效提高ATP-ADP高能磷酸基团的含量,促进ATP的合成,进而维持果蔬品质[6-7]。ZHANG等[5]在对油桃的研究中发现1-MCP处理可显著延缓能量代谢相关酶活性的降低,提高了桃果的抗冷害能力,进而提升了桃果贮期品质。
1-MCP是一种环丙烯衍生物,与其他采后保鲜技术相比,1-MCP具有环保、安全、保鲜效果显著等多个优势,为果蔬采后保鲜提供了一种有效策略。研究表明,1-MCP对果蔬采后颜色变化、乙烯合成、呼吸、衰老、软化等生理活动有重要影响[8-11]。ZHANG等[5]研究发现1-MCP可通过调节活性氧代谢、能量代谢,进而影响油桃品质,ZHOU等[12]在黄桃的研究中证实1-MCP处理可以通过调节蔗糖代谢促进酚类物质的积累,减轻了桃果褐变程度。虽然现有研究已表明1-MCP在桃果保鲜领域潜力巨大,但目前1-MCP对桃果贮期保鲜效果的研究主要集中在抗氧化方面,蔗糖代谢与能量代谢的系统性研究较少,未能全面揭示1-MCP对桃果的调控机制。因此,本研究通过分析1-MCP处理油桃后其蔗糖代谢及能量代谢相关指标的变化,探究1-MCP处理对桃果蔗糖代谢及能量代谢的影响,为1-MCP在油桃贮藏中的应用提供新的见解。
1 材料与方法
1.1 材料与试剂
‘早红宝石’油桃,采自运城市临猗县角杯乡油桃种植园,果实大小均匀,颜色相近,没有明显的外观缺陷果实(七成熟,果肉硬度:8.9 N;可滴定酸:0.4%;果肉L*值:69.71,a*值:-2.32,b*值:5.33;可溶性固形物含量(soluble solids content,SSC)为7.39%),立即运往实验室并在5 ℃条件下预冷3 h以去除田间热。
乙醇,天津市北辰方正试剂厂;1-MCP,安徽添福生物科技有限公司;1,4-二硫苏糖醇、β-巯基乙醇、二甲基对苯二胺、蒽酮、甘油、4-羟乙基哌嗪乙磺酸、交联聚乙烯吡咯烷酮(polyvinlypolypy rrolidone,PVPP)、三氯乙酸、3,5-二硝基水杨酸、6-磷酸果糖、6-磷酸葡萄糖,阿拉丁试剂(上海)有限公司;SDH、Ca2+-ATP酶测定试剂盒,南京建成生物研究所;以上试剂均为分析纯。
1.2 仪器与设备
O2/CO2气体分析仪,上海昕瑞仪器仪表有限公司;保鲜库、密闭大帐,山西农科院保鲜所;UX620H电子天平,深圳市三利化学品有限公司;Ultrospec 2100 pro紫外线/可见光光谱分析仪,北京盛科信德科技有限公司;HS-2900P色谱仪,Agilent公司;PAL-1测糖仪,ATAGO公司。
1.3 实验方法
1.3.1 油桃处理方法
为了减少温度波动对油桃品质的影响,油桃预冷后在(5±0.5)℃和70%~80%相对湿度的保鲜库中将油桃分为2个处理,每个处理设置3个重复,每个重复50个油桃。对照组(control check,CK):将密闭大帐置于保鲜库中,随后将油桃果实放入,静置12 h后,随后将桃果转入内衬有保鲜袋的周转框中。1-MCP 处理组:将密闭大帐置于保鲜库中,随后将桃果放入,采用1 μL/L 1-MCP熏蒸油桃12 h,待熏蒸完成后将果实转入内衬有保鲜袋的周转框中。处理好的桃果在此保鲜库中贮藏35 d,每隔7 d测定一次油桃指标。
1.3.2 指标测定
1.3.2.1 呼吸速率、SSC的测定
按照焦旋等[13]的方法测定呼吸速率,在各处理中分别挑选4个感官品质相近的油桃置于2 L密闭容器中1 h后,测定瓶内CO2含量,计算呼吸速率,单位mg/(kg·h);SSC测定:每次随机取3个桃果挤汁,并用PAL-1测糖仪测定,单位为%。
1.3.2.2 可溶性糖含量的测定
按照董欣瑞等[4]的方法测定可溶性糖含量,略作修改。取5 g新鲜果肉研成匀浆,加入20 mL 95%(体积分数)乙醇并超声提取1 h。果糖与葡萄糖含量采用蒽酮-硫酸法,蔗糖含量采用NaOH-蒽酮-硫酸法,单位均为g/kg。
1.3.2.3 蔗糖代谢相关酶活性的测定
粗酶液制备:每个处理取2 g果肉并研磨成浆,加10 mL提取液[2 mmol/L 1,4-二硫苏糖醇,10 mmol/L 氯化镁,10 mmol/L β-巯基乙醇,20%(体积分数)甘油]浸提10 min,随后0 ℃、90 000 r/min条件下离心5 min取上清液。
酸性转化酶(acid invertase,AI)活性测定:依次加入500 μL 100 mmol/L醋酸钠(pH 4.8)、100 μL 100 mmol/L蔗糖、100 μL粗酶提取物。采用DNS法测定540 nm处测定吸光值。酶活性单位为U/g。
中性转化酶(neutral invertase,NI)活性的测定与AI相似,不同之处在于反应体系缓冲液为100 mmol/L 磷酸钾(pH 7.5)。酶活性单位为U/g。
蔗糖磷酸合成酶(sucrose phosphate synthase,SPS)、蔗糖合成酶(sucrose synthase,SS)酶活性测定按WANG等[14]的方法。SPS测定体系:500 μL粗酶提取液,6-磷酸果糖、6-磷酸葡萄糖与二磷酸尿苷葡萄糖均为25 mmol/L。酶活性单位为U/g。
SS测定体系:60 mmol/L果糖、25 mmol/L 二磷酸尿苷葡萄糖和500 μL粗酶提取液。在620 nm处测定吸光值,酶活性单位为U/g。
1.3.2.4 桃果能量水平测定
参照林毅雄等[15]的方法测定能荷、ATP、ADP、AMP含量。其中ATP、ADP、AMP含量单位为mg/kg。
1.3.2.5 桃果能量代谢相关酶活性的测定
按照ZHANG等[5]的方法提取线粒体:取10 g果肉与20 mL Tris-HCl缓冲液(pH 7.5)混合后研磨成浆。0 ℃、90 000 r/min条件下离心5 min收集沉淀即为线粒体粗提物。
CCO活性测定体系:100 μL线粒体粗提液,80 μL 0.04%(体积分数)细胞色素C溶液,3 mL Tris-HCl缓冲液(pH 7.5),0.5 mL 0.4%(体积分数)二甲基对苯二胺溶液。测定510 nm处吸光值。单位为U/mg。
H+-ATPase活性测定体系:100 μL线粒体粗提液,50 μL 6 mmol/L ATP。反应30 min后加入显色液,测定660 nm处吸光值。单位为U/mg。
SDH活性与Ca2+-ATPase活性按照试剂盒说明书步骤操作,酶活性单位为U/mg。
1.4 数据处理
Origin 2022软件作图,所有指标均测定3次后取平均值,并进行显著性分析,P<0.05表示差异显著。
2 结果与分析
2.1 1-MCP处理对呼吸速率及SSC的影响
如图1-a所示,0~7 d时各组呼吸速率并无明显差异,7 d后CK组呼吸速率大幅升高。21 d时达到最大值40.92 mg/(kg·h),而同时期1-MCP处理后桃果呼吸速率仅为CK组的69.59%,呼吸高峰推迟至28 d。SSC变化与呼吸速率变化较为相似(图1-b),但CK组SSC 21 d时急剧减少,1-MCP处理明显延缓了贮藏后期SSC的降低。以上结果表明,1-MCP在降低油桃呼吸速率及维持SSC方面效果较好。
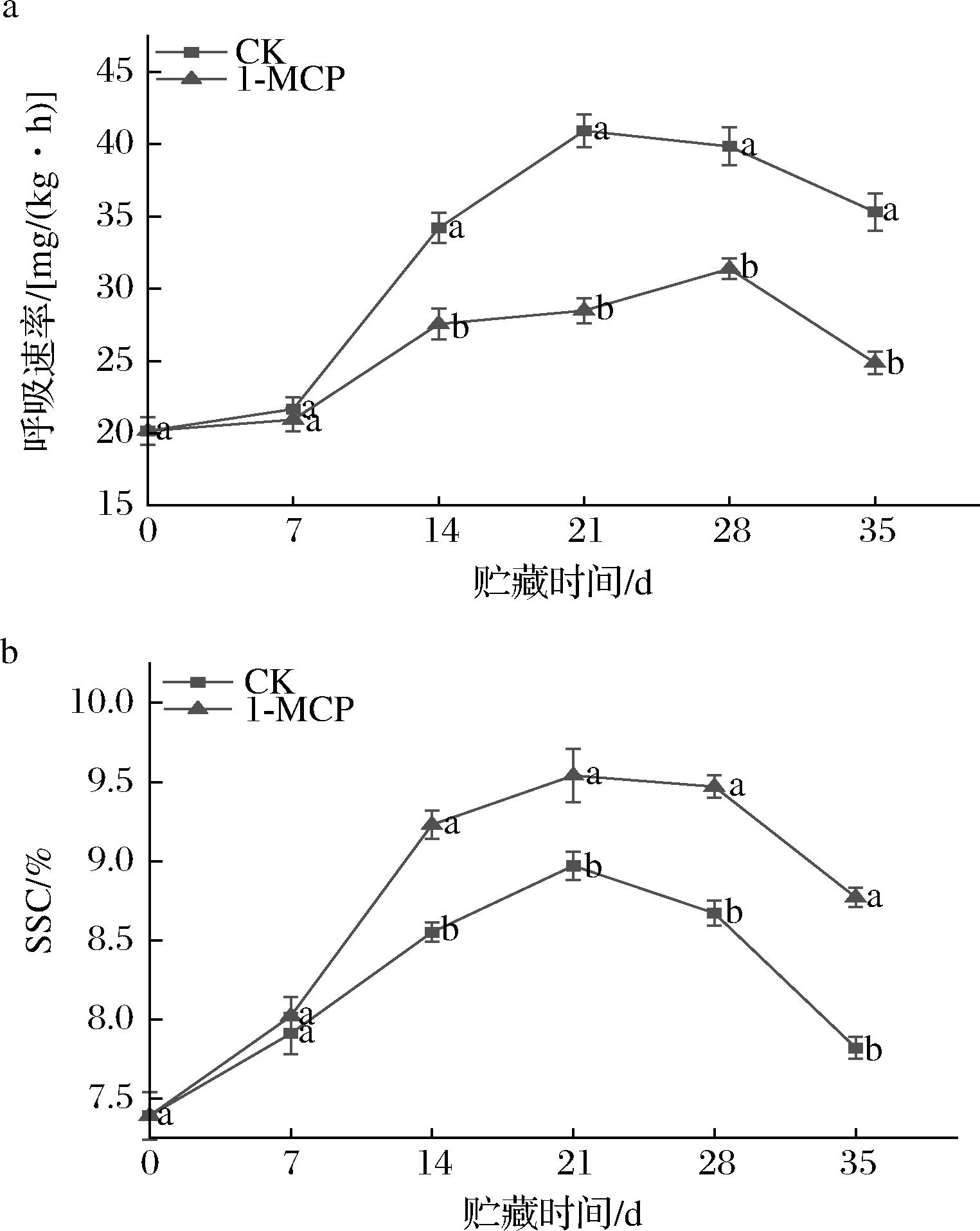
a-呼吸速率;b-SSC
图1 1-MCP处理对油桃呼吸速率及SSC的影响
Fig.1 Effects of 1-MCP treatment on respiration rate and SSC in nectarines
注:不同字母表示同一时间不同处理有显著性差异(P<0.05)(下同)。
2.2 1-MCP处理对可溶性糖含量的影响
油桃果实中的主要可溶性糖为蔗糖,其含量高于葡萄糖与果糖。如图2-a所示,0~7 d时,蔗糖含量小幅上升,随后CK组蔗糖含量急剧减少,而1-MCP处理组下降幅度较为平缓且蔗糖含量始终高于CK组。葡萄糖和果糖的含量逐渐增加,CK组增加幅度显著高于1-MCP处理组(P<0.05)。如图2-b、图2-c所示葡萄糖、果糖初始含量分别为5.01、7.26 g/kg,35 d时CK组分别为17.17、14.92 g/kg,与1-MCP组相比提高了62.74%和49.05%。以上结果表明,1-MCP 在抑制蔗糖降解及葡萄糖、果糖含量升高方面效果显著。
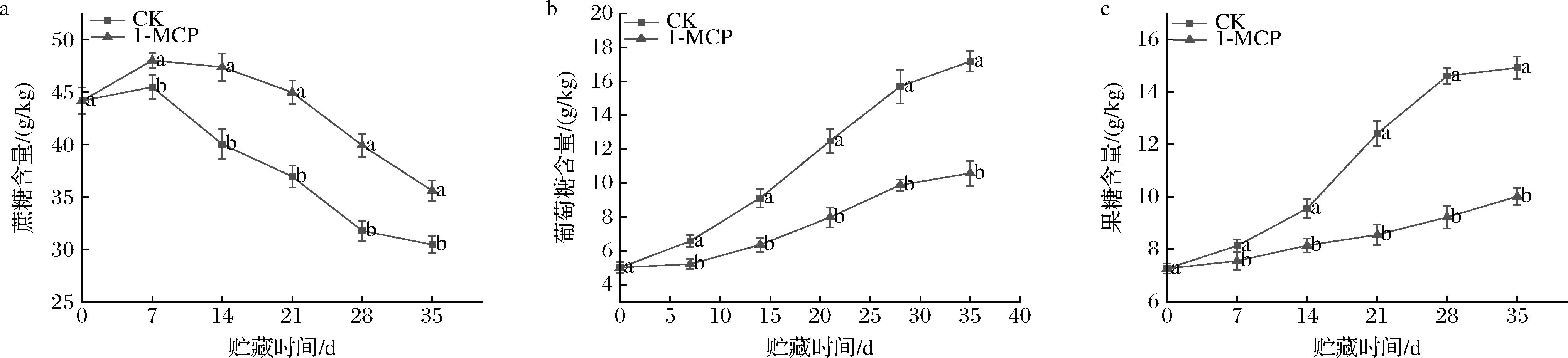
a-蔗糖含量;b-葡萄糖含量;c-果糖含量
图2 1-MCP处理对油桃可溶性糖含量的影响
Fig.2 Effects of 1-MCP treatment on soluble sugar content in nectarines
2.3 1-MCP处理对蔗糖代谢相关酶活性的影响
如图3-a所示,CK组SPS活性在0~7 d时急剧减少,7 d时酶活性仅为55.62 U/g,而同时期1-MCP处理组酶活性为73.51 U/g,显著高于CK组(P<0.05)。7 d后2个处理的酶活性逐渐升高,21 d时达到峰值,随后酶活性逐渐降低,但1-MCP处理组SPS酶活性始终高于CK组。如图3-b所示,SS活性变化与SPS较为相似,但CK组在0~7 d时酶活性下降幅度较小,1-MCP组则呈小幅上升趋势。21~28 d时两处理的SS活性均大幅下降,与21 d时相比,分别下降了33.09%、15.68%。如图3-c所示,NI活性于0~7 d时降幅较大,随后均呈上升趋势,35 d时CK组、1-MCP组酶活性分别较初始时提高了35.78%、12.19%。AI活性0~21 d时逐渐增大,随后不断降低,但整个贮期1-MCP组酶活性均显著低于CK组。以上结果表明,1-MCP处理有利于提高蔗糖合成酶的酶活性,同时抑制蔗糖降解酶的活性。
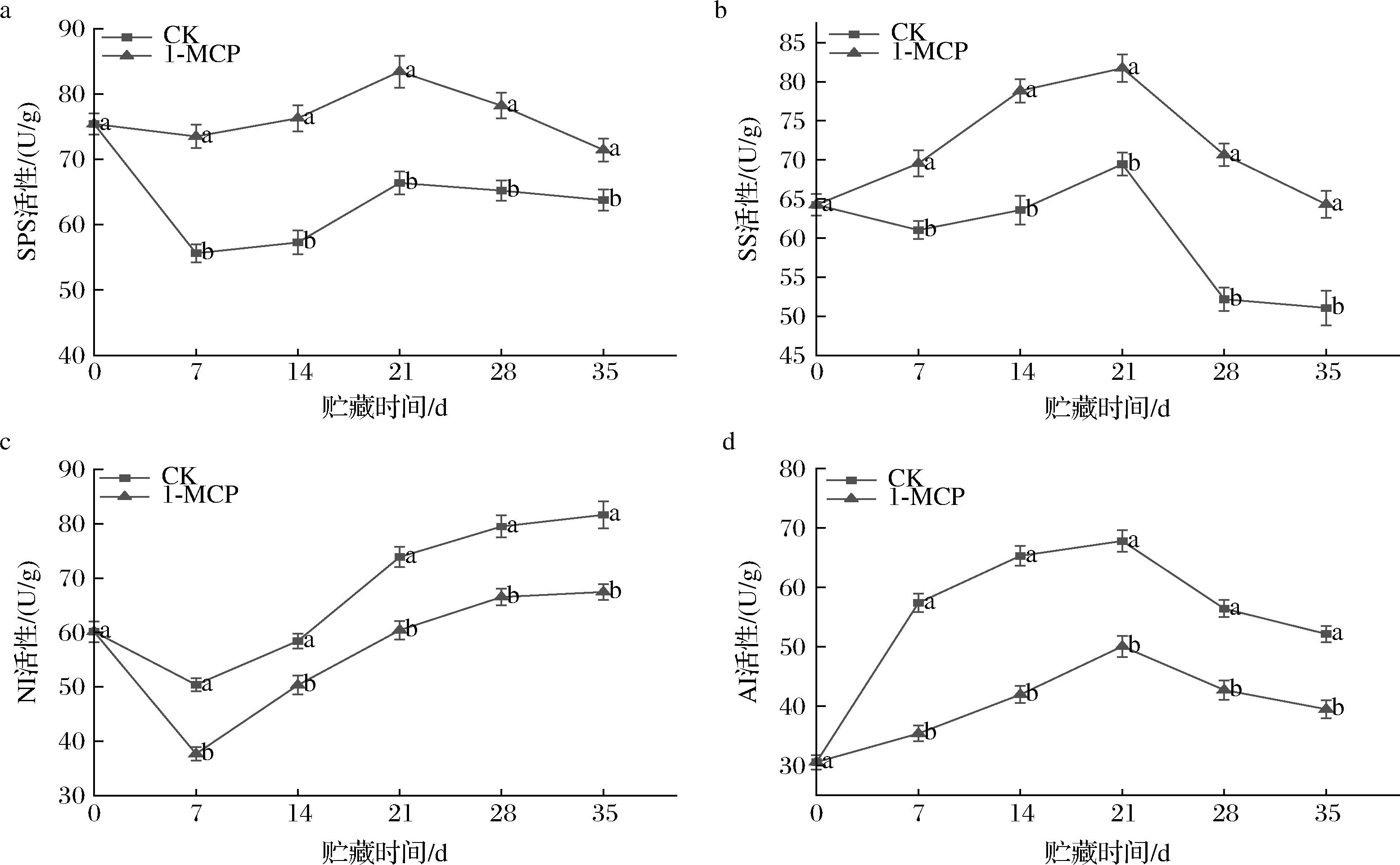
a-SPS活性;b-SS活性;c-NI活性;d-AI活性
图3 1-MCP处理对蔗糖代谢相关酶活性的影响
Fig.3 Effects of 1-MCP treatment on the activity of sucrose metabolism related enzymes
2.4 1-MCP处理对油桃果实ADP、AMP、ATP含量及能荷的影响
如图4-a所示,0~21 d时CK组油桃果实ADP含量逐渐减少,而1-MCP组在前7 d时ADP含量小幅上升,21 d后两处理的ADP含量短暂升高,35 d时CK组、1-MCP组ADP含量分别为18.42、28.18 mg/kg。如图4-b所示AMP含量逐渐升高且CK组均显著高于1-MCP组(P<0.05),35 d时CK组AMP含量为1-MCP组的1.19倍。如图4-c所示,油桃果实的ATP含量在贮藏过程中持续降低,CK组降幅较大,1-MCP处理后明显抑制了ATP含量的下降,35 d时,较CK组提高了79.42%。如图4-d所示,各处理组果实能荷水平在前14 d时差异并不显著,14 d后CK组能荷水平大幅降低,35 d时仅为1-MCP的87.69%。以上结果表明,1-MCP处理油桃可维持果实较高的贮期能量水平。
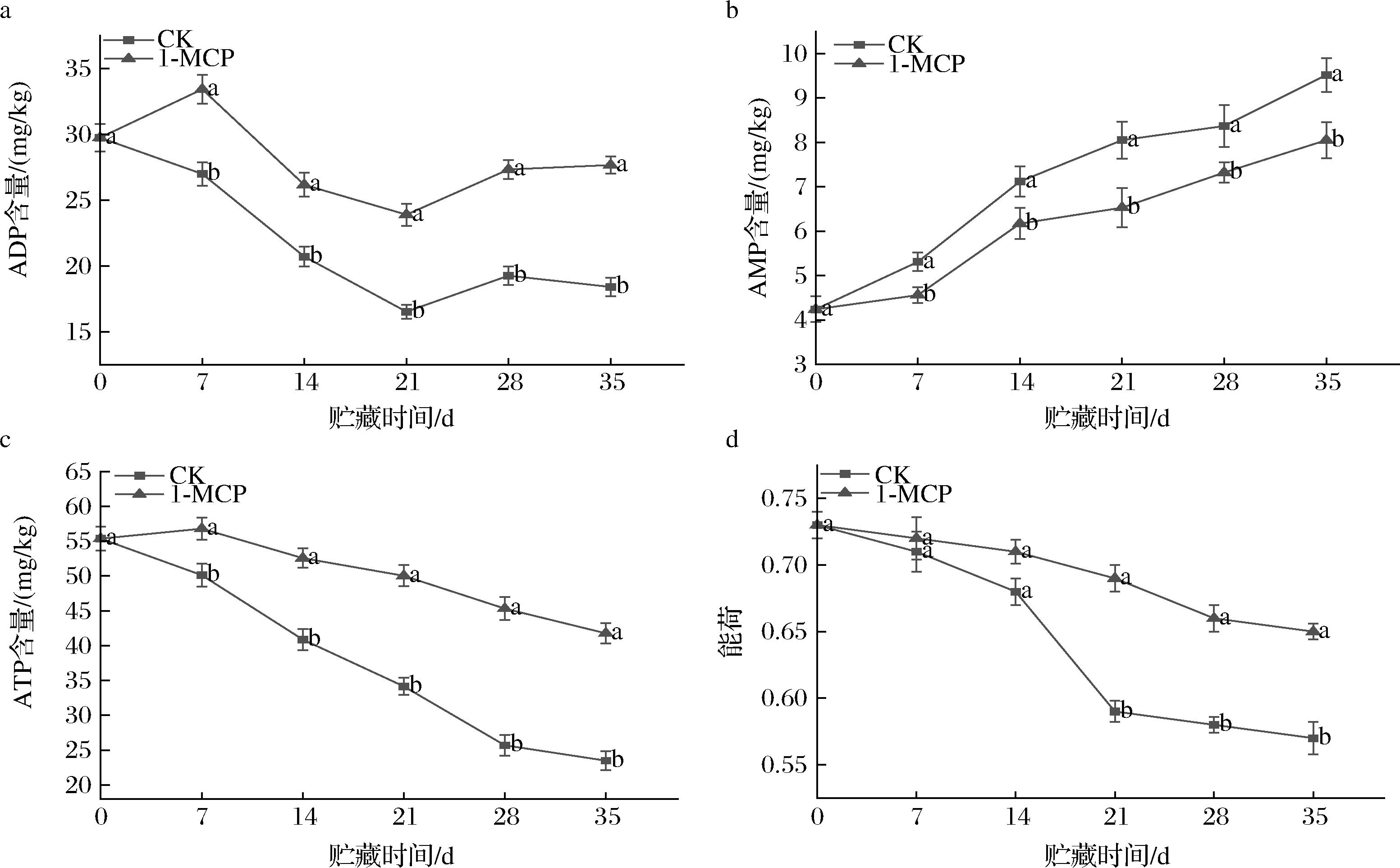
a-ADP含量;b-AMP含量;c-ATP含量;d-能荷
图4 1-MCP处理对ADP、AMP、ATP含量及能荷的影响
Fig.4 Effects of 1-MCP treatment on the contents of ADP,AMP,ATP and energy charge
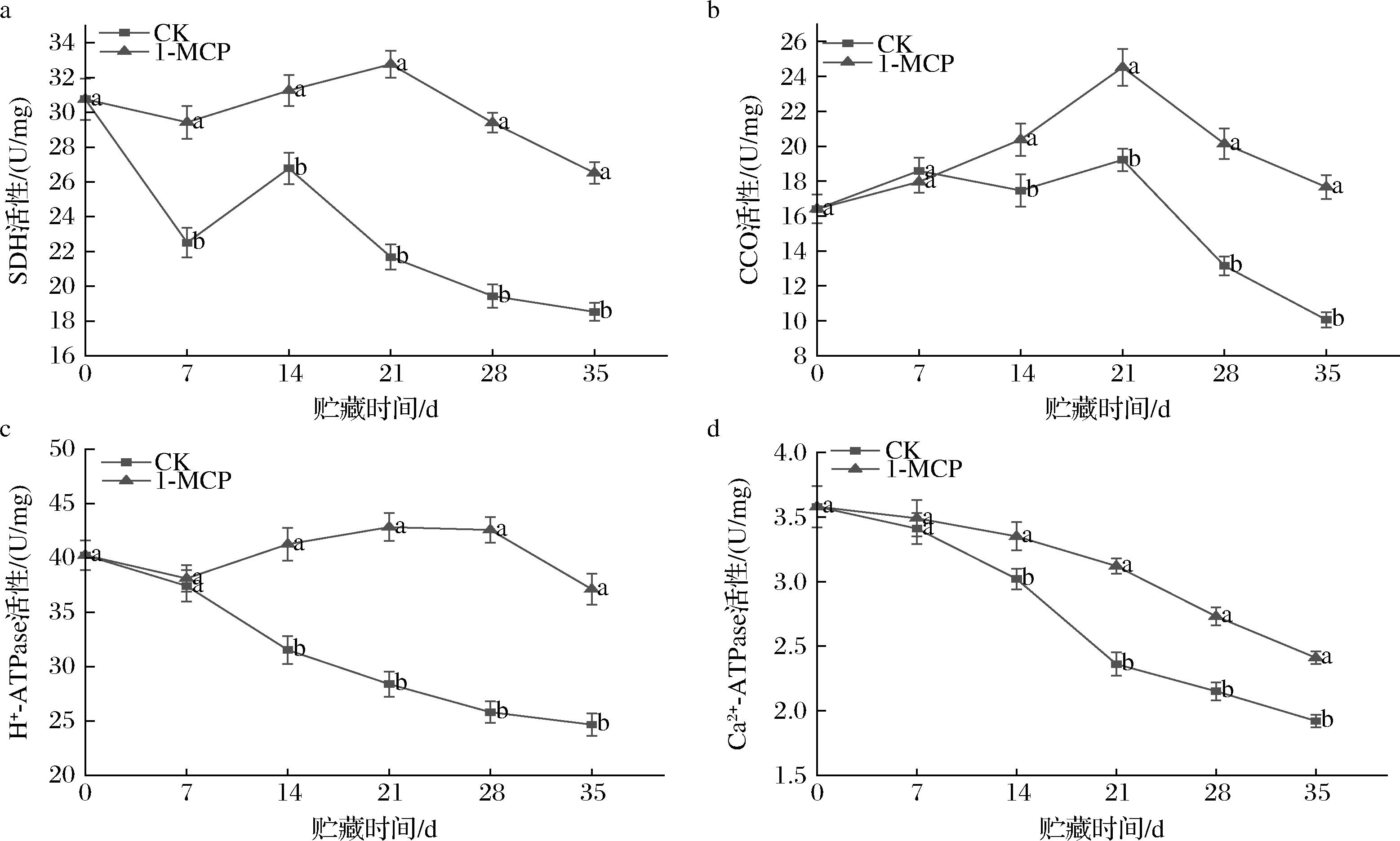
a-SDH活性;b-CCO活性;c-H+-ATPase活性;d-Ca2+-ATPase活性
图5 1-MCP处理对能量代谢相关酶活性的影响
Fig.5 Effects of 1-MCP treatment on the activity of energy metabolism related enzymes
2.5 1-MCP处理对油桃能量代谢相关酶活性的影响
如图5-a所示,SDH活性在0~7 d有所下降,CK组SDH活性减少了36.65%,而1-MCP组仅减少了4.51%,CK组仅在7~14 d时SDH活性有所增加,1-MCP 组在7~21 d时活性不断升高,21 d后2组酶活性均下降,但1-MCP组酶活性显著高于CK组。如图5-b所示,1-MCP处理油桃后其果实CCO活性在0~21 d时逐渐增加,而CK组在此期间虽有波动,但整体仍呈上升趋势,其酶活性增加幅度小于1-MCP处理组,21 d后酶活性急剧减少,35 d时1-MCP组酶活性为CK组的1.75倍。如图5-c所示,1-MCP处理组H+-ATPase活性在0~7 d时降低,7~28 d时不断升高,28~35 d降低,而CK组在0~35 d均不断降低,35 d时仅为1-MCP 组的66.43%。如图5-d所示,CK组与1-MCP组Ca2+-ATPase活性均不断降低,且7 d时两处理无显著差异,7 d后CK组Ca2+-ATPase活性下降幅度明显高于1-MCP组,35 d时CK组与1-MCP 组Ca2+-ATPase活性分别为1.92、2.41 U/mg。以上结果表明,1-MCP处理可以使能量代谢相关酶活性维持在较高水平,延缓了酶活性的降低。
3 讨论
低温保鲜是果蔬采后最有效的保鲜技术。然而单一的低温保鲜处理容易诱发果蔬发生一系列生理改变,如乙烯生成增加,糖类及能量代谢紊乱等,最终导致果蔬贮期品质下降。1-MCP通过调节果蔬呼吸速率、乙烯合成、活性氧及能量代谢,进而提高果蔬保鲜水平[4,16-17]。本研究同样发现,1-MCP处理不仅抑制了油桃呼吸速率的升高,而且将呼吸高峰推迟至28 d,这对于延缓果实衰老进程有重要意义。SSC含量是衡量油桃贮期品质变化的重要指标。在本研究中,其中前3周2个处理的油桃SSC含量均逐渐增加,这可能是由于桃果后熟所致;此外,1-MCP处理组的SSC含量始终高于CK组,这可能是由于桃果的呼吸速率受到抑制,降低了贮期SSC的消耗。
可溶性糖与果品风味和营品质密切相关,果品采后通过糖代谢调节可溶性糖含量维持细胞膜稳定性,提高果品贮期品质。蔗糖是是油桃果实含量最高的糖类物质,在糖代谢过程中,蔗糖在转化酶(AI和NI)催化下转化为葡萄糖和果糖,而葡萄糖和果糖作为底物在SS和SPS的作用下生成蔗糖,因此油桃采后品质劣变进程中常常伴随着蔗糖含量的下降,同时,蔗糖作为植物体重要的抗冷剂,可提高果蔬对低温胁迫的抗性,维持较高水平的蔗糖含量有效延缓了水蜜桃[18]、黄桃[5]、杏[15]贮期膜脂氧化进程,较好的维持了细胞膜的完整性,进而提高果品的贮藏品质。此外,SUN等[19]使用NO处理桃果,发现常温货架期间提高蔗糖代谢合成酶活性,促进蔗糖的生物合成同样有利于提升桃果品质。本研究结果表明,1-MCP处理组油桃的蔗糖含量始终高于CK组。1-MCP处理一方面可提高油桃果实SPS和SS活性,另一方面抑制AI、NI 活性,促进了果糖和葡萄糖向蔗糖的转化,最终延缓了蔗糖的分解,35 d时蔗糖含量较CK组提高了16.91%。这与YU等[20]采用1-MCP对桃果进行保鲜所得结论一致。以上结果表明,1-MCP通过调节桃果贮藏期间蔗糖代谢水平,保持了果实较高的蔗糖含量,对延缓膜脂氧化,提高果实贮期品质有重要意义。
能量代谢是果蔬采后进行生理代谢活动的基础,能量代谢水平是决定果蔬贮期品质的关键因素。当能量代谢降低时,常常伴随着ATP、ADP含量及能荷水平的不断降低以及AMP含量的逐渐升高,加速了果品采后品质劣变进程[21]。LIN等[22]研究发现AMP含量的大幅上升,同时降低ATP、ADP含量及能荷水平,可加速龙眼果肉的降解。在本研究中,虽然CK组与1-MCP处理组桃果的ATP和ADP含量以及能荷水平均不断降低,但是1-MCP处理后桃果实中ATP和ADP含量以及能量电荷水平显著高于同时期CK组,从而确保了桃果正常生命活动的能源供应,一定程度上延缓了SSC含量的下降。这与HUANG等[16]研究发现1-MCP处理可以延缓猕猴桃采后能荷水平及ATP、ADP含量的降低,可有效维持猕猴桃品质的结论一致。此外,SDH与CCO是参与呼吸作用的关键酶,其活性可以反映线粒体的能量合成状态。本研究结果表明,1-MCP处理增强了低温贮藏过程中油桃果实SDH和CCO的活性。该结果与JIN等[23]采用草酸处理桃果可显著提高SDH和CCO活性,增强其能量代谢水平的结论一致。H+-ATPase和Ca2+-ATPase酶活性能够反映线粒体能量代谢水平的能力,H+-ATPase可以为各种营养物质和离子跨膜的运输提供能量,并保持细胞质pH相对稳定。Ca2+-ATPase在维持膜内外离子平衡及细胞膜完整性中起重要作用[24]。本研究结果表明,35 d时1-MCP 处理组H+-ATPase和Ca2+-ATPase活性分别较CK组提高了50.52%、25.52%。较高的Ca2+-ATPase和H+-ATPase活性更有利于桃果ATP、ADP和能荷处于较高水平。该结果与HUANG等[25]关于壳聚糖与硫氢化钠协同处理可以提高SDH、CCO、H+-ATPase和Ca2+-ATPase活性,进而提高油桃贮藏品质的结论相似。这表明1-MCP处理可以更好地维持线粒体的功能,保障细胞能量供应。
4 结论
综上所述,1-MCP处理油桃后显著降低了其呼吸速率,延缓SSC的下降,降低了与蔗糖分解代谢相关酶(AI、NI)的活性,并增强了与蔗糖合成代谢相关酶(SS、SPS)的活性,诱导果实保持更高的蔗糖水平。此外,1-MCP处理提高了SDH、CCO、H+-ATP和Ca2+-ATP等能量代谢相关酶的活性,使得桃果保持较高的ATP、ADP含量及能荷水平,确保油桃各项生理活动的能源供应,有利于维持油桃贮期品质。
[1] ZHANG W L,ZHAO H D,ZHANG J,et al.Different molecular weights chitosan coatings delay the senescence of postharvest nectarine fruit in relation to changes of redox state and respiratory pathway metabolism[J].Food Chemistry,2019,289:160-168.
[2] YU F,NI Z M,SHAO X F,et al.Differences in sucrose metabolism in peach fruit stored at chilling stress versus nonchilling stress temperatures[J].HortScience,2015,50(10):1542-1548.
[3] YU L N,LIU H X,SHAO X F,et al.Effects of hot air and methyl jasmonate treatment on the metabolism of soluble sugars in peach fruit during cold storage[J].Postharvest Biology and Technology,2016,113:8-16.
[4] 董欣瑞,张珮,袁楚珊,等.1-MCP联合乙烯吸附剂处理对黄桃果实冷害与糖代谢的影响[J].中国食品学报,2022,22(9):208-216.DONG X R,ZHANG P,YUAN C S,et al.Effects of 1-MCP combined with ethylene adsorbent on chilling injury and sugar metabolism of peach fruit[J].Journal of Chinese Institute of Food Science and Technology,2022,22(9):208-216.
[5] ZHANG W L,ZHAO H D,JIANG H T,et al.Multiple 1-MCP treatment more effectively alleviated postharvest nectarine chilling injury than conventional one-time 1-MCP treatment by regulating ROS and energy metabolism[J].Food Chemistry,2020,330:127256.
[6] ZHANG L,WANG J W,ZHOU X,et al.Effect of ATP treatment on enzymes involved in energy and lipid metabolisms accompany peel browning of ‘Nanguo’ pears during shelf life after low temperature storage[J].Scientia Horticulturae,2018,240:446-452.
[7] ZHU J,LI C Y,FAN Y T,et al.γ-Aminobutyric acid regulates mitochondrial energy metabolism and organic acids metabolism in apples during postharvest ripening[J].Postharvest Biology and Technology,2022,186:111846.
[8] WANG C L,DU J M,HOU D H,et al.Quality retention and delay postharvest senescence of figs (Ficus carica L.) using 1-methylcyclopropene and modified atmosphere packaging during cold storage[J].Food Bioscience,2023,53:102748.
[9] XU F X,LIU S Y,LIU Y F,et al.Effectiveness of lysozyme coatings and 1-MCP treatments on storage and preservation of kiwifruit[J].Food Chemistry,2019,288:201-207.
[10] LYU J Y,ZHANG M Y,BAI L,et al.Effects of 1-methylcyclopropene (1-MCP) on the expression of genes involved in the chlorophyll degradation pathway of apple fruit during storage[J].Food Chemistry,2020,308:125707.
[11] LIU R L,GAO H Y,CHEN H J,et al.Synergistic effect of 1-methylcyclopropene and carvacrol on preservation of red pitaya (Hylocereus polyrhizus)[J].Food Chemistry,2019,283:588-595.
[12] ZHOU H J,YE Z W,WANG L F,et al.1-MCP regulates taste development in cold-stored peach fruit through modulation of sugar,organic acid,and polyphenolic metabolism[J].Postharvest Biology and Technology,2025,225:113518.
[13] 焦旋,高阳,高振峰,等.压差预冷对油桃贮运品质及抗氧化性的影响[J].食品与发酵工业,2020,46(22):173-179.JIAO X,GAO Y,GAO Z F,et al.Improving quality and antioxidant capacity of nectarine by forced-air precooling during storage and transportation[J].Food and Fermentation Industries,2020,46(22):173-179.
[14] WANG Z,CAO J K,JIANG W B.Changes in sugar metabolism caused by exogenous oxalic acid related to chilling tolerance of apricot fruit[J].Postharvest Biology and Technology,2016,114:10-16.
[15] 林毅雄,林艺芬,陈艺晖,等.采前喷施胺鲜酯对采后龙眼果实贮藏期间果皮能量代谢的影响[J].食品科学,2022,43(5):175-184.LIN Y X,LIN Y F,CHEN Y H,et al.Effect of pre-harvest spray application of diethyl aminoethyl hexanoate on the energy metabolism in longan fruit pericarp during postharvest storage[J].Food Science,2022,43(5):175-184.
[16] HUANG H,GUO L F,WANG L,et al.1-Methylcyclopropene (1-MCP) slows ripening of kiwifruit and affects energy status,membrane fatty acid contents and cell membrane integrity[J].Postharvest Biology and Technology,2019,156:110941.
[17] 林静颖,李辉,袁芳,等.1-甲基环丙烯处理对采后‘油木奈’果实呼吸速率和活性氧代谢的影响[J].食品科学,2020,41(23):205-211.LIN J Y,LI H,YUAN F,et al.Effect of 1-methylcyclopropene treatment on respiration rate and reactive oxygen species metabolism during postharvest storage of ‘Younai’ plum fruit[J].Food Science,2020,41(23):205-211.
[18] ZHAO H D,JIAO W X,CUI K B,et al.Near-freezing temperature storage enhances chilling tolerance in nectarine fruit through its regulation of soluble sugars and energy metabolism[J].Food Chemistry,2019,289:426-435.
[19] SUN Z,LI Y,ZHOU J,et al.Effects of exogenous nitric oxide on contents of soluble sugars and related enzyme activities in ‘Feicheng’ peach fruit[J].Journal of the Science of Food and Agriculture,2011,91(10):1795-1800.
[20] YU L N,SHAO X F,WEI Y Y,et al.Sucrose degradation is regulated by 1-methycyclopropene treatment and is related to chilling tolerance in two peach cultivars[J].Postharvest Biology and Technology,2017,124:25-34.
[21] ZHOU Q,ZHANG C L,CHENG S C,et al.Changes in energy metabolism accompanying pitting in blueberries stored at low temperature[J].Food Chemistry,2014,164:493-501.
[22] LIN Y X,LIN H T,LIN M S,et al.Hydrogen peroxide reduced ATPase activity and the levels of ATP,ADP,and energy charge and its association with pulp breakdown occurrence of longan fruit during storage[J].Food Chemistry,2020,311:126008.
[23] JIN P,ZHU H,WANG L,et al.Oxalic acid alleviates chilling injury in peach fruit by regulating energy metabolism and fatty acid contents[J].Food Chemistry,2014,161:87-93.
[24] LIN Y F,CHEN M Y,LIN H T,et al.DNP and ATP induced alteration in disease development of Phomopsis longanae Chi-inoculated longan fruit by acting on energy status and reactive oxygen species production-scavenging system[J].Food Chemistry,2017,228:497-505.
[25] HUANG H K,YE M T,CAI X L,et al.Synergistic regulation of Chitosan and NaHS on energy metabolism and endogenous H2S metabolism of postharvest nectarines[J].Scientia Horticulturae,2023,311:111792.