蜡样芽孢杆菌(Bacillus cereus)是一种兼性厌氧的革兰氏阳性菌,可通过水解淀粉造成谷物黏稠腐败[1],或通过分解蛋白导致乳制品凝固及苦味产生[2]。当菌体数量超过105 CFU/g时,会分泌呕吐毒素或腹泻毒素,引发食源性疾病[3]。该菌在腐乳成品以及发酵过程中广泛存在,在腐乳原料(大豆)及发酵环境中也有分布[4-5]。蜡样芽孢杆菌在营养胁迫或极端环境下产生芽孢,其芽孢在巴氏杀菌处理后能以休眠状态存活多年,条件适宜时重新萌发为营养体,对食品安全存在持续威胁。其芽孢的抗性得益于其紧密的多层结构,包括芽孢衣、芽孢内膜等以及2,6-吡啶二羧酸(2,6-pyridinedicarboxylic acid,DPA)、α/β型小酸溶性蛋白(α/β-type small acid-soluble proteins,SASPs)等保护性成分。芽孢灭活已成为食品生产加工过程中的重要考虑因素。
传统的热处理对营养体有效,但通常难以在不破坏食品感官品质和营养风味的条件下消除芽孢,非热杀菌技术因此成为研究热点。光动力技术(photodynamic technology,PDT)是一种新型非热杀菌手段,具有成本低、高效安全等特点[6]。PDT通过特定波长的光源激活光敏剂,通过产生活性氧(reactive oxygen species,ROS),破坏蛋白质、脂质等细胞成分,诱导细胞损伤或死亡[7]。姜黄素是一种从姜黄中提取的天然多酚,具有吸收光谱广泛、安全性高等特点[8],是一种极具潜力的天然光敏剂。PDT已被广泛证实可有效灭活细菌营养体[9-11],但其对细菌芽孢的研究主要聚焦于合成新型光敏剂[12],比较不同光敏剂和优化光参数的灭活效果[13],以及拟合灭活动力学曲线[14]。本研究对比姜黄素与PDT协同处理对蜡样芽孢杆菌营养体和芽孢的灭活差异,探究其差异形成机制,并通过扫描电镜(scanning electron microscope,SEM)和透射电镜(transmission electron microscope,TEM)直接观察PDT对芽孢造成的损伤,并将该技术应用于腐乳中蜡样芽孢杆菌的灭活,为PDT在食品行业中的应用提供参考。
1 材料与方法
1.1 材料与试剂
姜黄素(纯度>98%),上海麦克林生化科技股份有限公司;无水乙醇,天津永大化学试剂有限公司;PBS(0.1 mol/L,pH 7.2~7.4),博士德生物工程有限公司;营养肉汤(nutrient broth,NB)、营养琼脂(nutrient agar,NA)、甘露醇卵黄多黏菌素琼脂平板(mannitol yolk polymyxin agar,MYP),广东环凯微生物科技有限公司;孔雀绿,福州飞净生物科技有限公司;活性氧(reactive oxygen species,ROS)试剂盒,碧云天生物技术有限公司;2.5%(体积分数)戊二醛,源叶生物有限公司;丙酮,北京索莱宝生物科技有限公司。
1.2 仪器与设备
LED蓝光设备(420 nm),徐州爱佳电子科技有限公司;X3FR高速冷冻离心机,赛默飞世尔科技公司;Infinite M200 PRO酶标仪,瑞士帝肯公司;SU-8010 SEM、H-7600 TEM,日本日立公司。
1.3 实验方法
1.3.1 细菌菌株与培养
蜡样芽孢杆菌菌种CMCC 63303购自广东省微生物菌种保藏中心。NA平板上活化蜡样芽孢杆菌后接种至NB肉汤,37 ℃下120 r/min振荡培养得到营养体悬液。
营养体悬液均匀涂布于NA平板,37 ℃培养,用孔雀绿染色在显微镜下观察监测芽孢的形成,当芽孢的浓度>95%时,从平板上刮落菌体,收集于无菌PBS中。4 ℃下7 000×g离心收集菌体沉淀,PBS多次洗涤。1 g/mL溶菌酶溶液在37 ℃下处理菌体30 min,去除残留营养体,PBS多次洗涤,得到芽孢悬液,保存于4 ℃备用。
1.3.2 姜黄素溶液的配置
姜黄素粉末溶于无水乙醇,制成20 mmol/L姜黄素母液,0.22 μmol/L滤膜过滤除菌,无菌PBS稀释为不同浓度,4 ℃避光保存。
1.3.3 光源
采用的光动力设备见本团队的前期研究报道[15],设备顶部由高度抛光的不锈钢制成,均匀分布8个10 W无焊LED,光源垂直照射样品板,距离10 cm,光密度为69.97 mW/cm2。光剂量的计算如公式(1)所示:
E=P×t
(1)
式中:E,光剂量,J/cm2;P,光密度,W/cm2;t,光照时间,s。
1.3.4 姜黄素浓度对PDT的影响
营养体:将1 mL蜡样芽孢杆菌营养体分别和25、50、75、100、250 μmol/L(工作浓度,下同)姜黄素溶液等体积混匀于6孔板,37 ℃避光孵育30 min,LED蓝光设备下光照30 min。对照组为:-P-L(无姜黄素,不光照),+P-L(250 μmol/L姜黄素,不光照),-P+L(无姜黄素,光照30 min)。
芽孢:1 mL芽孢悬液分别与100、250、500、1 000、1 500 μmol/L姜黄素溶液等体积混匀,37 ℃避光孵育60 min,光照60 min。对照组为:-P-L(无姜黄素,不光照),+P-L(1 500 μmol/L姜黄素,不光照),-P+L(无姜黄素,光照60 min)。
1.3.5 光照时间对PDT的影响
营养体:1 mL营养体与100 μmol/L姜黄素溶液等体积混匀,37 ℃避光孵育30 min,分别光照0、5、10、15、20、30 min。设置对照组-P-L(无姜黄素,不光照),-P+L(无姜黄素,光照30 min)。
芽孢:1 mL芽孢与1 000 μmol/L姜黄素溶液等体积混匀,37 ℃暗孵育60 min,分别光照0、15、30、45、60、90 min。设置对照组-P-L(无姜黄素,不光照),-P+L(无姜黄素,光照90 min)。
1.3.6 ROS的测定
采用LI等[16]的方法,利用2,7-二氯荧光素二乙酸酯(2′,7′-dichlorodihydrofluorescein diacetate,DCFH-DA)荧光探针来测定ROS水平。将营养体和芽孢分别与探针充分混匀(体积比为1 000∶1),37 ℃避光孵育20 min,用PBS洗去多余探针。
装载探针的营养体和芽孢悬液分别与250 μmol/L姜黄素溶液混匀,37 ℃避光孵育20 min,光照30 min。比较同等PDT条件下营养体和芽孢的灭活率,并采用酶标仪在488 nm/525 nm的激发和发射波长下测定荧光强度。
1.3.7 SEM和TEM观察芽孢形态变化
1 mL芽孢悬液分别与1 000 μmol/L姜黄素溶液等体积混匀,避光孵育60 min,光照60 min。同时设置高温处理组(121 ℃,20 min)作为对照。电镜制样方法参照GUAN等[17]和SEO等[18]进行些许改动。
SEM:芽孢离心保留菌体,2.5%戊二醛固定,4 ℃过夜静置,PBS洗去固定液,3次重复,梯度酒精(体积分数为30%、50%、70%、80%、90%和95%)脱水,每次15 min,完成后用无水酒精再脱水2次,每次20 min。临界点干燥,真空离子喷金,观察并拍摄。
TEM:前处理同SEM,将酒精梯度脱水后的菌体用纯丙酮处理20 min,丙酮与包埋剂等体积混合处理1 h,丙酮与包埋剂混合液(体积比为1∶3)处理3 h,纯包埋剂70 ℃固化过夜,切片,双重染色后晾干,观察并拍摄。
1.3.8 光动力在腐乳中蜡样芽孢杆菌的应用
将结束前发酵未开始腌制的市售广式腐乳进行人工染菌,将腐乳浸没在过夜培养的蜡样芽孢杆菌菌液中(约108 CFU/mL),放置晾干。腐乳浸没在250 μmol/L姜黄素溶液内1 min捞出,暗孵育30 min,光照30 min。未处理组和光动力后的腐乳取最外层、内层和中心层3个部位采用MYP培养基进行蜡样芽孢杆菌计数。
1.4 数据处理与统计分析
使用SPSS 26.0进行统计分析。数据以“平均值±标准差”表示,使用单因素方差分析进行比较,实验重复3次,P<0.05认为是显著的。
2 结果与分析
2.1 姜黄素浓度对PDT的影响
图1-a和图1-b分别为姜黄素浓度对PDT灭活营养体和芽孢的影响。对照组(-P-L、+P-L、-P+L)之间均无明显差异,说明光敏剂和光源光照为PDT的关键要素,姜黄素或光照的单独作用无法实现有效灭菌。当光照剂量为125.95 J/cm2(30 min光照时间),在25 μmol/L姜黄素作用下,对营养体的灭活效果达到2.29 lg CFU/mL。随着姜黄素浓度升高,营养体显著下降。当姜黄素浓度升至250 μmol/L时,营养体减少了4.29 lg CFU/mL。光动力对芽孢的灭活效果同样具有姜黄素依赖性,灭活效果随姜黄素浓度升高而提升。在251.89 J/cm2的光照(光照时长为60 min)下,当姜黄素浓度为100 μmol/L时,灭活了1.19 lg CFU/mL芽孢。当姜黄素浓度为1 500 μmol/L时,芽孢减少了约3.27 lg CFU/mL。王晓迪等[19]同样发现增加光敏剂的浓度可以增强PDT的灭活效果。在光动力对芽孢进行灭活时,达到相同的灭活效果所需的光照剂量和姜黄素浓度远高于营养体,说明芽孢对光动力的敏感性远不如营养体。
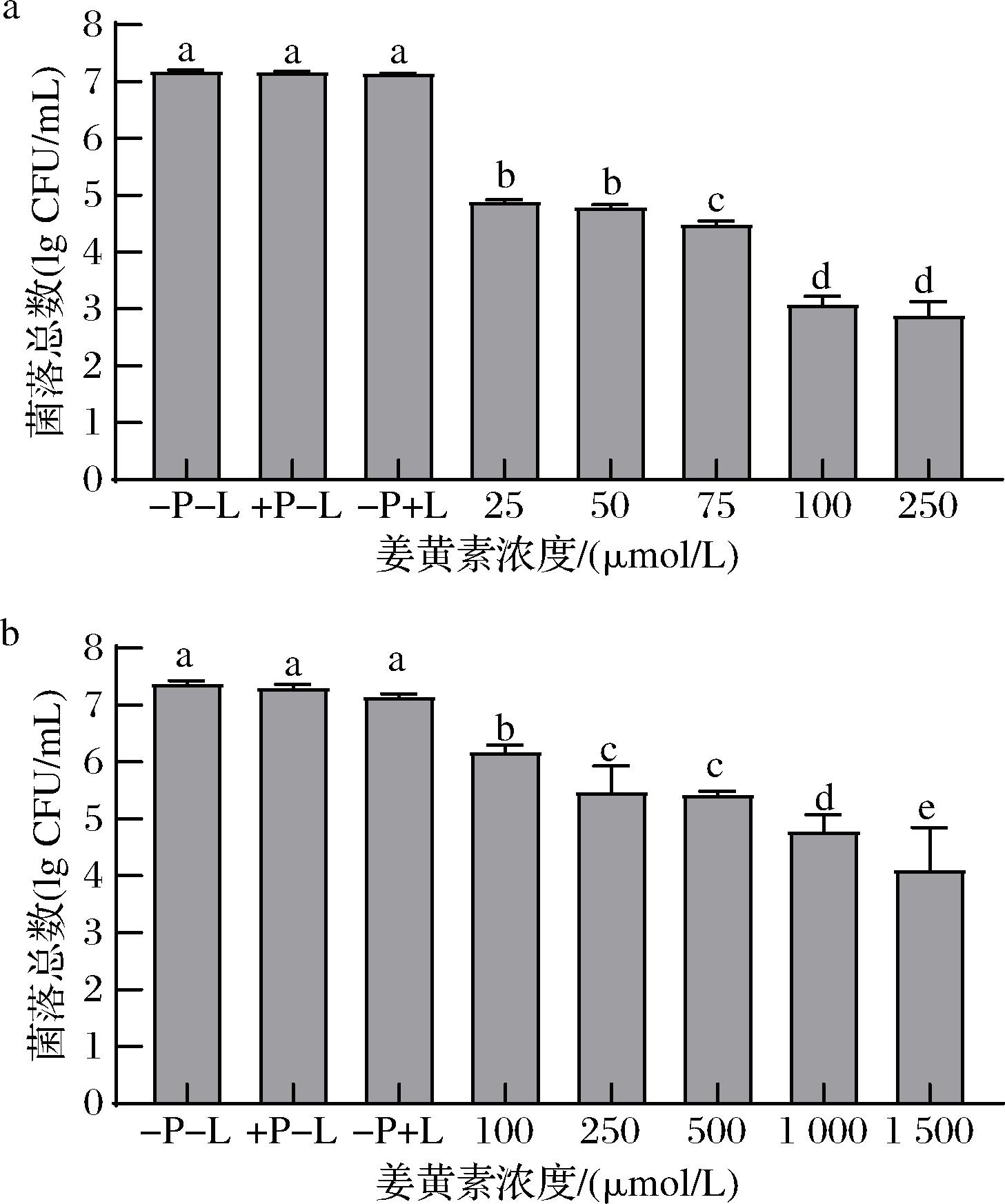
a-营养体;b-芽孢
图1 姜黄素浓度对PDT的影响
Fig.1 Effect of curcumin concentration on PDT inactivation
注:不同字母表明具有显著性差异(P<0.05)(下同)。
2.2 光照时间对PDT的影响
延长光照时间,光动力对营养体和芽孢的灭活效果均增强(图2)。100 μmol/L的姜黄素作用下,光照5 min即可灭活3.06 lg CFU/mL营养体。当光照时间为15 min时,灭活量达4.02 lg CFU/mL。继续延长光照时间,其灭菌率无显著提升。对芽孢进行60 min 光照,约灭活2.01 lg CFU/mL,继续光照,灭菌效果增强不显著。因此在光动力的实际应用中,可优化光照时长以兼顾效率与效果,在保障灭菌效果的前提下,适当缩短光照时间。
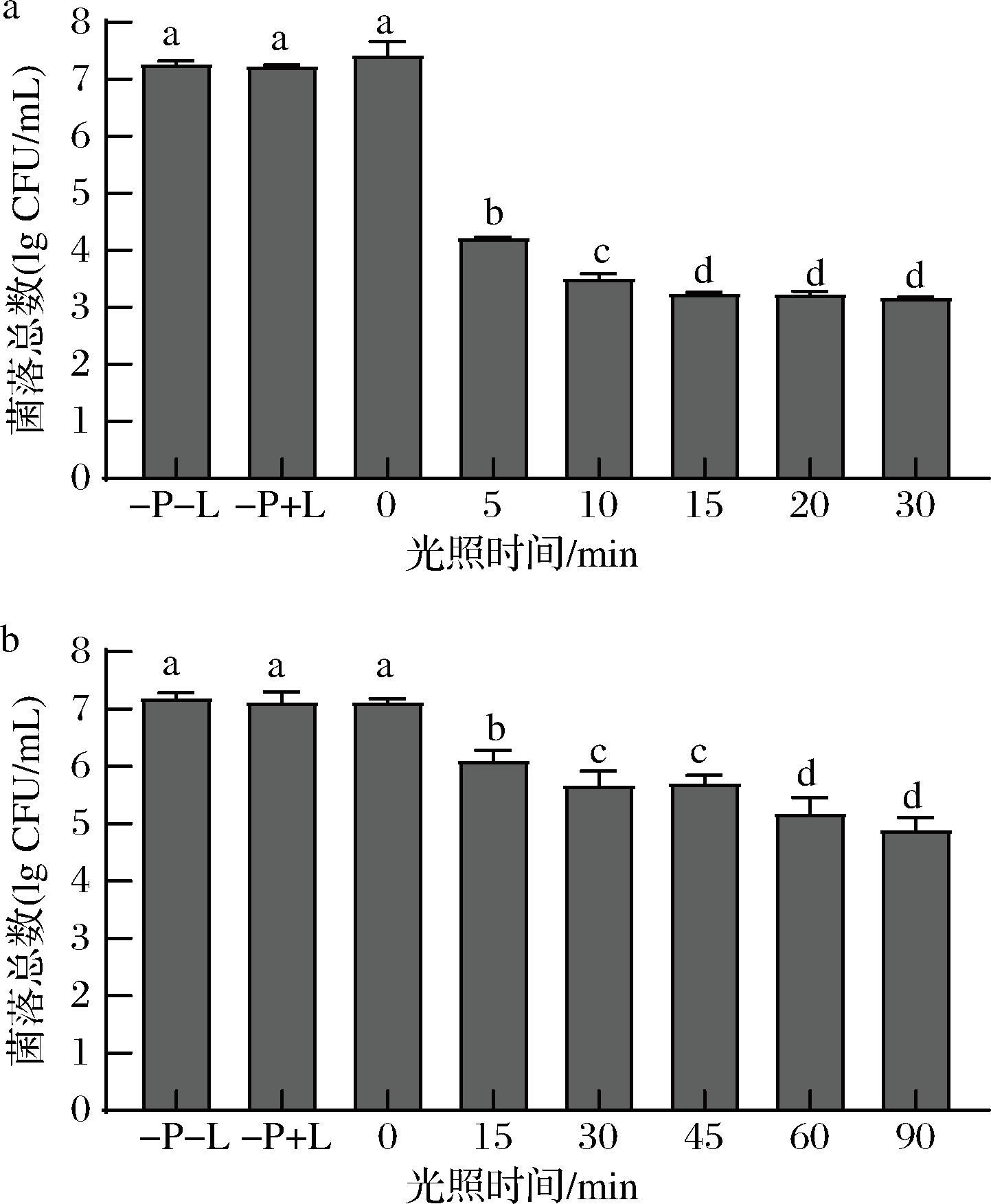
a-营养体;b-芽孢
图2 光照时间对PDT的影响
Fig.2 Effect of light time on PDT inactivation
2.3 PDT诱导ROS的产生
如图3所示,相同的PDT处理条件下(250 μmol/L姜黄素,光照剂量为125.95 J/cm2),营养体实现灭活达7.18 lg CFU/mL,ROS对应的荧光强度为142.67,此时芽孢的灭活率为43.62%(灭活量约0.29 lg CFU/mL),荧光强度为50.25。ROS介导的氧化损伤是PDT灭菌的核心机制,ROS稳定剂的加入显著增强光动力的杀菌作用,而ROS清除剂的存在则使得PDT的效果减弱[20]。在同一PDT处理条件后,芽孢产生的ROS远低于营养体,致使PDT对芽孢的灭活率更低。与2.1节和2.2节结果一致:芽孢达到与营养体相近的灭活量,所需的PDT条件远高于营养体。相比营养体,芽孢具有更为致密的多层结构,包括芽孢外壁、芽孢衣、芽孢外膜、皮层、芽孢壁、芽孢内膜和核区等,这些结构对维持芽孢的强抗逆性具有重要作用。其独特的结构可作为渗透性屏障,降低芽孢的通透性,阻碍对光敏剂的吸附吸收,这可能是造成芽孢ROS的产生量更低的原因。
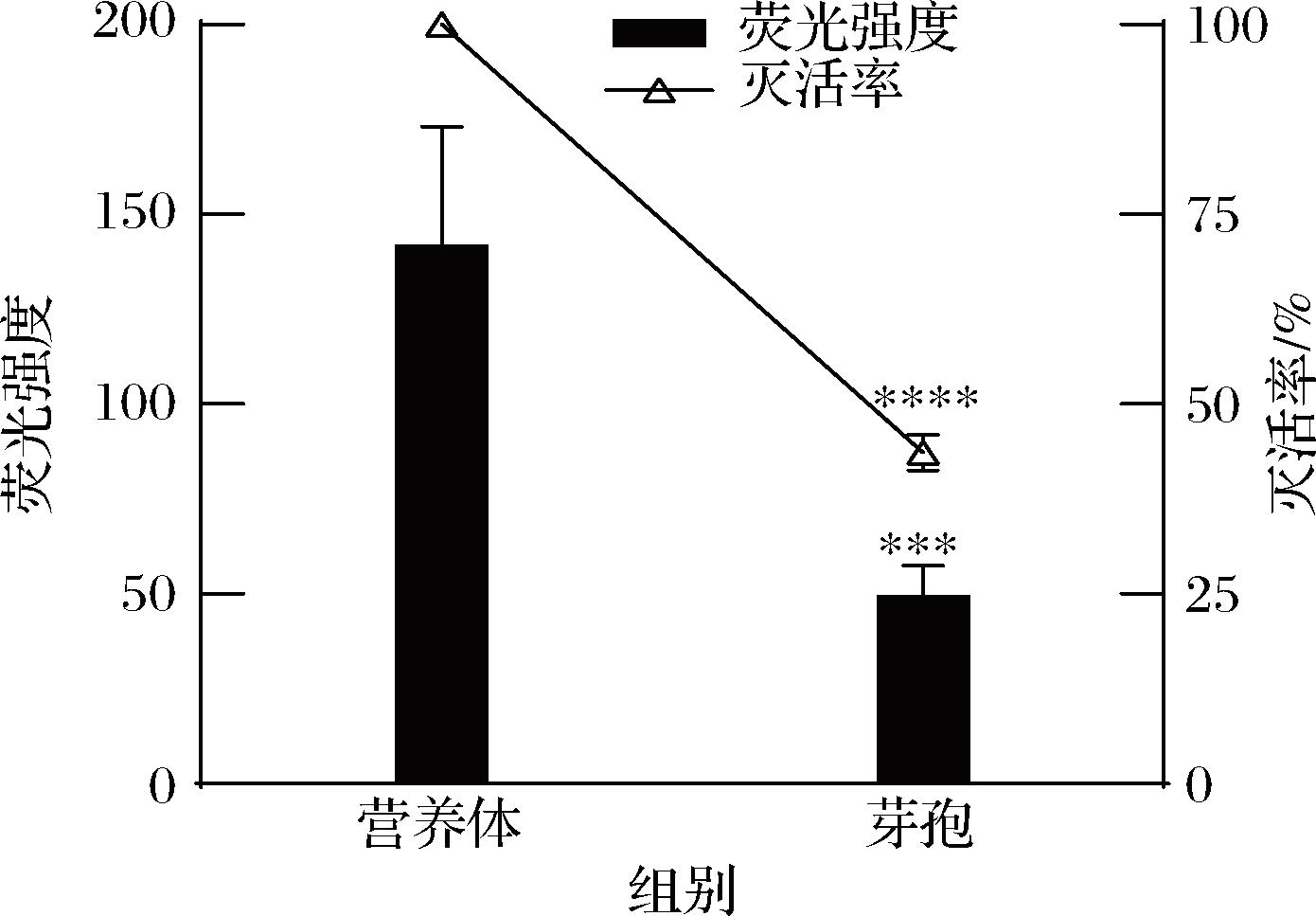
图3 PDT诱导产生的ROS水平
Fig.3 ROS production of B.cereus induced by PDT
注:***,P<0.001;****,P<0.000 1。
2.4 PDT处理后芽孢的形态变化
通过SEM可观察芽孢的表面形态变化。图4-a为未处理组的蜡样芽孢杆菌芽孢,饱满圆润,略带褶皱,呈椭圆状。图4-e为高温灭菌组,芽孢结构被严重破坏,出现孔洞,内容物泄露,呈塌陷皱缩状。图4-c为PDT组的芽孢,部分芽孢结构破坏,内容物外泄,出现皱缩,同时存在结构相对完整、并无明显破损的芽孢。
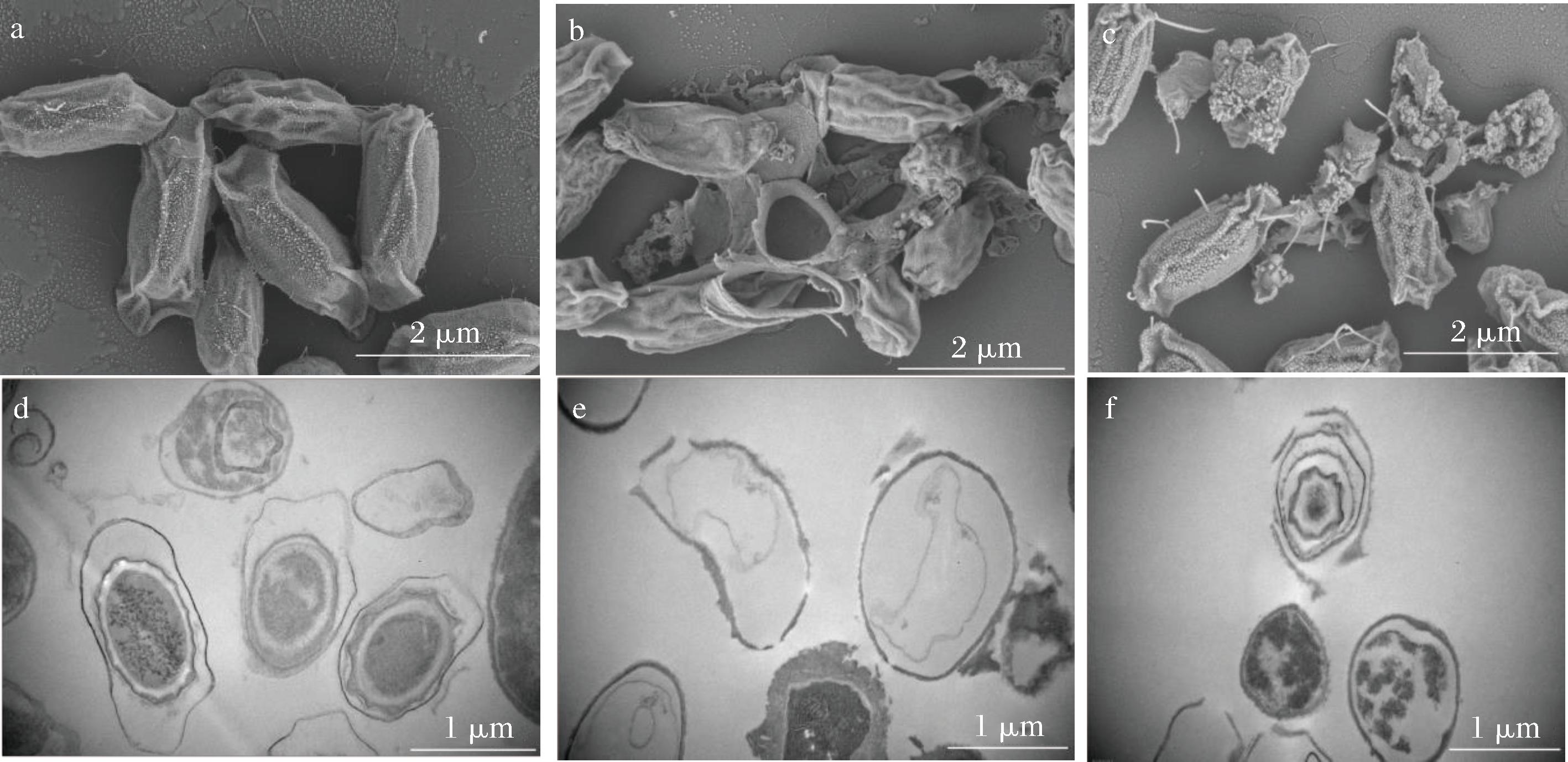
a-未处理组SEM图;b-高温灭菌组(121 ℃,20 min)SEM图;c-PDT组SEM图;d-未处理组TEM图;e-高温灭菌组(121 ℃,20 min)TEM图;f-PDT组TEM图
图4 PDT处理对芽孢形态的影响
Fig.4 Effect of PDT on morphology of B.cereus spore
TEM可观察到芽孢的内部结构。未处理组的芽孢多层结构完整,芽孢外壁、皮层、核心等结构清晰可见(图4-d)。高温灭菌后的芽孢外壁破损出现孔洞、存在脱落,内容物几乎完全泄露(图4-e)。PDT处理后,芽孢外壁等多个结构层出现程度不一的损坏,但破损程度不如高温处理组,内容物出现部分流失。
可见虽然PDT对芽孢的灭活作用远不如营养体,但对芽孢的结构造成了破坏(破坏程度不及高温处理)。其结构损伤促进光敏剂向芽孢内部渗透,进一步氧化损伤亚细胞结构和其他芽孢成分而加速芽孢灭活,或直接导致芽孢的死亡,并降低出芽活性。芽孢外壁还可能与芽孢的黏附、传播和毒性等关系密切[21],PDT可能同时干扰了蜡样芽孢杆菌芽孢黏附和毒性相关的生物活性,削弱其定殖和侵染的能力,从而降低其环境适应性。PDT破坏蜡样芽孢杆菌芽孢多层结构,致使其完整性受损,出芽活性和环境适应性降低,说明PDT对致病菌芽孢的控制具有潜力。
2.5 姜黄素与光动力协同灭菌在腐乳中的应用
腐乳的菌含量由外而内呈现减少的趋势,外层菌含量最高,中心层最低(图5)。姜黄素浓度为250 μmol/L,光照剂量为125.95 J/cm2的PDT处理下,灭菌效果并不显著,最外层约灭活0.13 lg CFU/mL,内层灭活0.37 lg CFU/mL,中心层灭活0.25 lg CFU/mL,其灭菌效果远不如PDT在蜡样芽孢杆菌悬液中的灭活效果。其原因可能是姜黄素与细菌的接触以及光照强度受腐乳的粗糙表面影响,或需进一步优化姜黄素浓度和光照时间等参数设置,未来可借助其他非热杀菌技术协同增效。
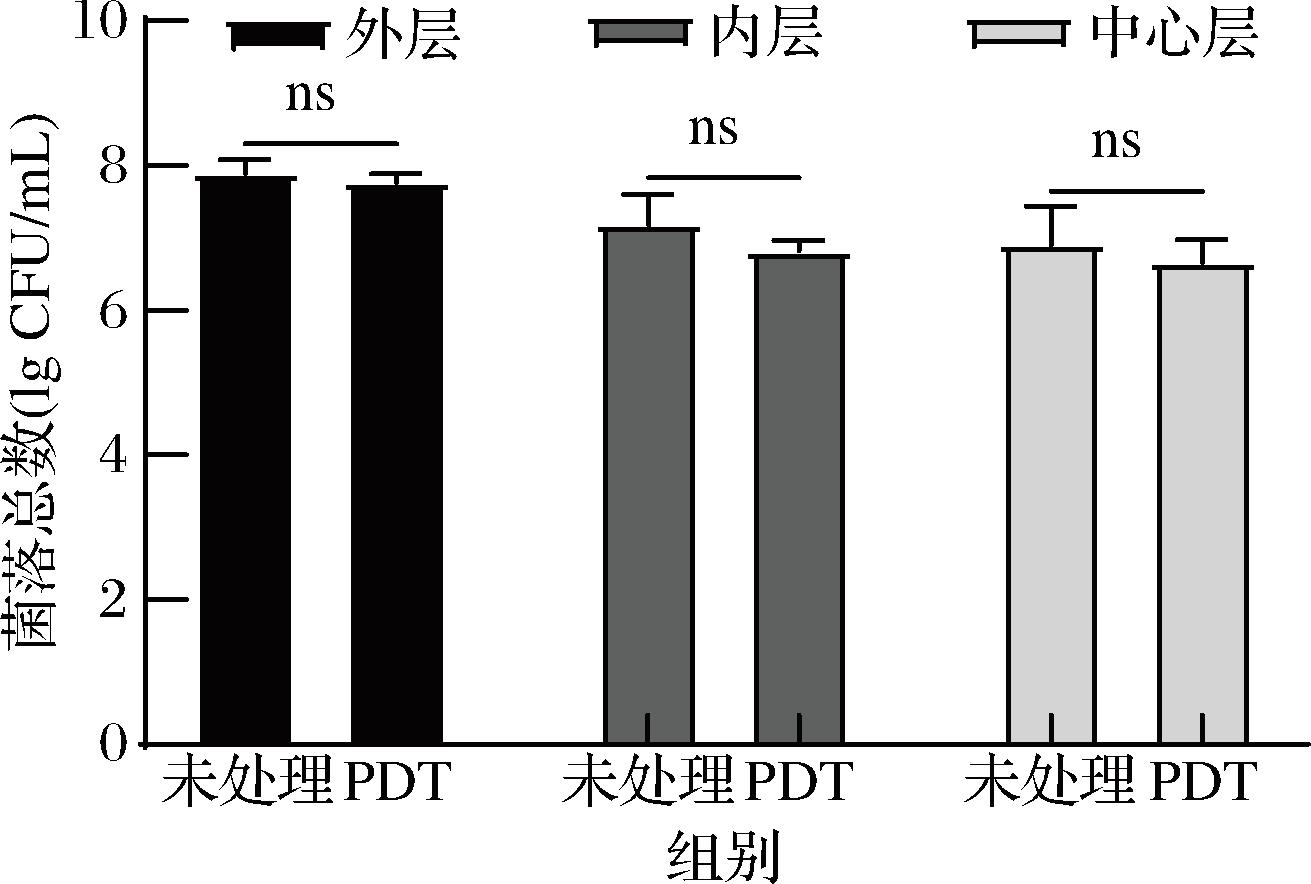
图5 光动力对腐乳中蜡样芽孢杆菌的应用
Fig.5 Application of PDT on B.cereus in sufu
注:ns,无显著性差异(P>0.05)。
3 结论与讨论
姜黄素与光动力协同灭菌效果呈现姜黄素浓度和光照时间依赖性。PDT对芽孢的灭活效果远不如营养体,在250 μmol/L姜黄素,30 min光照条件下,营养体灭活4.29 lg CFU/mL;在1 500 μmol/L姜黄素,60 min光照条件下,芽孢最高减少约3.27 lg CFU/mL。ROS生成量差异是导致PDT灭活效果不同的重要因素——营养体的ROS水平远高于芽孢。此外PDT会引发芽孢结构损伤,包括形成芽孢外壁孔洞、内容物泄露等,从而导致芽孢的灭活和生理活性的破坏。证明了PDT对蜡样芽孢杆菌的营养体和休眠体的控制均具有应用潜力。但PDT在腐乳基质中的应用受限,可结合其他非热杀菌手段协同增效。本文阐述了光动力对蜡样芽孢杆菌的差异性灭活机制,表明了光动力对蜡样芽孢杆菌的作用潜力,并为传统发酵食品的微生物安全控制提供了新思路。
[1] TAN L J,XIE Y,ZHANG W D,et al.Spoilage potential of Bacillus isolated from cooked sausage:Bidirectional verification from in vitro to in situ[J].International Journal of Food Microbiology,2025,433:111114.
[2] TATSINKOU FOSSI B,TATAH KIHLA AKOACHERE J F,NCHANJI G T,et al.Occurrence,heat and antibiotic resistance profile of Bacillus cereus isolated from raw cow and processed milk in Mezam Division,Cameroon[J].International Journal of Dairy Technology,2017,70(1):43-51.
[3] XIAN J L,WANG H F,DIAO S Y,et al.Lactococcus lactis subsp.lactis LJL7 m20 strongly inhibits growth of the Bacillus cereus group from sufu[J].Food Bioscience,2024,62:105549.
[4] JIN Z K,LI L,ZHENG Y,et al.Inhibition of Bacillus cereus by garlic (Allium sativum) essential oil during manufacture of white sufu,a traditional Chinese fermented soybean curd[J].LWT,2020,130:109634.
[5] WAN H F,LIU T,SU C W,et al.Evaluation of bacterial and fungal communities during the fermentation of Baixi sufu,a traditional spicy fermented bean curd[J].Journal of the Science of Food and Agriculture,2020,100(4):1448-1457.
[6] ZHU S Y,SONG Y K,PEI J L,et al.The application of photodynamic inactivation to microorganisms in food[J].Food Chemistry:X,2021,12:100150.
[7] LIU D,GU W M,WANG L,et al.Photodynamic inactivation and its application in food preservation[J].Critical Reviews in Food Science and Nutrition,2023,63(14):2042-2056.
[8] YU X P,ZOU Y,ZHANG Z Q,et al.Recent advances in antimicrobial applications of curcumin-mediated photodynamic inactivation in foods[J].Food Control,2022,138:108986.
[9] SARAIVA B B,RODRIGUES B M,DA SILVA R C Jr,et al.Photodynamic inactivation of Pseudomonas fluorescens in Minas Frescal cheese using curcumin as a photosensitizer[J].LWT,2021,151:112143.
[10] YUAN Y,LIU Q Y,HUANG Y J,et al.Antibacterial efficacy and mechanisms of curcumin-based photodynamic treatment against Staphylococcus aureus and its application in juices[J].Molecules,2022,27(20):7136.
[11] CHEN H M,ZHOU Q,HUANG L J,et al.Curcumin-mediated photodynamic treatment extends the shelf life of salmon (Salmo salar) sashimi during chilled storage:Comparisons of preservation effects with five natural preservatives[J].Food Research International,2023,173:113325.
[12] EICHNER A,GOLLMER A,SP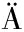 TH A,et al.Fast and effective inactivation of Bacillus atrophaeus endospores using light-activated derivatives of vitamin B2[J].Photochemical &Photobiological Sciences,2015,14(2):387-396.
TH A,et al.Fast and effective inactivation of Bacillus atrophaeus endospores using light-activated derivatives of vitamin B2[J].Photochemical &Photobiological Sciences,2015,14(2):387-396.
[13] DO PRADO-SILVA L,BRANCINI G T P,BACHMANN L,et al.Controlling Alicyclobacillus acidoterrestris spores contamination on orange surfaces using different photosensitizers and light sources[J].Food Control,2025,167:110798.
[14] DO PRADO-SILVA L,ALVARENGA V O,BRAGA G 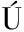 L,et al.Inactivation kinetics of Bacillus cereus vegetative cells and spores from different sources by antimicrobial photodynamic treatment (aPDT)[J].LWT,2021,142:111037.
L,et al.Inactivation kinetics of Bacillus cereus vegetative cells and spores from different sources by antimicrobial photodynamic treatment (aPDT)[J].LWT,2021,142:111037.
[15] 蓝彩娟,陈洁怡,何雨薇,等.壳聚糖-姜黄素光动力协同作用对圣女果食源性致病菌的灭活效果[J].食品科学,2023,44(21):258-266.LAN C J,CHEN J Y,HE Y W,et al.Synergistic photodynamic effect of chitosan and curcumin on the inactivation of foodborne pathogens on cherry tomatoes[J].Food Science,2023,44(21):258-266.
[16] LI H,HE C,LI G J,et al.The modes of action of Epsilon-polylysine (ε-PL) against Botrytis cinerea in jujube fruit[J].Postharvest Biology and Technology,2019,147:1-9.
[17] GUAN G L,ZHANG L N,ZHU J X,et al.Antibacterial properties and mechanism of biopolymer-based films functionalized by CuO/ZnO nanoparticles against Escherichia coli and Staphylococcus aureus[J].Journal of Hazardous Materials,2021,402:123542.
[18] SEO C W,KIM Y K,AN J L,et al.The effect of photodynamic therapy using Radachlorin on biofilm-forming multidrug-resistant bacteria[J].Osong Public Health and Research Perspectives,2022,13(4):290-297.
[19] 王晓迪,郑双芝,庞一,等.光动力技术对副溶血性弧菌的灭活作用[J].食品与发酵工业,2024,50(3):119-125.WANG X D,ZHENG S Z,PANG Y,et al.Inactivation effect of photodynamic technology on Vibrio parahaemolyticus[J].Food and Fermentation Industries,2024,50(3):119-125.
[20] SHENG L N,LI X R,WANG L X.Photodynamic inactivation in food systems:A review of its application,mechanisms,and future perspective[J].Trends in Food Science &Technology,2022,124:167-181.
[21] KOOPMAN N,REMIJAS L,SEPPEN J,et al.Mechanisms and applications of bacterial sporulation and germination in the intestine[J].International Journal of Molecular Sciences,2022,23(6):3405.