玉米须为玉米的雌花花柱和花头,是玉米的主要副产物之一,经除杂后鲜用或晒干生用,是我国民间较为常用的中药材[1],具有多种药理活性并且未发现其安全性问题[2],常被应用于治疗痛风、水肿、膀胱炎、高血糖、高血脂等疾病[3]。目前我国关于玉米须实际应用的报道较少,大量玉米须未得到合理利用造成极大的资源浪费,并且对其研究主要集中在活性物质提取、制备复合饮品方面[4-5]。因此可考虑以玉米须为原料,提高其利用率,以充分研究开发多元化的玉米须产品。
多糖是由单糖经糖苷键连接而成的一种天然生物大分子,具有广泛的生物活性,与蛋白质和核酸共同组成维持生命体活动的三大生物大分子[6]。玉米须中包含多种活性物质如多糖、黄酮、多酚、苷类等[7],其中玉米须多糖是其最主要的功能活性成分且占比较大,有抑菌、利尿、降血糖、降血脂、抗氧化、抗高尿酸血症等多种生物活性,但是目前关于玉米须多糖的研究尚处于起步阶段,且多聚焦于玉米须粗多糖的提取和生物活性研究[8],有关均一多糖的制备、结构鉴定和活性揭示鲜有报道。因此,本研究选取玉米须为原材料提取粗多糖并对其分离纯化得到玉米须均一多糖(corn silk polysaccharide,以下命名为CSPSS),深入探究玉米须多糖的结构特征及其降血糖活性,以期为其产业开发和相关基础理论研究提供支持。
1 材料与方法
1.1 材料与试剂
苯酚、硫酸、氯仿、氢氧化钠、三氟乙酸、甲醇、乙腈、1-苯基-3-甲基-5-吡唑啉酮(1-phenyl-3-methyl-5-pyrazolinone,PMP),天津市大茂化学试剂厂;葡聚糖标准品,北京拜尔迪生物公司;DEAE Sepharose Fast Flow、Sephacryl S300,美国通用电气医疗公司;3,5-二硝基水杨酸、对硝基苯基-α-D-吡喃葡萄糖苷(p-nitrophenyl-α-D-pyranglucoside,PNPG)、阿卡波糖、α-淀粉酶、α-葡萄糖苷酶、葡萄糖、蛋黄粉,上海源叶生物科技有限公司。
1.2 仪器与设备
UF-20中空纤维超滤装置,大城县华泰净化技术有限公司;AKAT prime plus纯化系统,安玛西亚生物科学公司;M3酶标仪,美谷分子仪器有限公司;PRIMAIDE高效液相色谱仪、S-3400扫描电子显微镜,日立科学仪器有限公司;Lamda 35紫外可见分光光度计、Spectrum 3红外光谱仪、TGA 8000热重分析仪,美国PE公司;AVANCE NEO 600M超导核磁共振仪、D8X射线衍射仪,德国布鲁克公司;Q-20差示扫描量热仪,美国TA公司;ZS90纳米粒度Zeta电位测定仪,英国马尔文有限公司;ACCU-CHEK Guide血糖仪,德国罗氏诊断公司。
1.3 实验方法
1.3.1 玉米须粗多糖的提取
玉米须经除杂、清洗、干燥后粉碎,粉末过0.25 mm筛后按1∶20(g∶mL)料液比加入体积分数为80%的乙醇溶液,在60 ℃下提取1 h,经此预处理的玉米须粉烘干后密封备用。取预处理后玉米须粉按1∶20(g∶mL)料液比加入蒸馏水,沸水提取2 h,重复2次。将水提液经50 kDa超滤膜超滤分离,截留液经减压浓缩后冻干。取适量冻干样品配制10 mg/mL样品溶液,加入适量无水乙醇至溶液乙醇体积分数达到30%,于4 ℃ 静置过夜后离心收集沉淀并冷冻干燥,制得玉米须多糖CSPB-30。
1.3.2 玉米须粗多糖的分离纯化
取CSPB-30多糖样品复溶于蒸馏水,离心(10 000 r/min,10 min)后取上清液过0.45 μm水系滤膜即可上柱纯化。离子层析:柱型XK 26 mm×100 cm,填料DEAE Sepharose Fast Flow,先用蒸馏水洗脱500 mL 后,再用0~2 mol/L NaCl溶液进行线性洗脱,收集18 mL/管,采用苯酚硫酸法跟踪测定每5管的糖含量,绘制洗脱曲线,分别收集不同洗脱峰,浓缩后于4 ℃下透析48 h,透析液再次浓缩后冻干。凝胶层析:柱型XK16 mm×100 cm,填料Sephacryl S300,苯酚硫酸法测定糖含量,收集单一洗脱峰,浓缩后透析72 h,透析液再次浓缩后冻干,得到玉米须纯化多糖CSPSS。
1.3.3 总糖和蛋白质含量的测定
参考DUBOIS等[9]的方法,以葡萄糖为标准品,通过苯酚-硫酸法测定总糖含量。通过BCA试剂盒测定蛋白质含量。
1.3.4 分子质量测定
参考文献[10]方法,以不同分子质量葡聚糖为标准品(T5、T11、T20、T50、T500),采用高效液相色谱法测定CSPSS的分子质量,并检验CSPSS是否为均一多糖。
色谱条件:UltrahydrogelTM Linear(7.8 mm×300 mm)水相凝胶色谱柱+保护柱(6 mm×40 mm),柱温为(35±0.1) ℃,进样量20 μL,流速为0.5 mL/min,流动相为0.02 mol/L磷酸盐缓冲液(pH=7.4)。
1.3.5 单糖组成分析
参考宫春宇等[11]文献方法并稍作调整,采用PMP柱前衍生高效液相色谱法分析CSPSS的单糖组成及摩尔比,单糖标准品分别为10 mmol/L的木糖(xylose,Xyl)、鼠李糖(rhamnose,Rha)、甘露糖(mannose,Man)、阿拉伯糖(arabinose,Ara)、葡萄糖(glucose,Glc)、半乳糖(galactose,Gal)、葡萄糖醛酸(glucuronicacid,GlcA)、半乳糖醛酸(galacturonicacid,GalA)。
1.3.6 紫外可见光谱
称取CSPSS 4 mg溶解于4 mL蒸馏水,5 000 r/min离心10 min后取上清液进行紫外可见光谱分析,在200~400 nm进行全波段扫描。
1.3.7 红外光谱分析
采用KBr压片法测定玉米须多糖的傅里叶红外吸收光谱。精密称取CSPSS 2 mg与200 mg的KBr固体粉末混合均匀,使用研钵对其研磨后压制成片进行红外光谱扫描,扫描范围为4 000~400 cm-1,观察图谱出峰情况。
1.3.8 核磁共振波谱
取CSPSS 30 mg充分溶解于0.5 mL的重水中并冷冻干燥,重复过程3次。将CSPSS再次溶解于重水中,10 000 r/min离心5 min,取上清液过0.45 μm滤膜,滤液转移到核磁管中,在室温下置于核磁共振仪(600 MHz),化学位移以ppm表示,记录CSPSS的1H NMR谱和13C NMR谱。
1.3.9 X射线衍射分析
参考REN等[12]研究方法,称取CSPSS 40 mg并研磨成细粉,进行X射线衍射分析,设置检测条件:Cu-Kα辐射,衍射角度5°~80°,扫描步长0.02°,管流180 mA,管压40 kV。
1.3.10 热稳定性分析
根据CHEN等[13]分析方法,使用热重分析仪测定CSPSS的热稳定性。精密称取4 mg的CSPSS样品置于铝坩埚中,并以空铝坩埚为对照进行测定,设置氮气流速为50 mL/min,升温速率为10 ℃/min,检测温度为30~800 ℃。
1.3.11 刚果红实验
根据ZHANG等[14]研究方法稍作改动,通过刚果红实验判断CSPSS样品是否为三螺旋结构。配制2 mL质量浓度为2 mg/mL的CSPSS溶液,再加入2 mL浓度为80 μmol/L刚果红混合均匀,最后加入1 mol/L的NaOH溶液使得混合液中NaOH最终浓度分别为0、0.1、0.2、0.3、0.4、0.5 mol/L,以蒸馏水代替多糖作为对照组,在200~800 nm进行紫外光谱扫描,以NaOH浓度为横坐标,最大吸收波长(λmax)为纵坐标绘制曲线。
1.3.12 粒径、电位测定
使用去离子水准确配制4 mL质量浓度为1 mg/mL的CSPSS均一多糖样品溶液,10 000 r/min离心5 min后过0.45 μm水系滤膜,测定CSPSS的粒径分布和Zeta电位[15]。
1.3.13 扫描电子显微镜
取适量CSPSS,通过扫描电子显微镜观察CSPSS在×500、×1 000、×5 000、×10 000倍数下的表面形态。
1.3.14 CSPSS体外降血糖活性
1.3.14.1 α-葡萄糖苷酶抑制率
参照YANG等[16]报道并稍作改进。分别取不同浓度CSPSS溶液20 μL于96孔板,加入40 μL的α-葡萄糖苷酶溶液(1 U/mL)混合,37 ℃培养箱中孵育10 min,然后加入40 μL的PNPG溶液(10 mmol/L)再次孵育30 min,最后加入1 mol/L碳酸钠溶液100 μL 于405 nm处测定吸光度值,并设置空白组和阿卡波糖阳性对照组。根据以下公式计算CSPSS对α-葡萄糖苷酶的抑制率,以CSPSS浓度为横坐标,抑制率为纵坐标绘图,CSPSS半数抑制浓度(IC50)的计算如公式(1)所示:
抑制率![]()
(1)
式中:A1,CSPSS、α-葡萄糖苷酶和PNPG反应体系的吸光度值;A0,缓冲液代替α-葡萄糖苷酶溶液的吸光度值;A,缓冲液代替CSPSS的吸光度值。
1.3.14.2 α-淀粉酶酶抑制率
参考UNUOFIN等[17]文献方法并稍作修改。分别取不同浓度CSPSS溶液0.5 mL于试管,加入α-淀粉酶溶液0.5 mL后,37 ℃水浴反应15 min,然后加入质量浓度为10 g/L的可溶性淀粉溶液1 mL,37 ℃水浴继续反应15 min,再加入二硝基水杨酸试剂1 mL,100 ℃水浴反应5 min,冷却至室温,最后加入10 mL蒸馏水稀释反应体系,540 nm处测定吸光度值,并设置空白组、背景组和阿卡波糖阳性对照组。CSPSS对α-淀粉酶的抑制率的计算如公式(2)所示,并计算IC50值:
抑制率![]()
(2)
式中:A1,CSPSS、α-淀粉酶和淀粉反应体系的吸光度值;A0,缓冲液代替α-淀粉酶溶液的吸光度值;A,缓冲液代替CSPSS的吸光度值。
1.3.15 CSPSS体内降血糖活性
采用斑马鱼模式生物评价玉米须多糖体内降血糖活性。研究所涉及动物实验由齐齐哈尔大学科技伦理委员会审议通过,伦理编号:20231204-SP-001,斑马鱼由杭州环特生物科技股份有限公司提供,实验动物使用许可证号为:SYXK(浙)2022-0003。成年斑马鱼饲养条件:水温为(28±0.5) ℃,水质pH值为6.5~7.5,电导率为450~550 μs,自动计时器控制昼夜周期为14 h/10 h(光照/黑暗)交替循环。按照雌雄1∶2比例随机捞选成熟斑马鱼,使其自然交配产卵。将健康胚胎保存在培养皿中,置于28 ℃恒温培养箱,培养至受精后5 d(dpf),每隔24 h更换一次培养水并及时吸出死卵和卵膜。
随机选取540尾体态健康的5 dpf斑马鱼幼鱼放置于六孔板中,每孔均处理20尾。通过30 mg/mL葡萄糖和1 mg/mL蛋黄粉联合浸泡48 h建立斑马鱼Ⅱ型糖尿病模型,在模型组基础上分别水溶给予50、250和500 μg/mL的CSPSS,阳性对照组给予500 μg/mL的降血糖药物阿卡波糖,每孔10 mL药液,同时设置对照组和模型组,所有实验组均设置3个重复孔。浸泡48 h后,每组随机选取10尾斑马鱼并使用研磨仪将斑马鱼研磨均匀,加入5 μL PBS,4 ℃ 下7 000 r/min离心5 min,吸取2 μL上清液,使用血糖仪检测各组斑马鱼的血糖水平。
2 结果与分析
2.1 玉米须粗多糖的分离纯化
通过离子层析对玉米须多糖CSPB-30进行分离纯化,如图1所示,明显看到2个分离的洗脱峰,其中0~20管的小峰对应为水相洗脱组分,30~50管的大峰对应为氯化钠线性洗脱的组分。继续对氯化钠洗脱组分进行凝胶纯化,观察到对称的单一洗脱峰,收集该部分洗脱液制得玉米须纯化多糖(CSPSS)。
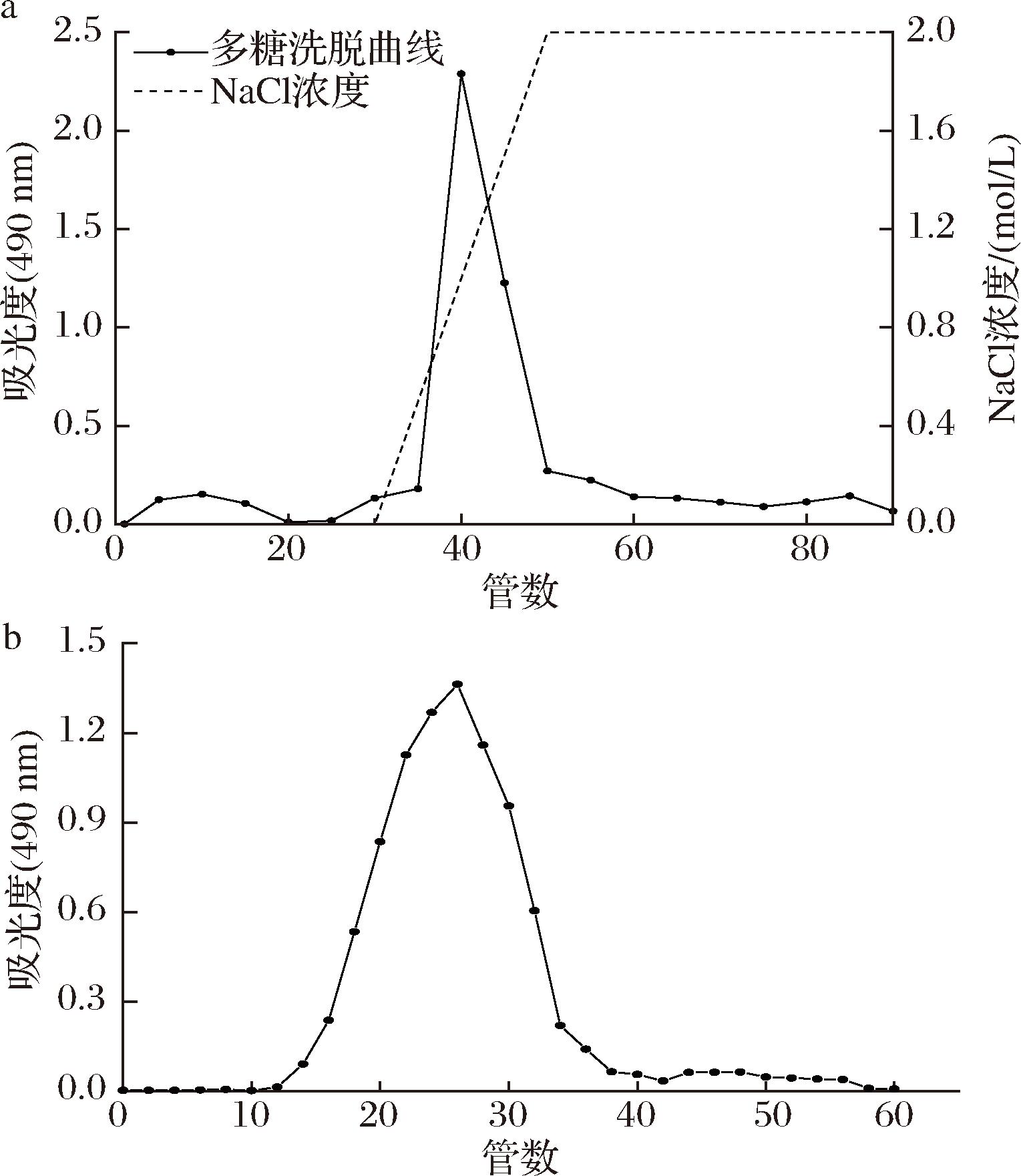
a-离子层析洗脱曲线;b-凝胶层析洗脱曲线
图1 离子层析和凝胶层析洗脱曲线
Fig.1 Ion chromatography andgel chromatography
2.2 多糖和蛋白质含量的测定
成分测定显示,CSPSS含量达到(91.60±1.06)%,蛋白质含量仅为(2.48±0.08)%,多糖含量非常高,表明CSPSS的纯度很高。
2.3 结构表征
2.3.1 纯度鉴定及分子质量测定
CSPSS高效液相色谱图(图2-a)显示为对称的单一色谱峰,表明CSPSS为均一多糖。对高效液相色谱葡聚糖标准品出峰时间和lg(分子质量)值进行回归分析得到线性回归方程y=-1.099 1x+14.422,R2=0.996 8,再将CSPSS的出峰时间带入方程中,经计算CSPSS的分子质量为(6.88±0.28)×104 Da。
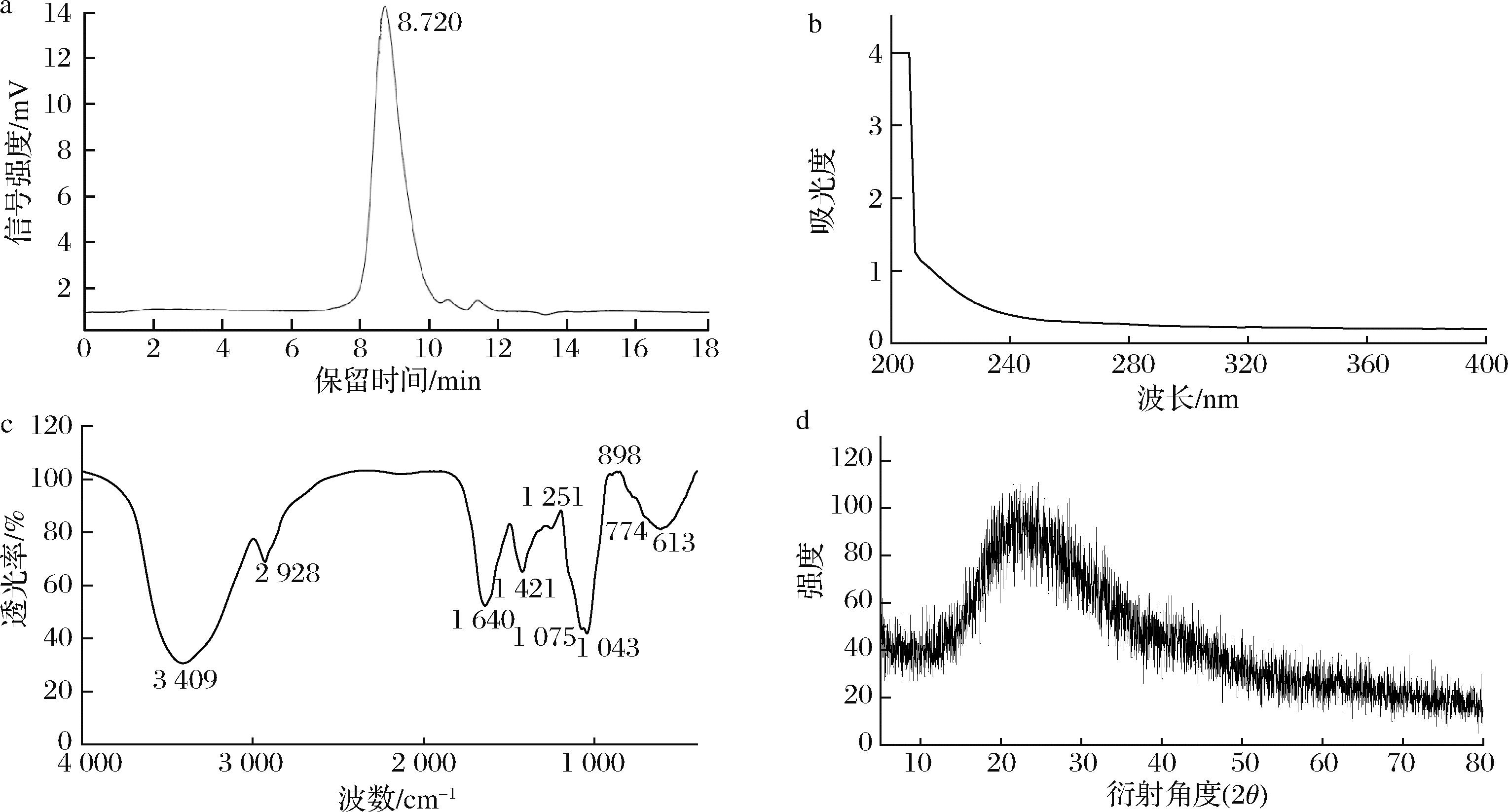
a-高效液相色谱图;b-紫外光谱图;c-红外光谱图;d-射线衍射图谱
图2 CSPSS结构表征
Fig.2 Structural characterization of CSPSS
2.3.2 单糖组成分析
通过对比CSPSS和单糖标准品的出峰时间(表1)和峰面积,确定CSPSS主要由鼠李糖、半乳糖醛酸、半乳糖、木糖组成,摩尔比为0.78∶1.08∶1.00∶2.81,此外,还存在1个未知糖,所占摩尔比为1.10。关于玉米须多糖的单糖组成报道不一,DENG等[18]通过高效液相色谱法测得玉米须多糖由甘露糖、鼠李糖、葡萄糖、半乳糖、阿拉伯糖、木糖、半乳糖醛酸组成,王磊等[19]通过气相色谱法测得玉米须多糖由鼠李糖、阿拉伯糖和甘露糖3种单糖组成,这可能是由于玉米须多糖的提取及分离纯化程度不同造成单糖组成结果的不同。
表1 各单糖高效液相色谱出峰时间 单位:min
Table 1 Peak time of monosaccharidein high-performance liquid chromatography

组别未知糖甘露糖鼠李糖葡萄糖醛酸半乳糖醛酸葡萄糖半乳糖木糖阿拉伯糖标准品—17.04723.20028.82732.78739.46045.84048.30750.173CSPSS13.089—23.785—32.531—44.96948.819—
注:“—”为未检出。
2.3.3 紫外可见光谱
由图2-b可知,CSPSS在260 nm和280 nm并没有峰出现,表明CSPSS几乎不含核酸和蛋白质,这与本研究蛋白质含量测定的结果相符合。
2.3.4 红外光谱
根据红外光谱图(图2-c)分析,3 000~3 750 cm-1存在宽谱带,3 409.25 cm-1处出现强吸收峰是由糖环碳上O—H伸缩振动所引起,2 928.58 cm-1处的吸收峰是由烷基的C—H伸缩振动所引起,这2组峰为多糖类物质的典型基团羟基和烷基。1 640.60 cm-1和1 421.28 cm-1处的吸收峰归属于羧基中的C![]() O不对称伸缩振动和C—O伸缩振动,证明CSPSS中含有糖醛酸;1 251 cm-1处的吸收峰归属于C—O—C的特征吸收峰;1 000~1 077 cm-1吸收峰归属为C—O—H和C—O—C键的伸缩振动,证明CSPSS存在吡喃糖环[20];898.02 cm-1处为β构型糖苷键的吸收峰,774.1 cm-1和613.98 cm-1处为吡喃糖环特征吸收峰[21-22]。综合上述,CSPSS是一种具有β构型和吡喃糖环的酸性多糖。
O不对称伸缩振动和C—O伸缩振动,证明CSPSS中含有糖醛酸;1 251 cm-1处的吸收峰归属于C—O—C的特征吸收峰;1 000~1 077 cm-1吸收峰归属为C—O—H和C—O—C键的伸缩振动,证明CSPSS存在吡喃糖环[20];898.02 cm-1处为β构型糖苷键的吸收峰,774.1 cm-1和613.98 cm-1处为吡喃糖环特征吸收峰[21-22]。综合上述,CSPSS是一种具有β构型和吡喃糖环的酸性多糖。
2.3.5 X射线衍射分析
可通过观察X射线图谱中的衍射峰从而判断CSPSS是否为晶体结构,若衍射峰形状窄为晶体结构,衍射峰宽且弥散则不具有晶体结构。如图2-d所示,在衍射角度10°~40°时出现弥散宽峰,说明CSPSS的结晶度很低,共同存在结晶和非结晶区域,属于无定型结构,该结果与JIA等[23]分析报道的玉米须多糖锌复合物X射线结果相同。
2.3.6 核磁共振波谱
根据1H NMR光谱(图3-a)显示,CSPSS在4.4~5.0 ppm和5.0~5.5 ppm均有吸收峰,说明CSPSS多糖的糖链含有α构型和β构型糖苷键。
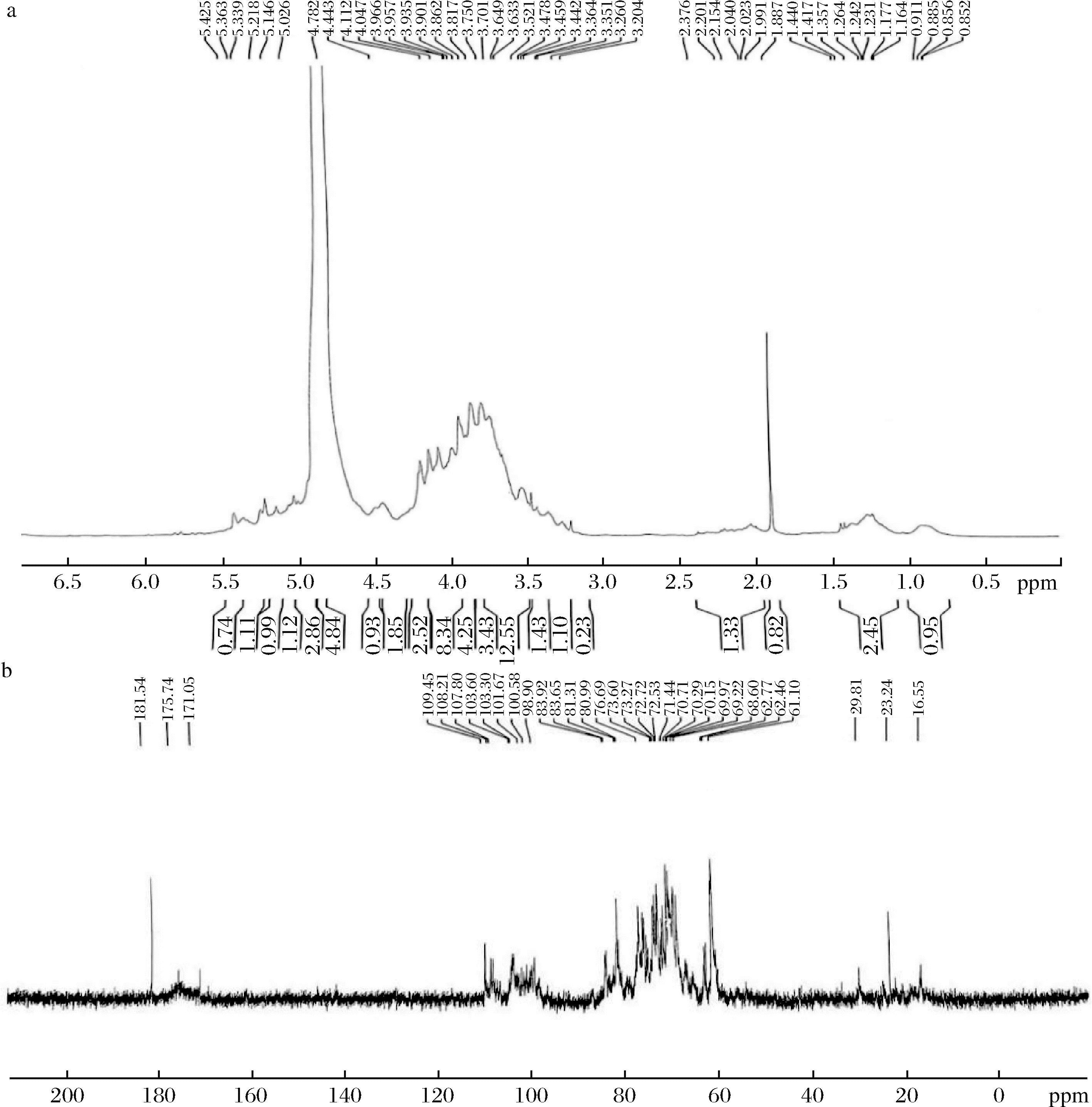
a-1H-NMR;b-13C-NMR
图3 CSPSS的1H-NMR和13C-NMR图谱
Fig.3 1H-NMR and 13C-NMR spectra of CSPSS
根据13C NMR光谱(图3-b)显示,170~180 ppm附近出现信号峰表明CSPSS中存在糖醛酸;异头碳共振所引起的信号峰在90.0~110 ppm,共有8个,表明CSPSS含有八类糖残基;在95~100 ppm和100~105 ppm均存在信号峰,表明CSPSS同时含有α构型和β构型糖苷键,此结果与1H NMR检测结果相同,但先前红外光谱检测时并未检测到α构型糖苷键,这可能是由于其含量较少所导致。16 ppm附近的信号峰为鼠李糖C-6甲基碳的伸缩振动所引起。
2.4 热稳定性分析
采用热重法确定CSPSS在逐渐升温中引起的质量变化从而分析其热稳定性,即热重曲线(thermogravimetric curve,TG),对TG的温度一阶求导以探究CSPSS分解速率和温度之间的关系,即DTG曲线。如图4所示,CSPSS在升温过程中存在3个质量损失阶段。第一阶段约在30~200 ℃,该阶段是由于CSPSS中的结合水流失所造成质量下降[24];第二阶段约在200~350 ℃,该阶段是由于CSPSS多糖自身碳骨架分解所导致质量迅速下降;第三阶在350~800 ℃,CSPSS质量随温度升高缓慢匀速下降,这可能是由于大部分CSPSS多糖经高温灼烧后已碳化,而剩余少量CSPSS多糖的热稳定性较高[25-26]。CSPSS最终剩余质量仅为2.58%,此值可视同灰分,侧面表明CSPSS纯度较高,几乎不存在杂质。根据DTG曲线发现,温度约170 ℃时CSPSS分解速率逐渐增大,升温至298.72 ℃时分解速率达到最大,提示CSPSS的加热温度不宜超过170 ℃。
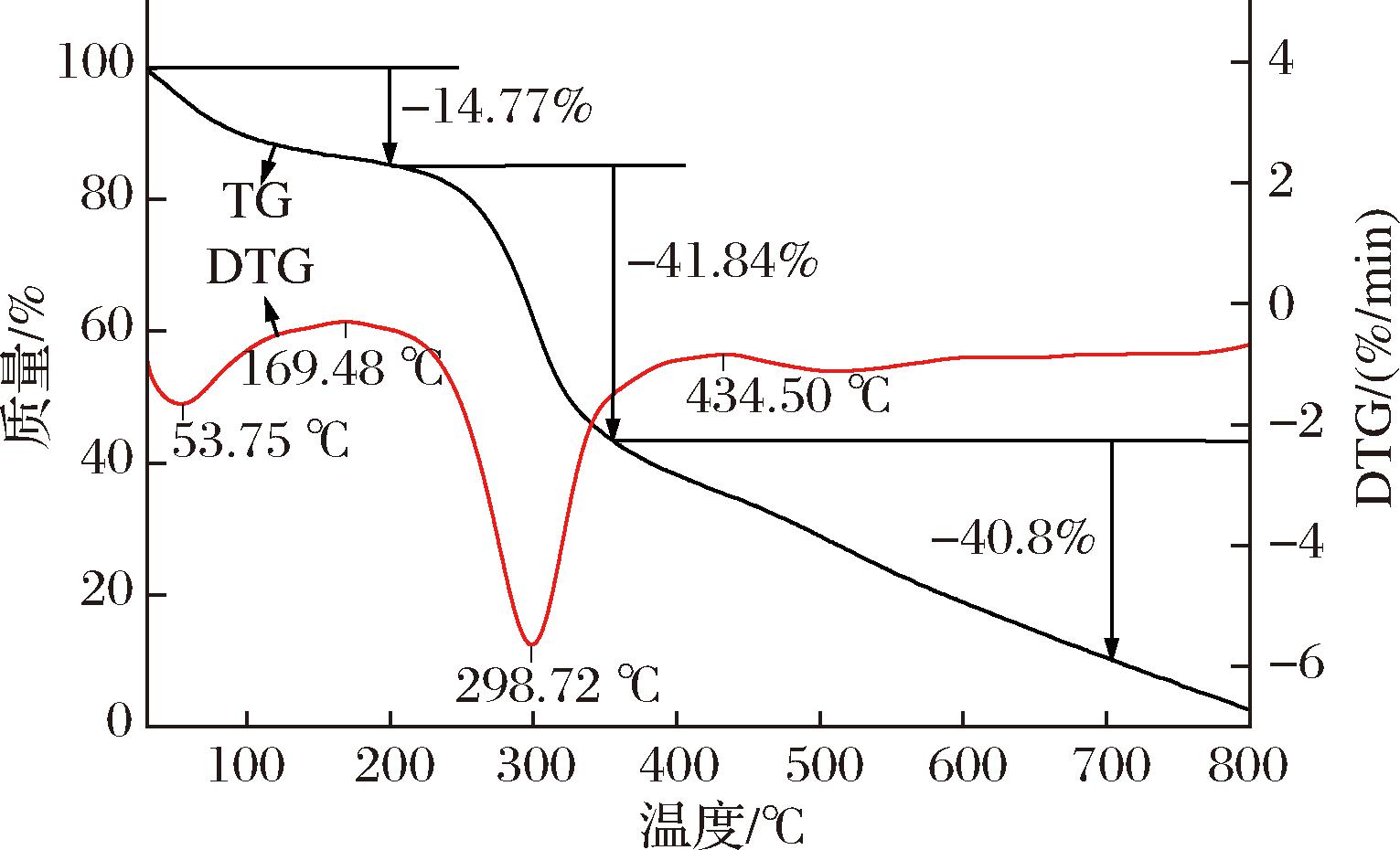
图4 CSPSS的TG-DTG曲线
Fig.4 TG-DTG curve of CSPSS
2.5 刚果红实验
刚果红试剂可以与存在三螺旋结构的多糖在弱碱性溶液中发生络合反应,络合物与刚果红相比产生红移现象,即碱性浓度逐渐升高络合物的最大吸收波长随之增大,但是碱性浓度过高时会破坏络合物结构导致最大波长下降。因此可通过刚果红实验判断CSPSS的糖链构象是否为三螺旋结构。如图5所示,刚果红与CSPSS络合物在不同浓度氢氧化钠溶液下没有发生红移,最大波长没有呈现先升高后下降,因此表明CSPSS不具有三螺旋结构。
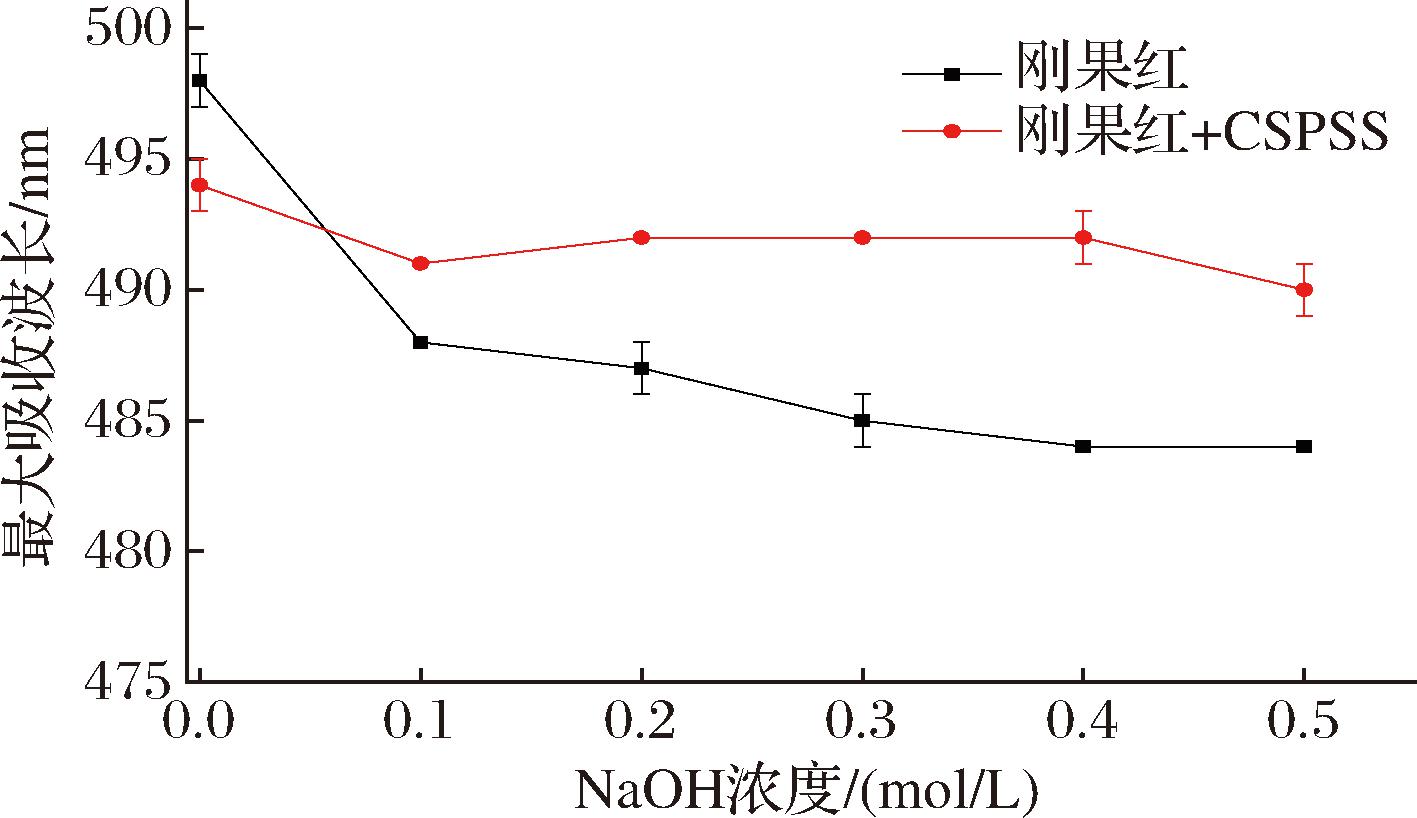
图5 刚果红与CSPSS的复合物在不同氢氧化钠浓度下的最大吸收波长
Fig.5 Maximum absorption wavelength of the complex of Congo red and CSPSS at different sodium hydroxide concentrations
2.6 粒径、电位测定
多糖的粒径大小及其分布与其物理性质、空间构象和生物活性等均存在部分关联,一般来说,多糖的粒径越小越易于被生物体吸收从而更好地发挥生物活性。Zeta-电位的绝对值在一定程度上可以反映多糖的稳定性,通常多糖的Zeta电位绝对值越大,分子间斥力越大越不易发生聚集从而体系更加稳定,Zeta电位为0~±5 mV时胶体易快速凝聚,±10~±30 mV时表示胶体开始变得不稳定,且通过大量文献比较后发现,多糖溶液的电位值一般在±10~±30 mV。
CSPSS的粒径大小为(173.07±11.67) nm,相比于纯化后的藜麦多糖[27]、霸王花多糖[28]的468、197 nm,粒径更小,同时多分散系数为0.24±0.01,表明CSPSS的粒径较小且分布较为均匀。CSPSS的Zeta-电位为(-23.40±0.56) mV,处于多糖溶液的常规电位值范围,表明CSPSS多糖溶液较为不稳定,但其点位绝对值较大,明显高于六妹羊肚菌均一多糖的-3.25 mV[29]。此外,Zeta电位为负值,说明CSPSS为阴离子多糖。有研究表明多糖中存在的负电荷主要由糖醛酸所产生[30],本研究单糖组成实验证明CSPSS含有半乳糖醛酸,与此实验结果互相印证。
2.7 扫描电子显微镜
图6为CSPSS在不同放大倍数下的扫描电镜图像(×500、×1 000、×5 000和×10 000)。在×500和×1 000倍下,CSPSS多糖呈现较为光洁的片状结构,表面存在部分大小不一的孔洞;在×5 000和×10 000倍下,明显看出CSPSS表面通过相互堆积产生交联,并形成无序排列的凹洞,凹洞的形成可能是由于CSPSS片状结构破碎后的碎裂面经高倍放大后所呈现,也可能由于制备CSPSS时经冷冻干燥导致CSPSS失去结合水所造成。本研究制得的CSPSS与红枣均一多糖和短管兔耳草均一多糖的表态形态较为相似,均为存在不规则孔洞的片状结构[31-32]。

a-×500倍下扫描电子显微镜图;b-×1 000倍下扫描电子显微镜图;c-×5 000倍下扫描电子显微镜图;d-× 5000倍下扫描电子显微镜图
图6 CSPSS的扫描电子显微镜图
Fig.6 Scanning electron micrograph of CSPSS
2.8 CSPSS体外降血糖活性
图7-a显示了不同浓度的CSPSS对α-葡萄糖苷酶活性的抑制能力,由图7-a可以看出随着CSPSS浓度增加,其对α-葡萄糖苷酶抑制能力逐渐增强,具有明显的量效关系。质量浓度为1~4 mg/mL时抑制率上升较快随后趋于稳定,质量浓度为12 mg/mL时抑制率达到最大,为74.65%,经计算CSPSS对α-葡萄糖苷酶的半抑制质量浓度IC50值为(3.56±0.27) mg/mL。研究显示,黄精多糖和滇黄精多糖对α-葡萄糖苷酶的IC50分别为4.57、2.63 mg/mL[25];知母多糖AABP-1B和AABP-2B则分别为0.78、0.94 mg/mL[33];六堡茶多糖TPS-5为4.923 mg/mL[34]。
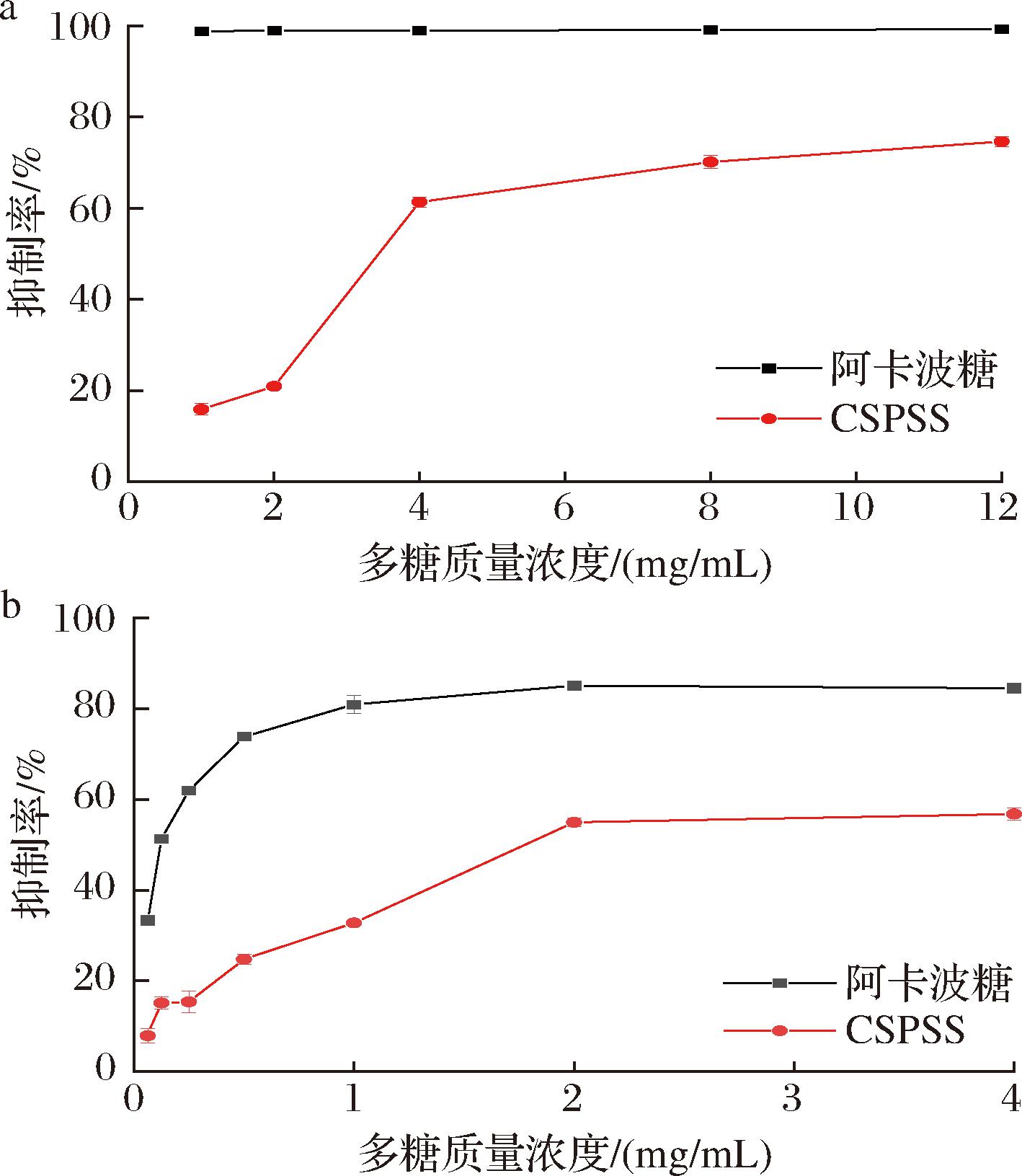
a-α-葡萄糖苷酶;b-α-淀粉酶
图7 CSPSS对α-葡萄糖苷酶和α-淀粉酶抑制活性
Fig.7 α-Glucosidase and α-amylase inhibitory activity of CSPSS
CSPSS对α-淀粉酶抑制活性如图7-b所示,由图7-b可以看出CSPSS和降糖药物阿卡波糖对α-淀粉酶均具有一定的抑制作用并呈现明显剂量依赖性。当CSPSS质量浓度为0.062 5~2 mg/mL时,抑制能力上升较快后逐渐平缓,最大抑制率为56.77%,经计算阿卡波糖的IC50仅为(0.13±0.89) mg/mL,CSPSS的IC50为(2.29±0.36) mg/mL。而黄精多糖、滇黄精多糖对α-淀粉酶没有抑制作用[25];知母多糖AABP-1B和AABP-2B对α-淀粉酶的IC50分别为0.63和1.83 mg/mL[33];六堡茶多糖TPS-5为5.078 mg/mL[34]。
综合CSPSS体外对α-葡萄糖苷酶和α-淀粉酶抑制能力的实验结果,表明CSPSS具有一定的体外降血糖作用,其对2种酶的IC50均处于中等偏下水平,可见其体外降血糖效果在多糖中大概处于中等偏上。
2.9 CSPSS体内降血糖活性
如图8所示,浸泡96 h,质量浓度低于1 mg/mL时,死亡率最大3.33%;质量浓度为1.5 mg/mL时,死亡率最大26.67%,可见实验剂量对斑马鱼无毒副作用。由图9可知,模型组斑马鱼的血糖值显著高于对照组,是对照组的4.74倍,阿卡波糖阳性对照组斑马鱼的血糖值相比模型组降低56.46%,表明该建立Ⅱ型糖尿病斑马鱼模型的方法切实可行,可以用于评价药物的降血糖效果。相比模型组,CSPSS质量浓度为50 μg/mL时血糖值与之无显著性差异;质量浓度为250 μg/mL时降糖率为19.96%;质量浓度为500 μg/mL时,血糖值下降至4.3 mmol/L,降糖率为33.63%。结果表明,CSPSS在250、500 μg/mL浓度时可显著降低Ⅱ型糖尿病斑马鱼的血糖值。劳乔聪[35]采用1 mmol/L四氧嘧啶与4%蔗糖联用建立糖尿病斑马鱼模型,确定模型组血糖值(3.88 mmol/L)是对照组(1.08 mmol/L)的3.59倍,阳性药物二甲双胍组和实验材料青钱柳组的斑马鱼血糖值与模型组相比分别降低37.86%和20.17%,可以看出不同建模方法对斑马鱼血糖的影响效果不同,本研究采用的建模方法相比血糖升高率更大。斑马鱼被应用于降血糖研究才刚刚起步,相关报道不多。但有报道显示,与高血糖模型组斑马鱼相比,随着多花黄精多糖质量浓度(60、120、240 μg/mL)逐渐升高,斑马鱼组织糖含量有降低的趋势,且呈剂量相关性,但降糖率很低[36];500 μg/mL的毛木耳多糖可以使斑马鱼体内葡萄糖水平降低31.9%[37]。可见CSPSS与毛木耳多糖体内降糖效果可能相近,优于多花黄精多糖。由于斑马鱼模型具有实验时长短、用药剂量较少等诸多优势,相信未来会有更多相关研究报道。
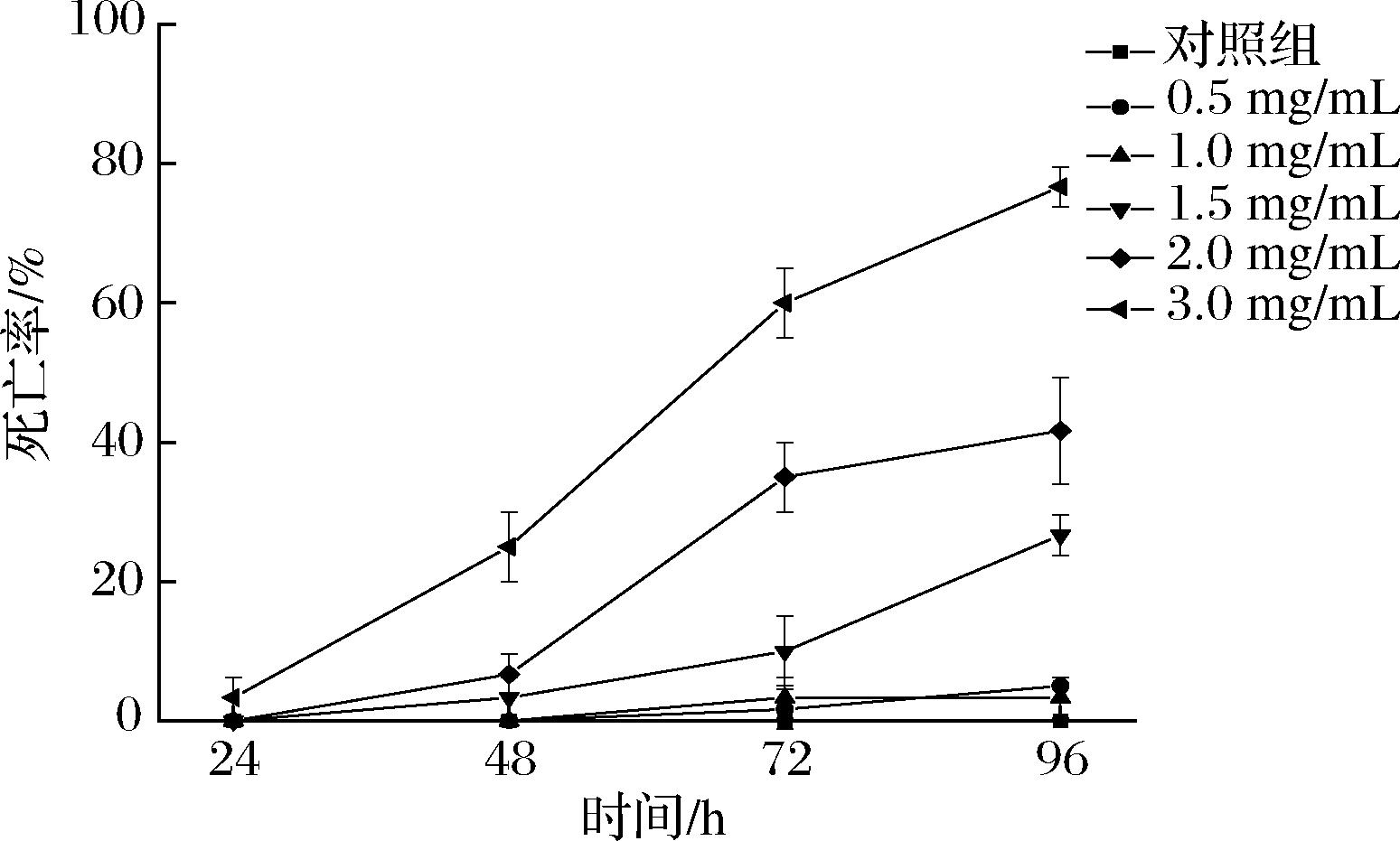
图8 斑马鱼对玉米须多糖最大耐受剂量
Fig.8 Maximum tolerance dose of zebrafish to corn silk polysaccharide
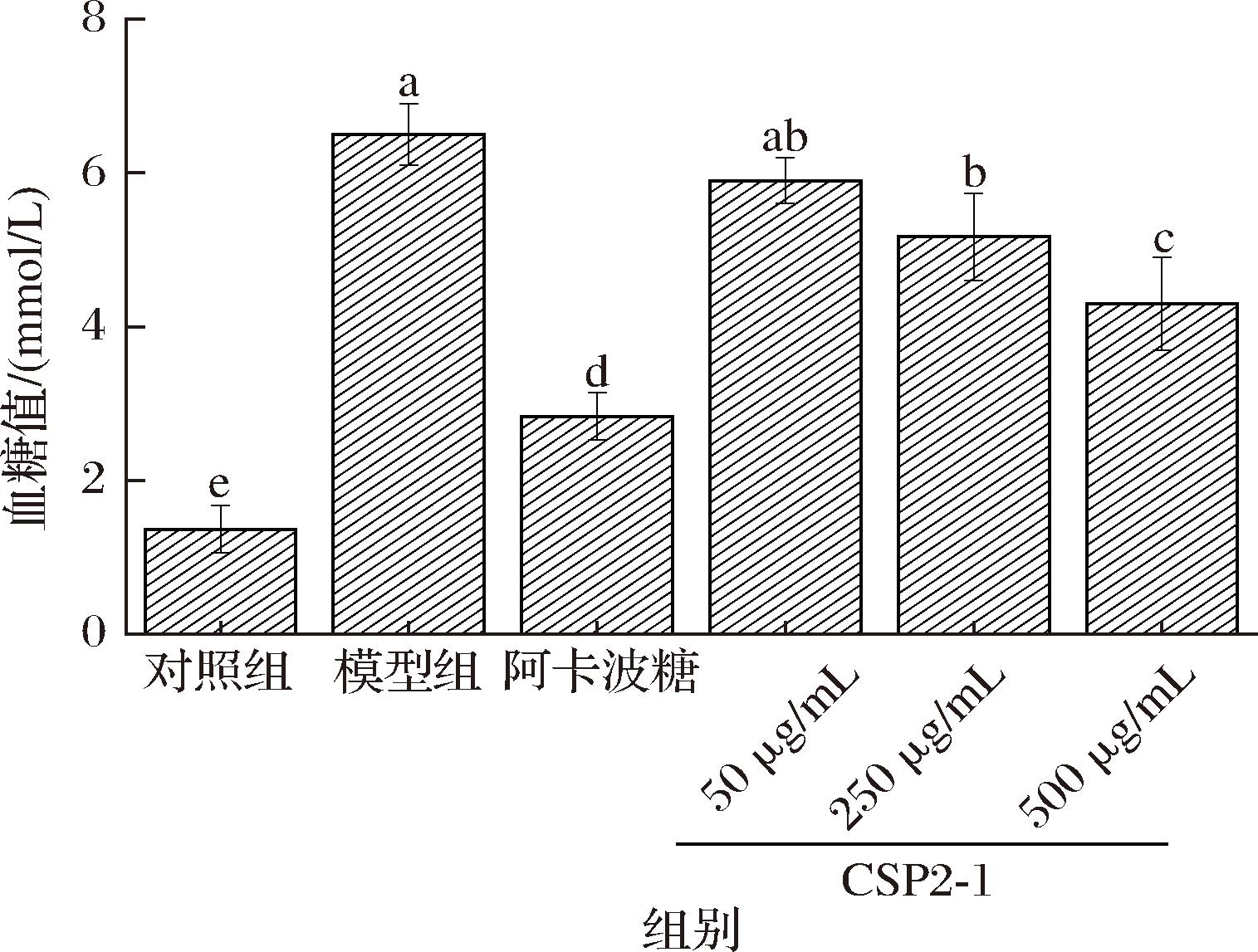
图9 CSPSS对Ⅱ型糖尿病斑马鱼血糖值的影响
Fig.9 Effect of CSPSS on blood glucose of zebrafish with type Ⅱ diabetes
注:不同小写字母表示差异显著(P<0.05)(下同)。
3 结论
本研究采用热水浸提法、超滤、乙醇沉淀分离制得玉米须多糖,先后经DEAE Sepharose Fast Flow离子层析和Sephacryl S300凝胶层析分离纯化成功得到一个均一多糖组分CSPSS,并对该组分的结构特征和降血糖活性进行研究。结果表明,CSPSS总糖含量为(91.60±1.06)%,蛋白质含量为(2.48±0.08)%,分子质量为(6.88±0.28)×104 Da;主要由鼠李糖、半乳糖醛酸、半乳糖、木糖组成,其摩尔比为0.78∶1.08∶1.00∶2.81,除此之外还存在未知单糖,所占摩尔比为1.10;红外光谱、核磁共振波谱显示,CSPSS为酸性多糖,糖环类型为吡喃糖环,存在α构型和β构型糖苷键以及羰基、羟基等官能团;X射线衍射、热稳定性和刚果红实验结果提示,CSPSS结晶度很低属于无定型结构,不具有三螺旋构型,热稳定性较好且加热温度不宜超过170 ℃;扫描电镜观察发现CSPSS为片状结构,表面较为光滑,分子间作用力强产生交联现象;体外降血糖实验提示,CSPSS对α-葡萄糖苷酶和α-淀粉酶均具有抑制作用,且抑制率与CSPSS浓度呈正相关,半数抑制质量浓度分别为(3.56±0.27) mg/mL和(2.29±0.36) mg/mL,表明CSPSS具有一定体外降血糖能力;体内降血糖活性结果表明,CSPSS在250、500 μg/mL质量浓度时可显著降低Ⅱ型糖尿病斑马鱼的血糖值,具有较好的体内降血糖活性。综上所述,本研究通过分离纯化得到玉米须均一多糖并探究其结构和体内外降血糖活性,证明了玉米须多糖的潜在药理价值,为深入研究其降糖活性与结构间的构效关系提供数据支持,同时为其进一步在功能性食品和药用领域方面的开发应用提供理论依据。
[1] 宋有洪,吴菲,吴玉银,等.玉米花丝药用价值研究进展[J].中国农业大学学报,2020,25(2):12-23.SONG Y H,WU F,WU Y Y,et al.Progress on the medicinal values of the maize silk[J].Journal of China Agricultural University,2020,25(2):12-23.
[2] 张晓玉,潘宇翔,王佳,等.玉米须中正丁醇萃取物的活性成分分析及其降血糖作用[J].食品研究与开发,2022,43(14):52-61.ZHANG X Y,PAN Y X,WANG J,et al.Active components analysis and hypoglycemic potential of N-butanol fraction from corn silk[J].Food Research and Development,2022,43(14):52-61.
[3] 李敏,马晓娟,史大卓,等.玉米须防治心血管疾病的现代药理研究进展[J].中医药学报,2023,51(8):98-103.LI M,MA X J,SHI D Z,et al.Progress in modern pharmacological research on prevention and treatment of cardiovascular diseases by corn stigma[J].Acta Chinese Medicine and Pharmacology,2023,51(8):98-103.
[4] 段晋娇,黄琼.玉米须苹果复合保健饮料配方的研制[J].粮食与食品工业,2022,29(6):20-23.DUAN J J,HUANG Q.Study on the formula of corn silk and apple compound health drink[J].Cereal &Food Industry,2022,29(6):20-23.
[5] 刘霞,马泽刚,马林.玉米须绞股蓝复合饮料的制备工艺及生物活性研究[J].湖北农业科学,2022,61(14):131-135.LIU X,MA Z G,MA L.Study on processing technology and the biological activity of the Stigma maydis-Gynostemma pentaphyllum(Thunb.)Makino compound beverage[J].Hubei Agricultural Sciences,2022,61(14):131-135.
[6] 张政.金线莲水溶性多糖的结构及其免疫活性研究[D].南昌:南昌大学,2021.ZHANG Z.Study on the structure and immune activity of water soluble polysaccharide from Anoectochilus roxburghii[D].Nanchang:Nanchang University,2021.
[7] 闫书博,冯聪慧,张原宾,等.玉米须功能性成分及药理价值研究进展[J].食品工程,2023(3):7-9;21.YAN S B,FENG C H,ZHANG Y B,et al.Research progress on functional components and pharmacological value of corn whisker[J].Food Engineering,2023(3):7-9;21.
[8] 班歆甜,柴军红,姜浩,等.玉米须多糖的化学结构及药理活性研究进展[J].中医药学报,2022,50(4):96-102.BAN X T,CHAI J H,JIANG H,et al.Research progress on chemical structure and pharmacological activity of stigma maydis polysaccharides[J].Acta Chinese Medicine and Pharmacology,2022,50(4):96-102.
[9] DUBOIS M,GILLES K A,HAMILTON J K,et al.Colorimetric method for determination of sugars and related substances[J].Analytical Chemistry,1956,28(3):350-356.
[10] LI C,LI X S,YOU L J,et al.Fractionation,preliminary structural characterization and bioactivities of polysaccharides from Sargassum pallidum[J].Carbohydrate Polymers,2017,155:261-270.
[11] 宫春宇,徐硕,徐先梅,等.超滤分离制备玉米须粗多糖及其促益生菌增殖活性研究[J].食品与发酵工业,2021,47(17):166-171.GONG C Y,XU S,XU X M,et al.Structure and components of crude polysaccharide separated by ultrafiltration from Stigma maydis and its activity for promoting probiotics proliferation[J].Food and Fermentation Industries,2021,47(17):166-171.
[12] REN Y P,LIU S X.Effects of separation and purification on structural characteristics of polysaccharide from quinoa (Chenopodium quinoa Willd)[J].Biochemical and Biophysical Research Communications,2020,522(2):286-291.
[13] CHEN G J,CHEN K W,ZHANG R F,et al.Polysaccharides from bamboo shoots processing by-products:New insight into extraction and characterization[J].Food Chemistry,2018,245:1113-1123.
[14] ZHANG J X,WEN C T,GU J Y,et al.Effects of subcritical water extraction microenvironment on the structure and biological activities of polysaccharides from Lentinus edodes[J].International Journal of Biological Macromolecules,2019,123:1002-1011.
[15] ZHAO R X,QI J R,LIU Q R,et al.Fractionation and characterization of soluble soybean polysaccharide esterified of octenyl succinic anhydride and its effect as a stabilizer in acidified milk drinks[J].Food Hydrocolloids,2018,85:215-221.
[16] YANG B,WU Q J,SONG X,et al.Physicochemical properties and bioactive function of Japanese grape (Hovenia dulcis) pomace insoluble dietary fibre modified by ball milling and complex enzyme treatment[J].International Journal of Food Science &Technology,2019,54(7):2363-2373.
[17] UNUOFIN J O,OTUNOLA G A,AFOLAYAN A J.Inhibition of key enzymes linked to obesity and cytotoxic activities of whole plant extracts of Vernonia mesplilfolia less[J].Processes,2019,7(11):841.
[18] DENG W W,YANG X,ZHU Y,et al.Structural characterization and hypolipidemic activities of purified stigma maydis polysaccharides[J].Food Science &Nutrition,2019,7(8):2674-2683.
[19] 王磊,刘秀凤,邱芳萍,等.微波辅助提取玉米须多糖及其组成的研究[J].食品与生物技术学报,2009,28(1):72-75.WANG L,LIU X F,QIU F P,et al.Extraction of corn-silk polysaccharides by microwave-assisted technology[J].Journal of Food Science and Biotechnology,2009,28(1):72-75.
[20] JI X L,LIU F,PENG Q,et al.Purification,structural characterization,and hypolipidemic effects of a neutral polysaccharide from Ziziphus Jujuba cv.Muzao[J].Food Chemistry,2018,245:1124-1130.
[21] GENG L H,HU W C,LIU Y J,et al.A heteropolysaccharide from Saccharina japonica with immunomodulatory effect on RAW 264.7 cells[J].Carbohydrate Polymers,2018,201:557-565.
[22] WANG Y G,WANG F,MA X Q,et al.Extraction,purification,characterization and antioxidant activity of polysaccharides from Piteguo fruit[J].Industrial Crops and Products,2015,77:467-475.
[23] JIA Y N,LI N N,WANG Q R,et al.Effect of Fe (Ⅲ),Zn (Ⅱ),and Cr (Ⅲ) complexation on the physicochemical properties and bioactivities of corn silk polysaccharide[J].International Journal of Biological Macromolecules,2021,189:847-856.
[24] XIAO Y H,LIU S C,SHEN M Y,et al.Physicochemical,rheological and thermal properties of Mesona chinensis polysaccharides obtained by sodium carbonate assisted and cellulase assisted extraction[J].International Journal of Biological Macromolecules,2019,126:30-36.
[25] 王艺.黄精、滇黄精多糖的结构表征与降血糖活性分析[D].陕西:陕西师范大学,2019.WANG Y.Structural characterization and hypoglycemic activity analysis of polysaccharides from Polygonatum sibiricumRedand PolygonatumkingianumColl.et Hemsl[D].Shaanxi:Shaanxi Normal University,2019.
[26] 王新,何玲玲,孔玉梅,等.苦丁茶冬青叶多糖KPS IIIa的热分析研究[J].食品科学,2009,30(9):44-46.WANG X,HE L L,KONG Y M,et al.Study on thermal decomposition of polysaccharide fraction KPS Ⅲa purified from leaves of Llex kudingcha C.J.Tseng[J].Food Science,2009,30(9):44-46.
[27] 任益平.藜麦多糖的提取纯化及其性质研究[D].陕西:陕西科技大学,2020.REN Y P.Study on the extraction,purification and properties of quinoa polysaccharide[D].Shaanxi:Shaanxi University of Science and Technology,2020.
[28] 何慕雪,孟凡成,王春明,等.1种水溶性霸王花多糖的分离纯化及结构鉴定[J].食品科学,2017,38(18):106-112.HE M X,MENG F C,WANG C M,et al.Isolation,purification and structural characterization of a water-soluble polysaccharide from the flower of Hylocereus undatus (Haw.) Britton &Rose[J].Food Science,2017,38(18):106-112.
[29] 张祚.六妹羊肚菌多糖(MSP)的分离纯化、结构鉴定及生物活性研究[D].武汉:武汉轻工大学,2022.ZHANG Z.Isolation,purification,structure identification of Morchella sextelata polysaccharide (MSP) and its biological activity analysis[D].Wuhan:Wuhan Light Industry University,2022.
[30] 王瓅.毛竹笋多糖对脂代谢和肠道菌群的调节作用[D].南京:南京财经大学,2021.WANG L.Effects of bamboo shootpolysaccharides on lipidmetabolism and intestinalflora[D].Nanjing:Nanjing University of Finance and Economics,2021.
[31] 赵建成.红枣多糖的分离纯化、结构表征及活性功能研究[D].宁夏:宁夏大学,2022.ZHAO J C.Study on isolation,purification,structure characterization andactive function of Jujube polysaccharide[D].Ningxia:Ningxia University,2022.
[32] 龚瑞雪.短管兔耳草多糖的分离纯化、结构解析和抗肿瘤活性研究[D].重庆:重庆医科大学,2021.GONG R X.Isolation,purification,structural analysisand anti-tumor activity of polysaccharides from Lagotis brevitubamaxim[D].Chongqing:Chongqing Medical University,2021.
[33] 陈君诚.知母多糖的结构鉴定、降血糖机制及其对肠道菌群的影响[D].广州:华南理工大学,2021.CHEN J C.Structural identification and hypoglycemic activity ofpolysaccharides from Anemarrhena asphodeloides Bunge and their effect on gut microflora[D].Guangzhou:South China University of Technology,2021.
[34] WEI L,HUANG L,DU L J,et al.Structural characterization and in vitro antioxidant,hypoglycemic and hypolipemic activities of a natural polysaccharide from Liupao tea[J].Foods,2023,12(11):2226.
[35] 劳乔聪.斑马鱼糖尿病模型的建立及在评价青钱柳功效中的应用研究[D].浙江:浙江农林大学,2018.LAO Q C.Study on validation of Cyclocarya paliurus (Batal.) Iljinskajain reducing glucose level in diabetic zebrafish model[D].Zhejiang:Zhejiang Agriculture and Forestry University,2018.
[36] 龙瑞阳.毛木耳多糖提取、结构及其锌复合物制备与生物活性研究[D].广州:广州大学,2023.LONG R Y.Extraction,structure,preparation and biological activity of polysaccharides from Auricularia auricula and their zinc compounds[D].Guangzhou:Guangzhou University,2023.
[37] 曹语珈,王凯,王子丽,等.多花黄精多糖对斑马鱼2型糖尿病合并骨质疏松症模型的药效学研究[J].中草药,2021,52(21):6545-6551.CAO Y J,WANG K,WANG Z L,et al.Pharmacodynamics study of polysaccharide from Polygonatum cyrtonemaon zebrafish model with type 2 diabetic and osteoporosis[J].Chinese Traditional and Herbal Drugs,2021,52(21):6545-6551.