红枣(Ziziphus jujube Mill.)是鼠李科枣属植物的成熟果实,它最初产于我国,兼具药用与食用价值,在传统中医药中应用已有4 000余年历史[1]。我国红枣主产区集中于新疆、青海、甘肃、宁夏、陕西等地,其中新疆凭借得天独厚的光热资源,已成为全国最大的优质红枣生产基地[2-3]。2023年,新疆红枣种植面积达44.5万hm2,产量达326.66万t,占全国红枣总产量的50%以上[4]。然而,鲜枣采后易褐变腐烂,贮藏与运输成本高昂,严重制约了产业发展。因此,开发红枣深加工技术(如果酒、发酵饮料等),延伸产业链并提升附加值,对推动新疆红枣产业可持续发展,提高红枣的经济效益至关重要[4]。
目前,红枣加工仍以干制为主,深加工产品如果酒、蜜饯、发酵果汁等市场占比有限。其中,红枣果酒因能保留红枣中多酚、黄酮等功能性成分,并富集发酵产生的活性物质(如多糖、有机酸),成为提升产业经济效益的重要方向[5]。然而,红枣果胶含量高达1.5%~2.5%,加工过程中果胶与纤维素、半纤维素形成胶体网络,导致取汁困难、黏度升高、浊度增加,且果胶酯酶催化生成的甲醇易超标(>400 mg/L),影响产品安全性与品质[6]。果胶酶的应用是解决上述问题的核心手段之一。果胶酶一般是由多聚半乳糖醛酸酶(水解组成果胶酸的D-半乳糖醛酸α-1,4-糖苷键)、果胶裂解酶(分解α-1,4糖苷键生成半乳糖醛酸)、果胶酯酶等组成的复合酶系[7],其中,多聚半乳糖醛酸酶主导的果胶降解,分解果胶主链,释放大量还原糖和可溶性物质;果胶酯酶适度脱甲基化果胶,释放部分甲醇,促进半乳糖醛酸生成;果胶裂解酶裂解果胶分支,协同多聚半乳糖醛酸酶释放更多酚酸和黄酮类物质,从而降低果汁黏度、提高出汁率,同时促进多酚、黄酮、花青素等活性物质的溶出[8]。然而,不同来源的果胶酶因酶系组成、最适pH及温度差异,对产品理化性质与功能性成分的影响显著不同。邱晓坤等[9]发现,黑加仑果汁经低酯活性果胶酶处理后,甲醇含量降低23%,同时出汁率提高18%,说明果胶酯酶活性与甲醇生成量呈正相关。DUCASSE等[10]研究表明,特定果胶酶可选择性释放葡萄酒中的结合态酚类物质,使花青素含量提升15%~20%;卫晓涵等[11]对比发现,果胶酶EX-V处理的软枣猕猴桃果汁透光率达91.2%,浊度较对照组降低64%,且贮藏期悬浮稳定性显著改善。上述研究证实,果胶酶的筛选需兼顾“提质”(多酚富集、澄清度提升等)与“降害”(甲醇抑制)的双重目标,且其效果高度依赖原料特性。骏枣作为高果胶、高活性成分的新疆特色品种,其果酒加工中果胶酶的适配性尚未系统研究。因此,对比不同果胶酶对骏枣果酒关键指标(甲醇、多酚、有机酸等)的影响,明确酶解作用与品质的关联机制,是优化工艺、实现产品高值化的必要前提。
本研究以新疆骏枣为原料酿制果酒,选取5种商业果胶酶HC、EX-V、EX、OP、JZ,以非酶处理组(CK)为对照,系统分析其对骏枣果酒理化性质(澄清度、总酸、pH、酒精度、还原糖、有机酸)及功能性成分(甲醇、酚酸类、黄酮类)的影响。通过对比各指标差异,采用主成分分析(principal component analysis,PCA)方法构建评价模型,对骏枣果酒品质进行综合评价,从而选择最适合骏枣果酒加工的果胶酶品种,旨在为高品质骏枣果酒产品的研发及产业化发展提供科学依据。
1 材料与方法
1.1 材料与试剂
新疆骏枣(Zizyphus jujuba),长圆形[(2.36±0.15) cm,(3.69±0.25) cm],单果重(13.24±1.57) g,色泽(a:21.08±1.46;b:15.75±2.30;L:31.98±3.37),硬度(0.86±0.09) kg/cm2,果胶含量0.93%,总糖(103.26±3.15) mg/g,总酸(6.98±0.81) mg/g,新疆于田县丝路新味农副产品合作社;酒庄(JZ)果胶酶(多聚半乳糖醛酸酶7 500 PGNU/g),法国Lamothe-Abiet公司;HC果胶酶(多聚半乳糖醛酸酶62%、果胶酯酶34%、果胶裂解酶4%,体积分数)、EX果胶酶(多聚半乳糖醛酸酶82%、果胶甲酯酶16%、果胶裂解酶2%,体积分数)、EX-V果胶酶(多聚半乳糖醛酸酶80%、果胶甲酯酶18%、果胶裂解酶2%,体积分数),法国Lallemand公司;OP果胶酶(多聚半乳糖醛酸酶4 400 PGNU/g),法国Laffort公司;果酒专用酵母RW,安琪酵母股份有限公司;氢氧化钠,天津市光复科技发展有限公司;3,5-二硝基水杨酸、酚酞,上海化学试剂采购供应站试剂厂;葡萄糖、无水乙醇、硫酸,天津市致远化学有限公司;叔戊醇,上海源叶生物科技有限公司;芦丁、槲皮素,中国食品药品检定研究院;奎尼酸、绿原酸、隐绿原酸、没食子酸、对香豆酸、槲皮苷、山奈酚、儿茶素、香草酸、咖啡酸、阿魏酸、表儿茶素、香草醛、杨梅素、根皮苷、根皮素、白藜芦醇、大豆苷元、甘草素、芹菜素、木犀草素、山奈素、异槲皮苷、牡荆素、丁香酸、远志山酮Ⅲ、毛蕊异黄酮苷,上海纯优生物科技有限公司;4-羟基苯甲酸、柚皮素、橙皮苷,北京百灵威科技有限公司。所有标准品纯度均在98%以上,试剂均为分析纯。甲醇和甲酸(质谱纯),美国西格玛奥德里奇(上海)贸易有限公司。
1.2 仪器与设备
BC/BD-272SCN冰箱,青岛海尔特种电冰柜有限公司;TU-1810紫外分光光度计,北京普析通用仪器有限责任公司;FiveEasy20台式pH计、ME204/02电子天平,梅特勒-托利多仪器(上海)有限公司;Wine Scan葡萄酒全自动分析仪,福斯华(北京)科贸有限公司;2010 plus气相色谱,日本岛津仪器有限责任公司;XevoTQ-S micro超高效液相色谱-串联质谱仪,美国Waters公司;PS410分光色差仪,三恩时科技有限公司;FHM-1硬度计,竹村电机制作所;游标卡尺,温岭市三菱工具有限公司。
1.3 实验方法
1.3.1 工艺流程
骏枣果酒的制作工艺流程如下:
骏枣(干枣)洗净→去核复水→榨汁→酶解→离心→接种酵母发酵→过滤→杀菌→骏枣果酒。
简单流程是,将骏枣按一定比例加水[料液比为1∶3(kg∶L)]浸泡48 h后破碎呈浆状,先进行低温冷冻(-20 ℃)化汁(可溶性固形物24.5%),在枣汁中分别加入不同的果胶酶(0.04 g/kg)于50 ℃酶解48 h,12 000 r/min离心20 min得到骏枣汁。取发酵液体积0.2%的干酵母,加入少量红枣汁中,于37 ℃下活化30 min,将活化好的菌种按体积百分比接种至红枣酶解液中,置于25 ℃振荡培养箱进行动态发酵,发酵周期为12 d,过滤,灭菌得到骏枣果酒。
1.3.2 总酸、pH、酒精度、还原糖、有机酸的测定
总酸采用GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》方法测定;pH采用pH计直接测定;还原糖含量的测定参考方锐琳等[12]的方法;酒精度和有机酸采用葡萄酒全自动分析仪测定。
1.3.3 澄清度和甲醇的测定
澄清度参考CHEN等[13]的方法,以蒸馏水为参比,在680 nm波长处测定红枣果酒的透光率。甲醇含量参照GB 5009.266—2016《食品安全国家标准 食品中甲醇的测定》进行测定。
1.3.4 多酚类物质的测定
样品处理:直接吸取骏枣果酒样,经0.22 μm微孔滤膜过滤后待测。
标准溶液配制:分别准确称取芦丁、槲皮素、奎尼酸、绿原酸、隐绿原酸、没食子酸、对香豆酸、槲皮苷、山奈酚、儿茶素、香草酸、咖啡酸、阿魏酸、表儿茶素、香草醛、杨梅素、根皮苷、根皮素、白藜芦醇、大豆苷元、甘草素、芹菜素、木犀草素、山奈素、槲皮素-3-葡萄糖苷、牡荆素、丁香酸、远志山酮Ⅲ、毛蕊异黄酮苷、4-羟基苯甲酸、柚皮素、橙皮苷10 mg,用甲醇溶解并定容至10 mL的容量瓶中,配制成1 mg/mL的贮备液,分别精密量取各对照品贮备液0.5 mL于25 mL 容量瓶中,加入甲醇定容,制备成质量浓度各为20 μg/mL的混合标准品贮备液,精密量取混合对照品贮备液适量,用甲醇稀释,得系列标准溶液浓度,依次为20、10、5、2.5、1 μg/mL,以0.22 μm有机滤膜滤过后上机。
液相色谱条件:采用ACQUITY UPLC C18色谱柱(2.1 mm×100 mm,1.7 μm),进样量为5 μL,柱温35 ℃,流速0.3 mL/min,流动相A为甲醇,B为0.1%(体积分数)甲酸水溶液,梯度洗脱程序:0~2 min,98% B;2~4 min,98%~60% B;4~6 min,60% B;6~9 min,60%~25% B;9~11 min,25%~0% B;11~13 min,0% B;13~14 min,0~98% B,柱后平衡5 min。
质谱条件:采用XevoTQ-S micro超高效液相色谱-串联质谱仪,在电喷雾离子源(electrospray ionization,ESI)正离子模式下进行,多反应监测模式,离子源温度550 ℃;电喷雾电压:5 500 V;检测模式:MRM;气帘气压力:30 psi;喷雾器压力50 psi;辅助加热器压力:60 psi;碰撞气流速:10 mL/min。
1.4 数据处理
实验重复3次,采用Origin 2019软件绘图,以IBM SPSS Statistics 26.0分析软件对数据进行差异显著性和PCA。
2 结果与分析
2.1 不同果胶酶处理对骏枣果酒发酵过程中总酸的影响
由图1可知,所有骏枣果酒总酸含量随发酵时间延长呈现先下降后趋于平缓的趋势,但果胶酶组在发酵过程中总酸含量显著高于CK组,其主要原因可能是果胶酶通过水解果胶分子中的α-1,4糖苷键,释放游离半乳糖醛酸等酸性组分在后续发酵过程中易被酵母代谢[14]。果胶酶处理可提高底物可及性,加速酵母对糖类的利用,促进酒精发酵并生成酸性副产物(如乙酸),但部分有机酸可能因pH下降形成晶体沉淀,或因与多酚结合形成复合物,从而降低酸度[15]。此外,商业果胶酶制剂常含有少量纤维素酶或半纤维素酶杂质,其协同作用可能进一步分解细胞壁多糖,释放结合态酸类物质,这些物质在发酵中可能被氧化或酯化,间接减少总酸含量[16]。研究表明,JZ和EX组总酸含量始终高于其他果胶酶组,发酵12 d时总酸含量分别为6.8、6.7 g/L,HC组总酸含量最低,发酵结束达到6.3 g/L。
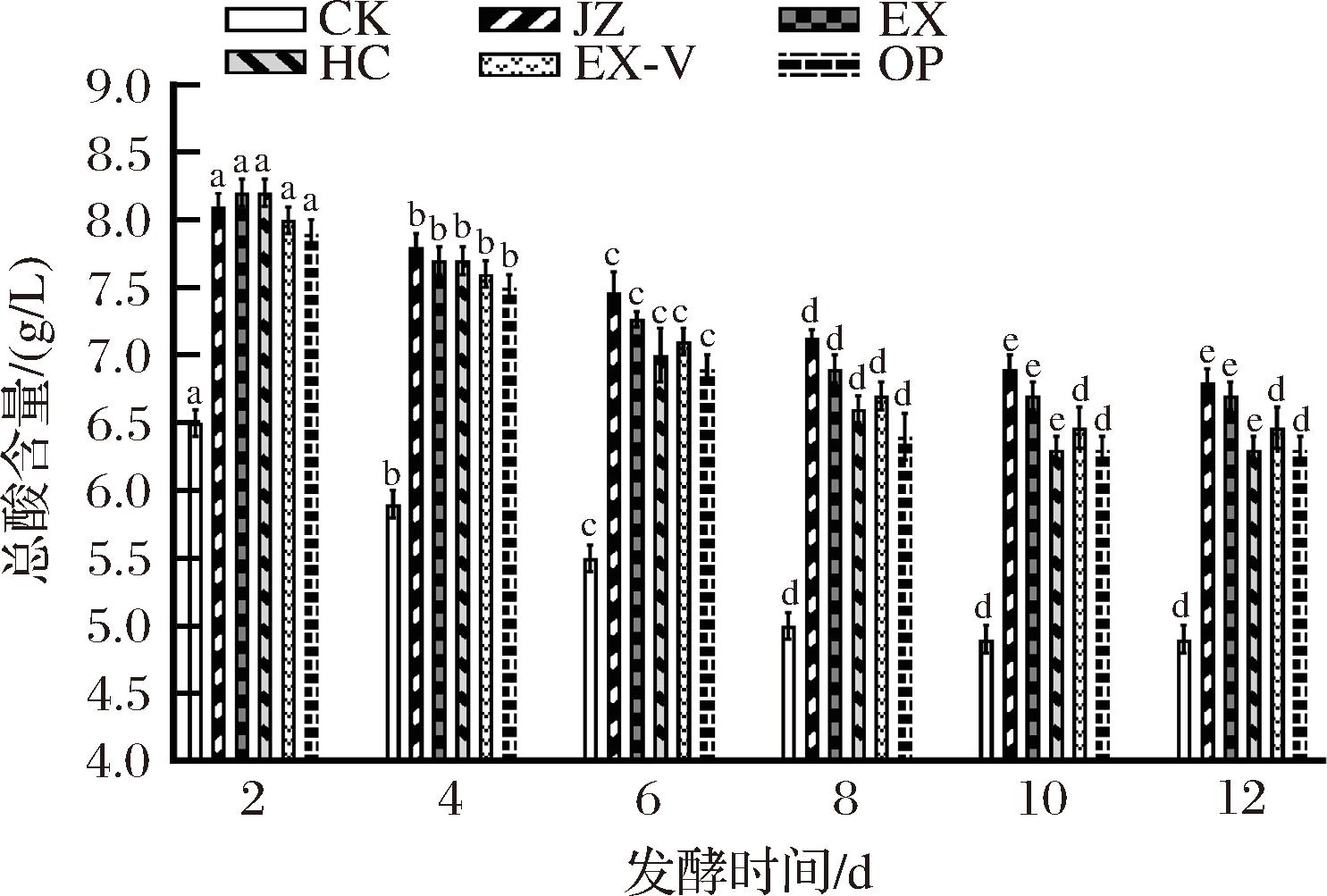
图1 不同果胶酶处理枣酒发酵过程中总酸变化
Fig.1 Changes in total acids during the fermentation of jujube wine with different pectinase treatments
注:相同指标不同字母表示显著差异(P<0.05)(下同)。
2.2 不同果胶酶处理对骏枣果酒发酵过程中pH的影响
由图2可知,骏枣果酒发酵过程中pH呈现先上升后趋于平缓的趋势,果胶酶组的pH均显著低于CK,与总酸含量降低的结果相吻合。主要原因可能是果胶酶通过降解果胶释放的游离半乳糖醛酸被微生物进一步代谢。例如,酵母在酒精发酵过程中可能将部分有机酸转化为中性或弱碱性产物(如乳酸或乙醇),从而降低体系氢离子浓度[14]。研究表明,果胶酶处理可加速苹果酸-乳酸发酵,导致苹果酸含量下降和pH升高[17]。5种果胶酶处理组相比,HC组在发酵结束后的pH值(4.32)高于其他4个果胶酶组,其原因可能是该酶制剂中含有果胶酯酶,能够分解原料中的部分多糖,释放氨基糖类物质,中和部分酸性成分[18]。JZ组pH值在第10天达到最大(4.20),然而,随着发酵的进行,到12 d时,pH值降到4.16,说明该酶促进了一些碱性物质的降解同时又释放更多的有机酸,导致游离酸增加,这些酸的浓度不断升高会导致pH值下降[19]。
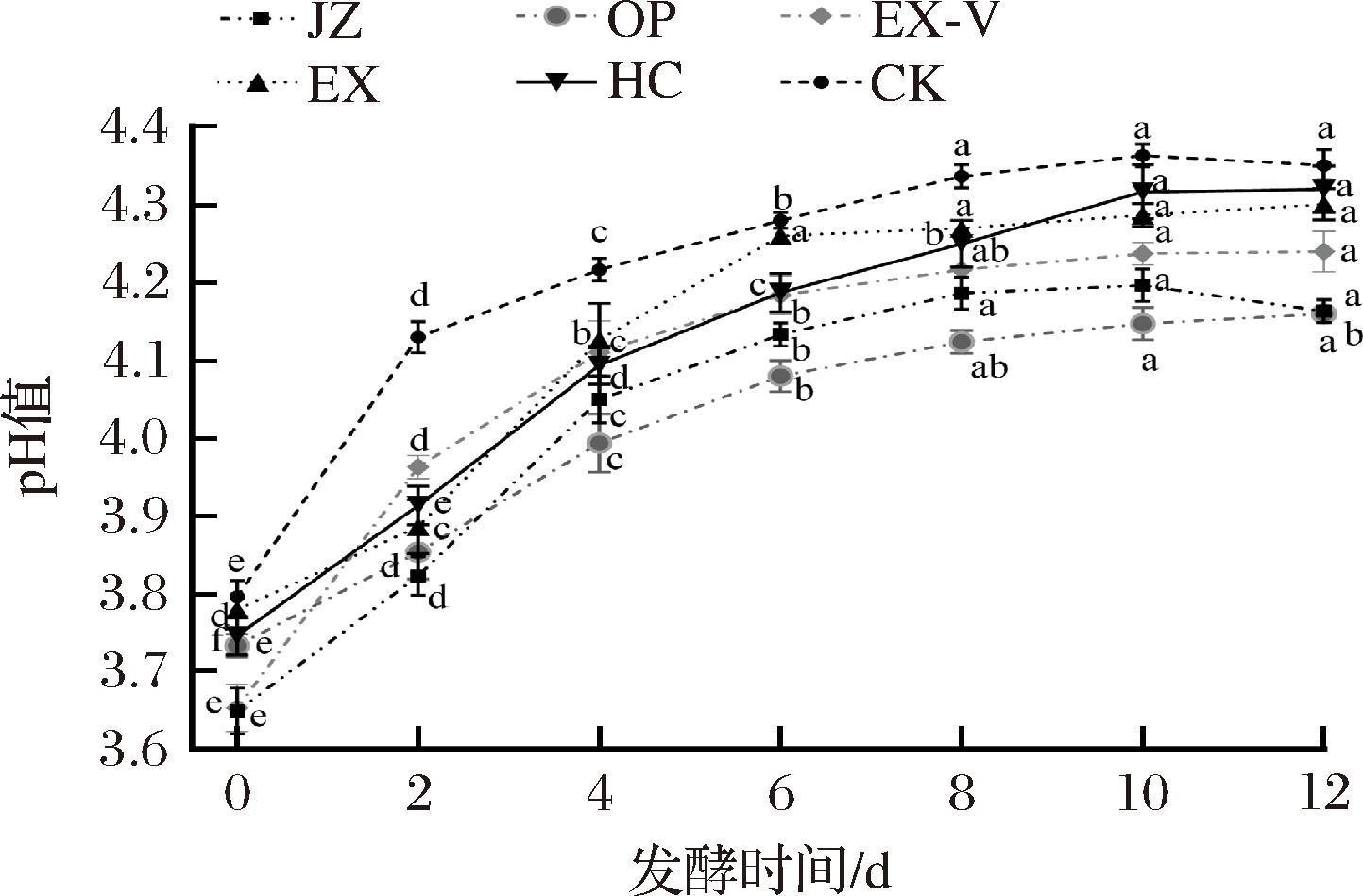
图2 不同果胶酶处理枣酒发酵过程中pH变化
Fig.2 Changes in pH during the fermentation of jujube wine with different pectinase treatments
2.3 不同果胶酶对骏枣果酒发酵过程中酒精度和还原糖的影响
由图3可知,骏枣果酒酒精度在发酵过程中呈先上升后趋于平缓的趋势,还原糖随着酒精发酵不断消耗呈先下降后趋于平缓趋势。主要原因是发酵前期,酵母菌通过糖酵解途径将葡萄糖、果糖等还原糖转化为丙酮酸,进而生成乙醇和CO2,在此阶段,酵母处于对数生长期,代谢活跃,还原糖被高效消耗,从而导致酒精度上升;发酵后期,发酵液中大部分还原糖被酵母消耗,维生素、矿物质及氮源缺乏导致酵母代谢受阻,因此,酒精度上升和还原糖下降都趋于稳定[20]。结果显示,各果胶酶组酒精度和还原糖含量显著高于CK组,此结果与钟思彦等[21]的研究结论一致。发酵12 d时,HC果胶酶组的酒精度最高,为11.72%vol,EX-V组的酒精度次之,为11.60%vol。OP组在发酵结束时还原糖含量(9.93 g/L)最高,但酒精度(11.14%vol)最低,这与WEI等[22]研究得出消耗糖越多得到的酒精度越高的结果一致。不同果胶酶由于水解果胶物质的能力不同,能供给酵母菌繁殖的营养成分有差异,导致酵母的发酵能力以及酒精度提升进程有所不同。
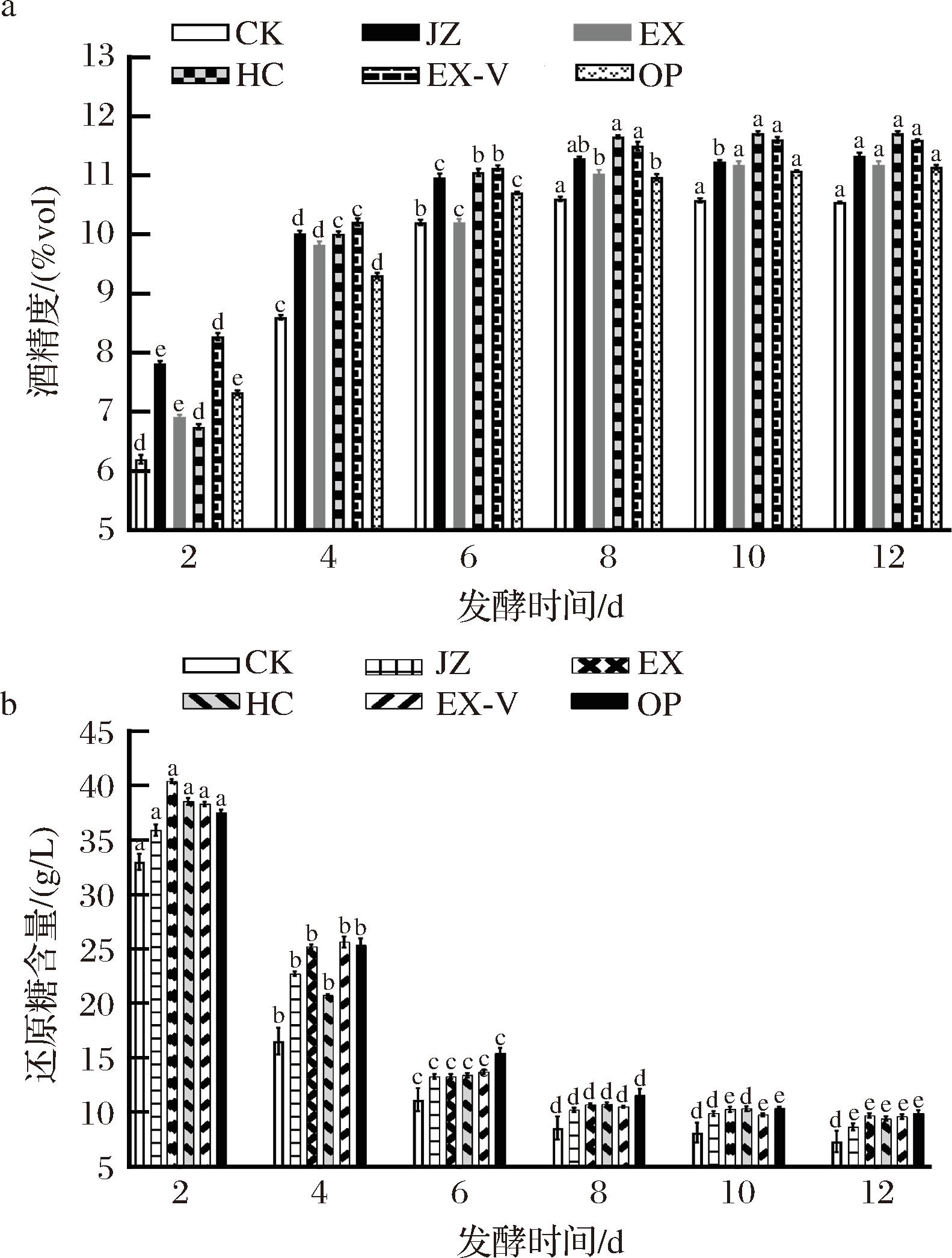
a-酒精度;b-还原糖含量
图3 不同果胶酶处理枣酒发酵过程中酒精度和还原糖变化
Fig.3 Changes in alcohol and sugars during the fermentation of jujube wine with different pectinases treatments
2.4 不同果胶酶对发酵骏枣果酒澄清度和甲醇的影响
不同种类的水果、同一种水果的不同品种作为发酵原料,由于其果胶含量不同,导致最终酿造的果酒中甲醇含量也有显著差异[23]。甲醇主要是由果胶甲酯酶作用于半乳糖醛酸甲酯上的酯键,经水解后释放出的,ZHAO等[24]对红枣中的内源性果胶甲酯酶进行灭活处理后,枣酒中甲醇含量降低了1.5倍。这些研究结果均进一步证实了果胶甲酯酶催化果胶分子中甲氧基的水解生成甲醇的机理。如图4所示,CK组的甲醇含量为283.77 mg/L,虽然果胶酶处理组的甲醇含量显著提高,但满足GB/T 15037—2006《葡萄酒》规定的甲醇含量(≤400 mg/L),这与张萃异等[25]的研究结果一致。此外,添加果胶酶的酒样透光率均显著高于CK组,其中HC果胶酶组的甲醇含量最低(313.76 mg/L),透光率最高,达到92.0%,这主要归因于不同果胶酶的种类、含量及酶活性的差异导致果胶酶水解果胶主链的程度不同,同时证实了果胶酶降低果汁黏度,促进胶体颗粒(如果肉碎片、蛋白质-多酚复合物)聚集沉淀,提高骏枣果酒的澄清度。
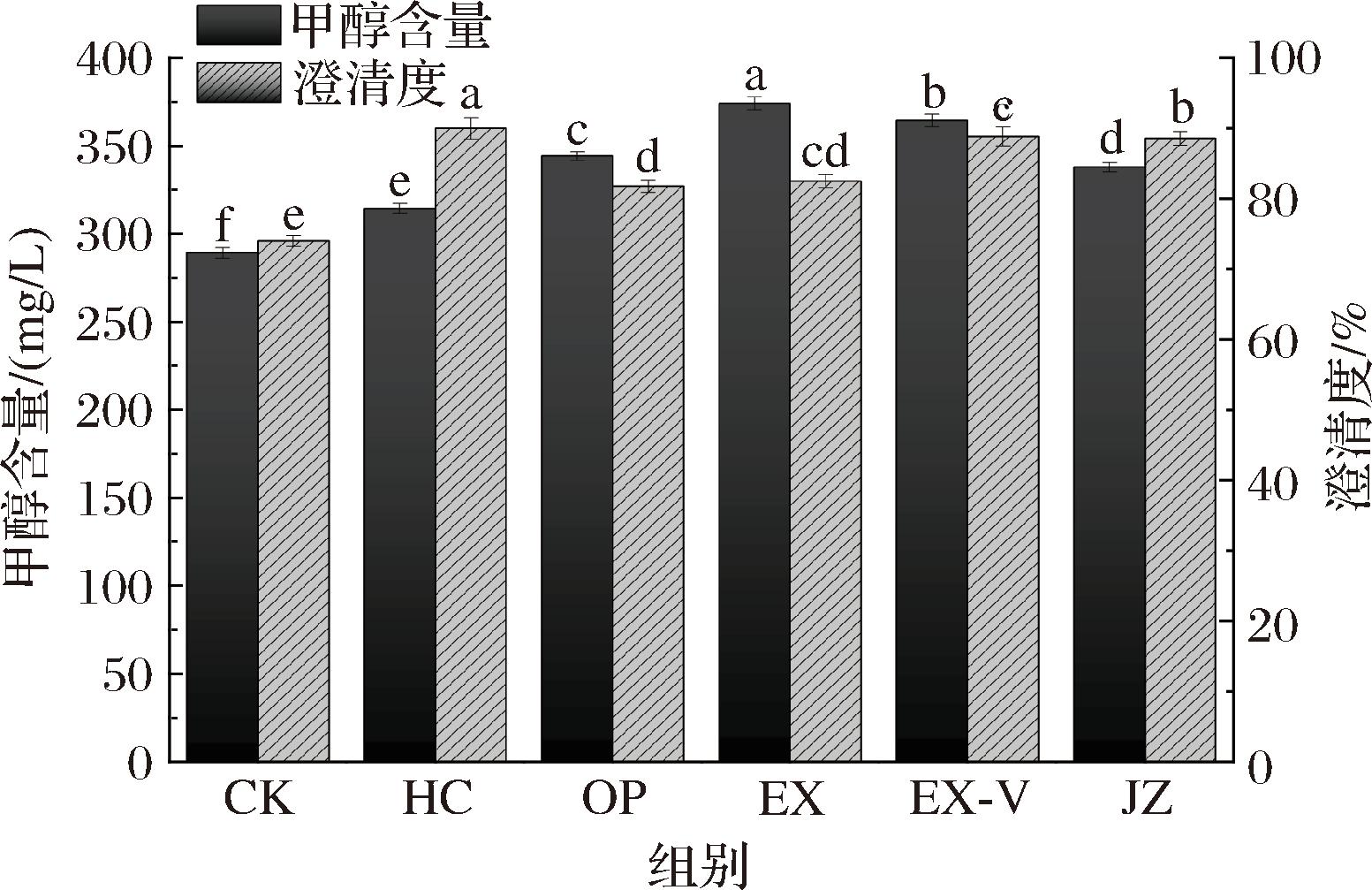
图4 不同果胶酶处理对骏枣果酒甲醇和澄清度的影响
Fig.4 Effect in methanol and clarification of jujube wine with different pectinase treatments
2.5 不同果胶酶对发酵骏枣果酒有机酸的影响
在骏枣果酒发酵过程中,有机酸可以与酒精反应生成酯类,酯类在果酒的口感和香气中起着至关重要的作用,是平衡和增强果酒感官特征的关键调节剂[26],其有机酸含量变化如表1所示。所有骏枣果酒中均检出5种有机酸,乳酸含量最高(3 084.75~3 305.18 mg/L),其次是苹果酸(1 103.26~1 406.27 mg/L)和柠檬酸(674.81~929.70 mg/L)。骏枣果酒发酵后,果胶酶组的总有机酸含量均显著高于CK组,主要原因是果胶酶通过特异性地降解果胶网络破坏植物细胞壁完整性,促进苹果酸、柠檬酸及酒石酸等天然存在于枣果液泡中的有机酸溶出,因细胞壁结构瓦解而大量释放至发酵体系[27]。但果胶酶组内之间相比,HC组苹果酸和酒石酸含量最高,EX组乳酸含量最高,JZ组柠檬酸和富马酸含量最高。由此可见,发酵过程中产生的乳酸、苹果酸为酵母菌生长提供适宜环境,调节口感并促进风味物质形成。
表1 不同果胶酶处理对骏枣果酒有机酸含量差异分析 单位:mg/L
Table 1 Analysis of the differences in organic acid contents of jujube wine with different pectinase treatments

果胶酶类型乳酸苹果酸柠檬酸酒石酸富马酸总和CK3 305.18±0.47a1 103.26±0.36e772.29±0.61e397.25±0.41f5.89±0.84ab5 583.87JZ3 084.75±0.45f1 396.21±0.60b929.70±0.54a480.86±0.43e6.50±0.50a5 898.02HC3 121.31±0.55e1 406.27±0.47a850.46±0.58b619.23±0.43a6.47±0.23a6 003.74EX3 302.28±0.38b1 352.22±0.69c791.75±0.58d492.92±0.69d5.89±0.58ab5 945.06EX-V3 242.19±0.41d1 396.17±0.67b674.81±0.32f517.57±0.84c4.97±0.32b5 835.71OP3 300.20±0.59c1 218.20±0.41d846.10±0.62c566.23±0.4b6.46±0.44a5 937.19
注:不同字母表示显著差异(P<0.05)(下同)。
2.6 不同果胶酶处理对果酒多酚类物质的影响
多酚类物质在果酒中发挥着重要作用,它可以决定产品的色泽和风味,具有神经保护、抗氧化、癌症预防、免疫调节等健康益处[28]。为了更好地分析不同果胶酶对骏枣果酒酚类物质之间的差异,本研究进一步采用LC-MS/MS对5种不同果胶酶处理的发酵骏枣果酒中多酚类物质的组成和含量进行测定,共检测出32种酚类单体,包括11种酚酸类、21种黄酮类化合物,其组成及含量变化见表2。由表2可知,添加果胶酶能增加骏枣果酒的多酚类物质含量,其中JZ组的多酚类物质含量最高,其次是HC和EX组,可能是由于不同果胶酶降解果胶,导致植物细胞壁松散,细胞结构崩解,提升溶剂对多酚的渗透能力,增强多酚类化合物的浸提和积聚,从而导致骏枣果酒中多酚类物质含量显著上升[29]。在骏枣果酒发酵后,含量较高的多酚类化合物是芦丁(1.009×106~1.371×106 μg/L)、奎宁酸(2.144×104~3.740×104 μg/L)、杨梅素(1.071×104~1.646×104 μg/L)、4-羟基苯甲酸(5 283.22~7 017.91 μg/L)。大多酚类物质会产生苦涩味,但儿茶素和绿原酸等可与果酒中生物碱和有机酸等相互作用形成络合物,阻止酚酸类物质与唾液蛋白结合,使骏枣果酒呈味特性发生改变,降低苦涩感,从而提高果酒鲜醇度[30]。
表2 不同果胶酶处理对骏枣果酒多酚类物质的差异分析 单位:μg/L
Table 2 Analysis of the differences of polyphenolic compounds in jujube wine with different pectinase treatments

序号化合物名称CKJZHCEXEX-VOP1奎尼酸2.144×104±0.31f3.568×104±0.57b3.740×104±0.96a3.104×104±0.96d3.093×104±0.57e3.156×104±0.92c2没食子酸95.83±0.34d128.23±0.34b133.29±0.59a88.48±0.48e89.55±0.92e97.83±0.69c34-羟基苯甲酸5 383.34±0.48e6 920.59±0.58b7 017.91±0.45a5 922.73±0.33d5 945.30±0.44c5 283.22±0.55f4绿原酸32.23±0.21c45.59±0.66a35.41±1.01b32.87±0.44c32.48±0.56c36.23±0.39b5(+)-儿茶素213.32±0.22e391.65±0.48a288.65±0.60b214.13±0.31e263.94±0.55c258.61±0.60d6隐绿原酸19.67±0.37c28.80±0.89a22.15±0.61b17.37±0.67d19.21±0.42c21.55±0.76b7香草酸401.26±0.58a316.10±0.25b237.26±0.60e297.22±0.35c221.97±0.32f294.40±0.69d8咖啡酸58.29±0.37a50.89±0.32bc50.46±0.56c43.09±0.43d51.29±0.50b42.64±0.17d9丁香酸51.34±0.48a29.21±0.57e32.20±0.29d34.18±0.23b17.14±0.26f33.33±0.53c10阿魏酸267.57±.0.28a254.22±0.50b151.16±0.07e101.30±0.56f154.56±0.51d247.33±0.63c11对香豆酸312.33±0.12d424.29±0.47b476.24±0.52a202.64±0.63f407.39±0.47c275.36±0.57e12表儿茶素2 135.49±0.25d3 216.48±0.18a2 816.52±0.18b1 637.77±0.11f2 083.23±0.21e2 278.85±0.18c13橙皮苷208.15±0.57a170.63±0.57e186.05±0.63c127.72±0.24f174.87±0.29d201.27±0.58b14远志山酮Ⅲ58.14±0.18e128.13±0.31a78.06±0.15c48.21±0.27f92.37±0.15b66.84±0.19d15芦丁1.009×106±0.28b1.371×106±0.41a1.220×106±0.55c1.057×106±0.40d1.023×106±0.37e1.017×106±0.46f16毛蕊异黄酮苷77.27±0.22c84.50±0.40a79.48±0.17b46.53±0.28f64.64±0.14e72.43±0.45d17牡荆素38.09±0.11d64.14±0.21a49.14±0.48b28.99±0.29f35.41±0.44e45.32±0.47c18异槲皮苷33.44±0.11c46.11±0.22a40.00±0.28b23.42±0.20f25.41±0.29e33.28±0.36d19杨梅素1.218×104±0.36d1.646×104±0.46a1.553×104±0.41b1.142×104±0.56e1.071×104±0.25f1.431×104±0.19c20槲皮素10.07±0.21e16.56±0.11a15.31±0.29b5.06±0.14f12.05±0.18c10.55±0.24d21根皮苷431.58±0.53d606.22±0.11a516.14±0.10b359.60±0.26f422.08±0.38e459.19±0.12c22白藜芦醇14.00±0.13d32.35±0.43a27.26±0.57b13.01±0.20e6.35±0.07f19.25±0.47c23大豆苷元20.54±0.24d35.92±0.12a29.28±0.52b18.38±0.15e10.12±0.11f23.98±0.05c24甘草素9.33±0.20c12.50±0.23a11.03±0.13b7.40±0.19e8.58±0.16d8.30±0.21d25槲皮苷1 241.37±0.15d2 212.39±0.43a2 075.54±0.53b9 52.25±0.41f1 600.41±0.37c1 184.13±0.19e26根皮素57.47±0.20d81.84±0.15a77.27±0.22b51.48±0.23e45.52±0.25f63.09±0.11c27芹菜素2 100.83±0.25d3 071.22±0.30a2 381.31±0.40b1 780.42±0.23f2 306.98±0.25c1 794.20±0.15e28柚皮素45.78±0.13c80.13±0.11a27.78±0.59f37.26±0.17e49.20±0.39b41.27±0.31d29山奈酚398.06±0.12b643.03±0.33a343.16±0.12e224.12±0.19f365.04±0.18d384.48±0.25c30山奈素2.11±0.10d3.30±0.13b4.37±0.20a2.25±0.18d2.73±0.24c2.99±0.13bc31木犀草素4.48±0.24d7.26±0.30b10.61±0.60a3.71±0.20e5.81±0.11c4.35±0.13d32香草醛4.11±0.11c6.11±0.27a5.60±0.32b3.41±0.18d5.34±0.08b3.67±0.11d总和1.056×1061.442×1061.290×1061.112×1061.079×1061.076×106
2.7 不同果胶酶处理的骏枣果酒综合品质的PCA
PCA是利用降维的思想,把多个独立的指标转化为几个综合指标(主成分)的多元统计方法,最终以几个主成分代替多个指标进行综合评价[31],是一种可以避免人为因素的干扰,广泛应用于食品品质的综合分析方法[32-33]。该方法为了综合评价5种果胶酶对骏枣果酒的品质影响,对总酸、还原糖、酒精度、澄清率、甲醇含量、pH、总有机酸、总黄酮和总酚酸物质共9个品质指标进行PCA。结果如表3所示,特征值大于1的主成分有3个,累计方差贡献率达到90.742%,能够全面反映骏枣果酒品质指标的信息。其中,PC1(44.742%)整合了澄清度、酒精度、总酸、有机酸及总酚酸,揭示果胶酶通过协同降解果胶主链、调控酸类代谢及释放酚类物质的核心作用;PC2(25.761%)关联甲醇含量与pH,反映甲醇生成与果胶酶类型密切相关,而pH变化则受有机酸和发酵副产物的双重调控,指向安全性及发酵环境稳定性;PC3(20.239%)以还原糖和总黄酮为核心,体现酶解对糖基释放及功能成分溶出的调控效应。
表3 特征值和方差贡献率
Table 3 Eigenvalue and variance contribution rate

主成分特征值方差贡献率/%累计方差贡献率/%PC14.02744.74244.742PC22.31925.76170.503PC31.82220.23990.742
各指标变量的PC载荷与相对应的特征值开平方根的比值,即为特征向量。3个PC的特征向量和载荷如表4所示。以特征向量为权重,通过与相应品质指标的标准化值线性加权求和构建3个PC的函数表达式:
F1=-0.146X1+0.417X2+0.398X3+0.207X4+0.099X5+0.449X6+0.390X7+0.483X8-0.080X9
F2=-0.568X1+0.169X2+0.347X3+0.342X4+0.561X5+0.106X6+0.270X7+0.114X8+0.001X9
F3=0.086X1+0.288X2+0.139X3+0.504X4+0.254X5+0.144X6+0.244X7+0.016X8-0.701X9
表4 PC的特征向量和载荷
Table 4 Eigenvectors and loadings of PCs
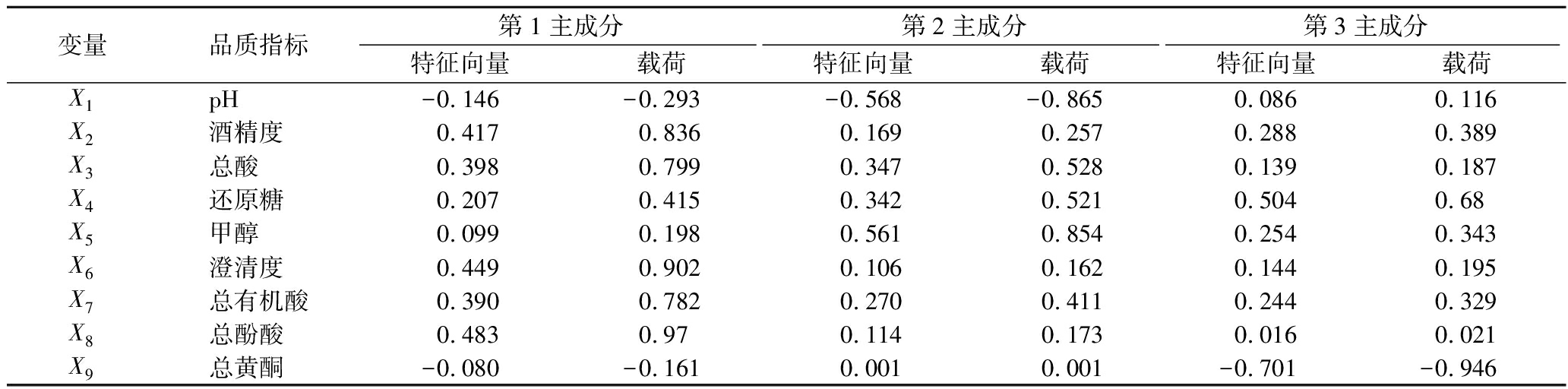
变量品质指标第1主成分第2主成分第3主成分特征向量载荷特征向量载荷特征向量载荷X1pH-0.146-0.293-0.568-0.8650.0860.116X2酒精度0.4170.8360.1690.2570.2880.389X3总酸0.3980.7990.3470.5280.1390.187X4还原糖0.2070.4150.3420.5210.5040.68X5甲醇0.0990.1980.5610.8540.2540.343X6澄清度0.4490.9020.1060.1620.1440.195X7总有机酸0.3900.7820.2700.4110.2440.329X8总酚酸0.4830.970.1140.1730.0160.021X9总黄酮-0.080-0.1610.0010.001-0.701-0.946
基于PCA构建的综合评价模型,本研究以3个PC的贡献率为加权系数,构建出不同果胶酶处理的骏枣果酒PCA的综合评价函数:F=0.493F1+0.284F2+0.223F3。其中,F1~F3分别代表各主成分得分,权重系数反映了其对整体品质的解释能力。根据综合评价函数计算出5种果胶酶(HC、JZ、OP、EX-V、EX)和非酶处理组CK骏枣果酒的模型评价得分F,结果如表5所示。F值大小排序为HC>EX-V>EX>JZ>OP>CK,结果表明HC果胶酶因其在功能性成分保留、甲醇控制及风味复杂度上的综合优势,更适合作为骏枣果酒生产的首选酶制剂,不仅在还原糖、pH、酒精度、澄清度等表现突出,有效平衡骏枣果酒的风味、营养价值和发酵效率;EX-V与EX综合评分次之,表明复合酶系更适配骏枣果胶结构,促进果胶分解的同时,释放更多多酚类物质;JZ、OP仅含高活性多聚半乳糖醛酸,无法有效处理高酯化果胶,虽能显著提升澄清度与酒精度,但单一酶导致酚类释放不足,而骏枣果胶侧链分支较多,需果胶裂解酶辅助裂解,释放深层结合的酚类物质。该PCA模型通过量化多维指标,实现了果酒品质的客观排序,为酶制剂优选提供了可量化的理论依据。
表5 不同果胶酶处理的骏枣果酒的综合评价得分
Table 5 Evaluation scores of jujube wine with different pectinase treatments
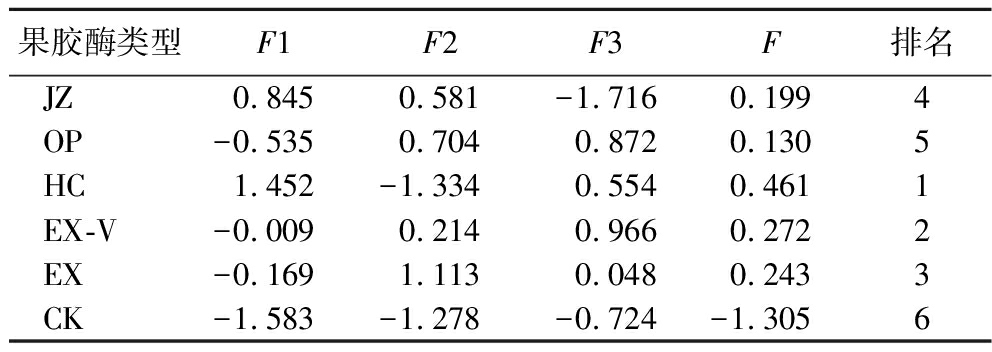
果胶酶类型F1F2F3F排名JZ0.8450.581-1.7160.1994OP-0.5350.7040.8720.1305HC1.452-1.3340.5540.4611EX-V-0.0090.2140.9660.2722EX-0.1691.1130.0480.2433CK-1.583-1.278-0.724-1.3056
3 结论
本研究对比5种商业果胶酶(HC、ZJ、OP、EX-V和EX)处理对骏枣果酒的品质影响,并结合主成分分析进行综合评价。结果表明由于不同果胶酶的酶系组成差异及其与骏枣果胶结构的适配性,果胶酶组与CK及果胶酶组间的骏枣果酒品质均有显著性差异,主成分综合评分排序为HC>EX-V>EX>JZ>OP>CK,验证HC果胶酶在骏枣果酒加工中的综合优势,突显了“酶-原料适配性”研究对骏枣深加工产业的核心价值,为开发低甲醇、高活性的特色果酒产品提供了理论支撑与技术路径。实际生产中,复合酶(HC、EX/EX-V)因酶系协同效应,更适配骏枣高酯化的果胶结构,在功能性成分释放、风味协调及安全性控制上显著优于单一酶(JZ、OP)。未来可结合代谢组学等进一步探索HC与EX-V复配策略,果胶酶系组成与骏枣果胶精细结构互作机制,协同优化酚类、酸度与安全性,推动骏枣果酒品质升级,为推动新疆红枣深加工产业的标准化与高值化发展提供参考。
[1] ZHANG L,LIU X Q,WANG Y J,et al.In vitro antioxidative and immunological activities of polysaccharides from Zizyphus Jujuba cv.Muzao[J].International Journal of Biological Macromolecules,2017,95:1119-1125.
[2] 包艳丽,程红梅,张利召.新疆红枣产业发展研究[J].农村经济与科技,2022,33(1):145-146;152.BAO Y L,CHENG H M,ZHANG L Z.Research on the development of the jujube industry in Xinjiang[J].Rural Economy and Science-Technology,2022,33(1):145-146;152.
[3] 靳娟,李丽莉,杨磊,等.新疆红枣产业发展现状分析[J].新疆农业科学,2024,61(S1):106-110.JIN J,LI L L,YANG L,et al.Analysis on the development status of Xinjiang jujube industry[J].Xinjiang Agricultural Sciences,2024,61(S1):106-110.
[4] 新疆统计局.新疆维吾尔自治区2023年国民经济和社会发展统计公报[R].乌鲁木齐:新疆统计局,2024.Xinjiang Bureau of Statistics.Statistical Bulletin on National Economic and Social Development of Xinjiang Uygur Autonomous Region 2023[R].Urumqi:Xinjiang Bureau of Statistics,2024.
[5] 王淑豪,冯雪,赵京涛,等.红枣蒸馏酒原酒发酵工艺优化及品质分析[J].中国酿造,2024,43(2):152-159.WANG S H,FENG X,ZHAO J T,et al.Optimization of fermentation technology and quality analysis of jujube original wine[J].China Brewing,2024,43(2):152-159.
[6] 黄孟阳.红枣酒发酵过程中甲醇变化规律及控制研究[D].西安:陕西师范大学,2017.HUANG M Y.Study on the methanol variation and control during the fermentation of red date wine[D].Xi'an:Shaanxi Normal University,2017.
[7] 余淑琪,丘佳慧,杜芷君,等.发酵果酒中甲醇的研究进展及控制方法[J].中国酿造,2024,43(7):33-40.YU S Q,QIU J H,DU Z J,et al.Research progress and control methods of methanol in fermented fruit wine[J].China Brewing,2024,43(7):33-40.
[8] JIAO S L,LI Y,WANG Z S,et al.Optimization of enzyme-assisted extraction of bioactive-rich juice from Chaenomeles sinensis (Thouin) Koehne by response surface methodology[J].Journal of Food Processing and Preservation,2020,44(9):e14638.
[9] 邱晓坤,宿珈嘉,聂江力,等.黑加仑果胶酶酶解榨汁工艺优化[J].食品研究与开发,2024,45(15):117-123.QIU X K,SU J J,NIE J L,et al.Blackcurrant juice extraction process with pectinase[J].Food Research and Development,2024,45(15):117-123.
[10] DUCASSE M A,CANAL-LLAUBERES R M,DE LUMLEY M,et al.Effect of macerating enzyme treatment on the polyphenol and polysaccharide composition of red wines[J].Food Chemistry,2010,118(2):369-376.
[11] 卫晓涵,张玉姣,纪超凡,等.低果胶酯酶活性果胶酶生产菌株的筛选及应用[J].中国食品学报,2025,25(2):213-223.WEI X H,ZHANG Y J,JI C F,et al.Screening of pectinase-producing strains with low pectin esterase activity and its application[J].Journal of Chinese Institute of Food Science and Technology,2025,25(2):213-223.
[12] 方锐琳,邓利珍,田煜琦,等.护色剂对全组分芒果汁高温灭菌过程的品质和风味影响[J].食品科学,2025,46(8):72-80.FANG R L,DENG L Z,TIAN Y Q,et al.Impact of color fixatives on the quality and flavor of whole mango juice during high-temperature sterilization[J].Food Science,2025,46(8):72-80.
[13] CHEN X X,PENG M D,WU D H,et al.Physicochemical indicators and sensory quality analysis of kiwi wines fermented with different Saccharomyces cerevisiae[J].Journal of Food Processing and Preservation,2022,46(11):e17132.
[14] JAYANI R S,SAXENA S,GUPTA R.Microbial pectinolytic enzymes:A review[J].Process Biochemistry,2005,40(9):2931-2944.
[15] YANG H,CAI G L,LU J,et al.The production and application of enzymes related to the quality of fruit wine[J].Critical Reviews in Food Science and Nutrition,2021,61(10):1605-1615.
[16] 蒋艺轩,冯作山,白羽嘉,等.不同成熟度杏果实发酵杏果酒品质分析[J].食品研究与开发,2024,45(6):69-77.JIANG Y X,FENG Z S,BAI Y J,et al.Quality of apricot wine fermented with different maturity levels of apricot fruits[J].Food Research and Development,2024,45(6):69-77.
[17] MEKOUE N J,PONCET-LEGRAND C,SIECZKOWSKI N,et al.Interactions of wine tannins and saliva in astringency:A mechanistic approach[J].Food Chemistry,2016,212:354-361.
[18] SHARMA H P,PATEL H,SUGANDHA.Enzymatic added extraction and clarification of fruit juices-a review[J].Critical Reviews in Food Science and Nutrition,2017,57(6):1215-1227.
[19] 程拯艮.果胶酶和浸渍处理对苹果酒品质特性影响的研究[D].西安:西北农林科技大学,2016.CHEN Z G.Effect of pectinase and maceration treatment on quality characteristic of apple wines[J].Xi’an:Northwest A&F University,2016.
[20] 刘士伟,刘胜楠,米倩雯,等.植物乳杆菌发酵人参中活性成分改变及抗氧化作用[J].食品科学,2023,44(20):252-259.LIU S W,LIU S N,MI Q W,et al.Changes in active components and antioxidant properties of ginseng fermented by Lactobacillus plantarum[J].Food Science,2023,44(20):252-259.
[21] 钟思彦,徐玉娟,余元善,等.酶解对香蕉果酒发酵前后风味的影响[J].食品工业科技,2024,45(3):98-106.ZHONG S Y,XU Y J,YU Y S,et al.Effect of enzymatic hydrolysis on flavor of banana wine before and after fermentation[J].Science and Technology of Food Industry,2024,45(3):98-106.
[22] WEI J P,ZHANG Y X,QIU Y,et al.Chemical composition,sensorial properties,and aroma-active compounds of ciders fermented with Hanseniaspora osmophila and Torulaspora quercuum in co-and sequential fermentations[J].Food Chemistry,2020,306:125623.
[23] JANUSZEK M,SATORA P,TARKO T.Oenological characteristics of fermented apple musts and volatile profile of brandies obtained from different apple cultivars[J].Biomolecules,2020,10(6):853.
[24] ZHAO Y,YU X B,ZHAO W,et al.Inactivation of endogenous pectin methylesterases by radio frequency heating during the fermentation of fruit wines[J].Fermentation,2022,8(6):265.
[25] 张萃异,刘辉,张碧颖,等.不同果胶酶处理对户太八号葡萄酒品质的影响[J].中国酿造,2024,43(5):68-74.ZHANG C Y,LIU H,ZHANG B Y,et al.Effect of different pectinase treatments on the quality of Hutai No.8 wine[J].China Brewing,2024,43(5):68-74.
[26] CHEN L H,PENG Q H,LIU B,et al.Study on the dynamic changes of nutrient components and flavor compounds during the fermentation process of high-quality highland barley wine[J].International Journal of Gastronomy and Food Science,2024,35:100860.
[27] 刘淑珍,苏颖玥,陈红梅,等.酿造技术对野生猕猴桃果酒有机酸组成及其品质的影响[J].酿酒科技,2021(4):71-78.LIU S Z,SU Y Y,CHEN H M,et al.Influence of fermentation technology on organic acid composition and quality of wild kiwifruit wine[J].Liquor-Making Science &Technology,2021(4):71-78.
[28] 邰振甲,王欣卉,宋雪健,等.植物多酚的生物合成、非生物胁迫调控与生理功能研究进展[J].食品工业科技,2025,46(15):425-434.TAI Z J,WANG X H,SONG X J,et al.Research progress of the biosynthesis,abiotic stress regulation and physiological functions in plant polyphenols[J].Science and Technology of Food Industry,2025,46(15):425-434.
[29] 王思溥,朱丹,牛广财,等.黑果腺肋花楸酵素自然发酵过程中主要成分与抗氧化活性变化[J].食品工业科技,2023,44(15):93-100.WANG S P,ZHU D,NIU G C,et al.Changes of main components and antioxidant activity of black chokeberry Jiaosu in natural fermentation[J].Science and Technology of Food Industry,2023,44(15):93-100.
[30] TIAN T T,SUN J Y,WU D H,et al.Objective measures of greengage wine quality:From taste-active compound and aroma-active compound to sensory profiles[J].Food Chemistry,2021,340:128179.
[31] YAN Y H,ABDULLA R,MA Q L,et al.Comprehensive identification of chemical fingerprint and screening of potential quality markers of Aloe vera (L.) burm.f.from different geographical origins via ultra-high-performance liquid chromatography hyphenated with quadrupole-orbitrap-high-resolution mass spectrometry combined with chemometrics[J].Journal of Chromatographic Science,2023,61(4):312-321.
[32] 陈菊,陆敏,黄正连,等.基于主成分和聚类分析贵州黔东南红酸汤品质的综合评价[J].中国酿造,2023,42(6):146-150.CHEN J,LU M,HUANG Z L,et al.Comprehensive evaluation of southeast Guizhou red sour soup quality based on principal component analysis and cluster analysis[J].China Brewing,2023,42(6):146-150.
[33] 齐亭亭,张智锋,杨新宇,等.基于主成分分析对不同品种红枣发酵果醋品质的综合评价[J].食品科学,2024,45(24):170-177.QI T T,ZHANG Z F,YANG X Y,et al.Comprehensive quality evaluation of red jujube vinegars made from different varieties based on principal component analysis[J].Food Science,2024,45(24):170-177.