大曲作为我国白酒酿造过程中不可或缺的糖化发酵剂,在推动发酵进程和形成白酒独特风味方面发挥着关键作用[1]。根据发酵过程的最高温度不同,大曲可分为高温大曲、中高温大曲、中温大曲和低温大曲等不同类型[2-3]。其中,高温大曲主要用于酱香型白酒的生产,其以小麦和母曲为主要原料,经历拌曲配料、曲块成型、入仓堆积、仓内发酵、拆曲出房及贮藏成熟等步骤制作而成,生产过程的最高发酵温度可达60~70 ℃[4]。由于曲块堆积发酵过程中存在空间异质性,不同位置曲块实际所处的发酵微环境如温度、湿度和氧含量等外界条件均存在明显差异,这导致同一曲房通常会生产出黑色、白色和黄色3种颜色的高温大曲[5]。此外,因酒曲制作工艺复杂、生产环境开放以及企业间制曲标准不同,不同企业生产的高温大曲在微生物群落结构和品质特性等方面同样表现出较大差异。例如,杨晨等[6]对产自茅台镇某公司的高温大曲开展研究,发现芽孢杆菌属(Bacillus)、克罗彭斯特德菌属(Kroppenstedtia)、嗜热真菌属(Thermomyces)和曲霉菌属(Aspergillus)是其中主要的微生物类群;SHI等[7]研究发现,除Thermomyces和嗜热子囊菌属(Thermoascus)外,在贵州茅台高温大曲中还存在较高丰度的红曲霉菌属(Monascus);而吴正坤等[8]研究则发现,湖北白云边酒业高温大曲中芽孢杆菌和根毛霉属(Rhizomucor)是其中的主要优势菌属。上述结果表明,不同地区企业及同一区域内不同企业生产的高温大曲在微生物群落结构方面均存在巨大差异。前期的研究进一步发现,即使是同一公司生产的3种不同颜色高温大曲,在理化品质、微生物群落结构和功能等方面也表现出明显差异[9]。因此,深入挖掘各地酿酒企业生产的不同颜色高温大曲在品质及微生物群落结构方面的特征,不仅有助于深化对我国不同地区高温大曲品质差异性的认识,同时也可为后续揭示各企业相同香型白酒在风格品质方面的差异提供一定科学依据。
在研究技术方面,Illumina MiSeq高通量测序技术通过并行测序策略,能够在单次实验中同时产生数百万条高质量的DNA序列。相较于传统的培养和克隆测序方法,Illumina MiSeq不仅可以克服大量微生物难以培养的问题,还能全面、高效地捕捉微生物群落的多样性和结构特征。目前,该技术已成功应用于发酵食品[10]、环境微生物[11]和酿酒微生物[12]等多个研究领域,展现出极强的跨学科适应性。大曲质量除受到其中所蕴藏的微生物影响外,大曲水分含量、酸度、氨基酸态氮含量、淀粉含量和蛋白质含量等理化特性也是评估大曲质量的重要指标。其中,水分含量对大曲的贮存稳定性、酶活力的变化、有机酸以及挥发性香气成分的变化有显著影响[13];酸度则反映了大曲发酵过程中有机酸的积累情况[3],对后续酿造过程中的pH调控具有重要意义;氨基酸态氮含量是评价大曲蛋白质降解程度的关键指标,氨基酸和小肽作为风味前体物,在发酵过程中转化成具有特定风味的物质[14],对白酒的香气有直接的影响;而淀粉含量和蛋白质含量则直接影响白酒酿造过程中碳源和氮源等营养成分的供给能力,同时对于酒体风味、滋味及浊度产生一定影响[15]。通过将这些指标与微生物指标相结合,能够更全面地评价大曲的品质特性及其与酒曲微生物之间的相互关系。
湖北襄阳地处鄂西北地区,位于汉江中游,是我国重要的酿酒产区之一。该地区拥有多家生产不同香型白酒的企业,具备较为成熟的制曲工艺和发酵车间,然而目前针对该地区酒企所制作的高温大曲品质特征及其真菌群落结构的研究尚少。本研究以襄阳地区某酒厂生产的黑色、白色和黄色3种不同颜色高温大曲为研究对象,采用国标中规定的理化检测手段评估其各项品质特性,同时借助Illumina MiSeq高通量测序技术深入分析了高温大曲中的真菌多样性。本研究增进了人们对襄阳地区高温大曲真菌多样性及其品质特征的认识,为相关企业进一步提高大曲质量提供了重要参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
高温大曲样品:于2024年10月采集自襄阳地区某酒厂制曲车间,其中黑色(简称:黑曲,编号:B1~B10)、白色(简称白曲,编号:W1~W10)和黄色(简称:黄曲,编号:Y1~Y10)高温大曲样品各采集10份,共计30份样品。3种颜色高温大曲均使用相同原料于同一批次生产,在实验室条件下将采集到的大曲样品粉碎并置于-20 ℃下保存备用。
1.1.2 试剂
葡萄糖、氢氧化钠、酒石酸钾钠、碘、乙醇、硫酸铜、硫酸铵、甲醛、盐酸、硫酸、硼酸、次甲基蓝、甲基红和溴甲酚绿(均为分析纯),西陇化工股份有限公司;样本宏基因组DNA提取试剂盒,美国Omega Bio-Tek公司;dNTP和rTaq聚合酶,宝日医生物技术(北京)有限公司;引物ITS3F/ITS4R(ITS3F:5′-GCATCGATGAAGAACGCAGC-3′;ITS4R:5′-TCCTCCGCTTATTGATATGC-3′),上海桑尼生物科技有限公司;Illumina MiSeq测序试剂盒v3,美国Illumina公司。
1.2 仪器与设备
SH-10A水分测定仪,上海力辰仪器科技有限公司;AW-1水分活度仪,无锡碧波电子设备厂;PHS-3C数显台式酸度计,上海越平科学仪器有限公司;K1100全自动定氮仪,济南海能仪器股份有限公司;Vetiri PCR梯度基因扩增仪,美国AB公司;MiSeq PE300高通量测序平台,美国Illumina公司;R930机架式服务器,美国DELL公司。
1.3 实验方法
1.3.1 高温大曲各项理化指标的测定
高温大曲的水分含量、酸度、氨基酸态氮含量、淀粉含量和蛋白质含量均参照轻工行业标准QB/T 4257—2011《酿酒大曲通用分析方法》进行测定[16]。高温大曲的水分活度使用水分活度仪按照说明书中的方法进行测定。
1.3.2 宏基因组DNA提取、PCR扩增和高通量测序
首先按照DNA提取试剂盒提供的方法,完成高温大曲样品宏基因组DNA的提取。利用添加了核苷酸标签的引物ITS3F/ITS4R对DNA模板中真菌内源转录间隔区(nternally transcribed spacer,ITS)进行聚合酶链式反应(polymerase chain reaction,PCR)扩增。使用琼脂糖凝胶电泳对扩增产物进行检测,将合格的PCR产物送至公司进行Illumina MiSeq高通量测序。
1.3.3 序列质控和生物信息学分析
使用QIIME(v 1.9.1)平台对高通量测序数据进行生物信息学分析,具体步骤如下:a)删除测序数据中的接头序列;b)将测序数据根据引物中的barcode标签信息划分到各个样本中;c)对下机数据进行质量控制(剔除双端序列拼接时错配率≥0.2、引物碱基错配数≥2 bp或barcode碱基有错配的序列);d)质量合格的序列按照97%相似度构建分类操作单元(operational taxonomic units,OTU),随后使用vsearch软件识别并去除属于嵌合体的OTU[17];e)选取OTU中的代表性序列与Unite(v 10.0)数据库中进行比对以确定各OTU的注释信息[18];f)基于OTU水平的数据计算3种颜色高温大曲各样品真菌的发现物种数指数和香农指数用于评估各样品真菌的丰度和多样性。
1.4 数据处理与统计分析
本研究首先使用GraphPad Prism(v10.4.1)软件绘制小提琴图,以直观展示高温大曲的理化指标数据;随后,使用R(v 4.3.2)软件ggplot2包(v 3.5.1)绘制发现物种数指数和香农指数曲线图及箱形图,以评估样本测序量是否足够以及不同颜色高温大曲α多样性差异;进一步使用R软件中的“ade4”包(v1.7.15)和“vegan”包(v2.6.2),基于加权和非加权UniFrac距离进行主坐标分析(principal coordinates analysis,PCoA)和置换多元方差分析(PERMANOVA,置换次数=999),以评估微生物群落结构的差异;此外,R软件还被用于绘制柱形图,以展示真菌类群的相对含量,并通过花瓣图和瀑布图对样品中的OTU分布和平均相对含量超过1.0%的OTU进行可视化。本研究对于不同颜色高温大曲中的核心OTU进行了Spearman检验,并使用Gephi(v 0.9.2)软件构建了核心OTU的共生网络图。此外,本研究利用LEfSe分析即线性判别分析,确定了3种颜色曲种真菌各分类水平上具有统计学差异的微生物类群,同时对优势菌属与理化指标之间的相关进行了Spearman相关性检验。
2 结果与分析
2.1 三种颜色高温大曲样品的理化指标分析
理化指标是评估大曲品质的重要参照,本研究3种颜色高温大曲的水分含量、水分活度、酸度、氨基酸态氮、淀粉含量和蛋白质含量的测定结果如图1所示。
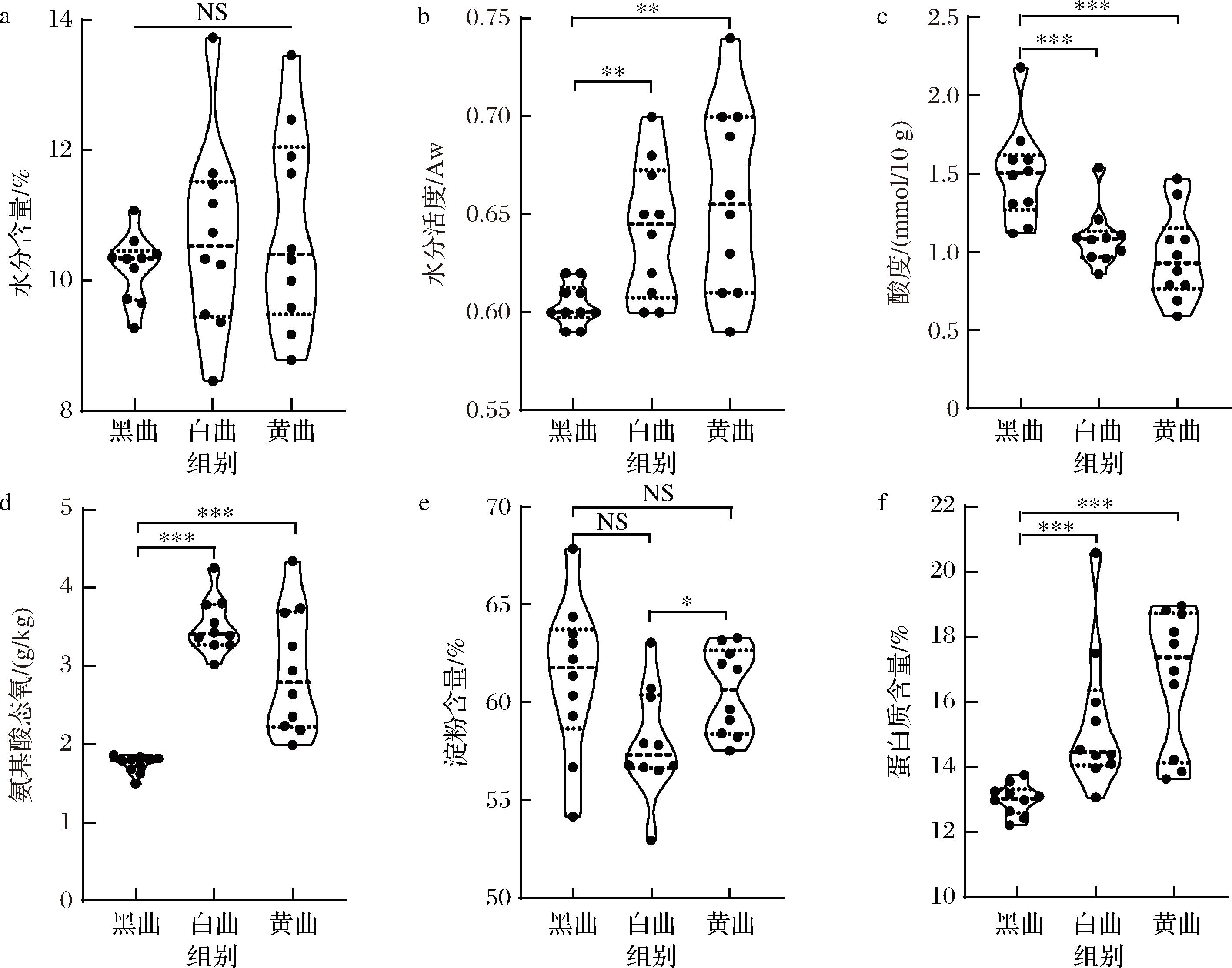
a-水分含量;b-水分活度;c-酸度;d-氨基酸态氮;e-淀粉含量;f-蛋白质含量
图1 三种颜色高温大曲的理化指标分析
Fig.1 Analysis of physicochemical indicators of three colors of high-temperature Daqu
注:NS代表P>0.05,差异不显著;*代表P<0.05,差异显著;**代表P<0.01,差异非常显著;***代表P<0.001,差异极显著。
由图1可知,3种颜色高温大曲的水分含量不存在显著差异,各样品水分含量均介于8%~14%。然而,经Mann-Whitney检验发现,黑曲的水分活度、氨基酸态氮和蛋白质含量显著低于白曲和黄曲(P<0.05),同时其酸度显著高于白曲和黄曲(P<0.05)。影响食品中水分活度的因素包括食品组分、水分含量和温度等[19],龙树瑺等[20]的研究进一步指出,大曲中不同微生物代谢可以产生差异性的代谢产物,这对大曲水分活度带来很大影响。考虑到纳入本研究的3种颜色高温大曲在水分含量方面的差异并不显著,因此水分活度的差异可能与3种大曲中微生物代谢产物不同存在一定关系。大曲中的酸性成分主要来源于微生物代谢糖类产生的有机酸[21],本研究发现黑曲中的酸度显著较高,表明黑曲在发酵过程中可能经历了更强的有机酸合成的过程。此外,与ZHAO等[22]之前研究所报道的结果一致,本研究也发现黑曲中的蛋白质含量较低。该结果预示着黑曲中菌群代谢蛋白质的能力相对较强,从而能更有效的将其中的蛋白质降解。与此同时,黑曲中的氨基酸态氮含量显著较低则可能与其较高的发酵温度有关,温度升高可以促使氨基酸与糖类物质发生更多的缩合反应[23],从而减少了其氨基酸态氮的含量。
2.2 三种颜色高温大曲样品的测序结果与真菌α多样性分析
通过对所有样品进行基于Illumina MiSeq平台的高通量测序,共获得1 942 637条原始序列,经质控剔除不合格序列后最终保留了1 937 256条高质量序列用于后续分析,平均每个样品含有64 575条合格序列。在97%的相似度阈值下对这些序列进行OTU划分,共得到5 882个OTU,平均每个样品OTU的数量为1 536个。
为了评估样本的测序量是否足够,本研究利用发现物种数指数和香农指数曲线评估了样本的测序量,结果如图2-a和图2-b所示。
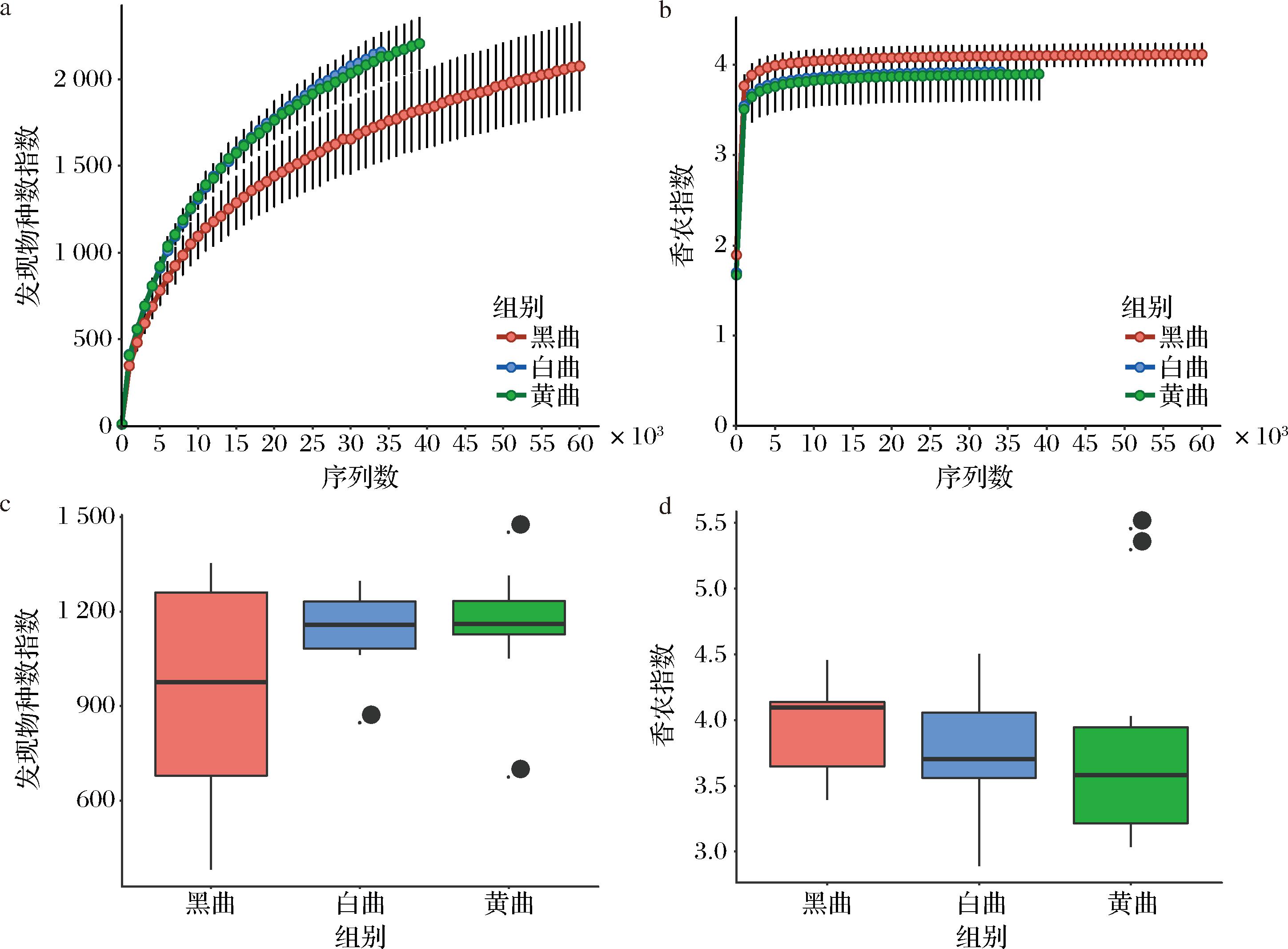
a-样品中真菌发现物种数指数曲线;b-为样品中真菌香农指数曲线;c-不同颜色大曲发现物种数指数箱形图;d-不同颜色大曲香浓指数箱形图
图2 三种颜色高温大曲测序量评估及α多样性比较分析
Fig.2 Evaluation of sequencing depth and comparison analysis of α-diversity in three colors of high-temperature Daqu
由图2-a和图2-b可知,随测序深度的增加,发现物种数指数曲线不断上升,而香农指数曲线在测序深度达到10 000条序列时已经趋于稳定,表明在此测序深度之后,增加测序量虽然可能发现更多低丰度的真菌,但整体真菌多样性已趋于饱和。因此,本研究中各样本的测序深度可以有效揭示样品中真菌群落的组成。本研究在测序深度为33 010条序列时(测序量最低的样本中所包含的序列数)对各样品的α多样性进行了评估。结果显示,黑曲、白曲和黄曲的真菌平均发现物种数指数分别为943、1 139、1 154(图2-c),平均香农指数分别为3.95、3.74、3.83(图2-d)。经Mann-Whitney检验发现,上述指标在3组样品间不存在显著差异(P>0.05)。尽管如此,该结果显示与其他2种颜色高温大曲相比,黑曲中真菌的丰度相对较低,但多样性相对较高。通过对测序序列进行分类学地位注释,结果发现所有测序序列可以注释到9个门、18个纲、36个目、75个科和117个属,其中分别有0.05%和0.33%的序列无法确定门和属水平的具体分类学地位。优势真菌门和真菌属(平均相对含量>1.0%)的结果如图3所示。
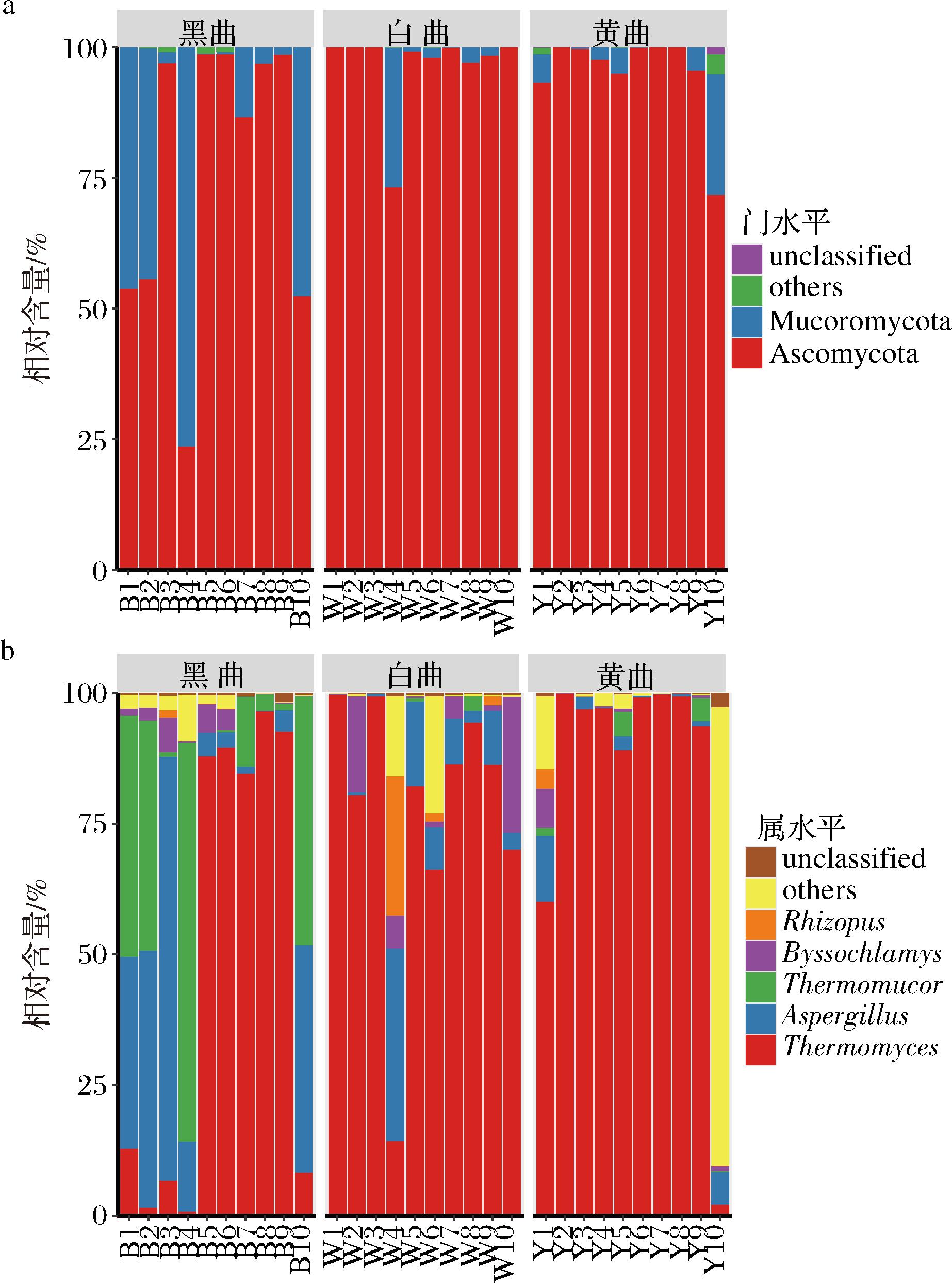
a-门水平;b-属水平
图3 三种颜色高温大曲中真菌在门水平和属水平的主要组成
Fig.3 The primary fungal composition at the phylum and genus levels in high-temperature Daqu of three colors
注:图中“unclassified”表示在相应分类学地位水平,无法明确这些微生物的具体分类学地位;“others”代表所有样品中除“unclassified”外,平均相对含量小于1%的所有微生物类群。其中门水平,“other”分类中主要包含的菌门为Basidiomycota、Mortierellomycota等;属水平,“others”分类中主要包含的菌属为Rhizomucor、Penicillium、Alternaria和Pichia等。
由图3-a可知,高温大曲中的优势真菌门分别为子囊菌门(Ascomycota,89.37%)和毛霉菌门(Mucoromycota,10.31%)。由图3-b可知,所有样品中平均相对含量在1%以上的优势真菌属分别为Thermomyces(69.98%)、Aspergillus(11.67%)、Thermomucor(8.25%)、丝衣霉菌属(Byssochlamys,2.94%)和根霉菌属(Rhizopus,1.18%)。Thermomyces、Aspergillus和Thermomucor均为高温大曲中常见的优势真菌属,这些菌属对高温具有较强的耐受性[24]。ZHU等[25]的研究发现,Thermomyces在贵州和山东地区高温大曲中的含量亦比较高,其占两地高温大曲中真菌的比例分别高达31.8%和48.1%。Thermomyces作为生产淀粉酶、纤维素酶和蛋白酶的代表性菌属,有助于降解发酵原料中的蛋白质和大分子多糖,促进白酒酿造体系中微生物生长和风味物质的产生[26]。而Aspergillus主要来自于高温大曲制作原料小麦,可以参与糖异生Ⅰ和蔗糖降解Ⅲ等代谢途径[27],在大曲风味形成和微生物群落更替中发挥着重要作用[28]。FAN等[29]的研究结果则发现,Thermomucor与酒曲的糖化力和液化力具有显著正相关关系,预示着该菌具有生产淀粉酶和葡萄糖苷酶的能力。而Rhizopus则以生产淀粉酶而闻名,该菌属可以促进淀粉转化为葡萄糖,为后续酵母菌提供碳源,并促进白酒中的酯类物质的产生[30]。上述结果表明高温大曲中的优势真菌在高温大曲的发酵过程中,不仅成功适应了高温环境,而且通过各自特有的酶系和代谢途径发挥着重要的调控蛋白质、多糖等大分子物质的降解与转化的作用,从而促进了后续生产中原料的糖化、液化及风味物质的生成。
2.3 三种颜色高温大曲样品中的核心真菌菌群分析
在对高温大曲真菌群落在门和属水平分析结果的基础上,本研究进一步在OTU水平对3种高温大曲中的核心菌群进行了探究。本研究将在所有样品中均出现的OTU定义为高温大曲的核心OTU,这些OTU的分布情况及核心OTU在不同颜色高温大曲中的共生网络如图4所示。
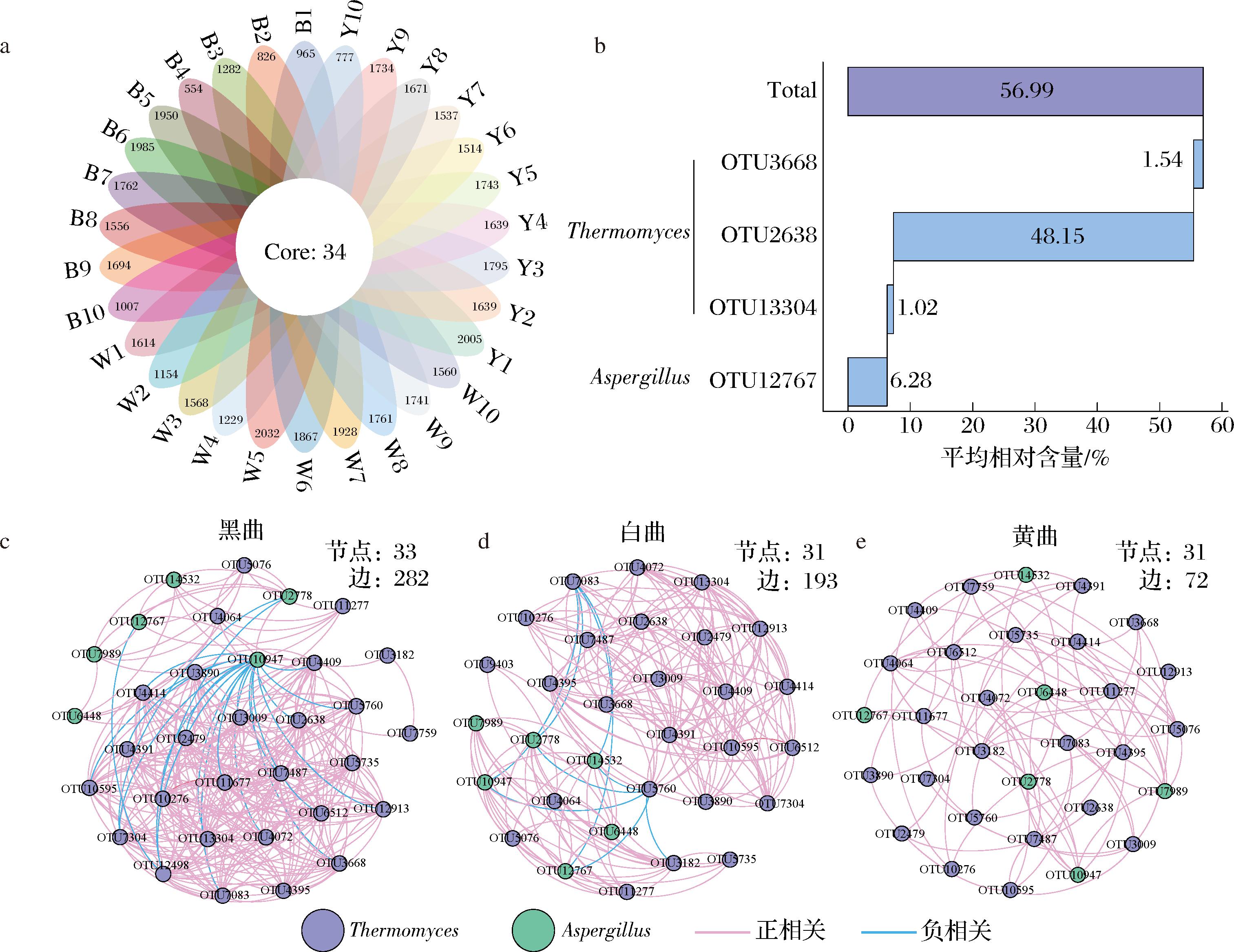
a-为所有样品中的OTU数量分布;b-相对含量>1.0%的核心OTU及其相对含量;c-黑曲中核心OTU的共生网络;d-白曲中核心OTU的共生网络;e-黄曲中核心OTU的共生网络
图4 三种颜色高温大曲中的OTU分布情况及核心菌群的共生网络分析
Fig.4 Distribution of OTUs and symbiotic network analysis of core group in three colors of high-temperature Daqu
注:网络中列出的相关关系均存在显著性,即P<0.05。
由图4-a所示,在30份大曲样品中均存在的核心OTU共34个,这些OTU占所有真菌的比例平均为62.3%。由图4-b可知,有4个核心OTU的平均相对含量>1.0%,它们分别为注释结果为Thermomyces的OTU2638(48.15%)、OTU3668(1.54%)和OTU13304(1.02%),以及注释结果为Aspergillus的OTU12767(6.28%),这4个OTU在样品中的平均累计相对含量高达56.99%。这表明Thermomyces和Aspergillus是高温大曲中的关键功能菌群,是后续深入探究高温大曲发酵特性与功能机制的重要靶向研究对象。
本研究基于Spearman秩和检验分别构建了3种颜色高温大曲中核心OTU彼此间的共生网络。由图4-c可知,黑曲、白曲和黄曲样品分别形成了由33、31、31个核心OTU参与的共生网络,彼此间分别存在282、193、72对显著相关关系,其中正相关关系占全部相关关系的比例分别为92.20%、95.34%、100%。由此可见,不同颜色高温大曲中的核心OTU共生网络存在一定的差异性,其中黑曲的微生物交互作用最强,白曲次之,而黄曲的菌群间相互作用相对简单。黑曲中复杂而紧密的网络预示着其菌群之间存在较强的协同作用,这有助于形成稳定的发酵生态系统,促进关键酶类和代谢产物的有效转换,从而对大曲的风味形成和发酵性能产生积极影响;相比之下,黄曲则完全由正相关构成,但显著相关关系的对数明显较少,表明其菌群相互依赖性较弱,微生物间的功能分工较为单一。值得注意的是,SHI等[7]解析贵州茅台不同颜色高温大曲真菌群落结构关系时发现,虽然黄曲中核心菌群均呈正相关关系,但白曲中菌群间的相互作用最强,这表明不同企业生产的同种颜色高温大曲的菌群特征并不完全一致,这可能也是不同白酒企业产品品质存在一定差异的原因之一。
2.4 三种颜色高温大曲菌群群落结构差异分析及优势真菌与理化指标间的相关性分析
本研究基于非加权和加权UniFrac距离对3组样品真菌β多样性进行了分析(图5-a和图5-b)。分析结果显示,白色和黄色大曲样品在PCoA图上存在一定重叠,而黑色大曲则与它们有明显的分离趋势。置换多元方差分析(permutation multivariate analysis of variance,PERMANOVA)结果进一步证实,不同颜色大曲整体菌群群落结构的差异达到了显著水平(P<0.01)。本研究通过LEfSe分析,进一步揭示了3种颜色高温大曲中相对含量存在显著差异的微生物类群,结果如图5-c和图5-e所示。结果发现,在属水平,黑曲中Thermomucor、Aspergillus和Trichomonascus相对含量显著较高;而黄曲中Thermomyces和毕赤酵母属(Pichia)的相对含量显著较高,同时Thermomyces在黑曲中的相对含量最低;白曲中未发现显著高于另外2种颜色大曲的真菌属。Spearman秩和检验结果表明(图5-d),高温大曲优势菌属中,Aspergillus、Thermomucor和Byssochlamys与酸度呈显著正相关(P<0.05),而Thermomyces与酸度呈显著负相关(P<0.05)。此外,Thermomucor与水分活度、氨基酸态氮、蛋白质含量呈显著负相关(P<0.05);而Aspergillus和Thermomyces与蛋白质含量分别呈显著负相关和显著正相关关系(P<0.05)。

a-基于非加权UniFrac距离的主坐标分析;b-基于加权UniFrac距离的主坐标分析;c-差异菌群LEfSe分析;d-优势菌属与理化指标间的相关性分析;e-差异菌属在3种颜色高温大曲中的具体含量
图5 三种颜色高温大曲差异菌群分析和相关性分析
Fig.5 Differential microbial community analysis and correlation analysis in in three colors of high-temperature Daqu
注:中标有×的方格表示P>0.05,即对应菌属与理化指标间不存在显著相关关系;未标有×的方格表示P<0.05,即对应菌属与理化指标间存在显著相关关系,圆点上的数字为两者之间的相关性系数。不同小写字母表示差异显著(P<0.05)。
上述结果表明,整体菌群群落结构方面,黑色大曲拥有更为独特的耐热真菌类群。其中,部分研究发现Thermomucor与糖化和液化活性呈显著正相关,预示着该菌属是淀粉酶或葡萄糖苷酶的重要产生菌[29]。SHI等[7]的研究则发现,随着大曲颜色的加深即发酵温度的升高,Aspergillus的相对含量呈逐渐上升的趋势,这与本研究的结果一致。此外,与白色和黄色大曲相比,Trichomonascus在黑色高温大曲中显著富集的结果与CAI等[31]之前的研究结果也一致。该菌属据报道与温度呈正相关关系,并且具有促进酸、醛、酮和呋喃等风味化合物的形成的作用[14]。上述结果表明,温度是高温大曲真菌群落结构演变及形成的重要驱动因素,在较高温度条件下形成的黑色大曲中富集了较多的耐热微生物,这些菌在原料糖化、液化和风味化合物的形成中发挥着重要作用。黄曲中富集的菌属中,Thermomyces在不同颜色高温大曲中所占比例与ZHU等[32]基于茅台酒业高温大曲的研究相吻合。该菌在原料分解及风味物质产生方面均发挥着重要的作用,而Pichia据报道不仅具有较强的酯化能力,同时它还可以利用蔗糖和葡萄糖产生多种芳香类化合物如乙醇、乙酸乙酯和4-羟基-2-丁酮等[33]。因此,黄色大曲在后续酿酒过程中对原料分解利用和风味物质形成发挥着重要作用。在菌群与理化指标相关性方面,Aspergillus与酸度呈显著正相关关系,该结果与REN等[34]的研究结果一致,导致该结果的主要原因可能与Aspergillus在代谢中可以产生柠檬酸等有机酸存在一定关系[35]。与此同时,该菌属可以分解蛋白质产生多种氨基酸或寡肽[36],这可以解释其与蛋白质含量之间呈现出显著负相关的关系。Byssochlamys据报道与窖泥中的总酸亦呈现正相关关系[37],表明该菌自身可以合成酸类物质或者其具有促进酸类合成的作用,这可能是该菌与酸度指标之间存在正相关关系的主要原因。而Thermomyces据报道具有合成蛋白质的潜在代谢功能[38],这可能是本研究中其与蛋白质含量之间存在正相关关系的主要原因。值得注意的是,通过查阅中英文文献,尚未发现有关于Thermomucor与水分活度、氨基酸态氮、蛋白质含量之间存在负相关关系的报道,同时由于关于该菌相关功能的研究较为有限,导致该结果出现的具体原因还需要后续研究进一步揭示。
3 结论
本研究综合运用国标检测方法和高通量测序技术系统揭示了不同颜色高温大曲的理化特性、真菌群落特征及其相互作用规律。研究表明,Thermomyces、Aspergillus、Thermomucor和Byssochlamys等菌属是高温大曲中的优势真菌属,这些菌属在驱动大曲酸度、氨基酸态氮、蛋白质含量等指标变化方面发挥着重要作用。3种颜色大曲在真菌群落结构方面表现出显著差异,温度是高温大曲真菌群落结构演变及形成的重要驱动因素。理化特性方面,黑曲表现出显著区别于白曲和黄曲的理化特性,其较高的酸度与Thermomucor、Aspergillus等耐热真菌的富集密切相关,而较低的水分活度、氨基酸态氮及蛋白质含量则可能与菌群代谢活性增强及高温诱导的缩合反应有关。黄曲中富集的Thermomyces和Pichia在促进原料分解与芳香物质合成方面发挥着重要作用。本研究还首次发现了Thermomucor与水分活度、氨基酸态氮、蛋白质含量之间存在显著负相关关系。后续研究可结合代谢组学和功能验证进一步探究核心菌属的代谢途径及一些菌属与理化指标间相关关系的内在机制,从而为企业酒曲品质改良提供更为科学的指导。
[1] 尉嘉眙,常强,蒋超,等.大曲理化性质与白酒产品风味的相关性分析[J].食品工业科技,2020,41(18):244-251.WEI J Y,CHANG Q,JIANG C,et al.Correlation analysis between physicochemical properties of Daqu and flavor of liquor products[J].Science and Technology of Food Industry,2020,41(18):244-251.
[2] FU G M,DENG M F,CHEN K D,et al.Peak-temperature effects of starter culture (Daqu) on microbial community succession and volatile substances in solid-state fermentation (Jiupei) during traditional Chinese special-flavour Baijiu production[J].LWT,2021,152:112132.
[3] WANG Y R,HOU Q C,NI H,et al.Multi-method joint analysis reveals differences in the quality and microbial composition of high-temperature and medium-high-temperature Daqu[J].LWT,2024,209:116804.
[4] SHI G L,FANG C,XING S,et al.Heterogenetic mechanism in high-temperature Daqu fermentation by traditional craft and mechanical craft:From microbial assembly patterns to metabolism phenotypes[J].Food Research International,2024,187:114327.
[5] GE D Y,CAI W C,GUO Z,et al.Comparative analysis of bacterial community structure and physicochemical quality in high-temperature Daqu of different colors in Qingzhou production area[J].Heliyon,2024,10(11):e31718.
[6] 杨晨,杨栩松,郭壮,等.茅台镇某酒厂高温大曲微生物多样性与感官品质关联性分析[J].中国酿造,2023,42(11):48-53.YANG C,YANG X S,GUO Z,et al.Correlation analysis of microbial diversity and sensory quality of high-temperature Daqu from a distillery in Maotai town[J].China Brewing,2023,42(11):48-53.
[7] SHI W,CHAI L J,FANG G Y,et al.Spatial heterogeneity of the microbiome and metabolome profiles of high-temperature Daqu in the same workshop[J].Food Research International,2022,156:111298.
[8] 吴正坤,刘蒲临,杨团元,等.不同贮存期高温大曲微生物群落演替与理化指标相关性分析[J].中国酿造,2023,42(7):160-166.WU Z K,LIU P L,YANG T Y,et al.Correlation analysis of microbial community succession and physicochemical properties of Daqu in different storage periods[J].China Brewing,2023,42(7):160-166.
[9] HOU Q C,WANG Y R,QU D W,et al.Microbial communities,functional,and flavor differences among three different-colored high-temperature Daqu:A comprehensive metagenomic,physicochemical,and electronic sensory analysis[J].Food Research International,2024,184:114257.
[10] SUN X D,LYU G Z,LUAN Y S,et al.Analyses of microbial community of naturally homemade soybean pastes in Liaoning province of China by Illumina Miseq sequencing[J].Food Research International,2018,111:50-57.
[11] NYGAARD A B,TUNSJØ H S,MEISAL R,et al.A preliminary study on the potential of Nanopore MinION and Illumina MiSeq 16S rRNA gene sequencing to characterize building-dust microbiomes[J].Scientific Reports,2020,10:3209.
[12] ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Research International,2022,153:110955.
[13] 丁伟,魏莎莎,闫裕峰,等.山西老陈醋大曲制备过程中理化因子、微生物群落变化及风味形成规律[J].中国酿造,2022,41(5):52-59.DING W,WEI S S,YAN Y F,et al.Changes of physicochemical factors,microbial community and flavor formation in the preparation process of Shanxi aged vinegar Daqu[J].China Brewing,2022,41(5):52-59.
[14] DU Y K,XIN W,XIA Y,et al.Analysis of fermentation control factors on volatile compounds of primary microorganisms in Jiang-flavor Daqu[J].Journal of Food Biochemistry,2022,46(10):e14277.
[15] MORENO-ARRIBAS M V,PUEYO E,POLO M C.Analytical methods for the characterization of proteins and peptides in wines[J].Analytica Chimica Acta,2002,458(1):63-75.
[16] 中华人民共和国工业和信息化部.QB/T 4257-2011 酿酒大曲通用分析方法[S].北京:中国轻工业出版社,2011.Ministry of Industry and Information Technology.QB/T 4257-2011 General methods of analysis for Daqu[S].Beijing:China Light Industry Press,2011.
[17] ROGNES T,FLOURI T,NICHOLS B,et al.VSEARCH:A versatile open source tool for metagenomics[J].PeerJ,2016,4:e2584.
[18] K LJALG U,NILSSON R,ABARENKOV K,et al.Towards a unified paradigm for sequence-based identification of fungi[M].Wiley Online Library.2013.
LJALG U,NILSSON R,ABARENKOV K,et al.Towards a unified paradigm for sequence-based identification of fungi[M].Wiley Online Library.2013.
[19] LABUZA T P,KAANANE A,CHEN J Y.Effect of temperature on the moisture sorption isotherms and water activity shift of two dehydrated foods[J].Journal of Food Science,1985,50(2):385-392.
[20] 龙树瑺,葛东颖,蔡文超,等.长治地区清香型大曲理化特性与细菌类群的关联性分析[J].食品工业科技,2023,44(17):115-120.LONG S C,GE D Y,CAI W C,et al.Correlation analysis between physicochemical characteristics and bacterial taxa of Fen-flavor Daqu in Changzhi area[J].Science and Technology of Food Industry,2023,44(17):115-120.
[21] 王俏,郭聃洋,王旭亮,等.中国白酒不同香型酒曲理化性能对比分析[J].酿酒科技,2015(6):6-10.WANG Q,GUO D Y,WANG X L,et al.Comparative analysis of physiochemical properties of Baijiu (liquor) starter of different flavor types[J].Liquor-Making Science &Technology,2015(6):6-10.
[22] ZHAO J Z,YANG Y,CHEN L Q,et al.Quantitative metaproteomics reveals composition and metabolism characteristics of microbial communities in Chinese liquor fermentation starters[J].Frontiers in Microbiology,2023,13:1098268.
[23] MARTINS S I F S,JONGEN W M F,VAN BOEKEL M A J S.A review of Maillard reaction in food and implications to kinetic modelling[J].Trends in Food Science &Technology,2000,11(9-10):364-373.
[24] WANG L.Research trends in Jiang-flavor Baijiu fermentation:From fermentation microecology to environmental ecology[J].Journal of Food Science,2022,87(4):1362-1374.
[25] ZHU C T,CHENG Y X,SHI Q L,et al.Metagenomic analyses reveal microbial communities and functional differences between Daqu from seven provinces[J].Food Research International,2023,172:113076.
[26] REN H W,SUN Y F,YANG Y F,et al.Unraveling the correlations between microbial communities and metabolic profiles of strong-flavor Jinhui Daqu with different storage periods[J].Food Microbiology,2024,121:104497.
[27] ZHANG Y D,XU J G,DING F,et al.Multidimensional profiling indicates the shifts and functionality of wheat-origin microbiota during high-temperature Daqu incubation[J].Food Research International,2022,156:111191.
[28] YI Z L,JIN Y L,XIAO Y,et al.Unraveling the contribution of high temperature stage to Jiang-flavor Daqu,a liquor starter for production of Chinese Jiang-flavor Baijiu,with special reference to metatranscriptomics[J].Frontiers in Microbiology,2019,10:472.
[29] FAN G S,FU Z L,TENG C,et al.Effects of aging on the quality of roasted sesame-like flavor Daqu[J].BMC Microbiology,2020,20(1):67.
[30] CHEN T Y,WANG H Y,SU W,et al.Analysis of the formation mechanism of volatile and non-volatile flavor substances in corn wine fermentation based on high-throughput sequencing and metabolomics[J].Food Research International,2023,165:112350.
[31] CAI W C,XUE Y A,WANG Y R,et al.The fungal communities and flavor profiles in different types of high-temperature Daqu as revealed by high-throughput sequencing and electronic senses[J].Frontiers in Microbiology,2021,12:784651.
[32] ZHU Q,CHEN L Q,PU X X,et al.The differences in the composition of Maillard components between three kinds of sauce-flavor Daqu[J].Fermentation,2023,9(9):860.
[33] LI H,HUANG J,LIU X P,et al.Characterization of interphase microbial community in Luzhou-flavored liquor manufacturing pits of various ages by polyphasic detection methods[J].Journal of Microbiology and Biotechnology,2017,27(1):130-140.
[34] REN T T,SU W,MU Y C,et al.Study on the correlation between microbial communities with physicochemical properties and flavor substances in the Xiasha round of cave-brewed sauce-flavor Baijiu[J].Frontiers in Microbiology,2023,14:1124817.
[35] ZHANG M Z,WU X F,MU D D,et al.Profiling the influence of physicochemical parameters on the microbial community and flavor substances of Zaopei[J].Journal of the Science of Food and Agriculture,2021,101(15):6300-6310.
[36] WANG Y R,XIANG F S,ZHANG Z D,et al.High-throughput sequencing-based analysis of fungal diversity and taste quality evaluation of Douchi,a traditional fermented food[J].Food Science &Nutrition,2020,8(12):6612-6620.
[37] CAI W C,XUE Y A,TANG F X,et al.The depth-depended fungal diversity and non-depth-depended aroma profiles of pit mud for strong-flavor Baijiu[J].Frontiers in Microbiology,2022,12:789845.
[38] LI J,WU J,XU N F,et al.Dynamic evolution and correlation between microorganisms and metabolites during manufacturing process and storage of Pu-erh tea[J].LWT,2022,158:113128.