鱼糜制品因其丰富营养、独特风味等特点备受消费者的青睐。鱼糜在加工过程中,漂洗工序除去了鱼肉中的健康脂质组分,以提高鱼糜在冷冻期间的贮存稳定性和品质[1]。而脂质对鱼糜制品的营养和风味的改善起着重要作用,因此工业生产中常通过添加外源性油脂来提升鱼糜制品的品质。随着健康饮食概念的传播,越来越多的消费者开始减少富含饱和脂肪酸的动物油脂的摄入量。因此用不饱和脂肪含量高的植物油取代动物油脂用于生产更健康的鱼糜产品成为近年来的流行趋势[2],但鱼糜制品中直接添加外源性油脂也存在油脂氧化变质、凝胶性能下降等品质问题[3-4]。
Pickering乳液是由纳米颗粒稳定的乳液。纳米颗粒吸附在Pickering乳液液滴的油水界面,通过空间位阻抑制液滴凝聚,从而稳定乳液。与传统乳液相比,Pickering乳液具有更好的贮存稳定性、加热稳定性和冻融稳定性[5],而利用Pickering乳液作为鱼糜等肉制品中的脂肪替代物的研究也逐渐成为热点。WANG等[6]的研究表明天然淀粉稳定的Pickering乳液促进了肌原纤维蛋白凝胶的氢键和疏水相互作用,使凝胶网络结构更紧密,提升了凝胶强度和保水性。CEN等[7]的研究表明用藜麦蛋白基稳定的Pickering乳液显著降低了鱼糜凝胶的凝固点,显著提高了肌原纤维蛋白凝胶的冻融稳定性。CAO等[8]的研究表明用大豆蛋白稳定的Pickering乳液可以增强肌原纤维蛋白凝胶的持水性,同时抑制油脂氧化。
肌原纤维蛋白(myofibrillar protein,MP)是肌肉组织中最丰富的蛋白质,是提供优异的水结合能力、凝胶形成能力和乳化性能的主要蛋白质[9]。MP的良好性能为其开发成为食品级Pickering乳液的稳定剂提供了基础。MP属于盐溶性蛋白,而在水溶液或低离子强度溶液中,单体肌球蛋白会通过静电吸引组装和聚集形成高度有序的肌丝结构从而限制MP的功能特性[10]。此外过量的钠摄入会引起多种慢性疾病,如高血压和心血管疾病[11]。因此通过改性方法开发低盐或无盐环境下的MP乳液是目前研究的趋势。其中ZHAO等[12]通过研究海藻酸钠与MP的相互作用发现,海藻酸钠的加入增强了MP低盐环境下分子间静电斥力,有效阻止了蛋白质聚集,同时随着海藻酸钠添加浓度的增加MP乳化性能提高。LAN等[13]的研究表明超声波处理能够改变低盐溶液中MP的二级结构和三级构象,提高MP的溶解度和乳化特性。SUN等[14]通过热处理结合微射流处理MP 制备微凝胶颗粒,结果表明相比于天然MP,微凝胶颗粒具有更小的颗粒尺寸和更好的两亲性,同时颗粒在油水界面具有更快的扩散速率,具有更好的界面性能。
本文通过不同温度条件下的超声微波协同处理以改善无盐条件下的内源性MP油水界面特性,并以MP颗粒为Pickering稳定剂包裹亚麻籽油构建MP基Pickering乳液,进一步探究MP基Pickering乳液对鱼糜凝胶品质的影响。研究结果可为MP基Pickering乳液在鱼糜制品工业化应用中提供一定的理论依据。
1 材料与方法
1.1 材料与试剂
鮸鱼鱼糜(AAA级),舟山兴业有限公司;亚麻籽油(特级),益海嘉里金龙鱼粮油食品股份有限公司;其余试剂均为分析级,上海阿拉丁生物科技有限公司。
1.2 仪器与设备
IKA25高速剪切机,德国IKA有限公司;BILON-CW-1000 超声微波催化合成仪,上海比朗仪器制造有限公司;CR 22 N高速离心机,日本Hitachi公司;Spark20M酶标仪,瑞士Tecan公司;Nicolet iS20红外光谱仪,美国Thermo Fisher Scientific公司;AXR激光共聚焦显微镜,日本Nikon公司;Color Quest XE色差仪,美国Hunter Lab公司;TA-XTplusC质构仪,英国Stable Micro System公司。
1.3 实验方法
1.3.1 肌原纤维蛋白的提取
肌原纤维蛋白提取参考HUANG等[15]方法并稍作修改,冷冻鮸鱼鱼糜4 ℃环境下解冻,与4倍体积缓冲液A(0.1 mol/L NaCl,20 mmol/L K2HPO4/KH2PO4,2 mmol/L MgCl2,1 mmol/L EDTA,pH=7)混合,8 000 r/min剪切30 s后4 ℃ 10 000×g 下离心15 min,再取沉淀与6倍体积缓冲液B(0.6 mol/L NaCl,20 mmol/L K2HPO4/KH2PO4,pH=7)混合,6 000 r/min下剪切30 s,在4 ℃环境下浸提2 h后4 ℃ 3 000×g下离心15 min,离心后取上清液,用4层纱布过滤,滤液与10倍体积4 ℃去离子水混合后,在4 ℃ 16 000×g下离心10 min获得沉淀物,即为肌原纤维蛋白。
1.3.2 超声微波改性肌原纤维蛋白颗粒的制备
将提取的肌原纤维蛋白分散在去离子水中,控制蛋白质量浓度为15 mg/mL。未处理的肌原纤维蛋白悬浊液记为Control组。另将4组40 mL蛋白质量浓度为15 mg/mL的肌原纤维蛋白悬浮液,分别通过超声微波催化合成仪设置不同温度(40、50、60、70 ℃)进行超声微波协同处理,控制超声功率为200 W,微波功率为5 W/g,处理时间为10 min,处理后的蛋白液分别记为40 ℃-UM-MP组、50 ℃-UM-MP组、60 ℃-UM-MP组和70 ℃-UM-MP组。
1.3.3 蛋白颗粒表面疏水性的测定
采用溴酚蓝法测定样品的表面疏水性[16]。各组蛋白颗粒稀释至1 mg/mL 加入1/10体积的溴酚蓝水溶液(bromophenol blue,BPB 1 mg/mL),涡旋10 min后,8 000×g离心15 min,取上清液0.4 mL用去离子水稀释至4 mL,振荡混匀后于595 nm测定样品吸值。其中空白组用去离子水替代蛋白样品。每组样品平行测定3次。表面疏水性由BPB结合量来表示,计算如公式(1)所示:
BPB结合量![]()
(1)
式中:A0代表空白组吸光值,AS代表样品吸光值。
1.3.4 傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)的测定
冷冻干燥48 h的样品使用FTIR仪ATR模式分析样品,光谱在波数范围 4 000~400 cm-1,定量分析了酰胺Ⅰ带(1 700~1 600 cm-1)蛋白质样品的二级结构变化,用PeakFit v4.12进行了峰拟合计算。
1.3.5 Pickering乳液的制备
将Control组、40 ℃-UM-MP组、50 ℃-UM-MP组、60 ℃-UM-MP组、70 ℃-UM-MP组蛋白分别以体积比1∶1混合亚麻籽油,再用高速剪切机10 000 r/min剪切2 min形成Control组、40 ℃-UM-PE组、50 ℃-UM-PE组、60 ℃-UM-PE组和70 ℃-UM-PE组Pickering乳液。
1.3.6 乳液界面吸附蛋白含量测定
乳液界面蛋白吸附含量(adsorbed protein,AP)采用离心法测定并稍作修改[17],将各组乳液15 000×g离心30 min后,油滴和吸附的蛋白质在离心管顶部分离成奶油层,水相沉淀到底部。然后用注射器小心吸取水相,用双缩脲法测定水相中蛋白质浓度。每组样品平行测定3次。通过公式(2)计算得出AP:
(2)
式中:C0为用于制备乳液的蛋白溶液的初始蛋白质浓度,CS为离心后水相中蛋白质浓度。
1.3.7 乳液微观结构观察
用尼罗红(1 mg/mL,溶于乙醇)对亚麻籽油进行荧光染色,激发波长位于561 nm。用异硫氰酸荧光素(1 mg/mL,溶于二甲基亚砜)对处理后的蛋白液进行荧光染色,激发波长位于488 nm。亚麻籽油和蛋白液用高速剪切机10 000 r/min剪切2 min均质后形成乳液,再用激光共聚焦显微镜观察乳液的微观结构。
1.3.8 鱼糜凝胶的制备
将冷冻鱼糜在4 ℃下解冻12 h,各称取5组250 g鱼糜加入预冷好的斩拌机中,每组鱼糜斩拌30 s,加入5 g NaCl,并分别添加Control组、40 ℃-UM-PE组、50 ℃-UM-PE组、60 ℃-UM-PE组、70 ℃-UM-PE组乳液,控制添加量为8 mL/100 g并调节水分含量至78%。然后在冰浴条件下斩拌5 min(斩拌20 s,停20 s防止过热),斩拌好的鱼糜灌入肠衣中,经过2段加热(40 ℃,120 min;90 ℃,30 min)形成凝胶,随后立即冰水浴冷却,冷却后于4 ℃冰箱贮存备用。各组鱼糜凝胶分别记为Control组、40 ℃-UM-SG组、50 ℃-UM-SG组、60 ℃-UM-SG组和70 ℃-UM-SG组。
1.3.9 鱼糜凝胶白度的测定
采用手持式色差仪对室温平衡后的鱼糜凝胶进行白度的测定,记录L*(亮度)、a*(红色/绿色)、b*(黄色/蓝色)值,每组样品平行测定10次。
凝胶白度(whiteness,W)根据公式(3)计算:
(3)
1.3.10 鱼糜凝胶的凝胶强度测定
将鱼糜凝胶切成22 mm×20 mm的圆柱体在室温下平衡30 min,用质构仪测定凝胶强度。探头型号P/5S,参数设定:测前速度1 mm/s;测试速度2 mm/s;测后速度10 mm/s;位移15 mm;触发力10 g。每组样品平行测定15次。
1.3.11 鱼糜凝胶持水性(water holding capacity,WHC)的测定
参考XUE等[18]的方法并稍作修改,将各组鱼糜凝胶切成大小一致的小块称取质量m1(约3 g)鱼糜凝胶用3层滤纸包裹,放入50 mL离心管中,10 000×g离心15 min,记录离心后鱼糜凝胶的质量m2。每组样品平行测定3次,凝胶持水性计算如公式(4)所示:
(4)
1.4 数据统计与分析
各实验平行重复3次以上。数据利用SPSS Statistics 25软件进行单因素方差分析,Duncan’s多重比较方法分析差异显著性(P<0.05表示差异显著)。采用Origin 2021软件绘图。
2 结果与分析
2.1 不同温度超声微波协同改性对MP颗粒表面疏水性的影响
蛋白质的表面疏水性与其表面疏水基团的含量、结构和分布有关,可以反映疏水基团的暴露程度,同时表面疏水性对蛋白质的乳化能力起着重要作用[19]。不同温度下超声微波协同改性的MP颗粒表面疏水性变化如图1所示,相比Control组,MP颗粒的表面疏水性均显著提升(P<0.05),且温度上升(40~70 ℃)对MP颗粒的疏水性有增强作用。其中40 ℃-UM-MP组表面疏水性相比Control组提升50.8%,而70 ℃-UM-MP组提升277.6%。肌球蛋白是MP中的主要功能蛋白,超声波的空化和物理剪切作用会导致肌动蛋白构象被破坏,降解为重链肌球蛋白,使其包裹在内的疏水基团暴露[20],从而增强MP颗粒的表面疏水性。在较低温度(40 ℃)时,肌球蛋白头部疏水区域开始暴露,而在较高温度时(60 ℃、70 ℃)肌球蛋白尾部结构也逐渐展开,暴露出内部疏水基团,较高的温度有助于肌球蛋白更快地展开[21-22]。此外,微波的电磁场也会改变MP的内部电荷场,破坏肽链间的静电相互作用,可能增强蛋白质的表面疏水性[21]。
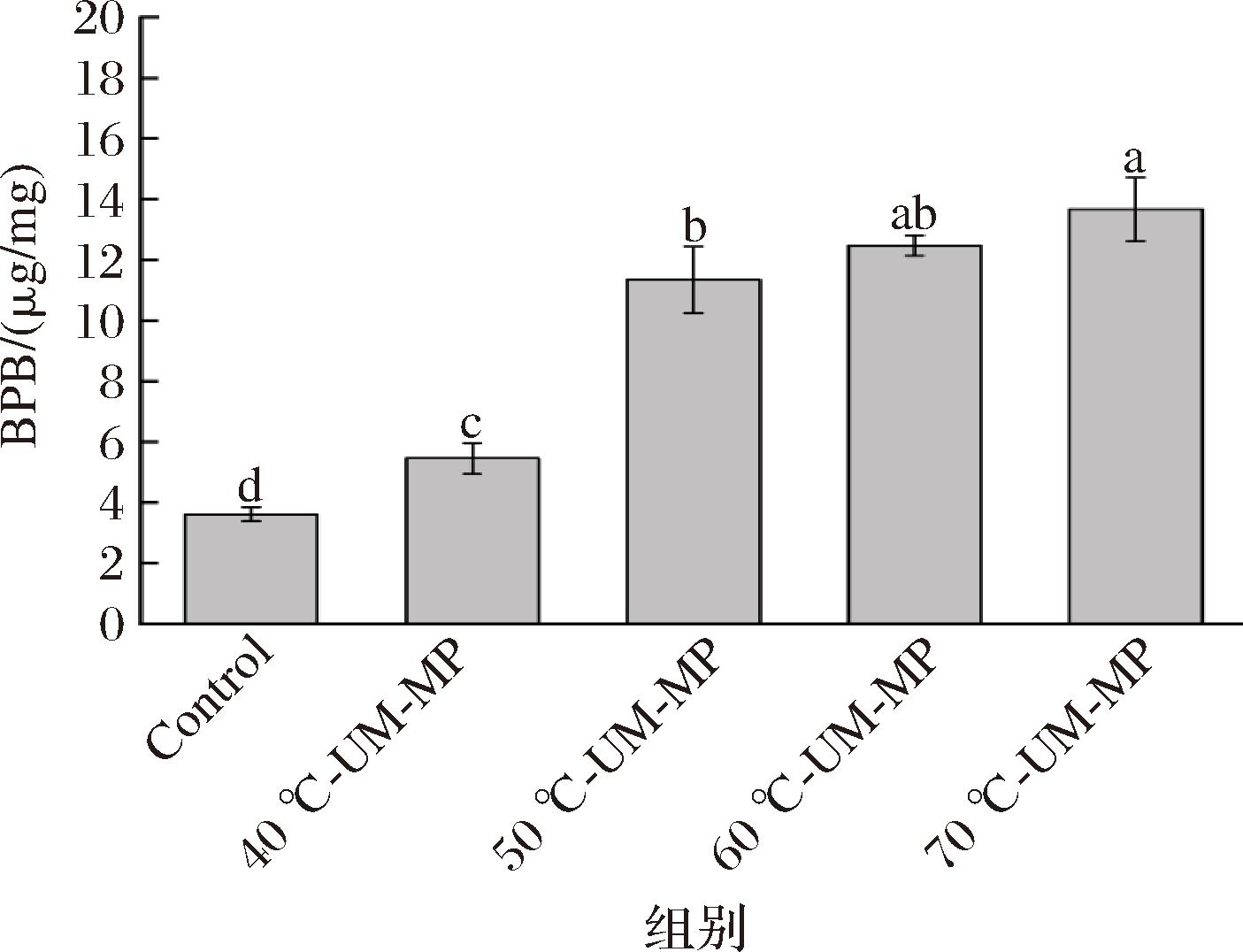
图1 不同温度超声微波协同改性对MP颗粒表面疏水性的影响
Fig.1 Effect of ultrasonic-microwave synergistic modification at different temperature on the surface hydrophobicity of MP particles
注:图中不同小写字母代表组别间差异显著(P<0.05)(下同)。
2.2 不同温度超声微波协同改性对MP颗粒二级结构的影响
乳液的界面特性与蛋白质二级结构的变化密切相关[23]。图2是不同温度超声微波协同改性MP颗粒的FTIR图和蛋白二级结构的含量分布。由图2-a可知,改性蛋白组酰胺A段特征峰发生红移,这说明改性处理可能使MP分子发生一定的聚集,N—H和O—H中的氢键等相互作用增强。而较高温度改性蛋白组(50~70 ℃)酰胺Ⅱ带发生蓝移且吸收峰强度有所增强,说明处理过程促进了MP中氨基(—NH2)的自交联反应[19]。由图2-b可知,改性后蛋白构象发生变化,其中60 ℃-UM-MP组和70 ℃-UM-MP组的α-螺旋和β-折叠总含量较其他组更高,说明较高改性温度诱导界面蛋白从无序结构转变为有序结构,有利于形成致密和刚性的界面蛋白膜[23]。同时改性蛋白组α-螺旋含量均高于Control组,有利于蛋白质与油相的有效相互作用,而较高改性温度组β-折叠含量的增加,可能反映了相邻MP分子之间较强的相互作用并聚集形成了结构更强的凝胶状界面层,有利于提升乳液稳定性[24]。
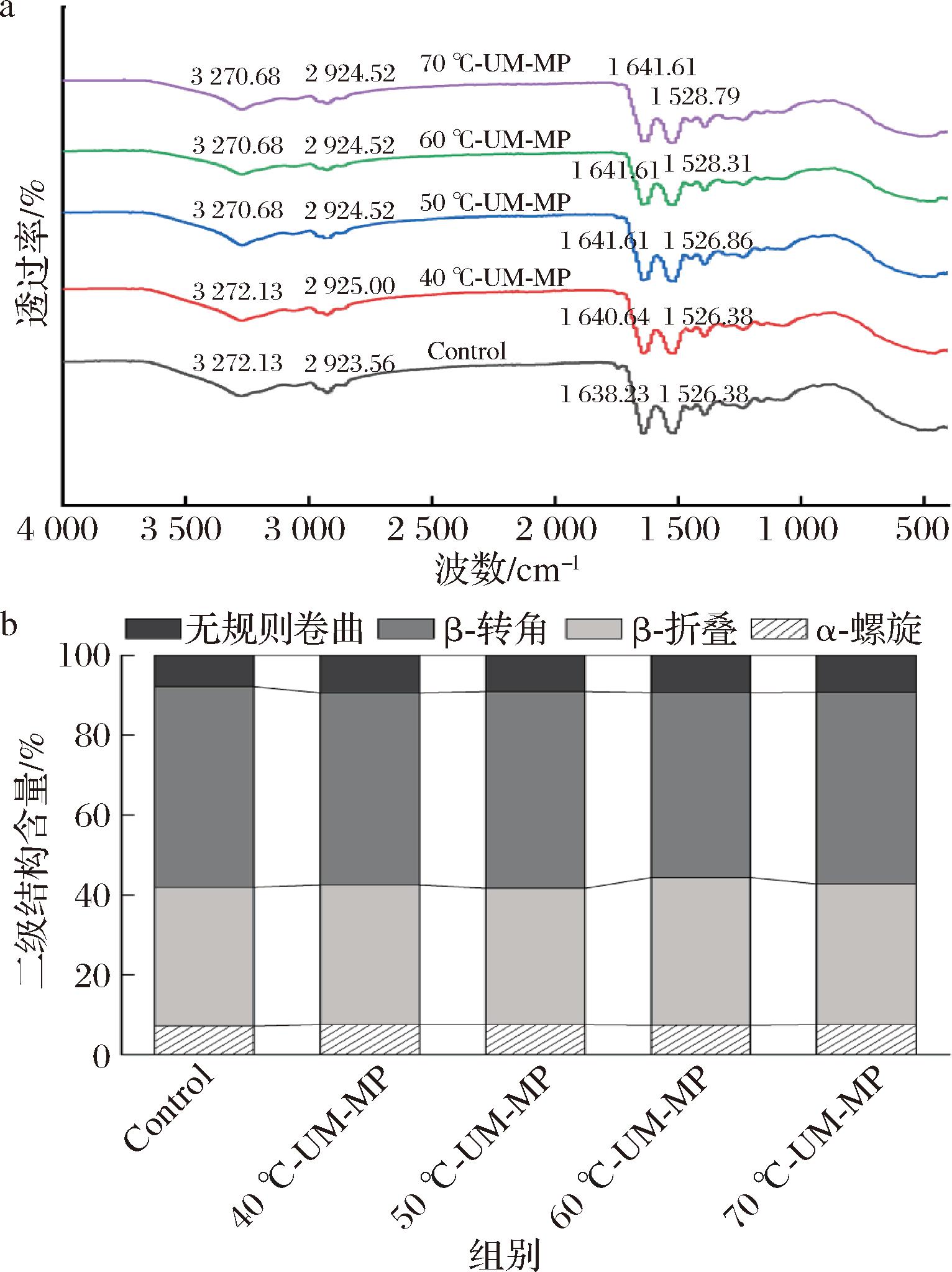
a-MP颗粒FTIR图;b-MP二级结构含量分布
图2 不同温度超声微波协同改性的MP颗粒FTIR图和MP二级结构含量分布
Fig.2 FTIR spectra of MP particles synergistically modified by ultrasound microwave at different temperature and secondary structure content distribution of MP particles
2.3 改性MP基Pickering颗粒对乳液界面吸附蛋白含量的影响
界面蛋白吸附量越大越能形成稳定的界面膜,从而形成屏障阻碍油滴间的聚集,使乳液更稳定[25]。如图3所示,改性MP颗粒制备的Pickering乳液其界面蛋白吸附量相比Control组均显著上升(P<0.05),且随处理温度的上升呈增加趋势。较高改性温度能更好地诱导MP构象展开,导致内部结合位点更多暴露。从而增强了MP颗粒间的相互作用,使得乳液界面蛋白吸附量增加。同时根据表面疏水性结果可知,超声微波协同处理使MP颗粒疏水基团暴露,从而增强了MP颗粒与油相的相互作用,使MP颗粒更稳定地吸附在油滴表面,从而提升乳液界面蛋白吸附量[19]。
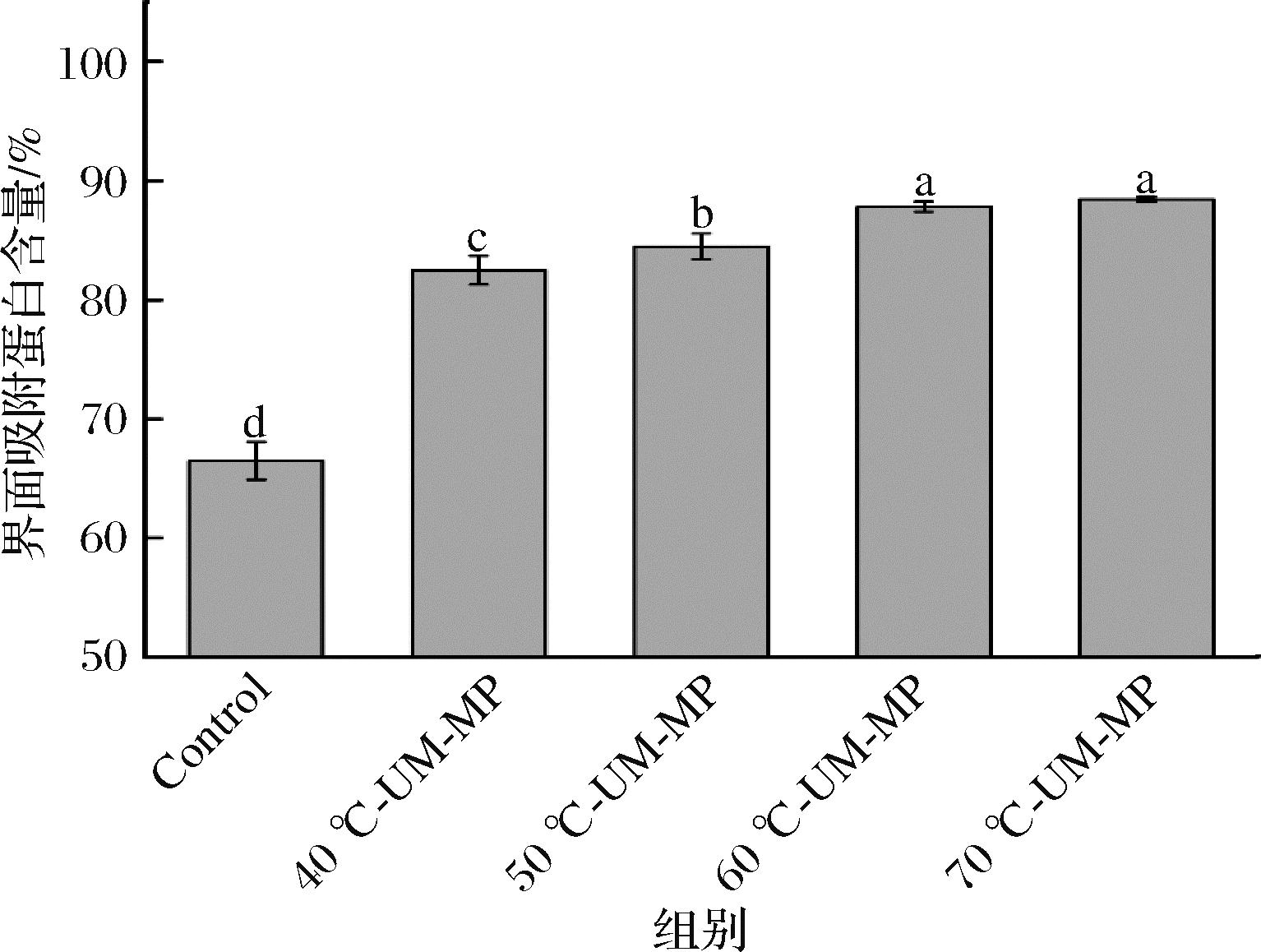
图3 改性MP基Pickering颗粒对乳液界面吸附蛋白含量的影响
Fig.3 Effect of modified MP-based Pickering particles on adsorbed protein content at the emulsion interface
2.4 改性MP基Pickering乳液的微观结构
图4为修饰改性的MP基所制备乳液的微观结构,其中红色为油滴,绿色为蛋白颗粒。Control组乳液中油滴不规则分布,吸附在油水界面的蛋白颗粒数量较少且形成的界面膜并不完整。与对照组相比,40 ℃-UM-PE组和50 ℃-UM-PE组油滴形状为圆形,分布较均匀,且油滴表面均有较多蛋白吸附,形成清晰完整的界面蛋白膜,证明超声微波改性对MP颗粒界面特性具有改善作用。60 ℃-UM-PE组和70 ℃-UM-PE组中乳液油滴表面的蛋白膜厚度尺寸明显增大,表明较高温度的超声微波处理可以提高MP颗粒的乳化能力,界面能够吸附较多蛋白质,与图3结果相符。同时60 ℃-UM-PE组和70 ℃-UM-PE组乳液液滴间的空间更为紧凑,乳液间可见部分蛋白桥接现象,有助于提高乳液的稳定性。
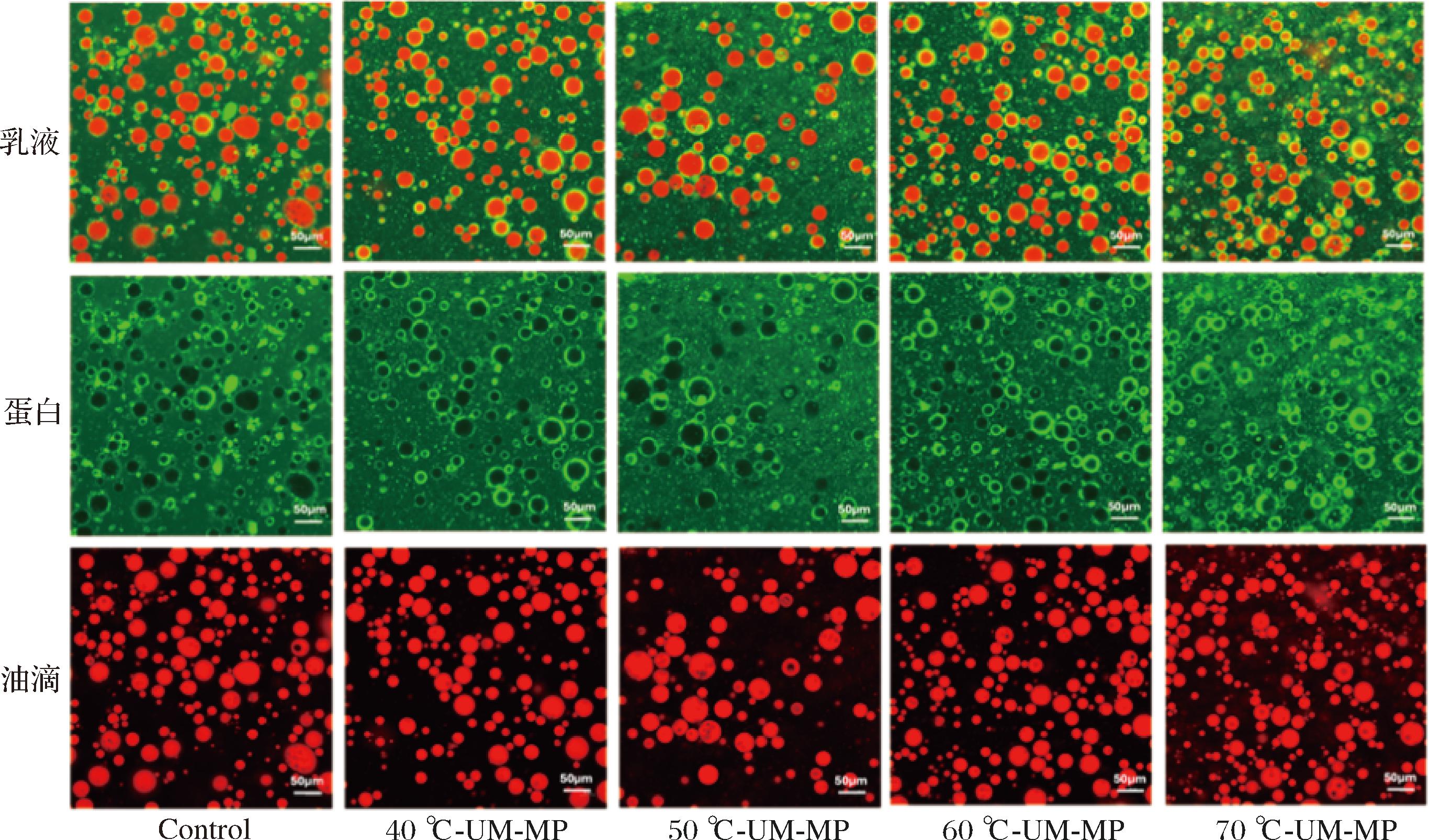
图4 改性MP基Pickering乳液的微观结构
Fig.4 Microstructure of modified MP-based Pickering emulsion
2.5 改性MP基Pickering乳液对鱼糜凝胶白度的影响
白度是鱼糜制品外观的重要参数,会影响消费者对产品的接受度。蛋白质凝胶的颜色变化主要与蛋白质的氧化变性、聚合程度、凝胶的持水性和表面的光学特性有关[26]。改性MP基Pickering乳液对鱼糜凝胶制品白度的影响如表1所示。结果表明60 ℃-UM-SG组和70 ℃-UM-SG组相比其他组,白度值有显著增加(P<0.05)。这可能因为较高改性温度的MP具有更好的界面吸附能力,可以更好地包裹黄色油滴,同时在鱼糜凝胶蒸煮过程中具有更好的热稳定性,最终使鱼糜凝胶制品有更高的白度值。此外可能是60 ℃-UM-SG组和70 ℃-UM-SG组具有更致密的蛋白质凝胶结构,增强了凝胶表面的光散射效应,从而增加凝胶的白度[26]。
表1 改性MP基Pickering乳液对鱼糜凝胶白度的影响
Table 1 Effect of modified MP-based Pickering emulsions on whiteness of surimi gel products
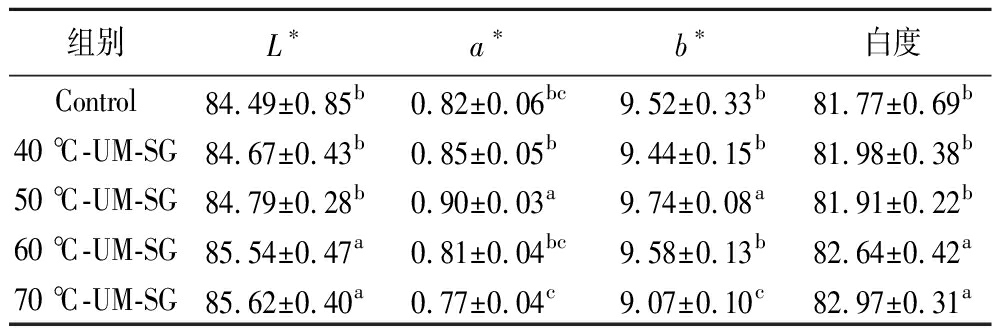
组别L∗a∗b∗白度Control84.49±0.85b0.82±0.06bc9.52±0.33b81.77±0.69b40 ℃-UM-SG84.67±0.43b0.85±0.05b9.44±0.15b81.98±0.38b50 ℃-UM-SG84.79±0.28b0.90±0.03a9.74±0.08a81.91±0.22b60 ℃-UM-SG85.54±0.47a0.81±0.04bc9.58±0.13b82.64±0.42a70 ℃-UM-SG85.62±0.40a0.77±0.04c9.07±0.10c82.97±0.31a
注:图中不同小写字母代表组别间差异显著(P<0.05)(下同)。
2.6 改性MP基Pickering乳液对鱼糜凝胶制品凝胶强度的影响
改性MP基Pickering乳液对鱼糜制品凝胶强度的影响如图5所示。与对照组相比,改性MP基Pickering乳液显著增加了鱼糜凝胶强度(P<0.05),且凝胶强度与改性温度基本呈正相关。原因可能是改性温度的提高有利于MP颗粒在油水界面形成更高机械强度的界面层[26]。DAI等[27]的研究也表明MP微凝胶热处理强度的提升可以提高乳液的稳定性,使界面膜从纯刚性结构转变为高机械强度的黏弹性结构,最终形成一个多层网络结构体系。此外可能是改性MP基Pickering乳液本身具有良好的黏弹性,充当了鱼糜凝胶网络结构中的活性填充物[28],增强了鱼糜凝胶的致密性,从而提高凝胶强度。同时鱼糜加热过程中,乳液界面MP颗粒可以通过二硫键和疏水相互作用与鱼糜肌原纤维蛋白结合[29],加强了鱼糜凝胶中蛋白质分子之间的交联,从而增强鱼糜凝胶的凝胶强度。
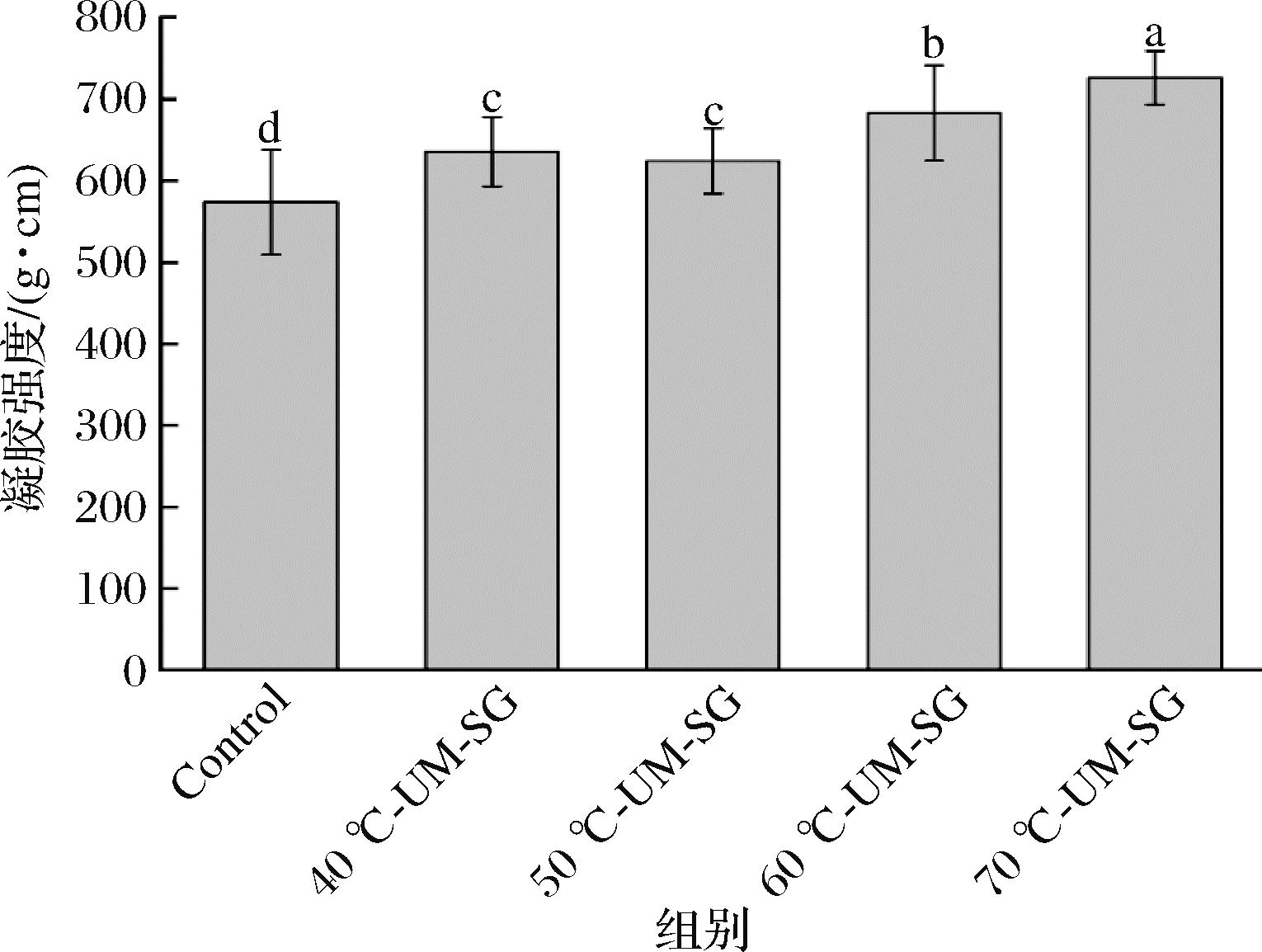
图5 改性MP基Pickering乳液对鱼糜凝胶制品凝胶强度的影响
Fig.5 Effect of modified MP-based Pickering emulsion on gel strength of surimi gel products
2.7 改性MP基Pickering乳液对鱼糜凝胶制品持水性的影响
WHC是鱼糜凝胶制品食用品质的关键因素,与多汁性和柔软度密切相关[8]。改性MP基Pickering乳液对鱼糜凝胶制品持水性的影响如图6所示。相比Control组,添加改性MP基Pickering乳液的WHC显著提高(P<0.05),且随处理温度的上升有提高趋势。前述结果也表明较高改性温度的MP基Pickering乳液对鱼糜凝胶结构具有改善作用,而良好的凝胶结构可以有效固定凝胶网络中的水[8],从而使得持水性增强。
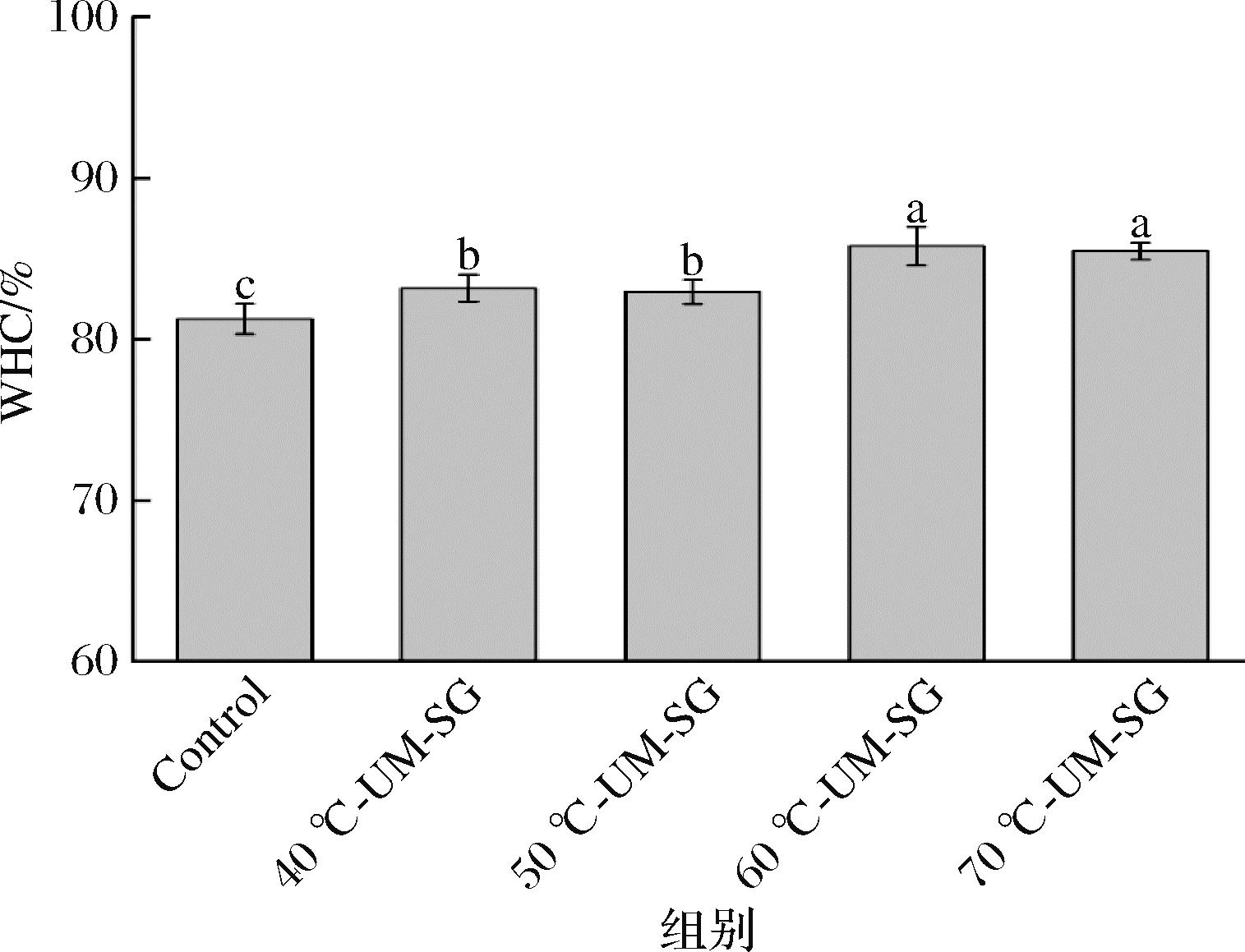
图6 改性MP基Pickering乳液对鱼糜凝胶制品持水性的影响
Fig.6 Effect of modified MP-based Pickering emulsion on water holding capacity of surimi gel products
3 结论
不同温度超声微波协同改性处理通过各自物理效应及热效应,诱导了蛋白质构象改变,导致活性基团与疏水基团暴露,从而增强MP颗粒疏水相互作用。同时乳液界面蛋白吸附能力显著增大,其微观结构也更为致密完整。此外,改性MP基Pickering乳液添加对鱼糜凝胶色泽、凝胶强度和持水性也具有显著改善作用。
[1] 宋春勇,洪鹏志,周春霞,等.负载白藜芦醇的红花籽油乳液对金线鱼鱼糜凝胶品质的影响[J].食品科学,2022,43(24):102-109.SONG C Y,HONG P Z,ZHOU C X,et al.Effect of safflower seed oil emulsion loaded with resveratrol on the quality of Nemipterus virgatus surimi gel[J].Food Science,2022,43(24):102-109.
[2] BOLGER Z,BRUNTON N P,MONAHAN F J.Impact of inclusion of flaxseed oil (pre-emulsified or encapsulated) on the physical characteristics of chicken sausages[J].Journal of Food Engineering,2018,230:39-48.
[3] GANI A,BENJAKUL S,NUTHONG P.Effect of virgin coconut oil on properties of surimi gel[J].Journal of Food Science and Technology,2018,55(2):496-505.
[4] SHI L,WANG X F,CHANG T,et al.Effects of vegetable oils on gel properties of surimi gels[J].LWT-Food Science and Technology,2014,57(2):586-593.
[5] ZHU X F,ZHANG N,LIN W F,et al.Freeze-thaw stability of Pickering emulsions stabilized by soy and whey protein particles[J].Food Hydrocolloids,2017,69:173-184.
[6] WANG Q L,LUAN Y,TANG Z W,et al.Consolidating the gelling performance of myofibrillar protein using a novel OSA-modified-starch-stabilized Pickering emulsion filler:Effect of starches with distinct crystalline types[J].Food Research International,2023,164:112443.
[7] CEN K Y,YU X,GAO C C,et al.Effects of different vegetable oils and ultrasonicated quinoa protein nanoparticles on the rheological properties of Pickering emulsion and freeze-thaw stability of emulsion gels[J].Journal of Cereal Science,2021,102:103350.
[8] CAO M M,ZHANG X C,ZHU Y Q,et al.Enhancing the physicochemical performance of myofibrillar gels using Pickering emulsion fillers:Rheology,microstructure and stability[J].Food Hydrocolloids,2022,128:107606.
[9] AMIRI A,SHARIFIAN P,MORAKABATI N,et al.Modification of functional,rheological and structural characteristics of myofibrillar proteins by high-intensity ultrasonic and papain treatment[J].Innovative Food Science &Emerging Technologies,2021,72:102748.
[10] GAO X,XIE Y R,YIN T,et al.Effect of high intensity ultrasound on gelation properties of silver carp surimi with different salt contents[J].Ultrasonics Sonochemistry,2021,70:105326.
[11] WANG J,HUANG X H,ZHANG Y Y,et al.Effect of sodium salt on meat products and reduction sodium strategies:A review[J].Meat Science,2023,205:109296.
[12] ZHAO N,ZOU H N,SUN S,et al.The interaction between sodium alginate and myofibrillar proteins:The rheological and emulsifying properties of their mixture[J].International Journal of Biological Macromolecules,2020,161:1545-1551.
[13] LAN M J,LI T S,LI L,et al.Ultrasonic treatment treated sea bass myofibrillar proteins in low-salt solution:Emphasizing the changes on conformation structure,oxidation sites,and emulsifying properties[J].Food Chemistry,2024,435:137564.
[14] SUN Y,MA L,FU Y,et al.Fabrication and characterization of myofibrillar microgel particles as novel Pickering stabilizers:Effect of particle size and wettability on emulsifying capacity[J].LWT,2021,151:112002.
[15] HUANG J J,BAKRY A M,ZENG S W,et al.Effect of phosphates on gelling characteristics and water mobility of myofibrillar protein from grass carp (Ctenopharyngodon idellus)[J].Food Chemistry,2019,272:84-92.
[16] HU Y P,GAO Y F,SOLANGI I,et al.Effects of tea polyphenols on the conformational,functional,and morphological characteristics of beef myofibrillar proteins[J].LWT,2022,154:112596.
[17] ZHOU L,ZHANG W G,WANG J Y,et al.Comparison of oil-in-water emulsions prepared by ultrasound,high-pressure homogenization and high-speed homogenization[J].Ultrasonics Sonochemistry,2022,82:105885.
[18] XUE S W,YANG H J,LIU R,et al.Applications of high pressure to pre-rigor rabbit muscles affect the functional properties associated with heat-induced gelation[J].Meat Science,2017,129:176-184.
[19] CHEN Y F,SUN Y,MENG Y L,et al.Synergistic effect of microfluidization and transglutaminase cross-linking on the structural and oil-water interface functional properties of whey protein concentrate for improving the thermal stability of nanoemulsions[J].Food Chemistry,2023,408:135147.
[20] LI J,DAI Z C,CHEN Z H,et al.Improved gelling and emulsifying properties of myofibrillar protein from frozen shrimp (Litopenaeus vannamei) by high-intensity ultrasound[J].Food Hydrocolloids,2023,135:108188.
[21] CAO H W,JIAO X D,FAN D M,et al.Microwave irradiation promotes aggregation behavior of myosin through conformation changes[J].Food Hydrocolloids,2019,96:11-19.
[22] LI Y L,XU Y J,XU X L.Continuous cyclic wet heating glycation to prepare myofibrillar protein-glucose conjugates:A study on the structures,solubility and emulsifying properties[J].Food Chemistry,2022,388:133035.
[23] WU Y M,WU Y Y,XIANG H,et al.Emulsification properties and oil-water interface properties of L-lysine-assisted ultrasonic treatment in sea bass myofibrillar proteins:Influenced by the conformation of interfacial proteins[J].Food Hydrocolloids,2024,147:109405.
[24] LI L X,CHEN L,NING C,et al.L-arginine and L-lysine improve the physical stability of soybean oil-myosin emulsions by changing penetration and unfolding behaviors of interfacial myosin[J].Food Hydrocolloids,2020,98:105265.
[25] XIA T H,XUE C H,WEI Z H.Physicochemical characteristics,applications and research trends of edible Pickering emulsions[J].Trends in Food Science &Technology,2021,107:1-15.
[26] WANG H N,ZHANG J X,XU Y X,et al.Effects of chickpea protein-stabilized Pickering emulsion on the structure and gelling properties of hairtail fish myosin gel[J].Food Chemistry,2023,417:135821.
[27] DAI H J,SUN Y,FENG X,et al.Myofibrillar protein microgels stabilized high internal phase Pickering emulsions with heat-promoted stability[J].Food Hydrocolloids,2023,138:108474.
[28] KHALESI H,LU W,NISHINARI K,et al.New insights into food hydrogels with reinforced mechanical properties:A review on innovative strategies[J].Advances in Colloid and Interface Science,2020,285:102278.
[29] BUAMARD N,BENJAKUL S.Effect of ethanolic coconut husk extract and pre-emulsification on properties and stability of surimi gel fortified with seabass oil during refrigerated storage[J].LWT,2019,108:160-167.