酸枣为鼠李科枣属植物,又名山枣,是广泛分布于我国北方地区的特有野生果树[1]。随着功能性食品市场的迅速扩展,酸枣作为一种药食同源的水果,其营养价值和健康效益受到广泛关注,但由于酸枣果肉口感酸涩,常作为酸枣仁药材生产的副产物被丢弃。特别是近年,国内市场对酸枣仁药材需求增加,在生产过程中大量酸枣果肉被丢弃,造成严重的资源浪费并增加环境承载压力[2],而使酸枣果肉得到充分利用是解决这一问题的有效途径。酸枣果肉中含有多糖类、氨基酸和维生素等活性物质,具有抗氧化、调节免疫力等保健价值[3]。其中膳食纤维是重要的功能成分之一,能够改善人体营养状况,是以多糖类为主的高分子成分的总称,是继六大营养素之外的人体“第七营养素”。
膳食纤维根据其水溶性可分为可溶性膳食纤维(soluble dietary fiber,SDF)和不溶性膳食纤维(insoluble dietary fiber,IDF)[4]。膳食纤维在调节身体的生理功能方面起着重要作用[5],能降低患糖尿病和其他疾病的风险。研究表明,SDF比IDF具有更强的生理功能[6],IDF主要通过促进肠道蠕动来发挥其生理功能,SDF则具有更显著的调节肠道菌群、改善能量代谢等功能。然而,天然来源的SDF通常含量较低,例如豆渣中SDF在总膳食纤维中所占比例不足10%[7]。因此,通过有效的提取将IDF转化为SDF,成为提高膳食纤维功能特性的重要研究方向。
酶法可以通过特定的酶解反应,有效降解IDF增加SDF的含量。因此,本实验以酸枣果肉为原料,通过响应面法优化酶提取SDF的工艺,以获得较高的得率,再比较分析SDF和IDF的结构特征、理化性质和功能特性的差异。为SDF和IDF在功能性食品中的不同应用提供重要的理论依据,为其在食品工业和健康产品中的高附加值应用奠定基础。
1 材料与方法
1.1 材料与试剂
酸枣,山东元康农业发展有限公司;纤维素酶,上海源叶生物科技有限公司;其他实验试剂均为国产分析纯。
1.2 仪器与设备
Frontier FT-IR型傅立叶变换红外光谱仪,美国珀金埃尔默;DZF-6090真空干燥箱,精宏设备有限公司;TGA/DSC 3+同步热分析仪,瑞士Mettler公司;SmartLabSE智能多功能X射线衍射仪,日本Rigaku公司。
1.3 实验方法
1.3.1 酸枣膳食纤维的提取
称取34 g新鲜酸枣果肉,以料液比1∶3(g∶mL)加入蒸馏水搅匀。调节pH值,加入纤维素酶,50 ℃水浴提取一定时间后100 ℃灭酶10 min,抽滤。上清液浓缩加入4倍体积无水乙醇,4 ℃静置12 h,离心,沉淀60 ℃真空干燥,透析(Mw 1 000),冻干,得到SDF。滤渣充分水洗、醇洗后经真空干燥得到IDF。
1.3.2 响应面(Box-Behnken)实验设计
以纤维素酶含量(A)、pH(B)和提取时间(C)为自变量,以SDF的得率Y为响应值,利用Design-Expert 13软件设计三因素三水平的响应面实验,实验因素水平的选取如表1所示。
表1 响应面试验因素水平设计
Table 1 Factor level design of response surface test

水平因素A(纤维素酶含量)/(g/L)B(pH)C(时间)/min-154.5600105.0901155.5120
1.3.3 国标法测定膳食纤维含量
根据GB/T 37492—2019《粮油检验 谷物及其制品水溶性膳食纤维的测定 酶重量法》测定样品中膳食纤维含量。
1.3.4 膳食纤维的结构特性
1.3.4.1 扫描电子显微镜(scanning electron microscope,SEM)分析
取少量样品分布在导电胶上,镀金,载物台放入扫描电镜中,抽真空,在10 kV电子枪加速电压下观察并拍摄照片[8]。
1.3.4.2 傅里叶红外光谱(Fourier transform infrared spectroscopy,FT-IR)分析
样品与适量KBr充分混合,研磨并压成薄片,通过FT-IR光谱仪记录4 000~400 cm-1的吸收光谱图[9]。
1.3.4.3 酸枣膳食纤维分子质量
参考CHEN等[10]方法,称取SDF 10 mg溶于水,配成10 mg/mL样品溶液,过0.45 μm滤膜,得到待测样品溶液。采用高效液相色谱-蒸发光散射检测器(high performance liquid chromatography combined with evaporative light-scattering detector,HPLC-ELSD)测定SDF分子质量。流动相:水,流速1.0 mL/min;柱温25 ℃;ELSD+DAD设置条件:EvT 55 ℃、NeT 55 ℃;流速1.8 L/min;进样量10 μL。以不同分子质量的标准品为对照品绘制标准曲线计算分子质量。
1.3.4.4 酸枣膳食纤维单糖组成
参考CHEN等[10]方法,称取10 mg样品,110 ℃下SDF用2 mol/L三氟乙酸(trifluoroacetic acid,TFA)水解2.5 h,IDF水解3.5 h。旋蒸除去TFA后衍生,萃取,收集水相进行分析。使用配备YMC-Triart C18HPLC柱(4.6 mm × 250 mm)的Agilent 1260 HPLC系统,柱温30 ℃,进样量10 μL,紫外检测器波长为250 nm,流动相为0.1 mol/L磷酸盐缓冲液(pH 6.83)和乙腈按体积配比为82∶18,流速1 mL/min。
1.3.4.5 X-射线衍射(X-ray diffraction,XRD)图分析
取一定量干燥的样品在稳定的X射线下检测。测定条件:铜靶;管压40 kV;扫描范围5°~60°;扫描速度2°/min[11]。
1.3.4.6 热重分析
氮气气氛下,设置温度30~600 ℃,升温速率10 ℃/min,氮气流量50 mL/min[11]。
1.3.5 理化性质
1.3.5.1 持水力
参考LI等[12]方法,称取0.5 g样品,与30 mL蒸馏水混匀,静置24 h,SDF醇沉,离心(5 000 r/min、15 min),弃去上清液,滤纸擦去残留液体后收集沉淀物称重。持水力的计算如公式(1)所示:
持水力![]()
(1)
式中:M1,样品质量,g;M2,离心管质量,g;M3,沉淀物质量,g。
1.3.5.2 持油力
参考LI等[12]方法,称取0.5 g样品,与15 mL橄榄油混匀,静置24 h后离心(5 000 r/min、15 min),弃去上清液,滤纸擦去残留液体后收集沉淀物称重。持油力的计算如公式(2)所示:
持油力![]()
(2)
式中:M1,样品质量,g;M2,离心管质量,g;M3,沉淀物质量,g。
1.3.5.3 膨胀力
参考WANG等[13]方法,称取0.3 g样品于有刻度的玻璃试管中,记录干样体积,与15 mL蒸馏水摇匀,室温静置24 h,SDF醇沉,记录样品膨胀后体积。膨胀力的计算如公式(3)所示:
膨胀力![]()
(3)
式中:V1,样品干样的体积,mL;V2,样品膨胀后体积,mL;M1,样品质量,g。
1.3.6 葡萄糖吸附能力(glucose adsorption capability,GAC)
参考JIANG等[14]方法,称取0.1 g样品,加入不同质量浓度的葡萄糖溶液10 mL(0.2、0.4、0.6、0.8、1.0、1.2 mg/mL)混匀。37 ℃水浴反应5 h,离心取上清液,按DNS法测定葡萄糖含量,对照为未加入样品的葡萄糖溶液。GAC的计算如公式(4)所示:
(4)
式中:M0,葡萄糖溶液原质量,mg;M1,离心后上清液葡萄糖溶液质量,g;M,样品质量,g。
1.3.7 α-淀粉酶抑制能力
参考KARIMI等[15]方法,称取样品(0.02、0.04、0.06、0.08、0.10、0.12 g)与1.8 mL淀粉酶(2 U/mL)和0.9 mL淀粉溶液混合,90 ℃水浴2 h,离心取上清液0.3 mL,加入125 μL的DNS试剂,煮沸5 min,定容至5 mL,540 nm处测吸光度值。抑制率的计算如公式(5)所示:
α-淀粉酶抑制能力![]()
(5)
式中:A1,样品反应后的吸光度;A2,PBS代替淀粉酶与样品反应后的吸光度;A3,空白组反应后的吸光度;A4,空白组中PBS代替淀粉酶反应后的吸光度。
1.3.8 胆固醇吸附能力(cholesterol adsorption capacity,CAC)
参考LI等[12]方法,新鲜蛋黄按体积比加入9倍蒸馏水进行稀释,搅拌成蛋黄乳液。0.1 g样品与10 mL乳液混合,调节pH值至2和7,37 ℃水浴2 h后离心,按邻苯二甲醛法测定50 μL上清液中胆固醇含量。CAC的计算如公式(6)所示:
(6)
式中:M1,样品质量,g;C1,DF吸附后上清液中胆固醇含量,mg;C2,空白组上清液中胆固醇含量,mg。
1.4 数据处理
所有试验均重复3次,结果表示为平均值,采用IBM SPSS Statistics 27统计软件进行方差分析,P<0.05为具有显著性差异,Origin 2021软件进行绘图和Spearman相关性分析。
2 结果与分析
2.1 响应面优化试验
2.1.1 响应面优化试验结果
对表2数据进行二次回归分析,得到纤维素酶含量(A)、pH(B)和提取时间(C)三因素对SDF提取率(Y)影响的回归模型为:Y=13.68+1.08A+1.82B+0.837 5C+0.110 0AB-0.645 0AC+0.385 0BC-1.35A2-1.35B2+1.03C2。
表2 Box-Behnken 试验结果
Table 2 Box-Behnken test results
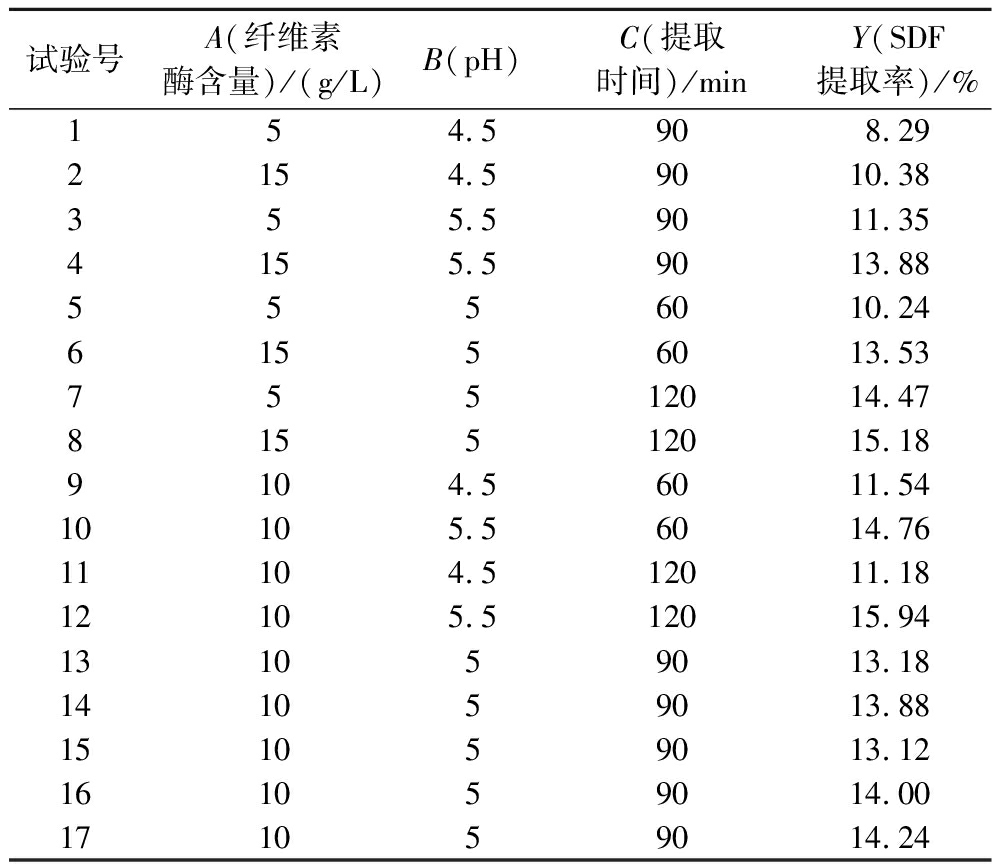
试验号A(纤维素酶含量)/(g/L)B(pH)C(提取时间)/minY(SDF提取率)/%154.5908.292154.59010.38355.59011.354155.59013.885556010.2461556013.5375512014.47815512015.189104.56011.5410105.56014.7611104.512011.1812105.512015.94131059013.18141059013.88151059013.12161059014.00171059014.24
由表3可知,该回归模型的P值为0.002 4,呈现极显著特征,失拟项为0.087 9(>0.05),不显著,表明所建立模型的回归方程有较好的拟合性,可以作为预测SDF优化提取工艺参数的模型。模型的相关系数R2=0.933 2,调整后的R2=0.847 4,表明模型与数据间存在强烈的相关性,模型拟合效果较好。方差分析结果显示,一次项A、B和C的P值小于0.05,表明这些因素对响应值有显著影响;二次项A2、B2和C2的P值小于0.05,表明这些二次效应对响应值也有显著影响。对比F值,三因素对响应值的影响主次顺序为pH>纤维素酶>时间。
表3 回归模型方差分析
Table 3 ANOVA of regression model
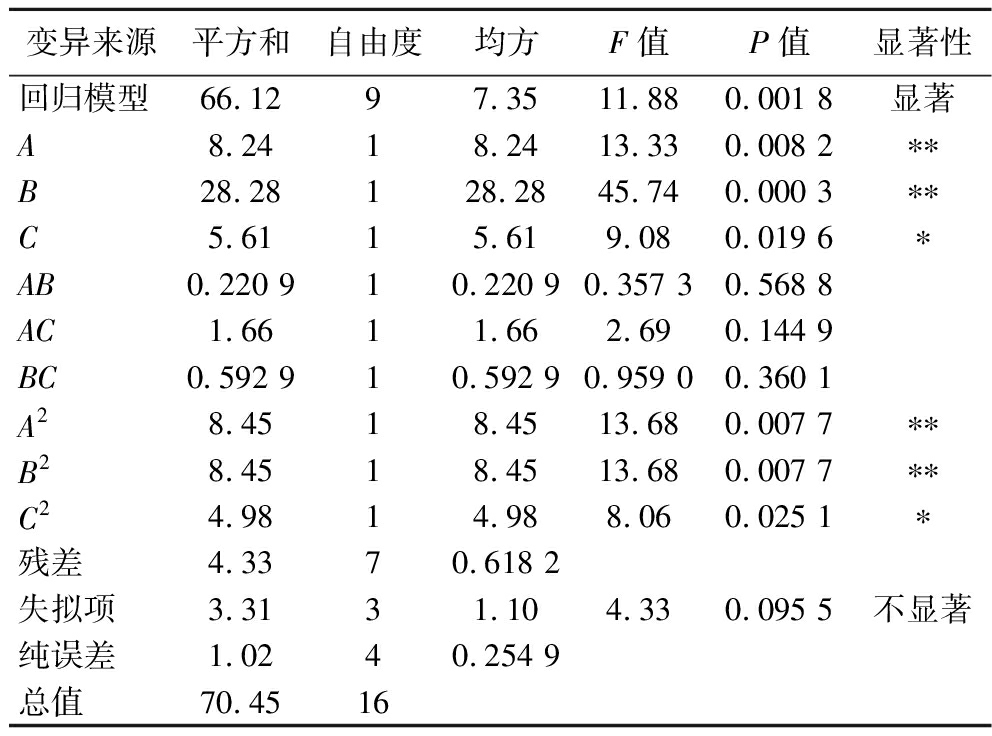
变异来源平方和自由度均方F值P值显著性回归模型66.1297.3511.880.001 8显著A8.2418.2413.330.008 2∗∗B28.28128.2845.740.000 3∗∗C5.6115.619.080.019 6∗AB0.220 910.220 90.357 30.568 8AC1.6611.662.690.144 9BC0.592 910.592 90.959 00.360 1A28.4518.4513.680.007 7∗∗B28.4518.4513.680.007 7∗∗C24.9814.988.060.025 1∗残差4.3370.618 2失拟项3.3131.104.330.095 5不显著纯误差1.0240.254 9总值70.4516
注:*P<0.05;**P<0.01。
2.1.2 响应面结果分析与模型验证
分析SDF提取中纤维素酶含量(A)、pH(B)和时间(C)3个变量对响应值的影响情况,两因素交互响应面3D图的趋势越陡,说明因素之间的交互作用越明显;响应面趋势越平缓,影响程度越不明显。如图1所示,在纤维素酶用量与pH交互图中,SDF提取率随着纤维素酶用量的增加呈现先上升后下降的趋势。当纤维素酶用量较小时,随着pH的增加,SDF提取率先大幅上升后下降;当纤维素酶用量较大时,随着pH的增加,SDF提取率先缓慢上升后下降,二者存在明显的交互作用对SDF得率的影响显著。大于纤维素酶用量与提取时间以及提取时间与pH的交互作用,这与表3中显著性分析的试验结果一致。
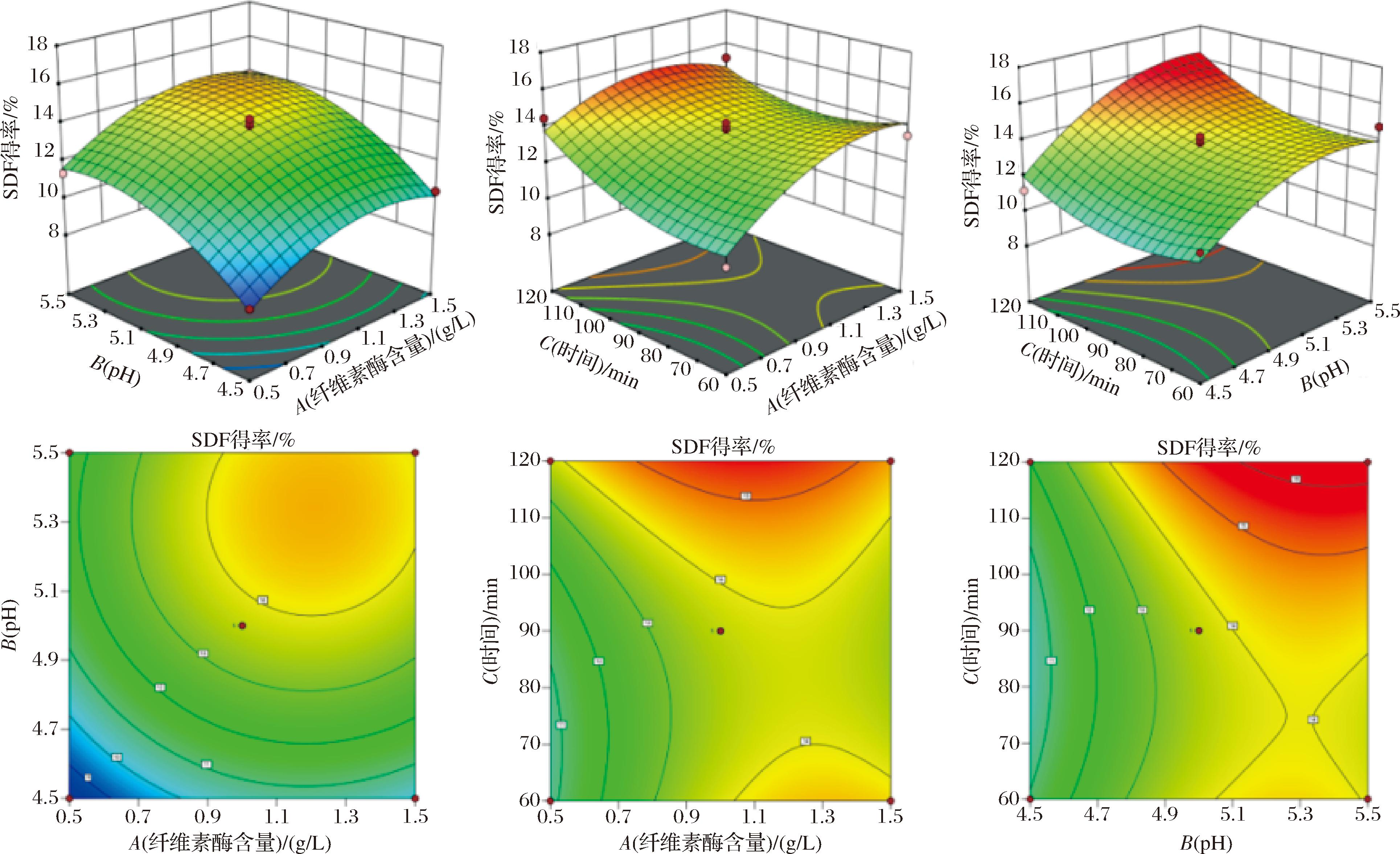
图1 各因素交互作用对SDF提取率的影响
Fig.1 Effect of each factor interaction on the extraction rate of SDF
根据响应面分析结果,SDF的最佳提取条件为纤维素酶用量10 g/L、pH 4.7、提取时间107 min。在此条件下,SDF得率最大预测值为12.77%,进行验证实验,并重复进行3次,平均得率为13.12%,与预测值无显著差异。结果表明,响应面优化实验是有效的,建立的回归方程模型是合理的,适用于预测酸枣SDF的提取率。
2.2 国标法测定膳食纤维的含量
SDF和IDF中膳食纤维含量分别为60.75%和78.80%,膳食纤维为主要成分表明其在食品工业和健康食品开发中具有重要潜力。
2.3 结构特性
2.3.1 SEM分析
SEM可以观察样品的微观结构,展现样品表面形态和孔径分布。如图2所示,SDF和IDF的微观结构差异明显。SDF表面较平滑但有微孔及纹理分布,而IDF表面更粗糙且有褶皱,增加了比表面积,更有利于对水、油等成分的吸附[16],这与IDF更好的持水、持油性质一致。验证微观结构与理化性质的一致性,为进一步的性质研究提供理论依据。

a-SDF;b-IDF
图2 SDF和IDF的SEM图(2 400×)
Fig.2 SEM plots of SDF and IDF(2 400×)
2.3.2 FT-IR分析
如图3所示,SDF和IDF在4 000~400 cm-1具有相似的峰型和位置,振动强度存在差异,表明其化学成分相似但含量不同。3 400 cm-1附近的宽而强吸收带归因于纤维素和半纤维素中O—H的伸缩振动。2 800~3 000 cm-1区域的吸收峰对应于C—H的伸缩振动,表明存在烷基或亚甲基结构。1 700~1 750 cm-1区域的吸收峰源于—C![]() O的伸缩振动,存在酯、羧酸或酮类化合物。1 000~1 300 cm-1区域吸收峰对应于C—O—C和C—O伸缩振动,800~1 200 cm-1区域吸收峰可能与C—C和C—O的振动相关,进一步证实了多糖结构的存在。这些特征与膳食纤维的典型化学组成一致[17],为酸枣膳食纤维的化学结构解析及功能性质研究提供了重要依据。
O的伸缩振动,存在酯、羧酸或酮类化合物。1 000~1 300 cm-1区域吸收峰对应于C—O—C和C—O伸缩振动,800~1 200 cm-1区域吸收峰可能与C—C和C—O的振动相关,进一步证实了多糖结构的存在。这些特征与膳食纤维的典型化学组成一致[17],为酸枣膳食纤维的化学结构解析及功能性质研究提供了重要依据。
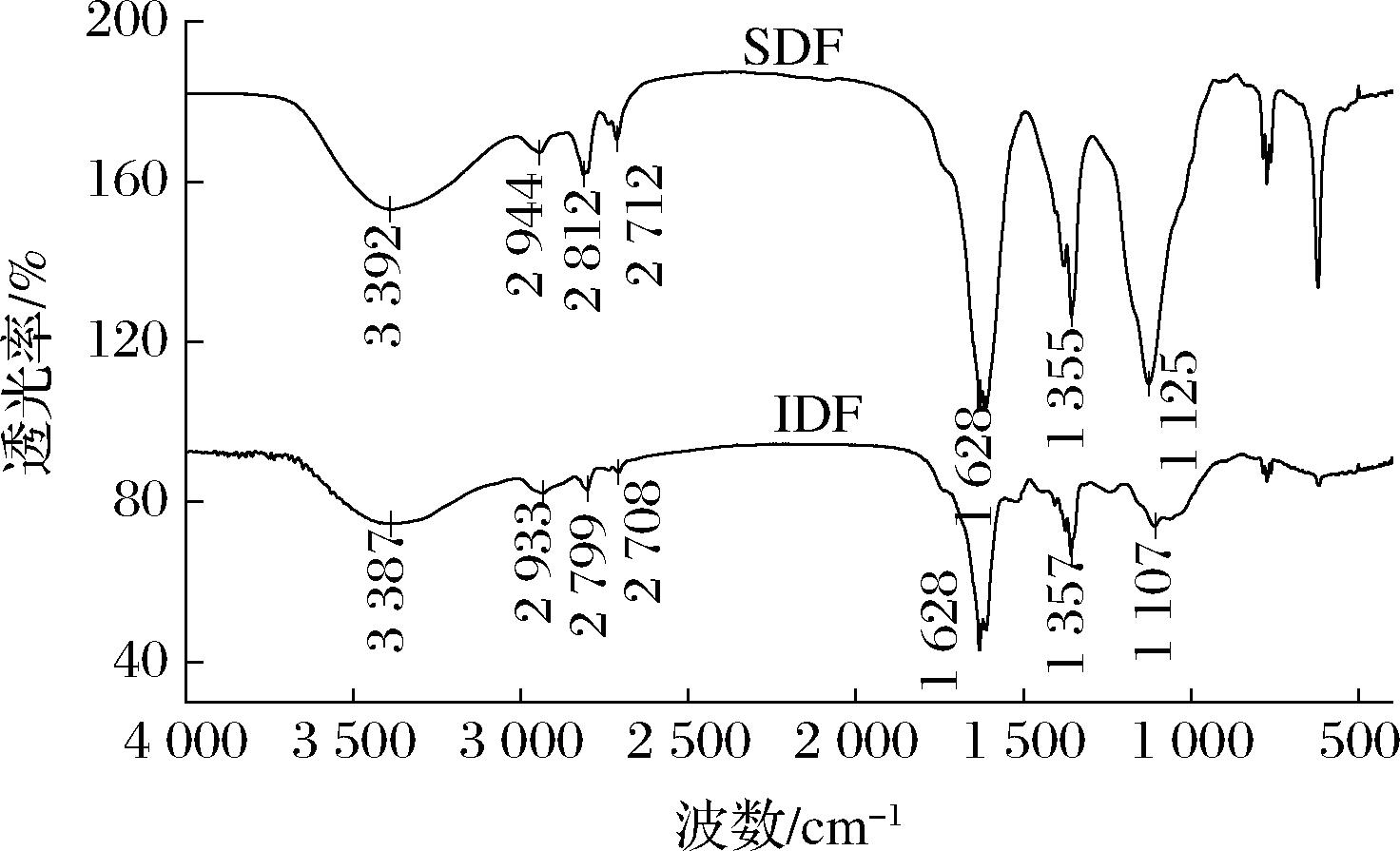
图3 SDF和IDF的红外光谱图
Fig.3 Infrared spectra of SDF and IDF
2.3.3 分子质量分布
分子质量分布如图4所示。SDF呈现出2个主峰,其保留时间分别为4.7、6.4 min,代入标准曲线lg Mw =-0.714 8x+9.261 3(R2=0.999 2),计算出相对平均分子质量分别为48.5、762 kDa。这2个分子质量峰的存在表明SDF由不同分子质量的多糖组分构成,其中48.5 kDa的组分代表较小的多糖片段,而762 kDa的组分则对应于较大的多糖聚合物。
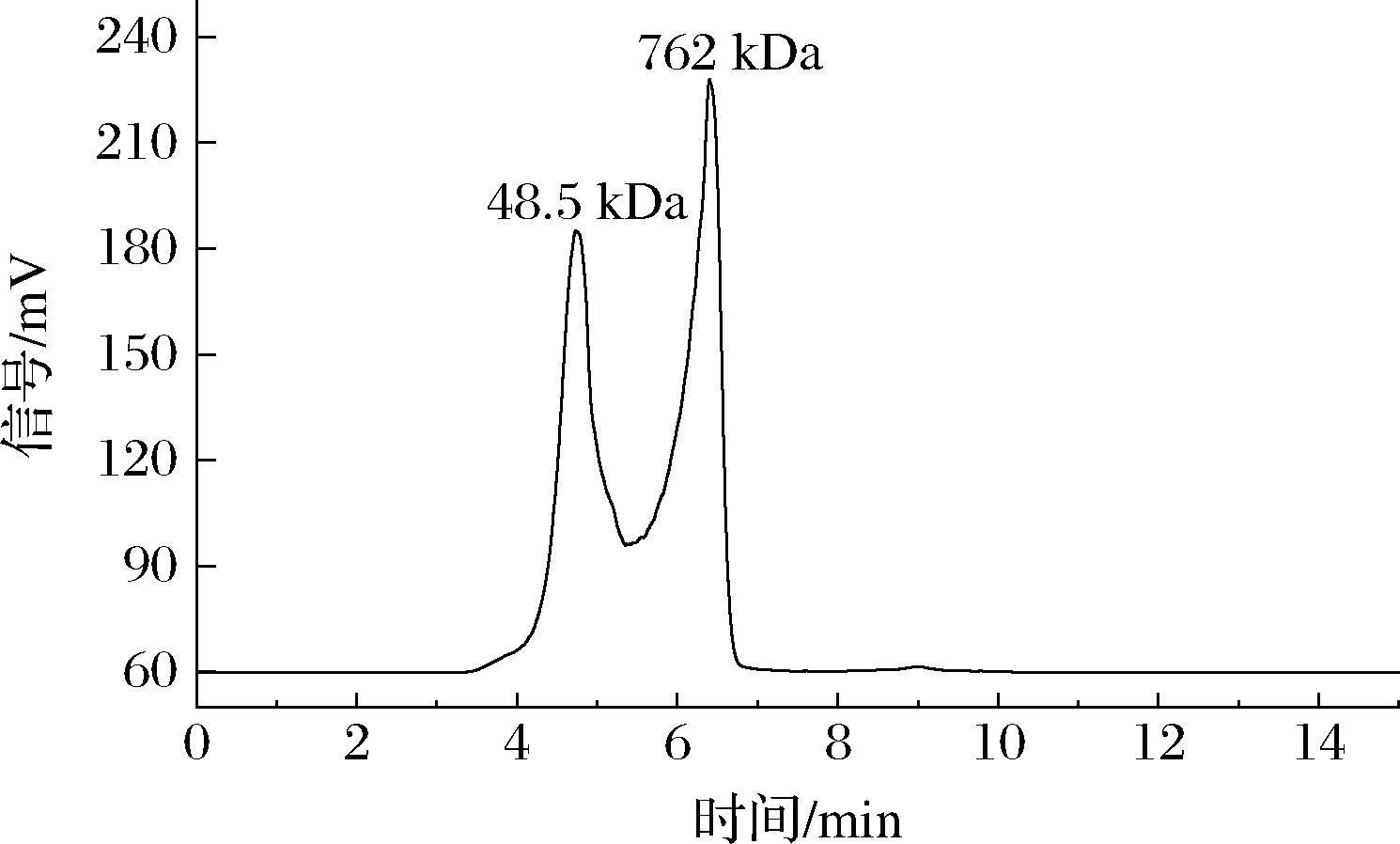
图4 SDF的分子质量分布色谱图
Fig.4 Molecular weight distribution chromatogram of SDF
这种分子质量分布特征与纤维素酶提取过程中多糖链的降解和分离有关。低分子质量的多糖可能更容易被肠道菌群发酵,产生有益的短链脂肪酸;高分子质量的多糖可能有更好的免疫调节作用。这些特性使酸枣SDF在食品工业和营养保健领域有广泛的应用潜力。
2.3.4 单糖组成分析
SDF和IDF的单糖组成及其摩尔比如表4和图5所示。SDF和IDF由同样的单糖组成,组成比例有所不同,玉米麸皮酶提取膳食纤维的研究中[18]有相似结果。Man、Rha、GalA、Gal和Xyl是半纤维素的主要成分,Glc是纤维素的主要成分,Rha和GalA是果胶的主要成分。SDF中Glc含量比例较高,可能是纤维素酶处理促进了纤维素的水解。这一发现为探索膳食纤维的结构与功能关系方面研究提供了有价值的线索。
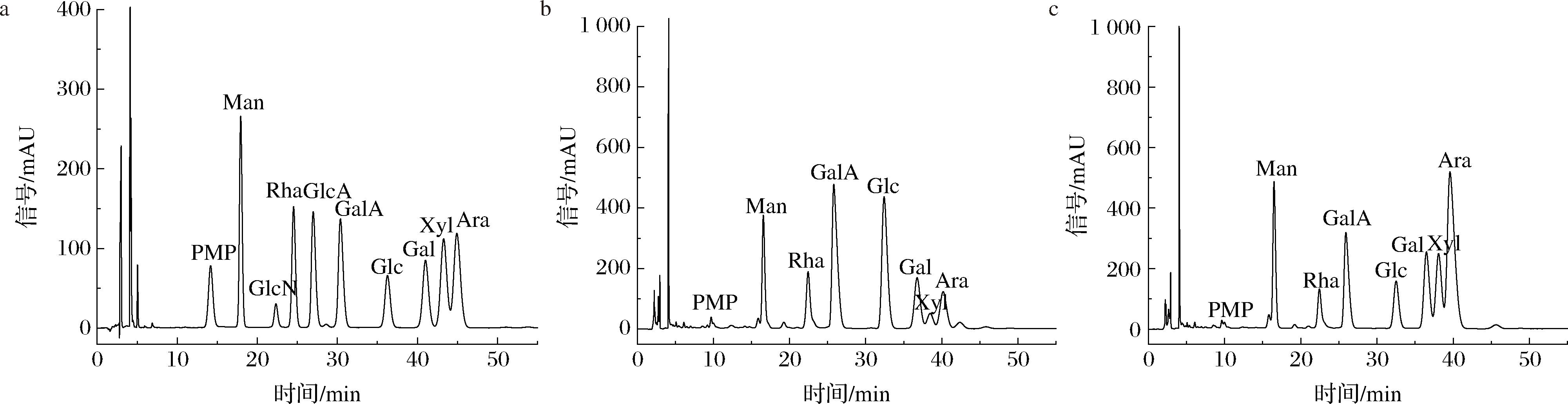
a-标准品;b-SDF;c-IDF
图5 SDF和IDF的高效液相色谱图
Fig.5 The high efficiency liquid chromatograms of SDF and IDF
表4 SDF和IDF的单糖组成(摩尔比值)
Table 4 Monosaccharide composition of SDF and IDF
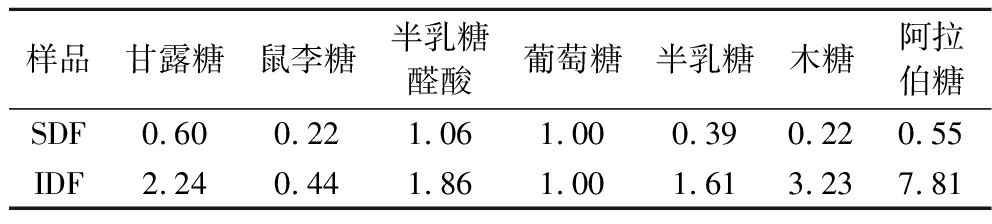
样品甘露糖鼠李糖半乳糖醛酸葡萄糖半乳糖木糖阿拉伯糖SDF0.600.221.061.000.390.220.55IDF2.240.441.861.001.613.237.81
2.3.5 X-射线衍射
具有结晶性的物质会显示出狭窄尖锐的衍射尖峰,不具有晶体构型的物质会显示出一个宽而弥散的衍射峰。如图6所示,SDF和IDF的XRD谱图相似,衍射峰分别位于19.1°和21.4°处,IDF观察到尖锐且强度较高的衍射峰,表明其高结晶特性;SDF峰形比较平缓,可能是酶解在一定程度上破坏了晶体结构,分子排列松散与其可溶性多糖的非晶态结构一致。
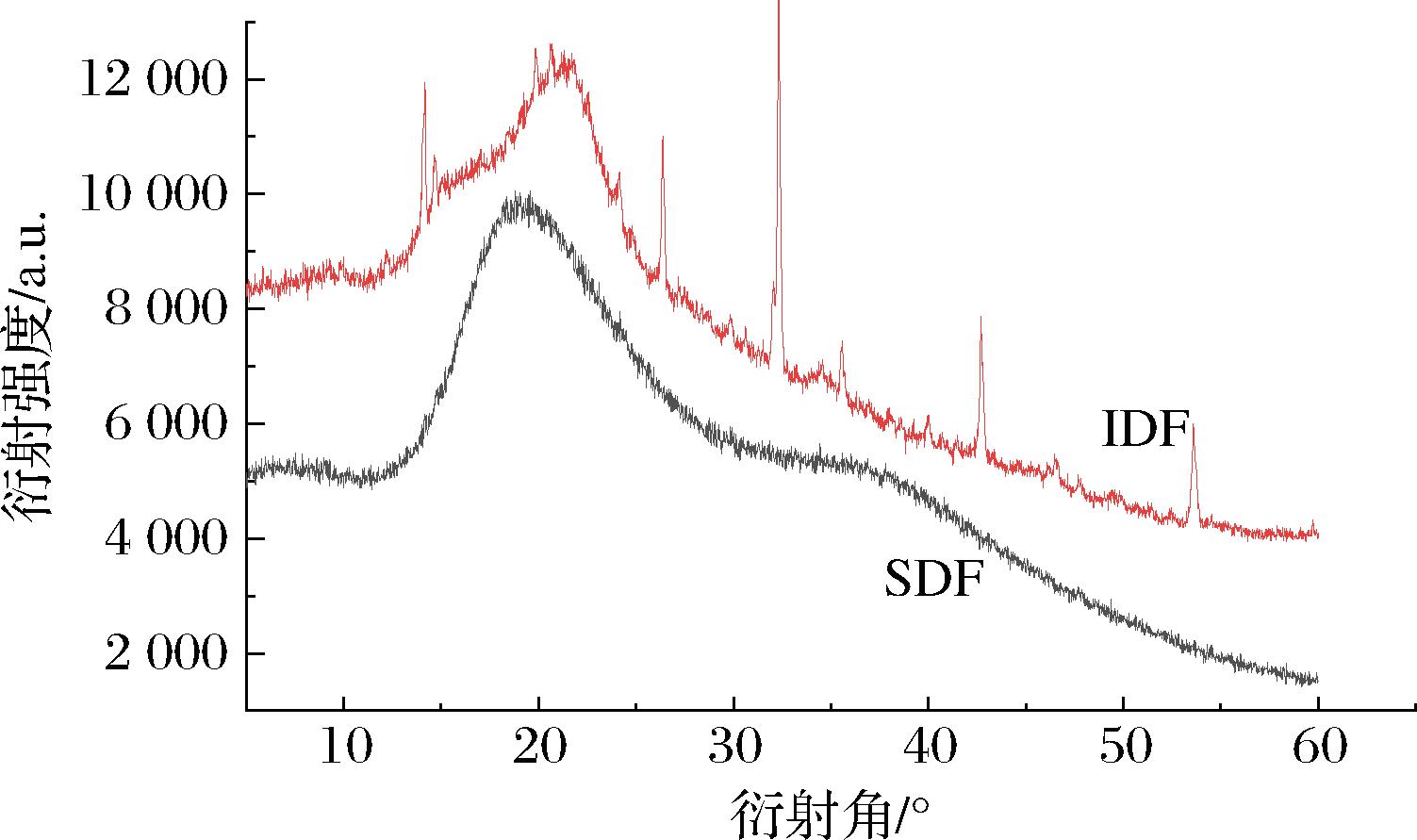
图6 SDF和IDF的X-衍射图
Fig.6 X-ray diffraction pattern of SDF and IDF
2.3.6 热重分析
通过热重分析对比样品热稳定性差异。如图7所示,SDF和IDF在30~600 ℃的热稳定趋势相似。第一阶段在30~200 ℃,游离水和结合水损失导致质量下降。第二阶段在200~350 ℃,SDF被热分解,氢键断裂,果胶和半纤维素被碳化[19];第三阶段在350~600 ℃,质量趋于稳定,SDF和IDF剩余质量百分比最终为37.70%和27.19%。综合以上结果,推测酸枣SDF的热稳定性优于IDF。
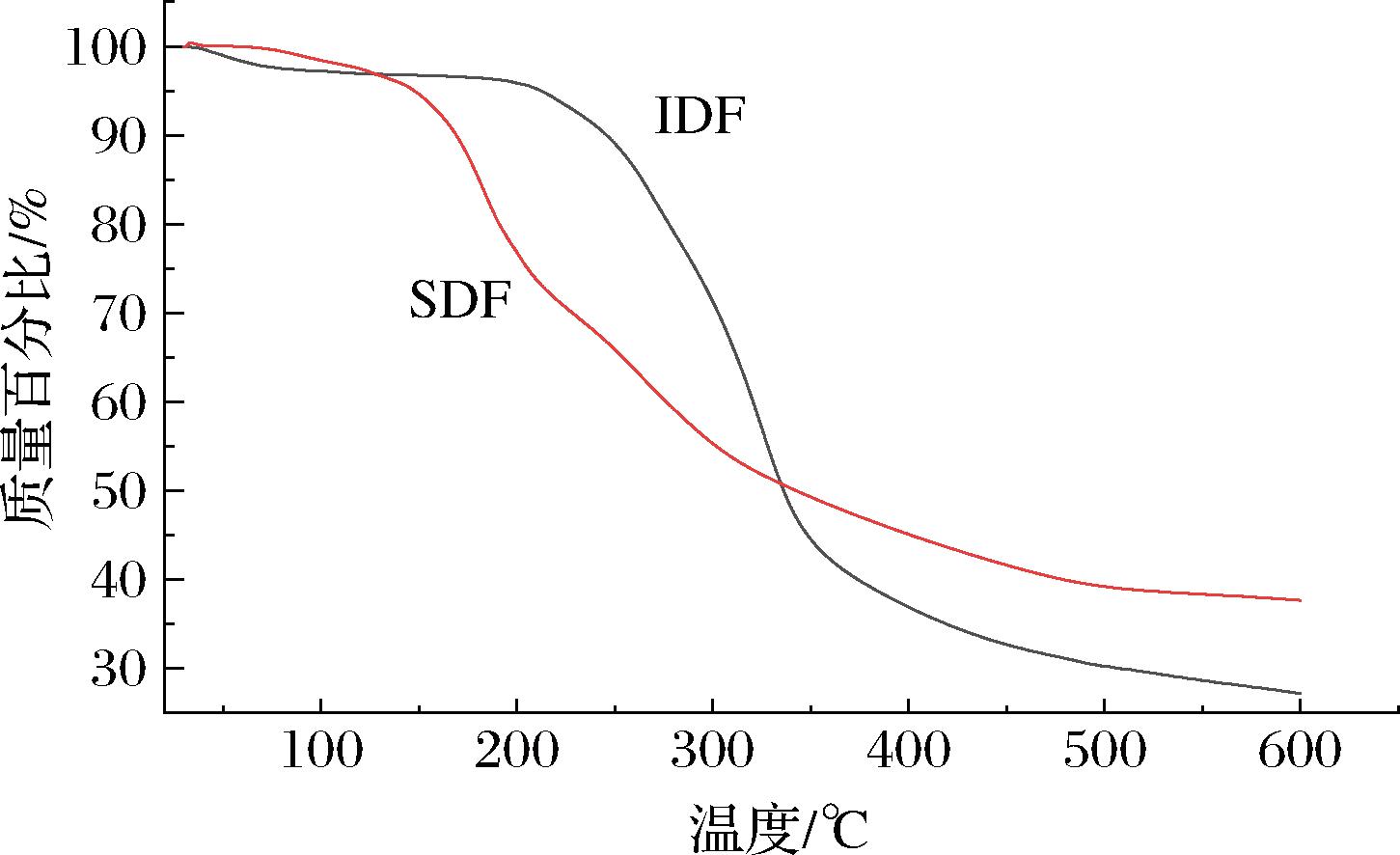
图7 SDF和IDF的热稳定性分析
Fig.7 Thermal stability analysis of SDF and IDF
2.4 理化性质
如表5所示,酸枣IDF的理化性质优于SDF。人体摄入高持水、持油力的膳食纤维,不仅可增强饱腹感、减少脂肪在胃肠道的堆积,还使肠道粪便质地变软,缩短排便时间。IDF更好的吸附能力与其粗糙的微观结构一致。与红外光谱中展现的羟基等亲水性基团和木质素等疏水区域作用符合。相比之下IDF更好的理化性质作为保水剂应用于食品或作为脂肪替代物以降低食品油腻感展现更大的优势。
表5 SDF和IDF的理化性质
Table 5 Physicochemical properties of SDF and IDF
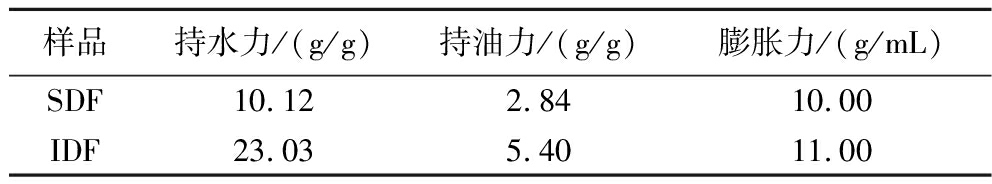
样品持水力/(g/g)持油力/(g/g)膨胀力/(g/mL)SDF10.122.8410.00IDF23.035.4011.00
2.5 GAC
GAC作为衡量膳食纤维体外降血糖最直接的指标之一。如图8所示,SDF和IDF的GAC均随葡萄糖溶液浓度升高呈上升趋势,此时样品吸收能力还未达到饱和。低浓度时IDF的GAC略高于SDF,当葡萄糖质量浓度达到1.2 mg/mL时,SDF表现更强的吸附能力可达74.65 mg/g。原因可能是足够的SDF可在水中溶解形成凝胶状黏性物质,可与葡萄糖结合降低体系中的葡萄糖水平[20];而IDF具有粗糙的表面结构,更有利于物理吸附。因此,在日常饮食中摄入足量膳食纤维,可以减少机体对葡萄糖的吸收,维持机体稳定的血糖水平。
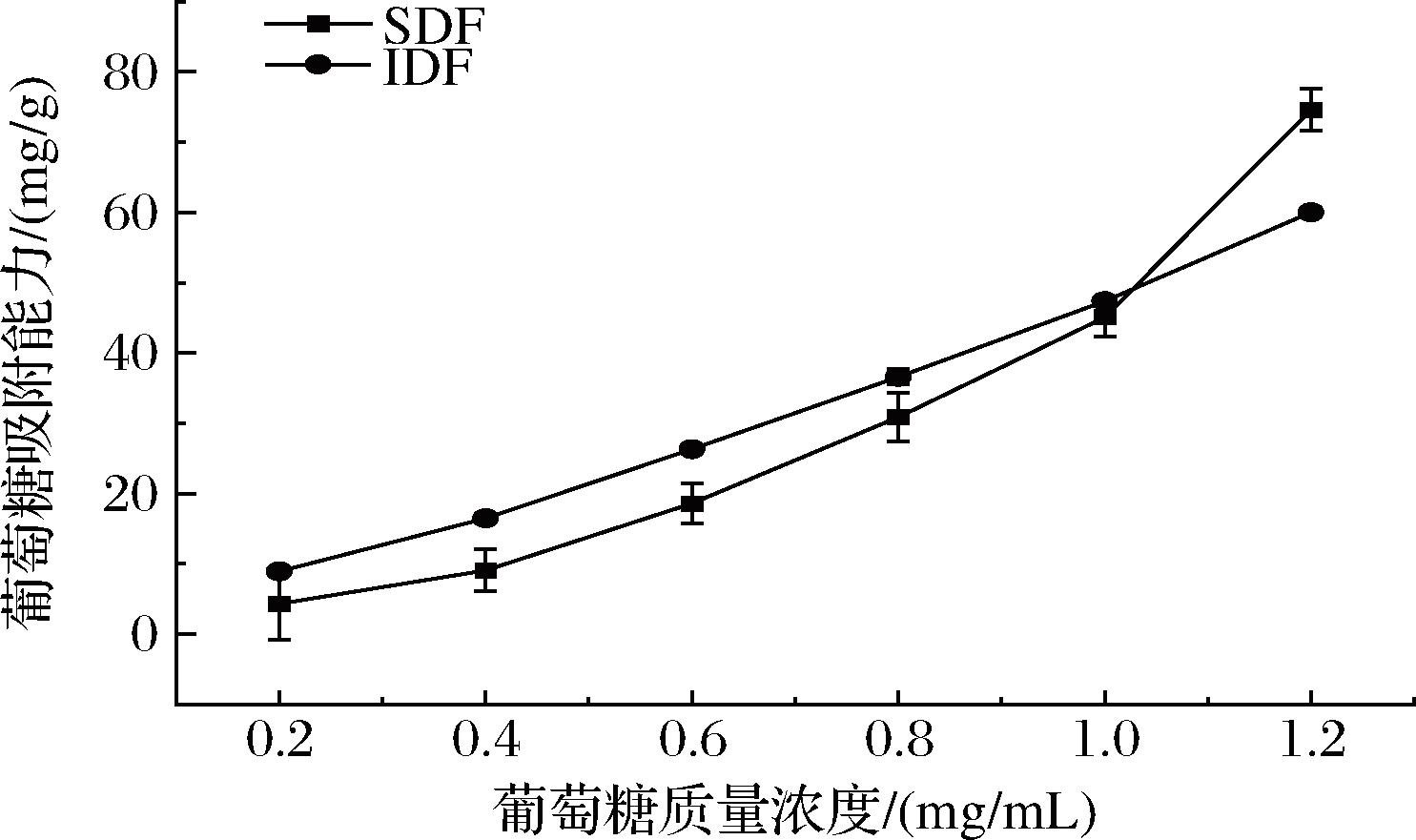
图8 SDF和IDF的葡萄糖吸附能力
Fig.8 Glucose adsorption capacity of SDF and IDF
2.6 α-淀粉酶抑制能力
α-淀粉酶是一种能够催化淀粉和糖原等多糖分解的关键酶[21]。如图9所示,酸枣SDF和IDF均有α-淀粉酶抑制能力。SDF和IDF对α-淀粉酶抑制能力随着样品质量的升高而增强,且SDF抑制能力始终高于IDF,最高可达到84.39%。YANG等[22]发现仙人草SDF对α-淀粉酶的抑制率为31.99%,酸枣膳食纤维与之相比,表现出更强的抑制效果,特别是SDF在降血糖方面表现出巨大潜力,值得进一步开发利用。
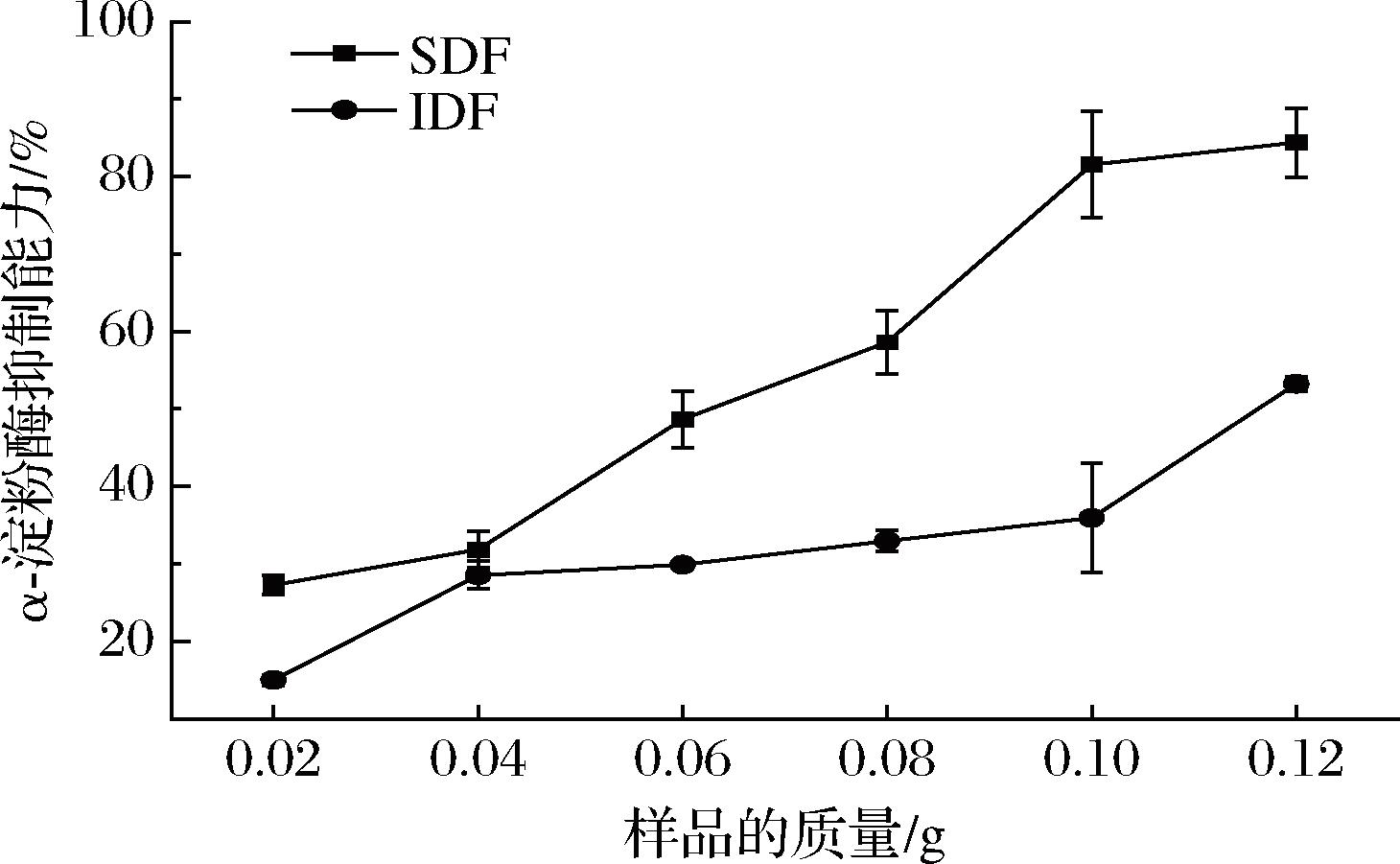
图9 SDF和IDF对淀粉酶活性的抑制能力
Fig.9 Inhibitory capacity of SDF and IDF on amylase activity
2.7 CAC
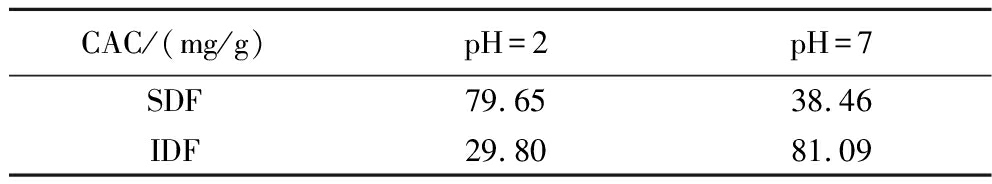
研究表明,膳食纤维CAC越强,越能有效减少机体对胆固醇的吸收[23]。如表6所示,在模拟人体胃(pH=2)和肠(pH=7)环境体系中,酸枣SDF和IDF均表现出较好的效果,但两者的吸附特点存在显著差别。pH=2时,SDF的CAC为79.65 mg/g显著高于IDF的38.46 mg/g;而pH=7时,IDF的CAC为81.09 mg/g显著高于SDF的29.80 mg/g。酸枣SDF和IDF在不同消化阶段对胆固醇的吸附具有互补作用,两者联合使用效果更好。蜜橘等果渣中膳食纤维的CAC为16.93~22.56 mg/g[24],酸枣膳食纤维与之相比有更好的效果,可作为体外降血脂的研究对象。
表6 SDF和IDF的胆固醇吸附能力
Table 6 Cholesterol adsorption capacity of SDF and IDF
CAC/(mg/g)pH=2pH=7SDF79.65 38.46IDF29.8081.09
3 结论
酸枣是膳食纤维良好的来源,根据酸枣SDF和IDF的结构、理化性质和功能特性的差异,可根据实际应用需求进行针对性选择利用。响应面优化实验可有效提高酸枣SDF的得率。IDF的表面更为粗糙,理化性质更好,证实微观结构与理化性质的一致性。总体来说SDF表现出更好的降糖效果,在低葡萄糖浓度下,IDF的GAC略高于SDF;而当质量浓度升至1.2 mg/mL时,SDF的GAC显著高于IDF;此外,α-淀粉酶抑制能力在不同梯度下SDF总是优于IDF。体外降脂实验中,SDF和IDF均表现出良好的胆固醇吸附能力。酸枣膳食纤维表现出色的功能特性,在功能性食品开发领域展现出巨大的应用潜力。为进一步推动酸枣膳食纤维在营养健康领域的应用,仍需深入探究其构效关系、体内代谢机制,并评估工业化生产的可行性。
[1] 鲁敏,张宏武,薄文浩,等.内蒙古酸枣资源利用现状及产业发展建议[J].内蒙古林业,2024(8):27-28.LU M,ZHANG H W,BO W H,et al.Utilization status of Zizyphus jujuba resources in Inner Mongolia and suggestions on industrial development[J].Inner Mongolia Forestry,2024(8):27-28.
[2] 郭盛,严辉,钱大玮,等.枣属药用植物资源产业化过程副产物及废弃物的资源价值发现与循环利用策略构建[J].南京中医药大学学报,2019,35(5):579-584.GUO S,YAN H,QIAN D W,et al.Resource value discovery and recycling strategy construction of by-products and wastes in industrialization of medicinal plant resources of Ziziphus genus[J].Journal of Nanjing University of Traditional Chinese Medicine,2019,35(5):579-584.
[3] YUE Y,WU S C,ZHANG H F,et al.Characterization and hepatoprotective effect of polysaccharides from Ziziphus jujuba Mill.var.spinosa (Bunge) Hu ex H.F.Chou sarcocarp[J].Food and Chemical Toxicology,2014,74:76-84.
[4] GILL S K,ROSSI M,BAJKA B,et al.Dietary fibre in gastrointestinal health and disease[J].Nature Reviews Gastroenterology &Hepatology,2021,18(2):101-116.
[5] HE Y,WANG B X,WEN L K,et al.Effects of dietary fiber on human health[J].Food Science and Human Wellness,2022,11(1):1-10.
[6] GUAN Z W,YU E Z,FENG Q,et al.Soluble dietary fiber,one of the most important nutrients for the gut microbiota[J].Molecules,2021,26(22):6802.
[7] LIN D R,NING H J,LIU Y,et al.Mechanism of promoting okara insoluble to soluble dietary fiber by high-pressure homogenization-microbial fermentation[J].Bioresource Technology,2025,416:131774.
[8] ZHANG M Y,LIAO A M,THAKUR K,et al.Modification of wheat bran insoluble dietary fiber with carboxymethylation,complex enzymatic hydrolysis and ultrafine comminution[J].Food Chemistry,2019,297:124983.
[9] AKPABLI-TSIGBE N D K,OSABUTEY J,MINTAH B K,et al.Cleavage of macromolecule (protein/polysaccharide)-phenolic bond in soybean cell wall through Lactobacillus casei and Lactobacillus helviticus mixed culture solid-state fermentation for chlorogenic acid extraction[J].Food Bioscience,2023,55:102903.
[10] CHEN H,YANG P,WU Z Y,et al.Multi-level fingerprint and immune activity evaluation of polysaccharides from Rhodiola rosea L[J].International Journal of Biological Macromolecules,2025,299:140197.
[11] WANG C R,LIN M F,LI Y B,et al.Improvement of soluble dietary fiber quality in Tremella fuciformis stem by steam explosion technology:An evaluation of structure and function[J].Food Chemistry,2024,437:137867.
[12] LI Y X,NIU L,GUO Q Q,et al.Effects of fermentation with lactic bacteria on the structural characteristics and physicochemical and functional properties of soluble dietary fiber from prosomillet bran[J].LWT,2022,154:112609.
[13] WANG C Z,LI L,SUN X,et al.High-speed shearing of soybean flour suspension disintegrates the component cell layers and modifies the hydration properties of okara fibers[J].LWT,2019,116:108505.
[14] JIANG C X,WANG R,LIU X L,et al.Effect of particle size on physicochemical properties and in vitro hypoglycemic ability of insoluble dietary fiber from corn bran[J].Frontiers in Nutrition,2022,9:951821.
[15] KARIMI A,AZIZI M H,AHMADI GAVLIGHI H.Fractionation of hydrolysate from corn germ protein by ultrafiltration:In vitro antidiabetic and antioxidant activity[J].Food Science &Nutrition,2020,8(9):5192.
[16] ZHANG Y F,ZHU J H,ZOU Y,et al.Insoluble dietary fiber from five commercially cultivated edible mushrooms:Structural,physiochemical and functional properties[J].Food Bioscience,2024,57:103514.
[17] ALBA K,MACNAUGHTAN W,LAWS A P,et al.Fractionation and characterisation of dietary fibre from blackcurrant pomace[J].Food Hydrocolloids,2018,81:398-408.
[18] LI S,HU N N,ZHU J Y,et al.Influence of modification methods on physicochemical and structural properties of soluble dietary fiber from corn bran[J].Food Chemistry:X,2022,14:100298.
[19] ZHANG S Y,ZHENG L L,ZHENG X Y,et al.Effect of steam explosion treatments on the functional properties and structure of Camellia (Camellia oleifera Abel.) seed cake protein[J].Food Hydrocolloids,2019,93:189-197.
[20] 王梦阳.香蕉皮膳食纤维的理化性质及其降血糖效果的研究[D].合肥:合肥工业大学,2022.WANG M Y.Study on physicochemical properties and hypoglycemic effect of banana peel dietary fiber[D].Hefei:Hefei University of Technology,2022.
[21] 卓思雨,梁颖康,欧成成,等.南瓜籽饼粕可溶性膳食纤维的提取及其结构与功能特性分析[J].食品工业科技,2025,46(18):272-282.ZHUO S Y,LIANG Y K,OU C C,et al.Extraction of soluble dietary fiber from pumpkin seed cake and analysis of its structure and functional properties[J].Science and Technology of Food Industry,2025,46(18):272-282.
[22] YANG C R,SI J Y,CHEN Y,et al.Physicochemical structure and functional properties of soluble dietary fibers obtained by different modification methods from Mesona chinensis Benth.residue[J].Food Research International,2022,157:111489.
[23] SI J Y,YANG C R,CHEN Y,et al.Structural properties and adsorption capacities of Mesona chinensis Benth residues dietary fiber prepared by cellulase treatment assisted by Aspergillus niger or Trichoderma reesei[J].Food Chemistry,2023,407:135149.
[24] 陈贵婷,石凯欣,张珮珮,等.不同品种柑橘皮渣膳食纤维构效关系比较[J].食品科学,2023,44(17):20-28.CHEN G T,SHI K X,ZHANG P P,et al.Comparative study on the structure-activity relationship of dietary fiber from different varieties of citrus peel and pomace[J].Food Science,2023,44(17):20-28.