近年来,抗生素污染已成为全球性的环境问题,引起了广泛关注。随着抗生素在医疗和畜牧业等领域的广泛使用,大量抗生素及其代谢物通过不同途径进入水环境,对生态系统和人类健康造成了严重威胁[1],同时对水生生物造成不可忽视的影响[2]。面对这一挑战,科研工作者一直在寻找高效、经济且环境友好的抗生素去除方法。传统的处理技术,如活性炭吸附、高级氧化和生物降解等,虽然在一定程度上能够去除水中的抗生素,但都存在各自的局限性。活性炭吸附能力强,但需要物理或化学活化,成本较高[3];高级氧化技术可以有效降解废水中的抗生素,但仍需提高适应性以及实用性[4];而生物降解法则常受到抗生素本身特性的制约,难以达到理想的处理效果[5]。
在探索新的水处理技术的过程中,天然材料因其独特的结构和性能,展现出了良好的应用潜力[6]。玉米醇溶蛋白是玉米加工以及生物乙醇工业的主要副产物,价格低廉易得,且被证明具有优越的生物相容性和可生物降解性[7]。由于玉米醇溶蛋白具有高度的疏水性能,使其在水溶液中具有良好的自组装特性,加上它由多种不同的氨基酸组成,含有氨基、羟基、羧基等多个自由官能团,能够通过多种作用力与特定的污染物相互作用,使其成为废水处理领域有前景的候选者[8]。目前玉米醇溶蛋白已被设计成纳米颗粒、纳米纤维、微/纳米膜等多种形式,针对废水中的重金属、有机染料、机油等污染物进行有效去除[9-11]。在现有的报道中,玉米醇溶蛋白对水体中抗生素污染物的去除还鲜有研究。
单宁是植物的多酚类次级代谢产物,主要存在于植物的叶、根、皮以及果实中,是继纤维素、半纤维素和木质素后,从植物中提取的最丰富的化合物[12]。单宁的结构中含有大量的酚羟基,具有亲水性、金属络合能力、阳离子交换能力等,其在水处理领域的应用越来越受到人们的关注[13]。单宁上丰富的羟基能够通过多种作用机制与抗生素分子相互作用,实现水体中抗生素的有效去除[14-15]。然而,单宁的水溶性特征限制了其单独作为吸附剂在实际水处理中的大规模应用[13-16]。为了克服这些局限性,单宁在水体应用时需要一个固定化或非水溶化的过程,因此,研究者们尝试了诸如负载、原位改性等多种方法。S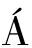 NCHEZ-MART
NCHEZ-MART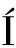 N等[17]用甲醛和乙醛凝胶化了4种不同天然植物来源的单宁提取物,考察了不同组合对水溶液中Zn2+、亚甲基蓝(methylene blue,MB)和十六烷基三甲基溴化铵(cetyl trimethyl ammonium bromide,CTAB)的去除效果,结果显示根据Langmuir一般吸附行为,这些单宁凝胶在去除这些污染物方面很有效。侯俊等[14]考察了二甲基二烯丙基氯化铵(dimethyl diallyl ammonium chloride,DMDAAC)改性的植物单宁絮凝剂(TGCC-A)对污水处理厂出水中抗生素抗性基因(antibiotics resistance genes,ARGs)丰度的影响,结果表明TGCC-A对污水处理厂二级出水中的ARGs具有良好的去除和控制效果。然而目前的报道中,改性单宁常以较大颗粒的粉末或固体泡沫的状态存在,相比较纳米材料而言,其去除效率有限。且单宁的固化过程通常会引入毒性化学试剂,这可能会在水处理过程中,引入二次污染。
N等[17]用甲醛和乙醛凝胶化了4种不同天然植物来源的单宁提取物,考察了不同组合对水溶液中Zn2+、亚甲基蓝(methylene blue,MB)和十六烷基三甲基溴化铵(cetyl trimethyl ammonium bromide,CTAB)的去除效果,结果显示根据Langmuir一般吸附行为,这些单宁凝胶在去除这些污染物方面很有效。侯俊等[14]考察了二甲基二烯丙基氯化铵(dimethyl diallyl ammonium chloride,DMDAAC)改性的植物单宁絮凝剂(TGCC-A)对污水处理厂出水中抗生素抗性基因(antibiotics resistance genes,ARGs)丰度的影响,结果表明TGCC-A对污水处理厂二级出水中的ARGs具有良好的去除和控制效果。然而目前的报道中,改性单宁常以较大颗粒的粉末或固体泡沫的状态存在,相比较纳米材料而言,其去除效率有限。且单宁的固化过程通常会引入毒性化学试剂,这可能会在水处理过程中,引入二次污染。
本文采用改性阳离子单宁(cationic tannin,CAT)与玉米醇溶蛋白(Zein)相结合,构建带正电荷的复合纳米颗粒(cationic tannin-zein,CAT-Zein),在克服单宁自身局限性的同时,有机结合醇溶蛋白纳米颗粒的高效吸附性以及单宁优异的水体污染物去除和絮凝能力,旨在有效去除水体中抗生素污染,并为开发高效、绿色的水处理材料提供新的思路。首先,采用反溶剂法制备阳离子单宁-玉米醇溶蛋白(CAT-Zein)复合纳米颗粒,对其进行粒径和zeta电位的检测以及微观形貌的观察,并且通过理化性质的表征探究纳米颗粒的形成机制。最后以头孢噻吩钠作为头孢类抗生素的模型污染物,考察CAT-Zein纳米颗粒对头孢类抗生素的去除效果,并进一步探索其影响因素。
1 材料与方法
1.1 材料与试剂
玉米醇溶蛋白,上海阿拉丁生化科技股份有限公司;头孢噻吩钠,上海源叶生物科技有限公司;阳离子单宁,索理思(上海)化工有限公司;盐酸、氢氧化钠、乙醇等试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
Zetasizer Nano ZS90动态光散射粒度分析仪(dynamic light scattering,DLS),英国马尔文仪器有限公司;3-30K冷冻离心机,德国Sigma公司;BT100-2J蠕动泵,保定兰格恒流泵有限公司;Mini Plus纯水仪,德国Sartorius公司;FD-1C50+冷冻干燥机,北京博医康实验仪器有限公司;UV1800紫外分光光度计,日本岛津仪器有限公司;Regulus8100扫描电子显微镜(scanning electron microscope,SEM),日本Hitachi公司;D8 Advance 型X射线衍射(X-ray diffraction,XRD)仪,德国Bruker公司;PerkinElmer Pyris1差示扫描量热(differential scanning calorimetry,DSC)仪,珀金埃尔默仪器有限公司;Nicolet iS10傅里叶红外光谱(Fourier transform infrared spectroscopy,FTIR)仪,美国Thermo Fisher科技有限公司。
1.3 实验方法
1.3.1 CAT-Zein纳米颗粒和Zein纳米颗粒的制备
参考王金霞等[18]的实验方法并稍作修改。采用反溶剂法制备CAT-Zein纳米颗粒。将50 mg玉米醇溶蛋白和阳离子单宁(2、2.5、3.3、5、10 mg)同时溶于5 mL体积分数为70%的乙醇溶液中,并超声溶解。用蠕动泵,以0.9 r/min的速度滴入25 mL的纯水中,750 r/min连续搅拌30 min。对照样Zein纳米颗粒的制备除了不加单宁以外,方法与上述CAT-Zein纳米颗粒制备一致。CAT-Zein纳米颗粒制备过程示意图如图1所示。
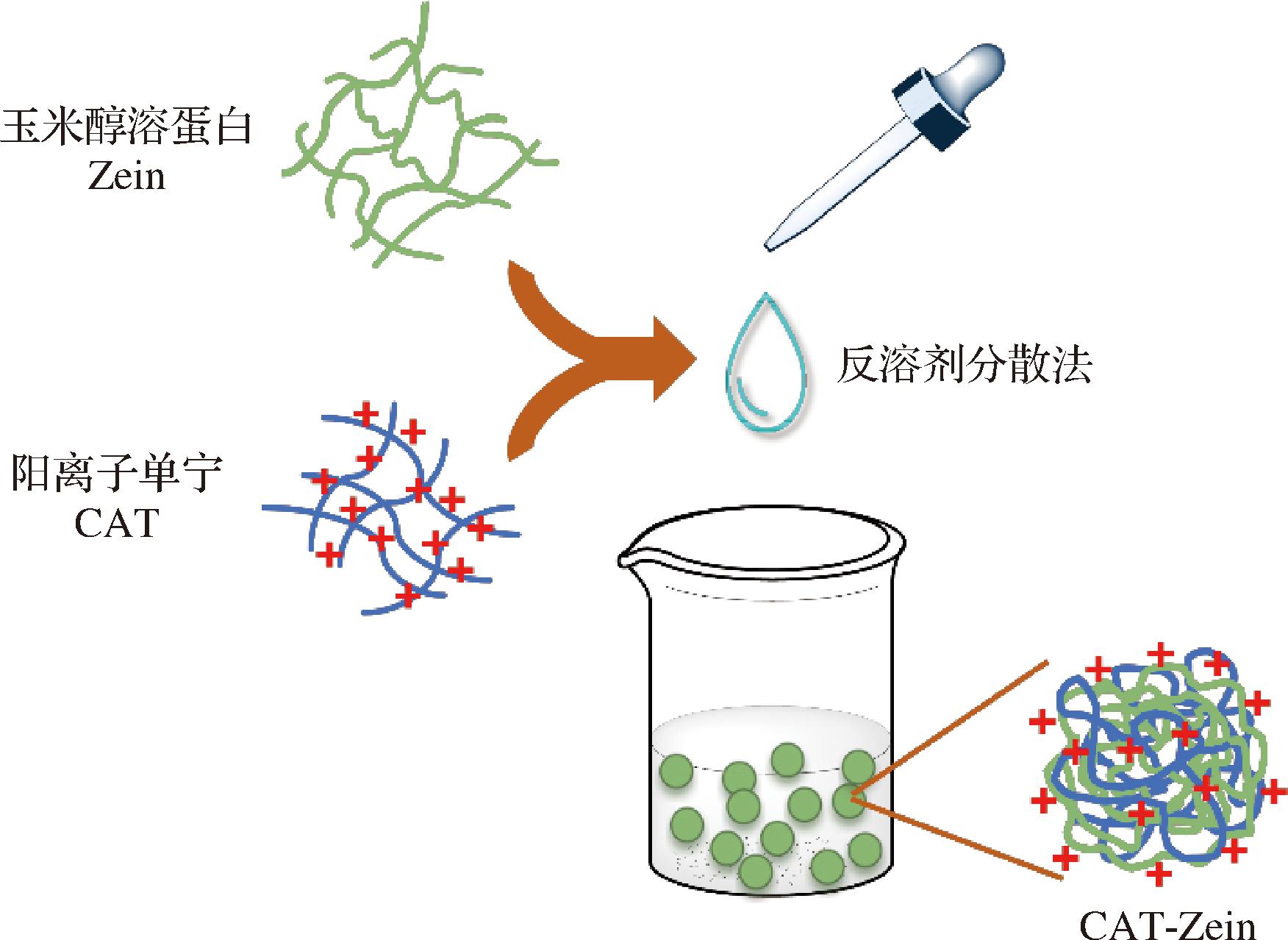
图1 CAT-Zein纳米颗粒制备过程示意图
Fig.1 Schematic diagram of CAT-Zein nanoparticle preparation process
根据实验结果,后续表征及性能测试,采用阳离子单宁和玉米醇溶蛋白质量比为1∶5的CAT-Zein纳米颗粒进行。
1.3.2 CAT-Zein纳米颗粒和Zein纳米颗粒粒径、PDI和zeta电位的测定
取制备好的Zein纳米颗粒和CAT-Zein纳米颗粒,用0.45 μm的滤膜过滤一次,取上述滤液用DSL测试样品的粒径、PDI和zeta电位。
1.3.3 CAT-Zein纳米颗粒和Zein纳米颗粒的形貌观察和结构表征
用SEM分别对2种纳米颗粒进行微观形貌观察,并进行FTIR、DSC、XRD参数的测定。
SEM微观形貌观察:取制备好的Zein纳米颗粒和CAT-Zein纳米颗粒混悬液,稀释20倍,再超声30 min 后取10 μL滴加在单晶抛光硅片上,在通风橱内风干过夜,喷金90 s后在10 kV电压下用SEM观察其微观形貌并拍摄照片。
FTIR检测:将冻干的玉米醇溶蛋白、阳离子单宁和CAT-Zein纳米颗粒分别与溴化钾研磨压片,用傅里叶红外光谱仪进行检测,波数为400~4 000 cm-1,分辨率为4 cm-1。
DSC检测:分别称取10 mg玉米醇溶蛋白、阳离子单宁和CAT-Zein纳米颗粒置于铝盘中,并以20 mL/min的速度不断通入氮气,让温度以10 ℃/min的升温速率从50 ℃升温至250 ℃,并使用空的密封铝盘作为基线,得到玉米醇溶蛋白、阳离子单宁和CAT-Zein纳米颗粒的DSC谱图。
XRD检测:在Cu靶和40 mA的电流条件下,使用X射线仪测量玉米醇溶蛋白、阳离子单宁和CAT-Zein纳米颗粒的晶体结构。扫描范围为2θ=5°~60°。扫描速度为5 °/min。
1.3.4 CAT-Zein纳米颗粒和Zein纳米颗粒的贮藏稳定性能考察
分别取10 mL新鲜制备的CAT-Zein纳米颗粒和Zein纳米颗粒存放在4、25 ℃条件下,于存放的第0、7、14、21、28天,取样,测定不同贮存条件下的粒径、PDI和zeta电位参数的变化情况。
1.3.5 头孢噻吩钠标准曲线的绘制
称取0.010 g头孢噻吩钠加入纯水中,并定容于100 mL容量瓶,得到100 mg/L头孢噻吩钠母液;梯度质量浓度设置为:10、20、30、40、50 mg/L,进行稀释。根据文献,头孢噻吩钠的最大吸收波长为254 nm[19],用纯水作为空白对照,用紫外分光光度计测定此波长下各溶液的紫外吸光度,绘制紫外吸光度-头孢噻吩钠浓度的标准曲线。
1.3.6 CAT-Zein纳米颗粒和Zein纳米颗粒对抗生素的去除研究
取2 mL新鲜制备的纳米颗粒混悬液稀释15倍,取10 mL稀释后纳米颗粒溶液加入10 mL 20 mg/L头孢噻吩钠溶液中,同时用磁力搅拌器搅拌混匀,先600 r/min搅拌1 min,再200 r/min搅拌4 min,并静置15 min后,将混合液12 000 r/min离心20 min。取上清液,紫外分光光度计测定254 nm波长处的吸光度,并根据标准曲线计算其中头孢噻吩钠的含量。水样中头孢噻吩钠去除率的计算如公式(1)所示:
去除率![]()
(1)
式中:m总为处理前水样中头孢噻吩钠总质量;m上清液为离心后上清液中头孢噻吩钠的质量。
1.3.7 pH值对于CAT-Zein 纳米颗粒的抗生素去除效果的影响
取9份2 mL新鲜制备的CAT-Zein纳米颗粒溶液稀释15倍,分别调pH值至3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0,并进行的粒径、PDI和zeta电位的测定。再分别各取10 mL加入已调成对应pH值的10 mL 20 mg/L头孢噻吩钠溶液中,用1.3.6节的方法,测定并计算各pH值条件下CAT-Zein纳米颗粒对头孢噻吩钠的去除率。
1.4 数据处理
所有实验至少进行3次,数据以“平均数±标准差”表示。本文数据分析和作图使用Origin Pro 2024软件完成。组间差异性采用T检验分析(P<0.05为显著性差异)。
2 结果与分析
2.1 CAT-Zein纳米颗粒和Zein纳米颗粒粒径、PDI和zeta电位的结果分析
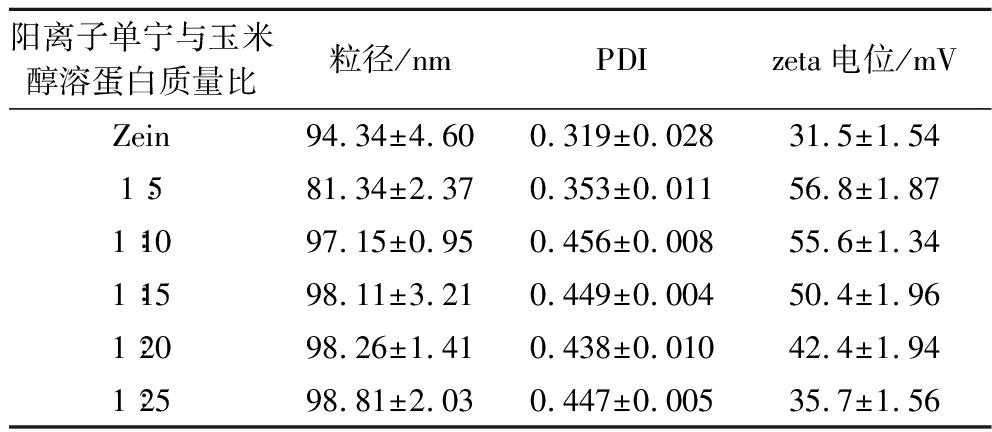
取新鲜制备的CAT-Zein纳米颗粒和Zein纳米颗粒使用动态光散射粒度分析仪(dynamic light scattering,DLS)测量粒径、PDI、和zeta电位,结果如表1所示。Zein纳米颗粒平均粒径为94.34 nm,当添加阳离子单宁形成CAT-Zein纳米颗粒时,随着阳离子单宁的添加质量比从1∶25到1∶5的逐渐升高,颗粒粒径有逐渐降低的趋势;当单宁添加质量比增加到1∶5时,CAT-Zein纳米颗粒的粒径平均粒径为81.34 nm,显著低于Zein纳米颗粒的粒径。这有可能是玉米醇溶蛋白与单宁之间的相互作用,形成了结构更加致密的CAT-Zein二元复合物[20]。并且,纳米颗粒粒径越小,在水溶液中有更好的分散性,越不易聚集产生沉淀[21]。PDI值为颗粒大小分布的量度,PDI值越小,粒径分布越集中,一般来说,PDI小于0.5被认为是纳米分散系的最佳分布[22]。本研究中的Zein纳米颗粒和不同阳离子单宁/玉米醇溶蛋白质量比的CAT-Zein纳米颗粒,粒径PDI值都在0.5以下,因此均具有良好的分散性和系统稳定性。
表1 纳米颗粒的粒径、PDI和zeta电位表征结果及单宁/玉米醇溶蛋白质量比的影响
Table 1 Particle Size,PDI,and zeta potential of nanoparticles and the effect of Tannin/Zein mass ratio
阳离子单宁与玉米醇溶蛋白质量比粒径/nmPDIzeta电位/mVZein94.34±4.600.319±0.02831.5±1.541∶581.34±2.370.353±0.01156.8±1.871∶1097.15±0.950.456±0.00855.6±1.341∶1598.11±3.210.449±0.00450.4±1.961∶2098.26±1.410.438±0.01042.4±1.941∶2598.81±2.030.447±0.00535.7±1.56
另外,随着阳离子单宁质量比的增加,CAT-Zein纳米体系的zeta电位逐渐增加。zeta电位可以用来表征纳米粒子的表面电荷,一般认为,水相体系中分散体zeta电位绝对值越大,粒子之间相互斥力越大,越不易聚集,颗粒的稳定性就越高[23]。因此,阳离子单宁的加入,增加了玉米醇溶蛋白纳米颗粒的稳定性,且随着单宁比例的提高,稳定性逐步增强,当质量比达到1∶5时,CAT-Zein纳米颗粒的zeta电位最高,稳定性最好。
另一方面,图2显示了Zein纳米颗粒和各比例的CAT-Zein纳米颗粒混悬液的外观形态,可见,各纳米体系均呈现良好的乳光状态,分散良好,无沉淀或析出物,且单宁添加质量比为1∶5时,纳米体系的浊度更低,这与上述该体系中纳米颗粒的粒径最小结论一致。因此,综合来看,当阳离子单宁和玉米醇溶蛋白的质量比为1∶5时,CAT-Zein纳米颗粒体系的分散程度最好,稳定性最好,因此后续实验采用该质量比(1∶5)进行。

图2 Zein纳米颗粒和不同阳离子单宁与玉米醇溶蛋白质量比的CAT-Zein纳米颗粒混悬液的外观形态
Fig.2 Appearance and morphology of Zein nanoparticles and CAT-Zein nanoparticles with different Tannin/Zein mass ratios
2.2 CAT-Zein纳米颗粒和Zein纳米颗粒的微观形貌分析
对CAT-Zein纳米颗粒和Zein纳米颗粒采用SEM进行微观形态学观察,结果如图3所示。2种纳米颗粒均呈现近球形颗粒形态,表面光滑,粒径约为100 nm,相对均匀,与DLS测得的粒径数据一致。SEM结果显示CAT-Zein纳米颗粒之间有轻微黏附,可能是由于玉米醇溶蛋白以及单宁之间的分子间作用力较大导致的。此结果表明Zein纳米颗粒和CAT-Zein纳米颗粒成功制备。

图3 Zein纳米颗粒和CAT-Zein纳米颗粒SEM微观形貌观察图
Fig.3 SEM images of Zein nanoparticles and CAT-Zein nanoparticles
2.3 FTIR测试结果分析
FTIR光谱图用于获得官能团以及分子状态的信息。玉米醇溶蛋白(Zein)、阳离子单宁(CAT)和CAT-Zein纳米颗粒的FTIR谱图如图4所示。单纯的Zein和CAT分别在3 310和3 147 cm-1处显示特征峰,根据之前的文献报道,3 100~3 500 cm-1的谱带是由羟基的伸缩振动引起的[24-25]。当Zein和CAT结合后,该谱带位移至CAT-Zein的3 422 cm-1,该结果表明Zein中的羟基和酰胺基与CAT中的羟基之间存在着较强的氢键作用[26-27]。另一方面,Zein在1 658、1 537 cm-1处的特征吸收峰,分别归于1 750~1 600 cm-1处由C![]() O键的伸缩振动引起的酰胺Ⅰ谱带,以及由N—H键的面内弯曲振动和C—N的伸缩振动引起的位于1 550~1 510 cm-1的酰胺Ⅱ谱带[11,24]。当与CAT结合后,Zein的酰胺Ⅰ谱带和Ⅱ谱带的吸收峰强度明显降低,且酰胺Ⅰ谱带位移至1 653 cm-1,此结果表明,由于CAT-Zein纳米颗粒中Zein的比例较高,Zein和CAT之间不仅存在着氢键的相互作用力,疏水相互作用力也是两者结合的作用力之一,此结果与SUN等[28]研究的玉米醇溶蛋白与藻酸丙二醇酯之间的疏水相互作用结果基本一致。因此,FTIR光谱结果表明,Zein和CAT之间存在着氢键和疏水作用等非共价相互作用力。
O键的伸缩振动引起的酰胺Ⅰ谱带,以及由N—H键的面内弯曲振动和C—N的伸缩振动引起的位于1 550~1 510 cm-1的酰胺Ⅱ谱带[11,24]。当与CAT结合后,Zein的酰胺Ⅰ谱带和Ⅱ谱带的吸收峰强度明显降低,且酰胺Ⅰ谱带位移至1 653 cm-1,此结果表明,由于CAT-Zein纳米颗粒中Zein的比例较高,Zein和CAT之间不仅存在着氢键的相互作用力,疏水相互作用力也是两者结合的作用力之一,此结果与SUN等[28]研究的玉米醇溶蛋白与藻酸丙二醇酯之间的疏水相互作用结果基本一致。因此,FTIR光谱结果表明,Zein和CAT之间存在着氢键和疏水作用等非共价相互作用力。
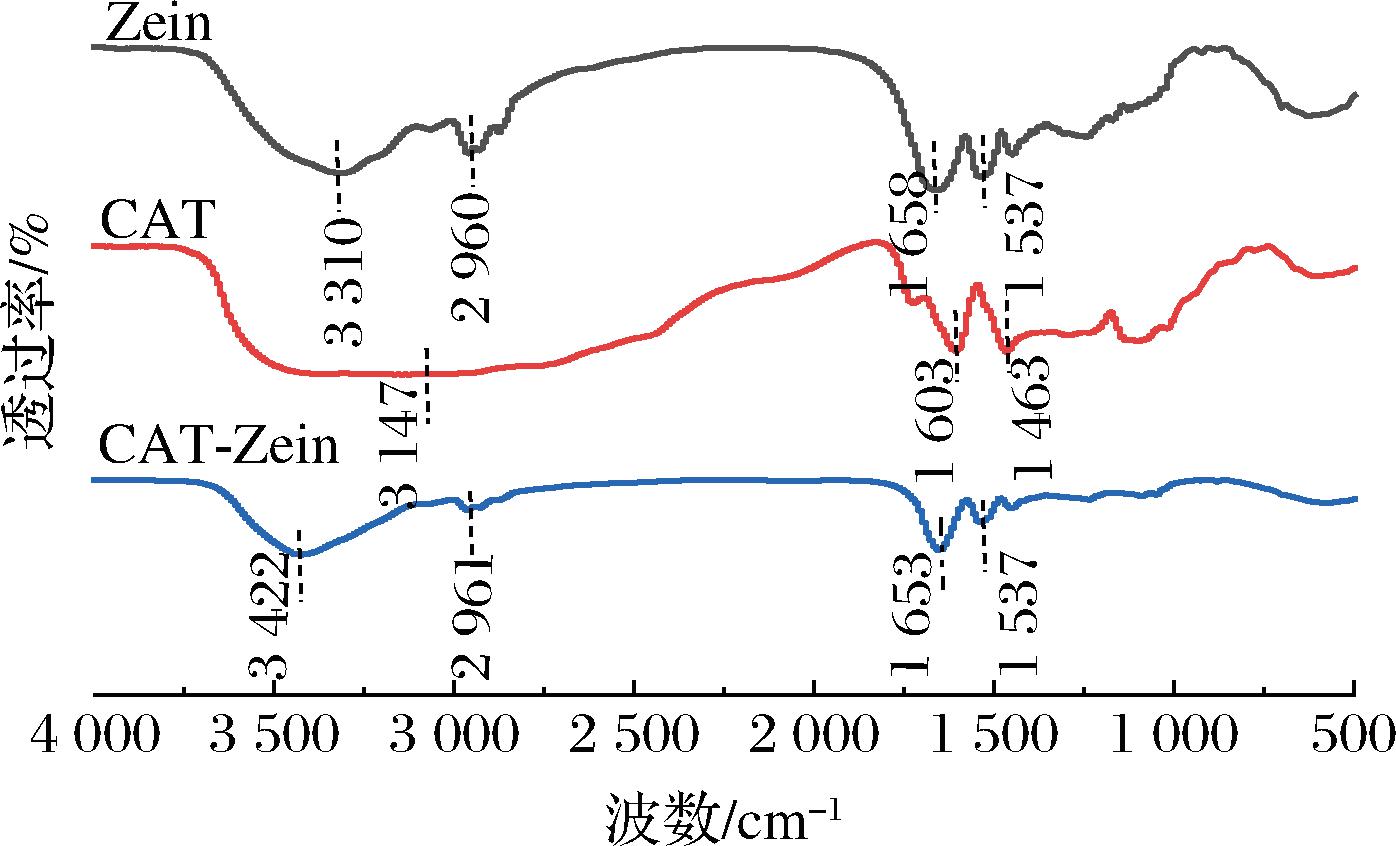
图4 玉米醇溶蛋白(Zein)、阳离子单宁(CAT)和CAT-Zein纳米颗粒的FTIR光谱图
Fig.4 FTIR spectra of Zein,CAT,and CAT-Zein nanoparticles
2.4 DSC测试结果分析
本文采用DSC来研究CAT-Zein纳米颗粒中CAT的添加对Zein热特性的影响,所得DSC曲线如图5所示。从图中可以看出Zein的特征吸热峰分布在100~140 ℃[29],而CAT的特征吸热峰则在100~175 ℃。这可能与聚合物中水的蒸发有关,亲水性CAT的吸热峰温度高于疏水性的Zein,这可能是因为CAT分子与水分子之间的亲和力较强[30]。该结果与LUO等[31]研究的亲水性羧甲基纤维素与疏水性的玉米醇溶蛋白的热特性一致。在CAT-Zein纳米颗粒的DSC曲线中,CAT的特征峰消失,并且在265.5 ℃ 出现新的特征吸热峰,说明CAT在制成纳米颗粒后其分子存在状态发生了改变。此研究结果表明CAT与Zein已经形成了一种新的复合物,而不仅仅是简单的物理混合,意味着Zein成功与CAT相结合形成了纳米颗粒。
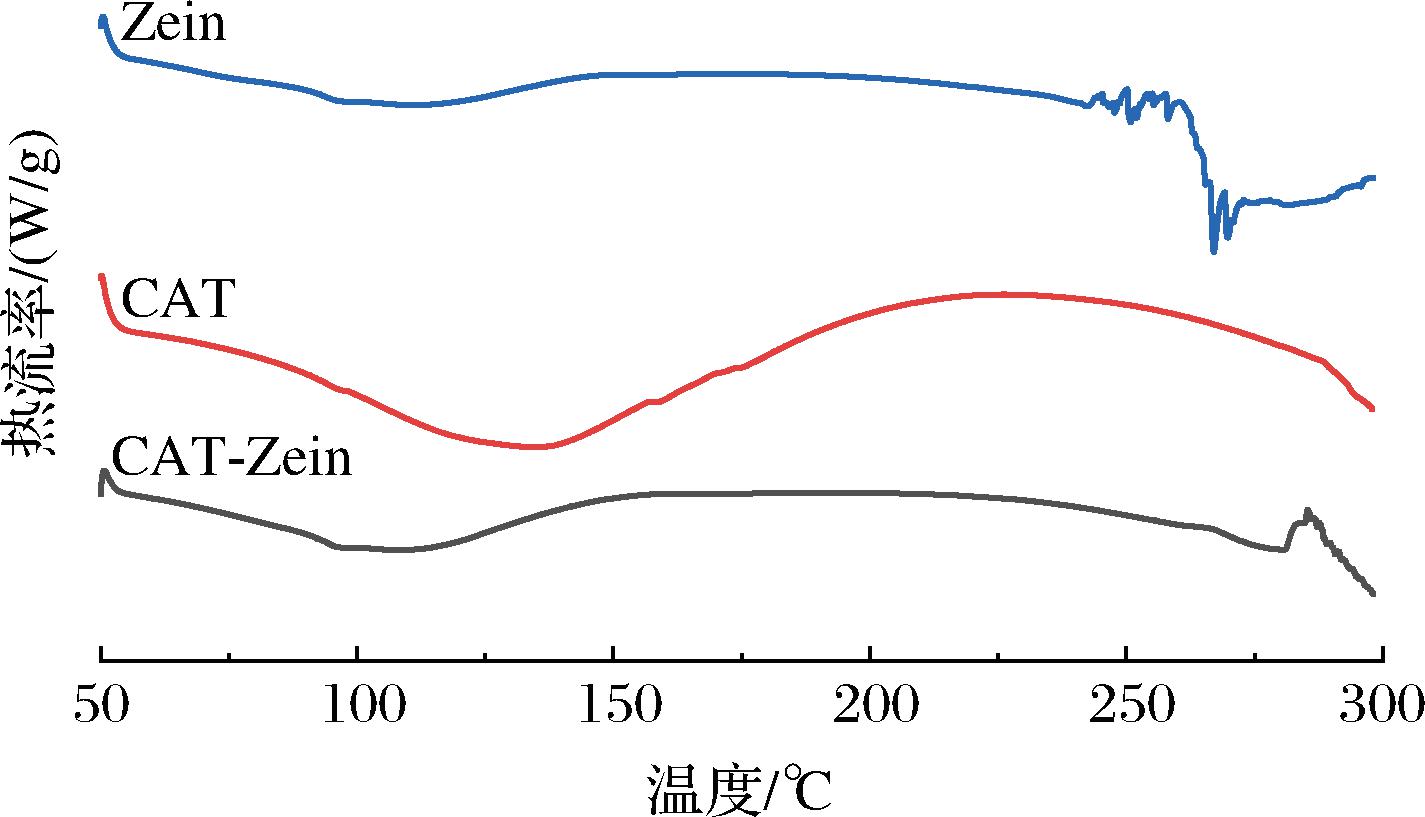
图5 玉米醇溶蛋白(Zein)、阳离子单宁(CAT)和CAT-Zein的DSC谱图
Fig.5 DSC spectra of Zein,CAT,and CAT-Zein nanoparticles
2.5 XRD测试结果分析
XRD法是一种通过X射线在晶体中的衍射现象分析物质结构的方法。本文中用XRD分析了Zein和CAT形成纳米颗粒前后的晶体结构的变化,结果如图6所示。在对Zein谱图的观察中,于9.1°和19.6°处分别存在与三螺旋晶体结构及无定形部分相关的特征峰[32]。24.52°处的宽峰表明CAT处于非晶态[33]。值得注意的是,当Zein与CAT形成CAT-Zein复合时,峰的位置与单独的Zein样品基本一致,但这些特征峰的强度普遍减弱,此结果表明,单宁的加入使得晶面直径减小,但对晶面间距没有显著影响[34]。这种现象可能源于CAT的引入导致Zein的晶体结构或分子排列发生了显著变化,改变了Zein分子之间的相互作用力,从而导致某些特征峰的强度降低,此结果与先前关于玉米醇溶蛋白与其他亲水性物质结合的XRD检测结果一致[35]。该结果为Zein与CAT之间的非共价作用力提供了有力的证据,与上述的FTIR、DSC的检测结果具有一致性,证明了CAT-Zein纳米颗粒的成功制备。
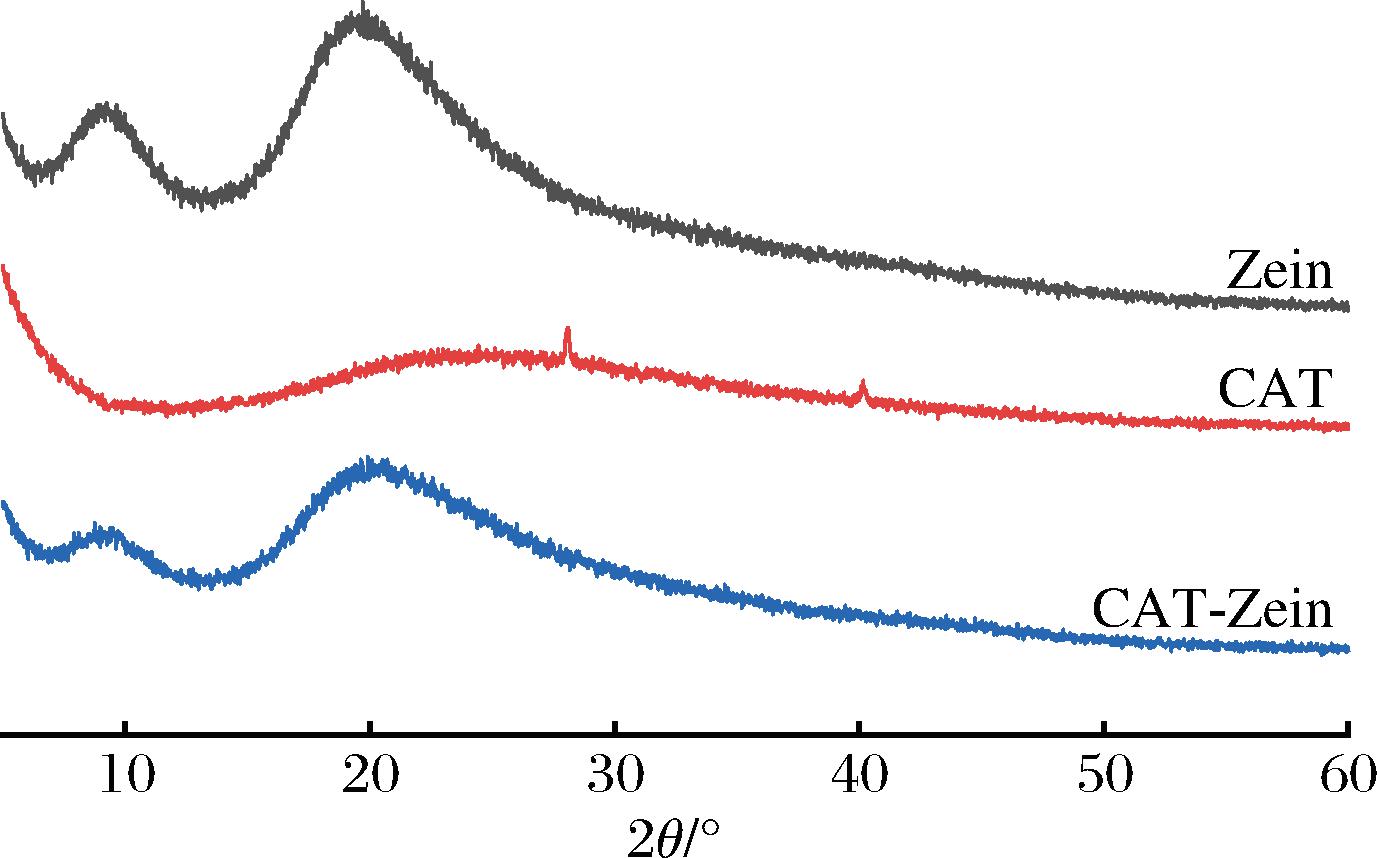
图6 玉米醇溶蛋白(Zein)、阳离子单宁(CAT)和CAT-Zein的XRD谱图
Fig.6 XRD patterns of Zein,CAT,and CAT-Zein nanoparticles
2.6 CAT-Zein纳米颗粒和Zein纳米颗粒的贮藏性能
为研究不同温度下CAT-Zein纳米颗粒和Zein纳米颗粒的贮藏稳定性,分别将新鲜制备好的纳米颗粒放置于4 ℃和25 ℃下贮存28 d,分别在第0、7、14、21、28天对Zein纳米颗粒和CAT-Zein纳米颗粒进行取样,测定其粒径、PDI和zeta电位,并对测定的数据进行分析,结果如图7所示。结果表明,在贮藏28 d内,2种纳米颗粒在4、25 ℃下平均粒径均在100 nm 左右,与初制备时无显著性变化。纳米颗粒粒径的PDI则始终小于0.5。这表明纳米粒子在长期贮存中,一直处于稳定分散状态,未产生明显的聚集。另外,在不同温度条件下贮存的CAT-Zein纳米颗粒和Zein纳米颗粒的zeta电位基本处于较高正电荷的状态,这也是2种纳米颗粒能够长期稳定,未聚集的原因之一。因此,CAT-Zein纳米颗粒和Zein纳米颗粒均具有良好的贮藏稳定性,使得其在实际应用中具有很大的潜力和可行性。
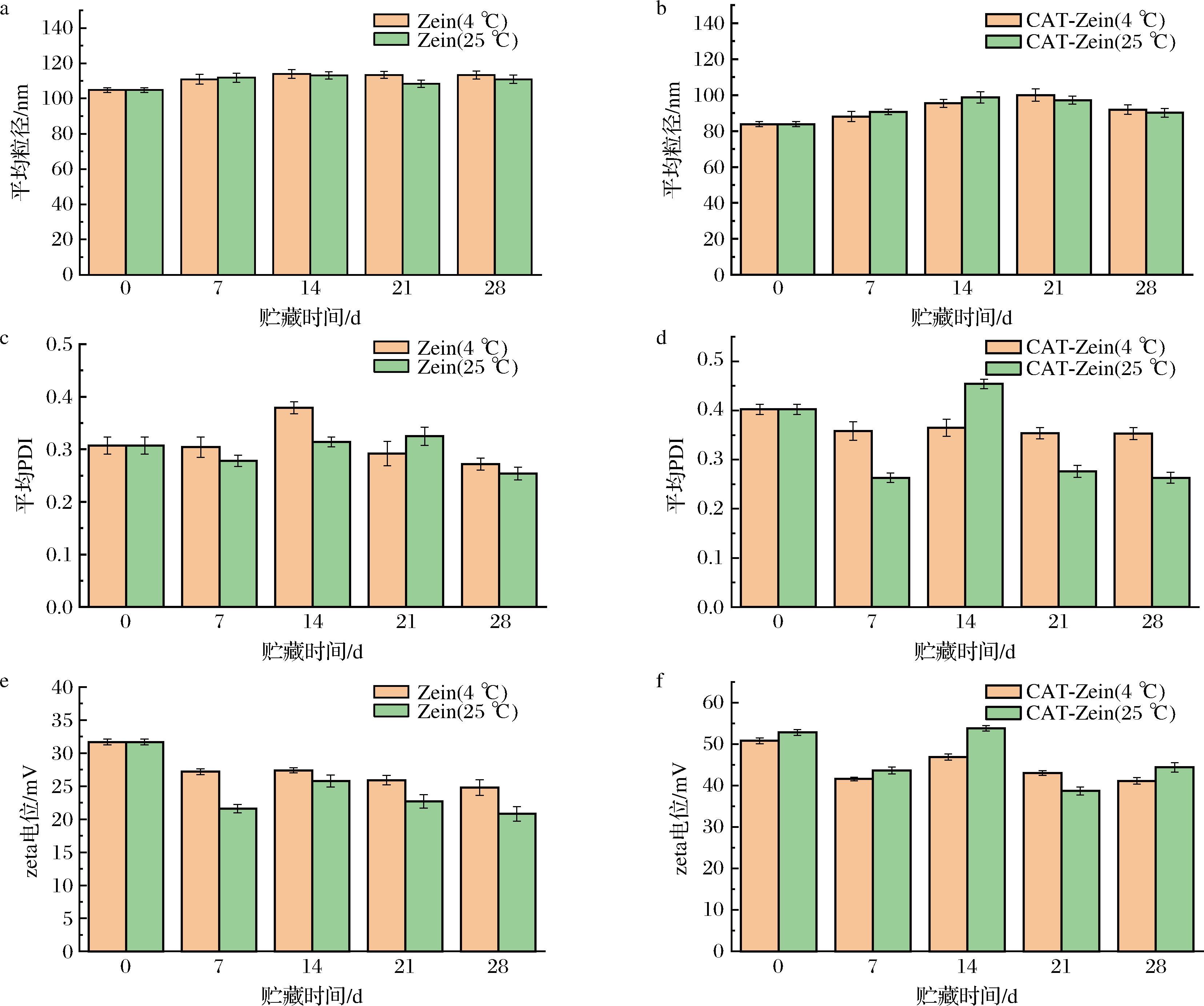
a-Zein纳米颗粒的粒径变化;b-CAT-Zein纳米颗粒的粒径变化;c-Zein纳米颗粒的PDI变化;d-CAT-Zein纳米颗粒的PDI变化;e-Zein纳米颗粒的Zeta电位变化;f-CAT-Zein纳米颗粒的Zeta电位变化
图7 CAT-Zein纳米颗粒和Zein纳米颗粒在贮藏28 d的粒径、PDI、zeta电位的变化
Fig.7 Changes in particle size,PDI,and zeta potential of Zein nanoparticles and CAT-Zein nanoparticles at 28 days of storage
2.7 CAT-Zein纳米颗粒和Zein纳米颗粒的抗生素去除效果
本文以头孢噻吩钠作为水体中头孢类抗生素的模型污染物。首先,使用紫外分光光度计在254 nm的波长下检测梯度浓度的头孢噻吩钠样品对应的吸光度,并拟合曲线。得到标准曲线如图8所示,曲线方程为:y=0.399 6x-0.015 2,R2=0.999 4,标准曲线线性关系良好。
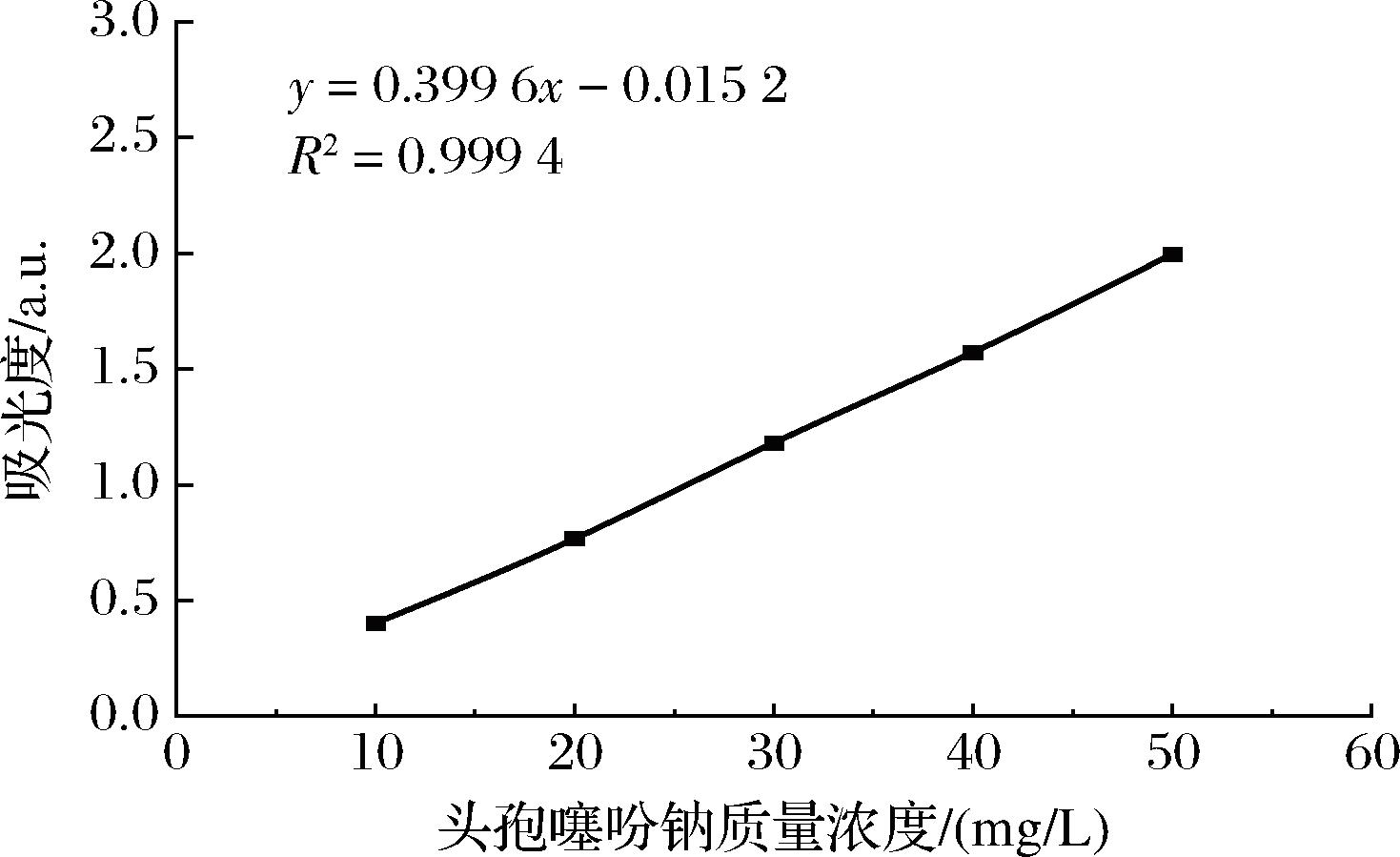
图8 紫外吸光度-头孢噻吩钠质量浓度标准曲线
Fig.8 Standard curve of UV absorbance with concentration of cefotephene sodium
CAT-Zein纳米颗粒和Zein纳米颗粒对水样中的头孢噻吩钠的去除效果如图9所示。CAT-Zein纳米颗粒对头孢噻吩钠的去除率为80.18%,去除效果良好,且相对于对照样Zein纳米颗粒的41.23%的去除率,显著提高。说明Zein纳米颗粒对头孢噻吩钠有一定的去除效果,而在其与阳离子单宁形成新的复合纳米体系后,去除效果大幅提升,这可能因为阳离子单宁的加入,增加了纳米体系的正电荷密度,同时给纳米体系提供了更多的能与抗生素分子相互作用的羟基等活性基团。
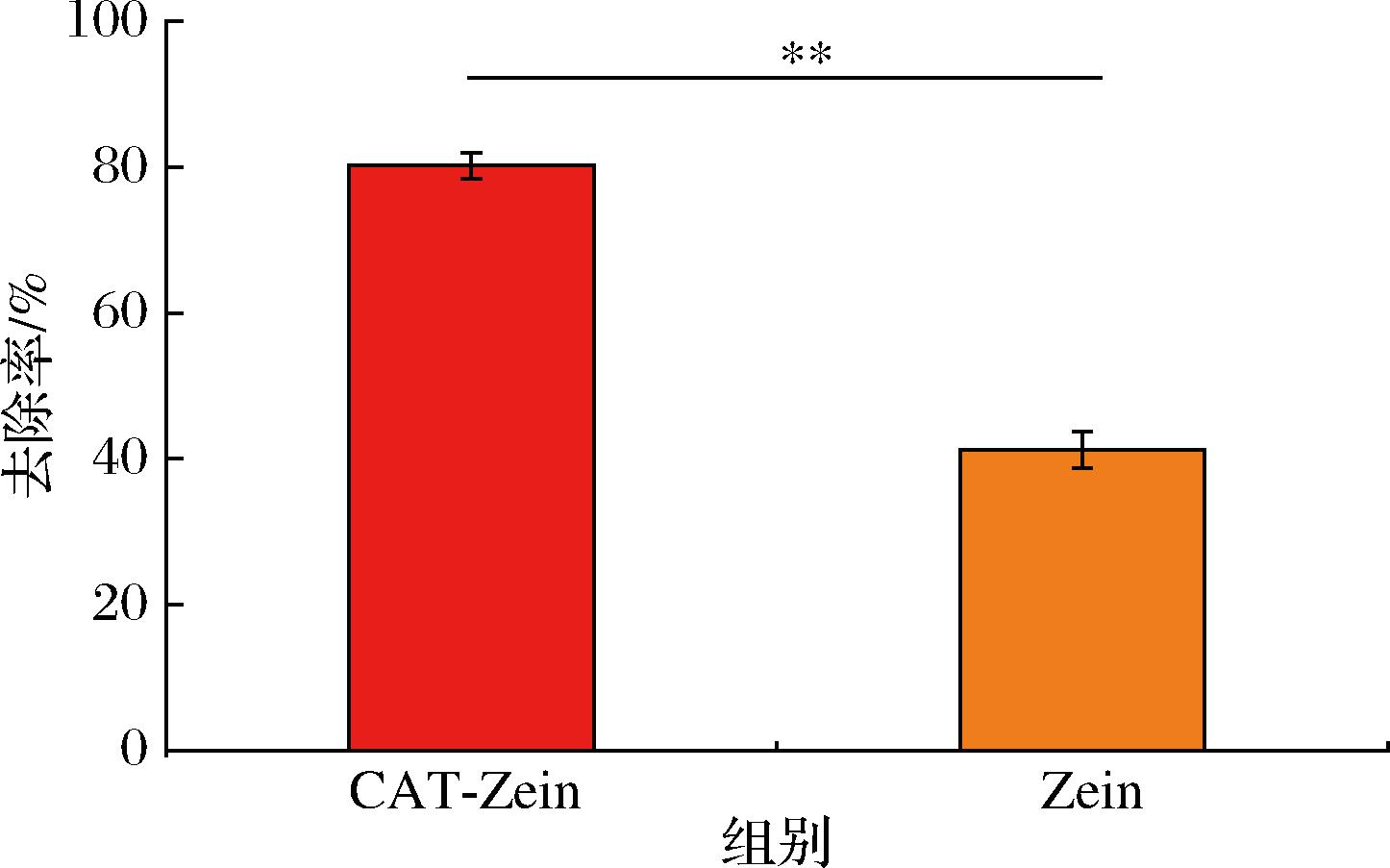
图9 CAT-Zein纳米颗粒和Zein纳米颗粒的抗生素去除效果比较
Fig.9 Comparison of antibiotic removal effects between Zein nanoparticles and CAT-Zein nanoparticles
注:**表示P<0.01。
2.8 pH对CAT-Zein 纳米颗粒的抗生素去除效果的影响
由于添加阳离子单宁,形成的二元复合CAT-Zein纳米颗粒对水体中头孢类抗生素头孢噻吩钠的去除效果显著增强,为了探究其内在机理,进一步对不同pH值下CAT-Zein 纳米颗粒的粒径、PDI、zeta电位进行了测试,并考察其与对应pH值下头孢噻吩钠去除率之间的关联性。
如表2所示,CAT-Zein纳米颗粒在所测的pH范围内,粒径几乎都在近100 nm,且PDI小于或接近0.5,分散程度良好。CAT-Zein纳米颗粒的zeta电位,在pH 3.0~7.0,随着pH值的增加逐渐上升,在pH=6.0时达到最大然后逐渐下降,在pH>8.0时纳米颗粒呈负电荷。此zeta电位的趋势结果,可能是因为玉米醇溶蛋白的等电点为6.2[21],而CAT-Zein复合纳米颗粒是在玉米醇溶蛋白的基础上进一步引入了阳离子单宁,因此,纳米体系在pH 3.0~7.0范围内会呈现出较高的正电荷。而pH=7.0时zeta电位下降,可能是此时的pH略大于玉米醇溶蛋白的等电点,使其所带电荷下降为近中性或弱负电荷,而阳离子单宁仍携带正电荷,导致体系的总体电荷下降。在pH 8.0~11.0时溶液的pH逐渐上升,溶液的碱性也随之增强,复合纳米颗粒也呈现出负电荷。
表2 不同pH下CAT-Zein纳米颗粒粒径、PDI和zeta电位表征结果
Table 2 Particle size,PDI,and zeta potential results of CAT-Zein nanoparticles at different pH
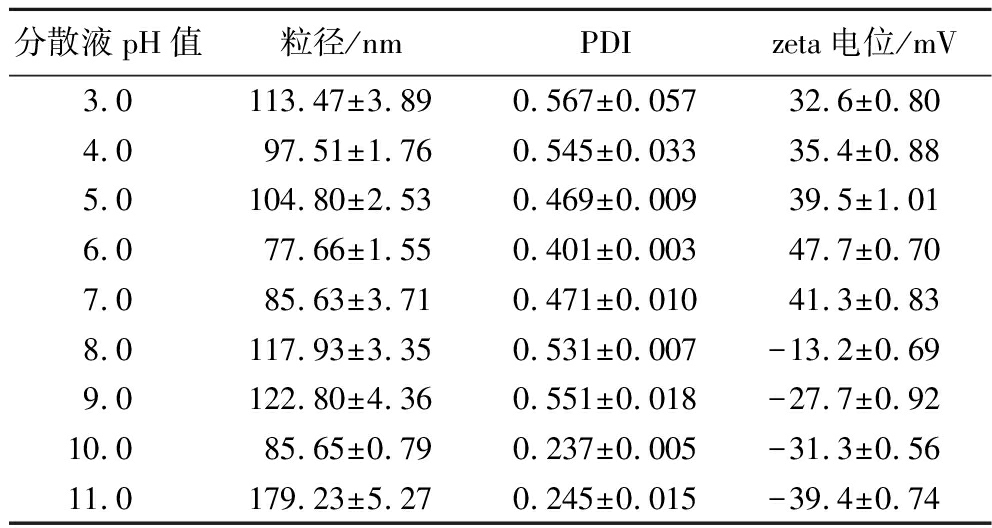
分散液pH值粒径/nmPDIzeta电位/mV3.0113.47±3.890.567±0.05732.6±0.804.097.51±1.760.545±0.03335.4±0.885.0104.80±2.530.469±0.00939.5±1.016.077.66±1.550.401±0.00347.7±0.707.085.63±3.710.471±0.01041.3±0.838.0117.93±3.350.531±0.007-13.2±0.699.0122.80±4.360.551±0.018-27.7±0.9210.085.65±0.790.237±0.005-31.3±0.5611.0179.23±5.270.245±0.015-39.4±0.74
pH值对于CAT-Zein纳米颗粒的抗生素去除效果的影响结果如图10所示。根据文献报道[36-37],头孢噻吩钠等头孢类抗生素都有羧基的存在,所以它们的pKa都相对较低,在pH>3.0的大多数pH范围内都会呈现负电荷。因此,在酸性条件下,带高正电荷的CAT-Zein纳米颗粒与带负电荷的头孢噻吩钠之间,具有强烈的静电吸引力。所以,在pH 3.0~6.0范围内随着CAT-Zein纳米颗粒zeta电位的逐渐上升,CAT-Zein纳米颗粒对头孢噻吩钠的去除率也呈上升趋势,当pH=6.0时,zeta电位达到了最大值,此时抗生素去除率效果也为最佳,达到近90%。另外,zeta电位绝对值越大,纳米颗粒的稳定性越高,分散性越好,这也有利于吸附质在纳米颗粒表面的固定和吸附,进一步优化了头孢噻吩钠的去除效果。而pH 7.0~11.0时去除率呈一个下降趋势,而这与溶液的电位值变化趋势相符合,即纳米颗粒与头孢噻吩钠之间静电引力下降。但可能因为纳米颗粒自身的吸附效应,在较高pH值(10.0~11.0)时,CAT-Zein纳米颗粒对头孢噻吩钠的去除率仍然在50%以上。
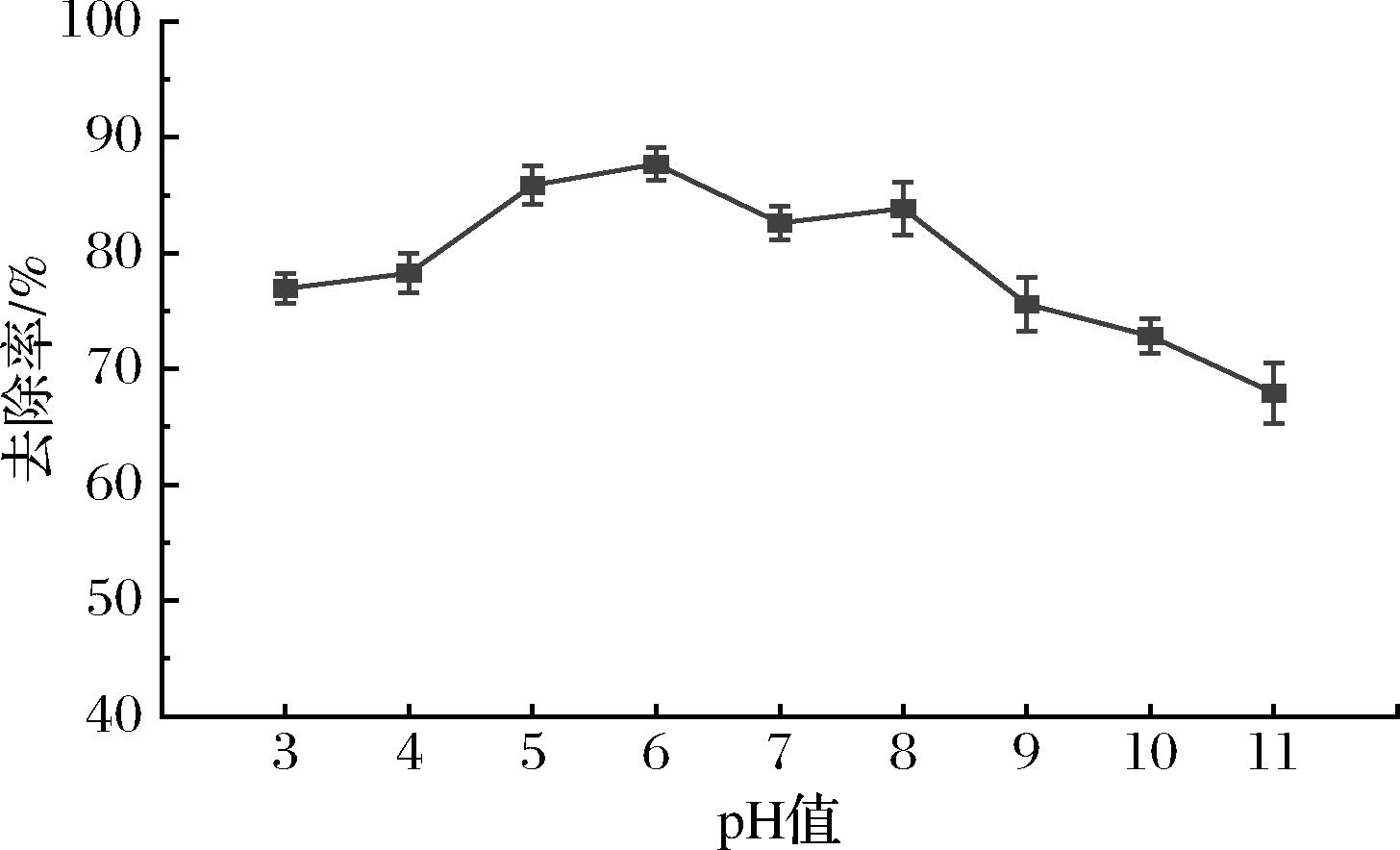
图10 不同pH值下CAT-Zein纳米颗粒对头孢噻吩钠的去除率
Fig.10 Removal rates of sodium cefathiophene by CAT-Zein nanoparticles at different pH levels
3 结论
本文研究了如何制备新型CAT-Zein纳米颗粒并对其进行表征,进一步对其在抗生素废水处理中的应用进行考察。首先,成功制备CAT-Zein纳米颗粒,FTIR、DSC、XRD等表征结果显示阳离子单宁和玉米醇溶蛋白之间通过氢键以及疏水作用力等分子间非共价作用力相互作用,形成了一种新型的复合纳米体系。CAT-Zein纳米颗粒平均粒径为81.34 nm,平均PDI为0.353,平均zeta电位为56.8 mV,微观形貌呈近球形的纳米颗粒状。CAT-Zein纳米颗粒以及其对照样Zein纳米颗粒在4 ℃和25 ℃贮存条件下,28 d内保持稳定分散状态,无明显聚集,显示出良好的贮存稳定性。在复合了阳离子单宁后,CAT-Zein纳米颗粒对头孢噻吩钠的去除率相较于Zein纳米颗粒显著提高。且研究发现pH值是CAT-Zein纳米颗粒对头孢类抗生素去除效果的重要影响因素,pH值可通过调整CAT-Zein纳米颗粒的表面电荷,来影响纳米颗粒和抗生素之间的静电引力,从而进一步影响抗生素的去除效果。当pH=6.0时,CAT-Zein纳米颗粒对头孢噻吩钠的去除效果最好,达到近90%的去除率,此结果与CAT-Zein在不同pH值下的zeta电位趋势一致。本研究中CAT-Zein纳米体系的成功构建突破了单宁在水处理应用中的局限性,并显示出在水体中头孢类抗生素高效的去除能力。另一方面,本研究中使用的玉米醇溶蛋白以及单宁均为植物来源,具有优越的生物相容性和可生物降解性,且纳米体系的制备方法温和,无有毒化学试剂的参与,为开发绿色环保的水处理材料提供了新的思路。
[1] GU D M,FENG Q Y,GUO C S,et al.Occurrence and risk assessment of antibiotics in manure,soil,wastewater,groundwater from livestock and poultry farms in Xuzhou,China[J].Bulletin of Environmental Contamination and Toxicology,2019,103(4):590-596.
[2] JOAKIM LARSSON D G,FLACH C F.Antibiotic resistance in the environment[J].Nature Reviews Microbiology,2022,20(5):257-269.
[3] MUHAMMAD S,ABDUL KHALIL H P S,ABD HAMID S,et al.Insights into agricultural-waste-based nano-activated carbon fabrication and modifications for wastewater treatment application[J].Agriculture,2022,12(10):1737.
[4] WANG J L,ZHUAN R.Degradation of antibiotics by advanced oxidation processes:An overview[J].Science of the Total Environment,2020,701:135023.
[5] KUMAR M,JAISWAL S,SODHI K K,et al.Antibiotics bioremediation:Perspectives on its ecotoxicity and resistance[J].Environment International,2019,124:448-461.
[6] SOON W L,PEYDAYESH M,MEZZENGA R,et al.Plant-based amyloids from food waste for removal of heavy metals from contaminated water[J].Chemical Engineering Journal,2022,445:136513.
[7] TADELE D T,ISLAM M S,MEKONNEN T H.Zein-based nanoparticles and nanofibers:Co-encapsulation,characterization,and application in food and biomedicine[J].Trends in Food Science &Technology,2025,155:104809.
[8] ESMALI F,ARANI M N,BETMOUSHOUL E,et al.Harnessing the power of hollow zein nanoparticles for enhanced antifouling and heavy metal removal of polyethersulfone membranes[J].Journal of Environmental Chemical Engineering,2024,12(5):113381.
[9] WEN H F,YANG C,YU D G,et al.Electrospun zein nanoribbons for treatment of lead-contained wastewater[J].Chemical Engineering Journal,2016,290:263-272.
[10] TENG D F,XU Y Q,ZHAO T N,et al.Zein adsorbents with micro/nanofibrous membrane structure for removal of oils,organic dyes,and heavy metal ions in aqueous solution[J].Journal of Hazardous Materials,2022,425:128004.
[11] WANG Y H,DU Y C,LIANG C,et al.One-step preparation of macroporous zein microspheres by solvent diffusion for dye adsorption[J].Separation and Purification Technology,2022,302:122112.
[12] ZHANG L L,GUAN Q H,JIANG J C,et al.Tannin complexation with metal ions and its implication on human health,environment and industry:An overview[J].International Journal of Biological Macromolecules,2023,253:127485.
[13] 周鹏,张建芳,欧丽君,等.单宁基阳离子型吸附树脂的制备及吸附性能研究[J].水处理技术,2018,44(8):53-56.ZHOU P,ZHANG J F,OU L J,et al.Research on preparation and adsorption property of tannin based cationic adsorbent resin[J].Technology of Water Treatment,2018,44(8):53-56.
[14] 侯俊,刘佳林,潘正国,等.改性植物单宁絮凝剂对污水中抗生素抗性基因的去除效果[J].水资源保护,2023,39(2):244-251;258.HOU J,LIU J L,PAN Z G,et al.Removal effect of modified plant tannin flocculant on antibiotic resistance genes in sewage[J].Water Resources Protection,2023,39(2):244-251;258.
[15] GREHS B W N,LOPES A R,MOREIRA N F F,et al.Removal of microorganisms and antibiotic resistance genes from treated urban wastewater:A comparison between aluminium sulphate and tannin coagulants[J].Water Research,2019,166:115056.
[16] TOMASI I T,MACHADO C A,BOAVENTURA R A R,et al.Tannin-based coagulants:Current development and prospects on synthesis and uses[J].Science of the Total Environment,2022,822:153454.
[17] S NCHEZ-MART
NCHEZ-MART N J,BELTR
N J,BELTR N-HEREDIA J,GIBELLO-PÉREZ P.Adsorbent biopolymers from tannin extracts for water treatment[J].Chemical Engineering Journal,2011,168(3):1241-1247.
N-HEREDIA J,GIBELLO-PÉREZ P.Adsorbent biopolymers from tannin extracts for water treatment[J].Chemical Engineering Journal,2011,168(3):1241-1247.
[18] 王金霞,王家薇,王开俊,等.玉米醇溶蛋白-槲皮素互作机制及其纳米颗粒的制备[J].中国粮油学报,2024,39(9):163-171.WANG J X,WANG J W,WANG K J,et al.Zein-quercetin nanoparticles:Interaction mechanism and preparation[J].Journal of the Chinese Cereals and Oils Association,2024,39(9):163-171.
[19] 刘欢.γ-Al2O3负载铁氧化物对头孢曲松钠吸附性能的研究[D].南昌:南昌大学,2022.LIU H.Study on adsorption performance of γ-Al2O3 supported iron oxide for ceftriaxone sodium[D].Nanchang:Nanchang University,2022.
[20] SUN C X,LIU F G,YANG J,et al.Physical,structural,thermal and morphological characteristics of zeinquercetagetin composite colloidal nanoparticles[J].Industrial Crops and Products,2015,77:476-483.
[21] 常大伟,曹佳怡,任娜,等.负载二氢杨梅素的玉米醇溶蛋白-阿拉伯胶纳米粒子的制备及分析[J].食品工业科技,2025,46(12):30-40.CHANG D W,CAO J Y,REN N,et al.Zein-gum arabic loaded with dihydromyricetin:Preparation and analysis of nanoparticles[J].Science and Technology of Food Industry,2025,46(12):30-40.
[22] SONG H D,HE A J,GUAN X,et al.Fabrication of chitosan-coated epigallocatechin-3-gallate (EGCG)-hordein nanoparticles and their transcellular permeability in Caco-2/HT29 cocultures[J].International Journal of Biological Macromolecules,2022,196:144-150.
[23] HE A J,GUAN X,SONG H D,et al.Encapsulation of (-)-epigallocatechin-gallate (EGCG) in hordein nanoparticles[J].Food Bioscience,2020,37:100727.
[24] TAO W,FERREIRA I M P L V O,HE J R,et al.Tailored zein-polysaccharide nanoparticles for anthocyanin encapsulation:Insights into preparation and characterization[J].Food Hydrocolloids,2025,166:111365.
[25] HE J B,TANG H,LIAO R F,et al.Gemini surfactant stabilized zein nanoparticles:Preparation,characterization,interaction mechanism,and antibacterial activity[J].International Journal of Biological Macromolecules,2025,305:141264.
[26] 孙翠霞.基于玉米醇溶蛋白的复合胶体颗粒制备、表征及其应用[D].北京:中国农业大学,2018.SUN C X.Fabrication,characterization and application of zein-based composite colloidal particles[D].Beijing:China Agricultural University,2018.
[27] 李文洁,赵渊,付连霏,等.负载柚皮素的表没食子儿茶素没食子酸酯共价修饰的玉米醇溶蛋白-透明质酸复合纳米颗粒的构建与表征[J].食品与发酵工业,2024,50(17):139-147.LI W J,ZHAO Y,FU L F,et al.Fabrication and characterization of naringenin-loaded gallocatechin-gallate covalently modified zein-hyaluronic acid composite nanoparticles[J].Food and Fermentation Industries,2024,50(17):139-147.
[28] SUN C X,DAI L,GAO Y X.Interaction and formation mechanism of binary complex between zein and propylene glycol alginate[J].Carbohydrate Polymers,2017,157:1638-1649.
[29] 任晓鸣.玉米醇溶蛋白与玉米肽复合纳米颗粒制备及其输送、抗氧化性质研究[D].广东:华南理工大学,2014.REN X M.Preparation of zein or corn peptides composite nanoparticles and its delivery and antioxidant properties[D].Guangdong:South China University of Technology,2014.
[30] PARVEEN S,MITRA M,KRISHNAKUMAR S,et al.Enhanced antiproliferative activity of carboplatin-loaded chitosan-alginate nanoparticles in a retinoblastoma cell line[J].Acta Biomaterialia,2010,6(8):3120-3131.
[31] LUO Y C,TENG Z,WANG Q.Development of zein nanoparticles coated with carboxymethyl chitosan for encapsulation and controlled release of vitamin D3[J].Journal of Agricultural and Food Chemistry,2012,60(3):836-843.
[32] AHAMMED S,LIU F,KHIN M N,et al.Improvement of the water resistance and ductility of gelatin film by zein[J].Food Hydrocolloids,2020,105:105804.
[33] XIA Q L,LIANG Y,CAO A L,et al.Preparation and characterization of pH-responsive metal-polyphenol structure coated nanoparticles[J].Food Science and Human Wellness,2024,13(3):1303-1310.
[34] DE OLIVEIRA MORI C L S,ALMEIDA DOS PASSOS N,OLIVEIRA J E,et al.Electrospinning of zein/tannin bio-nanofibers[J].Industrial Crops and Products,2014,52:298-304.
[35] SUN C X,DAI L,GAO Y X.Binary complex based on zein and propylene glycol alginate for delivery of quercetagetin[J].Biomacromolecules,2016,17(12):3973-3985.
[36] 张祥海.碳酸氢盐辅助CoxSy/γ-Al2O3催化过氧化氢降解头孢类抗生素的研究[D].北京:北京化工大学,2023.ZHANG X H.Bicarbonate-assisted CoxSy/γ-Al2O3 catalyzed hydrogen peroxide degradation of cephalosporin antibiotics[D].Beijing:Beijing University of Chemical Technology,2023.
[37] RIBEIRO A R,SCHMIDT T C.Determination of acid dissociation constants (pKa) of cephalosporin antibiotics:Computational and experimental approaches[J].Chemosphere,2017,169:524-533.