大米是我国主要粮食作物之一,米糠作为大米加工的副产物,每年约产生数百万吨。研究表明,米糠含有多种营养物质和活性成分,主要有膳食纤维、油脂、多酚、黄酮、γ-氨基丁酸等,具有抗氧化、调节睡眠,预防癌症、糖尿病、心血管疾病等作用[1]。目前对于米糠的利用主要是从中提取富含γ-谷维素、生育酚的米糠油,或是将米糠可溶性膳食纤维作为添加剂加入到饼干中,阻碍饼干中面筋网络结构的形成,使其更加松散,并降低了饼干引起的餐后血糖水平[2-3]。但对米糠富含的酚类物质的利用较少,米糠中的酚类物质多以氢键、酯键与不溶性膳食纤维形成强相互作用,难以释放和提取,导致对其的利用率较低[4]。有研究利用复合酶对米糠进行酶解,通过破坏细胞壁来促进酚类物质的提取和释放[5]。但酶解无法实现对米糠的大批量处理,成本较高且有试剂残留风险。此外,新鲜米糠中富含的油脂和脂肪酶,使得其在贮藏过程中易快速酸败,限制其后续加工利用[6]。目前对米糠的稳定化方法包括低温冷藏、热处理、酶处理、化学处理等,区别于其他处理方法,热处理操作简单、成本低、无试剂残留,处理过程中产生的高温、高压、高剪切力能够通过钝化脂肪酶活性来实现样品的稳定化,更适用于米糠大批量加工[7]。
热处理也是目前农产品加工的常用方法。研究提出对甘薯、薏仁麸皮、荞麦麸皮进行热处理后,其紧密的细胞壁结构被破坏,纤维素、半纤维素发生降解,可溶性膳食纤维含量增加,同时促进了酚类物质的释放,引起多酚含量增加,抗氧化活性增强[8-10]。米糠常用的热处理方法有汽爆膨化(steam explosion,SE)、挤压膨化(extrusion explosion,EE)、微波加热(microwave heating,MH)、蒸汽加热(steam heating,SH)等[11-12]。目前相关研究多围绕米糠蛋白、米糠膳食纤维、米糠油等成分展开,对米糠中酚类物质等的研究较少[2,12-13]。此外,现有研究仅探讨了单一热处理方式对米糠酚类物质的影响,鲜少对比不同热处理方式对其作用机制的差异[14]。基于此,本研究以新鲜米糠作为原料,分别进行SE、EE、MH、SH处理,详细分析不同热处理方式在米糠膳食纤维、游离氨基酸、多酚、黄酮、γ-氨基丁酸、贮藏性能等方面影响的差异性,筛选出既能促进酚类等活性成分释放,又能减少热敏性物质损失的热处理方法,以期更好实现米糠的高值化加工。
1 材料与方法
1.1 材料与试剂
米糠,重庆涪陵渝妹儿米业集团有限公司;大豆油,中粮福临门食品营销有限公司;纤维素含量检测试剂盒、半纤维素含量检测试剂盒、考马斯亮蓝(G250)、福林酚试剂,北京索莱宝科技有限公司;γ-氨基丁酸、没食子酸、芦丁、β-巯基乙醇、硼酸盐缓冲液,上海源叶生物科技有限公司;实验所用其他试剂均为分析纯,成都科隆化学品有限公司。
1.2 仪器与设备
QB-200汽爆机组,清正生态科技(苏州)有限公司;MG65-30双螺杆挤压膨化机,山东铭本机械科技有限公司;EG823LA6-N微波炉,美的微波炉制造公司;CM-5台式分光测色仪,日本柯尼卡美能达公司;Phenom Pro10102扫描电镜,荷兰Phenom World公司;BSC-150恒温恒湿箱,上海博讯实业有限公司;BIOTEK酶标仪,美国基因公司;Mastersizer 3000激光粒度仪,英国马尔文公司;LC-20A高效液相色谱仪,日本岛津公司;Biochrom30+全自动氨基酸分析仪,英国Biochrom公司。
1.3 实验方法
1.3.1 热处理米糠的制备
对照组米糠:新鲜米糠置于烘箱中平衡水分至10%左右,过60目筛后,装入密封袋置于4 ℃冰箱保存,记为CK组。
汽爆膨化米糠:米糠采用汽爆膨化设备在1.8 MPa下加热60 s,然后迅速打开设备释放蒸汽。取出后平衡水分至10%左右,冷却后进行粉碎,过60目筛,装入密封袋置于4 ℃冰箱保存,记为SE组。
挤压膨化米糠:采用螺杆挤压机进行处理,米糠中加入质量分数为8%的水,混合均匀后,送入螺杆挤压机。机器参数设置如下:螺杆转速为1 300 r/min,2~7区温度分别设置为55、75、95、115、130、145 ℃,取出后平衡水分至10%左右,冷却后进行粉碎,过60目筛,装入密封袋置于4 ℃冰箱保存,记为EE组。
微波加热米糠:采用半封装微波法处理,将米糠水分调节至20%,称取100 g于耐高温密封袋中,半封口摊匀后放入微波炉中以5 W/g的微波强度处理150 s。取出后平衡水分至10%左右,冷却后进行粉碎,过60目筛,装入密封袋置于4 ℃冰箱保存,记为MH组。
蒸汽加热米糠:将米糠均匀平铺在蒸格上,厚度为1~2 cm,沸水蒸汽蒸20 min。取出后平衡水分至10%左右,冷却后进行粉碎,过60目筛,装入密封袋置于4 ℃冰箱保存,记为SH组。
1.3.2 粒度分布的测定
粒度分布是采用激光粒度仪进行测定。分散介质为去离子水,具体参数为:颗粒类型为非球形,遮光度为8%~12%,材料折射率为1.468 3,吸收率为0.01,分散剂折射率为1.33,搅拌速度为2 400 r/min。
1.3.3 色度测定
采用测色仪对样品的颜色进行测定,其中光圈设置为3 mm。将样品置于透明圆形密封盒中,轻轻振荡,使样品均匀分布,随后放入到仪器上进行测定。L*、a*、b*分别代表亮度、红-绿值以及蓝-黄值。
1.3.4 褐变程度
称取样品1.0 g于4 mL纯水中,振摇混匀后超声30 min。6 000 r/min离心10 min,取上清液在294 nm 和420 nm处测定吸光度。
1.3.5 微观结构
首先采用50 mL的正己烷对样品进行脱脂处理,以5 000 r/min离心10 min,去除上清液后置于通风橱过夜风干,随后装入密封袋并置于干燥器中干燥。经离子溅射喷金后置于扫描电镜10 kV电子束下分别放大800×和2 000×进行观察。
1.3.6 膳食纤维的测定
可溶性膳食纤维(soluble dietary fiber,SDF)、不溶性膳食纤维(insoluble dietary fiber,IDF)及总膳食纤维(total dietary fiber,TDF)的含量测定方法参考GB 5009.88—2023《食品安全国家标准 食品中膳食纤维的测定》。
1.3.7 纤维素、半纤维素含量的测定
纤维素、半纤维素含量分别参照索莱宝纤维素含量检测试剂盒、半纤维素含量检测试剂盒进行测定。
1.3.8 可溶性糖、总糖含量的测定
采用蒽酮-硫酸法[15]对米糠中的可溶性糖和总糖含量进行测定。
1.3.9 可溶性蛋白含量的测定
参考REKOWSKI等[16]的方法,采用Bradford法测定米糠中可溶性蛋白含量,0.1 g米糠中加入3 mL质量分数为0.9% NaCl溶液,冰浴条件下机械均质,10 000×g离心10 min。取100 μL上清液,加入2.0 mL 考马斯亮蓝(G250)显色剂,混匀后静置3 min,在595 nm处测定吸光度,并采用蛋白标准品绘制标准曲线。
1.3.10 游离氨基酸含量的测定
米糠中游离氨基酸的含量测定方法参考GB/T 30987—2020《植物中游离氨基酸的测定》。
1.3.11 多酚、黄酮的提取
参考谢勇[17]的方法,并进行修改。游离酚的提取:称取1.0 g样品于离心管中,加入20 mL体积分数为80%的冷冻乙醇溶液,磁力搅拌20 min,5 000 r/min离心10 min,收集上清液,重复提取3次。合并上清液,在45 ℃条件下旋转蒸干,用体积分数为80%的冷冻甲醇溶液将旋蒸产物定容至10 mL容量瓶中,0.45 μm有机滤膜进行过滤,获得游离酚提取液。结合酚的提取:向提取残留物中加入50 mL正己烷进行脱脂处理,超声1 h后,弃去上清液。在残渣中加入15 mL盐酸/甲醇溶液,70 ℃水浴振荡1 h,加入20 mL乙酸乙酯,涡旋振动后5 000 r/min离心10 min。重复3次,并合并上清液,在45 ℃条件下旋蒸,并用冷冻甲醇定容至10 mL容量瓶,提取液均贮存在-20 ℃冰箱直至使用。
1.3.12 多酚、黄酮含量的测定
参考谢勇[17]的方法,分别对米糠多酚、黄酮含量进行测定。多酚含量的测定:取100 μL提取液,加入100 μL福林酚试剂、400 μL纯水,反应6 min后,加入0.8 mL纯水和1.2 mL 75 g/L的碳酸钠,避光反应90 min,在760 nm波长处测定吸光度。以没食子酸为标准品,绘制标准曲线。黄酮含量的测定:取1 mL 提取液,加入0.3 mL 50 g/L的亚硝酸钠溶液、4 mL 纯水,涡旋后反应5 min,加入0.3 mL 100 g/L的硝酸铝溶液、2 mL 1 mol/L NaOH溶液。静置10 min后在510 nm处测定吸光度。以芦丁为标准品,绘制标准曲线。
1.3.13 γ-氨基丁酸含量的测定
参考LIU等[18]的方法,将0.5 g样品与5 mL 100 g/L的三氯乙酸混合均匀后,置于40 ℃水浴锅中保持2 h。10 000 r/min离心15 min,并通过0.45 μm 过滤器获取上清液。将提取液与400 μL硼酸盐缓冲液(0.4 mol/L,pH=10.4)混合均匀,并加入适量衍生试剂,在室温下反应5 min后,立即进样检测。
色谱柱:(250 mm×4.6 mm,5 μm);流动相A:0.02 mol/L 乙酸钠溶液(每1 000 mL溶液中加入200 μL三乙胺后,加入乙酸将pH值调节至7.3),流动相B:乙腈;洗脱梯度:流动相A:流动相B=80∶20(mL∶mL);流速0.8 mL/min;检测器:紫外检测器;检测波长338 nm;柱温40 ℃;进样量20 μL。
1.3.14 脂肪酶活动度的测定
参考GB/T 5523—2008《粮油检验 粮食、油料的脂肪酶活动度的测定》。
1.3.15 游离脂肪酸(free fatty acid,FFA)值的测定
参考梁兰兰等[19]的测定方法并略作修改。称取4.0 g样品于离心管中,加入50 mL乙醚乙醇混合液(体积比2∶1),混匀后,室温下振荡40 min。静置片刻,待上层清液澄清后采用快速滤纸进行过滤,弃去最初几滴滤液,收集于离心管中。移取10 mL提取液于锥形瓶中,再加入10 mL上述乙醚乙醇混合液。加入0.2 mL 10 g/L的酚酞乙醇溶液后,立即用0.05 mol/L KOH标准液进行滴定,直至出现微红色且30 s内不消失。记下所需KOH标准液的体积(V)。取10 mL上述乙醚乙醇混合液,并加入酚酞乙醇溶液0.2 mL,用KOH标准液进行滴定,记下所消耗的KOH标准液体积(V0),作为试剂空白。FFA值计算如公式(1)所示:
FFA值![]()
(1)
式中:V,样品滴定所需0.05 mol/L KOH标准液的量,mL;V0,试剂空白滴定所需0.05 mol/L KOH标准液的量,mL;N,滴定时所需KOH的浓度,mol/L;G,样品干基重,g;0.208,油酸的毫克当量数;50,乙醚乙醇提取液的量,mL;10,用于滴定的提取液的量,mL;17%,米糠样品平均含油量。
1.4 数据处理与分析
采用Microsoft Excel 2019统计数据、SPSS 25.0分析显著性、Origin 2021软件作图,实验结果表示为“平均值±标准差”。
2 结果与分析
2.1 粒径
不同热加工米糠经粉碎过筛后,其颗粒分布含量如图1所示。与对照组相比,热处理组米糠粒径分布呈明显的右移分布。其中SH组米糠粉的粒径变化最大,D50为104 μm,D[3,2]值为66.2 μm,最小的是未处理组,相应值分别为67.8 μm和22.4 μm,SE组、MH组、EE组的粒径也呈增加的趋势。这和目前相关研究具有相同的结果,热处理后粒径增大可能与淀粉糊化有关,糊化过程中米糠中淀粉颗粒吸收水分膨胀增大,从而导致米糠粒径的增大[17]。SH处理过程中,米糠中淀粉不断与蒸汽接触,使得SH组粒径变化最大。其次,构成米糠细胞壁的纤维素、半纤维素因热处理发生降解作用,导致米糠结构变得松散,并产生膨化效果,从而引起粒径的增大[20]。以上表明,热处理会引起米糠粒径发生不同程度的增加。
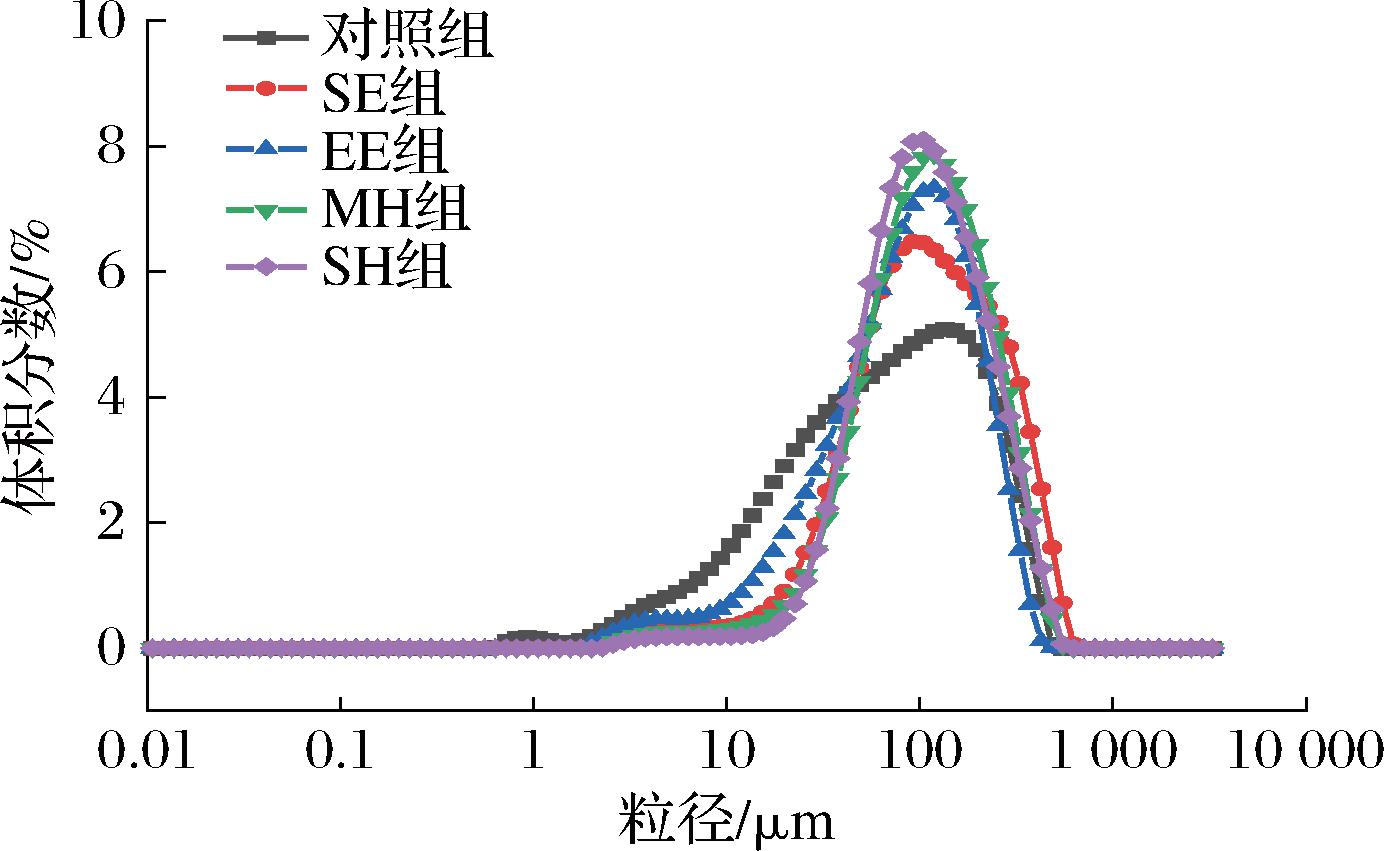
图1 不同热处理方式对米糠粒径的影响
Fig.1 Effects of different heat treatment methods on particle size of rice bran

图2 不同热处理方式对米糠颜色的影响
Fig.2 Effects of different heat treatment methods on color of rice bran
2.2 色度
测色仪可以反映不同样品之间的外观差异。如表1所示,热处理使米糠的L*值显著降低。从a*值来看,热处理米糠组a*值显著增加,表明颜色向红色发生转变。从b*值来看,米糠经热处理后,b*值显著增加,说明颜色均向黄色发生转变。这些颜色变化,一方面可能是由于热处理诱导美拉德反应产生棕色聚合物,另一方面可能是由于米糠脂肪发生热氧化引起[21]。褐变程度是由样品在294 nm和420 nm处的吸光度比值来表示,比值越低,褐变程度越明显,美拉德反应程度越深。除MH组外,其他3组米糠褐变程度变化显著,这可能是由于在高温、高压、高湿环境下,米糠中还原糖与氨基酸等氨基化合物发生美拉德反应程度更深引起[22]。以上结果表明,不同热处理方式会引起米糠发生不同程度的美拉德反应,并发生褐变。
表1 不同热处理方式对米糠颜色及褐变程度的影响
Table 1 Effects of different heat treatment methods on color and browning degree of rice bran
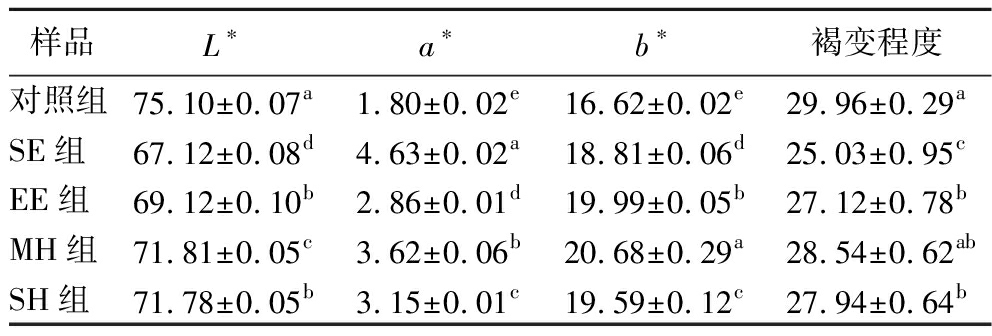
样品L∗a∗b∗褐变程度对照组75.10±0.07a1.80±0.02e16.62±0.02e29.96±0.29aSE组67.12±0.08d4.63±0.02a18.81±0.06d25.03±0.95cEE组69.12±0.10b2.86±0.01d19.99±0.05b27.12±0.78bMH组71.81±0.05c3.62±0.06b20.68±0.29a28.54±0.62abSH组71.78±0.05b3.15±0.01c19.59±0.12c27.94±0.64b
注:不同小写字母表示各组间差异显著(P<0.05)(下同)。
2.3 微观结构
由图3可知,热处理改变了米糠颗粒的形态。在放大800×时,对照组中米糠颗粒大部分呈块状且边缘结构完整。米糠颗粒表面的淀粉颗粒完整,呈现球形或椭球形。经热处理后,米糠颗粒完整性降低,米糠结构被破坏,边缘呈现不规则结构。淀粉颗粒发生糊化,球形或椭球形结构被破坏,并与其他组分融成一体,形貌完整的淀粉颗粒减少。此外,热处理后,米糠细胞壁结构发生不同程度的破坏,细胞壁变得疏松并发生破裂。放大2 000×时,热处理组米糠出现空隙结构,其中SE组和SH组可以观察到明显的薄层碎片。以上结果表明,热处理破坏米糠完整的细胞壁结构。疏松及空隙结构的形成能够增加米糠的比表面积,这可能有利于活性成分的溶出[23]。

图3 不同热处理方式对米糠微观结构的影响
Fig.3 Effects of different heat treatment methods on microstructure of rice bran
2.4 不同热处理方式对米糠膳食纤维组成和含量的影响
由图4可知,各组米糠膳食纤维主要成分是IDF,含量为31.06%~34.71%。与对照组相比,热处理后,IDF含量发生增加或减少,但未见显著性变化。另外,与对照组相比,除MH组外,热处理后米糠的SDF含量显著增加。其中,SE组和SH组增加最多,分别增加了69.96%、70.49%,EE组增加了40.98%,MH组增加最少,增加了10.30%。这可能是由于热处理不同程度上促进糖苷键的断裂,导致高分子多糖转化成为相对低分子的水溶性多糖,从而增加SDF的含量[24]。此外,热处理对细胞壁的破坏作用,增加了膳食纤维与溶剂的接触面积,提高SDF的溶解度[20]。SDF和IDF的含量变化引起TDF含量变化,经热处理后,SH组米糠TDF含量显著增加,说明热处理在一定程度上提高了米糠的营养价值。
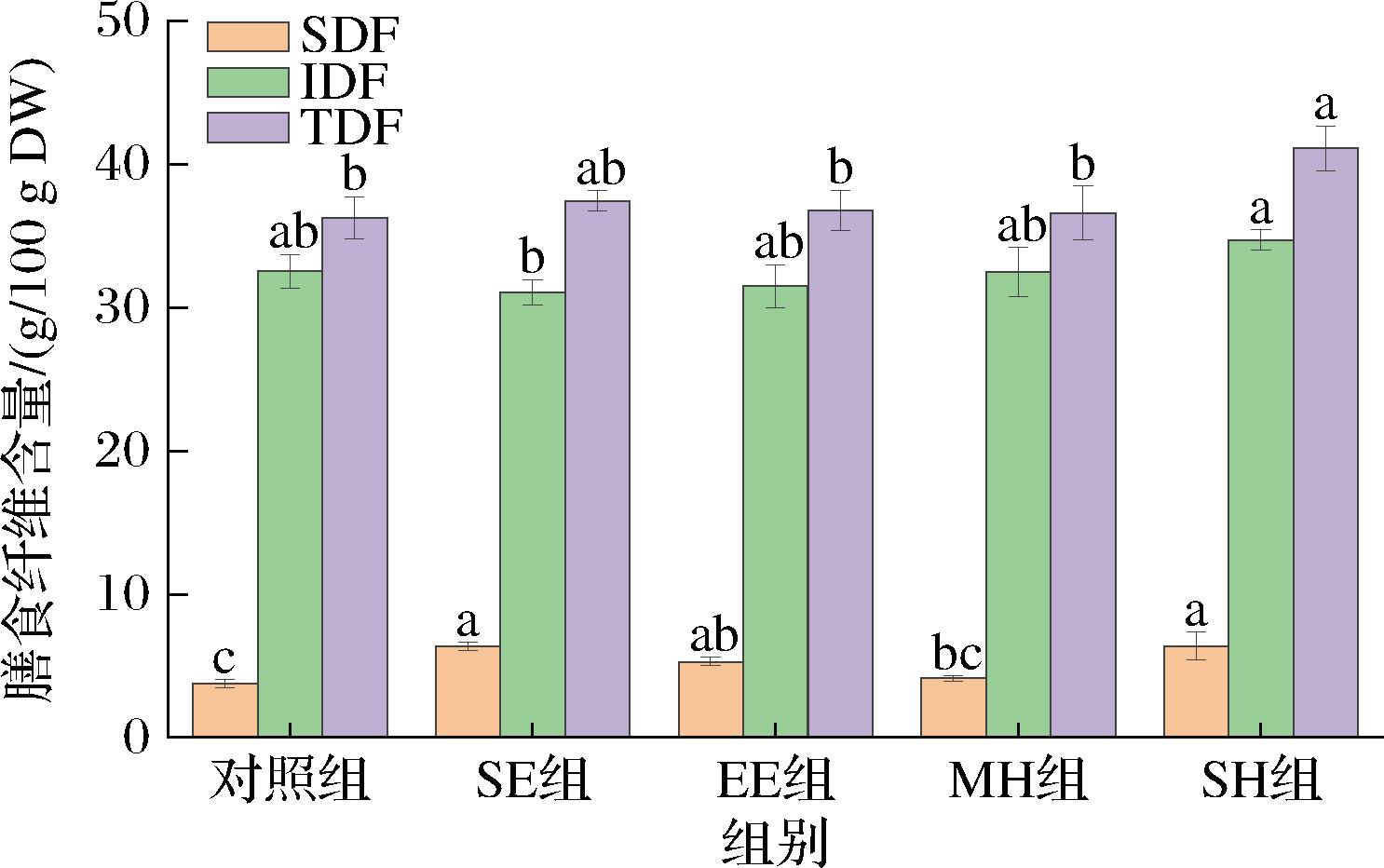
图4 不同热处理方式对米糠膳食纤维含量的影响
Fig.4 Effects of different heat treatment methods on dietary fiber content of rice bran
注:不同小写字母表示各组间差异显著(P<0.05)(下同)。
2.5 不同热处理方式对米糠化学成分的影响
米糠中的膳食纤维主要是不溶性的,由纤维素、部分半纤维素等构成,它们通过化学键和氢键相互连接,形成致密的细胞壁结构[20]。由表2可知,经热处理后,米糠纤维素、半纤维素含量均发生显著下降,说明热处理对米糠细胞壁产生了破坏作用。其中,EE组的降解作用最强,其次分别是SE组、SH组和MH组。热处理后米糠的游离糖含量和总糖含量显著增加。游离糖含量的增加可能与半纤维素降解有关,半纤维素中的乙酰基水解,转化为水溶性的低聚糖或单糖[25]。MH组可溶性糖含量显著低于其他处理组,可能与其对米糠细胞壁降解作用最弱有关。总糖含量的增加,一方面由游离糖含量的增加引起。另一方面,热处理破坏了细胞壁结构对淀粉等碳水化合物的“保护”作用,使得其更容易被水解或酸解[26]。SE组和EE组总糖含量显著高于MH和SH组,可能是由于SE、EE处理对细胞壁的破坏程度更强引起。以上表明,热处理通过破坏米糠细胞壁结构,降低了纤维素、半纤维素含量,并引起可溶性糖和总糖含量的增加。
表2 不同热处理方式对米糠化学成分的影响 单位:g/100 g
Table 2 Effects of different heat treatment methods on chemical constituents of rice bran
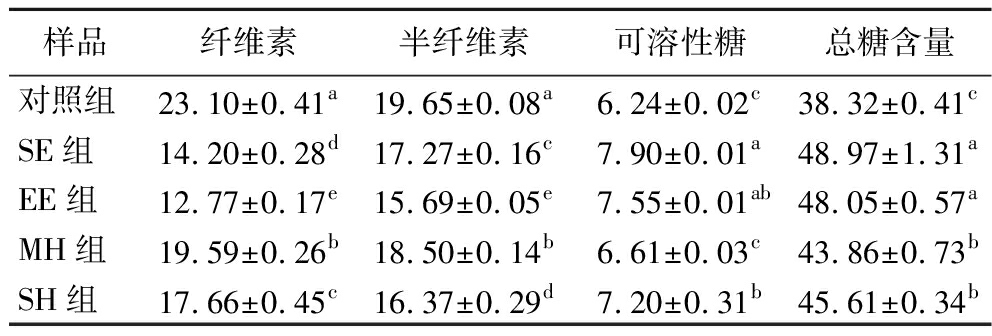
样品纤维素半纤维素可溶性糖总糖含量对照组23.10±0.41a19.65±0.08a6.24±0.02c38.32±0.41cSE组14.20±0.28d17.27±0.16c7.90±0.01a48.97±1.31aEE组12.77±0.17e15.69±0.05e7.55±0.01ab48.05±0.57aMH组19.59±0.26b18.50±0.14b6.61±0.03c43.86±0.73bSH组17.66±0.45c16.37±0.29d7.20±0.31b45.61±0.34b
2.6 不同热处理方式对米糠可溶性蛋白含量、游离氨基酸组成及含量的影响
由图5可知,CK组米糠可溶性蛋白含量为28.65 mg/g,热处理后,米糠中可溶性蛋白质含量均发生显著下降。高温会使蛋白质展开,并通过氢键、疏水相互作用和二硫键交换等相互作用产生无数交联,发生聚集[27]。并且,在较高温度下,蛋白的二级和三级结构丢失,蛋白质发生不可逆的变性,使内部的疏水残基暴露,增加蛋白质表面疏水性,从而引起可溶性蛋白含量下降[28]。MH组可溶性蛋白含量显著高于其他处理组与其美拉德反应程度最低有关,热处理过程中蛋白质会参与美拉德反应,导致产物中可溶性蛋白含量减少[29]。EE组和SH组可溶性蛋白含量显著低于其他处理组,说明EE处理过程中的高温、高剪切力以及SH处理产生的热蒸汽可能更易引起米糠蛋白结构发生变化。以上结果表明,热处理会导致米糠可溶性蛋白结构变化,并促进其参与美拉德反应,引起可溶性蛋白含量下降。
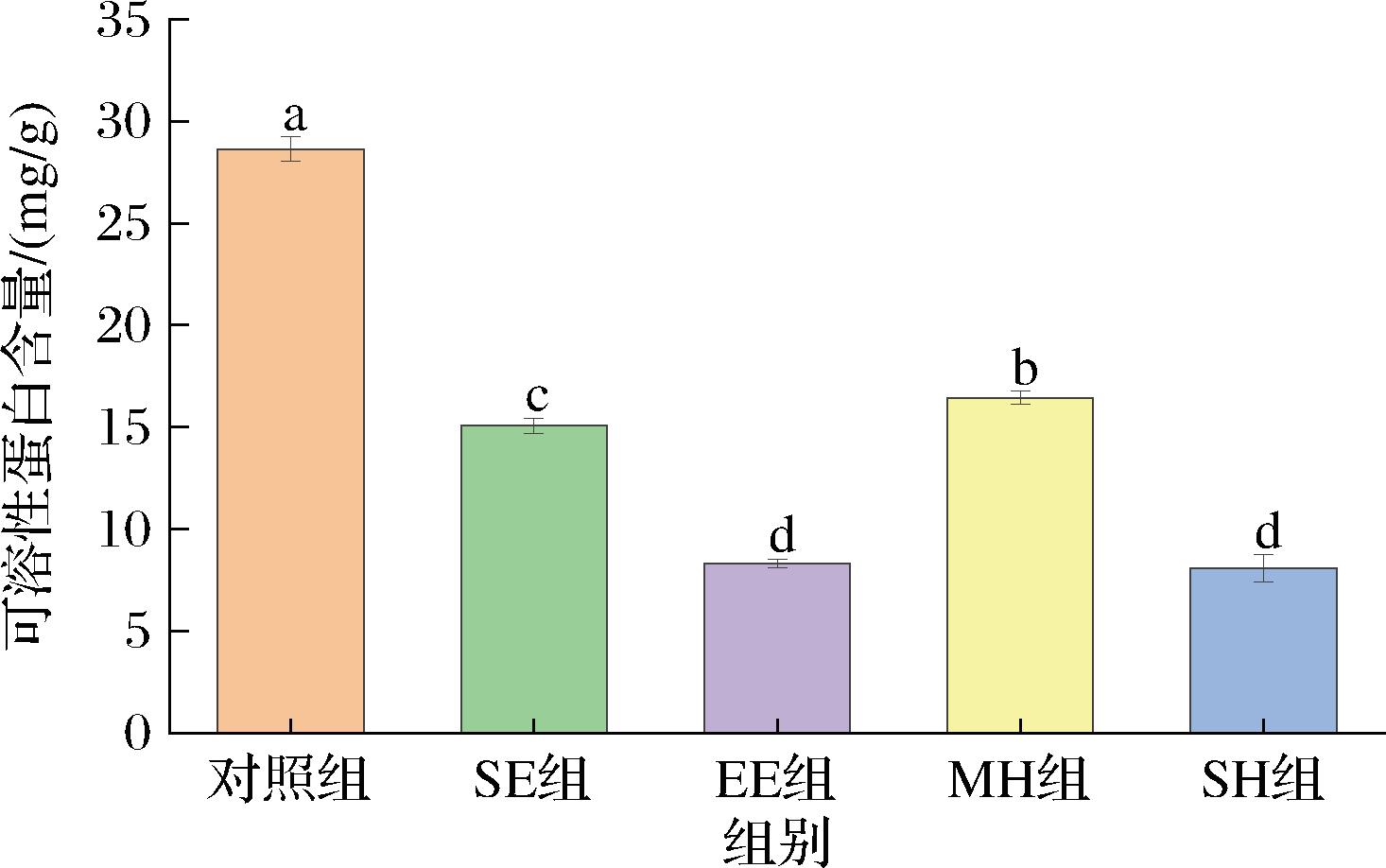
图5 不同热处理方式对米糠可溶性蛋白含量的影响
Fig.5 Effects of different heat treatment methods on soluble protein content in rice bran
不同处理组米糠的游离氨基酸组成和含量如表3 所示。对照组米糠游离氨基酸含量最多,为5.871 mg/g,主要是谷氨酸,占总游离氨基酸含量的23.10%。热处理促进还原糖与氨基酸发生美拉德反应,使得多数单个游离氨基酸含量以及游离氨基酸总量均显著降低。与对照组相比,MH组总游离氨基酸含量降低最多,降低了47.22%,SE组降低最少,降低了38.05%,EE组和SH组分别降低了39.14%、44.35%。从单个游离氨基酸来看,赖氨酸含量降低幅度最大,主要与它含有2个活泼的游离氨基基团,在加热过程中易与还原糖反应有关[29]。另外,碱性氨基酸含量(组氨酸、赖氨酸、精氨酸)的降低幅度要高于酸性氨基酸(天冬氨酸、谷氨酸)[30]。脯氨酸含量增加,但未见显著性变化。4组处理组中,SE组和EE组美拉德反应程度更深,但总游离氨基酸含量却高于其他处理组,可能是由于SE和EE处理对细胞壁的破坏作用更强,一定程度上促进了游离氨基酸的可提取性。此外,SE组苦味氨基酸(异亮氨酸、亮氨酸、苯丙氨酸)的含量要显著高于其他热处理组,可能是SE组美拉德反应程度更深,使得米糠苦味高于其他处理组。以上结果表明,热处理引起的美拉德反应使米糠游离氨基酸含量显著降低,SE处理和EE处理产生的负面影响要小于MH处理和SH处理。
表3 不同热处理方式对米糠氨基酸组成和含量的影响
Table 3 Effects of different heat treatment methods on amino acid composition and content of rice bran

氨基酸不同热处理方式对照组SE组EE组MH组SH组天冬氨酸(Asp)0.772±0.003a0.567±0.002d0.608±0.004b0.576±0.005cd0.595±0.016bc苏氨酸(Thr)0.177±0.009a0.085±0.005b0.082±0.003b0.077±0.009b0.081±0.001b丝氨酸(Ser)0.738±0.001a0.449±0.013d0.512±0.003b0.471±0.011c0.477±0.003c谷氨酸(Glu)1.356±0.005a0.656±0.10c0.785±0.006b0.476±0.017e0.601±0.007d甘氨酸(Gly)0.181±0.003a0.072±0.004b0.069±0.002b0.074±0.006b0.074±0.008b丙氨酸(Ala)0.365±0.004a0.278±0.007b0.267±0.004bc0.250±0.003c0.253±0.012c胱氨酸(Cys)0.218±0.004a0.154±0.007b0.135±0.006c0.149±0.003bc0.148±0.008bc缬氨酸(Val)0.196±0.013a0.092±0.007b0.062±0.004c0.069±0.007bc0.078±0.015bc蛋氨酸(Met)0.084±0.005a0.050±0.003b0.055±0.002b0.037±0.002c0.026±0.002d异亮氨酸(Ile)0.207±0.006a0.116±0.008b0.098±0.003c0.084±0.005c0.084±0.008c亮氨酸(Leu)0.186±0.016a0.177±0.014a0.126±0.004b0.091±0.016c0.096±0.006bc酪氨酸(Tyr)0.170±0.023ab0.178±0.008a0.141±0.003abc0.123±0.023c0.129±0.019bc苯丙氨酸(Phe)0.143±0.011a0.140±0.007a0.075±0.005c0.104±0.016c0.085±0.017c组氨酸(His)0.146±0.006a0.067±0.007b0.070±0.002b0.064±0.003b0.069±0.001b赖氨酸(Lys)0.336±0.006a0.090±0.010b0.060±0.004c0.054±0.009c0.059±0.003c精氨酸(Arg)0.410±0.009a0.248±0.004b0.183±0.004c0.167±0.008c0.168±0.006c脯氨酸(Pro)0.191±0.002ab0.218±0.023ab0.247±0.003a0.231±0.019ab0.244±0.039ab总含量 mg/g5.871±0.002a3.637±0.028b3.573±0.005c3.098±0.012e3.267±0.018d
2.7 不同热处理方式对米糠多酚、黄酮含量的影响
米糠中酚类化合物的含量以及它们以游离或结合形式存在,除了与水稻品种、种植环境和种植技术有关,还取决于加工处理。对照组米糠中游离多酚、结合多酚以及总酚含量分别为540.00、413.81、953.81 mg/100 g。由图6-a所示,经热处理后,除SE组外,游离多酚含量显著下降,EE组、MH组、SH组分别降低了9.7%、28.2%、17.2%。米糠中存在的部分热敏性酚类物质在热加工过程中被分解或氧化,从而使得游离多酚含量降低[31]。另一方面,米糠经处理后,粒径增大,减少了与提取液的接触面积,从而引起游离酚含量的减少[17]。相反的是,与对照组相比,稳定后米糠的结合多酚含量均发生增加,其中SE组、EE组、SH组显著增加,分别增加了14.4%、18.4%、19.6%。米糠中的大部分酚类物质以结合形式存在,与细胞壁的结构成分(纤维素、半纤维素等)共价结合,导致酚类物质难以释放和提取[4]。热处理导致米糠细胞壁结构的破坏,并促进纤维素、半纤维素降解,使得结合多酚更容易从细胞壁结构中释放出来,增加了活性物质的可提取性[32]。游离多酚和结合多酚的变化最终引起了总酚含量变化,由图6可知,与CK组相比,除EE组显著降低外,其他处理组总酚含量均未发生显著性变化。
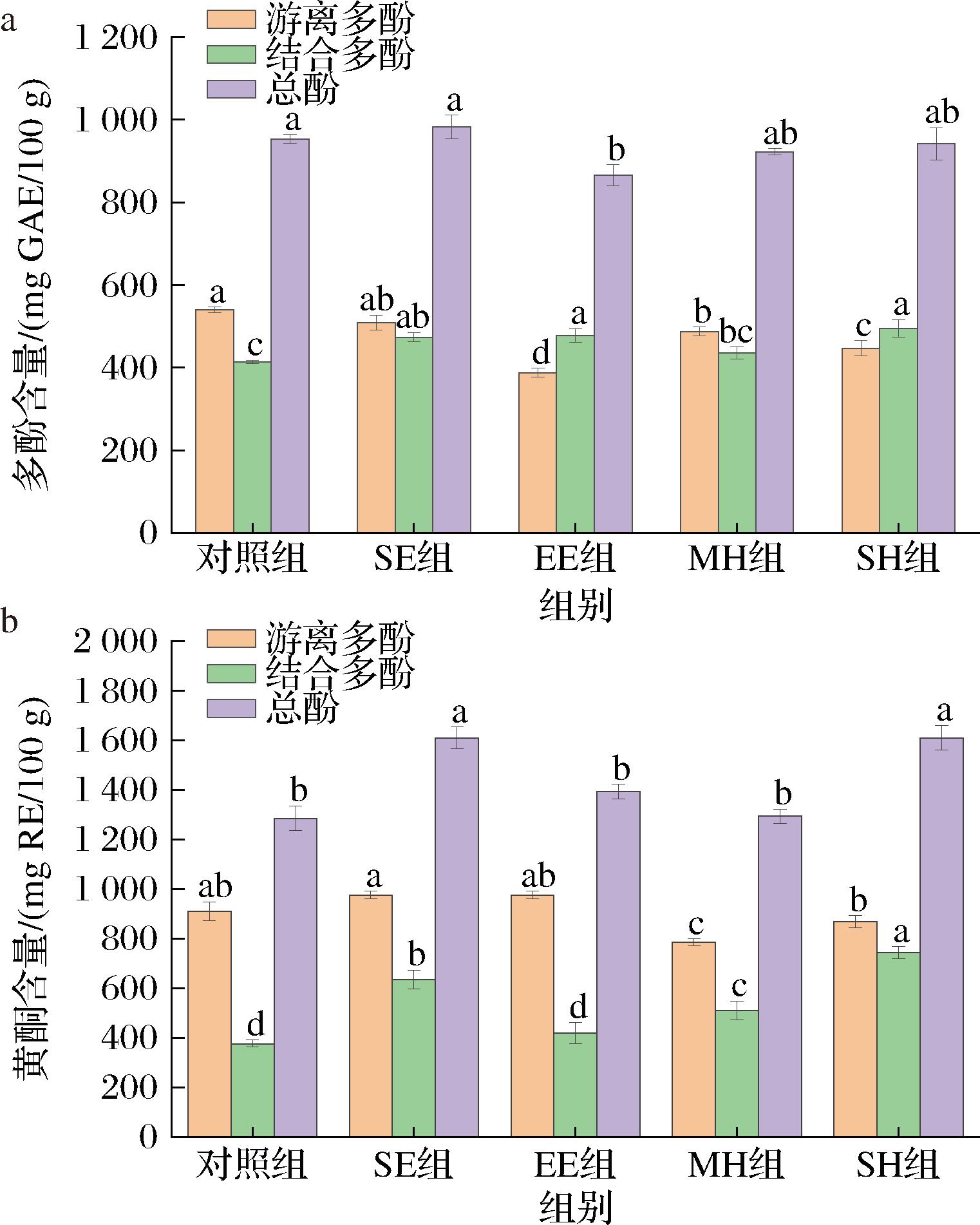
a-多酚含量;b-黄酮含量
图6 不同热处理方式对米糠多酚、黄酮含量的影响
Fig.6 Effects of different heat treatment methods on the contents of polyphenols and flavonoids in rice bran
由图6-b所示,黄酮的含量变化与多酚含量变化基本类似,MH组和SH组的游离黄酮含量显著下降,分别降低了13.75%、4.58%。除EE组外,其他处理组的结合黄酮含量显著增加,SE组、MH组、SH组分别增加了40.74%、26.19%、49.38%。此外,米糠中黄酮含量远高于多酚含量,这与之前的研究具有相同结论[33]。以上研究表明,部分热敏性活性成分因热处理发生降解,引起游离多酚、游离黄酮含量的下降,同时热处理对米糠细胞壁的降解作用,促进了结合多酚、结合黄酮的释放。
2.8 不同热处理方式对米糠γ-氨基丁酸含量的影响
由图7可知,与对照组相比,MH组和SH组γ-氨基丁酸含量发生显著增加,从1.973 mg/g分别增加到了2.299、2.196 mg/g,EE组未发生显著性增加。但SE组γ-氨基丁酸含量显著降低,降低至1.747 mg/g。热处理过程中施加的机械力破坏了米糠细胞壁结构,加速谷氨酸或谷氨酸脱羧酶的质量传递,并增强谷氨酸和酶之间的相互作用,可能会引起γ-氨基丁酸的积累增加[34]。其次,米糠细胞壁结构遭到破坏,多孔结构的形成,促进了溶剂对γ-氨基丁酸的可提取性。此外,TECHO等[35]提出加热温度对γ-氨基丁酸含量有显著影响,适当的加热温度可以提高γ-氨基丁酸的含量,但过度加温会导致其含量降低。同时热处理过程诱导了美拉德反应,并减少有益的生物活性化合物,包括γ-氨基丁酸[36]。γ-氨基丁酸作为一种非蛋白质氨基酸,会参与到美拉德反应中,这可能也是SE组、EE组γ-氨基丁酸含量低于MH组、SH组的原因。以上表明,热处理能够增加米糠γ-氨基丁酸含量,但过度的热处理会导致其含量降低。
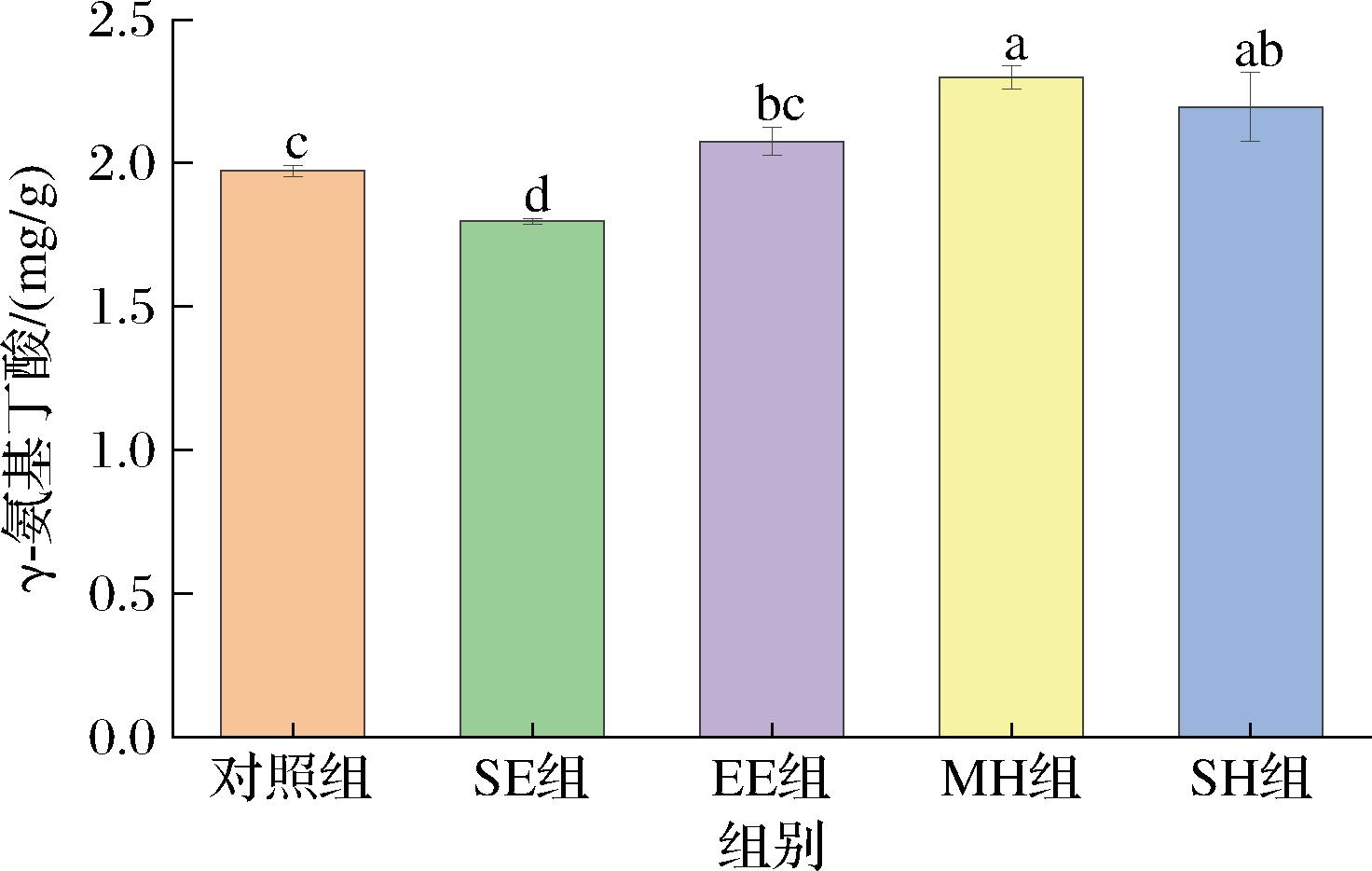
图7 不同热处理方式对米糠γ-氨基丁酸含量的影响
Fig.7 Effects of different heat treatment methods on γ-aminobutyric acid content in rice bran
2.9 不同热处理方式对米糠储藏性能的影响
新鲜米糠中的脂肪酶是米糠氧化变质的主要原因[6]。由图8-a可知,不同热处理方式均显著降低了米糠的脂肪酶活动度,其中EE组和SH组效果最佳,脂肪酶活动度分别降低至6.73、5.64 mg/g。MH组和SE组分别是8.23、11.65 mg/g。热处理通过对米糠进行加热,使脂肪酶变性失活[37]。SH组灭酶效果最好的原因是由于热处理过程中,部分蒸汽渗入米糠中,促进热量在米糠内部传递,使灭酶程度更加彻底[7]。
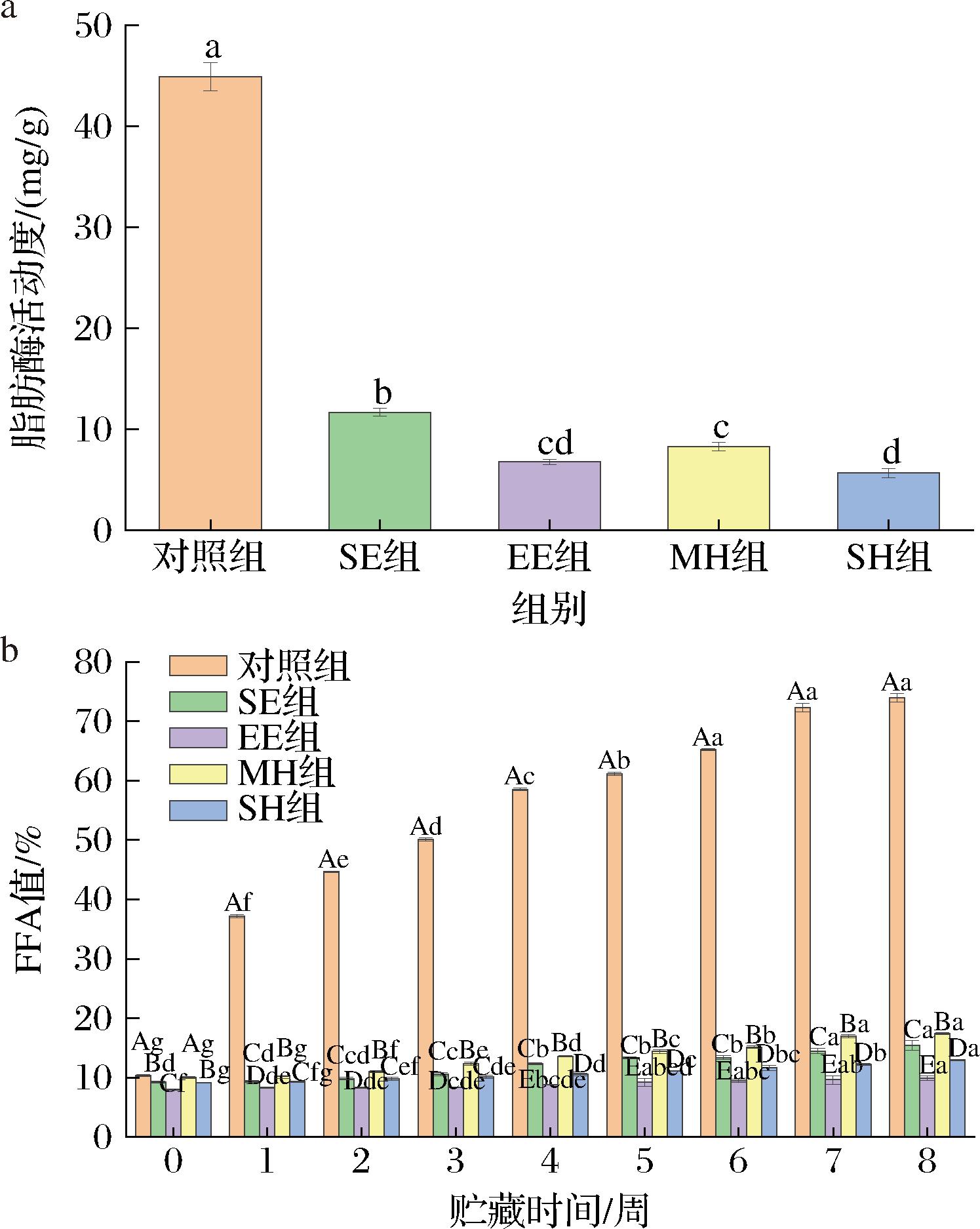
a-脂肪酶活动度;b-FFA值
图8 不同热处理方式对米糠脂肪酶活动度、FFA值的影响
Fig.8 Effects of different heat treatment methods on lipase activity and FFA value of rice bran
注:大写字母序列表示组间同一贮藏期的显著性差异,小写字母序列表示组内不同贮藏期的显著性差异。
游离脂肪酸值是衡量米糠稳定性的重要指标。米糠在37 ℃贮藏过程中FFA值变化如图8-b所示,各组米糠游离脂肪酸值的初始值在10%左右,其中,CK组米糠为10.34%,MH组为9.99%,SE组、EE组、SH组显著降低,分别为9.28%、8.00%、9.09%。处理组脂肪酸值均低于对照组,可能是由于脂肪酸在热处理过程中发生部分降解。在贮藏过程中,各组米糠FFA值均发生增加,但增加速度差异较大。对照组FFA值增加最为显著,从最初的10.21%增加至74.54%,增加了64.32%。热处理组FFA值比较稳定,但也有所增加,增长程度从低到高是EE组、SH组、SE组以及MH组,分别增长了1.46%、3.70%、6.69%、7.13%。热处理组中,SE组和MH组FFA值增长较多,可能是受脂肪酶活力影响。结果表明,对米糠进行热处理可以显著降低脂肪酶活动度,并有效抑制游离脂肪酸值在储藏过程中的升高,其中EE组效果要优于其他处理组,有利于米糠的后续加工利用。
3 结论与讨论
本研究探讨了不同热处理方式(SE、EE、MH、SH)对米糠营养物质、活性成分及贮藏性能等的影响。结果表明,不同热处理方式具有显著差异性。米糠在热处理过程中发生淀粉糊化,并产生膨化效果,导致米糠粒径的增加。不同热处理引起米糠发生不同程度的美拉德褐变和γ-氨基丁酸含量变化,SE 处理的高温、高压、高湿环境极易引发美拉德反应,部分γ-氨基丁酸作为非蛋白氨基酸参与反应中,导致其含量不增返降,褐变程度显著高于其他组(P<0.05)。同时热处理破坏了米糠完整细胞壁结构,使得SDF含量增加并促进多酚、黄酮的释放。与其他处理组相比,SE处理利用压力差,SH处理利用高温蒸汽渗入米糠内部,对细胞壁的破坏程度明显优于其他处理组,使得SDF、总酚、总黄酮含量均高于其他处理组。米糠可溶性蛋白、游离氨基酸含量也受热处理影响,发生显著下降(P<0.05)。相较其他组,MH 处理时间短、温度低、不涉及高压及高剪切力,对米糠相关指标影响弱,却利于热敏性物质保留,可溶性蛋白和γ-氨基丁酸含量高于其他处理组。脂肪酶活动度经过热处理均发生显著降低(P<0.05),其中EE产生的高剪切力及SH产生的蒸汽对脂肪酶的灭活效果最好。总体上,SH处理效果要优于其他处理组。后续研究可以对SH条件进行优化,在促进活性成分释放的同时,最大程度保留热敏性物质,更好实现米糠的高值化加工。
[1] PARK H Y,LEE K W,CHOI H D.Rice bran constituents:Immunomodulatory and therapeutic activities[J].Food &Function,2017,8(3):935-943.
[2] PUNIA S,KUMAR M,SANDHU K S,et al.Rice-bran oil:An emerging source of functional oil[J].Journal of Food Processing and Preservation,2021,45(4):e15318.
[3] JIA M Y,YU Q,CHEN J J,et al.Physical quality and in vitro starch digestibility of biscuits as affected by addition of soluble dietary fiber from defatted rice bran[J].Food Hydrocolloids,2020,99:105349.
[4] XUE P Y,LIAO W,CHEN Y,et al.Release characteristic and mechanism of bound polyphenols from insoluble dietary fiber of navel orange peel via mixed solid-state fermentation with Trichoderma reesei and Aspergillus niger[J].LWT,2022,161(9):113387.
[5] LIU L,WEN W,ZHANG R F,et al.Complex enzyme hydrolysis releases antioxidative phenolics from rice bran[J].Food Chemistry,2017,214(1):1-8.
[6] YU C W,PENG B,LUO T,et al.Bound lipase:An important form of lipase in rice bran (Oryza sativa)[J].Food Science and Human Wellness,2023,12(5):1779-1787.
[7] LIU Y Q,STRAPPE P,ZHOU Z K,et al.Impact on the nutritional attributes of rice bran following various stabilization procedures[J].Critical Reviews in Food Science and Nutrition,2019,59(15):2458-2466.
[8] LIU X R,MA Q W,SUN Y J,et al.Effects of processings and complexation on solubility,antioxidant and antibacterial properties of buckwheat polyphenols[J].Food and Bioprocess Technology,2024,17(6):1583-1595.
[9] TANG X J,WANG Z R,ZHENG J,et al.Physicochemical,structure properties and in vitro hypoglycemic activity of soluble dietary fiber from adlay (Coix lachryma-jobi L.var.ma-yuen Stapf) bran treated by steam explosion[J].Frontiers in Nutrition,2023,10:1124012.
[10] MUSILOV J,FRANKOV
J,FRANKOV H,FEDORKOV
H,FEDORKOV S,et al.Comparison of polyphenols,phenolic acids,and antioxidant activity in sweet potato (Ipomoea batatas L.) tubers after heat treatments[J].Journal of Agriculture and Food Research,2024,18(4):101271.
S,et al.Comparison of polyphenols,phenolic acids,and antioxidant activity in sweet potato (Ipomoea batatas L.) tubers after heat treatments[J].Journal of Agriculture and Food Research,2024,18(4):101271.
[11] LI J,LIU C,WU N N,et al.Improvement of gelation properties of indica rice flour with stabilized rice bran from different thermal treatment[J].Cereal Chemistry,2024,101(1):263-273.
[12] MA Q,WANG X,ZHANG R F,et al.Structural,physicochemical and functional properties of dietary fiber from black rice bran treated by different processing methods[J].Food Bioscience,2025,65(3):106025.
[13] RASHID M T,LIU K L,HAN S M,et al.The effects of thermal treatment on lipid oxidation,protein changes,and storage stabilization of rice bran[J].Foods,2022,11(24):4001.
[14] POKKANTA P,YUENYONG J,MAHATHEERANONT S,et al.Microwave treatment of rice bran and its effect on phytochemical content and antioxidant activity[J].Scientific Reports,2022,12(1):7708.
[15] PEDRO A C,S NCHEZ-MATA M C,PÉREZ-RODR
NCHEZ-MATA M C,PÉREZ-RODR GUEZ M L,et al.Qualitative and nutritional comparison of goji berry fruits produced in organic and conventional systems[J].Scientia Horticulturae,2019,257(15):108660.
GUEZ M L,et al.Qualitative and nutritional comparison of goji berry fruits produced in organic and conventional systems[J].Scientia Horticulturae,2019,257(15):108660.
[16] REKOWSKI A,LANGENK MPER G,DIER M,et al.Determination of soluble wheat protein fractions using the Bradford assay[J].Cereal Chemistry,2021,98(5):1059-1065.
MPER G,DIER M,et al.Determination of soluble wheat protein fractions using the Bradford assay[J].Cereal Chemistry,2021,98(5):1059-1065.
[17] 谢勇.不同热加工全谷青稞营养功能及对2型糖尿病的改善效果[D].重庆:西南大学,2021.XIE Y.Nutritional functions of whole-grain hullessbarley treated by various thermal processingand its alleviative effect on type 2 diabetic rats[D].Chongqing:Southwest University,2021.
[18] LIU R,HE X L,SHI J Q,et al.The effect of electrolyzed water on decontamination,germination and γ-aminobutyric acid accumulation of brown rice[J].Food Control,2013,33(1):1-5.
[19] 梁兰兰,卓训文.米糠游离脂肪酸值快速测定方法[J].粮食与油脂,2001,14(12):44.LIANG L L,ZHUO X W.Rapid determination method of free fatty acid value of rice bran[J].Journal of Cereals &Oils,2001,14(12):44.
[20] OUYANG H,WU L,HU Y,et al.Effect of steam explosion treatment on physicochemical,functional and structural properties of pomelo fruitlets[J].LWT,2023,184(12):114963.
[21] MIRANDA M,MAUREIRA H,RODR GUEZ K,et al.Influence of temperature on the drying kinetics,physicochemical properties,and antioxidant capacity of Aloe vera (Aloe barbadensis Miller) gel[J].Journal of Food Engineering,2009,91(2):297-304.
GUEZ K,et al.Influence of temperature on the drying kinetics,physicochemical properties,and antioxidant capacity of Aloe vera (Aloe barbadensis Miller) gel[J].Journal of Food Engineering,2009,91(2):297-304.
[22] ZHAO X X,GUO Y P,ZHANG Y M,et al.Effects of different heat treatments on Maillard reaction products and volatile substances of camel milk[J].Frontiers in Nutrition,2023,10:1072261.
[23] XI H H,WANG A X,QIN W Y,et al.The structural and functional properties of dietary fibre extracts obtained from highland barley bran through different steam explosion-assisted treatments[J].Food Chemistry,2023,406(9):135025.
[24] SAROJ R,KAUR S,AHMAD MALIK M,et al.Thermal processing of wheat bran:Effect on the bioactive compounds and dietary fiber[J].Bioactive Carbohydrates and Dietary Fibre,2024,32(2):100433.
[25] TANPICHAI S,WITAYAKRAN S,BOONMAHITTHISUD A.Study on structural and thermal properties of cellulose microfibers isolated from pineapple leaves using steam explosion[J].Journal of Environmental Chemical Engineering,2019,7(1):102836.
[26] SARAWONG C,SCHOENLECHNER R,SEKIGUCHI K,et al.Effect of extrusion cooking on the physicochemical properties,resistant starch,phenolic content and antioxidant capacities of green banana flour[J].Food Chemistry,2014,143(2):33-39.
[27] YEN P P L,PRATAP-SINGH A.Vacuum microwave dehydration decreases volatile concentration and soluble protein content of pea (Pisum sativum L.) protein[J].Journal of the Science of Food and Agriculture,2021,101(1):167-178.
[28] HALL A E,MORARU C I.Structure and function of pea,lentil and faba bean proteins treated by high pressure processing and heat treatment[J].LWT,2021,152(18):112349.
[29] YADAV G P,DALBHAGAT C G,MISHRA H N.Effects of extrusion process parameters on cooking characteristics and physicochemical,textural,thermal,pasting,microstructure,and nutritional properties of millet-based extruded products:A review[J].Journal of Food Process Engineering,2022,45(9):e14106.
[30] FENG L,MAN Y F,WANG S Q,et al.Changes in the contents of free amino acids,free sugars,hydrolysed amino acids and hydrolysed sugars in roasted and unroasted sesame seeds[J].European Food Research and Technology,2025,251(6):1209-1224.
[31] HONG Q Y,CHEN G J,WANG Z R,et al.Effects of different thermal processing methods on bioactive components,phenolic compounds,and antioxidant activities of Qingke (highland hull-less barley)[J].Food Science and Human Wellness,2023,12(1):119-129.
[32] PRADEEP P M,JAYADEEP A,GUHA M,et al.Hydrothermal and biotechnological treatments on nutraceutical content and antioxidant activity of rice bran[J].Journal of Cereal Science,2014,60(1):187-192.
[33] KUSUMAWARDANI S,LUANGSAKUL N.Assessment of polyphenols in purple and red rice bran:Phenolic profiles,antioxidant activities,and mechanism of inhibition against amylolytic enzymes[J].Current Research in Food Science,2024,9:100828.
[34] POOJARY M M,DELLAROSA N,ROOHINEJAD S,et al.Influence of innovative processing on γ-aminobutyric acid (GABA) contents in plant food materials[J].Comprehensive Reviews in Food Science and Food Safety,2017,16(5):895-905.
[35] TECHO J,SOPONRONNARIT S,DEVAHASTIN S,et al.Effects of heating method and temperature in combination with hypoxic treatment on γ-aminobutyric acid,phenolics content and antioxidant activity of germinated rice[J].International Journal of Food Science &Technology,2019,54(4):1330-1341.
[36] HUANG Y Y,LI H Y,YU X X,et al.Foodomics-based chemical profiling and signature compound characterization of air-fried potato chips:The effect of thermal processing and fish oil treatment on advancing safety,nutrition,and flavor attributes[J].Food Bioscience,2025,66(4):106211.
[37] PYNKET I,JANSSEN F,VAN GILS J,et al.Directing oat groat heat treatment conditions towards increased protein extractability[J].Current Research in Food Science,2024,9(2):100932.