紫外线(ultraviolet,UV)作为太阳辐射的关键组成部分,对生物分子具有显著的潜在损伤作用,可引发DNA损伤、蛋白质变性以及脂质过氧化等一系列不良生物学效应,严重威胁生物体的生理功能和健康[1]。为了防止紫外线辐射对皮肤造成损害,一些物理和化学防晒材料,如二苯甲酮类、樟脑衍生物类、nTiO2和nZnO等作为添加剂被广泛应用于防晒产品[2]。然而,由于其可能对人类健康以及生态环境造成危害,一种可以有效吸收紫外线辐射的天然紫外吸收剂——gadusol成为防晒产品的重点研究方向。gadusol是在一些原核生物和真核生物中合成的具有紫外吸收功能的天然产物,在海洋鱼类的卵巢和发育的胚胎、海绵藻类等的研究中均有报道[3-4]。gadusol基础骨架为环己烯酮,中性条件下具有较高的摩尔消光系数[ε=21 800 L/(mol·cm)][5],其最大吸收波长(296 nm)位于UVB(280~320 nm)区间,能有效地防止UVB引发细胞凋亡、诱变和癌变等一系列严重的DNA损伤[6-7]。gadusol通过以热量的形式有效消散光能,迅速失活而不会形成游离氧[8],有作为可生物降解防晒霜的潜力。
gadusol的生物合成途径起始于磷酸戊糖途径(pentose phosphate pathway,PPP)的中间体7-磷酸景天庚酮糖(sedoheptulose 7-phosphate,S7P)。提高PPP通量有望增加S7P的供应,从而为gadusol的合成提供充足的前体,促进gadusol产量的提升。在调控PPP以提高目标产物产量的研究中,对PPP途径中关键基因的调控是重要策略。氧化磷酸戊糖途径(oxidative branch of the pentose phosphate pathway,oxiPPP)由6-磷酸葡萄糖脱氢酶(glucose-6-phosphate dehydrogenase,ZWF1)、6-葡萄糖酸内酯酶(6-phosphogluconolactonase,SOL3)、6-磷酸葡萄糖酸脱氢酶(6-phosphogluconate dehydrogenase,GND2)等催化,oxiPPP中关键酶的过表达会影响细胞内NADPH水平[9-10]。非氧化PPP中的转酮醇酶(transketolase,TKL1)在木糖代谢中起着关键的作用。TKL1催化醛糖(如5-磷酸核糖)转化为酮糖(如5-磷酸木酮糖、6-磷酸果糖和S7P),其在PPP和糖酵解这2种主要代谢途径之间建立了可逆的联系(图1),当酵母用木糖作为碳源培养时,它发挥着关键的作用[11]。为了改善酵母在木糖中的生长以及木酮糖的消耗,过表达非氧化PPP酶来提高木糖利用成为研究者选择的策略之一[12]。这些蛋白相互催化,对木糖代谢途径以及PPP都具有良好的催化活性[13]。PPP代谢物的利用被认为是酵母高效利用木糖发酵的瓶颈,转醛醇酶(transaldolase,TAL1)和TKL1催化的非氧化PPP反应控制着PPP通量[12]。为了提高酵母在PPP途径的代谢通量,JIN等[14]尝试删除编码6-磷酸葡萄糖异构酶的PGI1基因,将糖酵解途径中的碳流量转移到PPP,但PGI1基因的缺失导致细胞生长和碳源利用缺陷,并没有提高类菌胞素氨基酸(mycosporine-like amino acids,MAAs)水平,而过表达ZWF1和GND1基因增加PPP碳通量使重组菌株中MAAs水平得到提升。YUAN等[15]的研究表明,额外的GLK和ZWF过表达会增加PPP通量。PARK等[16]为了加强菌株中木糖的同化,选择转录因子的STB5和编码转酮醇酶的TKL1基因进行过表达,有效提高了木糖消耗率,提高了shinorine的产量。这些酶在PPP的不同步骤发挥关键作用,对其进行调控能有效提高PPP通量。
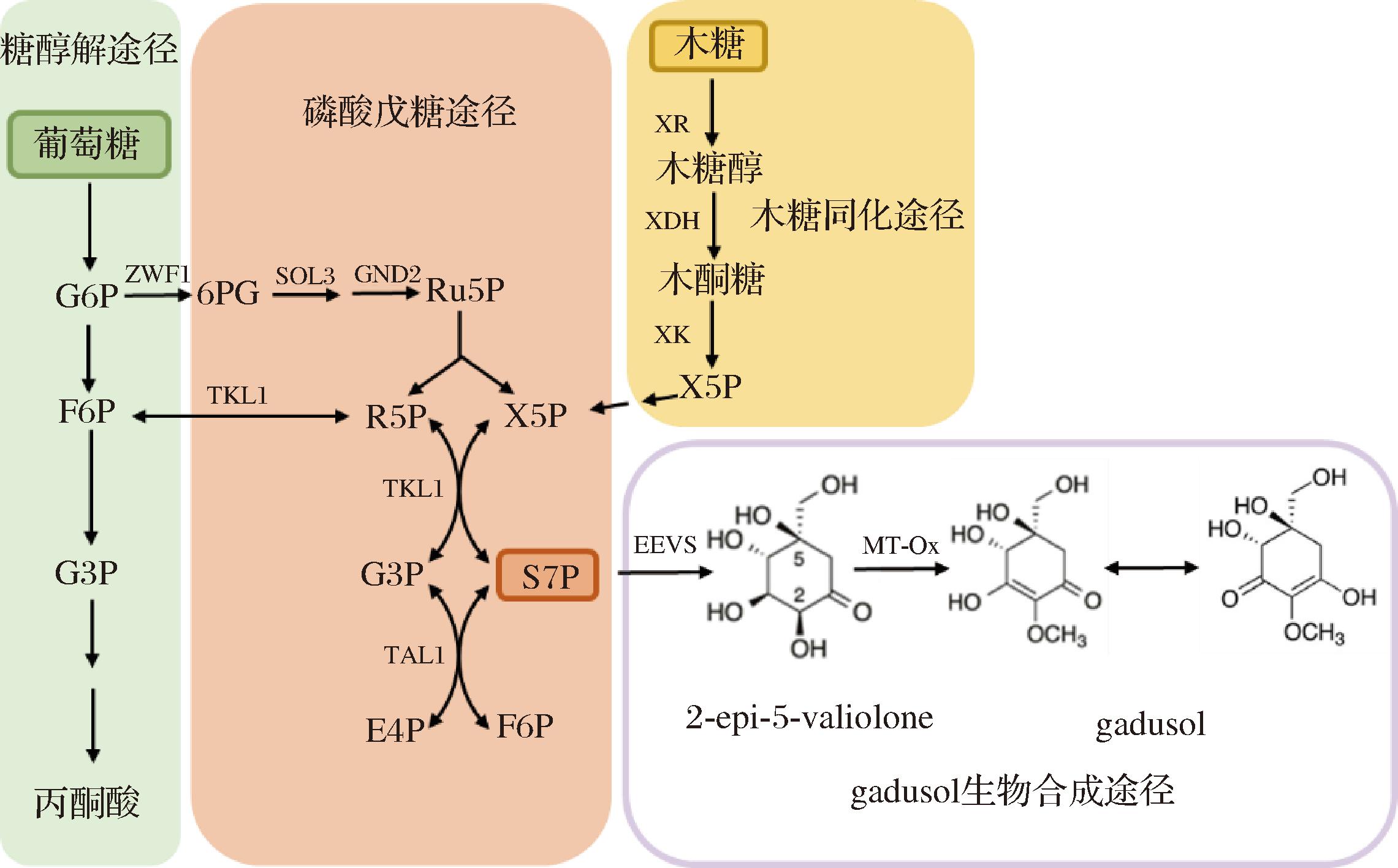
图1 毕赤酵母合成gadusol代谢路径
Fig.1 Metabolic pathway of gadusol production in K.phaffii
注:S7P通过糖磷酸环化酶(2-epi-5-epi-valiolone synthase,EEVS)和甲基转移-氧化还原酶(methyltransferase-oxidoreductase,MT-Ox)的催化反应转化为gadusol。木糖还原酶(xylose reductase,XR)、木糖醇脱氢酶(xylitol dehydrogenase,XDH)和木酮激酶(xylulokinase,XK)催化木糖的同化。G6P:6-磷酸葡萄糖(glucose 6-phosphate);6PG:6-磷酸葡萄糖酸内酯(6-phosphogluconolactone);Ru5P:5-磷酸核酮糖(ribulose 5-phosphate);X5P:5-磷酸木酮糖(xylulose 5-phosphate);R5P:5-磷酸核糖(ribose-5-phosphate);G3P:3-磷酸甘油醛(glyceraldehyde 3-phosphate);E4P:4-磷酸赤藓糖(erythrose 4-phosphate);F6P:6-磷酸果糖( fructose 6-phosphate)。
为了提高PPP通量以及木糖同化能力,本研究旨在通过调控PPP上的ZWF1、GND2、SOL3、TKL1基因,优化PPP通量,提高重组毕赤酵母(Komagataella phaffii)中gadusol的含量,为gadusol的工业化生产提供理论。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株与培养基
本研究所使用的质粒与菌株如表1所示。
表1 本研究使用的质粒与菌株
Table 1 Plasmids and strains used in this study
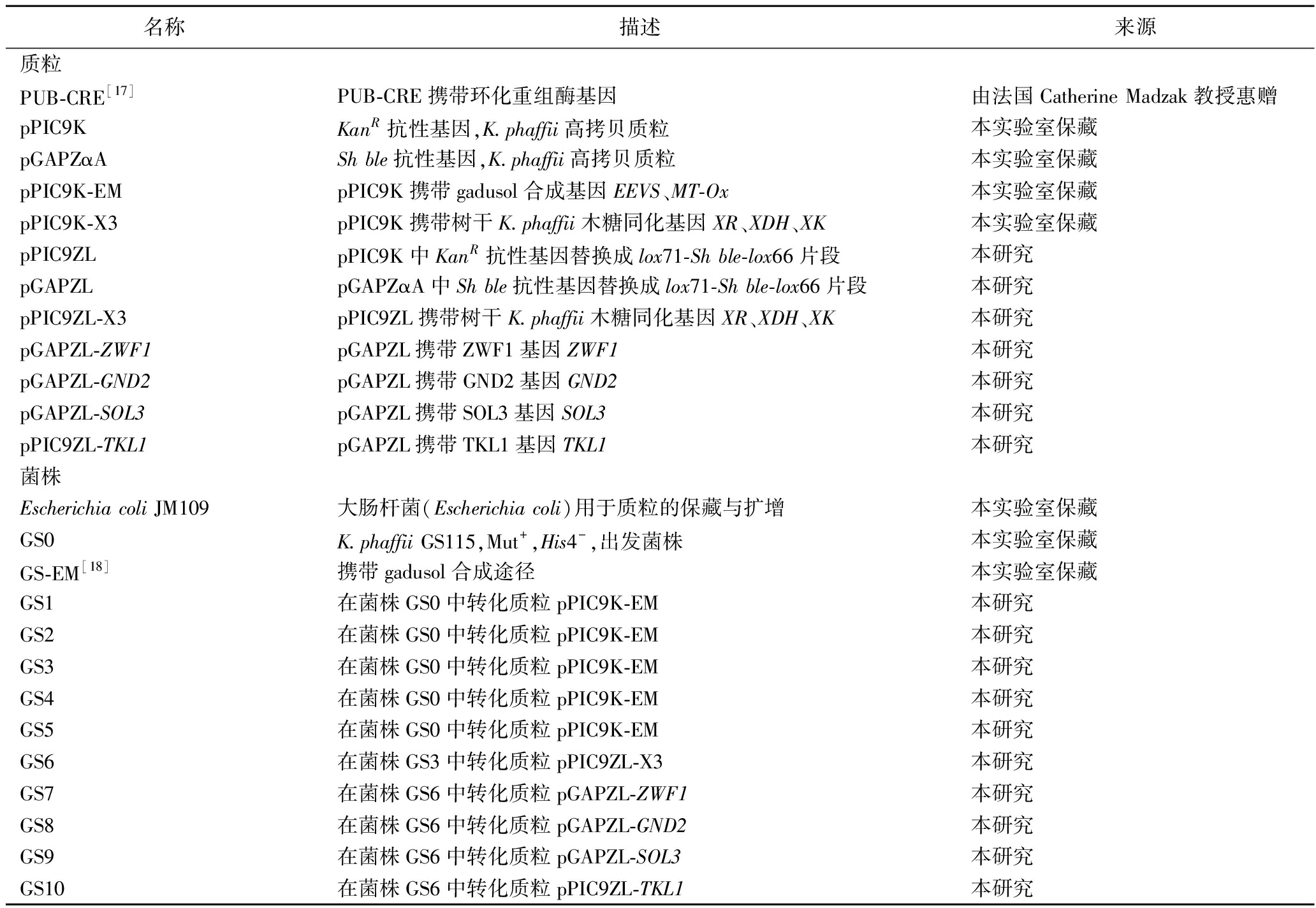
名称描述来源质粒PUB-CRE[17]PUB-CRE携带环化重组酶基因由法国Catherine Madzak教授惠赠pPIC9KKanR抗性基因,K.phaffii高拷贝质粒 本实验室保藏pGAPZαASh ble抗性基因,K.phaffii高拷贝质粒本实验室保藏pPIC9K-EMpPIC9K携带gadusol合成基因EEVS、MT-Ox本实验室保藏pPIC9K-X3pPIC9K携带树干K.phaffii木糖同化基因XR、XDH、XK本实验室保藏pPIC9ZLpPIC9K中KanR抗性基因替换成lox71-Sh ble-lox66片段本研究pGAPZLpGAPZαA中Sh ble抗性基因替换成lox71-Sh ble-lox66片段 本研究pPIC9ZL-X3pPIC9ZL携带树干K.phaffii木糖同化基因XR、XDH、XK本研究pGAPZL-ZWF1pGAPZL携带ZWF1基因ZWF1本研究pGAPZL-GND2pGAPZL携带GND2基因GND2本研究pGAPZL-SOL3pGAPZL携带SOL3基因SOL3本研究pPIC9ZL-TKL1pGAPZL携带TKL1基因TKL1本研究菌株Escherichia coli JM109大肠杆菌(Escherichia coli)用于质粒的保藏与扩增本实验室保藏GS0K.phaffii GS115,Mut+,His4-,出发菌株本实验室保藏GS-EM[18]携带gadusol合成途径本实验室保藏GS1在菌株GS0中转化质粒pPIC9K-EM本研究GS2在菌株GS0中转化质粒pPIC9K-EM本研究GS3在菌株GS0中转化质粒pPIC9K-EM本研究GS4在菌株GS0中转化质粒pPIC9K-EM本研究GS5在菌株GS0中转化质粒pPIC9K-EM本研究GS6在菌株GS3中转化质粒pPIC9ZL-X3本研究GS7在菌株GS6中转化质粒pGAPZL-ZWF1本研究GS8在菌株GS6中转化质粒pGAPZL-GND2本研究GS9在菌株GS6中转化质粒pGAPZL-SOL3本研究GS10在菌株GS6中转化质粒pPIC9ZL-TKL1本研究
本研究相关培养基及溶液的配制方法如下:
LB培养基(g/L):胰蛋白胨10,酵母提取物5,氯化钠10;添加20琼脂粉配制固体培养基;固体平板加卡那霉素使其终质量浓度为50 mg/L。
LLB(low salt LB)培养基(g/L):胰蛋白胨10,酵母提取物5,氯化钠5,调节pH值为7.5,固体培养基另加20琼脂粉,加入Zeocin使其终质量浓度为25 mg/L。
MD(minimal dextrose)培养基(g/L):酵母无氨基氮源(YNB)13.4,葡萄糖20,固体培养基另加20琼脂粉。
YPD培养基(g/L):酵母提取物10,胰蛋白胨20,葡萄糖20;固体培养基另加20琼脂粉;以G418(终质量浓度为250、500、1 000、2 000、4 000 mg/L)和潮霉素B(终质量浓度为700 mg/L)进转化子的筛选。
YPDZS固体培养基(g/L):在YPD培养基的基础上加入山梨醇182.2,琼脂粉20;以Zeocin(终质量浓度为100 mg/L)进转化子的筛选。
YP培养基(g/L):酵母提取物10,胰蛋白胨20。
YPX培养基(g/L):酵母提取物10,胰蛋白胨20,木糖20。
YPDX培养基(g/L):酵母提取物10,胰蛋白胨20,木糖10,葡萄糖10。
5 mmol/L PBS缓冲液(g/L):磷酸二氢钾0.12,磷酸氢二钠0.72,氯化钠4,氯化钾0.1,800 mL超纯水溶解,1 mol/L盐酸调pH值至7.0,超纯水定容至1 L。
由于葡萄糖、木糖及YNB和含氮化合物高温条件下会发生美拉德反应使培养基颜色加深,尤其是YPX培养基会变成棕红色,可能对细胞的生长造成影响[19],本研究中碳源氮源均分开灭菌,将碳源配制成10倍浓缩液加入到YP培养基中。固体培养基在相应培养基中添加20 g/L的琼脂粉。
1.1.2 实验试剂
葡萄糖、木糖、氯仿、甲醇,国药集团上海化学试剂公司;胰蛋白胨、酵母提取物、酵母基因组DNA快速抽提试剂盒,上海生工生物工程有限公司;博来霉素,上海懋康生物科技有限公司;PrimeSTAR® Max DNA Polymerase、限制性内切酶、T4 DNA连接酶、TB Green Premix Ex Taq Ⅱ酶,TaKaRa公司;2×Hieff Clone® MultiS Enzyme Premix、潮霉素B,翌圣生物科技(上海)股份有限公司;质粒小量提取试剂盒、胶回收纯化试剂盒、PCR纯化试剂盒,Omega生物试剂公司;毕赤酵母感受态细胞制备及转化试剂盒,碧云天生物技术;实验所用引物由上海生工生物工程有限公司及安升达生物科技有限公司合成,如表2所示。
表2 本研究使用的引物
Table 2 Primers used in this study

引物名称序列(5′→3′)pGA-FCGGTATCGATATCATGTAATTAGTTATGTCACGCpGA-RCGGTACAAACGAAGGTCTCACTTAATCTTC66-FCCTTCGTTTGTACCGTTCGTATAATGTATGCTATACGAAGTTATT-GCGGATCCCCCACA71-RATGATATCGATACCGTTCGTATAGCATACATTATACGAAGTTAT-CAAAGGAAAAGGGGGSh ble-FCAACCAATTAACCAATTCTGACCTTCGTTTGTACCGSh ble-RGGTGTTGCTCACATGTTGGTCTCCAGCX3-FGAGATTTCCTTCTATTTTAGATTCCTGACTTCAACTCAAGACGX3-RTTCTCGTAAGTGCCCTTAATGTTTCAATTCAGATTCCATTTTAGpPICZL-FTTGAAACATTAAGGGCACTTACGAGAAGACCpPICZL-RGAATCTAAAATAGAAGGAAATCTCATCGTTTGGATCCGAP-XhoICCGCTCGAGCGGGAAGGAAATCTCATCGTTTCGGAP-SacIITCCCCGCGGGGACAGCTTTCTAGAACGAP-EcoRCCGGAATTCCGGGAAGGAAATCTCATCGTTTCGGAP-FCGAAATACTGATCCCCGCGGGGACAGCTTTCTAGAACGAP-RTCGGTCATCCGCTCGAGCGGGAAGGAAATCTCATCGTTTCGAP-TK-FTGCATGCATGCAGAGATCAGATCTTTTTTGTAGAAATGTCZWF1-FCCGCTCGAGCGGATGACCGATACGAAAGCCGZWF1-RTCCCCGCGGGGATTACATCTTGTGCAGCACATCGND2-FCCGGAATTCCGGATGGTTGAAGCAACAGGAGGND2-RTCCCCGCGGGGATTAAGCATCGTAGGTACTGGSOL3-FCCGGAATTCCGGATGGTACAAATCTATTCCTSOL3-RTCCCCGCGGGGATCAGTATTTCGAAGTAGAAACTKL1-FCCGCTCGAGCGGATGACTCAATTCACTGACATTGTKL1-RCCGGAATTCCGGTTAGAAAGCTTTTTTCAAAGGAGyz-GAP-FGTAGAAATGTCTTGGTGTCCTCGTCCyz-AOX-FGCAGTCTCTCTATCGCTTCTGAACCyz-AOXTT-RGCTGCGAGATAGGCTGATCAGyz-ZL-FGAGAGCTTTGTTGTAGGTGGACCyz-ZL-RGCCACGTTGTGTCTCAAAATCTCTGHgy-FGAAGAATCTCGTGCTTTCAGCTTCGHgy-RGCATAAGGGAGAGCGTCGACTATTCqGAPDH-FACAAGGACTGGAGAGGTGGTAGAACqGAPDH-RGTCAACAACGGAGACATCGACGGqEEVS-FCCTGCTTCTGTTTCTACTAGAGTTGCqEEVS-RCTTCACCATGCAACAAAGCAGGCqMTOX-FGTCTATGGCTGAAGCTTTGCCTGqMTOX-RGAACTGTTCACCAGTAGCAGCC
1.2 仪器与设备
PowerPacTM基础电泳仪、GenePulser Xcell电穿孔仪、CFX96 Real-Time PCR仪,Bio-Rad公司;NanoDrop分光光度计,赛默飞世尔科技(中国)有限公司;紫外可见分光光度计TU-1 950,北京普析通用仪器有限责任公司;安捷伦液相色谱仪1260 Infinity Ⅱ,美国安捷伦科技公司;超高效液相色谱串联四极杆飞行时间质谱联用仪,美国沃特世公司。
1.3 工程菌株的构建
1.3.1 K.phaffii gadusol合成菌株的构建
前期研究中本团队已获得带有斑马鱼来源gadusol合成基因的质粒,在经过BstBⅠ酶线性化后整合至K.phaffii基因组AOX1的3’端,并通过100 mg/L博来霉素筛选得到GS-EM菌株,其gadusol产量非常低(5.9 mg/L,0.69 mg/g DCW)[18]。SCORER等[20]发现,G418抗性与拷贝数密切相关,在4 000 mg/L的G418抗性下目的基因的拷贝数为7~12,证明了利用G418直接筛选高拷贝转化子是可行的。因此,本研究将利用高浓度G418抗性重新快速筛选gadusol合成菌株。本研究所使用质粒及菌株如表1所示。将实验室保藏的质粒pPIC9K-EM用Sal Ⅰ酶进行线性化,使用胶回收纯化试剂盒将线性化片段纯化后电转整合至GS0基因组His4处,在组氨酸缺陷培养基(MD培养基)初步筛选,挑取MD平板上的His+转化子逐步点板至不同质量浓度的(250、500、1 000、2 000、4 000 mg/L)G418抗性平板来筛选高拷贝重组菌株。挑选G418抗性质量浓度为4 000 mg/L的YPD平板上的转化子进行验证,将PCR产物进行DNA测序,经比对序列正确,EEVS及MT-Ox基因成功导入K.phaffii中。
1.3.2 K.phaffii木糖同化菌株的构建
前期研究中已经通过基因合成的方式获得树干毕赤酵母(Scheffersomyces stipites)的木糖同化基因XR、XDH、XK,通过吉普森酶连以及酶切酶连的方式整合至pPIC9K,得到pPIC9K-X3质粒。为解决筛选标记缺乏问题,本研究选用Cre/loxP系统对抗性标记进行回收。本研究所使用的引物列于表2。使用带有lox71和lox66片段的引物对66-F/71-R和pGA-F/R从pGAPZαA质粒中通过PCR扩增博来霉素抗性基因Sh ble以及载体DNA片段1,X3-F/R从pPIC9K-X3质粒中获得载体DNA片段2,随后通过吉普森酶连法将Sh ble同2个载体DNA片段连接,得到质粒pGAPZL和pPIC9ZL-X3,其博来霉素两端带有loxP位点。将其转化入E.coli JM109中,在含有25 mg/L博来霉素的LLB平板上进行阳性克隆子筛选。提取阳性克隆子的质粒进行双酶切验证。Nsi Ⅰ 酶对pPIC9ZL-X3质粒进行线性化,胶回收纯化试剂盒将线性化片段纯化,使用碧云天K.phaffii化转试剂盒整合至K.phaffii基因组中,在100 mg/L博来霉素的YPDS平板上筛选,挑选转化子进行PCR验证,使用引物对PGK1-F/TEF-R和TEF2-F/XK-R进行PCR,验证木糖同化基因的存在。在所得菌株中转入PUB4-CRE质粒,在含有700 mg/L潮霉素B的YPD平板上筛选阳性克隆,使用引物对Hgy-F/R进行PCR,验证PUB-CRE质粒的存在。随后在含潮霉素B抗性的培养基中诱导Cre酶表达,对菌株中的博来霉素抗性标记进行回收,获得木糖同化菌株。
1.3.3 过表达菌株的构建
以质粒pGAPZL为载体过表达ZWF1、GND2及SOL3基因,以质粒pPIC9ZL为载体过表达TKL1基因,ZWF1、GND2、SOL3来自于K.phaffii GS115基因组,TKL1来自于酿酒酵母S288C基因组,与载体片段连接得到质粒pGAPZL-ZWF1,pGAPZL-GND2,pGAPZL-SOL3,pPIC9ZL-TKL1。以pGAPZL-ZWF1质粒的构建为例,以质粒pGAPZL为模板,使用引物对GAP-XhoI/GAP-SacII进行PCR扩增,以K.phaffii GS115基因组为模板,使用引物对ZWF1-F/R进行PCR扩增,获得带有Xho Ⅰ及Sac Ⅱ酶切位点的DNA片段,使用限制性内切酶Xho Ⅰ及Sac Ⅱ对载体片段及插入片段进行酶切获得相同的末端,使用T4 DNA连接酶进行酶连,将其转化入E.coli JM109中,在含有25 mg/L博来霉素的LLB平板上进行阳性克隆子筛选。提取阳性克隆子的质粒进行双酶切验证。质粒进行线性化后转化到K.phaffii中,在100 mg/L博来霉素的YPDS平板上筛选,使用引物对yz-GAP-F/yz-AOXTT-R进行PCR验证。
1.4 分析方法
1.4.1 残糖含量分析
取1 mL发酵液离心取上清液,使用乙醇进行醇沉除去大分子蛋白质后再次离心取上清液,用0.22 μm有机系微孔滤膜过滤后通过HPLC进行分析(配备Waters Sugar-pak1 6.5 mm×300 mm色谱柱),以超纯水为流动相,流速0.3 mL/min,时间40 min,柱温85 ℃[21],示差折光检测器。
1.4.2 发酵产物产量检测
取500 μL发酵液5 000 r/min离心5 min,分离培养基与细胞。培养基中的产物,采用甲醇醇沉的方法去除大分子蛋白质后再次离心取上清液,使用0.22 μm有机系微孔滤膜过滤后备用。胞内产物,将收集的细胞用预冷的5 mmol/L PBS缓冲液(调节pH值至7.0)洗涤2次后使用等体积PBS重悬,加入750 μL氯仿混合均匀,3 000 r/min涡旋15 min破坏细胞,使胞内gadusol释放出来[22]。取上层水层以12 000 r/min离心10 min,使用0.22 μm水系微孔滤膜进行过滤处理后备用。通过Agilent 1260 InfinityⅡ HPLC系统,Agilent ZORBAX Eclipse XDB-C18(4.6 mm×250 mm,5 μm)色谱柱和紫外-可见光检测器对gadusol进行定量。使用的流动相为甲醇和5 mmol/L PBS缓冲液(调节pH值至7.0),0~20 min为1%(体积分数)的甲醇,20~40 min甲醇梯度上升至95%,40~60 min调回1%甲醇使柱子达到平衡,流速为0.3 mL/min,温度为35 ℃,在296 nm处监测发酵产物的吸光值[23]。
1.4.3 Nanodrop UV-vis光谱法检测[7]
以GS0菌株发酵提取样品为空白,通过Nanodrop UV-vis光谱法在190~840 nm进行全波长扫描,确定合成物质的最大吸收波长。
1.4.4 实时荧光定量PCR测定基因拷贝数
为了测定基因组整合基因EEVS、MT-Ox的拷贝数,用NCBI网站对目标基因进行特异性引物设计,选择K.phaffii的3-磷酸甘油醛脱氢酶基因GAPDH作为内参,使用TB Green Premix Ex Taq Ⅱ酶在CFX96 Real-Time PCR仪进行扩增,具体实验方法参考文献中的描述[24]。用于qPCR的引物列于表2中。
2 结果与分析
2.1 K.phaffii工程菌的构建
将实验室保藏质粒pPIC9K-EM采用Sal Ⅰ酶线性化后转入K.phaffii GS0中,在含有4 000 mg/L G418的抗性平板上筛选获得5株阳性克隆菌株,PCR验证gadusol合成基因成功转入GS0,将其命名为GS1、GS2、GS3、GS4、GS5。将所得菌株在含有20 g/L葡萄糖的YPD培养基中进行发酵,取发酵第5天的菌体细胞制备gadusol,以GS0为空白对照进行检测。使用Nanodrop中UV-Vis光谱法对5株阳性克隆发酵提取物进行全波长扫描,发现在296 nm处出现最大吸收峰,其中GS3菌株发酵提取物具有最大吸收强度(图2-a)。将发酵提取物pH值调至pH 2.5,其最大吸收峰出现在268 nm处(图2-b),与文献报道一致。将GS3菌株发酵提取物进行HPLC检测,发现其与斑马鱼卵提取物出峰时间一致,均在8.1 min左右出现峰值,而对照菌株GS0中未检测到该峰(图2-c)。对胞内提取物部分进行超高效液相色谱串联四极杆飞行时间质谱联用仪(MALDI SYNAPT MS)分析(图2-d),结果表明重组菌株GS3能够合成gadusol,产量为140.7 mg/L(11.8 mg/g DCW),较GS-EM菌株(5.9 mg/L,0.69 mg/g DCW)[18]提高了22.8倍,通过qPCR测定EEVS和MT-Ox分别以5.5和6.7的拷贝存在于GS3菌株基因组中,结果表明,通过提高抗生素筛选浓度筛选高拷贝菌株来提高目标产物产量是可行的。
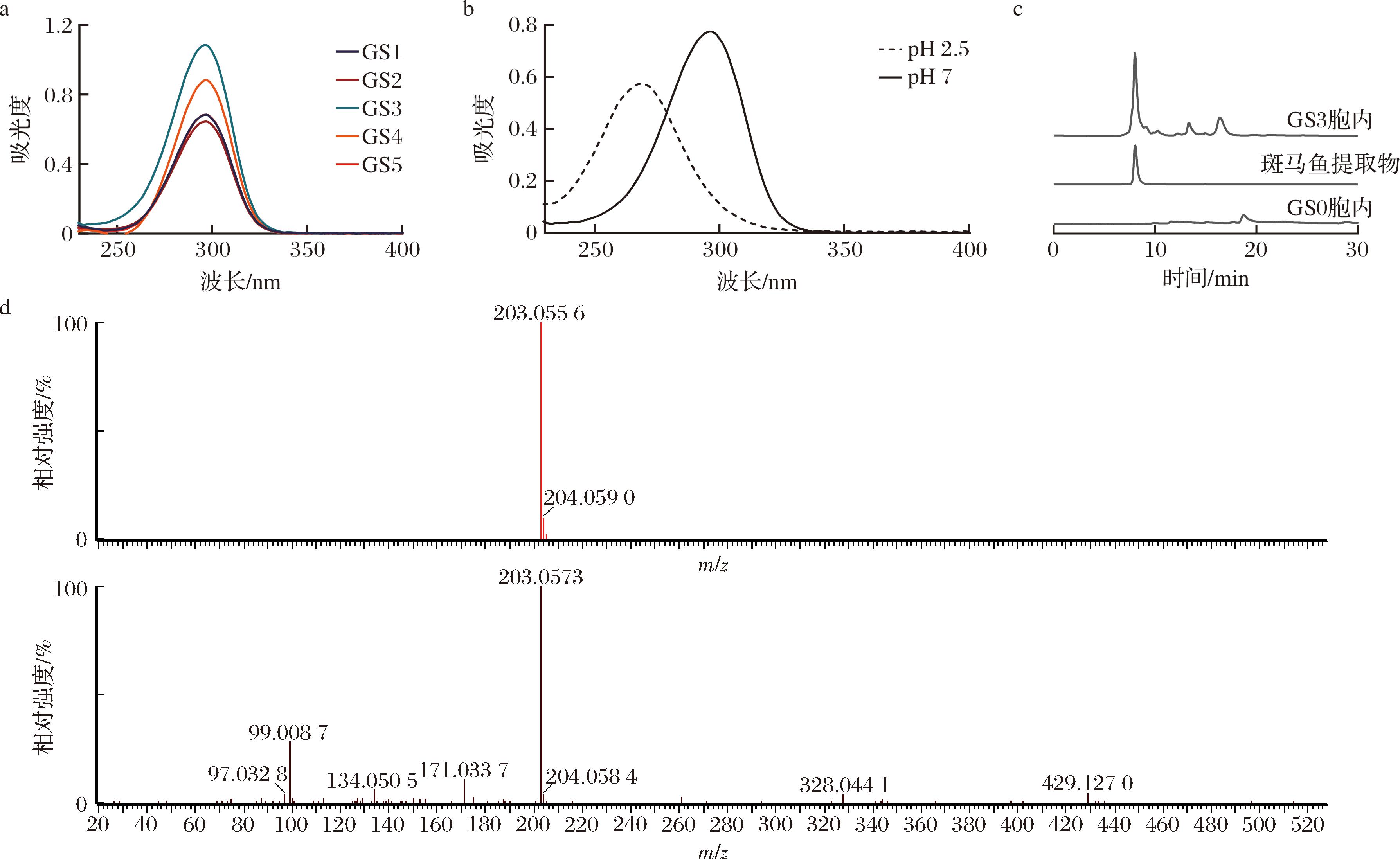
a-GS1-GS5胞内gadusol全波长扫描情况;b-GS3菌株产gadusol在pH 2.5和pH 7.0的紫外吸收光谱;c-斑马鱼提取物和酵母提取物HPLC分析结果;d-LC-MS分析结果
图2 工程菌gadusol合成情况分析
Fig.2 Analysis of gadusol synthesis in engineered strains
2.2 碳源比例对gadusol合成的影响
由图1可知,gadusol由EEVS和MT-Ox两步酶催化PPP中间体S7P而合成。当葡萄糖作为碳源时,大部分碳源进入糖酵解途径以供菌体生长,PPP代谢途径通量较少[25],而在能利用木糖代谢的菌株中,以木糖为碳源时其非氧化PPP碳通量增加且S7P积累显著[26]。为了提高菌株的木糖利用能力,本研究将由PPGK1、PTEF及PTEF2启动子控制的木糖同化基因XR、XDH、XK的质粒pPIC9ZL-X3线性化后整合至GS3基因组上,在含有100 mg/L博来霉素的YPDS平板上进行筛选。使用引物PGK1-F/TEF-R和TEF2-F/XK-R对阳性克隆进行PCR验证。在验证正确的菌株中转入PUB4-CRE质粒,利用Cre/loxP系统对博来霉素抗性标记进行回收,经过5~10次传代丢掉Cre酶表达质粒,获得木糖同化菌株GS6。
在3种不同比例的葡萄糖与木糖培养基中对菌株的生长能力进行了测定,结果如图3所示。单独使用葡萄糖为碳源时,GS0、GS3及GS6菌株的生长情况无明显差异,gadusol合成以及木糖同化途径基因的引入未对GS0菌株的生长造成影响(图3-a)。GS3和GS6的gadusol产量在20 g/L葡萄糖培养基中并无明显差异。随着木糖比例的增加,GS0、GS3及GS6的生长受到不同程度的抑制,木糖的利用也使菌株产gadusol能力增强。如图3-b所示,当木糖与葡萄糖质量比为1∶1时,GS3及GS6的生长情况较GS0好。3株菌均在第1天将葡萄糖全部消耗完,GS6在第4天将木糖消耗完毕,发酵结束时,GS3比GS0多消耗0.6 g/L木糖(图3-e和图3-f),推测是由于gadusol合成途径的引入消耗了磷酸戊糖途径中的S7P,从而导致GS3中木糖利用率的提升。但在发酵第1天GS0、GS3以及GS6均未显示出明显的木糖消耗,推测可能在葡萄糖存在的情况下木糖的利用受到抑制。单独使用木糖作为碳源时,结果如图3-c和图3-g所示,GS0及GS3在发酵第2天进入稳定期,最终仅消耗约5 g/L的木糖。而GS6在前期生长较为缓慢,48 h 后开始逐渐加快,发酵结束时消耗约18 g/L木糖。从gadusol的产量来看,添加木糖能够提高GS6中gadusol产量。在木糖与葡萄糖质量比为1∶1的培养基中,GS6的gadusol的产量最高为272.1 mg/L(24.6 mg/g DCW),是纯葡萄糖培养条件下(140.7 mg/L,11.8 mg/g DCW)的1.9倍,其产量与纯木糖培养基中发酵相比也有所提升。这些结果表明,通过PPP的木糖同化在增加gadusol产量方面是有效的,但由于木糖的不完全利用,一定量的葡萄糖的存在有助于促进细胞生长和gadusol的产生。
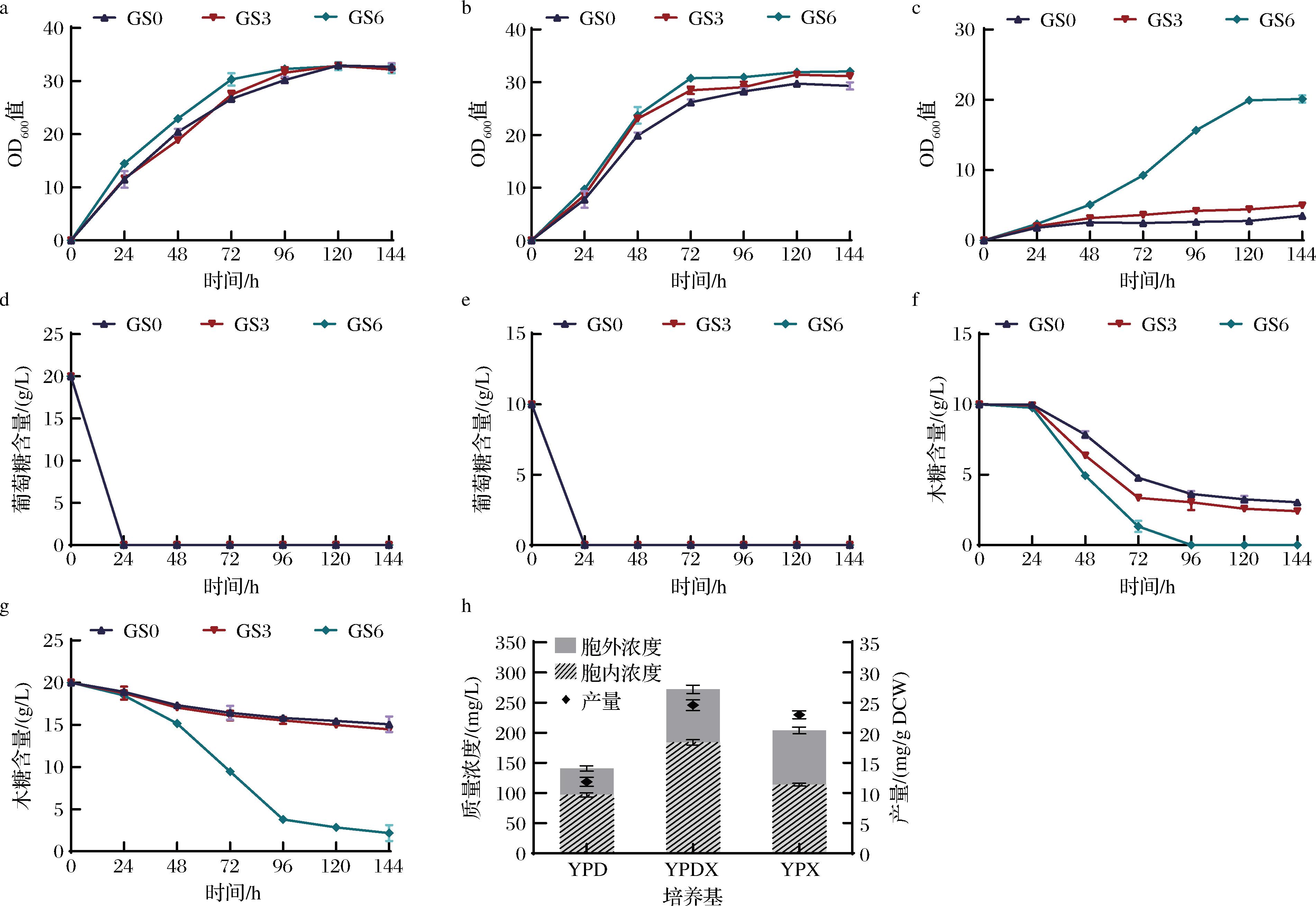
a~c-出发菌及工程菌在YPD、YPDX、YPX培养基中生长情况;d-出发菌及工程菌在YPD培养基中葡萄糖含量;e~f-出发菌及工程菌在YPDX培养基中葡萄糖及木糖含量;g-出发菌及工程菌在YPX培养基中木糖含量;h-gadusol合成情况
图3 木糖同化途径的引入及碳源组成对gadusol合成的影响
Fig.3 Improvement of gadusol production by introducing xylose assimilation pathway and using xylose as a carbon source
2.3 通过增加磷酸戊糖的碳通量来提高gadusol的产量
研究表明,PPP的单基因过表达对重组蛋白的生产产生积极的影响,其关键酶基因的过表达可以增加细胞PPP的碳通量[27]。为进一步提高PPP通量,本研究对oxiPPP中编码ZWF1、SOL3、GND2和非氧化PPP中编码TKL1的基因进行过表达,得到菌株GS7、GS8、GS9、GS10。在木糖与葡萄糖质量比为1∶1为碳源进行发酵(图4),菌株GS7、GS8、GS9、GS10中gadusol产量分别达到295.1 mg/L(25.8 mg/g DCW)、273.4 mg/L(23.6 mg/g DCW)、281.6 mg/L(24.2 mg/g DCW)、315.5 mg/L(28.3 mg/g DCW)。与GS6菌株相比,oxiPPP中ZWF1、GND2、SOL3的过表达使gadusol的产量分别提高了8.5%、0.5%、3.5%,由此推测ZWF1是oxiPPP的限速步骤,其过表达改善了PPP,提高了代谢通量。非氧化PPP中TKL1基因的过表达使gadusol的产量提高了15.9%,有效提高了PPP通量以及木糖的消耗率,作为糖酵解与PPP间可逆反应的催化酶,TKL1的过表达更好地提高了PPP通量,最终获得的工程菌gadusol产量为315.5 mg/L,是目前文献报道的K.phaffii中gadusol的最高产量(141.8 mg/L)[18]的2.2倍。
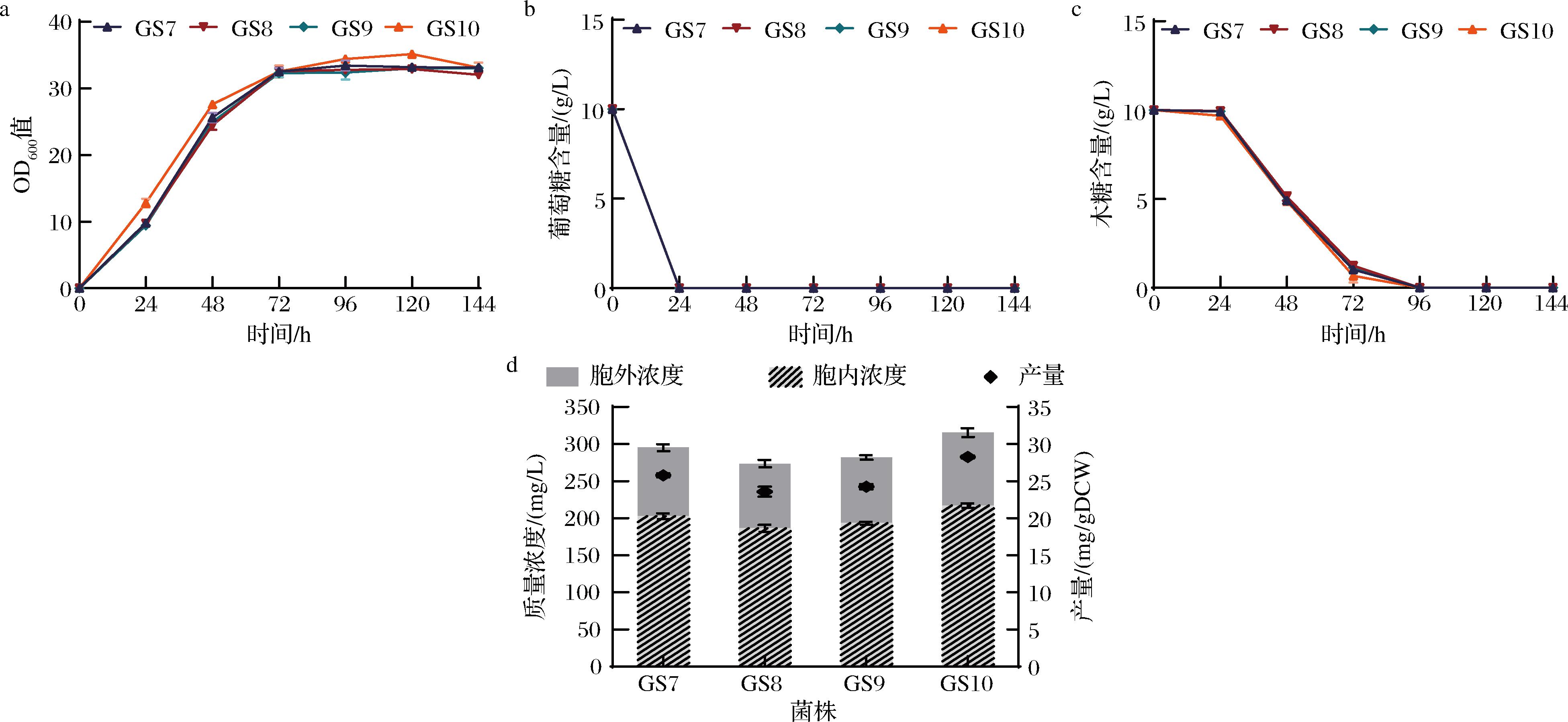
a-工程菌在YPDX培养基中生长情况;b-残葡萄糖含量;c-残木糖含量;d-gadusol合成情况
图4 ZWF1、GND2、SOL3及TKL1基因过表达对gadusol合成的影响
Fig.4 Improvement of gadusol production by overexpressing ZWF1、GND2、SOL3 and TKL1
3 结论
在前期研究中本团队已经获得产gadusol的工程菌株,仅有gadusol合成途径的GS-EM菌株gadusol产量较低[18]。研究表明,调整基因拷贝数以增加基因表达是增加靶代谢途径通量的有效方法[28],利用抗生素耐药基因筛选多拷贝插入片段是其策略之一,因为抗生素耐药水平与整合到转化体中的表达载体的数量大致相关[29]。SHEN等[30]在含有800 mg/L的博来霉素平板上筛选的高拷贝菌株腈水解酶的表达及活性都显著提高。本研究在转入gadusol合成途径后利用4 000 mg/L的G418进行高拷贝筛选,EEVS和MT-Ox分别以5.5和6.7的拷贝存在于GS3菌株基因组中,GS3菌株gadusol产量比GS-EM菌株提高了22.8倍。GS6菌株在葡萄糖与木糖质量比为1∶1 的培养基中细胞生物量及gadusol产量均比单一碳源培养基中高,但在发酵第1天,葡萄糖存在情况下木糖几乎不消耗,在发酵第4天木糖被完全消耗。GU等[31]在E.coli中引入木糖途径后发现以葡萄糖与木糖质量比为2∶1作为碳源进行发酵时异丁醇产量比用纯葡萄糖为唯一碳源时高11.7%。HOU等[32]发现多数工程菌株在共发酵时会顺序利用葡萄糖和木糖,木糖的代谢常因葡萄糖的存在而延迟。在利用木糖和葡萄糖发酵生产乙醇的研究中发现在葡萄糖与木糖质量比为1∶1时细胞生物量达到最高,而葡萄糖与木糖质量比为1∶5时木糖利用率达到最![]() 等[34]在探究不同糖源组合及比例对菌株生长和糖利用的影响时表示,在24 h内,葡萄糖和木糖均为2 g/L的培养基中木糖能完全消耗,而在5 g/L的木糖培养基中消耗率不到20%。葡萄糖和木糖的共利用能提高菌株中木糖的消耗从而使目标产物产量提升,合适的比例条件下木糖的利用可以不受到葡萄糖存在的限制。因此,葡萄糖及木糖比例的进一步优化有待研究,以实现木糖的快速消耗,提高重组菌株gadusol的生产效率。
等[34]在探究不同糖源组合及比例对菌株生长和糖利用的影响时表示,在24 h内,葡萄糖和木糖均为2 g/L的培养基中木糖能完全消耗,而在5 g/L的木糖培养基中消耗率不到20%。葡萄糖和木糖的共利用能提高菌株中木糖的消耗从而使目标产物产量提升,合适的比例条件下木糖的利用可以不受到葡萄糖存在的限制。因此,葡萄糖及木糖比例的进一步优化有待研究,以实现木糖的快速消耗,提高重组菌株gadusol的生产效率。
ZWF1、SOL3、GND2是oxiPPP关键酶,负责将糖酵解途径中的G6P转化为5-磷酸核酮糖而进入PPP[35]。非氧化PPP由一系列可逆反应组成,这些反应在糖酵解途径和PPP之间建立联系,其中TKL1催化R5P和F6P之间的转化。为了增加重组菌株PPP通量以及更多的利用木糖,本研究对PPP中关键酶基因ZWF1、GND2、SOL3及TKL1过表达。在葡萄糖与木糖质量比为1∶1的培养基发酵,ZWF1、SOL3及TKL1过表达菌株中均表现出gadusol产量的提升,GND2的过表达对gadusol产量的提升没有积极的影响,这可能与K.phaffii中GND2表现出高表达水平,而SOL3表现出低表达水平[10,36]有关,推测GND2不是氧化PPP的限速步骤,其过表达未起到增强oxiPPP通量的作用。ZWF1的过表达对gadsuol产量的提升效果比SOL3好,PRIELHOFER等[37]的研究也表明,在葡萄糖受限的情况下,与SOL3相比,ZWF1的过表达能显著上调K.phaffii中的蛋白质产生,作为PPP关键酶,其过表达促进了途径通量,可能为这些催化酶的产生提供了更有利的代谢环境,如更多的NADPH等还原力以及中间代谢产物,间接促进相关催化酶的生成,从而提高重组蛋白产量[38]。TKL1基因的过表达提高gadusol产量可能与木糖消耗率的提高有关,由TAL1和TKL1催化的非氧化PPP反应被认为是酵母高效利用木糖发酵的瓶颈[12],作为S7P上游的基因以及参与糖酵解与PPP间可逆反应的催化酶基因,TKL1基因的过表达能更好地提高细胞中PPP通量。未来,这些基因中的多个基因的联合过表达对gadusol的合成产生协同作用还是抑制作用值得进一步探究。
本研究在K.phaffii中异源表达gadusol合成基因,通过提高G418筛选浓度获得产gadusol的工程菌。通过引入S.stipites来源的木糖同化基因并进行碳源优化提升gadusol产量,为272.1 mg/L(24.6 mg/g DCW)。在此基础上,通过过表达PPP中的关键基因ZWF1、GND2、SOL3、TKL1,gadusol的产量分别提高了8.5%、0.5%、3.5%、15.9%,其中过表达TKL1基因的工程菌株中gadusol产量最高,达到315.5 mg/L(28.3 mg/g DCW)。K.phaffii作为gadusol生产的潜在宿主,在工业应用中仍需提高其产量和产率,其中碳源的比例以及PPP的代谢通量是提升gadusol产量的关键因素。
[1] CARVALHO P G,NAVEIRA R I,GRANONE L I,et al.A comparative review of natural and synthetic UV filters:Gadusol and benzophenone-3 as representative examples[J].Environmental Advances,2023,13:100404.
[2] 朱小山,黄静颖,吕小慧,等.防晒剂的海洋环境行为与生物毒性[J].环境科学,2018,39(6):2991-3002.ZHU X S,HUANG J Y,LYU X H,et al.Fate and toxicity of UV filters in marine environments[J].Environmental Science,2018,39(6):2991-3002.
[3] 顾智强,张振华,徐琰雯,等.南极绿藻中类菌胞素氨基酸对UV-B胁迫的响应[J].海洋科学,2018,42(12):37-46.GU Z Q,ZHANG Z H,XU Y W,et al.Study of response of mycosporine-like amino acids in Antarctic green algae to UV-B radiation[J].Marine Sciences,2018,42(12):37-46.
[4] COUTEAU C,COIFFARD L.Phycocosmetics and other marine cosmetics,specific cosmetics formulated using marine resources[J].Marine Drugs,2020,18(6):322.
[5] ORALLO D E,LORES N J,ARBELOA E M,et al.Sensitized photo-oxidation of gadusol species mediated by singlet oxygen[J].Journal of Photochemistry and Photobiology B:Biology,2020,213:112078.
[6] FRAIKIN G Y,BELENIKINA N S,RUBIN A B.Photochemical processes of cell DNA damage by UV radiation of various wavelengths:Biological consequences[J].Molecular Biology,2024,58(1):1-16.
[7] RICE M C,LITTLE J H,FORRISTER D L,et al.Gadusol is a maternally provided sunscreen that protects fish embryos from DNA damage[J].Current Biology,2023,33(15):3229-3237e4.
[8] ARBELOA E M,BERTOLOTTI S G,CHURIO M S.Photophysics and reductive quenching reactivity of gadusol in solution[J].Photochemical &Photobiological Sciences,2011,10(1):133-142.
[9] TOM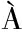 S-GAMISANS M,ANDRADE C C P,MARESCA F,et al.Redox engineering by ectopic overexpression of NADH kinase in recombinant Pichia pastoris (Komagataella phaffii):Impact on cell physiology and recombinant production of secreted proteins[J].Applied and Environmental Microbiology,2020,86(6):e02038-e02019.
S-GAMISANS M,ANDRADE C C P,MARESCA F,et al.Redox engineering by ectopic overexpression of NADH kinase in recombinant Pichia pastoris (Komagataella phaffii):Impact on cell physiology and recombinant production of secreted proteins[J].Applied and Environmental Microbiology,2020,86(6):e02038-e02019.
[10] CHEN S L,LIU T S,ZHANG W G,et al.Cofactor engineering for efficient production of α-farnesene by rational modification of NADPH and ATP regeneration pathway in Pichia pastoris[J].International Journal of Molecular Sciences,2023,24(2):1767.
[11] KLEIJN R J,VAN WINDEN W A,VAN GULIK W M,et al.Revisiting the 13C-label distribution of the non-oxidative branch of the pentose phosphate pathway based upon kinetic and genetic evidence[J].The FEBS Journal,2005,272(19):4970-4982.
[12] WALFRIDSSON M,HALLBORN J,PENTTIL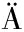 M,et al.Xylose-metabolizing Saccharomyces cerevisiae strains overexpressing the TKL1 and TAL1 genes encoding the pentose phosphate pathway enzymes transketolase and transaldolase[J].Applied and Environmental Microbiology,1995,61(12):4184-4190.
M,et al.Xylose-metabolizing Saccharomyces cerevisiae strains overexpressing the TKL1 and TAL1 genes encoding the pentose phosphate pathway enzymes transketolase and transaldolase[J].Applied and Environmental Microbiology,1995,61(12):4184-4190.
[13] KOBAYASHI Y,SAHARA T,SUZUKI T,et al.Genetic improvement of xylose metabolism by enhancing the expression of pentose phosphate pathway genes in Saccharomyces cerevisiae IR-2 for high-temperature ethanol production[J].Journal of Industrial Microbiology &Biotechnology,2017,44(6):879-891.
[14] JIN H,KIM S,LEE D,et al.Efficient production of mycosporine-like amino acids,natural sunscreens,in Yarrowia lipolytica[J].Biotechnology for Biofuels and Bioproducts,2023,16(1):162.
[15] YUAN L,QIN Y L,ZOU Z C,et al.Enhancing intracellular NADPH bioavailability through improving pentose phosphate pathway flux and its application in biocatalysis asymmetric reduction reaction[J].Journal of Bioscience and Bioengineering,2022,134(6):528-533.
[16] PARK S H,LEE K,JANG J W,et al.Metabolic engineering of Saccharomyces cerevisiae for production of shinorine,a sunscreen material,from xylose[J].ACS Synthetic Biology,2019,8(2):346-357.
[17] FICKERS P,LE DALL M T,GAILLARDIN C,et al.New disruption cassettes for rapid gene disruption and marker rescue in the yeast Yarrowia lipolytica[J].Journal of Microbiological Methods,2003,55(3):727-737.
[18] 易崇华,钱思雨,钮成拓,等.天然紫外吸收剂gadusol在毕赤酵母中的生物合成及其性能分析[J].生物工程学报,2024,40(9):3039-3056.YI C H,QIAN S Y,NIU C T,et al.Synthesis and properties of the natural ultraviolet absorber gadusol in Komagataella phaffii[J].Chinese Journal of Biotechnology,2024,40(9):3039-3056.
[19] 仪宏,王丽丽,冯惠勇,等.含葡萄糖培养基高温灭菌变色及其防范措施的研究[J].酿酒,2003(2):42-43.YI H,WANG L L,FENG H Y,et al.The color producing problem of glucose-containing medium during sterilization and its prevention measurements[J].Liquor-making,2003,30(2):42-43.
[20] SCORER C A,CLARE J J,MCCOMBIE W R,et al.Rapid selection using G418 of high copy number transformants of Pichia pastoris for high-level foreign gene expression[J].Nature Biotechnology,1994,12(2):181-184.
[21] CHEN H Q,CHEN H Q,LU H Q,et al.Carbohydrate analysis of Mortierella alpina by colorimetry and HPLC-ELSD to reveal accumulation differences of sugar and lipid[J].Biotechnology Letters,2021,43(7):1289-1301.
[22] KIM S,PARK B G,JIN H,et al.Efficient production of natural sunscreens shinorine,Porphyra-334,and mycosporine-2-glycine in Saccharomyces cerevisiae[J].Metabolic Engineering,2023,78:137-147.
[23] OSBORN A R,ALMABRUK K H,HOLZWARTH G,et al.De novo synthesis of a sunscreen compound in vertebrates[J].eLife,2015,4:e05919.
[24] 宣姚吉,周祥山,张元兴.实时荧光定量PCR检测毕赤酵母基因组中外源基因拷贝数[J].中国生物制品学杂志,2009(12):1236-1239;1243.XUAN Y J,ZHOU X S,ZHANG Y X.Determination of copy number of foreign gene in genome of Pichia pastoris by real-time fluorescent quantitative PCR[J].Chinese Journal of Biologicals,2009(12):1236-1239;1243.
[25] 王明,栾韬,赵建志,等.酿酒酵母转化木糖生产化学品的研究进展[J].生物工程学报,2021,37(3):1042-1057.WANG M,LUAN T,ZHAO J Z,et al.Progress in studies on production of chemicals from xylose by Saccharomyces cerevisiae[J].Chinese Journal of Biotechnology,2021,37(3):1042-1057.
[26] KWAK S,JO J H,YUN E J,et al.Production of biofuels and chemicals from xylose using native and engineered yeast strains[J].Biotechnology Advances,2019,37(2):271-283.
[27] NOCON J,STEIGER M G,PFEFFER M,et al.Model based engineering of Pichia pastoris central metabolism enhances recombinant protein production[J].Metabolic Engineering,2014,24:129-138.
[28] ZHANG X Y,CHEN S T,LIN Y,et al.Metabolic engineering of Pichia pastoris for high-level production of lycopene[J].ACS Synthetic Biology,2023,12(10):2961-2972.
[29] SHEN Q,YU Z,ZHOU X T,et al.Identification of a novel promoter for driving antibiotic-resistant genes to reduce the metabolic burden during protein expression and effectively select multiple integrations in Pichia pastoris[J].Applied Microbiology and Biotechnology,2021,105(8):3211-3223.
[30] SHEN Q,YU Z,LV P J,et al.Engineering a Pichia pastoris nitrilase whole cell catalyst through the increased nitrilase gene copy number and co-expressing of ER oxidoreductin 1[J].Applied Microbiology and Biotechnology,2020,104(6):2489-2500.
[31] GU P F,LI F F,HUANG Z S.Engineering Escherichia coli for isobutanol production from xylose or glucose-xylose mixture[J].Microorganisms,2023,11(10):2573.
[32] HOU J,QIU C X,SHEN Y,et al.Engineering of Saccharomyces cerevisiae for the efficient co-utilization of glucose and xylose[J].FEMS Yeast Research,2017,17(4):fox034.
[33] HUANG M T,CUI X X,ZHANG P N,et al.Engineered Saccharomyces cerevisiae harbors xylose isomerase and xylose transporter improves co-fermentation of xylose and glucose for ethanol production[J].Preparative Biochemistry &Biotechnology,2024,54(8):1058-1067.
[34] ![]() P,DE LORENZO V.Refactoring the upper sugar metabolism of Pseudomonas putida for co-utilization of cellobiose,xylose,and glucose[J].Metabolic Engineering,2018,48:94-108.
P,DE LORENZO V.Refactoring the upper sugar metabolism of Pseudomonas putida for co-utilization of cellobiose,xylose,and glucose[J].Metabolic Engineering,2018,48:94-108.
[35] PATRA K C,HAY N.The pentose phosphate pathway and cancer[J].Trends in Biochemical Sciences,2014,39(8):347-354.
[36] REBNEGGER C,GRAF A B,VALLI M,et al.In Pichia pastoris,growth rate regulates protein synthesis and secretion,mating and stress response[J].Biotechnology Journal,2014,9(4):511-525.
[37] PRIELHOFER R,CARTWRIGHT S P,GRAF A B,et al.Pichia pastoris regulates its gene-specific response to different carbon sources at the transcriptional,rather than the translational,level[J].BMC Genomics,2015,16(1):167.
[38] NOCON J,STEIGER M,MAIRINGER T,et al.Increasing pentose phosphate pathway flux enhances recombinant protein production in Pichia pastoris[J].Applied Microbiology and Biotechnology,2016,100(13):5955-5963.