肌醇(又称环己六醇),是一种具有六碳环醇结构的多元醇化合物[1-2]。由于其6个羟基的差向异构化,肌醇存在包括肌肌醇(myo-inositol,MI)和鲨肌醇(scyllo-inositol,SI)在内的9种可能的立体异构体[3-4]。其中,MI广泛存在于植物、动物和微生物中,而其他立体异构体在自然界中相对较少[5-6]。MI可以通过差向异构化转化为包括SI在内的其他肌醇[4]。SI可以抑制Aβ淀粉样蛋白和神经元聚集并减弱其在大脑中的毒性,被认为是治疗阿尔茨海默病等神经系统疾病的潜在药物[7]。因此,SI在制药领域具有巨大应用的潜力。
化学合成法是生产SI的经典方法[7],但生产过程步骤复杂,要求严格,产率低,成本高,需要使用危险化学品,对环境危害较大。与之相比,生物合成方法由于使用了更简单的前体、对环境无害以及反应条件更温和而更适合用于SI的生产。SI的生物合成研究首先采用的是将MI转化成SI的生物转化法,如TANAKA等[8]2017年通过代谢工程改造枯草芽孢杆菌,从50 g/L MI合成出27.6 g/L SI。2020年,MICHON等[9]在这一基础上,进一步实现了SI的从头合成,最终以更廉价的葡萄糖为底物生产了2 g/L的SI。2021年,RAMP等[10]通过代谢工程改造谷氨酸棒杆菌(Corynebacterium glutamicum),分别以葡萄糖和蔗糖为底物从头合成1.8 g/L和4.4 g/L的SI。
如图1所示,谷氨酸棒杆菌摄取葡萄糖并磷酸化获得葡萄糖-6-磷酸(glucose-6-phosphate,G6P),再在由ino1基因编码的内源肌醇磷酸合酶(myo-inositol 1-phosphate synthase,IPS)和由impA基因编码的内源肌醇单磷酸酶(myo-inositol 1-phosphatase,IMP)的作用下生成MI。MI在MI脱氢酶(IolG)的作用下被氧化为鲨肌糖(2-keto-myo-inositol,2KMI),同时伴随着NAD+到NADH的还原,随后2KMI在SI脱氢酶(IolW)的作用下被还原为SI,同时伴随着NADPH到NADP+的氧化[10]。G6P是中心代谢的一个关键节点,被多个途径所利用。G6P可以在pgi基因编码的磷酸葡萄糖异构酶催化下转化为果糖-6-磷酸,进入糖酵解途径,也可以在zwf基因编码的葡萄糖-6-磷酸脱氢酶催化下,氧化生成6-磷酸葡萄糖酸内酯,进入磷酸戊糖途径。由于中心代谢对G6P的竞争能力更强,G6P流向肌醇合成途径的通量很少,因此菌株合成MI和SI的天然能力较弱。此外,谷氨酸棒杆菌可以以MI和SI作为唯一碳源进行生长,与它们分解代谢相关的基因大多数都位于基因组的2个基因簇iol1和iol2中。MI到SI转化的中间产物2KMI在IolE、IolD、IolB、IolC、IolJ、IolA多个酶的作用下被分解成二羟-3-丙酮磷酸和乙酰辅酶A,分别进入糖酵解途径和三羧酸循环[4]。由于这种肌醇分解代谢途径的存在,即使合成MI和SI,也难以有效积累。
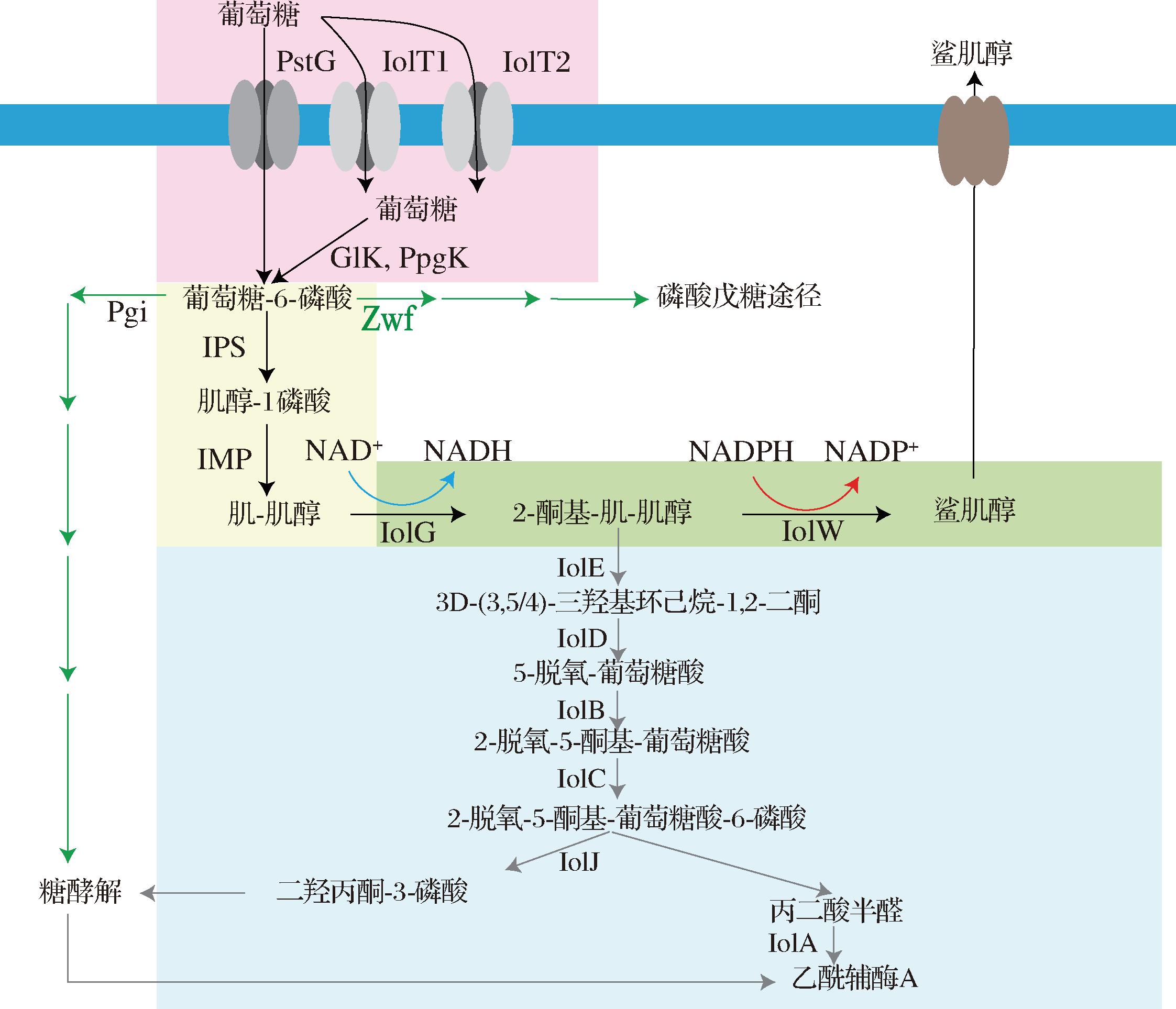
图1 谷氨酸棒杆菌中的鲨肌醇合成
Fig.1 Synthesis of SI in C.glutamicum
注:Pgi,磷酸葡萄糖异构酶;Zwf,葡萄糖-6-磷酸脱氢酶;PstG,葡萄糖特异性渗透酶;GlK,葡萄糖激酶;IolE,2-酮-肌醇脱水酶;IolD,3D-(3,5/4)-三羟基环己烷-1,2-二酮水解酶;IolB,5-脱氧葡萄糖醛酸异构酶;IolC,2-脱氧-5-酮-D-葡萄糖酸激酶;IolJ,特异性醛缩酶;IolA,甲基丙二酸半醛脱氢酶。
因此,为了以葡萄糖为底物从头合成SI,本研究计划通过基因敲除阻断谷氨酸棒杆菌SN01中的肌醇分解代谢,保留MI到SI转化路径中的关键酶,同时在基因组上整合外源IPS和IMP,以及用强启动子替换iolW天然启动子,完善菌株从头合成SI的能力。然后考虑到中心碳代谢和细胞生长对G6P的强烈竞争作用,用不同工具动态调控pgi和zwf的表达以及过表达内源IPS编码基因ino1,通过弱化竞争途径和强化合成途径优化关键前体G6P的代谢分配,促进SI的合成。此外,探索强化葡萄糖摄取和磷酸化提高前体G6P的富集,以及通过强化电子传递链功能提高辅因子NAD+供应对SI从头合成的影响。
1 材料与方法
1.1 材料与试剂
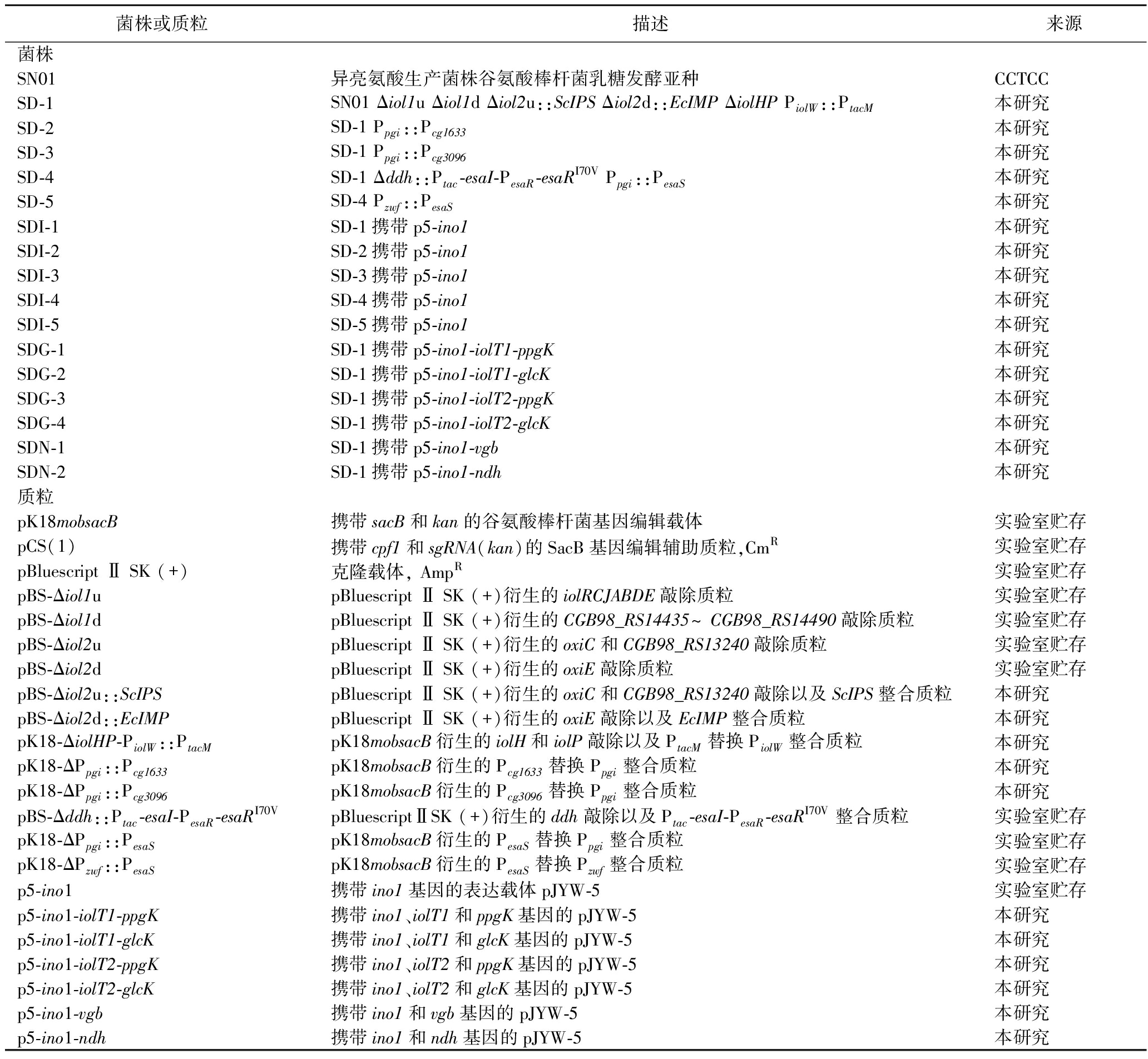
本研究中使用的菌株和质粒如表1所示。
表1 本文所用的菌株和质粒
Table 1 Strains and plasmids used in this paper
菌株或质粒描述来源菌株SN01异亮氨酸生产菌株谷氨酸棒杆菌乳糖发酵亚种CCTCCSD-1SN01 Δiol1u Δiol1d Δiol2u::ScIPS Δiol2d::EcIMP ΔiolHP PiolW::PtacM本研究SD-2SD-1 Ppgi::Pcg1633本研究SD-3SD-1 Ppgi::Pcg3096本研究SD-4SD-1 Δddh::Ptac-esaI-PesaR-esaRI70V Ppgi::PesaS本研究SD-5SD-4 Pzwf::PesaS本研究SDI-1SD-1携带p5-ino1本研究SDI-2SD-2携带p5-ino1本研究SDI-3SD-3携带p5-ino1本研究SDI-4SD-4携带p5-ino1本研究SDI-5SD-5携带p5-ino1本研究SDG-1SD-1携带p5-ino1-iolT1-ppgK本研究SDG-2SD-1携带p5-ino1-iolT1-glcK本研究SDG-3SD-1携带p5-ino1-iolT2-ppgK本研究SDG-4SD-1携带p5-ino1-iolT2-glcK本研究SDN-1SD-1携带p5-ino1-vgb本研究SDN-2SD-1携带p5-ino1-ndh本研究质粒pK18mobsacB携带sacB和kan的谷氨酸棒杆菌基因编辑载体实验室贮存pCS(1)携带cpf1和sgRNA(kan)的SacB基因编辑辅助质粒,CmR实验室贮存pBluescript Ⅱ SK (+)克隆载体, AmpR实验室贮存pBS-Δiol1upBluescript Ⅱ SK (+)衍生的iolRCJABDE敲除质粒实验室贮存pBS-Δiol1dpBluescript Ⅱ SK (+)衍生的CGB98_RS14435~ CGB98_RS14490敲除质粒实验室贮存pBS-Δiol2upBluescript Ⅱ SK (+)衍生的oxiC和CGB98_RS13240敲除质粒实验室贮存pBS-Δiol2dpBluescript Ⅱ SK (+)衍生的oxiE敲除质粒实验室贮存pBS-Δiol2u::ScIPSpBluescript Ⅱ SK (+)衍生的oxiC和CGB98_RS13240敲除以及ScIPS整合质粒本研究pBS-Δiol2d::EcIMPpBluescript Ⅱ SK (+)衍生的oxiE敲除以及EcIMP整合质粒本研究pK18-ΔiolHP-PiolW::PtacMpK18mobsacB衍生的iolH和iolP敲除以及PtacM替换PiolW整合质粒本研究pK18-ΔPpgi::Pcg1633pK18mobsacB衍生的Pcg1633替换Ppgi整合质粒本研究pK18-ΔPpgi::Pcg3096pK18mobsacB衍生的Pcg3096替换Ppgi整合质粒本研究pBS-Δddh::Ptac-esaI-PesaR-esaRI70VpBluescriptⅡSK (+)衍生的ddh敲除以及Ptac-esaI-PesaR-esaRI70V整合质粒实验室贮存pK18-ΔPpgi::PesaSpK18mobsacB衍生的PesaS替换Ppgi整合质粒实验室贮存pK18-ΔPzwf::PesaSpK18mobsacB衍生的PesaS替换Pzwf整合质粒实验室贮存p5-ino1携带ino1基因的表达载体pJYW-5实验室贮存p5-ino1-iolT1-ppgK携带ino1、iolT1和ppgK基因的pJYW-5本研究p5-ino1-iolT1-glcK携带ino1、iolT1和glcK基因的pJYW-5本研究p5-ino1-iolT2-ppgK携带ino1、iolT2和ppgK基因的pJYW-5本研究p5-ino1-iolT2-glcK携带ino1、iolT2和glcK基因的pJYW-5本研究p5-ino1-vgb携带ino1和vgb基因的pJYW-5本研究p5-ino1-ndh携带ino1和ndh基因的pJYW-5本研究
LB培养基(g/L):NaCl 5、胰蛋白胨5、酵母提取物2.5。LBB 培养基(g/L):胰蛋白胨5、酵母提取物2.5、NaCl 5和脑心浸液18.5。LBB培养基即LB培养基加入脑心浸液。
1.2 仪器与设备
752 紫外分光光度计,上海舜宇恒平科学仪器有限公司;DELTA 320型pH计,METTLER TOLEDO科技(中国)有限公司; SBA-40E 生物传感分析仪,山东省科学院生物研究所;Agilent 1200高效液相色谱仪(HPLC),美国Agilent公司;Hypersil 00S-2 250 mm×4.6 mm 5 μm C18分析柱,赛默飞世尔科技公司。
1.3 实验方法
1.3.1 菌株构建方法
1.3.1.1 底盘菌株SD-1的构建
构建了5个质粒用来分步敲除谷氨酸棒杆菌SN01中的24个肌醇分解代谢基因。其中pBS-Δiol1u、pBS-Δiol1d、pBS-Δiol2u和pBS-Δiol2d质粒构建具体步骤参考文献[11]。实验室前期构建的质粒pBS-Δiol2u经HindⅢ线性化后与扩增的酿酒酵母IPS基因ScIPS连接,构建质粒pBS-Δiol2u::ScIPS。同理,实验室前期构建的质粒pBS-Δiol2d经SalⅠ线性化后与扩增的大肠杆菌IMP基因EcIMP连接,构建质粒pBS-Δiol2d::EcIMP。以谷氨酸棒杆菌SN01基因组为模板,扩增iolHP-PiolW的上下游同源臂和PtacM启动子片段并连接,构建质粒pK18-ΔiolHP-PiolW::PtacM。
将pBS-Δiol1u、pBS-Δiol1d、pBS-Δiol2u::ScIPS、pBS-Δiol2d::EcIMP、pK18-ΔiolHP-PiolW::PtacM质粒陆续电转入菌株SN01中敲除肌醇分解代谢相关基因并敲入ScIPS和EcIMP基因和替换iolW天然启动子,最终获得底盘菌株SD-1。
1.3.1.2 下调G6P节点竞争途径通量菌株的构建
采用生长依赖型启动子和Esa群体感应系统2种方法动态下调竞争G6P的途径的通量。
本研究选择了Pcg1633和Pcg3096这2个生长后期下调型启动子替换pgi的天然启动子。以谷氨酸棒杆菌 SN01基因组为模板,扩增出Pcg1633片段、Pcg3096片段以及Ppgi上下游同源臂,分别连接构建质粒pK18-ΔPpgi::Pcg1633和pK18-ΔPpgi::Pcg3096。将这2个质粒分别电转入菌株SD-1中,获得菌株SD-2和SD-3。
本研究还选择了Esa群体感应系统的下调型启动子PesaS替换pgi和zwf的天然启动子。实验室前期已经构建了Esa感应元件整合质粒pBS-Δddh::Ptac-esaI-PesaR-esaRI70V以及响应元件整合质粒pK18-ΔPpgi::PesaS和pK18-ΔPzwf::PesaS[11]。将质粒pBS-Δddh::Ptac-esaI-PesaR-esaRI70V和pK18-ΔPpgi::PesaS陆续电转入SD-1中,获得菌株SD-4,继续将质粒pK18-ΔPzwf::PesaS电转入菌株SD-4中,获得菌株SD-5。
1.3.1.3 内源肌醇磷酸合酶基因ino1过表达菌株的构建
实验室之前已经构建质粒p5-ino1。将质粒p5-ino1 分别电转入菌株SD-1到SD-5中,获得菌株SDI-1~SDI-5。
1.3.1.4 促进G6P供应菌株的构建
为了提高菌株的葡萄糖摄取和磷酸化能力,促进G6P的供应,扩增内源肌-肌醇渗透酶基因iolT1、iolT2以及葡萄糖激酶基因ppgK和枯草芽孢杆菌的葡萄糖激酶基因glcK,插入质粒p5-ino1的ino1基因后,构建质粒p5-ino1-iolT1-ppgK、p5-ino1-iolT1-glcK、p5-ino1-iolT2-ppgK和p5-ino1-iolT2-glcK。将这4个质粒分别电转入菌株SD-1中,获得菌株SDG-1~SDG-4。
1.3.2 维持辅因子NAD+供应菌株的构建
为了强化菌株的NAD+供应和电子传递链功能,扩增透明颤菌血红蛋白基因vgb和谷氨酸棒杆菌NADH脱氢酶基因ndh,分别插入质粒p5-ino1的ino1基因后,构建质粒p5-ino1-vgb和p5-ino1-ndh,分别将它们电转入菌株SD-1中,获得菌株SDN-1~SDN-2。
1.3.3 摇瓶发酵
将保藏菌株涂布于LBB固体平板上,在30 ℃培养箱中活化培养36 h后,将菌苔转接到含有50 mL种子培养基的500 mL挡板摇瓶中,在30 ℃,200 r/min摇床预培养18 h。最后将菌液以1.8的初始OD562转接到含有50 mL发酵培养基的500 mL挡板摇瓶中,在30 ℃,200 r/min摇床发酵培养72 h。每隔12 h取样2 mL,用于测定OD562、残糖、pH和肌醇质量浓度。培养基根据需要添加抗生素。
1.3.4 发酵参数测定
对发酵所取样品进行发酵参数测定。OD562、残糖和pH测定方法参照文献[11]。肌醇质量浓度测定:将样品12 000 r/min离心10 min后取750 μL上清液,加入250 μL 20%(体积分数)三氯乙酸后静置至少4 h沉降蛋白质,12 000 r/min离心30 min后将上清液过膜处理,使用配备有Sugar-D色谱柱(4.6 mm I.D×250 mm)和示差检测器的HPLC测定MI和SI含量,流动相为乙腈/水(V乙晴∶V水=80∶20)。
2 结果与分析
2.1 谷氨酸棒杆菌SN01中肌醇分解代谢途径的阻断
谷氨酸棒杆菌SN01能以MI为唯一碳源生长[12]。为了有效地从头合成SI,需要破坏菌株对肌醇进行分解代谢的能力。如图2所示,谷氨酸棒杆菌中与肌醇分解代谢相关的基因主要位于簇iol1和iol2内。簇iol1中基因iolG编码的IolG和iolW编码的IolW都参与MI到SI的转化。在簇iol2中,基因oxiD编码MI脱氢酶的另一个同工酶OxiD[4]。因此,本研究使用了pBS-Δiol1u、pBS-Δiol1d、pBS-Δiol2u::ScIPS、pBS-Δiol2d::EcIMP和pK18-ΔiolHP-PiolW::PtacM这5个质粒将簇iol1和iol2内除这3个基因以外的基因全部敲除,同时为了初步强化SI的从头合成,在基因组上整合了来自酿酒酵母的IPS基因ScIPS和来自大肠杆菌的IMP基因EcIMP,并用强启动子PtacM代替天然PiolW启动子,获得了底盘菌株SD-1。
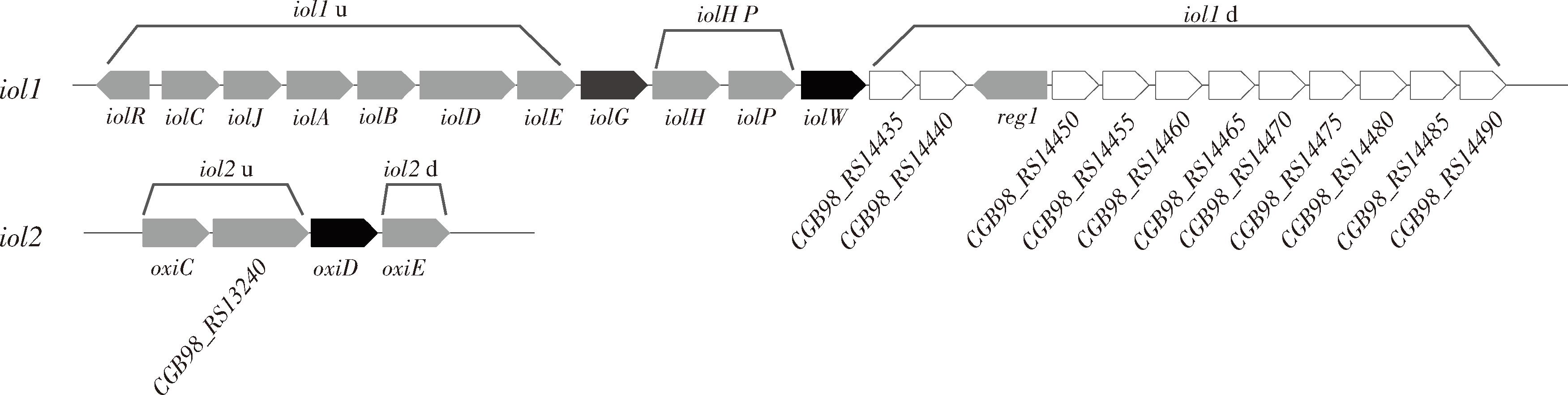
图2 簇iol1和iol2内与肌醇分解代谢相关的基因
Fig.2 Genes related to inositol catabolism in clusters iol1 and iol2
菌株SD-1的摇瓶发酵生长情况如图3所示,其中以原始菌株SN01作为对照。在发酵培养基中培养时,SD-1的生长与菌株SN01类似,均在48 h内快速生长至OD562值约63,并在48 h后达到稳定期。说明敲除肌醇分解代谢相关基因并不影响菌株在葡萄糖上的生长。此外,向培养基中添加20 g/L MI,探索菌株由MI到SI的转化能力。菌株在含MI的培养基中发酵培养时生长缓慢,72 h后OD562值仅为45,且剩余大量葡萄糖。发酵到72 h后可以转化得到18.65 g/L SI,没有剩余MI(数据未显示)。说明菌株具备将MI转化为SI的能力,分解代谢基本阻断,但阻断后MI的存在会影响菌株生长。这与RAMP等[10]的研究结果一致。生长抑制的出现可能是因为肌肌醇渗透酶IolT1和IolT2不仅可以转运葡萄糖,还可以转运MI,因此MI存在时会与葡萄糖竞争,从而减少葡萄糖摄取。另一个可能的原因是MI或其代谢产物因为无法被进一步降解用于细胞生长而在胞内积累,对代谢产生了抑制作用,从而导致生长和葡萄糖消耗减缓。
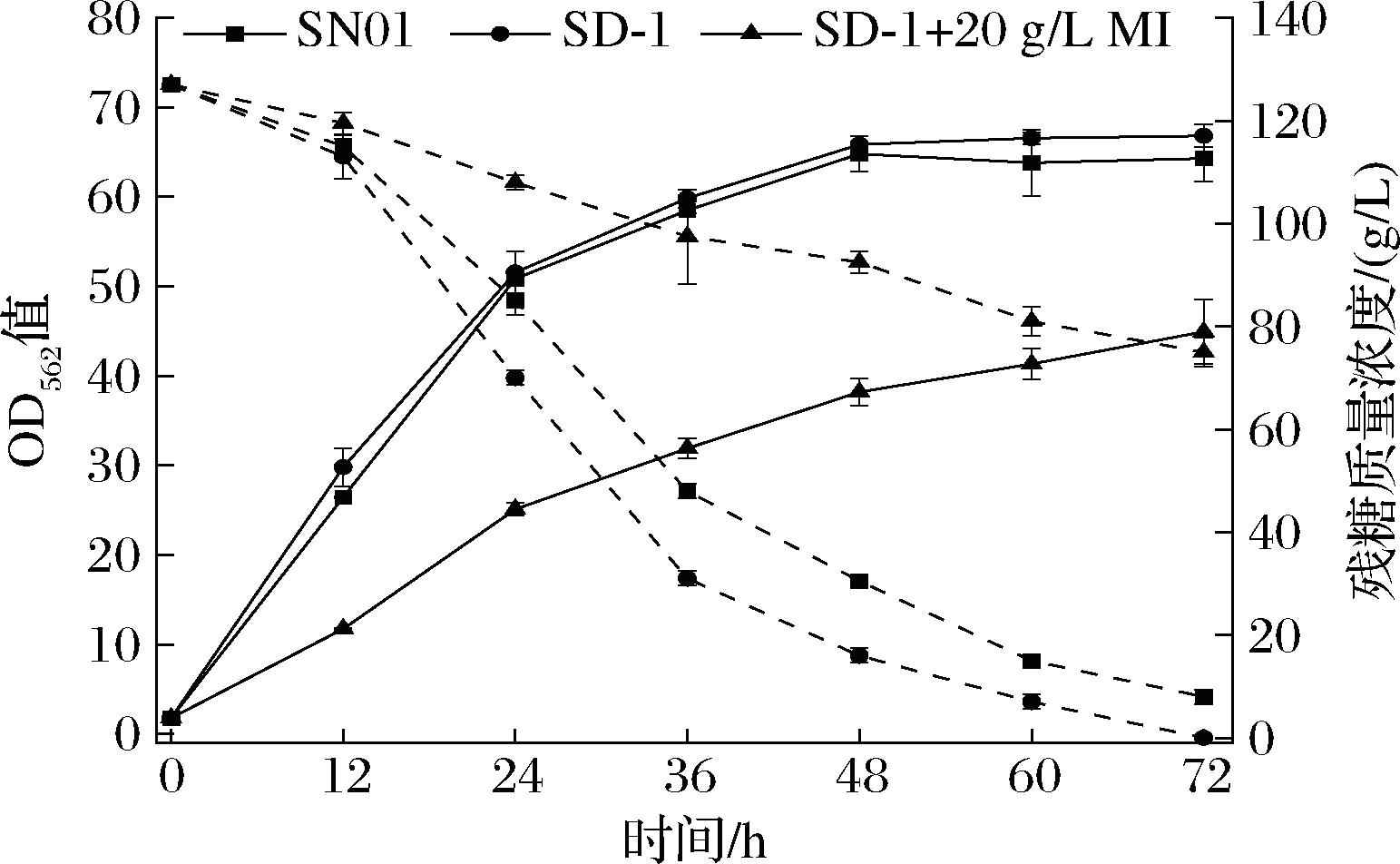
图3 底盘菌株SD-1和对照菌株SN01的OD562值和残糖
Fig.3 OD562 and glucose concentration of chassis strain SD-1
注:图中实线代表OD562值,虚线代表残糖质量浓度(下同)。
2.2 G6P竞争途径通量的限制
以葡萄糖为碳源发酵后,底盘菌株SD-1基本没有从头合成MI和SI的产量(图4),可能是G6P流向MI合成途径的通量不足,需要限制G6P流向竞争途径的通量。但G6P竞争途径主要包括糖酵解、磷酸戊糖途径等中心代谢途径,它们决定着细胞的生长代谢,如果直接阻断或者下调这些途径,会对细胞生长造成损伤,不利于产物合成。因此,为了减少G6P在中心代谢的节流对细胞生长的影响,用生长状态依赖型启动子和群体感应下调型启动子2种不同类型的启动子在生长后期下调糖酵解途径的pgi和磷酸戊糖途径的zwf基因的表达,以此来协调发酵不同阶段中细胞生长和产物生产2个过程的G6P分配。
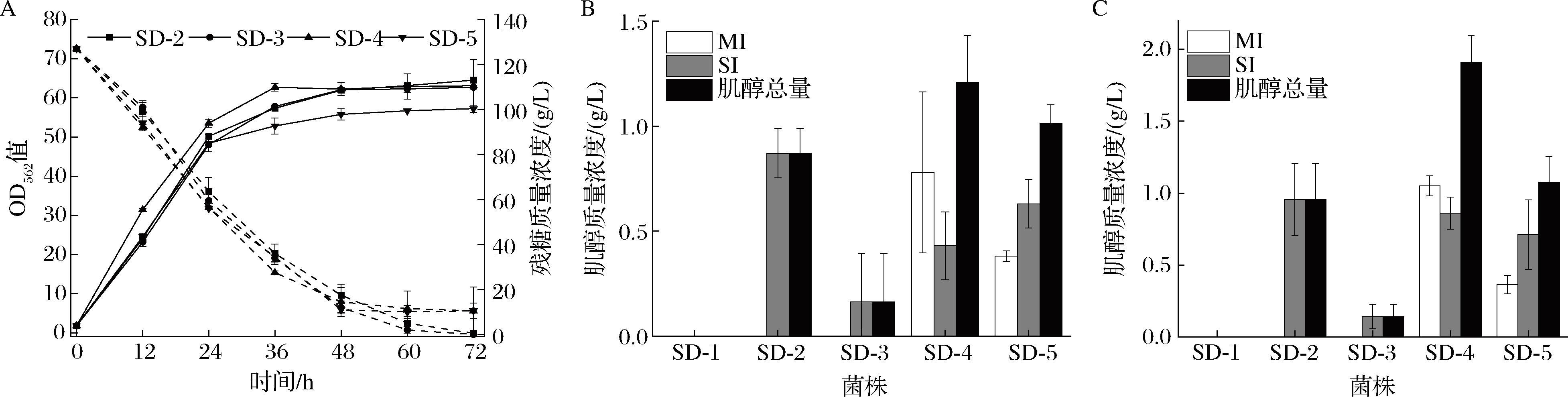
A-菌株SD-2~5的OD562值和残糖;B-发酵72 h菌株SD-2~5的肌醇产量,以菌株SD-1作为对照;C-发酵144 h菌株SD-2~5的肌醇产量,以菌株SD-1作为对照
图4 菌株SD-2~5的生长和肌醇生产
Fig.4 Growth and inositol production of strains SD-2~5
将底盘菌株SD-1中pgi的天然启动子替换为Pcg1633或Pcg3096这2个在指数期表达强度高,稳定期表达强度低的生长状态依赖型启动子[13],获得了菌株SD-2和SD-3。将Esa群体感应系统的感应元件引入底盘菌株SD-1中,并将pgi的天然启动子单独或和zwf的天然启动子一起替换为Esa群体感应系统的响应启动子PesaS,获得了菌株SD-4和SD-5。PesaS可以感应群体密度的变化,在细胞生长的稳定期动态下调其靶基因的表达。
菌株SD-2~5的摇瓶发酵情况如图4所示。菌株SD-2到SD-4的生长状况与SD-1类似,但SD-5在72 h后的OD562值约为57,显示出一定的生长受损,说明pgi和zwf的同时下调会影响细胞生长。从产量来看,发酵72 h后SD-2~5均能产生MI和SI,其中SD-4的总肌醇产量最高,为1.21 g/L,SD-2的SI产量最高,为0.87 g/L。144 h发酵结果趋势与72 h一致。结果表明,对G6P竞争途径通量的限制有利于MI和SI的从头合成。
2.3 G6P到MI合成途径的强化
IPS是MI生物合成中的关键限速酶[14]。为了进一步拉动MI和SI合成的通量,本研究通过过表达菌株内源的IPS编码基因ino1,增强G6P到2KMI的转化,促进MI的积累。将质粒p5-ino1电转入菌株SD-1到SD-5,获得了菌株SDI-1~SDI-5。
菌株SDI-1~5的摇瓶发酵情况如图5所示。与没有进行ino1过表达的SD-1~5菌株相比,过表达ino1后菌株生长均受到一定程度的抑制,72 h后的OD562值均不到61,但肌醇产量得到了提升。其中,菌株SDI-1的SI产量最高,达到了2.26 g/L,而菌株SDI-2的肌醇总量最高,达到了2.49 g/L。结果表明ino1的过表达对菌株SI生产的积极作用,但强化G6P到MI的合成途径和下调G6P的竞争途径的组合(即菌株SDI-2~5)并没有产生更优的SI合成效果,单独强化G6P到MI合成途径(即菌株SDI-1)的SI产量更高。因此,强化G6P到MI合成途径的通量比限制G6P竞争途径的通量更利于SI的从头合成。
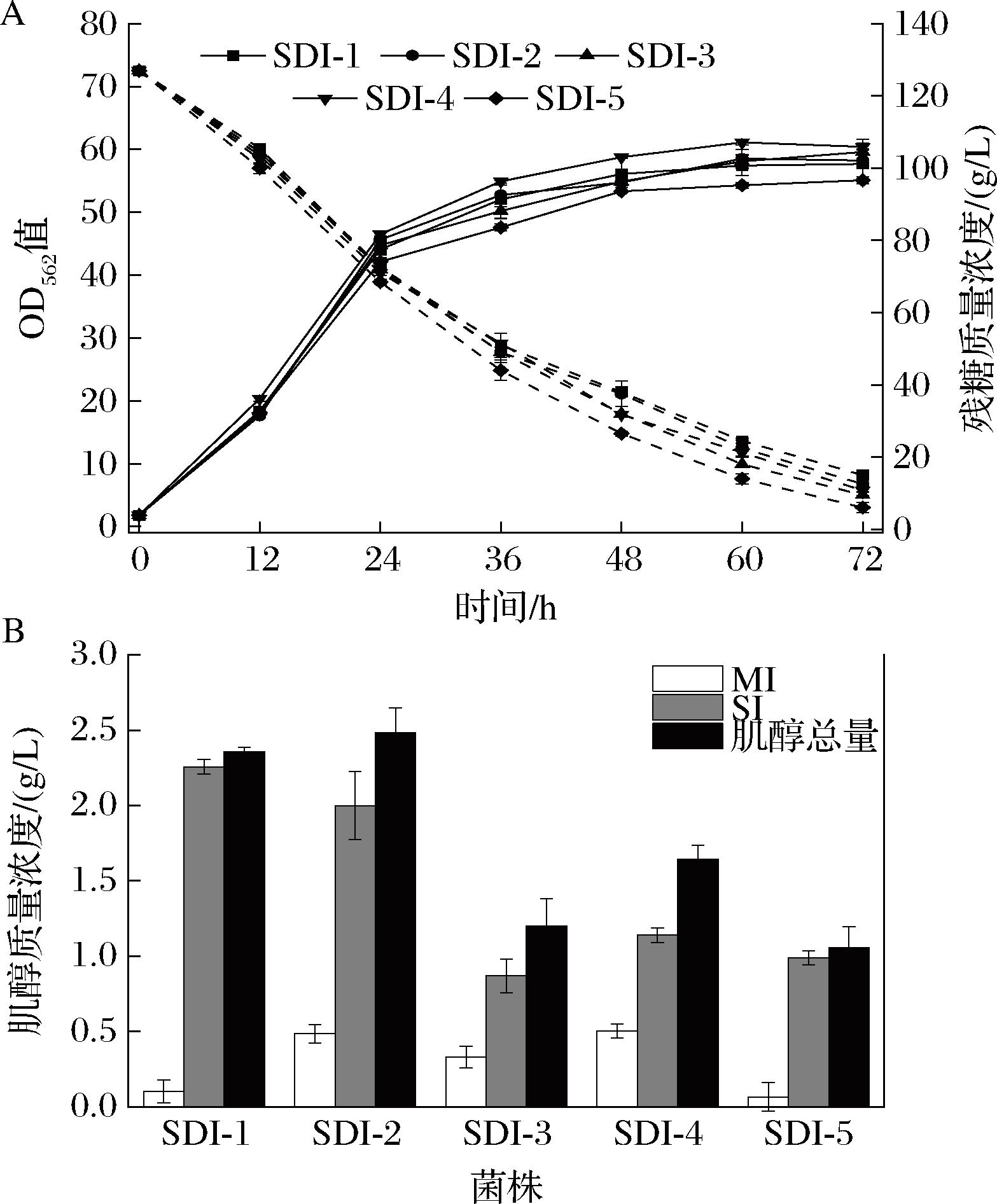
A-菌株SDI-1~5的OD562值和残糖;B-发酵72 h菌株SDI-1~5的肌醇产量
图5 菌株SDI-1~5的生长和肌醇生产
Fig.5 Growth and inositol production of strains SDI-1~5
2.4 前体G6P的富集
G6P作为MI和SI合成的关键前体,其在细胞中的积累量越高,流向MI和SI生产的通量也应该会越大。谷氨酸棒杆菌中葡萄糖的摄取和磷酸化主要由磷酸烯醇式丙酮酸-糖磷酸转移酶系统(phosphotransferase system,PTS)执行[15-16]。除了PTS系统外,肌肌醇渗透酶和葡萄糖激酶组成的偶联系统也参与葡萄糖的摄取和磷酸化,属于非PTS系统,但肌肌醇渗透酶和葡萄糖激酶表现出低表达水平以及对葡萄糖的低亲和力[16-17]。
本研究通过强化非PTS系统,将更多葡萄糖推入细胞,提高前体G6P的富集。选择了谷氨酸棒杆菌内源的肌肌醇渗透酶IolT1、IolT2和葡萄糖激酶PpgK,以及对葡萄糖具有高亲和力的枯草芽孢杆菌葡萄糖激酶GlcK[18],在质粒p5-ino1基础上进行组合共表达,构建的质粒p5-ino1-iolT1-ppgK、p5-ino1-iolT1-glcK、p5-ino1-iolT2-ppgK和p5-ino1-iolT2-glcK分别电转入菌株SD-1中,获得了菌株SDG-1到SDG-4。菌株SDG-1~4的摇瓶发酵情况如图6所示。
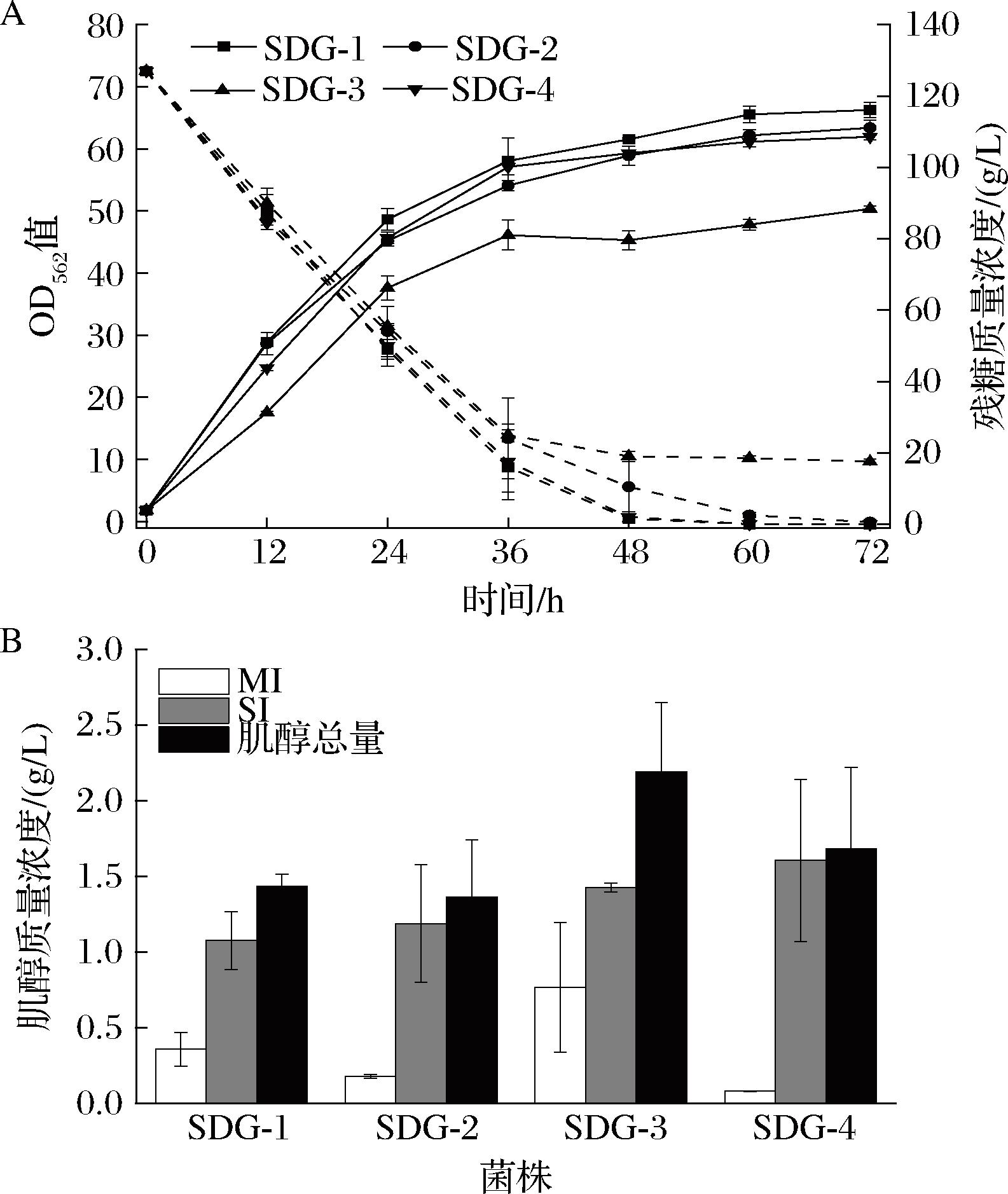
A-菌株SDG-1~4的OD562值和残糖;B-发酵72 h菌株SDG-1~4的肌醇产量
图6 菌株SDG-1~4的生长和肌醇生产
Fig.6 Growth and inositol production of strains SDG-1~4
与菌株SDI-1相比,菌株SDG-1、SDG-2和SDG-4的生长均得到了一定的恢复,剩余葡萄糖也随之降低,但SDG-3的生长被进一步抑制。然而,SDG-3反而获得了最高的肌醇总量,达到2.19 g/L,SDG-4获得了最高的SI产量,达到1.60 g/L,但均不如之前的最优菌株SDI-1的SI产量和肌醇总量。SI产量和生长结果表明,强化非PTS系统可以促进葡萄糖的摄取、增加葡萄糖的消耗,但葡萄糖消耗的增加似乎只有利于细胞生长,并没有将更多的G6P导向肌醇生产,肌醇合成可能还存在未知的阻碍。
2.5 辅因子NAD+的供应
IPS在将MI转换成2KMI的过程中,还需要NAD+作为反应的辅因子[19]。谷氨酸棒杆菌在进行有氧呼吸的过程中,电子传递链中NADH被氧化为NAD+。vgb编码的透明颤菌血红蛋白可以提高细胞对氧气的利用效率,加速电子传递链中NADH的氧化[20]。ndh编码的谷氨酸棒杆菌NADH脱氢酶也可以促进NADH向NAD+的转化,同时释放电子进入电子传递链[21]。因此,在质粒p5-ino1基础上构建了质粒p5-ino1-vgb和p5-ino1-ndh,分别电转入菌株SD-1中,获得了菌株SDN-1和SDN-2。
菌株SDN-1~2的摇瓶发酵情况如图7所示。与菌株SDI-1相比,菌株SDN-1和SDN-2的生长恢复了,且基本没有剩余葡萄糖。SDN-2的SI产量最高,为2.29 g/L,与SDI-1的SI产量(2.26 g/L)类似。SDN-1的肌醇总量最高,为2.79 g/L,高于SDI-1的肌醇总量(2.35 g/L),也高于前述总量最高的SDI-2的肌醇总量(2.49 g/L)。结果表明,辅因子NAD+的供应目前并不是阻碍SI生产的主要原因,但对肌醇总量的积累有微弱的促进作用。
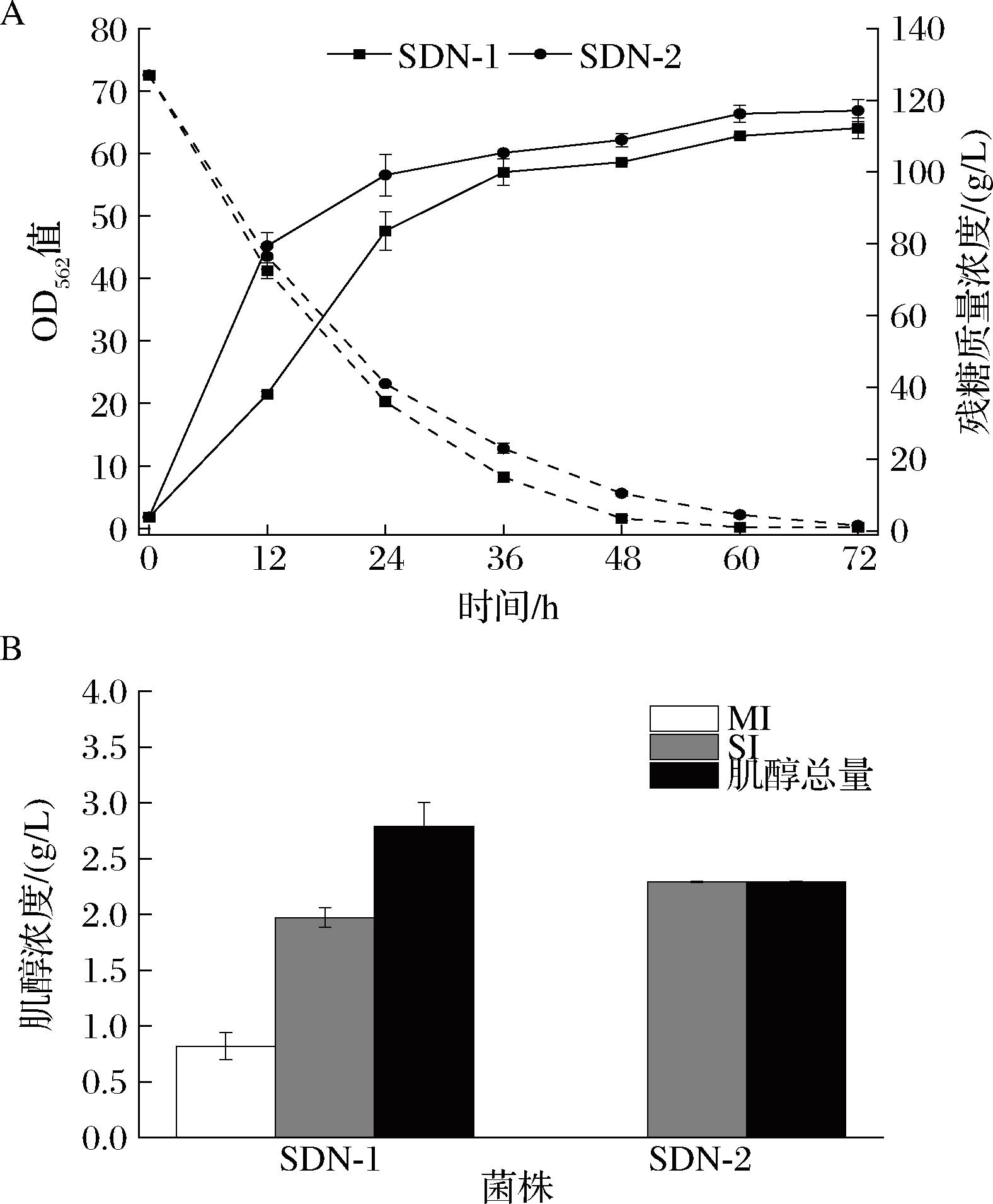
A-菌株SDN-1~2的OD562值和残糖;B-发酵72 h菌株SDN-1~2的肌醇产量
图7 菌株SDN-1~2的生长和肌醇生产
Fig.7 Growth and inositol production of strains SDN-1~2
3 结论
SI是治疗阿尔茨海默病的一种有前景的药物,在自然界中较为罕见。谷氨酸棒杆菌不仅可以以MI作为唯一碳源生长,还有以葡萄糖为底物经MI从头合成SI的所有基因,但并不积累SI。本研究敲除了谷氨酸棒杆菌SN01中肌醇降解相关基因,保留了参与MI到SI转化的iolG和iolW以及oxiD,同时在基因组上整合ScIPS和EcIMP,用强启动子PtacM代替天然PiolW启动子,获得了具有MI到SI转化能力的底盘菌株SD-1。随后通过替换启动子下调G6P竞争途径通量和过表达ino1强化G6P到MI合成途径通量,实现了SI的从头合成,但组合效果不如单独过表达ino1。之后尝试通过强化非PTS系统提高前体G6P的富集,以及通过强化电子传递链功能提高辅因子NAD+供应,发现具有一定的效果。本研究的最佳菌株SDN-2最终可以以葡萄糖为底物从头合成2.29 g/L SI,高于先前报道的枯草芽孢杆菌中2 g/L[9]和谷氨酸棒杆菌中1.8 g/L[10]的SI从头合成产量。虽然SI的产量离工业化生产尚有差距,但是本研究所探索的改造策略为SI的从头合成提供了一定的参考和进一步的研究思路。
[1] REYNOLDS T B.Strategies for acquiring the phospholipid metabolite inositol in pathogenic bacteria,fungi and protozoa:Making it and taking it[J].Microbiology,2009,155(Pt 5):1386-1396.
[2] SIRACUSA L,NAPOLI E,RUBERTO G.Novel chemical and biological insights of inositol derivatives in Mediterranean plants[J].Molecules,2022,27(5):1525.
[3] LI Y J,HAN P P,WANG J,et al.Production of myo-inositol:Recent advance and prospective[J].Biotechnology and Applied Biochemistry,2022,69(3):1101-1111.
[4] RAMP P,PFLEGER C,DITTRICH J,et al.Physiological,biochemical,and structural bioinformatic analysis of the multiple inositol dehydrogenases from Corynebacterium glutamicum[J].Microbiology Spectrum,2022,10(5).
[5] KANG D M,MICHON C,MORINAGA T,et al.Bacillus subtilis IolQ (DegA) is a transcriptional repressor of iolX encoding NAD+-dependent scyllo-inositol dehydrogenase[J].BMC Microbiology,2017,17(1):154.
[6] MORINAGA T,ASHIDA H,YOSHIDA K I.Identification of two scyllo-inositol dehydrogenases in Bacillus subtilis[J].Microbiology,2010,156(Pt 5):1538-1546.
[7] THOMAS M P,MILLS S J,POTTER B V L.The “other” inositols and their phosphates:Synthesis,biology,and medicine (with recent advances in myo-inositol chemistry)[J].Angewandte Chemie-International Edition,2016,55(5):1614-1650.
[8] TANAKA K,NATSUME A,ISHIKAWA S,et al.A new-generation of Bacillus subtilis cell factory for further elevated scyllo-inositol production[J].Microbial Cell Factories,2017,16(1):67.
[9] MICHON C,KANG C M,KARPENKO S,et al.A bacterial cell factory converting glucose into scyllo-inositol,a therapeutic agent for Alzheimer’s disease[J].Communications Biology,2020,3:93.
[10] RAMP P,LEHNERT A,MATAMOUROS S,et al.Metabolic engineering of Corynebacterium glutamicum for production of scyllo-inositol,a drug candidate against Alzheimer’s disease[J].Metabolic Engineering,2021,67:173-185.
[11] 纪国徽.代谢工程改造谷氨酸棒杆菌合成D-手性肌醇[D].无锡:江南大学,2024.JI G H.Metabolic engineering Corynebacterium glutamicum for D-chiro-inositol production[D].Wuxi:Jiangnan University,2024.
[12] JI G H,JIN X,SHI F.Metabolic engineering Corynebacterium glutamicum for D-chiro-inositol production[J].World Journal of Microbiology &Biotechnology,2024,40(5):154.
[13] HU C H,SHI F,CHEN R,et al.Rearrangement in the regulation of sigD gene expression promotes 4-hydroxyisoleucine production in Corynebacterium glutamicum[J].Systems Microbiology and Biomanufacturing,2025,5(1):276-287.
[14] YOU R,WANG L,SHI C R,et al.Efficient production of myo-inositol in Escherichia coli through metabolic engineering[J].Microbial Cell Factories,2020,19(1):109.
[15] RUAN H Z,YU H B,XU J Z.The glucose uptake systems in Corynebacterium glutamicum:A review[J].World Journal of Microbiology and Biotechnology,2020,36(9):126.
[16] XU J Z,RUAN H Z,YU H B,et al.Metabolic engineering of carbohydrate metabolism systems in Corynebacterium glutamicum for improving the efficiency of L-lysine production from mixed sugar[J].Microbial Cell Factories,2020,19(1):39.
[17] LINDNER S N,SEIBOLD G M,HENRICH A,et al.Phosphotransferase system-independent glucose utilization in Corynebacterium glutamicum by inositol permeases and glucokinases[J].Applied and Environmental Microbiology,2011,77(11):3571-3581.
[18] MESAK L R,MESAK F M,DAHL M K.Bacillus subtilis GlcK activity requires cysteines within a motif that discriminates microbial glucokinases into two lineages[J].BMC Microbiology,2004,4:6.
[19] MAJUMDER A L,CHATTERJEE A,GHOSH DASTIDAR K,et al.Diversification and evolution of L-myo-inositol 1-phosphate synthase[J].FEBS Letters,2003,553(1-2):3-10.
[20] TSAI P S,RAO G,BAILEY J E.Improvement of Escherichia coli microaerobic oxygen metabolism by Vitreoscilla hemoglobin:New insights from NAD(P)H fluorescence and culture redox potential[J].Biotechnology and Bioengineering,1995,47(3):347-354.
[21] CHEN C,CUI Z Z,ZHAO J T,et al.Improving diacetyl production in Corynebacterium glutamicum via modifying respiratory chain[J].Journal of Biotechnology,2021,332:20-28.