中国是全球最大的生猪生产国,根据国家统计局数据,2024年中国猪肉产量为5 706万t[1]。每年猪油总量可达到2 000万t左右[2]。猪油因饱和脂肪含量高、热量高而被诟病,限制了其在食品加工中的广泛应用。民间熬制猪油的风味深受消费者喜爱。另外,猪油是制备肉味香精的重要原料,其加热氧化产生的风味物质对肉味香精特征风味形成有重要贡献[3]。肉味香精在方便食品、速冻食品等食品中广泛应用。因此分析猪油风味对于研制猪油风味料具有重要意义。
食品风味分析一般先萃取富集样品的挥发性成分,再采用气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)、气相色谱-嗅闻(gas chromatography-olfactometry,GC-O)进行分析。徐永霞等[3]曾采用顶空固相微萃取(headspace solid phase micro-extraction,HS-SPME)/GC-MS分析猪脂肪控制氧化产物中挥发性风味物质。但HP-SPME用于萃取分析油脂的挥发性成分时往往效果并不理想,因为挥发性香气成分亲脂性强,易溶解在油脂中。溶剂辅助蒸发(solvent assistant flavor evaporation,SAFE)是一种先用溶剂萃取样品中风味物质,再用高真空蒸馏将其蒸出,具有风味物质萃取回收率高的优点。本课题组曾采用SAFE结合GC-MS、GC-O的方法分析了熬制牛油中挥发性香气成分,鉴定出2-甲基-3-呋喃硫醇、3-甲硫代丙醛、(E,E)-2,4-壬二烯醛、12-甲基十三醛、1-辛烯-3-酮等化合物。另外,也可通过SAFE装置直接高真空蒸馏富集分离食品的挥发性成分。本课题组前期采用SAFE装置直接蒸馏,再结合GC-MS、GC-O分析了氧化猪脂(精炼)香气成分,鉴定出1-辛烯-3-醇、己醛、(E)-2-辛烯醛、(E)-2-壬烯醛、(E,E)-2,4-癸二烯醛、戊醛等化合物。在风味分析时,GC-MS可用于鉴定挥发性化合物的结构,而GC-O则用于筛选对总体香气有贡献的气味活性化合物。GC-O检测方法包括强度法、频率法、稀释法。GC-O检测频率高,强度大,或稀释因子高的化合物,往往对总体香气有重要贡献[4-6]。例如,王蒙等[7]采用SAFE法提取及稀释法GC-O分析,从炖煮猪肉汤中鉴定出3-甲硫基丙醛、γ-癸内酯、(E,E)-2,4-癸二烯醛、1-辛烯-3-醇等重要香气物质。
本实验采用SAFE和高真空蒸馏2种方法萃取熬制猪油的挥发性组分,再结合GC-MS、GC-O鉴定香气物质。研究结果可为猪肉味香精的制备及猪油的开发利用提供参考。
1 材料与方法
1.1 材料与试剂
猪油(大约克白猪,河北),取猪背部的皮下脂肪使用,北京物美超市;异辛烷、氢氧化钠、甲醇、硫酸氢钠、石油醚、乙醇、盐酸、无水硫酸钠(均为分析纯)、C5~C29正构烷烃(色谱纯),国药试剂北京有限公司;甲醇(分析纯),迪马科技;9-芴甲基氯甲酸酯、邻苯二甲醛,美国Agilent公司;氨基酸标准品(色谱纯),西格玛公司;脂肪酸甲酯标准品(色谱纯)、内标化合物邻二氯苯(99%),北京百灵威科技有限公司。
用于定性定量分析风味化合物的标准品,包括:丁醛(≥99%)、3-甲基丁醛(≥99%)、2-甲基丁醛(≥99%)、戊醛(≥99%)、己醛(≥99%)、庚醛(≥99%)、(E,E)-2,6-壬二烯醛(≥99%)、(E)-2-己烯醛(≥95%)、辛醛(≥95%)、(E)-2-庚烯醛(≥99%)、壬醛(≥99%)、(E)-2-辛烯醛(≥99%)、(E,E)-2,4-庚二烯醛(≥99%)、癸醛(≥99%)、(E)-2-壬烯醛(≥99%)、苯甲醛(≥95%)、(E)-2-癸烯醛(≥99%)、(E,E)-2,4-辛二烯醛(≥99%)、苯乙醛(≥95%)、(E,E)-2,4-壬二烯醛(≥99%)、(E)-2-十一烯醛(≥99%)、(E,E)-2,4-癸二烯醛(≥99%)、(E)-2-十二烯醛(≥99%)、1-辛烯-3-酮(≥99%)、2-十一酮(≥99%)、1-辛烯-3-醇(98%))、1-庚醇(≥99%)、2-辛烯-1-醇(≥99%)、1-辛醇(≥99%)、苯乙醇(≥99%)、丁酸(≥99%)、γ-辛内酯(≥99%),4-羟基-2,5-二甲基-2(3H)-呋喃酮(≥99%)、甲硫醇(≥99%)、二甲基二硫(≥99%)、二乙基二硫(≥99%)、4-甲基噻唑(≥99%)、4,5-二甲基噻唑(≥99%)、2-甲基-3-呋喃硫醇(≥99%)、糠硫醇(≥99%)、3-甲硫基丙醛(≥99%)、2,5-二甲基吡嗪(≥99%)、2,3-二甲基吡嗪(≥99%)、2-乙基-5-甲基吡嗪(≥99%)、三甲基吡嗪(≥99%)、2,5-二甲基-3-乙基吡嗪(≥99%)、吲哚(≥99%)、2-戊基呋喃(≥99%)、糠醛(≥99%)、对甲酚(≥99%)、4-乙基苯酚(≥99%),北京百灵威科技有限公司。
1.2 仪器与设备
C21-SDHCB8E30电磁炉、FC30E炒锅,浙江苏泊尔股份有限公司;N-EVAP-12干浴氮吹仪,美国Organomation Associates公司;KT-36B循环冷却旋转蒸发仪,北京一恒仪器科技有限公司;ALPHA2-4LSC冷冻干燥机,德国Christ公司;7890A-5975C GC-MS、7890A GC(配有FID检测器和DATU2000气味测量仪)、LC1200 HPLC,美国Agilent公司;DATU2000嗅闻仪,美国DATU Inc公司;DF2101S集热式恒温加热磁力搅拌器,河南省予华仪器有限公司;MS205DU电子分析天平,瑞士METTLER TOLEDO公司。
1.3 实验方法
1.3.1 猪脂肪氨基酸分析
氨基酸提取:准确称取0.5 g猪脂肪,加入10 mL V石油醚∶V乙醇=1∶1,超声30 min萃取,如此超声萃取3次。萃取后的残渣加入3 mL 6 mol/L盐酸,110 ℃加热水解24 h,所得水解液旋转蒸发除盐酸,再采用C18固相萃取柱(200 mg/3 mL,40 μm)处理,收集流出液,冻干,去离子水定容至50 mL,备用。
氨基酸衍生及高效液相色谱分析,参考王天泽等[8]的方法。衍生剂为9-芴甲基氯甲酸酯和邻苯二甲醛,衍生后样品采用Poroshell HPH-C18分析柱(100 mm×4.6 mm,5.0 μm)分析,平行3份样品。
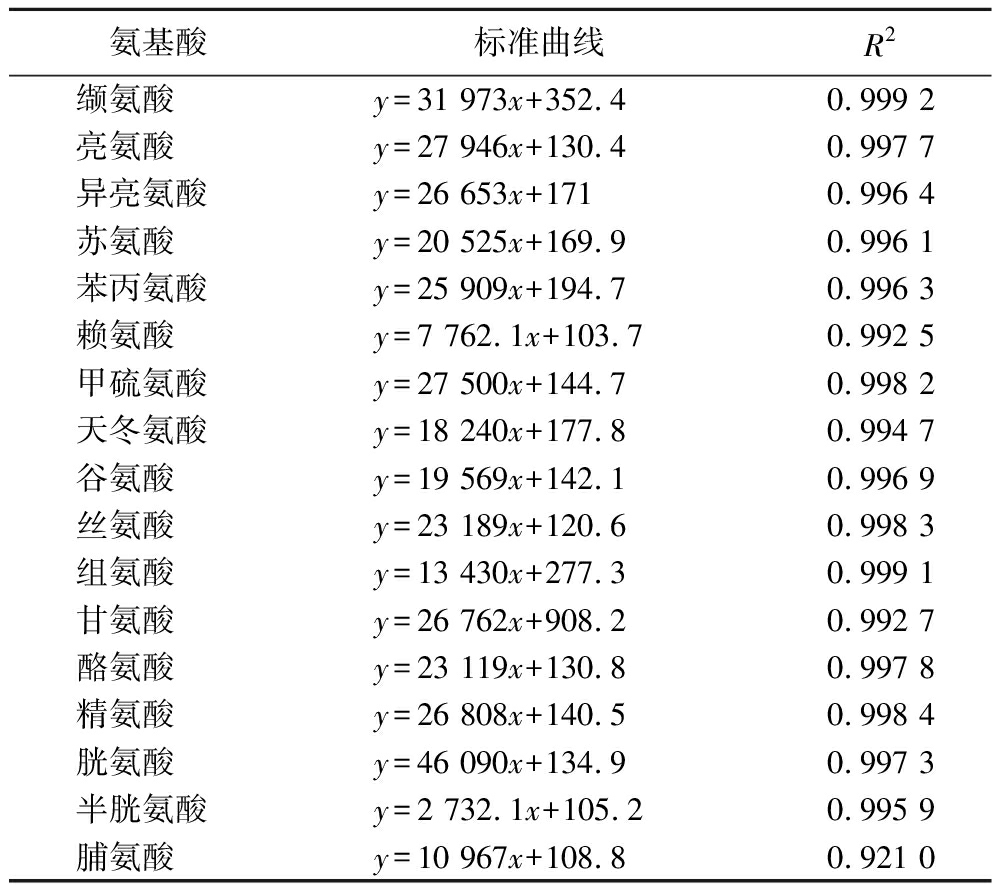
根据每个氨基酸的浓度和HPLC图对应峰面积建立标准曲线,如表1所示,回归系数几乎均达到0.99以上。
表1 氨基酸分析标准曲线
Table 1 Calibration curves for amino acid analysis
氨基酸标准曲线R2缬氨酸y=31 973x+352.40.999 2亮氨酸y=27 946x+130.40.997 7异亮氨酸y=26 653x+1710.996 4苏氨酸y=20 525x+169.90.996 1苯丙氨酸y=25 909x+194.70.996 3赖氨酸y=7 762.1x+103.70.992 5甲硫氨酸y=27 500x+144.70.998 2天冬氨酸y=18 240x+177.80.994 7谷氨酸y=19 569x+142.10.996 9丝氨酸y=23 189x+120.60.998 3组氨酸y=13 430x+277.30.999 1甘氨酸y=26 762x+908.20.992 7酪氨酸y=23 119x+130.80.997 8精氨酸y=26 808x+140.50.998 4胱氨酸y=46 090x+134.90.997 3半胱氨酸y=2 732.1x+105.20.995 9脯氨酸y=10 967x+108.80.921 0
注:x,浓度(mmol/L);y,峰面积。
1.3.2 熬油方法
猪脂肪(500.0±0.1) g,切成1 cm3的小块,放入铁炒锅(口径32 cm,配有锅盖,锅内含温度计),电磁炉加热,不断搅拌,加热温度(150±2) ℃,加热时间20 min。放置室温,待分析。
1.3.3 脂肪酸分析
脂肪酸衍生参照GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》。准确称取熬制的猪油60 mg加入4 mL异辛烷中,加2 mL内标十七烷酸甲酯溶液(溶于异辛烷,5 g/L)、200 μL 2 mol/L氢氧化钾-甲醇溶液,猛烈振摇30 s后静置。取上层溶液加入1 g无水硫酸氢钠,过滤,参照文献[9]进行GC-MS分析。
采用脂肪酸甲酯标品,对脂肪酸进行鉴定。脂肪酸甲酯含量先按如下公式(1)计算,再根据GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》中脂肪酸甲酯和脂肪酸之间的转化系数计算各脂肪酸含量:
(1)
式中:xi,脂肪酸含量,mg/g;Ai,脂肪酸甲酯峰面积;As,十七烷酸甲酯的峰面积;Vs,内标十七烷酸甲酯的体积,mL;Cs,十七烷酸甲酯的质量浓度,g/L;m,猪油质量,mg;F,代表脂肪酸甲酯和脂肪酸之间的转换系数,参照GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》。
1.3.4 高真空蒸馏
对熬制的猪油500 g直接采用SAFE装置进行高真空蒸馏,恒温水浴50 ℃,循环水温度50 ℃,系统压力小于10-5 Pa,收集瓶中加入二氯甲烷收集馏出物,蒸馏结束后,氮吹浓缩到0.3 mL,-30 ℃保存,待GC-MS和GC-O分析。
1.3.5 SAFE
将熬制的猪油500 g用二氯甲烷溶剂(500 mL)萃取,重复萃取3次,所得萃取溶液合并,采用SAFE装置蒸馏,恒温水浴30 ℃,循环水温度50 ℃,系统压力小于10-5 Pa。收集馏出液,无水硫酸钠干燥,韦氏浓缩柱(50 cm×1 cm)蒸馏浓缩至5 mL,氮吹至0.3 mL,-30 ℃保存,待GC-MS和GC-O分析。
1.3.6 GC-MS分析
GC条件:DB-WAX(30 m×0.25 mm×0.25 μm)色谱柱,柱温40 ℃,4.5 ℃/min升至180 ℃,然后7 ℃/min升至230 ℃。载气为He,流速1 mL/min。进样口温度250 ℃;分流比20∶1,进样1 μL。
MS条件:电子轰击离子源,能量70 eV;离子源温度230 ℃;四级杆温度150 ℃;全扫描模式,质量扫描范围50~450 amu;辅助加热线温度230 ℃,溶剂延迟4 min。
在相同气-质条件下进样C5~C29正构烷烃,按公式(2)计算保留指数(retention index,RI):
(2)
式中:tn,碳数为n的正构烷烃的保留时间;tn+1,碳数为n+1的正构烷烃的保留时间;ti,出峰在n和n+1的正构烷间的i化合物的保留时间。
化合物采用检索质谱库、核对RI、进样标品、以及结合如下的GC-O嗅闻的气味进行鉴定。
1.3.7 化合物定量分析
除了下一段所涉及化合物外,其余均采用内标法半定量,将10 μL 1,2-邻二氯苯(溶于二氯甲烷,0.6 μg/μL)作为标准物加入到浓缩液中。按照公式(3)计算化合物含量:
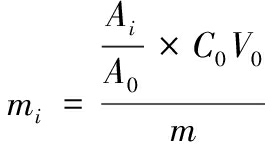
(3)
式中:mi,化合物在样品中的含量,ng/g猪油;Ai,化合物的峰面积;A0,内标的峰面积;C0,内标的浓度,V0,所加内标的体积,mL;m,样品的质量,g。
由于GC-MS全扫描未检测到2-乙基-3,5-二甲基吡嗪、2-甲基-3-呋喃硫醇、3-甲硫基丙醛、4-羟基-2,5-二甲基-3(2H)-呋喃酮、4-乙基苯酚,因此这5种化合物采用MS的SIM扫描模式分析,建立标准曲线进行定量。它们扫描的离子分别为135、114、104、128、122。定量曲线为:2-乙基-3,5-二甲基吡嗪,y=4.149x-0.140(R2=0.997 6,质量浓度范围1.0~20 mg/L);2-甲基-3-呋喃硫醇,y=109.56x+0.012(R2=0.999 8,质量浓度范围40~250 mg/L);3-甲硫基丙醛,y=1.511x-0.919(R2=0.990 8,质量浓度范围50~250 mg/L);4-羟基-2,5-二甲基-3(2H)-呋喃酮,y=0.158x-0.100(R2=0.995 8,质量浓度范围1.0~50 mg/L);4-乙基苯酚,y=1.515x-0.888(R2=0.989 5,质量浓度范围1.0~50 mg/L)。其中,x:化合物的峰面积与内标1,2-邻二氯苯的峰面积比值,y:化合物在浓缩液中的含量。化合物在样品中的含量![]()
1.3.8 GC-O分析
毛细管柱为DB-WAX(30 m×0.25 mm×0.25 μm),起始柱温40 ℃,5 ℃/min升至230 ℃;载气为N2(纯度为99.999%),流速1 mL/min,进样口250 ℃,不分流模式,进样1 μL。气味测量仪的空气流速60 mL/min,加湿器温度70 ℃。
挑选3名训练有素的评价员,进行强度法嗅闻,记录嗅闻的每种香气特征与强度。香气强度越大得分越高,满分5分。以3名评价员的均值为结果。
1.4 数据处理
实验结果表示为“平均值±标准差”(n=3)。所有表格使用Microsoft excel 2019软件绘制。采用Origin Pro 2025绘制Pearson相关性分析热图。采用SIMCA14.1软件进行正交偏最小二乘法-判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)。通过软件SPSS 24.0进行单因素方差分析(analysis of variance,ANOVA),P<0.05判定为差异显著。
2 结果与分析
2.1 氨基酸组成分析结果
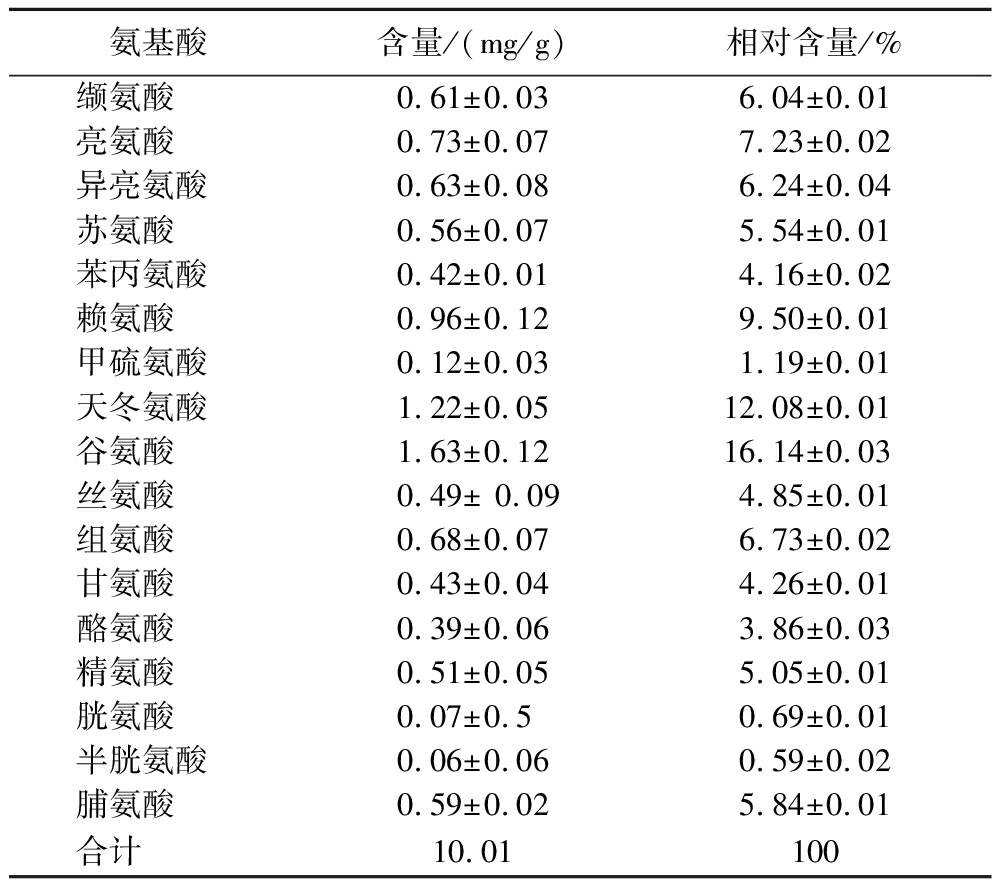
猪脂肪中含有少量肌肉组织[10],肌肉组织中所含的氨基酸加热时可参与美拉德反应及发生Strecker降解反应产生挥发性风味化合物[11]。例如,半胱氨酸与还原糖发生美拉德反应可生成2-甲硫基-3-呋喃硫醇[7]。由表2可知,共检测出17种氨基酸,含量最高的为谷氨酸,其次为天冬氨酸、赖氨酸。王蒙等[7]分析大约克猪肉的主要氨基酸也为谷氨酸、天冬氨酸、赖氨酸。赵健等[12]分析黑猪肉氨基酸组成,谷氨酸为含量最高的氨基酸。
表2 猪脂肪中的氨基酸组成
Table 2 Amino acid composition in the pork fat
氨基酸含量/(mg/g)相对含量/%缬氨酸0.61±0.036.04±0.01亮氨酸0.73±0.077.23±0.02异亮氨酸0.63±0.086.24±0.04苏氨酸0.56±0.075.54±0.01苯丙氨酸0.42±0.014.16±0.02赖氨酸0.96±0.129.50±0.01甲硫氨酸0.12±0.031.19±0.01天冬氨酸1.22±0.0512.08±0.01谷氨酸1.63±0.1216.14±0.03丝氨酸0.49± 0.094.85±0.01组氨酸0.68±0.076.73±0.02甘氨酸0.43±0.044.26±0.01酪氨酸0.39±0.063.86±0.03精氨酸0.51±0.055.05±0.01胱氨酸0.07±0.50.69±0.01半胱氨酸0.06±0.060.59±0.02脯氨酸0.59±0.025.84±0.01合计10.01100
注:相对含量/%=(每种氨基酸含量/总含量)×100。
2.2 脂肪酸组成分析结果
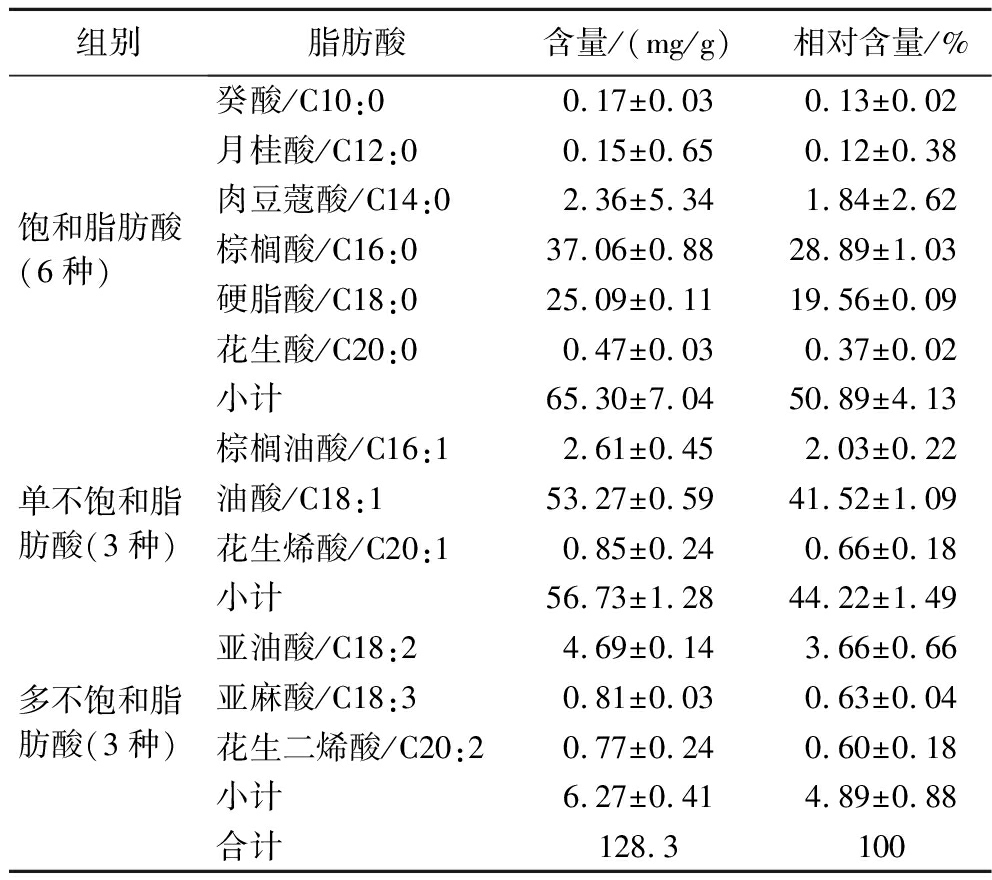
由表3可知,猪油中共检测出12种脂肪酸。饱和脂肪酸6种,单不饱和脂肪酸3种,多不饱和脂肪酸3种,含量高的脂肪酸有棕榈酸、硬脂酸、油酸、亚油酸。这与LIAN等[13]分析猪背部皮下脂肪和LI等[14]分析猪腹部皮下脂肪中脂肪酸组成结果一致。
表3 猪油脂肪酸组成及含量
Table 3 Fatty acid composition and content of the lard
组别脂肪酸含量/(mg/g)相对含量/%饱和脂肪酸(6种)癸酸/C10:00.17±0.030.13±0.02月桂酸/C12:00.15±0.650.12±0.38肉豆蔻酸/C14:02.36±5.341.84±2.62棕榈酸/C16:037.06±0.8828.89±1.03硬脂酸/C18:025.09±0.1119.56±0.09花生酸/C20:00.47±0.030.37±0.02小计65.30±7.0450.89±4.13单不饱和脂肪酸(3种)棕榈油酸/C16:12.61±0.452.03±0.22油酸/C18:153.27±0.5941.52±1.09花生烯酸/C20:10.85±0.240.66±0.18小计56.73±1.2844.22±1.49多不饱和脂肪酸(3种)亚油酸/C18:24.69±0.143.66±0.66亚麻酸/C18:30.81±0.030.63±0.04花生二烯酸/C20:20.77±0.240.60±0.18小计6.27±0.414.89±0.88合计128.3100
注:相对含量/%=(每种脂肪酸含量/总含量)×100。
2.3 挥发性风味化合物分析结果
2.3.1 GC-MS分析结果
脂肪加热氧化能够产生令人喜爱的风味[15],如BI等[16]发现随着蒸煮时间的延长,猪脂肪的香味更为强烈。电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043086,下同)所示为猪油分别采用SAFE和高真空蒸馏所得提取物的气-质联机分析结果。2种检测方式共鉴定出85种化合物,包括醛类19种、酮类7种、醇类13种、酸类17种、内酯类7种、含硫化合物7种、含氮杂环化合物8种、含氧杂环化合物2种及其他类5种。检测出的醛类、醇类、酸类化合物数量较多,这与赵健等[12]分析黑猪肉香气成分结果相似。醛类、酮类、醇类、酸类化合物来源于熬制过程中脂肪的水解和氧化反应[17]。例如,壬醛可来源于油酸的氧化降解[5],己醛可来源于亚油酸的氧化降解[18]。而检测到的含硫化合物、含氧杂环化合物、含氮杂环化合物则来源于美拉德反应,例如1-脱氧戊糖与乙醛和H2S反应,经脱水和芳构化可生成2,5-二甲基噻吩[19]。糠醇来源于美拉德反应中还原糖的降解[12]。吡嗪类化合物如2,5-二甲基吡嗪、三甲基吡嗪、甲基吡嗪、2,3-二甲基吡嗪可由2分子α-氨基酮缩合反应产生[20],尤其在天冬氨酸和谷氨酸含量高时更易生成吡嗪[21]。其他类化合物中的柠檬烯、苯酚、对甲酚、麦芽酚可能来源于喂养的饲料[17,19]。2种方式中含量最高的均为酸类,分别为3 566.21、759.13 ng/g,质量分数占44.34%、70.09%,这与CHANG等[22]分析猪肉汤中香气成分结果一致。其中,采用SAFE共鉴定出78种化合物,含量相对较高的化合物(>200 ng/g)有己醛、(E)-2-庚烯醛、壬醛、乙偶姻、2,3-丁二醇、乙酸、3-甲基戊酸、癸酸、十二酸、十四酸、十六酸、2,3-二羟基噻吩。采用高真空蒸馏方法共鉴定出47种化合物,含量相对较高的化合物(>40 ng/g)有辛醛、2,3-丁二醇、乙酸、丁酸。有39种化合物在2种提取方法中共同被鉴定出,包括辛醛、2,3-丁二醇、乙酸等。史亚静等[23]采用吹扫捕集/GC-MS分析猪油风味物质,检测到较高含量的(E)-2-庚烯醛、乙酸、壬醛。LI等[14]采用SPME/GC-MS分析猪油检测到的高含量化合物为己醛、(E)-2-庚烯醛、壬醛等。
相比之下,采用SAFE方法检测出的化合物种类和含量均明显大于高真空蒸馏方法,表明分析油溶性物料中风味物质时,采用溶剂萃取→高真空蒸馏的SAFE方法具有优势。为了更直观地观察2种萃取方法的检测结果差别,以检测出的化合物作为因变量,2种提取方式作为自变量进行OPLS-DA,自变量拟合指数(R2X)为0.928,因变量拟合指数(R2Y)为0.981,模型预测指数(Q2)为0.999,R2和Q2都超过0.5,表示模型拟合结果可接受。如图1-a所示,2种提取方法的挥发性组成明显地被区分,表明采用这2种萃取方法的萃取结果差异较大。进一步地通过变量重要性投影(variable importance projection,VIP)分析,筛选出了22个代表差异性的标志物(VIP>1),如图1-b所示,按VIP值由高到低顺序分别为:十六酸、(E)-2-庚烯醛、2,5-二甲基吡嗪、γ-辛内酯、己醛、2,3-二羟基噻吩、壬醛、十二酸、(E)-2-辛烯醛、γ-戊内酯、2,3-丁二醇、十四酸、2(5H)-呋喃酮、乙偶姻、3-甲基戊酸、2-十三酮、庚醛、癸酸、5-甲基噻唑、苯甲酸、(E,E)-2,4-庚二烯醛、三甲基吡嗪。这些化合物中包括了醛类、酮类、酸类、醇类、吡嗪等各类化合物,其在SAFE方法中检测出的含量均高于高真空蒸馏方法,甚至有的在高真空蒸馏方法未检测到,表明采用SAFE方法萃取分析更佳。
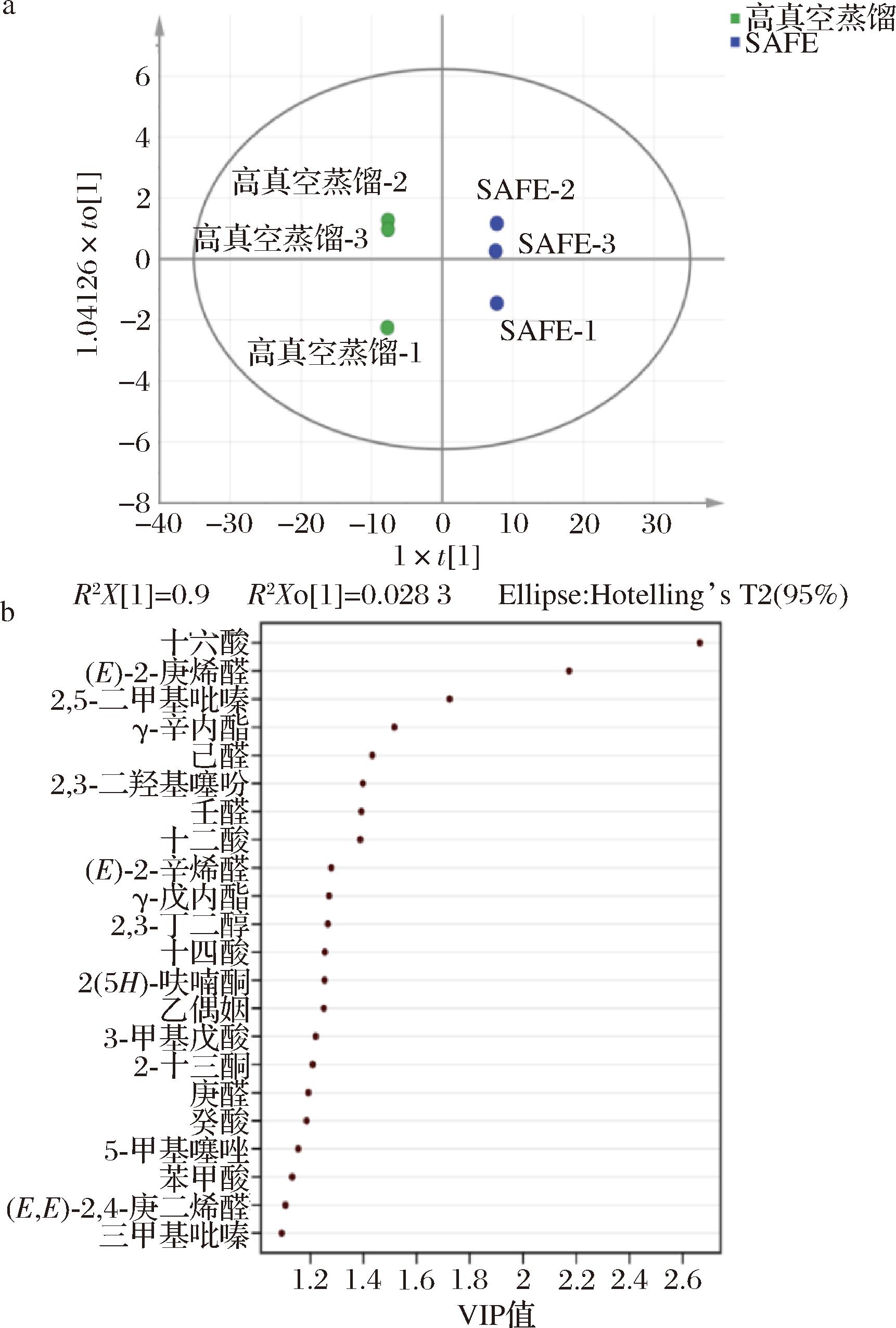
a-得分图;b-VIP图
图1 采用OPLS-DA比较采用2种方法萃取分析的熬猪油挥发性风味物质
Fig.1 OPLS-DA analysis of volatile flavor compounds in the lard using two extraction methods
2.3.2 GC-O分析结果
由附表2可知,采用2种提取方式GC-O共鉴定出53种气味活性化合物,包括醛类24种、酮类2种、醇类5种、酸类1种、内酯类2种、含硫化合物8种、含氮杂环化合物7种、含氧杂环化合物2种以及其他类2种。GC-O分析检测到的气味类型包括青香、油脂香、蘑菇香、甜香、烤香等,以青香、油脂香、烤香描述词出现的频率高。其中,采用SAFE/GC-O方法共检测出41种气味活性化合物,气味强度相对较高(≥4分)的化合物共17种,这些化合物对猪油风味的贡献大。包括a)具有青香、脂肪香香气特征的己醛、庚醛、辛醛、(E)-2-庚烯醛、(E)-2-辛烯醛、(E,E)-2,4-庚二烯醛、(E)-2-壬烯醛、苯甲醛、(E)-2-癸烯醛、(E,E)-2,4-壬二烯醛、(E)-2-十二烯醛、1-辛烯-3-醇、4-乙基苯酚;b)可构成甜香香气特征的2-戊基呋喃;c)可构成肉香、烤香香气特征的2-甲基-3-呋喃硫醇、3-甲硫基丙醛、3,5-二甲基-2-乙基吡嗪。高真空蒸馏/GC-O检测到的气味活性化合物同样有41种,与气质检测结果类似,这些化合物的GC-O分析气味强度均较低,这与高真空蒸馏的萃取含量低有关。其中,气味强度相对较高(≥2分)的化合物有16种,这些化合物对猪油风味的贡献也较大,体现在3方面:a)具有青香、油脂香香气特征的戊醛、己醛、(E,E)-2,6-壬二烯醛、(E)-2-己烯醛、辛醛、(E)-2-辛烯醛、癸醛、(E)-2-壬烯醛、(E)-2-十一烯醛、(E)-2-十二烯醛;b)可构成甜香、奶香香气特征的苯乙醛、3-甲基丁醛、γ-辛内酯、4-羟基-2,5-二甲基-3(2H)-呋喃酮;c)可构成烤香香气特征的2,3-二甲基吡嗪、对甲酚。2种萃取方式中均检测到己醛、(E)-2-辛烯醛、(E)-2-壬烯醛、(E)-2-十二烯醛的气味强度较高。猪油没有特征香气物质,以上分析表明,构成熬猪油的香气包括了油脂香、青香、奶香、肉香、烤香的系列化合物。LI等[14]采用芳香物萃取稀释分析/GC-O分析猪脂肪中的香气成分,检测到(E,E)-2,4-庚二烯醛、(E)-2-壬烯醛和4-羟基-2,5-二甲基-3(2H)-呋喃酮有较高的稀释因子。WANG等[24]采用SAFE/GC-O的提取方式检测猪肉汤中的香气物质,己醛、辛醛、(E,E)-2,4-壬二烯醛具有较高的稀释因子。值得注意的是,高真空蒸馏/GC-O检测到的一些沸点低的气味活性化合物(如丁醛),而SAFE/GC-O方法未检测到,可能与这些成分在SAFE的萃取、浓缩步骤中挥发损失有关。因此,本文采用的高真空蒸馏方法与SAFE法有一定的互补性。上述的气味活性化合物中,苯乙醛、3-甲基丁醛和3-甲硫基丙醛可来源于所检测到的苯丙氨酸、亮氨酸、甲硫氨酸的Strecker降解[19],γ-辛内酯可来源于γ-羟基脂肪酸的环化脱水[18],4-羟基-2,5-二甲基-3(2H)-呋喃酮可来源于美拉德反应中1-脱氧葡萄糖的环化[25],2-戊基呋喃可由亚油酸氧化降解产生[26]。
针对上述2种方法中嗅闻气味强度较大的化合物,进一步计算气味活性值(odor activity value,OAV),结果如表5所示。可知采用SAFE法检测到的OAV≥1的化合物有25种,包括庚醛、(E,E)-2,4-庚二烯醛、(E)-2-壬烯醛、(E)-2-十二烯醛、γ-辛内酯、4-羟基-2,5-二甲基-3(2H)-呋喃酮、2-甲基-3-呋喃硫醇、3-甲硫基丙醛、3,5-二甲基-2-乙基吡嗪、2-戊基呋喃等,这些化合物被认为是猪油香味的关键化合物。相比之下,高真空蒸馏检测到的OAV≥1的化合物有13种,均被包括在SAFE法检测到的化合物中,而高真空蒸馏/GC-O分析检测到的一些低沸点化合物大部分不在其中,表明其对猪油总体风味的贡献相对较小,主要对猪油风味有修饰作用。
2.3.3 Pearson相关性分析
脂肪降解可生成大量醛类、酮类、呋喃类、醇类、酸类和内酯类等化合物[25,28]。据报道,油酸、亚油酸是动物肉加热氧化降解产生风味物质的主要脂肪酸[29-30]。基于SAFE/GC-MS检测的化合物,采用Pearson分析了猪油中的脂质氧化挥发性风味物质与其脂肪酸组成的相关性。图2为根据相关系数绘制的热图,红色越深,表示相关性越大。在加热条件下,脂肪酸的氧化反应为自由基反应机制,饱和脂肪酸和不饱和脂肪酸均可发生氧化降解反应产生挥发性风味物质[14,19],且两者可能还存在复杂的交互作用。由图2可知,因为不饱和脂肪酸的氧化速率更快[5],饱和脂肪酸对应的红色区域远少于不饱和脂肪酸,即生成的挥发性风味物质主要与不饱和脂肪酸的氧化降解反应有关[14,31]。对于饱和脂肪酸,呈极强正相关(相关系数≥0.9)的为戊醛、(E)-2-庚烯醛、(E)-2-辛烯醛、丁酸、辛酸、十四酸、十六酸与棕榈酸;庚醛、辛醛、庚酸、5-丙基-二氢-2(3H)-呋喃酮与硬脂酸。对于不饱和脂肪酸,呈极强正相关(相关系数≥0.9)的包括(E)-2-己烯醛、(E,E)-2,4-壬二烯醛、(E)-2-十一烯醛、2-十五酮、2-戊醇、1-戊烯-3-醇、壬酸、5-乙酰基-二氢-2(3H)-呋喃酮与油酸;(E)-2-己烯醛、壬醛、(E,E)-2,4-壬二烯醛、(E)-2-十一烯醛、(E,E)-2,4-癸二烯醛、2-十三酮、2-十五酮、2-戊醇、1-戊烯-3-醇、2-己醇、十二酸、5-乙酰基-二氢-2(3H)-呋喃酮、γ-辛内酯与花生烯酸;(E)-2-癸烯醛、2-壬酮、2-十一酮、1-辛醇、2-癸烯-1-醇、乙酸与亚油酸。(E)-2-己烯醛、(E,E)-2,4-壬二烯醛、(E)-2-十一烯醛、2-十五酮、2-戊醇、1-戊烯-3-醇、壬酸、5-乙酰基-二氢-2(3H)-呋喃酮与亚麻酸;(E)-2-己烯醛、壬醛、(E,E)-2,4-壬二烯醛、(E)-2-十一烯醛、(E,E)-2,4-癸二烯醛、2-十三酮、2-十五酮、2-戊醇、1-戊烯-3-醇、2-己醇、十二酸、5-乙酰基-二氢-2(3H)-呋喃酮、γ-辛内酯与花生二烯酸。总之,以上分析表明不饱和脂肪酸氧化降解生成的挥发性风味物质远多于饱和脂肪酸氧化降解生成的挥发性风味物质。
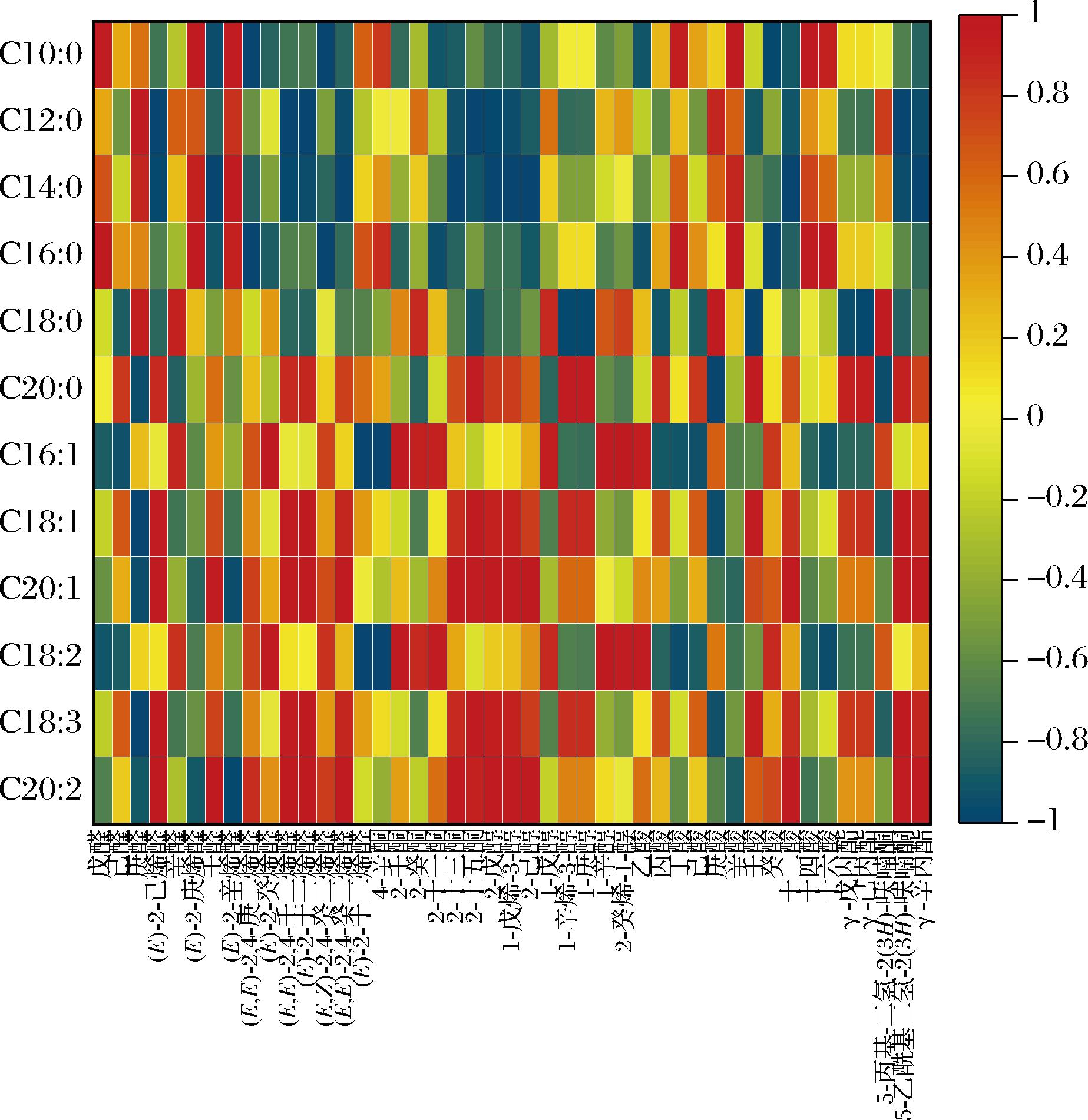
图2 脂肪酸与脂质氧化降解挥发性风味化合物相关性分析热图
Fig.2 Heat map of Pearson correlation analysis coefficients between fatty acids and the volatile flavor compounds derived from lpid oxidative degradation
3 结论
猪脂肪中含量最高氨基酸为谷氨酸、天冬氨酸、赖氨酸。猪油主要脂肪酸为棕榈酸、硬脂酸、油酸、亚油酸。采用SAFE/GC-MS和高真空/GC-MS从猪油中共检测到85种挥发性化合物。SAFE法检测出挥发性化合物的个数和含量几乎都高于高真空蒸馏法,OPLS-DA结果显示,尤其22种差异大的挥发性化合物在SAFE法中几乎均具有更高的含量。但采用高真空蒸馏法可检测到一些低沸点的挥发性化合物。采用2种萃取方式结合GC-O分析检测到猪油中53种香气活性化合物,结合计算OAV确定了25种关键香气化合物,包括2-甲基-3-呋喃硫醇、3-甲硫基丙醛、3,5-二甲基-2-乙基吡嗪、4-羟基-2,5-二甲基-3(2H)-呋喃酮、己醛、辛醛、(E)-2-辛烯醛、(E)-2-壬烯醛、(E)-2-十二烯醛、1-辛烯-3-醇等。Pearson相关性分析显示,猪油中的油酸、亚油酸、亚麻酸、花生烯酸、花生二烯酸是产生风味化合物的主要脂肪酸。
[1] 国家统计局.中华人民共和国2024年国民经济和社会发展统计公报[EB/OL].(2025-02-28)[2025-04-17].https://www.stats.gov.cn/sj/zxfb/202502/t20250228_1958817.html.National Bureau of Statistics.Statistical Communiqué of the People’s Republic of China on the 2024 National Economic and Social Development[EB/OL].(2025-02-28)[2025-04-17].https://www.stats.gov.cn/sj/zxfb/202502/t20250228_1958817.html.
[2] 朱巍,刘成国.猪油油脂产品开发利用研究进展[J].肉类研究,2016,30(2):40-44.ZHU W,LIU C G.Progress in development and utilization of lard products[J].Meat Research,2016,30(2):40-44.
[3] 徐永霞,张若洁,徐竞一,等.猪脂肪控制氧化及挥发性氧化产物研究[J].食品科学,2010,31(21):76-80.XU Y X,ZHANG R J,XU J Y,et al.Optimization of conditions for controlled oxidation of lard and analysis of volatile oxidation products[J].Food Science,2010,31(21):76-80.
[4] SHAKOOR A,PEI Z Y,AL-DALALI S,et al.Unveiling improval changes in fried chicken flavor by glucose-curing treatment based on molecular sensory science[J].Journal of Food Composition and Analysis,2023,124:105697.
[5] DU W B,ZHEN D W,WANG Y T,et al.Characterization of the key odorants in grilled mutton shashlik with or without suet brushing during grilling[J].Flavour and Fragrance Journal,2021,36(1):111-120.
[6] 王嘉楠,刘洋,李凯旋,等.炸鸡翅营养组分变化及关键香气成分分析[J].食品科学技术学报,2024,42(2):142-155.WANG J N,LIU Y,LI K X,et al.Analysis of changes in nutritional compositions and key aroma compounds in fried chicken wings[J].Journal of Food Science and Technology,2024,42(2):142-155.
[7] 王蒙,侯莉,曹长春,等.清炖猪肉汤香气物质的分析鉴定[J].食品科学,2015,36(24):105-111.WANG M,HOU L,CAO C C,et al.Characterization of the aroma compounds in stewed pork broth[J].Food Science,2015,36(24):105-111.
[8] 王天泽,谭佳,杜文斌,等.北京油鸡鸡汤滋味物质分析[J].食品科学,2020,41(8):159-164.WANG T Z,TAN J,DU W B,et al.Analysis of taste compounds in stewed chicken broth of Beijing Youji[J].Food Science,2020,41(8):159-164.
[9] 李凯旋,王璇,刘洋,等.烹饪方式对烤羊排脂肪酸组成及挥发性风味物质的影响[J].食品科学,2024,45(18):143-151.LI K X,WANG X,LIU Y,et al.Effects of cooking methods on fatty acid composition and volatile substances in oven-roasted lamb chops[J].Food Science,2024,45(18):143-151.
[10] KIM S A,LEE J E,KIM D H,et al.A highly sensitive indirect enzyme-linked immunosorbent assay (ELISA) based on a monoclonal antibody specific to thermal stable-soluble protein in pork fat for the rapid detection of pork fat adulterated in heat-processed beef meatballs[J].Food Science of Animal Resources,2023,43(6):989-1001.
[11] XU C H,YIN Z Z.Unraveling the flavor profiles of chicken meat:Classes,biosynthesis,influencing factors in flavor development,and sensory evaluation[J].Comprehensive Reviews in Food Science and Food Safety,2024,23(4):13391.
[12] 赵健,王蒙,谢建春,等.黑猪肉关键香气物质分析鉴定[J].食品科学,2018,39(2):203-209.ZHAO J,WANG M,XIE J C,et al.Characterization of key aroma compounds in pork from black pig[J].Food Science,2018,39(2):203-209.
[13] LIAN F L,CHENG J H,SUN D W.Insight into the effect of microwave treatment on fat loss,fatty acid composition and microstructure of pork subcutaneous back fat[J].LWT,2023,187:115297.
[14] LI J,XU Y X,DU W B,et al.Comparative analysis of aroma compounds in Chinese traditional dry-rendered fat by HS/GC-IMS,SPME/GC-MS,and SPME/GC-O[J].Journal of Food Composition and Analysis,2022,107:104378.
[15] 甄大卫,徐玉霞,张晨萍,等.调控氧化猪脂的香气成分分析[J].食品科学技术学报,2022,40(4):96-106.ZHEN D W,XU Y X,ZHANG C P,et al.Analysis of aroma compounds in lard oxidized in control[J].Journal of Food Science and Technology,2022,40(4):96-106.
[16] BI J C,LI Y,YANG Z,et al.Effect of different cooking times on the fat flavor compounds of pork belly[J].Journal of Food Biochemistry,2022,46(8):14184.
[17] 肖群飞,范梦蝶,赵健,等.猪五花肉炖煮肉汤香气物质的分析鉴定[J].食品工业科技,2017,38(22):273-279;295.XIAO Q F,FAN M D,ZHAO J,et al.Characterization of the aroma compounds in stewed meat broth of pork belly[J].Science and Technology of Food Industry,2017,38(22):273-279;295.
[18] 王璇,胡晴晴,何金鑫,等.不同烤制时间的鸡翅理化指标及风味物质组成差异[J].中国食品学报,2024,24(12):414-431.WANG X,HU Q Q,HE J X,et al.Differences in physicochemical characteristics and volatile flavor composition for roasted chicken wings at different roasting times[J].Journal of Chinese Institute of Food Science and Technology,2024,24(12):414-431.
[19] SOHAIL A,AL-DALALI S,WANG J N,et al.Aroma compounds identified in cooked meat:A review[J].Food Research International,2022,157:111385.
[20] LI J,HU Q Q,HE J X,et al.Debittering and improving flavour of enzymatic soy protein hydrolysate using the Maillard reaction of Arabinose[J].Flavour and Fragrance Journal,2025,40(2):205-224.
[21] FU Y,ZHANG Y H,SOLADOYE O P,et al.Maillard reaction products derived from food protein-derived peptides:Insights into flavor and bioactivity[J].Critical Reviews in Food Science and Nutrition,2020,60(20):3429-3442.
[22] CHANG Y,WANG S Q,CHEN H T,et al.Characterization of the key aroma compounds in pork broth by sensory-directed flavor analysis[J].Journal of Food Science,2021,86(11):4932-4945.
[23] 史亚静,葛柳凤.不同制作工艺对猪油理化与风味品质的影响[J].肉类研究,2020,34(4):40-45.SHI Y J,GE L F.Effects of production conditions on physicochemical and flavor quality of lard[J].Meat Research,2020,34(4):40-45.
[24] WANG Y,SONG H L,ZHANG Y,et al.Determination of aroma compounds in pork broth produced by different processing methods[J].Flavour and Fragrance Journal,2016,31(4):319-328.
[25] ZHANG C P,WANG X,LIU Y,et al.Characteristics of meat flavoring prepared using hydrolyzed plant protein mix by three different heating processes[J].Food Chemistry,2024,446:138853.
[26] DU W B,ZHAO M Y,ZHEN D W,et al.Key aroma compounds in Chinese fried food of youtiao[J].Flavour and Fragrance Journal,2020,35(1):88-98.
[27] GEMERT L J V.Odour thresholds:compilations of odour threshold values in air,water and other media[M].2nd ed.The Netherlands:Oliemans Punter &Partners B,2011.
[28] BASSAM S M,NOLETO-DIAS C,FARAG M A.Dissecting grilled red and white meat flavor:Its characteristics,production mechanisms,influencing factors and chemical hazards[J].Food Chemistry,2022,371:131139.
[29] NAVARRO M,DUNSHEA F R,LISLE A,et al.Feeding a high oleic acid (C18:1) diet improves pleasing flavor attributes in pork[J].Food Chemistry,2021,357:129770.
[30] YU Y R,WANG G Y,YIN X Y,et al.Effects of different cooking methods on free fatty acid profile,water-soluble compounds and flavor compounds in Chinese Piao chicken meat[J].Food Research International,2021,149:110696.
[31] YANG X L,PEI Z Y,DU W B,et al.Characterization of volatile flavor compounds in dry-rendered beef fat by different solvent-assisted flavor evaporation (SAFE) combined with GC-MS,GC-O,and OAV[J].Foods,2023,12(17):3162.