药食同源理念是中华传统饮食智慧与中医药文化深度交融的结晶,千百年来始终守护着中华民族的健康。随着老龄化进程加速和健康消费观念升级,我国药食同源食品产业迎来爆发式增长,2024年市场规模已突破3 500亿元,发展势头迅猛。不同于普通中药材,药食同源食品既是餐桌上的日常食材,消费量庞大,又是药柜里的治病良药,现代科学研究也已证实,其富含的生物活性成分具有抗氧化、抗菌、抗病毒、抗炎及抗癌等多重功效[1]。近年来,随着市场需求持续攀升,药食同源原料人工种植面积不断扩大[2]。受水源、土壤等影响,药食同源食品在种植、采收、加工、炮制和贮藏等多环节易遭受外源性污染,造成农药残留、重金属超标等食品安全隐患[3]。这不仅损害了产品品质,更对消费者健康构成潜在威胁。特别是汞这种具有高度生物毒性的重金属元素,一旦污染了药食同源食品,长期食用将造成人体神经、消化和免疫系统不可逆转的伤害[4]。为此,我国2020年版《中国药典》制定了严格的限量标准,明确规定药食同源药材和饮片中Hg2+含量不得超过0.2 mg/kg[5]。建立高灵敏度和高特异性的检测方法,实现对Hg2+残留量的精准监测,已成为把控药食同源食品质量的关键环节。
电化学检测方法具有操作简单、成本低、灵敏度高等优点,已成为食品安全检测领域极具潜力的新兴技术[6]。然而,传统的Hg2+电化学检测方法选择性较差,易受其他重金属离子(如Cu2+、Pb2+)及样品基质的干扰,在实际应用中,往往需要额外增加化学掩蔽等预处理手段,大大限制了其在实际样品检测中的应用。ONO等[7]研究发现,胸腺嘧啶(T)可通过N-Hg2+配位作用,特异性地结合Hg2+并形成稳定的T-Hg2+-T结构,该结构的结合常数大于天然A-T碱基对,具有很强的稳定性和特异性。基于此原理构建的Hg2+检测方法,能够克服传统Hg2+电化学检测方法依赖化学掩蔽的局限,通过T-Hg2+-T配位的分子识别机制特异性捕获样品中的Hg2+,避免了其他离子的干扰,其选择性得到了显著提升。
DNA序列的合成便捷性与修饰灵活性为信号放大提供了新思路,通过合理的序列设计,能够在核酸工具酶或化学熵变化驱动下实现扩增或自组装,进而形成复杂的核酸结构实现信号的有效放大[8]。其中,杂交链式反应(hybridization chain reaction,HCR)技术作为一种典型的无酶核酸信号放大策略,主要利用2个发卡探针在引发链触发下发生交替杂交,实现信号的级联放大。HCR技术操作简便、反应条件温和、结果可靠,在痕量测量中显示出强大的信号放大能力[9]。
金磁纳米粒子是一种复合纳米材料,以Fe3O4磁性颗粒为内核,表面包覆金纳米层,具有优异的超顺磁特性和生物相容性,能够在外加磁场作用下,实现快速分离,在复杂样品检测中展现显著优势[10]。本研究以金磁纳米粒子为载体,固定Hg2+特异性识别适配体探针(aptamer,Apt),构建基于HCR的电化学传感检测方法对荷叶、金银花、白芷、鱼腥草4种典型的药食同源食品中Hg2+进行测定。
1 材料与方法
1.1 材料与试剂
Tris-EDTA(TE)缓冲液、4S Green Plus无毒核酸染料、50×TAE缓冲液、6×甘油凝胶上样缓冲液I(含溴酚蓝、EDTA),生工生物工程(上海)股份有限公司;硫酸亚铁,天津市光复科技发展有限公司;氨水,天津市大茂化学试剂厂;氯化铁、氯金酸、柠檬酸三钠,国药集团化学试剂有限公司;2-巯基乙醇、硝酸汞、琼脂糖,上海阿拉丁生化科技股份有限公司;荷叶、金银花、白芷、鱼腥草,政通大药房旗舰店。实验所用试剂均为分析纯。
实验中所有DNA序列的合成、纯化与修饰均由生工生物工程(上海)股份有限公司完成,其序列如表1所示。
表1 DNA名称及其序列
Table 1 DNA name and its nucleotide sequence
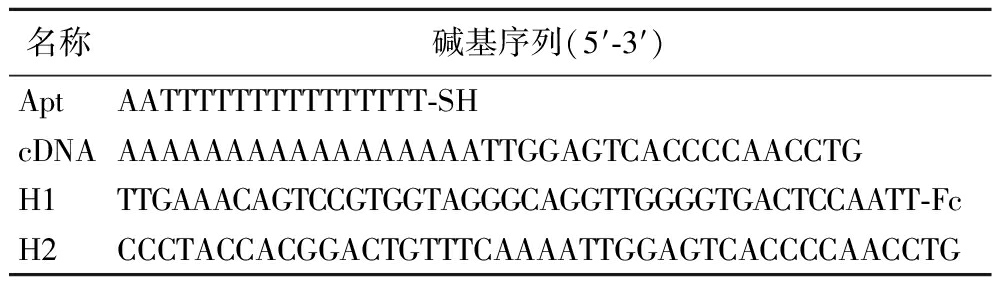
名称碱基序列(5′-3′)AptAATTTTTTTTTTTTTTT-SHcDNAAAAAAAAAAAAAAAAAATTGGAGTCACCCCAACCTGH1TTGAAACAGTCCGTGGTAGGGCAGGTTGGGGTGACTCCAATT-FcH2CCCTACCACGGACTGTTTCAAAATTGGAGTCACCCCAACCTG
1.2 仪器与设备
CHI660E电化学工作站,上海辰华仪器有限公司;KQ2200超声清洗器,昆山市超声仪器有限公司;BE-1100四维旋转混合仪,海门市其林贝尔仪器有限公司;Tecnai G2 F30透射电镜,美国FEI公司;MPMS XL-7超导干涉量子仪,美国Quantum Design公司;PowerPacTM Basic基础型电泳仪、GelDocXR凝胶成像系统,美国伯乐公司。
1.3 实验方法
1.3.1 金磁纳米粒子合成
首先采用化学共沉淀法制备Fe3O4,在60 ℃下向充分溶解的0.03 mol/L Fe2+/Fe3+溶液中加入25%(体积分数)氨水溶液,颜色变为黑色后,继续搅拌反应10 min,停止反应。冷却后洗涤3次,配制成5 g/L于4 ℃冰箱保存。
取2 mL 5 g/L的Fe3O4溶液与86 mL超纯水和4 mL 质量分数为1%的氯金酸溶液混合,加热、搅拌反应30 min,待溶液微沸时,快速加入8 mL 质量分数为1%的柠檬酸三钠溶液,持续搅拌反应,溶液颜色由黑色逐渐转变为红棕色后,继续搅拌10 min,停止反应,自然冷却后,洗涤,磁分离收集金磁纳米粒子,配制成5 g/L于4 ℃冰箱保存。
1.3.2 金磁-Apt探针制备
取5 g/L金磁纳米粒子15 μL,磁分离去除上清液,加入15 μL 含3 μmol/L Apt的TE缓冲液(pH值=7.4),于37 ℃下避光反应120 min。反应结束后,磁分离,收集上清液,加入TE缓冲液洗涤3次。随后加入100 μL 2.0 mmol/L巯基乙醇溶液反应90 min,用于封闭金磁表面未反应位点。封闭结束后,去除上清液,加入TE缓冲液洗涤,最后加入15 μL TE缓冲液重悬,4 ℃避光贮存。
1.3.3 Hg2+检测
取15 μL金磁-Apt探针,去除上清液之后加入15 μL 3 μmol/L cDNA溶液和Hg2+,于37 ℃下避光反应60 min。反应结束后,磁分离,去除上清液,加入TE缓冲液洗涤3次,然后加入30 μL 含4.5 μmol/L H1和H2的TE缓冲液,在37 ℃下避光反应80 min,磁分离去除上清液,清洗后加入15 μL TE缓冲液重悬,4 ℃下暂存。
电化学检测采用三电极体系,磁性玻碳电极为工作电极,Ag/AgCl电极为参比电极、铂电极为对电极。首先对工作电极进行预处理,依次用1.0、0.3、0.05 μm氧化铝粉末打磨抛光至镜面。然后依次用超纯水、体积分数为50%的乙醇溶液和超纯水超声清洗1 min。随后在0.5 mol/L硫酸溶液中用循环伏安法活化处理,直至得到稳定的循环伏安曲线,处理后的工作电极用超纯水冲洗,氮气吹干后备用[11]。
利用磁性玻碳电极内置的磁铁将反应后的金磁纳米粒子固定到工作电极表面,利用差分脉冲伏安法(differential pulse voltammetry,DPV)在0.1 mol/L PBS(pH值=7.0)中测定,参数为:扫描电位范围-0.4~0.6 V,振幅0.05 V,脉冲宽度0.025 s。通过循环伏安法(cyclic voltammetry,CV)在含有5 mmol/L[Fe(CN)6]3-/4-的0.1 mol/L KCl溶液中对传感器表面修饰过程进行电化学表征,参数为:扫描电位-0.2~0.6 V,扫描速度0.1 V/s。
1.3.4 实际样品处理
采用水浴浸提法对实际样品处理。分别称取0.500 0 g干燥后的荷叶、金银花、白芷、鱼腥草于50 mL 比色管中,加入少量水浸润后,加入10 mL硝酸-盐酸混合液,混合后室温下浸泡3 h,随后沸水浴加热1.5 h,消解后冷却至室温,5 000 r/min离心10 min,然后将上清液用0.22 μm滤膜过滤,并调节pH值至7.0保存备用。为减少操作误差和避免样品检测出现假阳性,本研究采用逐级稀释的方法,即在预处理后的样本中添加Hg2+标准溶液并定容至100 mL,逐级稀释制备含0.01、0.1、1 ng/mL的Hg2+样品,按照1.3.3节进行测定。
1.4 数据处理
电化学数据均采集于电化学工作站,以添加Hg2+前后的Fc电化学信号变化值ΔI为依据进行数据分析,如公式(1)所示:
ΔI=I0-IX
(1)
式中:I0,未添加Hg2+所测的Fc电流值;IX,添加Hg2+所测的Fc电流值。
2 结果与分析
2.1 实验原理
检测原理如图1所示。采用金磁纳米粒子为载体,利用Au-S键,将3′端修饰巯基的Apt负载于金磁纳米粒子表面,构建金磁-Apt探针。Apt探针序列富含T碱基,能够特异性识别Hg2+,形成T-Hg2+-T稳定结构。cDNA由两部分构成,靠近5′端的A碱基能够与Apt探针上的T碱基互补配对,靠近3′端的碱基序列则用于触发HCR。当样品中不含Hg2+时,cDNA通过与Apt互补配对结合到金磁纳米粒子上,暴露出3'端的触发碱基,添加发卡探针H1和H2后,启动HCR反应,直至耗尽发夹探针。若样品中存在Hg2+时,由于N-Hg2+结构的稳定性高于A-T结构,Apt优先与Hg2+结合形成T-Hg2+-T,导致游离的cDNA被磁分离去除,即使添加发卡探针,HCR反应也无法发生。可利用磁性玻碳电极内置的磁铁将反应后的金磁纳米粒子固定到检测表面测定,由于发卡探针H1的3′端修饰有电化学活性物质二茂铁(ferrocene,Fc),因此样品中不存在Hg2+时,由于发生HCR能够检测到更多的Fc信号(I0),而当样品中含有Hg2+时,HCR反应受抑制,Fc信号减弱(IX)。
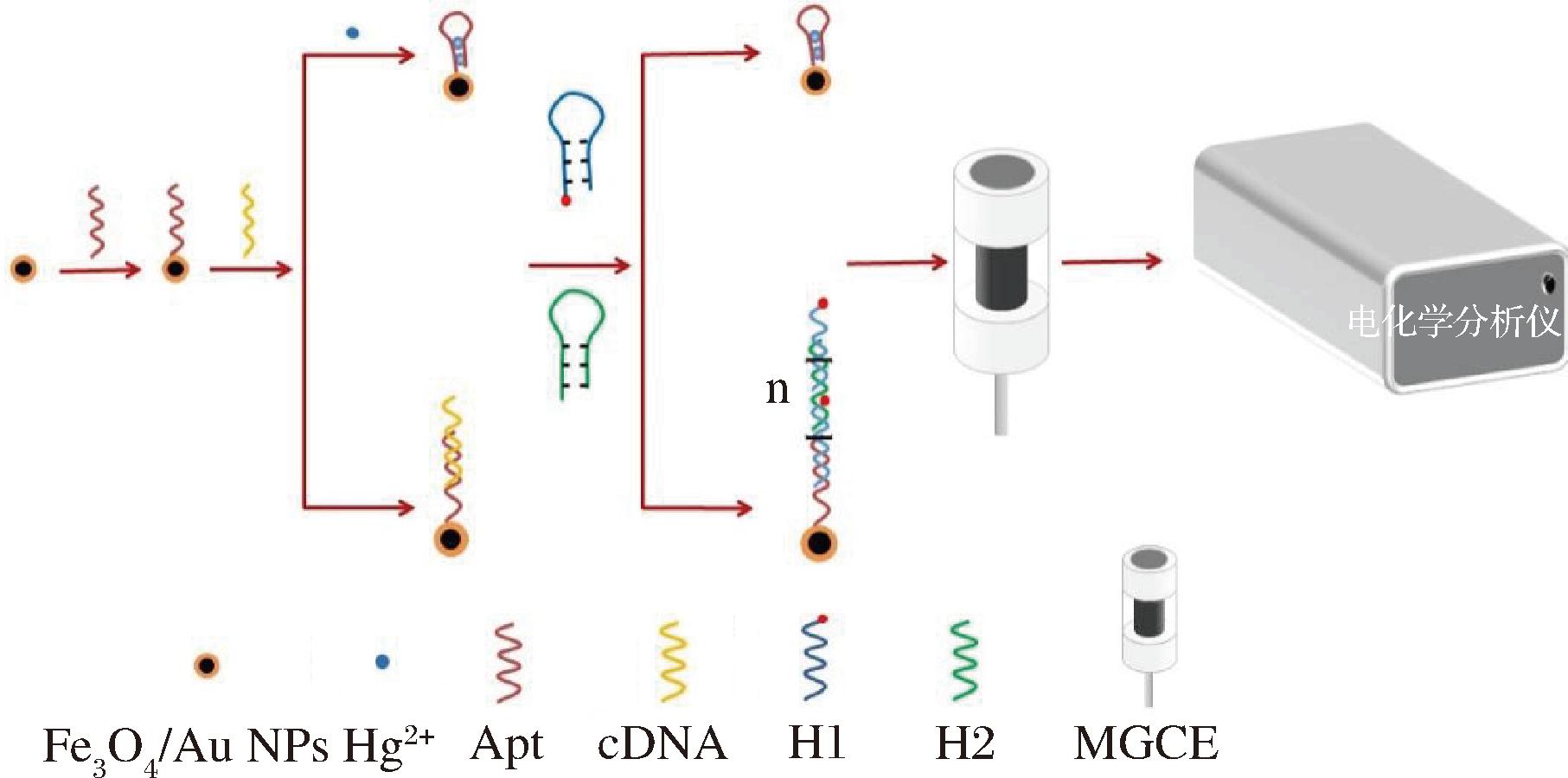
图1 以金磁纳米粒子为载体的基于杂交链式反应电化学传感技术检测Hg2+原理图
Fig.1 Schematic illustration of the Hg2+ detection mechanism via hybridization chain reaction-based electrochemical sensing platform using Fe3O4/Au NPs carriers
2.2 金磁纳米粒子的表征
合成后的金磁纳米粒子溶液呈红棕色、分散均匀,当外加磁场后,金磁纳米粒子被迅速吸引至外磁铁端,具有良好的磁分离特性(图2-a),进一步磁学性能分析表明,在300 K时,金磁纳米粒子具有良好的超顺磁特性(图2-b),磁饱和强度值为63 emu/g,明显优于文献[12]报道的金磁纳米粒子的磁性能。
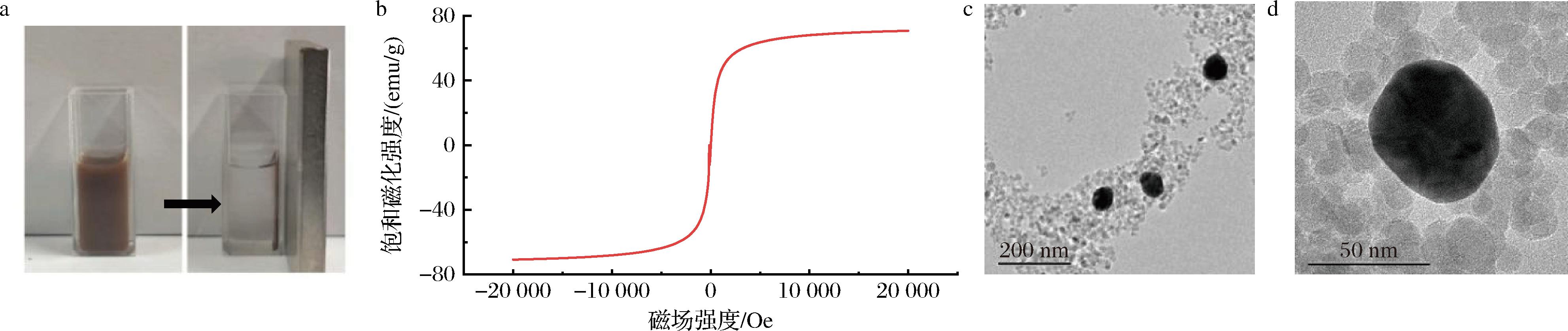
a-外加磁力吸附金磁纳米粒子;b-纳米粒子的磁响应力;c-Fe3O4/Au的透射电镜图(200 nm);d-Fe3O4/Au的透射电镜图(50 nm)
图2 纳米粒子的表征
Fig.2 Characterization of nanoparticles
利用透射电镜对所制备的金磁纳米粒子形貌进行表征,如图2-c和图2-d所示,在Fe3O4粒子周围聚集了大量的金纳米粒子,说明金磁纳米粒子已成功合成,其平均粒径大约为53.07 nm。
2.3 HCR反应验证
采用琼脂糖凝胶电泳检验HCR可行性。HCR是一种典型的触发式反应,其反应动力来自于触发链与发卡探针碱基互补配对后释放的化学能,是一个熵增过程。如图3所示,当体系中只有H1和H2时(泳道4),不会发生杂交反应。当体系中Apt和H1、H2共存时(泳道5),Apt不会触发HCR,没有高分子质量的DNA产物生成。只有当cDNA和H1、H2共同存在时(泳道6),cDNA才会触发HCR反应,发卡结构依次打开,生产高分子质量的DNA产物,出现HCR电泳的典型特征(逐级拖尾)。
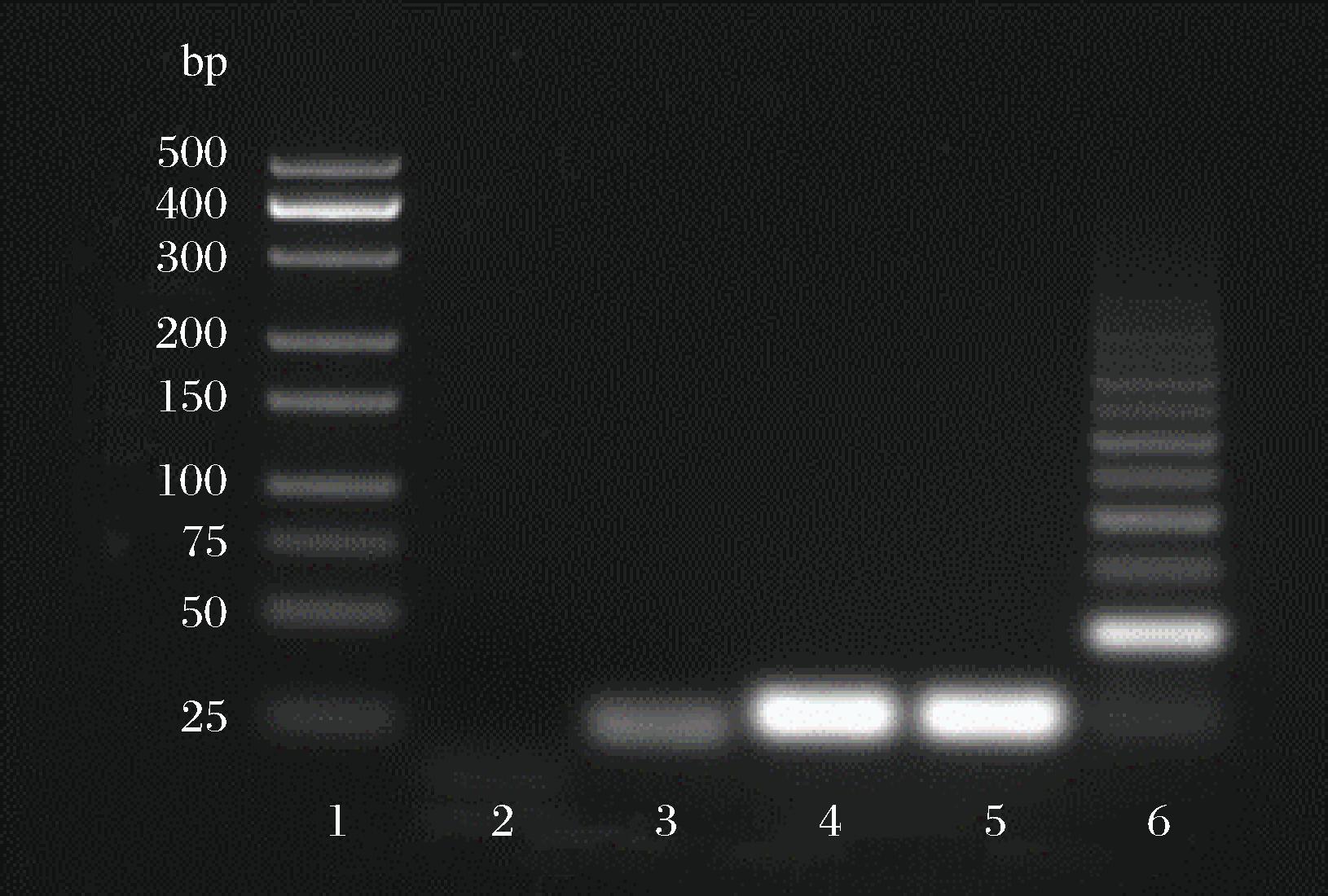
1-Marker;2-Apt;3-cDNA;4-H1&H2;5-Apt&H1&H2;6-H1&H2&cDNA
图3 HCR机理的琼脂糖凝胶电泳图
Fig.3 Agarose gel electrophoresis diagram of HCR mechanism
2.4 电化学适配体传感器的表征
采用CV对金磁-Apt探针在电极表面的修饰情况进行表征。图4为不同电极在含5 mmol/L[Fe(CN)6]3-/4-的0.1 mol/L KCl溶液中的CV曲线。裸磁性玻碳电极CV曲线呈现![]() 可逆的氧化还原峰。电极表面修饰了金磁纳米粒子后峰电流略有下降,这主要是由于Fe3O4较差的导电性,虽然其表面包覆的金纳米能弥补Fe3O4导电性不足的缺陷,但并未完全消除其影响。当金磁纳米粒子表面负载Apt探针后,峰电流进一步下降,这是因为带负电的磷酸骨架会排斥
可逆的氧化还原峰。电极表面修饰了金磁纳米粒子后峰电流略有下降,这主要是由于Fe3O4较差的导电性,虽然其表面包覆的金纳米能弥补Fe3O4导电性不足的缺陷,但并未完全消除其影响。当金磁纳米粒子表面负载Apt探针后,峰电流进一步下降,这是因为带负电的磷酸骨架会排斥![]() 阻碍电极表面的电子传递。加入cDNA后,cDNA与Apt互补配对形成双链DNA,进一步阻碍了电子传递,峰电流进一步降低。加入发卡探针H1和H2后,HCR反应形成一条dsDNA长链,导致电流进一步降低。以上结果证明,该电极被成功修饰。
阻碍电极表面的电子传递。加入cDNA后,cDNA与Apt互补配对形成双链DNA,进一步阻碍了电子传递,峰电流进一步降低。加入发卡探针H1和H2后,HCR反应形成一条dsDNA长链,导致电流进一步降低。以上结果证明,该电极被成功修饰。
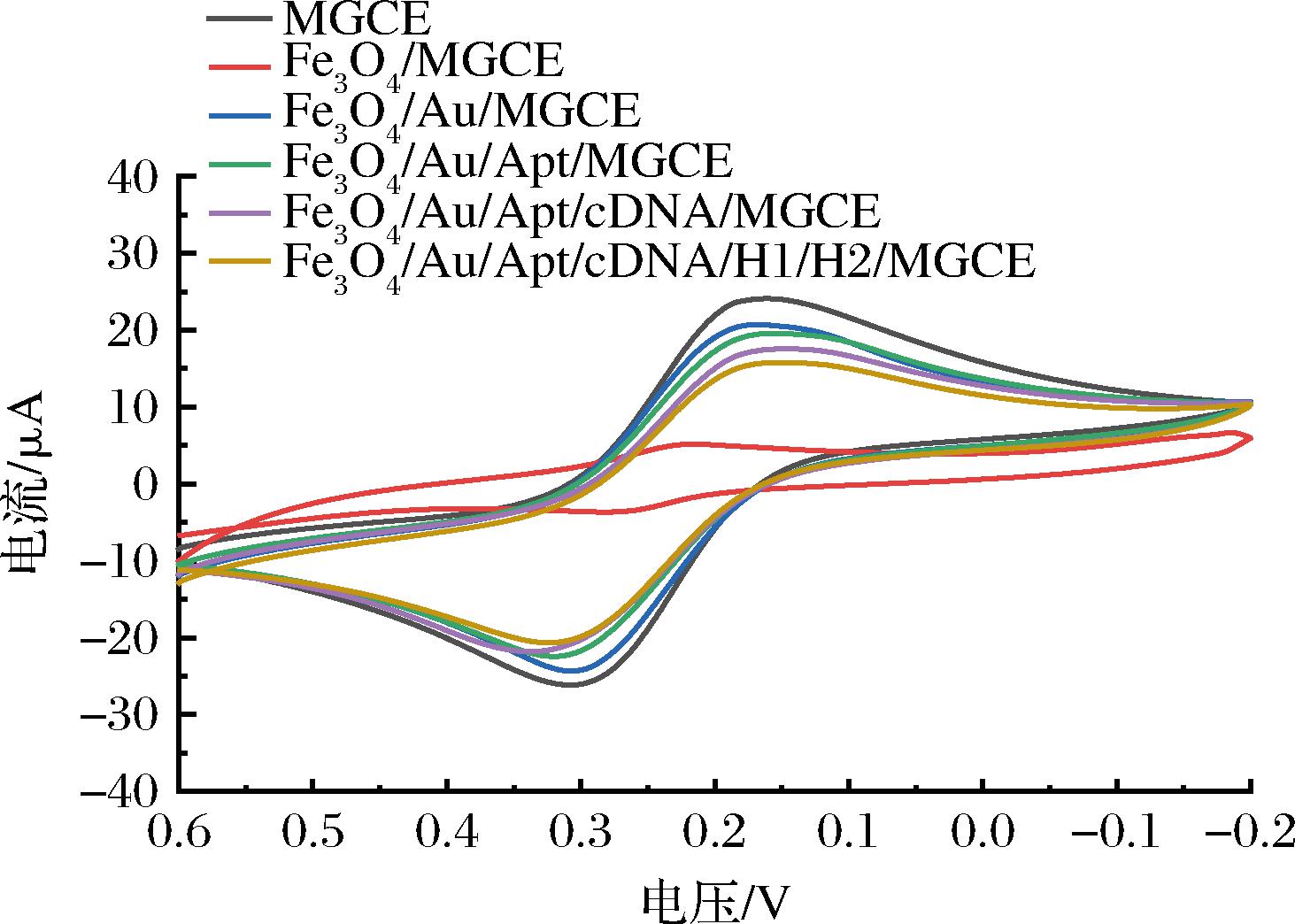
图4 不同电极的CV曲线图
Fig.4 CV curves of different electrodes
2.5 实验条件的优化
为获取最佳信号,分别考察了金磁纳米用量、金磁上负载的Apt浓度、识别反应时间、发卡探针浓度以及HCR反应时间对传感信号的影响。
实验考察了15、20、25、30、35 μg金磁纳米用量对电化学信号的影响。如图5-a所示,ΔI随着金磁纳米用量的增加而递增,当金磁纳米用量为25 μg时,ΔI最大,继续增加其用量,ΔI轻微下降,这可能是因为过多的金磁纳米会堆积在电极表面,阻碍了Fc与电极之间的电子传递过程。因此,金磁纳米的最佳用量为25 μg。
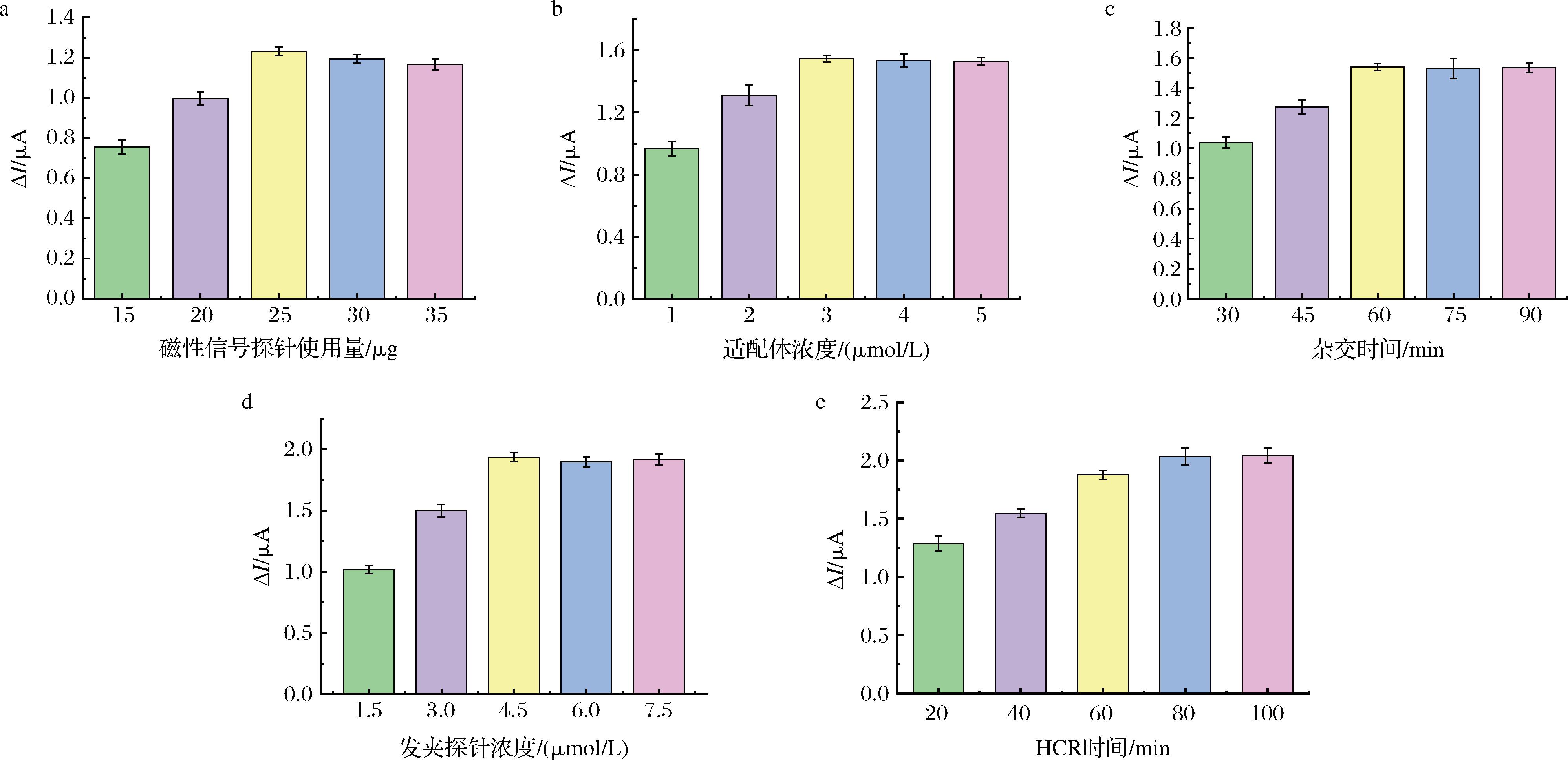
a-信号探针使用量;b-适配体浓度;c-杂交时间;d-发夹探针浓度;e-HCR时间
图5 实验条件优化
Fig.5 Optimization of experimental conditions
金磁纳米粒子上负载的Apt多少将影响后续杂交反应与HCR,因此考察了Apt浓度对信号的影响。如图5-b所示,当Apt浓度为1~3 μmol/L时,ΔI呈递增趋势,3 μmol/L时达到最大。继续增大Apt浓度,ΔI趋向平稳,表明Apt在金磁纳米粒子上的负载量已近饱和,因此选择3 μmol/L作为最佳Apt浓度。
分别考察了30、45、60、75、90 min这5个识别反应时间对电化学信号的影响。如图5-c所示,随着时间从30 min延长到60 min,ΔI也呈现上升趋势,并在60 min时ΔI趋于稳定,与文献报道的Hg2+识别反应时间50 min较为接近[13]。因此,确定最佳的识别时间为60 min。
HCR是无酶核酸信号放大技术,发卡探针浓度和HCR反应时间直接影响放大效果,并且用于电化学分析的电化学活性物主要源自H1上修饰的Fc,也会影响检测信号。如图5-d所示,当发夹探针浓度由3 μmol/L增加为4.5 μmol/L时,ΔI也随之增加,在4.5 μmol/L时达到最大。继续增加发夹探针浓度,ΔI保持不变。如图5-e所示,随着时间推移,ΔI持续增加。当HCR反应时间为80 min时,HCR基本结束,继续延长时间,ΔI趋于稳定。因此选择4.5 μmol/L的作为最佳发夹探针浓度,80 min作为最佳HCR反应时间。
2.6 汞离子的定量检测
在最优条件下,采用本实验所构建的基于HCR电化学传感检测方法对不同浓度的Hg2+进行测定。如图6-a所示,Fc的氧化峰电流强度随着Hg2+浓度(0.01~100 ng/mL)的增加而降低,ΔI总体呈上升趋势(图6-b)。以样品浓度的对数(lgC)为横坐标,ΔI为纵坐标作图(图6-c),结果显示Hg2+浓度在0.01~100 ng/mL,lgC与ΔI呈现良好的线性关系,线性回归方程为ΔI(μA)= 0.434 5+0.143 1 lgC (ng/mL),R2=0.994 0,其中C为Hg2+浓度。该方法检出限为0.01 ng/mL(3σ/k),显著低于2020年版《中国药典》中规定的有关于汞限量(不得过0.2 mg/kg)的要求,表明本方法能够满足Hg2+痕量检测的需求,这是由于HCR可在cDNA链触发下,引起2个发卡探针的交替杂交,实现检测信号的级联放大,因此显著提升了该方法对Hg2+的检测灵敏性。将该方法与文献报道的Hg2+检测方法对比(表2)发现,该方法具有较低的检出限和较宽的检测范围。
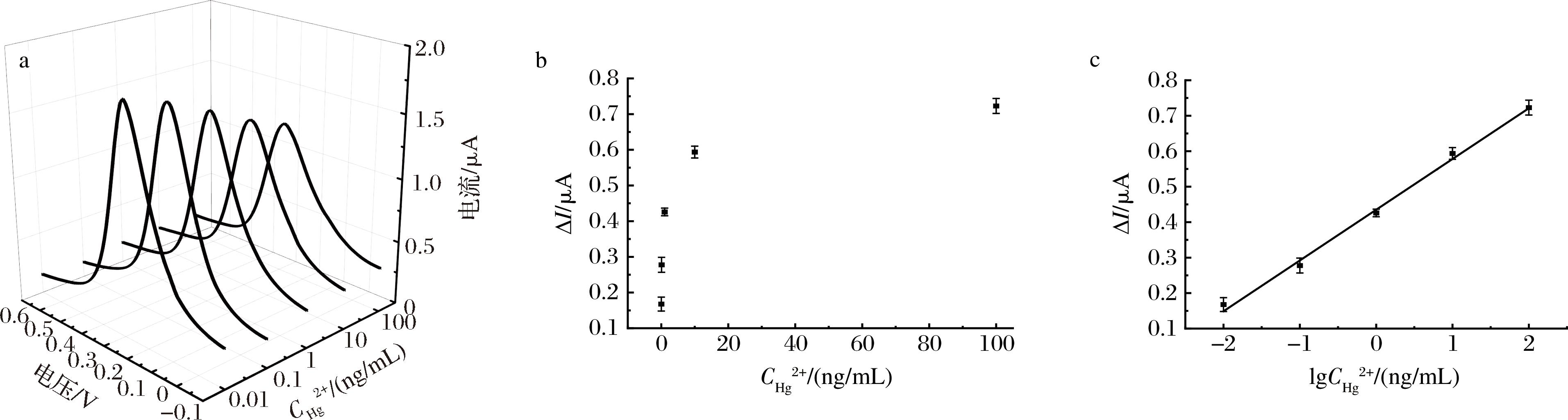
a-DPV响应曲线;b-浓度与ΔI关系图;c-浓度对数与ΔI关系图
图6 Hg2+的定量检测
Fig.6 Quantitative detection of Hg2+
表2 不同方法检测Hg2+比较
Table 2 Comparison of different methods for detecting Hg2+
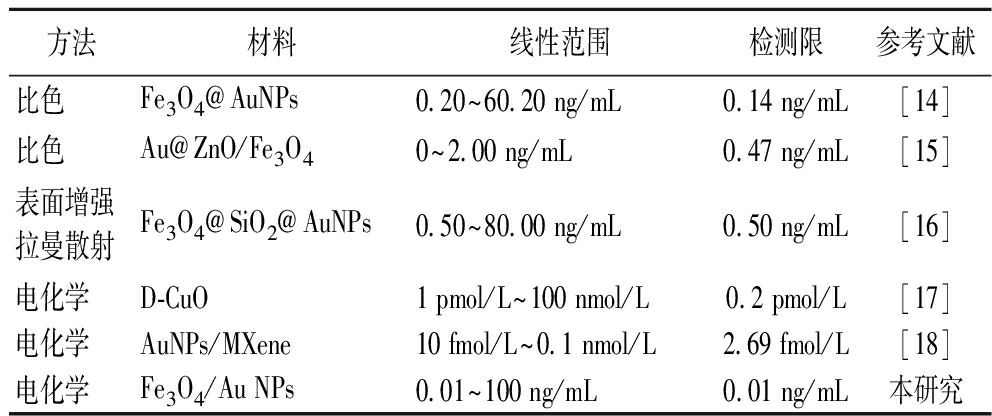
方法材料线性范围检测限参考文献比色Fe3O4@AuNPs0.20~60.20 ng/mL0.14 ng/mL[14]比色Au@ZnO/Fe3O40~2.00 ng/mL0.47 ng/mL[15]表面增强拉曼散射Fe3O4@SiO2@AuNPs0.50~80.00 ng/mL0.50 ng/mL[16]电化学D-CuO1 pmol/L~100 nmol/L0.2 pmol/L[17]电化学AuNPs/MXene10 fmol/L~0.1 nmol/L2.69 fmol/L[18]电化学Fe3O4/Au NPs0.01~100 ng/mL0.01 ng/mL本研究
虽然文献[17]和[18]因为电极表面修饰了3D多孔AuNPs/MXene和D-CuO/Au,提高了电极的导电性、增加了电活性面积,其检出限要优于本方法,然而它们的识别过程与电化学检测过程均在电极表面进行,而本方法却是以金磁纳米粒子为载体,其识别与HCR并未在电极表面进行,只有电化学检测时通过磁性玻碳电极内置的磁铁将金磁纳米粒子转移至检测表面进行测定,一定程度上避免了识别反应中样品复杂基质对后续检测的影响。
2.7 方法性能评估
为探究本方法的特异性,选取10 ng/mL的Ca2+、Mg2+、Al3+、Fe3+、Zn2+、Cu2+、Ni2+、Pb2+、Cd2+、Na+、K+、Cr3+、As3+为干扰离子,与1 ng/mL Hg2+和未添加任何干扰离子的空白样进行比较,分别测定其ΔI值。如图7-a所示,只有Hg2+存在时,ΔI值才会出现显著变化,其他干扰离子存在时的ΔI值与空白样的ΔI值相差不大。这是主要是由于Apt中的T能够通过N-Hg2+配位作用,特异性识别Hg2+形成稳定的T-Hg2+-T结构,确保方法良好的抗干扰性能。将同一批次制备的金磁-Apt探针置于4 ℃冰箱保存14 d,每隔1 d,加入1 ng/mL Hg2+进行反应,测定其ΔI值。图7-b结果显示14 d后,仍能保持其初始值的92.6%,说明金磁-Apt探针具有良好的稳定性。
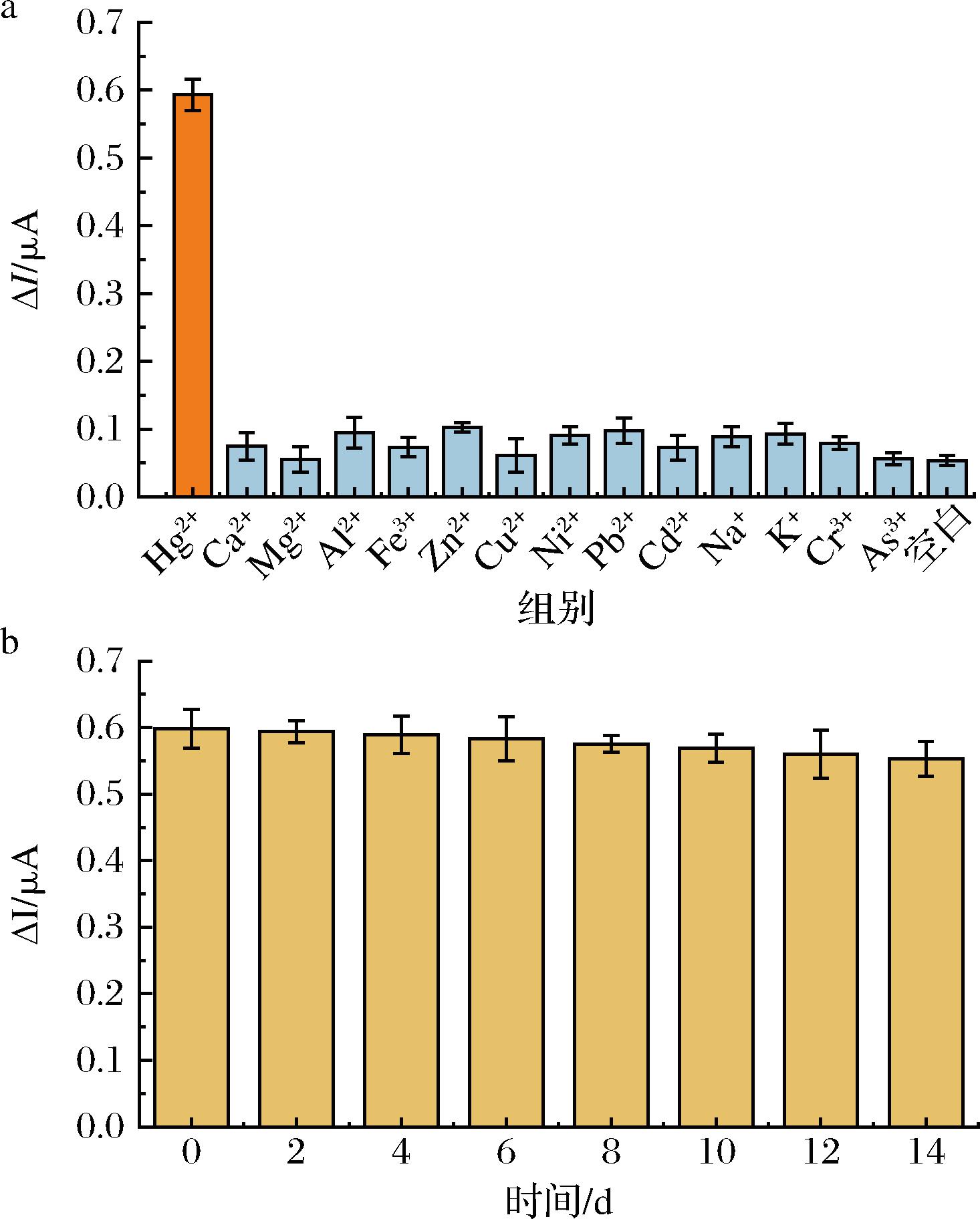
a-特异性;b-稳定性
图7 方法性能评估
Fig.7 Performance evaluation of method
2.8 实际样品检测
为探究本实验所构建的电化学传感检测方法是否能够用于药食同源食品中Hg2+测定,选择荷叶、金银花、白芷和鱼腥草4种典型的药食同源食品作为复杂基质,进行人工加标试验并测定其回收率。在最佳实验条件下,将不同浓度(0.01、0.1、1 ng/mL)的Hg2+分别添加到预处理后的样品中,按照本实验所构建的电化学传感检测方法进行测定。结果如表3所示,其加标回收率为95.28%~104.77%,相对标准偏差小于6.38%。说明本方法可以用于荷叶、金银花、白芷和鱼腥草这4种典型药食同源食品中Hg2+的检测。
表3 不同样品中Hg2+的检测
Table 3 Detection of Hg2+in different samples
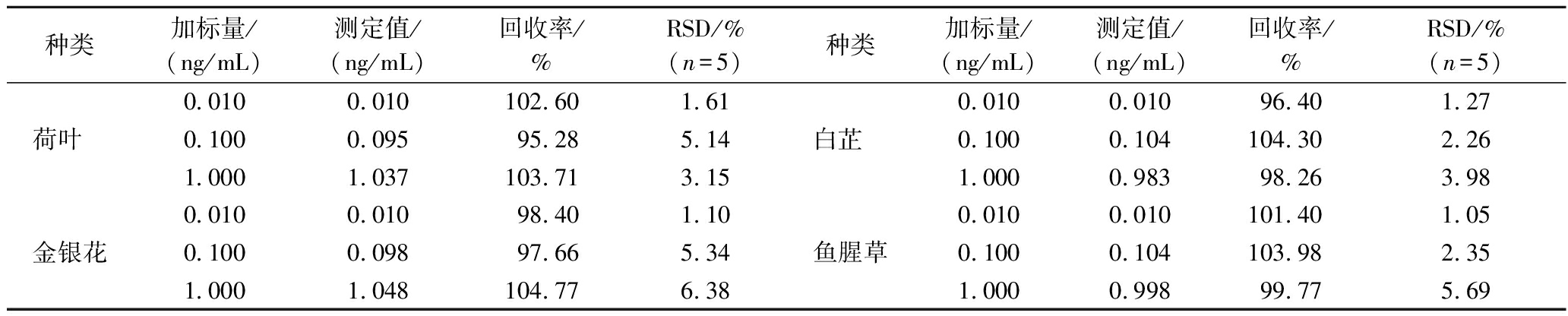
种类加标量/(ng/mL)测定值/(ng/mL)回收率/%RSD/%(n=5)种类加标量/(ng/mL)测定值/(ng/mL)回收率/%RSD/%(n=5)0.0100.010102.601.610.0100.01096.401.27荷叶 0.1000.09595.285.14白芷 0.1000.104104.302.261.0001.037103.713.151.0000.98398.263.980.0100.01098.401.100.0100.010101.401.05金银花0.1000.09897.665.34鱼腥草0.1000.104103.982.351.0001.048104.776.381.0000.99899.775.69
注:RSD:相对标准偏差(relative standard deviation)。
3 结论
本研究构建了一种以金磁纳米粒子为载体,基于HCR反应的Hg2+电化学传感检测方法,金磁-Apt探针能够特异性识别Hg2+或与cDNA互补配对,引发HCR反应产生dsDNA长链。在最佳条件下,该方法测得的ΔI值与浓度的对数呈现出良好的线性关系,检测限可达0.01 ng/mL,显著低于国家限量标准,能有效满足痕量Hg2+检测的需求。通过对荷叶、金银花、白芷和鱼腥草4种药食同源食品进行加标回收检验,其加标回收率为95.28%~104.77%,相对标准偏差小于6.38%,证明该传感检测方法可用于4种典型药食同源食品中Hg2+的高效检测,为痕量Hg2+检测提供了一种灵敏度高、特异性强的新策略。
[1] 王盟鑫,赵月伟,赵冬梅,等.我国药食同源物质活性成分提取及应用[J].中国果菜,2024,44(5):2-7.WANG M X,ZHAO Y W,ZHAO D M,et al.Research progress on extraction and application of active components of medicinal and edible homologous substances in China[J].China Fruit &Vegetable,2024,44(5):2-7.
[2] 王慧,张小波,汪娟,等.2020年全国中药材种植面积统计分析[J].中国食品药品监管,2022(1):4-9.WANG H,ZHANG X B,WANG J,et al.Statistical analysis of planting area of Chinese medicinal materials in China in 2020[J].China Food &Drug Administration Magazine,2022(1):4-9.
[3] 韩旭,骆骄阳,杨美华,等.中药饮片中重金属与有害元素残留现状及防控措施[J].世界中医药,2015,10(8):1152-1156;1162.HAN X,LUO J Y,YANG M H,et al.The present situation of Chinese herbal pieces with heavy metals and harmful elements and the control measures[J].World Chinese Medicine,2015,10(8):1152-1156;1162.
[4] RADWAN A,EL-SEWIFY I M,SHAHAT A,et al.Multiuse Al-MOF chemosensors for visual detection and removal of mercury ions in water and skin-whitening cosmetics[J].ACS Sustainable Chemistry &Engineering,2020,8(40):15097-15107.
[5] 国家药典委员会.中华人民共和国药典-三部:2020年版[M].北京:中国医药科技出版社,2020.NATIONAL PHARMACOPOEIA COMMISSION.Pharmacopoeia of the People’s Republic of China (2020)[M].Beijing:China Medical Science Press,2020.
[6] ZHOU H,QIU H M,ZHANG J H,et al.Design,preparation,and application of molecularly imprinted nanomaterials for food safety analysis with electrochemistry[J].Coordination Chemistry Reviews,2024,500:215523.
[7] ONO A,TOGASHI H.Highly selective oligonucleotide-based sensor for mercury(II) in aqueous solutions[J].Angewandte Chemie International Edition,2004,43(33):4300-4302.
[8] 郭雨湄,贾振军,刘瑞.核酸等温扩增方法在食品安全检测中的应用综述[J].食品与发酵工业,2025,51(11):435-448.GUO Y M,JIA Z J,LIU R.Isothermal nuleic acid amplification technology[J].Food and Fermentation Industries,2025,51(11):435-448.
[9] DIRKS R M,PIERCE N A.Triggered amplification by hybridization chain reaction[J].Proceedings of the National Academy of Sciences of the United States of America,2004,101(43):15275-15278.
[10] 韩博林,关桦楠,刘晓飞,等.金磁微粒的制备及其固定牛血清蛋白的研究[J].哈尔滨商业大学学报(自然科学版),2017,33(4):450-454;468.HAN B L,GUAN H N,LIU X F,et al.Preparation and application to immobilization of bovine serum albumen on gold magnetic particles[J].Journal of Harbin University of Commerce(Natural Sciences Edition),2017,33(4):450-454;468.
[11] 朱俊亚,李芳,赵兰馨,等.纳米磁珠-电化学适配体传感技术检测牛奶中氨苄青霉素[J].食品科学,2019,40(24):294-299.ZHU J Y,LI F,ZHAO L X,et al.Magnetic beads-based electrochemical aptasensor for the detection of ampicillin in milk[J].Food Science,2019,40(24):294-299.
[12] MEHDIPOUR M,GLOAG L,HAGNESS D,et al.Flow-based synthesis of gold-coated magnetic nanoparticles for magnetoplasmonic sensing applications[J].Particle &Particle Systems Characterization,2022,39(8):2200051.
[13] ZHU Y,GAO J,XU P,et al.Electrochemical sensor based on Y-shaped DNA by “one-pot” method for mercury detection[J].Microchemical Journal,2024,204:111013.
[14] WANG L N,LIU F Y,SUI N,et al.A colorimetric assay for Hg (II) based on the use of a magnetic aptamer and a hybridization chain reaction[J].Microchimica Acta,2016,183(11):2855-2860.
[15] SEMONG O,BATLOKWA B S.Rapid colorimetric detection of Hg(II) based on Hg(II)-induced suppressed enzyme-like reduction of 4-nitrophenol by Au@ZnO/Fe3O4in a cosmetic skin product[J].Nanomaterials and Nanotechnology,2023,2023:3603680.
[16] ZHU J Q,WANG B L,YANG P,et al.The functional Fe3O4@SiO2@AuNPs SERS nanomaterials for rapid enrichment and detection of mercury ions in licorice[J].Chemosensors,2022,10(10):403.
[17] YU Y J,YU C,GAO R F,et al.Dandelion-like CuO microspheres decorated with Au nanoparticle modified biosensor for Hg2+ detection using a T-Hg2+-T triggered hybridization chain reaction amplification strategy[J].Biosensors and Bioelectronics,2019,131:207-213.
[18] LI L,YAN X Y,LIU Y,et al.Electrochemical/fluorescent dual-mode aptasensor based on 3D porous AuNPs/MXene for detection of ultra-trace mercury (Hg2+)[J].Bioelectrochemistry,2025,161:108833.