淀粉是人体生命中至关重要的碳水化合物,淀粉可根据其营养性质分为3种类型:快速消化淀粉(rapidly digestible starch,RDS)、慢速消化淀粉(slowly digestible starch,SDS)和抗性淀粉(resistant starch,RS)。RDS会迅速引起餐后血糖水平的上升,这对于糖尿病患者可能是有害的。相反,SDS则缓慢释放葡萄糖,有助于餐后维持稳定的血糖水平。RS无法被小肠中的酶分解,但可以被微生物发酵,产生短链脂肪酸,从而促进有益的肠道菌群和人体健康[1]。因此,减少淀粉的可消化性被认为是预防和管理糖尿病和肥胖等慢性疾病的有效方法[2]。高直链玉米淀粉(high amylose maize starch,HAMS)是一种天然的玉米淀粉,其直链淀粉含量超过总淀粉的50%。由于其绿色健康益处和广泛的工业应用,HAMS受到了广泛关注。HAMS中较高的直链淀粉含量有助于形成紧密堆积的淀粉颗粒,这些颗粒较不易被消化酶水解[3]。较高的直链淀粉含量增加了形成紧密排列的螺旋结构的可能性,这有助于减少热处理对淀粉结构的破坏,并减缓酶解的速度。挤压是一个将物料在机械压力和剪切作用下,通过模具连续推进的过程,这些变化会影响产品的微观结构、化学性质和宏观形态。挤出过程会导致淀粉的糊化、蛋白质降解,以及淀粉、脂质和蛋白质之间的复合物形成。这些变化影响产品的微观结构、化学性质和宏观形态。许多研究发现,挤压过程中会形成直链淀粉-脂质复合物,且复合物的数量受淀粉的具体类型和食品中脂质成分的影响[4]。淀粉中的直链淀粉与内源性和外源性脂质之间形成的复合物是直链淀粉影响挤出淀粉消化性的关键因素(RS5)[5]。这可以归因于直链淀粉溶解度的降低和V型晶体的结构障碍,这保护了其不受酶解。许多研究发现,在挤出过程中,直链淀粉-脂质复合物的形成以及复合物的数量受特定类型淀粉和食品中脂质成分的影响[6-7]。
当前关于淀粉-脂质复合物的研究主要集中于单一脂肪酸体系(如硬脂酸、月桂酸或棕榈酸等),其制备工艺多采用物理复合方法,包括热混合、均质处理、超声波辅助以及微波辐射等技术。然而,这些传统方法存在明显的局限性:生产规模受限、需使用有机溶剂溶解脂质,难以满足工业化生产需求。相比之下,挤压加工技术因其操作简便、环境友好(无需添加化学试剂)等优势,在淀粉-脂质复合物的规模化制备中展现出重要应用潜力。乳化剂作为这些脂肪酸的载体可直接添加到食品当中,与淀粉复配挤出后,对淀粉的消化性(如水解速率、抗性淀粉形成等)会产生显著影响,以期为挤压淀粉基食品的消化性调控提供参考。单甘酯(monoglycerides of fatty acid,MGF)凭借其多功能、低成本、高安全性,成为食品工业中最基础的乳化剂之一,尤其适合需要改善质构和稳定性的产品。大豆卵磷脂(soybean lecithin,SL)是天然、多功能、营养强化型乳化剂,尤其适合追求清洁标签、健康功能的高端食品。柠檬酸脂肪酸甘油酯(citric and fatty acid esters of glycerol,CFG)是高安全性、耐酸耐热的功能性乳化剂,可用于婴幼儿食品。本研究采用了单甘酯、大豆卵磷脂、柠檬酸脂肪酸甘油酯和高直链玉米淀粉,利用挤压机进行共挤出。研究了不同乳化剂对与高直链玉米淀粉共同挤出的复合物的结构特性、理化性质和体外淀粉消化性的影响。采用现代分析技术对长程有序结构(晶体结构)、短程有序结构和颗粒形态进行表征,并分析了挤出后的理化性质。该研究为工业化生产挤出淀粉产品和低消化性食品的进一步开发提供了有价值的参考。
1 材料与方法
1.1 材料与试剂
高直链玉米淀粉,科赫(上海)生物科技有限公司;单甘酯、大豆卵磷脂,河南万邦化工科技有限公司;柠檬酸脂肪酸甘油酯,河南高宝实业有限公司;α-淀粉酶(货号:10080-100G,CAS号:9000-90-2),Sigma-Aldrich化学有限公司(美国);糖化酶(货号:S10017-250 g,CAS号:9032-08-0),上海源叶生物科技有限公司;总淀粉(AA/AMG)、D-葡萄糖(GOPOD格式)测定试剂盒,Megazyme公司(爱尔兰);所有化学试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
YB-7LD搅拌机,江苏联合纬创机械有限公司;FMHE36-24双螺杆挤压机,湖南富马科食品工程技术有限公司;SU8100扫描电子显微镜(scanning electron microscope,SEM),日本日立公司;D2 PHASER型X射线衍射(X-ray diffraction,XRD)仪,德国布鲁克AXS有限公司;Xeuss 3.0 C小角X射线散射仪,法国Xenocs S.A.S公司;NEXUS-870衰减全反射傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)仪,美国Thermo Nicolet科学仪器有限公司;DSC3+差示扫描量热(differential scanning calorimetry,DSC)仪,瑞士梅特勒-托利多公司;DAWN HELEOS 8+高效凝胶尺寸排阻色谱、多角度激光检测器和示差检测器,美国怀雅特技术公司。
1.3 实验方法
1.3.1 高直链玉米淀粉共挤压复合物的制备
使用搅拌机将高直链玉米淀粉与乳化剂混合,添加量为1%(质量分数,下同),将混合物倒入喂料器中,设置喂料速度为5 kg/h,液体喂料速度为2.5 kg/h,螺杆转速150 r/min,从喂料区到挤出区共6个区域,喂料区为开放式不设温度,第Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ区域温度分别设为50、70、85、85、50 ℃。将挤出的复合物在40 ℃鼓风干燥箱中干燥12 h,将复合物研磨,过80目筛装入密封袋中,用于后续分析。挤压机参数为:双螺杆,单个螺杆直径20 mm,L/D为40∶1,模具直径为1 mm,切刀转速为1 200 r/min。
1.3.2 SEM观察微观结构
SEM用于分析微观结构。用牙签将样品粉末涂抹在双面碳涂层胶带表面,并喷涂一层薄金膜。微观照片在加速电压为3.0 kV的条件下,以不同的放大倍率拍摄。
1.3.3 X射线散射分析
样品的X射线散射图谱使用X射线衍射仪测定。测试条件为:40 kV和40 mA Cu-K-α辐射,扫描范围为4°~35°,扫描步频为0.05 °/s,结晶度的计算如公式(1)所示,相对结晶度通过Jade 6.0软件计算。
结晶度![]()
(1)
1.3.4 小角XRD分析
样品的层状结构通过小角X射线散射系统测定。按m(样品粉末)∶m(超纯水)=2∶3的比例混合。制备的样品在室温下静置12 h以达到平衡。随后,将淀粉浆液转移到样品池中,测试条件为:单色Cu-K-α射线,管压40 kV,管流50 mA,曝光时间3 min。此外,使用空气散射作为背景[8],分析时统一扣除空气背景。通过XSACT软件分析获得了二维散射图案,并将其转换为一维散射曲线(0.01 Å-1<q<0.20 Å-1)。这里的q(nm-1)表示散射向量,定义为q=4πsinθ/λ(λ=1.54 Å;2θ为散射角)。使用XSACT软件(版本2.7.1)进行数据收集和处理。
1.3.5 FTIR分析
使用衰减全反射(attenuated total reflection,ATR)FTIR仪测定样品短程有序结构,测试条件为:扫描范围400~4 000 cm-1,分辨率4 cm-1,扫描次数32。以空气作为背景,首先采集样品的光谱数据,然后扣除背景信号,得到最终的光谱图。使用Omnic软件对1 200~800 cm-1的光谱做去卷积处理,设定半峰宽为55 cm-1,增强因子为2.5。得到1 047、1 022、995 cm-1处的峰高,通过计算1 047 cm-1/1 022 cm-1和995 cm-1/1 022 cm-1峰高比值来评估样品短程有序结构的变化。
1.3.6 热特性分析
样品的热特性通过DSC仪进行分析。按m(样品)∶m(去离子水)=1∶3比例混合,放入铝坩埚中并封闭,在4 ℃下静置24 h以达到水分平衡,然后进行DSC分析。样品从30 ℃加热至130 ℃,升温速率为10 ℃/min,使用空坩埚作为参考。通过计算吸热焓(ΔH)以及热转变参数,包括起始温度(To)、峰值温度(Tp)和结束温度(Tc)[9]。
1.3.7 体外消化性测定
1.3.7.1 体外消化实验
将0.1 g样品分散在5 mL醋酸钠缓冲液(pH值=5.2,0.5 mol/L)中。将样品在沸水浴中加热20 min 后,置于37 ℃孵育10 min。加入5 mL酶溶液(α-淀粉酶200 U/mL和糖化酶200 U/mL)。反应液在37 ℃下振荡孵育,振荡速度为180 r/min。在0、5、10、15、20、30、45、60、90、120、180 min时取样。取0.1 mL 反应液加入0.9 mL无水乙醇以终止反应,并以4 000 r/min 离心10 min,利用D-葡萄糖(GOPOD法)试剂盒测定葡萄糖释放量。RDS、SDS和RS的计算如公式(2)~公式(4)所示:
(2)
(3)
RS/%=100-RDS-SDS
(4)
式中:G0表示游离葡萄糖的含量;G20和G120分别表示在水解20 min和120 min后释放的葡萄糖量;TS代表总淀粉含量;因子0.9(162/180)为葡萄糖转化系数。
1.3.7.2 一级动力学拟合
淀粉消化曲线拟合为一阶动力学方程,如公式(5)所示:
Ct=(C∞-C0)×(1-e-kt)+C0
(5)
式中:Ct和C0分别表示t min和0 min时刻的淀粉消化比;C∞表示消化完成时淀粉水解速率;k为淀粉消化速率系数。
对数斜率(logarithm-of-slope,LOS)分析方法有助于识别不同的消化相,如变换后的方程如公式(6)所示:
(6)
采用非线性最小二乘拟合方法计算k和C∞的值[10]。
1.3.7.3 并联与顺序动力学模型(combination of parallel and sequential kinetic model,CPS)
假设存在2个不同的可消化组分C1(t)和C2(t),并且每个消化过程都遵循伪一级动力学,下面的公式(7)概括了t时刻淀粉消化总量Ct。
Ct=C0+(C1∞)×(1-e-k1t)+if(t≥t2 start,((C2∞)×(1-e-k2×(t-t2 start))),0)
(7)
式中:C0表示0时刻消化的淀粉;C1∞和C2∞分别表示可消化组分1和2在无限时间内消化的最大淀粉量;k1和k2分别为可消化组分1和2的速率常数;t2 start表示慢消化部分的消化起始时间。
1.3.7.4 估计血糖指数(estimated glycemic index,eGI)
水解指数(hydrolysis index,HI)计算为样品淀粉水解曲线下的面积(area under the curve,AUC)与葡萄糖相应AUC的百分比。血糖指数的估算如公式(8)所示[11]:
eGI=0.549×HI+39.71
(8)
1.4 数据处理
数据作图采用Origin(2025),使用SPSS(23.0)对数据进行方差分析(analysis of variance,ANOVA)和邓肯(Duncan)检验(P<0.05),所有实验进行3次,结果以“平均值±标准差”的形式呈现。
2 结果与分析
2.1 SEM分析微观结构
淀粉颗粒的变化通过SEM显示。样品的形态如图1所示。未处理的高直链玉米淀粉颗粒呈球形、棒状或丝状,表面相对光滑。挤出后,高直链玉米淀粉经历了部分糊化,其结构被破坏并发生聚集。由于热效应和剪切应力的影响,损坏了颗粒,挤出后的淀粉颗粒结构转变为粗糙、不规则的结构,可能有溶解的淀粉附着在挤出颗粒的表面[12],形成致密的颗粒结构,帮助抵抗水分和淀粉酶的渗透。淀粉颗粒被破坏并积累了一些碎片,这种形态特征可能是由淀粉糊化和交联作用引起的[13]。不同乳化剂与高直链玉米淀粉挤出后在外观形貌上并无明显差异。

A-高直链玉米淀粉(500×);a-高直链玉米淀粉(3 000×);B-挤压高直链玉米淀粉(500×);b-挤压高直链玉米淀粉(3 000×);C-高直链玉米淀粉+1%单甘脂共挤压(500×);c-高直链玉米淀粉+1%单甘脂共挤压(3 000×);D-高直链玉米淀粉+1%大豆卵磷脂共挤压(500×);d-高直链玉米淀粉+1%大豆卵磷脂共挤压(3 000×);E-高直链玉米淀粉+1%柠檬酸脂肪酸甘油酯共挤压(500×);e-高直链玉米淀粉+1%柠檬酸脂肪酸甘油酯共挤压(3 000×)
图1 不同乳化剂与高直链玉米淀粉共挤压的SEM图
Fig.1 SEM image of different emulsifiers extruded with high amylose maize starch
2.2 复合物的晶型和结晶度分析
使用X射线散射仪来研究淀粉结构的变化。样品的X射线衍射图谱和相对结晶度如图2所示。HAMS在2θ=5.8°、17.3°、20.2°、22.1°、24.1°处出现峰,呈现典型的B型晶体。挤出后,衍射峰发生了变化,V型峰出现在2θ≈7.8°、13.3°、20.2°处,形成尖锐的峰,这是典型的V型结晶的特征峰[14]。B型晶体的强度减弱,出现了V型晶体,表明结晶结构被破坏并形成了新的结构。挤压高直链玉米淀粉(extruded high amylose maize starch,EHAMS)样品出现了V型晶体,已有研究表明,V型衍射峰可能是由于直链淀粉与内源性脂质之间形成复合物所致[15]。相对结晶度的结果表明,挤出破坏了淀粉的晶体结构,促进了V型复合物的形成。B型晶体呈双螺旋结构排列。含有SL的样品表现出较高的B型晶体相对结晶度,这可能与它们在挤出后促进淀粉退化中双螺旋的形成有关。添加MGF时,V型的相对结晶度最高,表明V型结构的形成较多。推测直链淀粉通过疏水相互作用与疏水性客体分子构建稳定的复合物[16]。
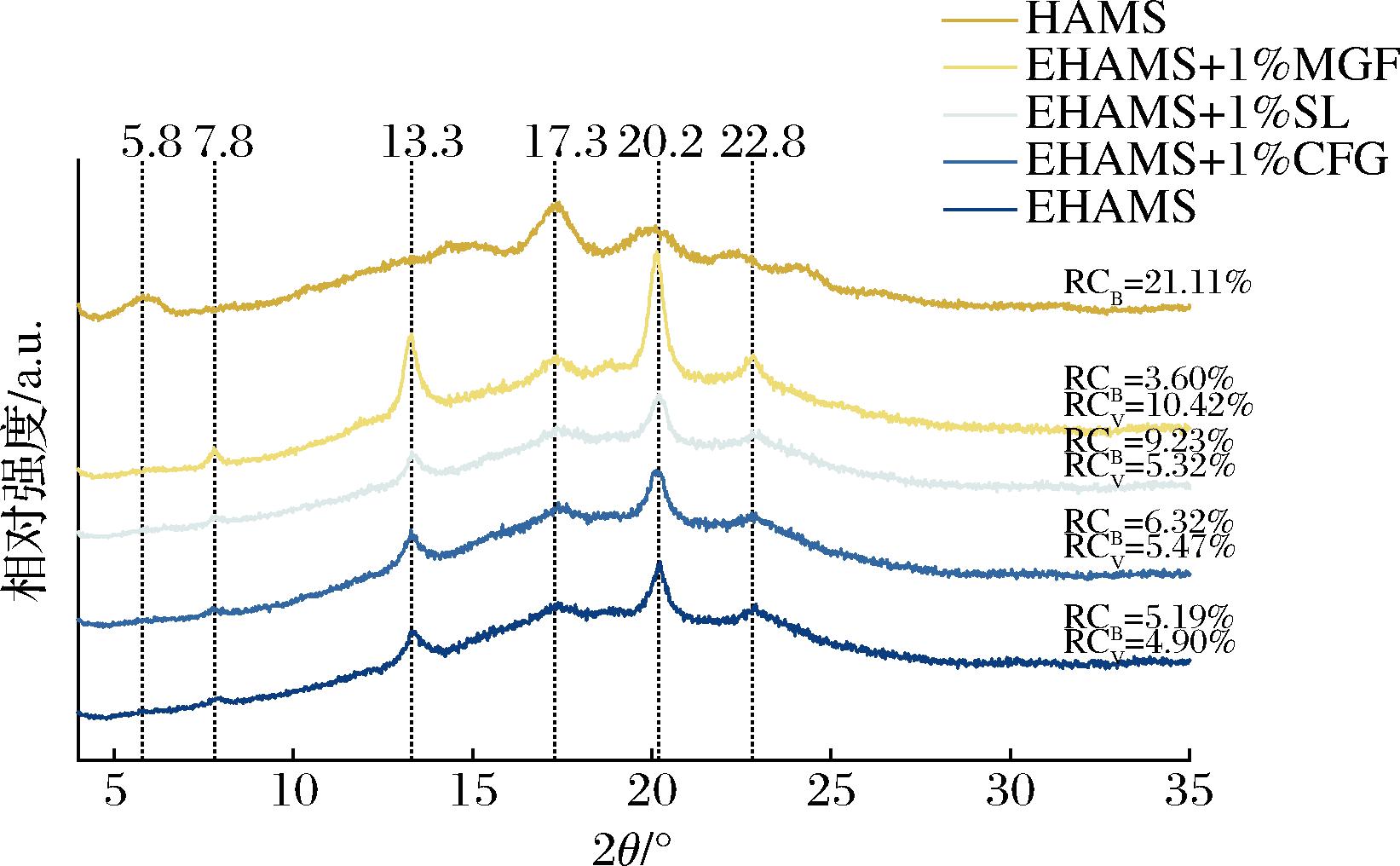
图2 不同乳化剂与高直链玉米淀粉共挤压复合物的XRD图谱
Fig.2 XRD pattern of different emulsifiers extruded with high amylose maize starch
注:RC:相对结晶度;RCB:B型相对结晶度;RCV:V型相对结晶度。
2.3 复合物的半晶体结构分析
淀粉半晶体结构通过小角XRD进行表征,这些结构由无定形和晶体层的交替堆叠组成,如图3所示。淀粉的分形结构通常通过分形维数来评估,该维度通过幂律散射方程计算:I~q^-α,其中I表示散射强度,α是用于估算分形维数的指数。淀粉的紧密性和有序度可以通过评估散射物体结构的分形维数来确定。淀粉的分形特性可分为2个部分:质量分形(Dm)和表面分形(Ds)。对于质量分形,Dm=α(1<α<3),代表结构的紧密性。Dm值越高,结构密度越大。对于表面分形,分形维数Ds由公式给出:Ds =6-α,其中α的取值范围为2~3。在这种情况下,Ds值接近2表示表面更光滑[15]。如表1所示,挤出改变了样品的分形维数。HAMS表现为表面分形,表面较光滑。挤出后,由于淀粉结构的破坏以及客体分子与淀粉之间的相互作用,表面变得更加粗糙,结构相较于HAMS变得松散。EHAMS+1%SL的Dm值较EHAMS大,表明其具有更紧凑的结构。相比之下,其他样品Dm值较小,表明这些物质抑制了紧凑结构的形成。
表1 不同乳化剂与高直链玉米淀粉共挤压复合物的层状参数和分形维数
Table 1 Lamellar parameters and fractal dimensions of different emulsifiers extruded with high amylose maize starch
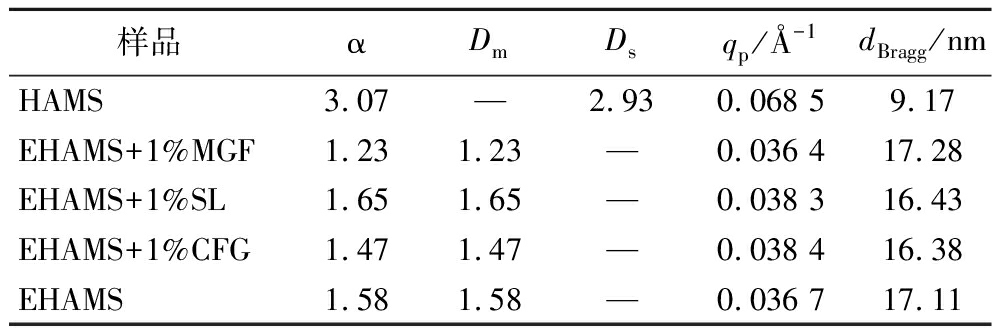
样品αDmDsqp/Å-1dBragg/nmHAMS3.07—2.930.068 59.17EHAMS+1%MGF1.231.23—0.036 417.28EHAMS+1%SL1.651.65—0.038 316.43EHAMS+1%CFG1.471.47—0.038 416.38EHAMS1.581.58—0.036 717.11
注:α为分形维数指数;Dm为质量分形;Ds为表面分形;—表示不属于该分形;qp为肩状峰散射矢量大小;dBragg为晶面间距。
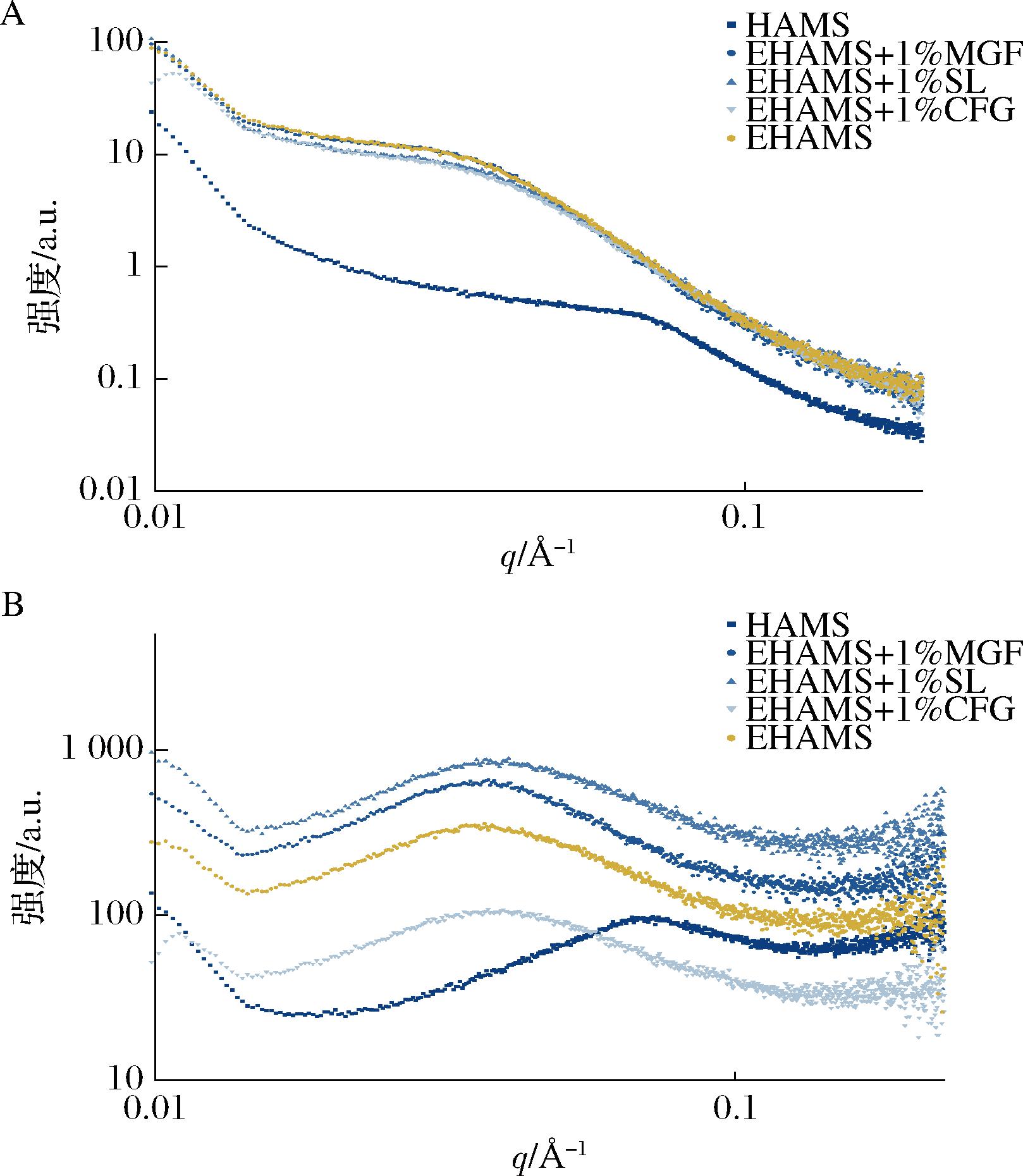
A-小角X射线散射图谱;B-洛伦兹修正的图谱
图3 不同乳化剂与高直链玉米淀粉共挤压复合物的小角XRD图谱和洛伦兹修正的图谱
Fig.3 Small angle X-ray scattering and Lorentz correction patterns of samples
经过Lorentz修正后,可以强调肩峰。使用Woolf-Bragg方程(d=2π/q)来确定有序纳米尺度聚集体的尺寸。如表1所示,HAMS的散射峰出现在高q区域(约q=0.068 Å-1),对应的dBragg值为9.17 nm,与其他研究中淀粉中具有9~10 nm周期性的半晶体层结构一致[17]。挤压后,散射峰移到q=0.035 Å-1-0.039 Å-1,表明半晶体层结构的厚度增加。基于淀粉的三相模型,除了结晶物质外,淀粉还包含2种无定形成分:(Ⅰ)无定形背景区(主要由直链淀粉组成)和(Ⅱ)无定形层区(主要由支链淀粉组成)。由于其接近结晶层结构,后者通常会被压缩,特别是在半晶体层结构的过渡层(结晶层结构与无定形层结构之间的界面区)[18]。因此,挤出可能导致双螺旋结构的某些尾端解离,并扩展无定形层结构[19]。HAMS挤压后,EHAMS的dBragg值为17.11 nm,说明其层状结构膨胀,结合图2其结晶峰的数量和面积下降,可能原因是无定型层结构扩展,导致dBragg值增大。添加乳化剂共挤压后,EHAMS+1%MGF的dBragg值最大,可能是MGF作为配体,形成的V型复合物疏水核心较长,dBragg值增大,图2其V型结晶峰最为明显。
2.4 复合物的短程有序性分析
如图4所示,红外光谱图可以分为3个区域:800~1 500 cm-1(指纹区域),2 800~3 000 cm-1(C—H伸缩振动区域),3 000~3 500 cm-1(O—H伸缩振动区域)。在2 929 cm-1附近的吸收峰与C—H键的非对称伸缩振动相关,而1 648 cm-1附近的峰则来源于淀粉中的结合水[20]。FTIR光谱还用于分析短程有序结构。通常,1 047 cm-1和1 022 cm-1的光谱带被认为分别代表淀粉的结晶区和无定形区[21]。因此,1 047 cm-1/1 022 cm-1的吸收比值用于估算淀粉的短程有序度。995 cm-1处的吸收峰与淀粉中分子间氢键的形成有关。
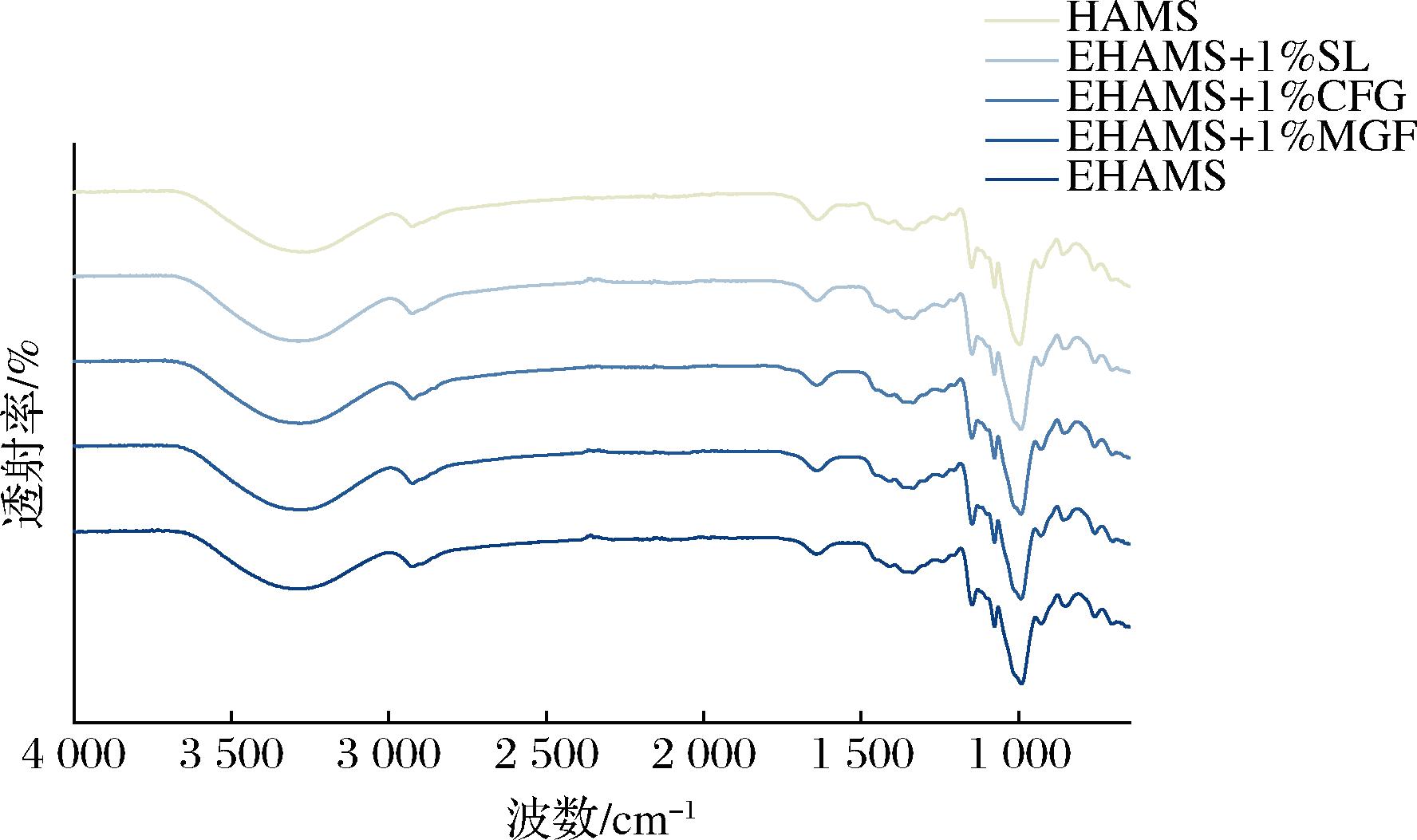
图4 不同乳化剂与高直链玉米淀粉共挤压复合物的红外光谱图
Fig.4 ATR-FTIR spectra of different emulsifiers extruded with high amylose maize starch
基于解卷积后的光谱(图5)中1 047、1 022和995 cm-1的峰值强度,计算得到了R1 047/1 022(短程有序度)和R995/1 022(双螺旋度)比值,数据见表2,这里,短程有序度代表淀粉中结晶区与无定形区的比值,而双螺旋度不仅代表结晶相中的双螺旋结构,还表示无定形区域中的短程分子有序度。挤出后,所有样本的短程有序度和双螺旋度均降低,表明结晶区被破坏,无定形区增多,这与X射线散射分析结果一致。添加3种乳化剂的样品中,EHAMS+1%SL的短程有序度和双螺旋度最高,表明添加SL的样品具有更紧凑的结构和更好的有序性。含有其他乳化剂的样品没有显著增加短程有序性,表明这些物质在退化过程中阻碍了淀粉分子的交联。
表2 不同乳化剂与高直链玉米淀粉共挤压复合物的1 045 cm-1/1 022 cm-1和995 cm-1/1 022 cm-1的吸收比值
Table 2 the absorbance ratios of 1 045 cm-1/1 022 cm-1 and 995 cm-1/1 022 cm-1 for different emulsifiers extruded with high amylose maize starch

样品有序度(1 047 cm-1/1 022 cm-1)双螺旋度(995 cm-1/1 022 cm-1)HAMS1.82±0.01a1.72±0.09aEHAMS+1%MGF1.44±0.03d1.23±0.02dEHAMS+1%SL1.49±0.04bc1.28±0.01bcdEHAMS+1%CFG1.43±0.02d1.25±0.02cdEHAMS1.49±0.05bc1.32±0.04bc
注:不同小写字母表示差异显著(P<0.05)(下同)。
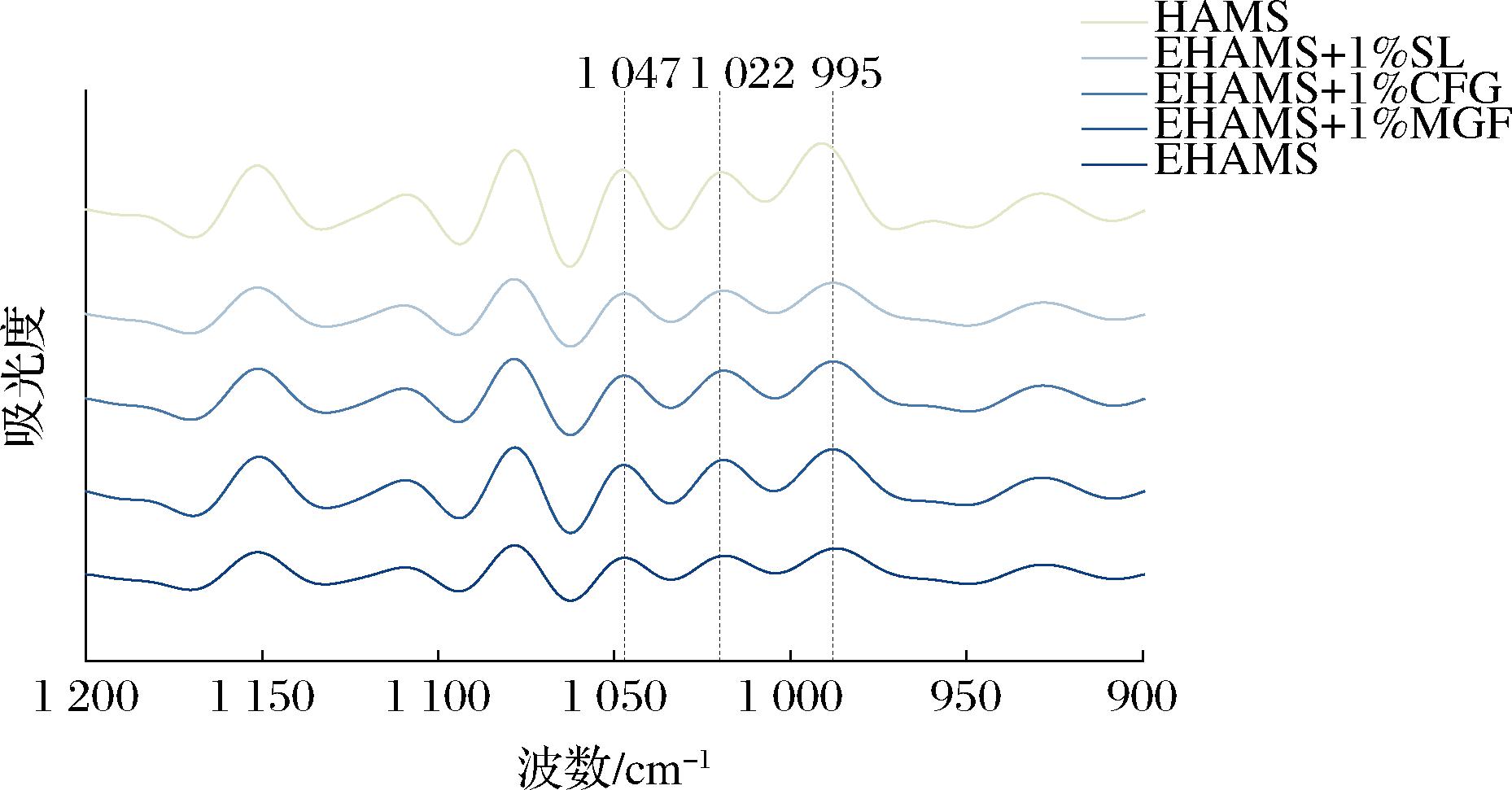
图5 不同乳化剂与高直链玉米淀粉共挤压复合物的红外光谱解卷积图
Fig.5 Deconvolution of ATR-FTIR spectra of different emulsifiers extruded with high amylose maize starch
2.5 复合物的热力学特性分析
复合物的热特性如表3所示,挤出后糊化温度的升高表明挤出处理显著增强了体系的热稳定性。糊化温度的变化可能与淀粉分子的构象和分布差异以及分子成分内部组织的不同有关[22]。ΔH的降低表明淀粉在挤出过程中经历了预糊化,ΔH反映了淀粉颗粒内分子间和分子内螺旋氢键断裂时的能量变化[23],挤出引起的淀粉颗粒结构破坏可以解释挤出后ΔH的降低。HAMS的ΔH最高,因为其糊化度最低,需要最多的能量才能破坏其结构。EHAMS+1%SL和EHAMS+1%CFG的ΔH最低。这可能是由于添加SL和CFG影响了淀粉分子间氢键的形成,导致破坏这些氢键所需的能量降低。红外光谱分析中的结果也支持这一点,显示出较低的双螺旋度。
表3 不同乳化剂与高直链玉米淀粉共挤压复合物的热力学参数
Table 3 The thermal properties of different emulsifiers extruded with high amylose maize starch
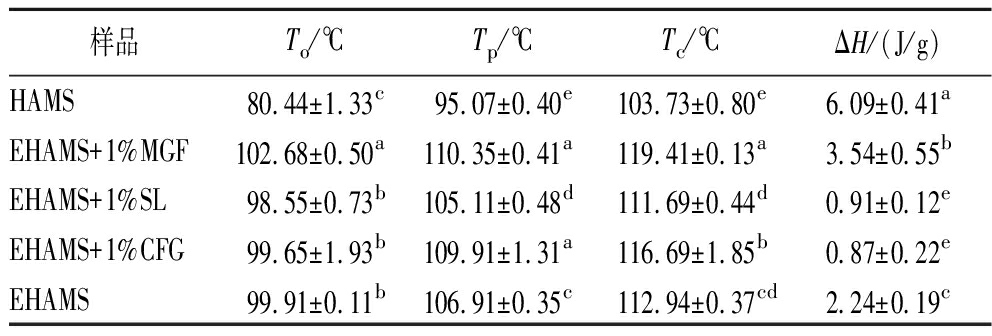
样品To/℃Tp/℃Tc/℃ΔH/(J/g)HAMS80.44±1.33c95.07±0.40e103.73±0.80e6.09±0.41aEHAMS+1%MGF102.68±0.50a110.35±0.41a119.41±0.13a3.54±0.55bEHAMS+1%SL98.55±0.73b105.11±0.48d111.69±0.44d0.91±0.12eEHAMS+1%CFG99.65±1.93b109.91±1.31a116.69±1.85b0.87±0.22eEHAMS99.91±0.11b106.91±0.35c112.94±0.37cd2.24±0.19c
注:To为起始温度;Tp为峰值温度;Tc为结束温度;ΔH为吸热焓。
2.6 复合物的体外消化性分析
对于均匀系统,简单的一阶动力学模型可能足以描述整个消化曲线,从而得出一个单一的速率常数。然而,这样的模型不足以揭示具有多个可消化部分(例如,快速和慢速消化)的淀粉消化特征的机理细节。因此,提出了对数斜率模型(logarithmic slope model,LOS),用以区分消化过程中的不同阶段。然而,该模型仅适用于拟合具有顺序可消化部分的淀粉消化曲线。消化系统可能还包括顺序和并行模式的组合,称为“CPS动力学”。拟合这种消化系统并识别消化模式(顺序、并行或两者的结合)对于阐明淀粉消化特性及研究淀粉的结构-性质关系非常有帮助[10]。
不同样品的消化曲线如图6所示,呈指数衰减模式。在最初的20 min内,淀粉的消化量迅速增加,随后进入较慢的消化阶段,直到达到最大消化水平的大约40%。这表明消化过程遵循一阶动力学。不同挤压复合物的最大消化水平差异不大,但消化速率不同。不同样品的LOS图如图7所示。实验噪声的LOS点已从线性拟合中排除。大多数LOS图显示出不连续的线性关系,表明消化过程中存在2种不同的消化部分(快速消化和慢速消化),每个阶段的斜率在不同样品之间有显著差异。
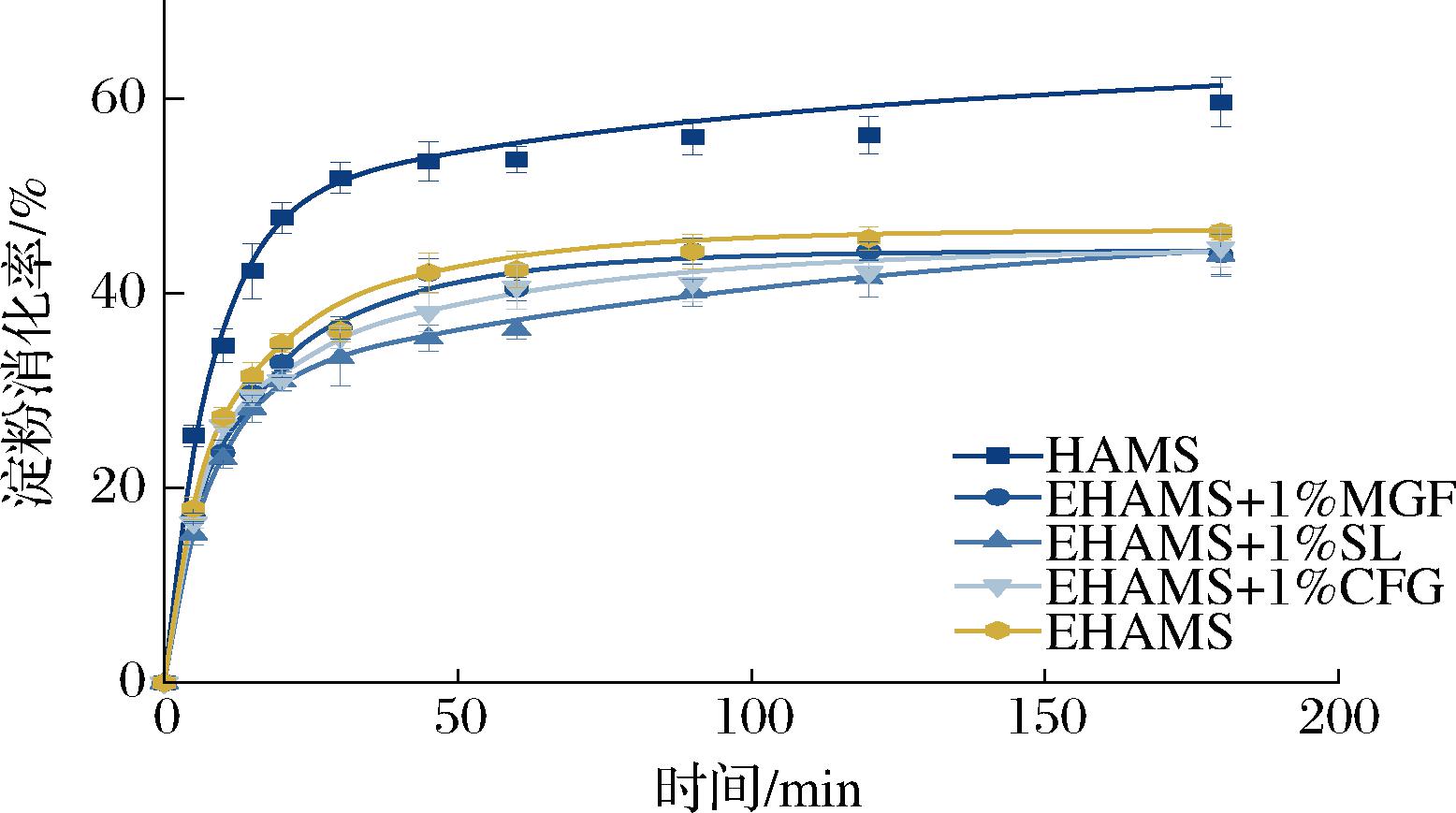
图6 不同乳化剂与高直链玉米淀粉共挤压复合物的淀粉消化曲线
Fig.6 Starch digestion curves of different emulsifiers extruded with high amylose maize starch
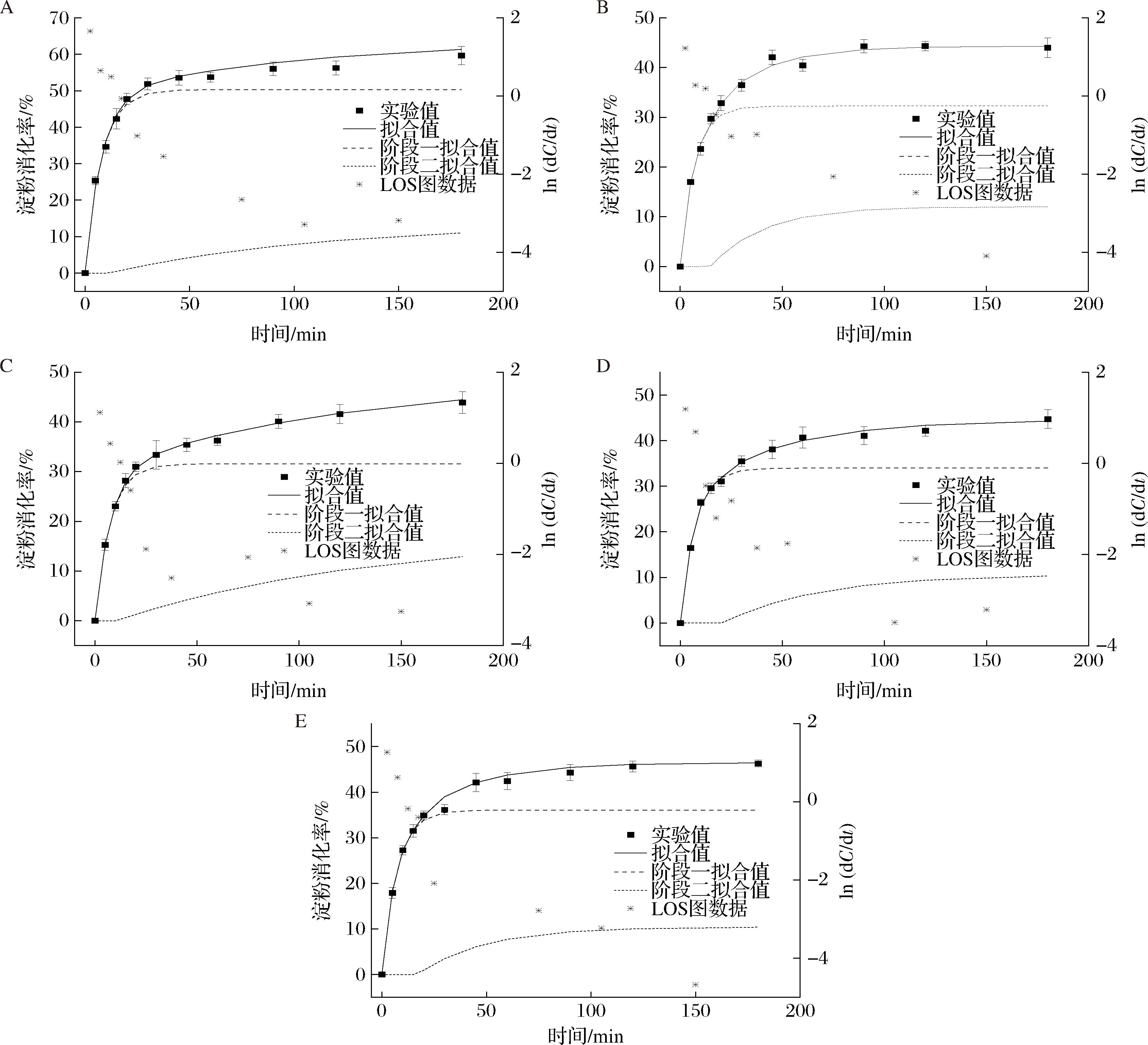
A-高直链玉米淀粉;B-高直链玉米淀粉+1%单甘脂共挤压;C-高直链玉米淀粉+1%大豆卵磷脂共挤压;D-高直链玉米淀粉+1%柠檬酸脂肪酸甘油酯共挤压;E-挤压高直链玉米淀粉
图7 不同乳化剂与高直链玉米淀粉共挤压复合物的LOS/CPS动力学模型
Fig.7 The kinetic model of LOS/CPS of different emulsifiers extruded with high amylose maize starch
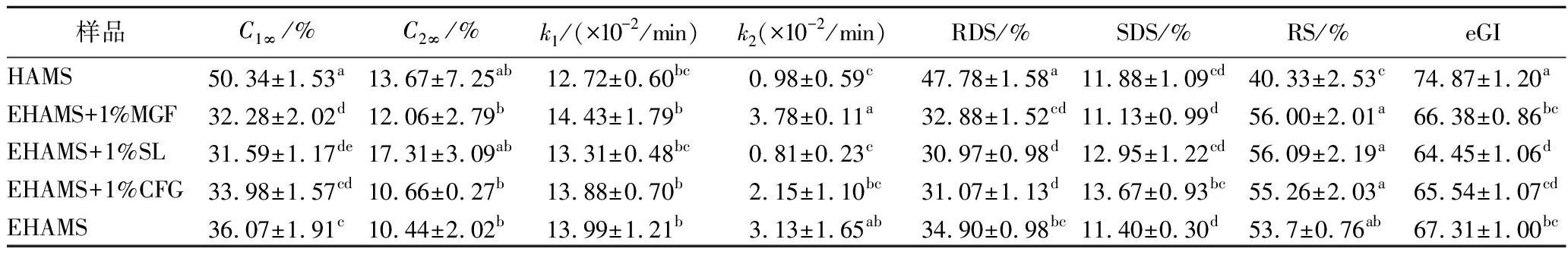
为了分析顺序和并行消化模式,采用CPS模型拟合了各种挤压玉米淀粉的消化曲线(如图7所示)。该模型准确地再现了整个消化曲线。这表明可消化组分1和2并不是同时开始,而是消化过程遵循顺序和并行模式的组合。可消化组分1在大约20 min 内迅速达到最大消化水平,而可消化组分2在其完成后开始占主导地位,表现出20 min后的缓慢增加。这是因为在淀粉消化的初始阶段,淀粉颗粒的外层直接与酶接触,从而导致快速消化,而中间和内部区域仅部分暴露于酶,因此消化较慢[24]。这可以合理地解释为快速消化的淀粉在慢速消化淀粉表面形成保护层,当这一保护层破裂时,加速了慢速消化淀粉的消化速率。CPS动力学模型拟合参数如表4所示。挤压造成C1∞、C2∞减小,这造成了样品RDS减少,SDS和RS的上升,可以明显降低样品的eGI。添加乳化剂会造成C1∞进一步减少,C2∞的回升,说明组分1可消化的最大淀粉量下降,组分2可消化的最大淀粉量上升,RDS下降,SDS上升进一步说明了此结果,添加3种乳化剂形成复合物的RS含量并没有明显的差异。对添加乳化剂的样品综合C1∞、C2∞、k1和k2考虑,添加SL的样品的k1和k2最低,这说明在整个消化过程中,其消化曲线更平缓,有利于葡萄糖的缓慢释放,eGI值较低。而添加MGF的样品,其形成的V型结构较多(V型相对结晶度最大),RS含量较高,但其k1和k2较大,消化速率较快,不利于葡萄糖的缓慢释放,造成其eGI值较大。
表4 不同乳化剂与高直链玉米淀粉共挤压复合物的CPS动力学模型拟合参数、RDS、SDS、RS含量和eGI
Table 4 CPS kinetics model fitting parameters,RDS,SDS,RS contents,and eGI for different emulsifiers extruded with high amylose maize starch
样品C1∞/%C2∞/%k1/(×10-2/min)k2(×10-2/min)RDS/%SDS/%RS/%eGIHAMS50.34±1.53a13.67±7.25ab12.72±0.60bc0.98±0.59c47.78±1.58a11.88±1.09cd40.33±2.53c74.87±1.20aEHAMS+1%MGF32.28±2.02d12.06±2.79b14.43±1.79b3.78±0.11a32.88±1.52cd11.13±0.99d56.00±2.01a66.38±0.86bcEHAMS+1%SL31.59±1.17de17.31±3.09ab13.31±0.48bc0.81±0.23c30.97±0.98d12.95±1.22cd56.09±2.19a64.45±1.06dEHAMS+1%CFG33.98±1.57cd10.66±0.27b13.88±0.70b2.15±1.10bc31.07±1.13d13.67±0.93bc55.26±2.03a65.54±1.07cdEHAMS36.07±1.91c10.44±2.02b13.99±1.21b3.13±1.65ab34.90±0.98bc11.40±0.30d53.7±0.76ab67.31±1.00bc
注:C1∞和C2∞分别表示可消化组分1和2在无限时间内消化的最大淀粉量;k1和k2分别为可消化组分1和2的速率常数。
3 结论
本研究评估了不同乳化剂对高直链淀粉挤出复合物的结构特性、理化特性和体外淀粉消化率的影响。挤压显著破坏了淀粉颗粒的微观结构,导致大量无定形片状物和不完全的淀粉颗粒。相关实验结果表明,添加乳化剂共挤压的淀粉晶体结构为B+V型,添加单甘脂挤出的复合物形成的V型结构最多,但会造成淀粉结构松散、分子尺寸差异较大、短程有序性和双螺旋度较小,表现为抗性淀粉含量较多,但消化速率较大;而添加大豆卵磷脂挤出的复合物的淀粉结构较为紧密,分子尺寸差异较小、短程有序性和双螺旋度较大,表现为消化速率较小。共挤压复合物的消化模式遵循顺序和并行模式的组合,添加3种乳化剂共挤压的复合物RS含量并没有明显的差异。添加大豆卵磷脂与高直链玉米淀粉共挤压的复合物,在整个消化过程中,其消化曲线更平缓,有利于葡萄糖的缓慢释放,eGI值较低,使其更适合低消化性食品。本研究结果可为挤压淀粉产品和低血糖生成指数类食品的进一步开发提供有价值的参考。
[1] 刘飞雁.杂粮挂面淀粉消化特性的影响因素及机制研究[D].无锡:江南大学,2021.LIU F Y.Study on influencing factors and mechanism of starch digestibility of coarse cereal dried noodles[D].Wuxi:Jiangnan University,2021.
[2] BIRT D F,BOYLSTON T,HENDRICH S,et al.Resistant starch:Promise for improving human health[J].Advances in Nutrition,2013,4(6):587-601.
[3] BENDIKS Z A,KNUDSEN K E B,KEENAN M J,et al.Conserved and variable responses of the gut microbiome to resistant starch type 2[J].Nutrition Research,2020,77:12-28.
[4] 詹锦玲,王瑞,田耀旗.高直链玉米淀粉配合体的抗消化特性与晶体结构[J].食品与发酵工业,2016,42(9):64-67.ZHAN J L,WANG R,TIAN Y Q.Resistant properties and crystalline structure of high amylose corn starch-emulsifier complexes[J].Food and Fermentation Industries,2016,42(9):64-67.
[5] KAMAU E H,NKHATA S G,AYUA E O.Extrusion and nixtamalization conditions influence the magnitude of change in the nutrients and bioactive components of cereals and legumes[J].Food Science &Nutrition,2020,8(4):1753-1765.
[6] MORALES-S NCHEZ E,CABRERA-RAM
NCHEZ E,CABRERA-RAM REZ A H,GAYT
REZ A H,GAYT N-MART
N-MART NEZ M,et al.Heating-cooling extrusion cycles as a method to improve the physicochemical properties of extruded corn starch[J].International Journal of Biological Macromolecules,2021,188:620-627.
NEZ M,et al.Heating-cooling extrusion cycles as a method to improve the physicochemical properties of extruded corn starch[J].International Journal of Biological Macromolecules,2021,188:620-627.
[7] SINGH S,GAMLATH S,WAKELING L.Nutritional aspects of food extrusion:A review[J].International Journal of Food Science &Technology,2007,42(8):916-929.
[8] ZHANG Z N,ZHANG M Q,ZHANG B,et al.Radio frequency energy regulates the multi-scale structure,digestive and physicochemical properties of rice starch[J].Food Bioscience,2022,47:101616.
[9] HAN X M,XING J J,HAN C,et al.The effects of extruded endogenous starch on the processing properties of gluten-free Tartary buckwheat noodles[J].Carbohydrate Polymers,2021,267:118170.
[10] LI C,HU Y M.Combination of parallel and sequential digestion kinetics reveals the nature of digestive characteristics of short-term retrograded rice starches[J].Food Hydrocolloids,2020,108:106071.
[11] GO I I,GARCIA-ALONSO A,SAURA-CALIXTO F.A starch hydrolysis procedure to estimate glycemic index[J].Nutrition Research,1997,17(3):427-437.
I I,GARCIA-ALONSO A,SAURA-CALIXTO F.A starch hydrolysis procedure to estimate glycemic index[J].Nutrition Research,1997,17(3):427-437.
[12] DURA A,B ASZCZAK W,ROSELL C M.Functionality of porous starch obtained by amylase or amyloglucosidase treatments[J].Carbohydrate Polymers,2014,101:837-845.
ASZCZAK W,ROSELL C M.Functionality of porous starch obtained by amylase or amyloglucosidase treatments[J].Carbohydrate Polymers,2014,101:837-845.
[13] JAFARI M,KOOCHEKI A,MILANI E.Effect of extrusion cooking on chemical structure,morphology,crystallinity and thermal properties of sorghum flour extrudates[J].Journal of Cereal Science,2017,75:324-331.
[14] LIU P F,GAO W,ZHANG X L,et al.Physicochemical properties of pea starch-lauric acid complex modified by maltogenic amylase and pullulanase[J].Carbohydrate Polymers,2020,242:116332.
[15] JIANG H,MCCLEMENTS D J,DAI L,et al.Effects of moisture content and retrogradation on structure and properties of indica rice flour and starch gels[J].Food Hydrocolloids,2024,150:109657.
[16] CHI C D,LI X X,HUANG S X,et al.Basic principles in starch multi-scale structuration to mitigate digestibility:A review[J].Trends in Food Science &Technology,2021,109:154-168.
[17] TANG J Y,ZHOU J W,ZHOU X Y,et al.Rearranged supramolecular structure of resistant starch with polymorphic microcrystals prepared in high-solid enzymatic system[J].Food Hydrocolloids,2022,124:107215.
[18] CAMERON R E,DONALD A M.A small-angle X-ray-scattering study of the annealing and gelatinization of starch[J].Polymer,1992,33(12):2628-2635.
[19] WANG H W,DING J T,XIAO N Y,et al.Insights into the hierarchical structure and digestibility of starch in heat-moisture treated adlay seeds[J].Food Chemistry,2020,318:126489.
[20] DONG H M,ZHANG Q,GAO J,et al.Preparation and characterization of nanoparticles from cereal and pulse starches by ultrasonic-assisted dissolution and rapid nanoprecipitation[J].Food Hydrocolloids,2022,122:107081.
[21] MA M T,ZHANG Y,CHEN X J,et al.Microwave irradiation differentially affect the physicochemical properties of waxy and non-waxy hull-less barley starch[J].Journal of Cereal Science,2020,95:103072.
[22] ZHANG X,CHEN H X,ZHANG N,et al.Extrusion treatment for improved physicochemical and antioxidant properties of high-molecular weight polysaccharides isolated from coarse tea[J].Food Research International,2013,53(2):726-731.
[23] XING B,TENG C,SUN M H,et al.Effect of germination treatment on the structural and physicochemical properties of quinoa starch[J].Food Hydrocolloids,2021,115:106604.
[24] ZHANG Z,ZHU M L,XING B,et al.Effects of extrusion on structural properties,physicochemical properties and in vitro starch digestibility of Tartary buckwheat flour[J].Food Hydrocolloids,2023,135:108197.