枸杞(Lycium chinense Miller),茄科枸杞属多年生木本植物,起源于中国,是中国西北地区种植最广泛、经济最重要的水果作物之一[1]。枸杞是药食同源的营养保健型蔬菜和名贵中药,含有丰富的类胡萝卜素、多糖、维生素、酚类、微量元素和矿物质[2]。
酵素,常被称作“酶”,实际上是一种由多种有效物质构成的化合物。它主要是在水果或蔬菜等原料的发酵过程中,借助多种有益微生物的作用而生成。酵素中富含多种营养成分,包括纤维素、酶、矿物质以及次生代谢产物等。这些成分赋予了酵素多种保健功能,如抗衰老、抗菌消炎、净化血液以及增强机体免疫力等作用[3]。
酵素风味(如果香、酸味、醇香等)的研究在提升产品感官品质与消费者接受度等方面具有重要意义。例如,酵素中酯类(如乙酸乙酯)和醛类(如己醛)的平衡赋予其独特的果香与清新感,避免过度酸涩或异味,可显著增强市场竞争力[4]。GC-MS是对风味物质进行评价的传统分析方法。然而,相较于GC-MS,另一种优于现有传统分析方法的方法是气相色谱-离子迁移率光谱法(gas chromatography-ion mobility spectrometry,GC-IMS),GC-IMS在多场景分析中展现出独特优势[5],包括检测效率高、分析成本低、良好的选择性、针对性高和操作简单,GC-IMS技术还可以获得更清晰的挥发性风味化合物含量的图像,通过外标法更准确地定性分析等,这些特性使得GC-IMS成为一种极具优势的分析工具[6]。作为一种新兴的食品检测方法,GC-IMS在食品行业具有无限的应用前景。
枸杞富含多糖、类胡萝卜素、黄酮等成分,发酵后可通过微生物代谢产生小分子肽、有机酸等新活性物质,提升抗氧化、抗炎或免疫调节能力[7]。传统枸杞食用方式吸收率有限,发酵可分解大分子物质(如纤维素),释放更多可吸收的营养成分,研究可揭示其增效机制,为功能性食品开发提供依据,研究其生物利用度变化对优化产品形式(如口服液、胶囊)有指导意义[8]。枸杞酵素的研究近年来在多个领域取得显著进展,涉及发酵工艺优化、活性成分解析、功能机制探索及产业化应用等,而枸杞酵素的相关产品虽然具有巨大潜力,但是对其的研究却相对较少。
本文以枸杞为主要研究对象,采用自然发酵的方法,利用GC-IMS技术对枸杞酵素在发酵过程中所表现出的特性及其风味物质进行了详细分析。研究深入探讨了枸杞酵素经过自然发酵后在理化性质、营养成分、抗氧化能力和挥发性物质方面的变化。这项研究旨在为枸杞产品的开发提供新的视角及理论基础,助力其在市场上的应用和推广。
1 材料与方法
1.1 材料与试剂
“宁农杞18号”采自宁夏芦花台园林场国家枸杞种质资源圃。
牛血清蛋白,上海源叶生物科技有限公司;DPPH、福林酚、亚硝酸钠、氯化铝、硫酸亚铁,上海阿拉丁生化科技股份有限公司;碳酸钠、氢氧化钠、盐酸、乙酸、乙酸钠、过氧化氢、水杨酸、过硫酸钾,美国Sigma公司;氯化钾、ABTS、乙醇、磷酸二氢钠、磷酸氢二钠,上海麦克林生化科技股份有限公司。试剂均为分析纯。
1.2 仪器与设备
Komak多功能破壁料理机(破壁机),广东伊莱特电器有限公司;Bifugo Stratos高速离心机,美国Thermo公司;ReadMax 1900光吸收全波长酶标仪,上海闪谱生物科技有限公司;FlavourSpec®气相色谱-离子迁移谱(GC-IMS)联用仪,德国G.A.S.公司。
1.3 实验方法
1.3.1 枸杞酵素的制备
选取大小均匀、无明显缺陷的宁农杞18号枸杞果实,用无菌水冲洗3次。然后将果实与水按照1∶3料液比(g∶mL)打碎混合,随后将其倒入无菌玻璃瓶中,并进行密封处理。接下来,将其置于常温下进行发酵,整个过程均在无菌操作台内进行,以确保操作的无菌性。发酵开始后,每5 d为一阶段取样,样品以8 000 r/min冷冻高速离心10 min后进行各项指标测定[9]。
1.3.2 理化指标的测定
利用手持pH计测定枸杞酵素的pH。
参照GB 12456—2021《食品安全国家标准 食品中总酸的测定》中的方法。
总糖的测量采用苯酚-硫酸法,稍作改动[10]。
1.3.3 营养物质含量的测定
总酚的测量采用Folin-Ciocalteu方法[11]。
总黄酮的测量采用NaNO2-Al(NO3)3比色法[12]。
抗坏血酸的测量采用2,6-二氯酚吲哚酚比色法[13]。
可溶性蛋白的测量采用Thomas Brilliant Blue G-250法[14]。
1.3.4 体外抗氧化活性的测定
参照LI等[15]的方法,测定枸杞酵素发酵液的DPPH自由基清除率。
参照LE等[16]的方法,测定枸杞酵素发酵液的ABTS阳离子自由基清除率。
参照HUANG等[17]的方法,测定枸杞酵素发酵液的羟自由基清除率。
1.3.5 挥发性物质的测定
分别取发酵0、5、10、15、20、25、30 d的枸杞发酵液样品7 mL,装入20 mL的顶空瓶中,在50 ℃孵育15 min后,将每种样品以500 μL顶空注入GC-IMS,对每种样品测定3组平行。进样温度280 ℃,色谱柱温度60 ℃,载气为高纯度氮气(纯度≥99.999%),气相色谱柱的流速设定为以下程序:初始流速2 mL/min保持5 min,10 min内线性升至10 mL/min保持10 min,5 min内线性升至15 mL/min保持5 min,20 min 内线性升至100 mL/min,保持10 min。风味分析采用Vocal分析光谱进行,挥发性化合物通过对比NIST数据库和IMS数据库,结合保留时间和离子迁移时间进行定性分析;分别使用Reporter插件和Gallery Plot插件绘制差异图谱及指纹图谱,直观比较样品之间挥发性物质相对含量的差异[18]。
1.4 数据处理
采用SPSS Statistics 26 软件进行显著性分析,结果以“平均值±标准差”表示。多组分析采用单因素方差分析(analysis of variance,ANOVA)和Tukey事后检验,P<0.05则差异有统计学意义。使用GraphPad Prism 8.0和Origin 2023进行绘图。使用Dynamic PCA插件进行主成分分析(principle component analysis,PCA),使用SIMCA 14.1版软件进行偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA)。
2 结果与分析
2.1 枸杞酵素发酵过程中理化指标的变化
2.1.1 枸杞酵素发酵过程中pH值与总酸的变化
枸杞酵素发酵过程中pH值和总酸的变化情况如图1所示。酵素发酵过程中存在各类微生物活动及生化反应,pH值与酵素发酵中微生物生长和代谢物积累的相对速率之间的相关性显著[19],在乳酸的典型发酵过程中,总酸是发酵的基本特性[20],因此,pH值和总酸是反应发酵过程正常与否的重要指标。本研究发现,整个发酵过程期间,pH值随着发酵时间的延长而持续下降,从最初的5.8下降至3.4,这可能是与乳酸菌等微生物经过一段时间繁殖后,产生一些酸性的次生代谢产物有关,表明微生物在发酵的酵素中均正常生长和繁殖。总酸含量随着发酵时间的延长而逐渐增加,从最初的2.53 g/L增加至6.33 g/L,发酵时间越长,总酸含量的增加越慢。这一发现可归因于发酵时间对酵素发酵过程中微生物生长变化和发酵速率的影响。
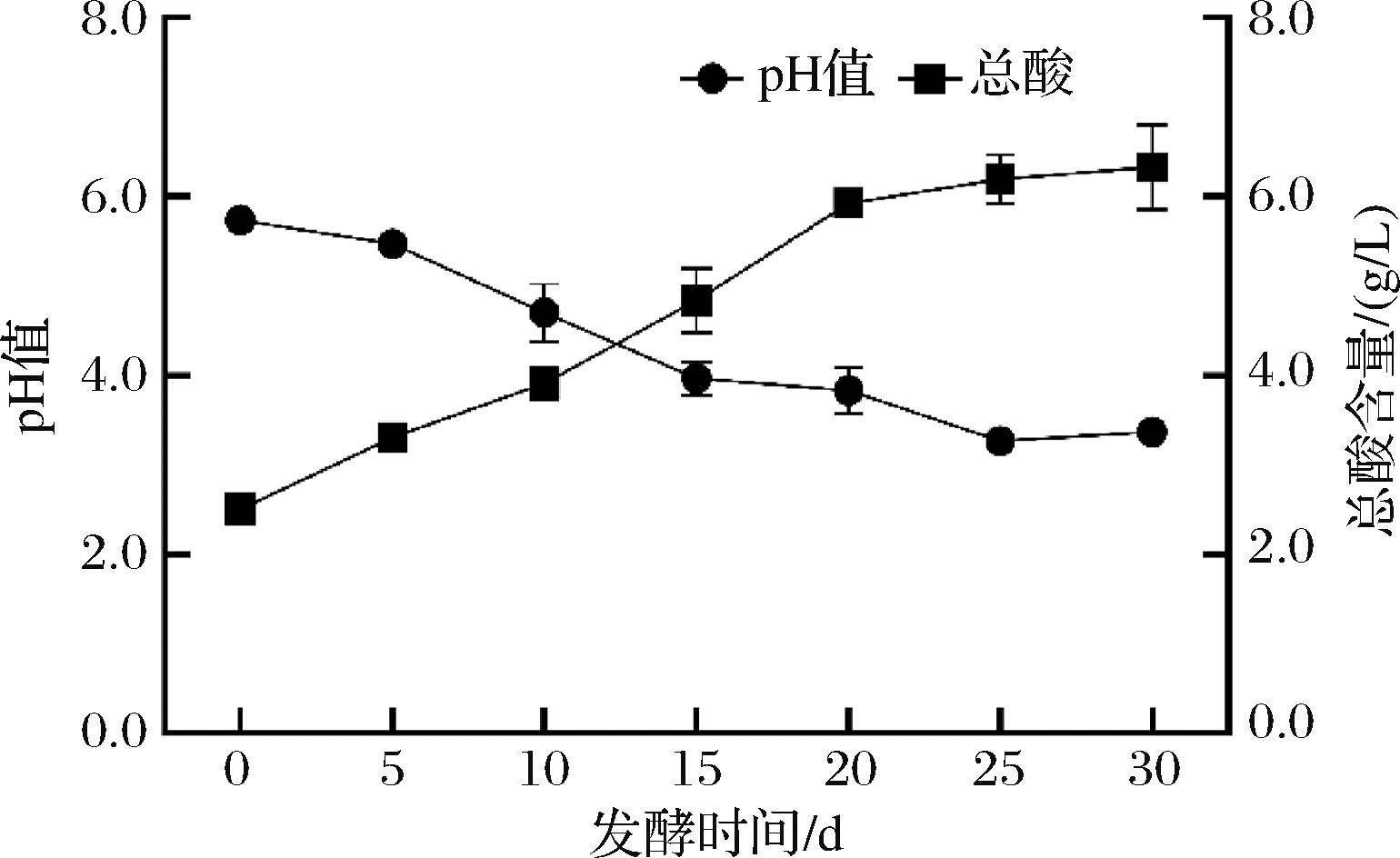
图1 枸杞酵素发酵过程中pH和总酸的变化
Fig.1 Changes in pH value and total titratable acidity during fermented goji berries fermentation
注:误差条表示平均值的标准偏差。
2.1.2 枸杞酵素发酵过程中总糖的变化
枸杞酵素发酵过程中总糖的变化情况如图2所示。糖类物质在发酵过程中能够有效反映微生物的生长与代谢状态。发酵过程中,可以观察到总糖含量呈现显著下降的趋势,从1.57 mg/mL下降至0.41 mg/mL。糖类(如葡萄糖、果糖、蔗糖等)是微生物生长和代谢的主要碳源。酵母、乳酸菌或真菌通过分解糖类获取能量(ATP)和合成细胞物质(如蛋白质、脂类等),导致总糖被快速消耗[21]。而在最后阶段,总糖含量的下降速度相对较慢,可能是由于微生物的繁殖和代谢活动逐渐达到阈值,使得枸杞酵素中的总糖含量减少速率降低。这一过程中,微生物能够利用枸杞发酵液中的糖类物质进行分解,进而促进糖类物质逐渐溶解于枸杞酵素中[22]。总糖含量下降的核心机制是微生物的代谢需求,包括糖的分解供能、细胞生长及产物合成。通过调控菌种选择、发酵条件(温度、pH、氧气)和工艺参数,可实现糖消耗速率的优化,从而控制枸杞酵素的品质[23]。
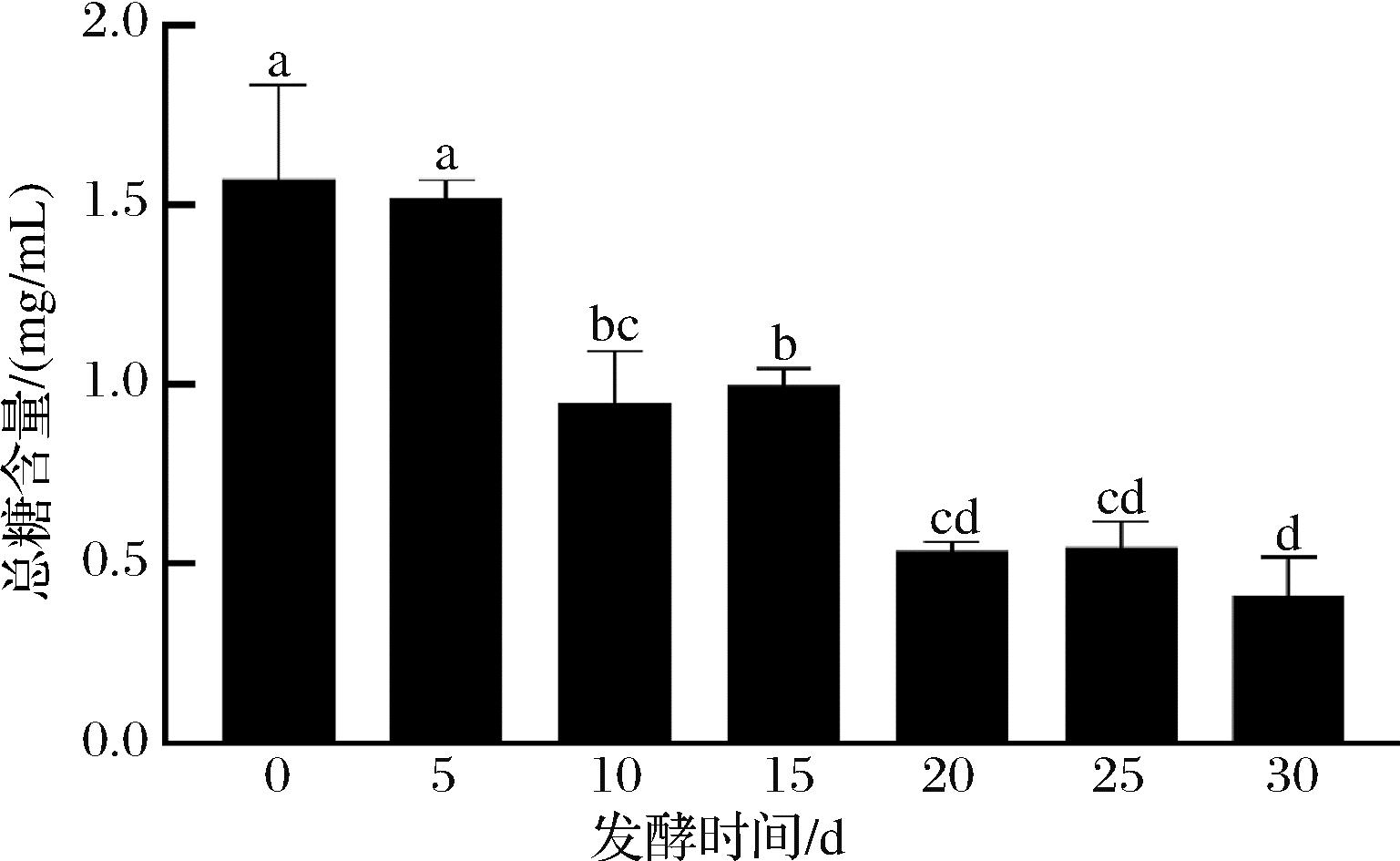
图2 枸杞酵素发酵过程中总糖含量的变化
Fig.2 Changes in total soluble sugar during fermented goji berries fermentation
注:误差条表示平均值的标准偏差,不同字母表示差异显著(P<0.05)(下同)。
2.2 枸杞酵素发酵过程中营养物质的变化
枸杞酵素发酵过程中营养物质的变化情况如图3所示。酚类和黄酮类化合物具有抗氧化功能,有助于延缓衰老过程,对促进人体健康具有显著作用[24]。不同发酵阶段,枸杞酵素的营养物质发生显著变化。发酵过程中,枸杞酵素中的总酚含量呈显著上升趋势(图3-A),从6.73 mg/mL上升至11.34 mg/mL,其原因可能与枸杞中的酚酸前体(如绿原酸、咖啡酸)在微生物作用下发生脱羧、羟基化等反应,生成新的酚类衍生物(如香草酸、阿魏酸)有关;发酵过程中,微生物在氧化胁迫下会合成酚类或黄酮类物质以清除自由基,间接导致产物中此类化合物积累等相关[25]。枸杞酵素的黄酮含量同样显著增高,从1.14 mg/mL上升至2.72 mg/mL,其原因可能与发酵产生的酶将部分多酚物质分解为黄酮醇物质;发酵产生的有机酸(如乳酸、乙酸)降低体系pH,增强酚类物质的溶解性(酚羟基在酸性条件下更易电离),同时稳定黄酮结构相关[26]。随着发酵的进行,枸杞酵素的可溶性蛋白含量和抗坏血酸含量显著降低,分别从1.23 mg/mL和5.19 mg/mL下降至0.48 mg/mL和1.76 mg/mL,其原因可能与微生物分泌的蛋白酶将大分子蛋白质水解为小肽或氨基酸,利用可溶性蛋白作为氮源,用于自身生长和代谢产物的合成,部分微生物可能利用维生素C作为辅助底物参与代谢等相关[27]。针对枸杞酵素发酵过程中可溶性蛋白和抗坏血酸含量降低的问题,可通过工艺控制,采用低温短时发酵,结合pH动态调控,并全程隔绝氧气以抑制抗坏血酸氧化,采用分段发酵方法并辅以外源补充等方法解决[28]。
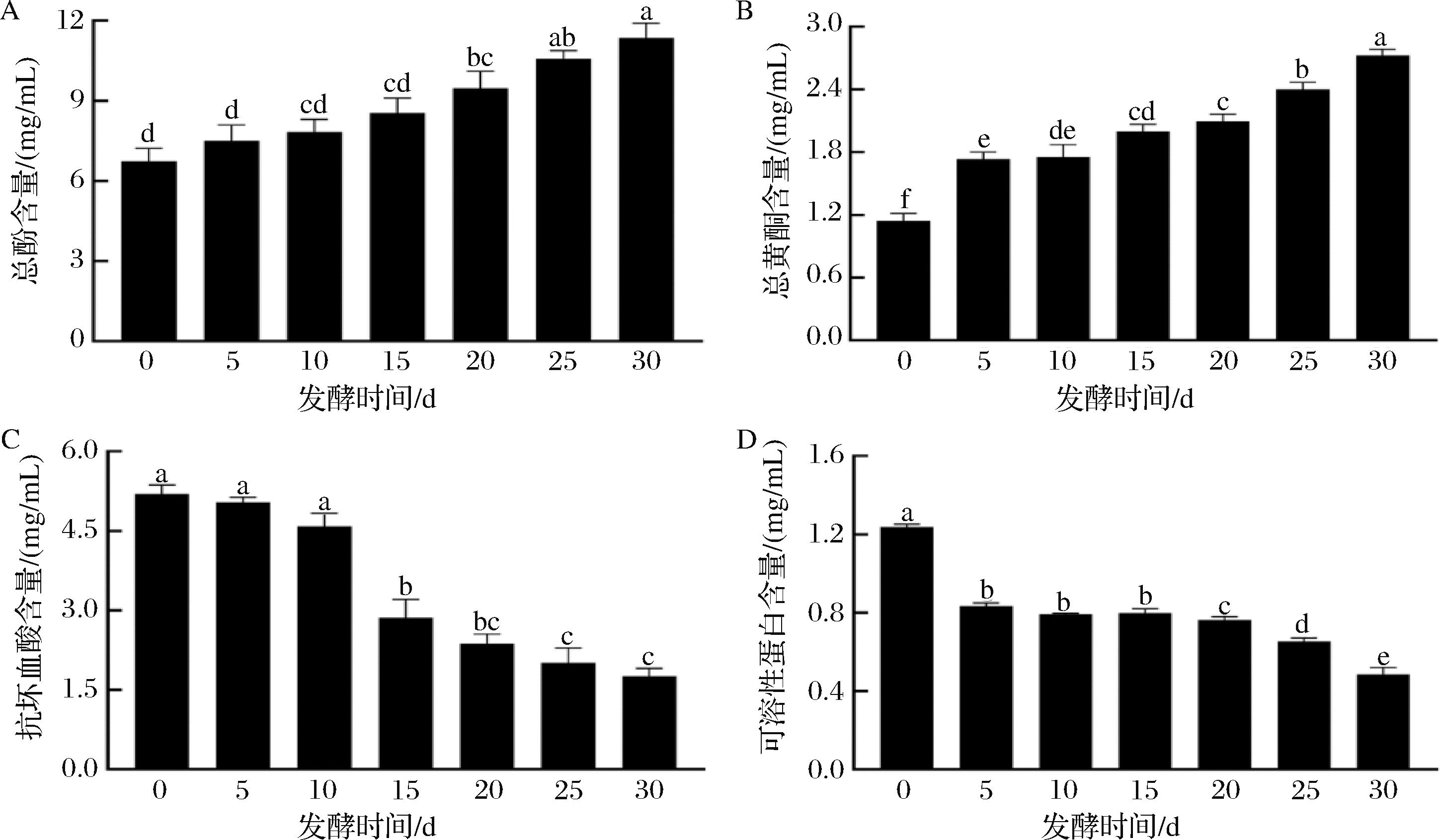
A-总酚;B-总黄酮;C-抗坏血酸;D-可溶性蛋白
图3 枸杞酵素发酵过程中营养物质含量的变化
Fig.3 Changes in nutrients during fermented goji berries fermentation
2.3 枸杞酵素发酵过程中体外抗氧化活性的变化
发酵过程中,枸杞酵素抗氧化活性产生了显著变化。如图4-A所示,枸杞酵素的DPPH自由基清除能力在发酵过程中显著提升,清除能力与未发酵前相比提高了29.7%(P<0.05),原因可能与发酵可以更好地促进枸杞中活性成分的溶解,从而提高酵素对DPPH 自由基的清除能力相关[29]。并且,与发酵前相比,枸杞酵素的ABTS阳离子自由基和羟自由基清除能力分别显著上升了49.3%和47.0%(图4-B、图4-C)。这些结果与2.2节枸杞酵素在发酵过程中总酚和黄酮含量上升的结果相一致,微生物在氧化胁迫下会合成酚类或黄酮类物质以清除自由基,可能解释了ABTS阳离子和羟自由基清除活性的升高[30]。
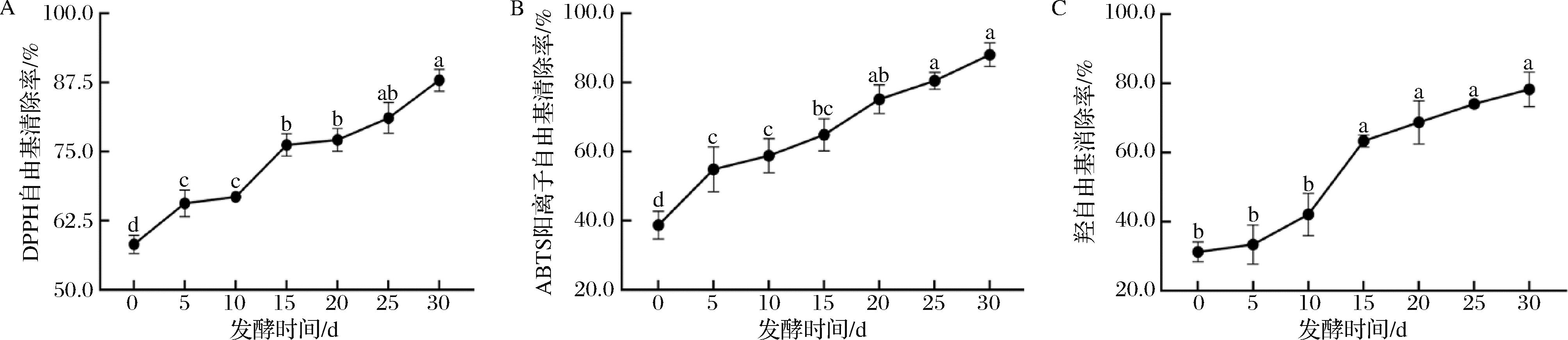
A-DPPH自由基;B-ABTS阳离子自由基;C-羟自由基
图4 枸杞酵素发酵过程中体外抗氧化活性的变化
Fig.4 Changes in antioxidant activity in vitro during fermented goji berries fermentation
2.4 枸杞酵素发酵过程中挥发性物质的变化
2.4.1 挥发性物质的定性分析
GC-IMS技术可以获得更清晰的挥发性风味化合物含量的图像,通过外标法更准确地定性分析。图5中,通过GC-IMS确定了自然发酵的枸杞酵素在不同发酵阶段的风味指纹图谱和差异图谱。GC-IMS的差异图谱如图5-A所示,图中的横坐标和纵坐标分别代表了分离枸杞酵素中物质相对于反应离子峰(reactive ion peak,RIP)的漂移时间和保留时间。在横坐标4.0的位置上,有一条垂直的线表示RIP,而在其两侧的斑点则代表了不同的物质。斑点的出现与否以及其颜色的深浅反映了物质的积累与分解程度。具体而言,颜色由白色到红色的变化表示物质浓度的变化,由低浓度逐渐升高,体现出物质在反应过程中的变化情况[31]。根据斑点的变化可以看出,这些枸杞酵素在离子峰的位置、数量、强度和时间上存在差异。发酵前后枸杞酵素差异图谱对比表明,未发酵和发酵的枸杞酵素在挥发性风味物质的种类和浓度上表现出显著的差异。这表明,通过自然发酵,枸杞酵素中的风味成分会发生变化,从而影响其整体风味特征。

A-差异图谱;B-指纹图谱
图5 枸杞酵素不同发酵时期挥发性物质GC-IMS指纹图谱及差异图谱
Fig.5 Fingerprints and difference map of volatile components in fermented goji berries with different fermentation periods
注:红色和蓝色分别表示挥发性物质的积累与分解程度。
如图5-B和电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.042454,下同)所示,所有样品中共鉴定出86种挥发物,包括醛类(22种)、醇类(19种)、酯类(15种)、酮类(15种)、烯烃类(5种)、脂肪酸类(4种)和未分类(6种)。发酵前后枸杞酵素指纹图谱可以看出,区域a显示了发酵前枸杞酵素的特征挥发物,随着发酵的进行而减少,减少程度最大的3种物质分别为,α-薄荷二烯-M、1-己醛-D和1-戊烯-3-醇。其中,α-薄荷二烯-M带有草木香气,1-己醛-D未发酵时的浓度,会呈现出强烈的绿草气味,1-戊烯-3-醇同样呈草木香。结果表明,未发酵枸杞酵素的气味主要以草木香为主。图5中的区域b显示了发酵后枸杞酵素的特征挥发物,其随着发酵的进行而增加,增加程度最大的3种物质分别为,2-甲基丁醇-D、乳酸乙酯-D和1-丙醇-M。2-甲基丁醇-D呈现酒味,乳酸乙酯-D呈现为成熟果香和黄油香气,1-丙醇-M则呈现典型的成熟果香[32]。结果表明,发酵后枸杞酵素的气味主要呈现味果香和酒香。这些结果表明,枸杞酵素发酵对枸杞酵素中风味物质的产生有显著影响,从草木香改变为成熟果香,使其具有更加成熟浓郁的风味。
2.4.2 挥发性物质的组成变化分析
枸杞酵素不同发酵时间挥发性物质的组成变化情况如图6所示。枸杞酵素中的醛类和未分类物质含量呈显著下降趋势,而醇类、酮类和烯烃类物质含量呈显著上升趋势,酯类和脂肪酸则变化不显著。醇类升高的原因主要有3点:a)微生物的厌氧代谢,比如乙醇的生成途径;b)枸杞酵素中含氮物质(如氨基酸、蛋白质)丰富,底物中的氨基酸分解产生高级醇;c)环境因素如温度、pH、氧气的影响,例如,微氧条件导致部分微生物合成其他醇类或中间产物。醇类的增加可以提供枸杞酵素独特的发酵风味。此外,枸杞酵素的酮类含量显著增加,而醛类含量显著降低。研究表明,高浓度的醛类和酮类化合物常常会导致不愉快的异味产生。此外,这些化合物在微生物的作用下呈现不稳定性[33]。因此,自然发酵在调节挥发性化合物含量方面具有显著作用,这一过程对于提升枸杞酵素的风味具有显著的积极影响。
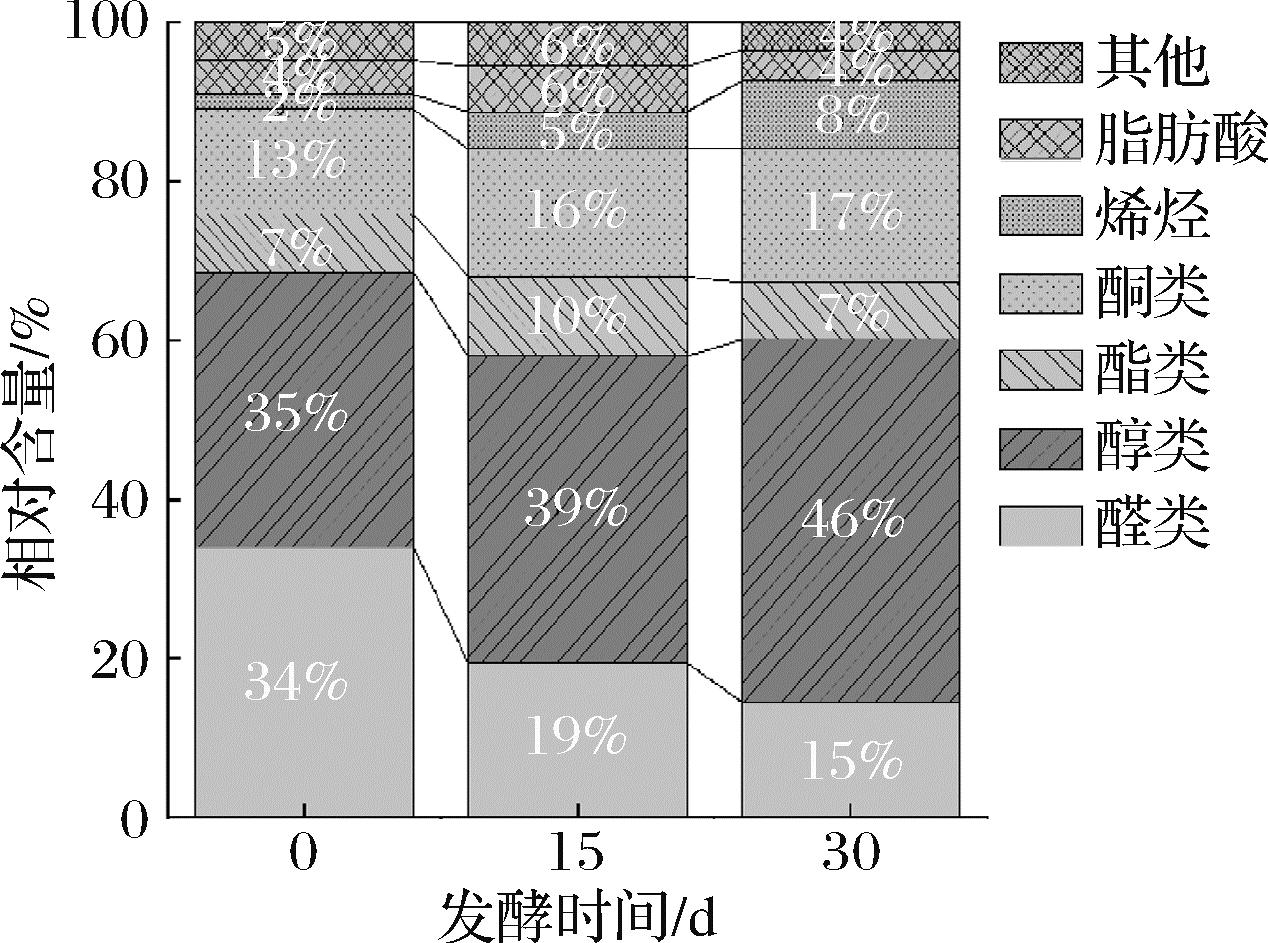
图6 枸杞酵素不同发酵时期挥发性化合物类别相对含量的变化
Fig.6 Changes of relative contents of volatile compound classes in fermented goji berries with different fermentation periods
基于不同阶段挥发性物质含量的差异,对不同阶段枸杞酵素样品进行PCA(图7-A)。当PCA中的第一主成分(PC1)与第二主成分(PC2)的累积贡献率达到60%时,则认为该PCA模型为有效的分离模型[34]。由图7-A可见,2个主成分(PC1和PC2)共同解释了98.08%的变异,发酵不同阶段的枸杞酵素样品在PCA分布图中占据相对独立的空间,指纹图谱分析结果与PCA结果一致。这些结果表明,枸杞酵素样品在发酵的不同阶段的风味差异明显,发酵前样品的风味和发酵后的样品差异显著。采用PLS-DA统计方法,将变量数据和分类信息分别归为2组数据集(图7-B)。通过对数据进行投影和判别计算,依据分组信息可有效挖掘组间的差异,从而区分不同发酵阶段样品的观测结果[35]。随后,为了进一步验证PLS-DA模型的可靠性和预测能力,本文进行了交叉验证方差分析和排列检验(200次迭代,R2X=0.976,R2Y=0.998,Q2=0.995)(图7-C)。生成的模型质量参数具有良好的稳定性和预测能力,保证了观测到的分离不是由随机效应引起的。上述结果表明,枸杞酵素发酵显著改变了枸杞酵素的挥发性物质组成,对风味改变具有显著影响。
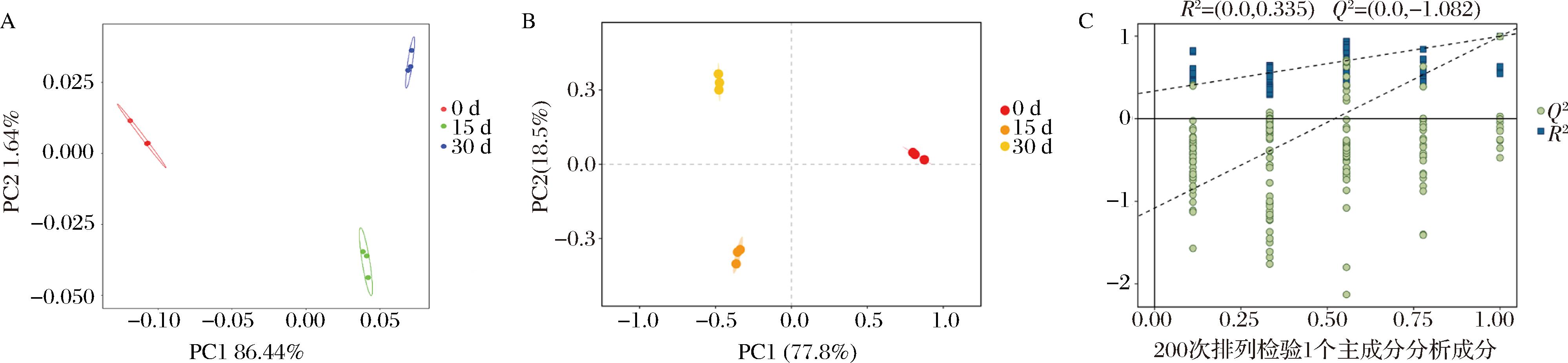
A-PCA;B-PLS-DA;C-置信检验分析
图7 枸杞酵素不同发酵时期挥发性化合物的PCA、PLS-DA和置信检验结果
Fig.7 PCA,PLS-DA,and permutation test results of volatile compound in fermented goji berries with different fermentation periods
3 结论
本研究以枸杞作为主要原料,在自然条件下进行为期30 d的发酵过程,制备枸杞酵素。对枸杞酵素发酵过程中的理化指标、营养物质含量和抗氧化活性进行测定,利用GC-IMS的技术分析发酵前后风味物质的成分变化。结果表明,发酵过程中,枸杞酵素pH值显著下降,发酵结束时维持在3.4左右;总酸含量显著增加至6.33 g/L;总糖含量显著减少至0.41 mg/mL。DPPH自由基、ABTS阳离子和羟自由基清除能力均显著高于未发酵样品。样品中共鉴定出86种挥发物,发酵前后枸杞酵素差异图谱和指纹图谱对比表明,未发酵的和发酵后的样品在挥发性风味物质的种类及其浓度方面有显著差异。随着发酵的进行,α-薄荷二烯-M、1-己醛-D和1-戊烯-3-醇3种物质相对含量降低程度最大,2-甲基丁醇-D、乳酸乙酯-D和1-丙醇-M三种物质相对含量升高程度最大,自然发酵对枸杞酵素中风味物质的产生有显著影响,从草木香改变为成熟果香;堆积图和多元统计分析结果表明,发酵过程显著改变了枸杞酵素的挥发性物质组成。本研究为枸杞发酵产品的开发与利用提供了重要的数据支持以及理论依据。这些信息将有助于推动相关领域的进一步研究和应用。
[1] LIU H,CUI B,ZHANG Z.Mechanism of glycometabolism regulation by bioactive compounds from the fruits of Lycium barbarum:A review[J].Food Research International,2022,159:111408.
[2] FENG L,TANG N C,LIU R J,et al.Effects of different processing methods on bioactive substances and antioxidation properties of Lycium barbarum (goji berry) from China[J].Food Bioscience,2021,42:101048.
[3] 王印壮,段定定,丁玉峰,等.葡萄酵素发酵过程中代谢产物的动态变化[J].食品科学,2022,43(18):98-104.WANG Y Z,DUAN D D,DING Y F,et al.Dynamic changes of metabolites during grape jiaosu fermentation[J].Food Science,2022,43(18):98-104.
[4] YUAN Y H,MU D D,GUO L,et al.From flavor to function:A review of fermented fruit drinks,their microbial profiles and health benefits[J].Food Research International,2024,196:115095.
[5] AN X,LI T T,HU J X,et al.Evaluation of physicochemical characteristics,bioactivity,flavor profile and key metabolites in the fermentation of goji juice by Lacticaseibacillus rhamnosus[J].Food Chemistry:X,2024,23:101755.
[6] YAN J,CHEN J B,HUANG Z W,et al.Characterisation of the volatile compounds in nine varieties and three breeding selections of celery using GC-IMS and GC-MS[J].Food Chemistry:X,2024,24:101936.
[7] MARINACCIO L,GENTILE G,LLORENT-MART NEZ E J,et al.Valorization of grape pomace extracts against cranberry,elderberry,rose hip berry,goji berry and raisin extracts:Phytochemical profile and in vitro biological activity[J].Food Chemistry,2025,463:141323.
NEZ E J,et al.Valorization of grape pomace extracts against cranberry,elderberry,rose hip berry,goji berry and raisin extracts:Phytochemical profile and in vitro biological activity[J].Food Chemistry,2025,463:141323.
[8] POGGIONI L,ROMI M,GUARNIERI M,et al.Nutraceutical profile of goji (Lycium barbarum L.) berries in relation to environmental conditions and harvesting period[J].Food Bioscience,2022,49:101954.
[9] 陈小伟,程勇杰,蒋立新,等.草莓酵素发酵过程中代谢产物及抗氧化性的变化研究[J].中国食品学报,2020,20(5):157-165.CHEN X W,CHENG Y J,JIANG L X,et al.Studies on the changes of metabolites and antioxidant activity during the fermentation process of strawberry Jiaosu[J].Journal of Chinese Institute of Food Science and Technology,2020,20(5):157-165.
[10] CHEN W,GAO L,SONG L R,et al.An improved phenol-sulfuric acid method for the quantitative measurement of total carbohydrates in algal biomass[J].Algal Research,2023,70:102986.
[11] DU G G,QING Y D,WANG H Z,et al.Effects of Tibetan kefir grain fermentation on the physicochemical properties,phenolics,enzyme activity,and antioxidant activity of Lycium barbarum (Goji berry) juice[J].Food Bioscience,2023,53:102555.
[12] NAHEED Z,CHENG Z H,WU C N,et al.Total polyphenols,total flavonoids,allicin and antioxidant capacities in garlic scape cultivars during controlled atmosphere storage[J].Postharvest Biology and Technology,2017,131:39-45.
[13] ZHANG Y Q,WANG H X,CHEN H J,et al.The crucial evaluation indexes and relative measurement methods of edible value for fresh fruits and vegetables:A review[J].Future Postharvest and Food,2024,1(2):222-236.
[14] LI M Y,WANG Y,WEI X H,et al.Effects of pretreatment and freezing storage on the bioactive components and antioxidant activity of two kinds of celery after postharvest[J].Food Chemistry:X,2023,18:100655.
[15] LI S C,ZHENG Y,LI M L,et al.Quantitative analyses of major enzyme activities in postharvest fruit[J].Future Postharvest and Food,2024,1(2):213-221.
[16] LE GRANDOIS J,GUFFOND D,HAMON E,et al.Combined microplate-ABTS and HPLC-ABTS analysis of tomato and pepper extracts reveals synergetic and antagonist effects of their lipophilic antioxidative components[J].Food Chemistry,2017,223:62-71.
[17] HUANG Z Y,WANG J,CHENG H,et al.Advantages of hydroxyl radical water treatment for the fruits and vegetables preservation[J].LWT,2023,184:115106.
[18] HUANG Y,WANG L,LI Y,et al.Comparative analysis of key flavor compounds in various Baijiu types using E-nose,HS-SPME-GC-MS/MS,and HS-GC-IMS technologies[J].Food Chemistry:X,2025:102689.
[19] 赵宇,杜庆萍,杨瑞,等.西梅酵素发酵过程中理化指标、抗氧化能力及挥发性物质的变化[J].食品工业科技,2025,46(17):335-343.ZHAO Y,DU Q P,YANG R,et al.Physicochemical properties and antioxidant capacity and volatile compound changes during the fermentation of Chinese prune Jiaosu[J].Science and Technology of Food Industry,2025,46(17):335-343.
[20] 戴芳,吴宇昊,祝振洲,等.不同物理场预处理对猕猴桃酵素品质的影响[J].食品工业科技,2025,46(17):96-105.DAI F,WU Y H,ZHU Z Z,et al.Effects of different physical field pretreatment on the quality of kiwifruit Jiaosu[J].Science and Technology of Food Industry,2025,46(17):96-105.
[21] DUR N-ARANGUREN D D,VILLABONA L C,L
N-ARANGUREN D D,VILLABONA L C,L PEZ G D,et al.Recovery of essential oils,polyphenols,fermentable sugars,and pectin from orange residues:Evaluation of extraction methodologies and characterization of value-added bioactive compounds[J].Separation and Purification Technology,2025,359:130590.
PEZ G D,et al.Recovery of essential oils,polyphenols,fermentable sugars,and pectin from orange residues:Evaluation of extraction methodologies and characterization of value-added bioactive compounds[J].Separation and Purification Technology,2025,359:130590.
[22] ZHANG T X,LIAO Z S,LI Z H,et al.Revealing the flavor differences of Sauvignon Blanc wines fermented in different oak barrels and stainless-steel tanks through GC-MS,GC-IMS,electronic,and artificial sensory analyses[J].Food Chemistry:X,2025,25:102188.
[23] FENG L,YANG J X,SUN L P,et al.Changes of unique flavor substances and metabolic pathway brought by Lacticaseibacillus rhamnosus WH.FH-19 fermented milk during fermentation and storage stage:HS-SPME-GC-MS and HPLC-MS-based analysis[J].Food Bioscience,2025,65:105974.
[24] MOHD ALI M,HASHIM N,ABD AZIZ S,et al.Quality prediction of different pineapple (Ananas comosus) varieties during storage using infrared thermal imaging technique[J].Food Control,2022,138:108988.
[25] JIA S,LU C,TONG X,et al.Efficient and green production of flavone-5-O-glycosides by glycosyltransferases in Escherichia coli[J].International Journal of Biological Macromolecules,2024,277:134477.
[26] PAN X F,SONG J L,PEI J W,et al.Evaluation of fermentation combined with pretreatment to enhance bioactive compounds content and antioxidant activity of wheat germ meal[J].Journal of Cereal Science,2025,121:104084.
[27] ZHANG T,CHANG M,ZHOU Y,et al.Dynamic alterations of flavor,functional nutrients,and microbial community during fermentation of different animal milk kefirs[J].Food Research International,2024,186:114305.
[28] LIU Y R,GU P,LAAKSONEN O,et al.Lactic acid bacteria incubation and aging drives flavor enhancement of goji berry juice[J].Journal of Food Composition and Analysis,2022,105:104202.
[29] WU H M,FU Q Q,TANG T T,et al.Dynamic changes of quality characteristics during fermentation of orange-fleshed sweet potato alcoholic beverage[J].LWT,2025,218:117509.
[30] GUO W K,CHENG M R,DONG X M,et al.Analysis of flavor substances changes during fermentation of Chinese spicy cabbage based on GC-IMS and PCA[J].Food Research International,2024,192:114751.
[31] HUANG H R,CHEN X Y,WANG Y,et al.Analysis of volatile compounds and vintage discrimination of raw Pu-erh tea based on GC-IMS and GC-MS combined with data fusion[J].Journal of Chromatography A,2025,1743:465683.
[32] LI X H,ZHANG C,LIU C R,et al.Effects of pre-and post-harvest konjac glucomannan phosphate ester composite film coating on the volatile profiles of mangoes during storage[J].LWT,2024,214:117171.
[33] CHEN H W,BAI S J,YANG B W,et al.Inter-and intra-varietal clonal differences influence the aroma compound profiles of wines analyzed by GC-MS and GC-IMS[J].Food Chemistry:X,2025,25:102136.
[34] 夏思,房祥军,吴伟杰,等.发酵型杨梅果浆的制备及其功能风味品质研究[J].浙江农业学报,2025,37(3):667-678.XIA S,FANG X J,WU W J,et al.Preparation of fermented Chinese bayberry (Myrica rubra) pulp and its functional activity and flavor quality[J].Acta Agriculturae Zhejiangensis,2025,37(3):667-678.
[35] SUN P Z,LIN S Y,LI X R,et al.Different stages of flavor variations among canned Antarctic krill (Euphausia superba):Based on GC-IMS and PLS-DA[J].Food Chemistry,2024,459:140465.