2001年,世界粮农组织(Food and Agriculture Organization of the United Nations,FAO)和世界卫生组织(World Health Organization,WHO)联合专家委员会给出了益生菌的定义:活的微生物,当摄取足够数量时,对宿主健康有益[1]。
益生菌通常以膳食补充剂或发酵剂的形式添加到食品中,近年来人们日益关注其促进健康的作用,但其安全性也同样重要。尽管传统上用于益生菌的微生物被认为具有长期安全使用历史[2],但近年来有报道指出,益生菌可能引发胃肠道副作用,如呕吐、恶心、腹泻等,尤其对于婴儿、老年人、孕妇及免疫力低下人群,其安全性不容忽视[3]。例如,BOUMIS等[4]发现,鼠李糖乳酪杆菌在遗传性出血性毛细血管扩张患者中可能引发感染性心内膜炎。因此,随着全球益生菌产品使用量的增加,其安全性评价变得越来越重要。未来,需要进一步建立模仿人类病理生理的动物模型和免疫功能低下的模型,以评估益生菌对特殊群体的毒力特性[5]。
1 国内外研究现状
1.1 国内研究现状
国内关于益生菌的研究主要集中在功能应用方面,如降糖降脂、调节肠道微生物群、免疫调节、抗氧化和各种疾病预防等,而对安全性的研究相对较少。近几年,随着对益生菌安全性评价的重视,相关研究逐渐增多。国内研究人员对益生菌进行安全性评价一般包括全基因组分析、体外评价和体内实验。
首先对待评价菌株进行全基因组序列分析,检测其是否存在毒力基因、耐药基因以及与产生有毒代谢产物相关的基因。如表1所示,LI等[6]对副干酪乳酪杆菌PS23进行安全性分析,发现其不含毒力或抗生素耐药性相关的基因,从而表明该菌株安全性较高。
表1 国内益生菌安全性评价研究情况
Table 1 Research on the safety evaluation of probiotics in China

菌株基因表型动物试验结论参考文献副干酪乳酪杆菌PS23毒力基因分析耐药基因分析药敏试验鸟氨酸脱羧酶活性检测小鼠遗传毒性试验小鼠经口毒性试验安全[6]植物乳植杆菌cqf-43毒力、耐药基因分析与溶血素、明胶酶和生物胺产生相关基因分析药敏试验生物胺检测试验溶血酶和明胶酶活性检测小鼠经口毒性试验安全[7]植物乳植杆菌LPJZ-658毒力基因分析耐药基因分析溶血试验药敏试验小鼠经口毒性试验安全[9]黏膜乳杆菌DCC1HL5毒力基因分析溶血试验药敏试验生物胺检测试验亚急性经口毒性试验(小鼠)安全[10]巨大芽孢杆菌BM24—药敏试验溶血试验小鼠毒性试验安全[8]
注:符号“—”表示所引文献未做该指标的研究(下同)。
体外评价中抗生素敏感性检测和溶血情况分析是必不可少的,有害代谢产物检测也是表型评价中常见的一部分,这些有害代谢产物主要包括生物胺含量以及氨基脱羧酶活性等。研究人员常通过表型与基因分析相结合的方法来对其进行评估。LIU等[7]通过抗生素的敏感性检测、溶血酶活性分析以及生物胺的检测与全基因组序列分析(毒力、耐药基因以及与溶血素和生物胺产生相关基因)相结合的方法来对一株从健康母猪粪便中分离得到的植物乳植杆菌cqf-43进行安全性分析,从而确定该菌株具有安全性。
此外,国内主要是以小鼠为动物实验的模型来进行体内毒性试验,通过口服、灌胃以及注射益生菌的方式处理,然后通过观察小鼠的体重、各项生理生化指标以及剖解后的脏器情况是否有异常来对益生菌进行体内安全评估。贾盛等[8]通过小鼠体内灌胃和腹腔注射试验来对一株从健康细毛羊粪便中分离得到的巨大芽孢杆菌BM24进行安全性评价,结果表明该菌株对小鼠无毒副作用,从而确定该菌株具有良好的安全性。
目前,我国正式发布的GB 31615.2—2025《食品安全国家标准 食品用菌种安全性评价程序》和团体标准T/CIFST 009—2022《食品用益生菌通则》都指出益生菌的安全性评价需要从体外评价和体内评价2个方面进行,如表2所示。体外评价至少要包括对抗生素抗性的分析、溶血性以及生物胺等有毒有害代谢产物的检测。体内评价是指要对待评价菌株进行动物致病性试验和毒理学试验,具体毒理学试验在GB 15193.1—2014《食品安全国家标准 食品安全性毒理学评价程序》中有详述。
表2 国内益生菌安全性评价方法指南
Table 2 Guidelines for the safety evaluation methods of probiotics in China

官方文件状态发布机构发布时间主要指标《新食品原料申报与受理规定》实施中中华人民共和国国家卫生和计划生育委员会2013-10-15分类学地位、生物学特征、菌种鉴定和鉴定方法及依据;新食品原料食用历史;成分分析报告;卫生学检验报告;毒理学评价报告;微生物耐药性试验报告和产毒能力试验报告;安全性评估意见;国内外研究利用情况和相关安全性评估资料GB 15193.1—2014《食品安全国家标准 食品安全性毒理学评价程序》实施中中华人民共和国国家卫生和计划生育委员会2014-12-24急性经口毒性实验、遗传毒性试验、28 d经口毒性试验、90 d经口毒性试验、致畸试验、生殖毒性试验和生殖发育毒性试验、毒物动力学试验、慢性毒性试验、致癌试验、慢性毒性和致癌合并试验T/CIFST 009—2022《食品用益生菌通则》实施中中国食品科学技术学会2022-06-16菌株水平鉴定;致病性评价(毒力基因分析、产毒试验、溶血性及其他活性物质评价);耐药性评价(耐药基因分析、药敏试验等);健康作用评价(以体外试验、动物实验为参考,人体试验为重要依据)GB 31615.2—2025《食品安全国家标准 食品用菌种安全性评价程序》实施中中华人民共和国国家卫生健康委员会;国家市场监督管理总局2025-03-16国内外安全性评价资料分析、全基因组测序、基因序列分析(毒力基因和耐药基因)、动物致病性试验、耐药性试验、产毒试验、其他活性物质(D-乳酸、代谢活性或溶血活性等)
此外,《新食品原料申报与受理规定》和GB 31615.2—2025《食品安全国家标准 食品用菌种安全性评价程序》均指出需要基于待评价菌种国内外使用历史及安全性评价资料(包括但不限于其致病性和产毒能力报告、临床试验资料、科技文献或综述等)对其进行综合分析。
1.2 国外研究现状
国外对益生菌进行安全性评价会对益生菌的基因组进行分析,确定其毒力基因和抗生素抗性基因情况(表3)。SENDELIUS等[11]对罗伊氏乳杆菌ATCC PTA4659进行毒力基因和耐药基因分析,发现其不含毒力和耐药基因,从而确定该菌对人类食用是安全的。此外,国外大部分在益生菌安全性方面的研究都会对其溶血活性、抗生素耐药性情况以及生物胺含量做表型试验进行分析,部分研究还会评价益生菌的有害酶活性。TANAKA等[12]对2株具有益生潜力的鼠李糖乳酪杆菌YM2-1和YM2-3进行体外安全性评价,发现2株菌都对主要抗生素敏感,致癌相关酶和溶血等方面的不良活性均低于研究采用的体外评价方法检测限,从而说明2株菌具有较高安全性。由表4 可知,发展中国家例如印度要求对益生菌进行动物致病性相关的评价,但发达国家和地区,如美国、欧洲等很少有权威监管机构在益生菌安全性评价中采用动物模型进行安全性评价,但都会采用基于全基因组学技术对毒力、耐药基因进行分析。国外很多相关专家考虑动物福利问题,会采用替代毒理学方法,如基于秀丽隐杆线虫、昆虫模型或者虾模型等进行益生菌的安全性评价[13-15]。
表3 国外益生菌安全性评价研究情况
Table 3 Research on the safety evaluation of probiotics abroad

菌株基因表型动物/临床试验结论参考文献或来源马克斯克鲁维酵母A4和A5—溶血试验小鼠经口毒性试验 安全[16]罗伊氏乳杆菌ATCC PTA 4659毒力基因分析耐药基因分析药敏试验生物胺含量检测试验临床安全性评价试验安全[11]鼠李糖乳酪杆菌YM2-1和YM2-3—药敏试验溶血试验致癌相关酶检测试验—安全[12]贝宁山魏斯菌LMG 25373T毒力基因分析耐药基因分析药敏试验溶血试验—安全[17]库德里阿兹威毕赤酵母Y1、乳酸乳球菌霍氏亚种LAB1—药敏试验溶血试验大蜡螟存活试验 安全[13]
表4 国外益生菌安全性评价方法指南
Table 4 Guidelines for the safety evaluation methods of probiotics abroad
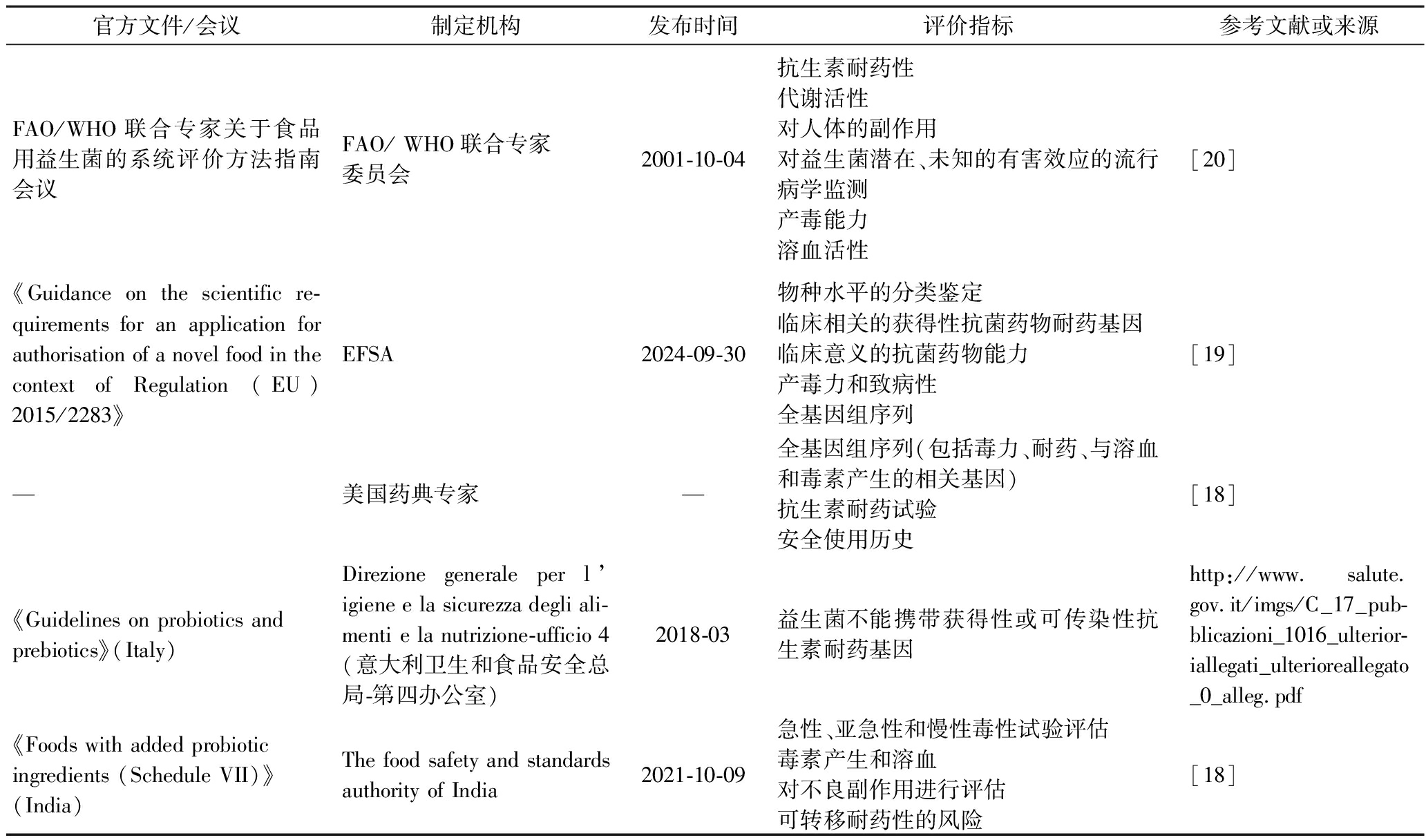
官方文件/会议制定机构发布时间评价指标参考文献或来源FAO/WHO联合专家关于食品用益生菌的系统评价方法指南会议FAO/ WHO联合专家委员会2001-10-04抗生素耐药性代谢活性对人体的副作用对益生菌潜在、未知的有害效应的流行病学监测产毒能力溶血活性[20]《Guidance on the scientific re-quirements for an application for authorisation of a novel food in the context of Regulation (EU) 2015/2283》EFSA2024-09-30物种水平的分类鉴定临床相关的获得性抗菌药物耐药基因临床意义的抗菌药物能力产毒力和致病性全基因组序列[19]—美国药典专家—全基因组序列(包括毒力、耐药、与溶血和毒素产生的相关基因)抗生素耐药试验安全使用历史[18]《Guidelines on probiotics andprebiotics》(Italy)Direzione generale per l’igiene e la sicurezza degli ali-menti e la nutrizione-ufficio 4(意大利卫生和食品安全总局-第四办公室)2018-03益生菌不能携带获得性或可传染性抗生素耐药基因http://www.salute.gov.it/imgs/C_17_pub-blicazioni_1016_ulterior-iallegati_ulterioreallegato_0_alleg.pdf《Foods with added probiotic ingredients (Schedule VII)》(India)The food safety and standards authority of India2021-10-09急性、亚急性和慢性毒性试验评估毒素产生和溶血对不良副作用进行评估可转移耐药性的风险[18]
注:符号“—”表示所引文献没有该项内容。
尽管全球监管机构对益生菌的安全原则已基本达成普遍共识,但由表4可知各国对益生菌安全性的监管要求差异很大,近20年,国际上还没有形成新的统一的标准。此外,发达国家美国并没有专门针对益生菌产品的法律法规,而是由食品药品管理局(Food and Drug Administration,FDA)按照“公认为安全”的管理模式进行监管。但是,美国药典专家基于FAO/WHO的指南以及FDA对乳酸菌等益生菌的相关规定,总结了美国食品用益生菌安全评价的关键点[18]。他们建议,所有益生菌都应进行全基因组测序,以鉴定是否存在溶血、毒素产生和耐药性相关基因。这一建议与欧洲食品安全局(European Food Safety Authority,EFSA)颁布的《Guidance on the scientific requirements for an application for authorisation of a novel food in the context of Regulation (EU) 2015/2283》(《根据法规(EU)2015/2283申请新食品授权的科学要求指南》)中的相关规定一致[19]。此外,FAO/WHO联合专家委员会、EFSA以及印度等权威机构和国家还指出,需要通过表型试验对益生菌的产毒能力、溶血活性以及抗生素耐药性进行验证[18,20]。
2 益生菌安全性评价方法
根据国内外对益生菌安全性评价的官方指南和相关学者的研究进展总结,益生菌的安全性评价主要包括对待评价菌株的国内外使用历史及安全性评价资料进行综合分析、对菌株进行鉴定分类、体外评价包括但不限于抗生素耐药性、溶血性和生物胺等在内的有害物质检测以及对菌株进行动物体内的致病性和毒理评价4个步骤,如图1所示。
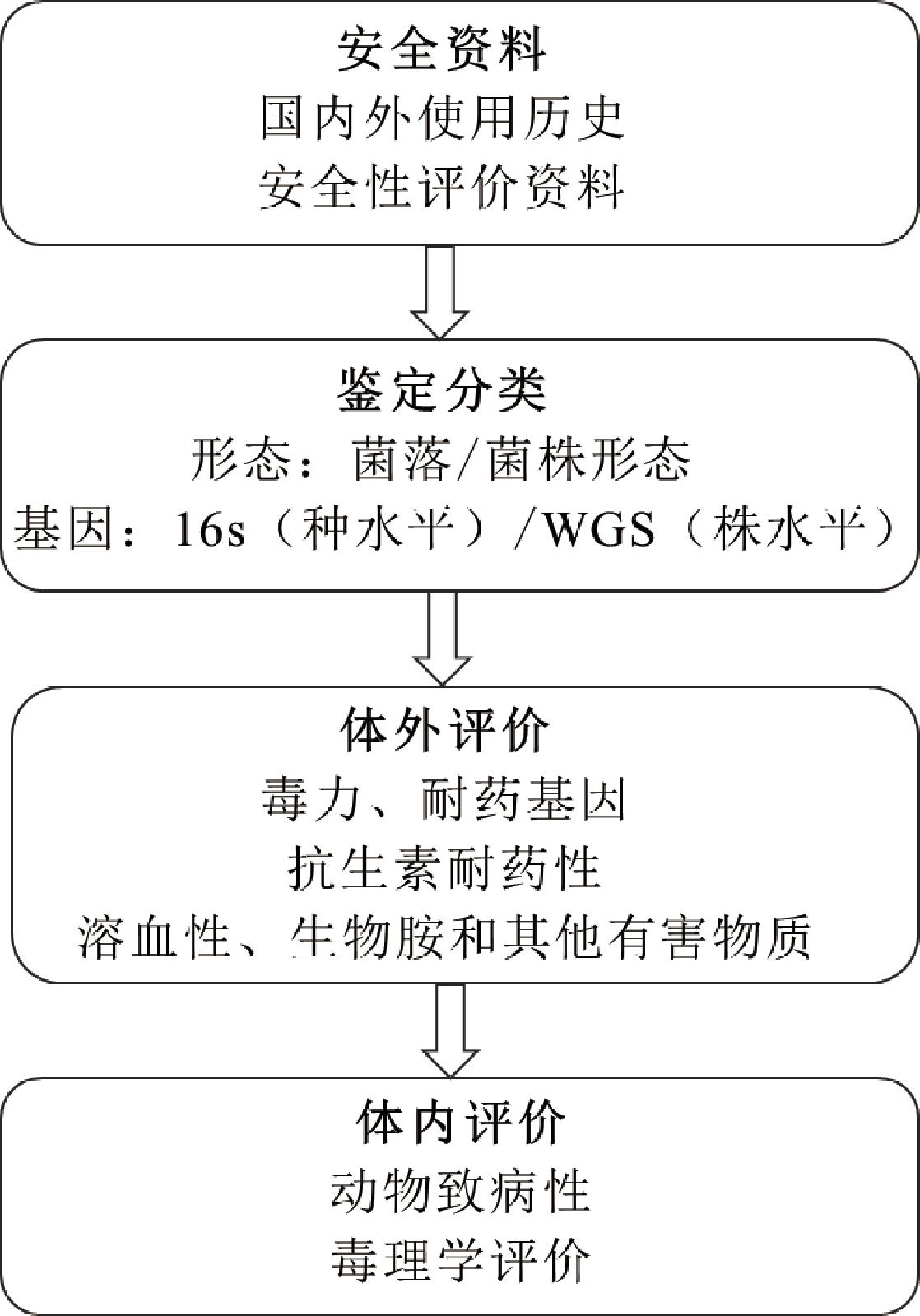
图1 益生菌安全性评价流程图
Fig.1 Flow chart of probiotic safety evaluation
注:WGS为全基因组测序(whole genome sequencing)。
2.1 国内外安全性评价资料综述
GB 31615.2—2025《食品安全国家标准 食品用菌种安全性评价程序》指出需对菌种国内、国外使用历史及安全性(包括但不限于其致病性和产毒能力报告、临床试验资料、科技文献或综述等)进行综合分析。若没有这些资料,则应提供同种其他菌株或与其亲缘关系相近种属的使用历史和安全性评价资料。此外,美国药典专家也建议提供待评价菌株的安全使用历史(属、种和菌株水平)[18]。总之,待评价菌株的国内外使用历史及安全性评价资料是评估其安全性的重要依据。通过全面、系统地收集和分析这些资料,可以更加准确地评估菌株的潜在危害,从而确保其在不同领域的应用安全。
2.2 菌株的分类鉴定
菌株的分类鉴定主要从表型和基因型两方面鉴定[21]。正确识别益生菌菌株是避免菌株信息错误的首要步骤。由于益生菌的作用是菌株特异性的,因此将益生菌鉴定到正确的菌株水平是非常有必要的[22]。
表型鉴定主要方法是观察菌落形态和菌体形态。菌落形态主要是观察益生菌在固定培养环境下的菌落的表面形态、大小、颜色、边缘、质地和形状等特征。菌体形态是指细菌细胞的大小、形状等特征,一般采用扫描电镜、透射电镜等显微镜来观察。这些特征对于细菌的分类和鉴定具有重要的理论和实践意义。
但是,基于表型研究需要依据经验判断,并不能够准确鉴定到菌种级别,因此需要进行基因型鉴定,如通过16S rRNA基因序列、脉冲场凝胶电泳[23]、WGS、随机扩增多态DNA[24]等方法鉴定。16S rRNA基因序列分析是一种广泛应用于益生菌分类和鉴定的方法,可以对细菌进行物种级别的鉴定。但是仅仅基于16S rRNA测序对菌株进行分类鉴定是不够的,因为该方法不能在菌株水平上区分细菌,甚至有些菌种水平也不能区分。目前,WGS已经成为一种不可取代的准确鉴定益生菌菌株的方法[25]。通过对全基因组数据分析,可获得毒力、耐药、有毒代谢产物等相关基因情况,从对益生菌进行安全性评估。
2.3 体外安全性评价
体外安全性评价的主要指标包括溶血活性、生物胺、抗生素耐药性和D-乳酸的含量等。
2.3.1 溶血活性
EFSA指出,即使是那些已经获得安全资格认证或具有长期传统消费历史的微生物,也必须对其溶血活性进行评估[26]。在实验室中,通常将目标菌株接种在血琼脂培养基上进行培养,根据溶血圈的情况对菌株的进行定性分析,随后通过分光光度计测定415 nm 或570 nm处的吸光度,以定量分析目标菌株释放的血红蛋白量[27]。尽管某些潜在的益生菌菌株可能携带溶血素相关基因,但它们在体外试验中未必会表现出典型的溶血现象[28]。因此,对这些“假定基因”的表达进行研究,有助于理解其调控机制和表达情况,从而在研究初期排除潜在的危害菌株。蛋白质组学能够提供细胞在任何生长阶段的全面蛋白质组信息,有助于鉴定细菌中可能存在的致病性蛋白质。因此,蛋白质组学可以作为一种有效的质量控制工具,用于评估益生菌在人类应用前的安全性[29]。
2.3.2 生物胺
生物胺是一类具有生物活性的低分子质量含氨基化合物,主要包括腐胺、尸胺、精胺、亚精胺、酪胺、苯乙胺、组胺和色胺等[30]。生物体内适量的生物胺可发挥促进生长、增强代谢活力、提升免疫力及清除自由基等积极作用。然而,过量摄入某些生物胺(如组胺和酪胺)可能导致中毒,引发头痛、血压波动、呼吸紊乱、心悸、呕吐等严重不良反应[31]。因此,对供人类食用的食品或药物中的生物胺进行量化分析具有重要意义。乳酸菌作为生物胺的潜在来源之一,用于益生菌的乳酸菌菌株应避免产生过量生物胺[31]。但是,目前关于益生菌对人体产生急性副作用的生物胺产量尚未有明确的上限标准,因此研究中常以商业参考菌株作为试验菌株的对照标准[21]。
生物胺的定性评估方法主要包括在含有或不含前体氨基酸的脱羧酶琼脂培养基上培养测试菌株,通过观察培养基的颜色变化来判断生物胺的产生情况。另一方面,定量评估则通常采用配备C18色谱柱和紫外检测器的高效液相色谱法(high performance liquid chromatography,HPLC)或靶向代谢组学方法对试验菌株进行分![]() 等[33]通过HPLC结合薄层色谱法,成功测定了益生菌无细胞上清液中生物胺的含量,为相关研究提供了可靠的技术支持。
等[33]通过HPLC结合薄层色谱法,成功测定了益生菌无细胞上清液中生物胺的含量,为相关研究提供了可靠的技术支持。
2.3.3 抗生素耐药性
益生菌的固有抗性在肠道菌群调节中可能发挥有益作用,通常不被视为安全问题。然而,位于益生菌可移动遗传元件上的耐药基因及其水平转移倾向可能对消费者构成潜在安全风险。因此,耐药性检测是益生菌安全性评价中的重要环节[21]。益生菌的耐药基因可通过转录组学方法进行研究。ALONSO等[34]利用转录组学方法分析了应激条件下益生菌菌株的抗生素耐药性基因表达情况,评估了其安全性。目前,转录组学在益生菌安全性评价中的应用仍较为有限。
益生菌的耐药表型可根据多种标准化方法进行测定,包括美国临床和实验室标准协会、欧洲抗微生物药敏试验委员会、EFSA下属的动物饲料添加剂和产品或物质小组以及国际乳品联合会推荐的方法。这些方法涵盖最小抑制浓度法、Epsilometer试验、琼脂稀释法、肉汤稀释法、Kirby-Bauer纸片扩散法,以及一些先进的分子生物学技术,如微阵列和PCR等[5,35-37]。这些方法的综合应用有助于全面评估益生菌的耐药性特征,为其安全性评价提供科学依据。
2.3.4 D-乳酸
乳酸菌属中的许多菌种具有独特的形态、代谢和生理特征。例如,乳杆菌属和链球菌属是2个常见的以乳酸作为碳水化合物代谢主要发酵副产物的菌属,其产生的乳酸包括L-乳酸、D-乳酸以及DL-乳酸消旋体[38]。由于人体对D-乳酸的代谢能力有限,过量的D-乳酸可能对人体产生潜在危害。尽管这种危害十分罕见,到目前为止,仅在患有短肠综合征的婴幼儿中报道过[39],还没有证据表明健康婴幼儿服用能够产生D-型乳酸的益生菌会导致任何不良反应,但还是应对其保持警惕。目前还没有建议对益生菌或者益生菌来源的发酵食品的D-乳酸水平设定更高的限量。因此,在评估新型益生菌菌株的安全性时,建议将其与商业菌株或已发表文献中的相关数据进行比较,以更好地评估其潜在风险[40]。
2.4 体内安全性评价
目前我国婴幼儿益生菌食品中用到的益生菌大多都依赖进口,我国的相关研究机构都致力于开发新的婴幼儿用益生菌,但研究机构在新资源申报中需要开展婴幼儿喂养实验,而我国法规规定用于婴幼儿喂养实验的益生菌需要在我国《可用于婴幼儿食品的菌种名单》中,这一矛盾成为我国婴幼儿用益生菌开发面临的主要问题[41]。因此,关于这方面的研究需要寻找合适的动物模型或替代模型来解决我国婴幼儿用益生菌开发过程中面临的临床试验无法实施的问题。
体内安全性评价的传统方法主要包括使用大/小鼠模型和猪模型等,如表5所示。大/小鼠模型因其与人类在基因、生理、胚胎发育、疾病模型及免疫系统等方面具有高度相似性,且其生理特征和行为(如体重、代谢率、运动水平等)易于量化和监测,成为目前应用最广泛的安全性评价模型。CRUZ等[42]通过大鼠模型评估了一种新型益生菌混合物的安全性。然而,大鼠模型存在成本较高以及动物福利和伦理问题等局限性。猪模型在生理、营养和代谢方面与人类具有较高的相似性,因此也被建议作为益生菌安全性评估的潜在模型。但由于猪模型的广泛不可获得性、处理大型动物的技术难度以及伦理问题的限制,其在益生菌安全性评估中的应用尚未得到普遍推广[21]。
表5 安全性评价的动物模型及其优缺点
Table 5 Animal models of safety evaluation and their advantages and disadvantages
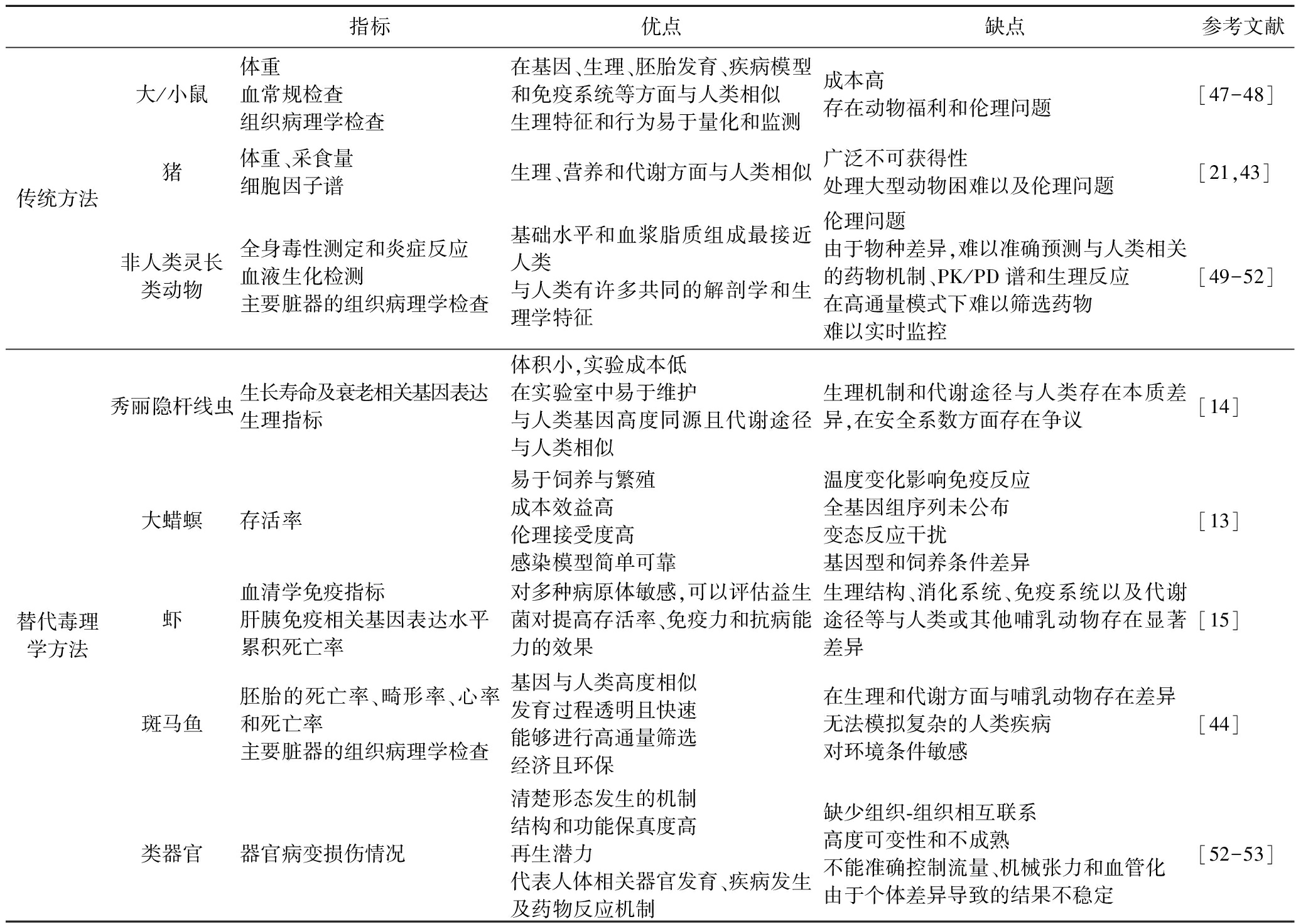
指标优点缺点参考文献传统方法大/小鼠体重血常规检查组织病理学检查在基因、生理、胚胎发育、疾病模型和免疫系统等方面与人类相似生理特征和行为易于量化和监测成本高存在动物福利和伦理问题[47-48]猪体重、采食量细胞因子谱生理、营养和代谢方面与人类相似广泛不可获得性处理大型动物困难以及伦理问题[21,43]非人类灵长类动物全身毒性测定和炎症反应血液生化检测主要脏器的组织病理学检查基础水平和血浆脂质组成最接近人类与人类有许多共同的解剖学和生理学特征伦理问题由于物种差异,难以准确预测与人类相关的药物机制、PK/PD谱和生理反应在高通量模式下难以筛选药物难以实时监控[49-52]替代毒理学方法秀丽隐杆线虫生长寿命及衰老相关基因表达生理指标 体积小,实验成本低在实验室中易于维护与人类基因高度同源且代谢途径与人类相似生理机制和代谢途径与人类存在本质差异,在安全系数方面存在争议[14]大蜡螟存活率易于饲养与繁殖成本效益高伦理接受度高感染模型简单可靠温度变化影响免疫反应全基因组序列未公布变态反应干扰基因型和饲养条件差异[13]虾血清学免疫指标肝胰免疫相关基因表达水平累积死亡率对多种病原体敏感,可以评估益生菌对提高存活率、免疫力和抗病能力的效果生理结构、消化系统、免疫系统以及代谢途径等与人类或其他哺乳动物存在显著差异[15]斑马鱼胚胎的死亡率、畸形率、心率和死亡率主要脏器的组织病理学检查基因与人类高度相似发育过程透明且快速能够进行高通量筛选经济且环保在生理和代谢方面与哺乳动物存在差异无法模拟复杂的人类疾病对环境条件敏感[44]类器官器官病变损伤情况清楚形态发生的机制结构和功能保真度高再生潜力代表人体相关器官发育、疾病发生及药物反应机制缺少组织-组织相互联系高度可变性和不成熟不能准确控制流量、机械张力和血管化由于个体差异导致的结果不稳定[52-53]
随着对动物福利的关注日益增加,越来越多的替代毒理学方法被用于替代大/小鼠等传统动物模型,例如秀丽隐杆线虫、大蜡螟、虾以及类器官模型等[14-15,43-44],如表5所示。秀丽隐杆线虫因其体积小、实验成本低、易于实验室培养以及与人类基因高度同源且代谢途径相似等优势,成为一种重要的模式生物。HARBEOUI等[14]利用秀丽隐杆线虫评估了尿路致病性大肠杆菌G1722、G1473和ER41的毒性。但由于线虫的生理机制和代谢途径与人类存在本质差异,其安全性评价结果的可靠性仍存在争议[45]。大蜡螟因其易于饲养与繁殖、成本效益高以及伦理接受度高等特点,也被用于益生菌安全性评价。MAIONE等[13]通过大蜡螟存活试验评估了库德里阿兹威毕赤酵母Y1和乳酸乳球菌霍氏亚种LAB1的安全性。然而,该模型也存在一定局限性,包括温度变化对免疫反应的影响、全基因组序列尚未公布以及变态反应的干扰等[46]。此外,有研究通过幼虾对植物乳植杆菌W2进行安全性评估[15],但由于虾的生理结构、消化系统、免疫系统及代谢途径与人类或其他哺乳动物存在显著差异,其实验结果难以直接外推至人类益生菌的安全性评价。
综上所述,尽管替代毒理学方法在益生菌安全性评价中展现出一定的潜力,但其应用仍需进一步深入研究,以明确其机制并验证其可靠性。
3 结论与展望
益生菌的安全性对人类健康具有重大影响,本文旨在综合国内外益生菌安全性研究的最新进展,并从全基因组分析、体外实验和体内实验等多个角度,对益生菌的安全评估进行综述。随着益生菌的广泛使用,以及下一代益生菌中发掘到尚缺乏长期使用历史的菌种,益生菌的安全评价受到了越来越多的关注。尽管如此,当前对益生菌安全性的研究仍面临一些挑战,具体包括:a)全球评价方法的共识与差异:尽管全球范围内对益生菌安全性评价方法已有一定共识,但在体内评价方法上仍存在差异,动物研究作为评估益生菌对人类安全性的工具,其适用性及寻找最合适的动物模型仍存在争议。b)特殊人群研究的不足:针对免疫功能低下、疾病易感和患病人群的益生菌安全性研究较少,需要进一步加强。c)替代毒理学研究的探索:益生菌安全性体内评价的替代毒理学研究尚处于探索阶段,需要对替代毒理学机制进行更深入的研究。
[1] 中国食品科学技术学会益生菌分会.益生菌的科学共识(2020年版)[J].中国食品学报,2020,20(5):303-307.Probiotics Society of the Chinese Institute of Food Science and Technology.Scientific consensus on probiotics (2020)[J].Journal of Chinese Institute of Food Science and Technology,2020,20(5):303-307.
[2] ŽUNTAR I,PETRIC Z,![]() D B,et al.Safety of probiotics:Functional fruit beverages and nutraceuticals[J].Foods,2020,9(7):947.
D B,et al.Safety of probiotics:Functional fruit beverages and nutraceuticals[J].Foods,2020,9(7):947.
[3] SOTOUDEGAN F,DANIALI M,HASSANI S,et al.Reappraisal of probiotics’ safety in human[J].Food and Chemical Toxicology,2019,129:22-29.
[4] BOUMIS E,CAPONE A,GALATI V,et al.Probiotics and infective endocarditis in patients with hereditary hemorrhagic telangiectasia:A clinical case and a review of the literature[J].BMC Infectious Diseases,2018,18(1):65.
[5] NATARAJ B H,KUMARI M,NAGPAL R,et al.Safety evaluation of indigenous probiotic Limosilactobacillus fermentum NCDC 400 using whole genome sequences and in vitro approaches[J].Food Bioscience,2023,56:103101.
[6] LI C H,CHEN T Y,WU C C,et al.Safety evaluation and anti-inflammatory efficacy of Lacticaseibacillus paracasei PS23[J].International Journal of Molecular Sciences,2022,24(1):724.
[7] LIU B H,ZHONG X X,LIU Z Y,et al.Probiotic potential and safety assessment of Lactiplantibacillus plantarum cqf-43 and whole-genome sequence analysis[J].International Journal of Molecular Sciences,2023,24(24):17570.
[8] 贾盛,候萌,陈伟丽,等.一株羊源巨大芽孢杆菌BM24的分离鉴定及安全性评价[J].动物营养学报,2024,36(9):6083-6094.JIA S,HOU M,CHEN W L,et al.Isolation,identification and safety evaluation of a sheep-derived Bacillus megaterium BM24[J].Chinese Journal of Animal Nutrition,2024,36(9):6083-6094.
[9] DENG L Q,LIU L M,FU T Y,et al.Genome sequence and evaluation of safety and probiotic potential of Lactiplantibacillus plantarum LPJZ-658[J].Microorganisms,2023,11(6):1620.
[10] DANG D T,LIU X M,CHEN H Q,et al.In silico,in vitro and in vivo safety assessment of three Limosilactobacillus mucosae strains for probiotic candidates[J].Food Bioscience,2024,57:103462.
[11] SENDELIUS M,AXELSSON J,LIU P D,et al.Genomic,phenotypic,and clinical safety of Limosilactobacillus reuteri ATCC PTA 4659[J].Journal of Industrial Microbiology &Biotechnology,2023,50(1):kuad041.
[12] TANAKA Y,ARYANTINI N P D,YAMASAKI E,et al.In vitro probiotic characterization and safety assessment of lactic acid bacteria isolated from raw milk of Japanese-Saanen goat (Capra hircus)[J].Animals,2022,13(1):7.
[13] MAIONE A,IMPARATO M,BUONANNO A,et al.Evaluation of potential probiotic properties and in vivo safety of lactic acid bacteria and yeast strains isolated from traditional home-made kefir[J].Foods,2024,13(7):1013.
[14] HARBEOUI H,DI MARTINO P,MAYOT G.A new killing assay with the Caenorhabditis elegans PX627 mutant to assess the virulence of uropathogenic Escherichia coli strains[J].Journal of Microbiological Methods,2023,214:106823.
[15] WEI C,LUO K,WANG M Y,et al.Evaluation of potential probiotic properties of a strain of Lactobacillus plantarum for shrimp farming:From beneficial functions to safety assessment[J].Frontiers in Microbiology,2022,13:854131.
[16] YOUN H Y,KIM D H,KIM H J,et al.A combined in vitro and in vivo assessment of the safety of the yeast strains Kluyveromyces marxianus A4 and A5 isolated from Korean kefir[J].Probiotics and Antimicrobial Proteins,2023,15(1):129-138.
[17] FANELLI F,MONTEMURRO M,VERNI M,et al.Probiotic potential and safety assessment of type strains of Weissella and Periweissella species[J].Microbiology Spectrum,2023,11(2):e03047-22.
[18] ROE A L,BOYTE M E,ELKINS C A,et al.Considerations for determining safety of probiotics:A USP perspective[J].Regulatory Toxicology and Pharmacology,2022,136:105266.
[19] TURCK D,BOHN T,CASTENMILLER J,et al.Guidance on the scientific requirements for an application for authorisation of a novel food in the context of Regulation (EU) 2015/2283[J].EFSA Journal,2024,22(9):e8961.
[20] 吴蜀豫,冉陆.FAO/WHO《食品益生菌评价指南》[J].中国食品卫生杂志,2003,15(4):377-379.WU S Y,RAN L.FAO/WHO guidelines for the evaluation of food probiotics[J].Chinese Journal of Food Hygiene,2003,15(4):377-379.
[21] HARANAHALLI NATARAJ B,BEHARE P V,YADAV H,et al.Emerging pre-clinical safety assessments for potential probiotic strains:A review[J].Critical Reviews in Food Science and Nutrition,2024,64(23):8155-8183.
[22] ZHANG Y M,OVERBECK T J,SKEBBA V L P,et al.Genomic and phenotypic safety assessment of probiotic Bacillus coagulans strain JBI-YZ6.3[J].Probiotics and Antimicrobial Proteins,2025,17(5):3440-3450.
[23] HUANG Y,EECKHAUT V,GOOSSENS E,et al.Bacterial chondronecrosis with osteomyelitis related Enterococcus cecorum isolates are genetically distinct from the commensal population and are more virulent in an embryo mortality model[J].Veterinary Research,2023,54(1):13.
[24] AKTEPE Y,AYD N F,
N F,![]() T,et al.Molecular characterization and multifunctional evaluation of lactic acid bacteria isolated from traditional sourdough[J].International Journal of Food Microbiology,2024,423:110845.
T,et al.Molecular characterization and multifunctional evaluation of lactic acid bacteria isolated from traditional sourdough[J].International Journal of Food Microbiology,2024,423:110845.
[25] KIM Y H,LEE D H,SEO H S,et al.Genome-based taxonomic identification and safety assessment of an Enterococcus strain isolated from a homemade dairy product[J].International Microbiology,2024,27(5):1513-1525.
[26] CAO Y H,WANG Z H,DAI X X,et al.Evaluation of probiotic properties of a Brevibacillus laterosporus strain[J].The FASEB Journal,2024,38(5):e23530.
[27] XIAO J M,CHEN C,FU Z X,et al.Assessment of the safety and probiotic properties of Enterococcus faecium B13 isolated from fermented chili[J].Microorganisms,2024,12(5):994.
[28] FU X M,LYU L,WANG Y,et al.Safety assessment and probiotic characteristics of Enterococcus lactis JDM1[J].Microbial Pathogenesis,2022,163:105380.
[29] STASTNA M.The role of proteomics in identification of key proteins of bacterial cells with focus on probiotic bacteria[J].International Journal of Molecular Sciences,2024,25(16):8564.
[30] NATRELLA G,VACCA M,MINERVINI F,et al.A comprehensive review on the biogenic amines in cheeses:Their origin,chemical characteristics,hazard and reduction strategies[J].Foods,2024,13(16):2583.
[31] SAHA TURNA N,CHUNG R,MCINTYRE L.A review of biogenic amines in fermented foods:Occurrence and health effects[J].Heliyon,2024,10(2):e24501.
[32] LEE Y R,YEONG W,BAEK K R,et al.Safety evaluation by phenotypic and genomic characterization of four Lactobacilli strains with probiotic properties[J].Microorganisms,2022,10(11):2218.
[33] ![]()
![]() M,et al.Determination of biogenic amines formation by autochthonous lactic acid bacteria from ‘Refošk’ grapes using different analytical methods[J].Lwt,2022,156:112908.
M,et al.Determination of biogenic amines formation by autochthonous lactic acid bacteria from ‘Refošk’ grapes using different analytical methods[J].Lwt,2022,156:112908.
[34] ALONSO GARC A E,BENOMAR N,LAVILLA LERMA L,et al.Changes in resistome profile of potential probiotic Lactiplantibacillus pentosus in response to edible oil adaptation[J].Food Microbiology,2023,109:104148.
A E,BENOMAR N,LAVILLA LERMA L,et al.Changes in resistome profile of potential probiotic Lactiplantibacillus pentosus in response to edible oil adaptation[J].Food Microbiology,2023,109:104148.
[35] FRANCO W.Postbiotics and parabiotics derived from bacteria and yeast:Current trends and future perspectives[J].CyTA-Journal of Food,2024,22(1):2425838.
[36] SANAHUJA I,RUIZ A,FIRMINO J P,et al.Debaryomyces hansenii supplementation in low fish meal diets promotes growth,modulates microbiota and enhances intestinal condition in juvenile marine fish[J].Journal of Animal Science and Biotechnology,2023,14(1):90.
[37] LEE J,JO J,SEO H,et al.The probiotic properties and safety of Limosilactobacillus mucosae NK41 and Bifidobacterium longum NK46[J].Microorganisms,2024,12(4):776.
[38] VITETTA L,COULSON S,THOMSEN M,et al.Probiotics,D-lactic acidosis,oxidative stress and strain specificity[J].Gut Microbes,2017,8(4):311-322.
[39] 刘勇,张勇,张和平.世界益生菌安全性评价方法[J].中国食品学报,2011,11(6):141-151.LIU Y,ZHANG Y,ZHANG H P.Evaluating methods of probiotic’s safety in the world[J].Journal of Chinese Institute of Food Science and Technology,2011,11(6):141-151.
[40] MELEH H U,CHOO S,MOHD DESA M N,et al.Isolation and safety characterisation of Lactobacilli strains with antimicrobial properties as potential probiotics for human use[J].LWT,2020,131:109796.
[41] 王世杰,何方,朱宏.婴幼儿用益生菌的研究现状及面临的挑战[J].食品科学技术学报,2020,38(1):12-16.WANG S J,HE F,ZHU H.Research status and challenges of probiotics for infants[J].Journal of Food Science and Technology,2020,38(1):12-16.
[42] CRUZ NETO J P R,DE OLIVEIRA A M,DE OLIVEIRA K  R,et al.Safety evaluation of a novel potentially probiotic Limosilactobacillus fermentum in rats[J].Probiotics and Antimicrobial Proteins,2024,16(3):752-762.
R,et al.Safety evaluation of a novel potentially probiotic Limosilactobacillus fermentum in rats[J].Probiotics and Antimicrobial Proteins,2024,16(3):752-762.
[43] CUEVAS-G MEZ I,DE ANDRÉS J,CARDENAS N,et al.Safety assessment and characterisation of Ligilactobacillus salivarius PS21603 as potential feed additive for swine[J].Beneficial Microbes,2022,13(5):397-406.
MEZ I,DE ANDRÉS J,CARDENAS N,et al.Safety assessment and characterisation of Ligilactobacillus salivarius PS21603 as potential feed additive for swine[J].Beneficial Microbes,2022,13(5):397-406.
[44] LIU Y W,HUANG Y,MOU Z,et al.Characterization and preliminary safety evaluation of nano-SiO2 isolated from instant coffee[J].Ecotoxicology and Environmental Safety,2021,224:112694.
[45] 孟艺伟,赵燕秋,孟庆洲,等.秀丽隐杆线虫模型在抗衰老研究中的应用[J].生物资源,2023,45(1):9-15.MENG Y W,ZHAO Y Q,MENG Q Z,et al.Application of Caenorhabditis elegans model in anti-aging research[J].Biotic Resources,2023,45(1):9-15.
[46] JIT REANU A,TRIFAN A,VIERIU M,et al.Current trends in toxicity assessment of herbal medicines:A narrative review[J].Processes,2022,11(1):83.
REANU A,TRIFAN A,VIERIU M,et al.Current trends in toxicity assessment of herbal medicines:A narrative review[J].Processes,2022,11(1):83.
[47] GU J Y,SONG K,FAN Y X,et al.Safety evaluation of Bifidobacterium animalis subsp.lactis BLa80 under in vitro and in vivo,conditions[J].Microbial Pathogenesis,2024,194:106809.
[48] HOU F Y,TANG J Y,LIU Y Y,et al.Safety evaluation and probiotic potency screening of Akkermansia muciniphila strains isolated from human feces and breast milk[J].Microbiology Spectrum,2023,11(2):e03361-22.
[49] JENSEN V F,JENSEN N K,SCHEFE L H,et al.The non-human primate in safety assessment of a bifunctional long-acting insulin analogue[J].International Journal of Toxicology,2023,42(3):254-268.
[50] BOLON B,EVERITT J I.Selected resources for pathology evaluation of nonhuman Primates in nonclinical safety assessment[J].Toxicologic Pathology,2022,50(5):725-732.
[51] QI J Y,ZHANG L Y,TAN F Z,et al.Preclinical efficacy and safety evaluation of AAV-OTOF in DFNB9 mouse model and nonhuman primate[J].Advanced Science,2024,11(3):2306201.
[52] WANG H,ZHU W,XU C,et al.Engineering organoids-on-chips for drug testing and evaluation[J].Metabolism,2025,162:156065.
[53] AHN S J,LEE S,KWON D,et al.Essential guidelines for manufacturing and application of organoids[J].International Journal of Stem Cells,2024,17(2):102-112.