杏仁为蔷薇科植物山杏(Prunus armeniaca L.var.ansu Maxim)、西伯利亚杏(Prunus sibirica L.)、东北杏[Prunus mandshurica(Maxim.)Koehne]或杏(Prunus armeniaca L.)的干燥成熟种子[1],同时杏仁也是一种药食两用的资源。在《中华本草》里有提到杏仁可以消炎、镇痛、镇咳平喘以及治疗糖尿病等。杏仁富含多种有效成分,如多肽、多糖、苦杏仁苷、多酚等,其中苦杏仁苷是一种特殊的氰苷[2]。多种成分彼此协同,共同发挥作用,使杏仁的营养价值和潜在功效得到了充分发挥。近年来,来自世界各地的科学家们一直在对杏仁进行广泛的研究,包括不限于杏仁活性成分的提取优化、降糖效果、抗氧化能力、抗菌性。
糖尿病是一种由胰岛素分泌受损或外周胰岛素抵抗所引起的慢性疾病。糖尿病人无法正常分泌或者利用胰岛素,从而造成血液中血糖升高,具体表现为高血糖、血脂异常、视力障碍、肾脏疾病等症状[3]。糖尿病被分为Ⅰ型糖尿病、Ⅱ型糖尿病(diabetes mellitus type 2,T2DM)、特殊类型糖尿病和妊娠期糖尿病,Ⅰ型和Ⅱ型糖尿病均表现出明显的遗传性,而环境因素(缺乏运动、过量饮食、年龄增长等)诱发的糖尿病主要为Ⅱ型糖尿病[4]。糖尿病患者中Ⅱ型糖尿病比较普遍,占总糖尿病患者的90%~95%,并且Ⅱ型糖尿病患者主要为中老年人群和肥胖人群[5]。
目前,糖尿病已与心脑血管疾病、癌症、慢性呼吸系统疾病一道,被并称为严重威胁人类健康的四大慢性病。2021年,全球共有5.29亿糖尿病患者,糖尿病年龄标准化患病率为6.1%,其中有43个国家/地区的糖尿病年龄标化患病率超过10%。全球范围来看,男性的糖尿病年龄标准化患病率高于女性,其中96.0%为Ⅱ型糖尿病。基于社会人口指数和身体质量指数等预测因素,预计到2050年,全球糖尿病患者数量将超过13.1亿[6]。若糖尿病得不到及时的控制和治疗,就会引起更加严重的并发症(如糖尿病视网膜病变、糖尿病肾病、糖尿病神经病变、冠状动脉粥样硬化性心脏病、脑血管疾病等),对人们的身体健康和生活品质造成严重影响。
因此,本文就杏仁对糖尿病的治疗现状,系统描述了杏仁中降糖活性物质、杏仁与其他坚果的降糖作用和杏仁降糖作用的临床试验,并从调控蛋白质表达和肠道微生物的角度综述了杏仁降糖相关机制的研究进展。
1 杏仁中降糖活性物质
杏仁作为药食两用资源,在食品工业与医药领域极具研究价值。其含有的蛋白质、多糖、多酚等非挥发性活性物质,通过调节免疫、抗氧化、改善脂质代谢等机制,展现出增强免疫力、延缓衰老、调节血脂及补脑益智等功效。尤为关键的是,这些活性成分在调控糖代谢、改善胰岛素抵抗方面表现突出,成为新型降血糖药物开发的重要研究对象。因此,不少学者对杏仁的降血糖作用进行了深入研究。
1.1 多肽
多肽类降血糖药物已经成为近年来的研究热点。它是由氨基酸序列组成的特异性蛋白质片段,一般由2个或2个以上20个以下的氨基酸通过肽键聚合而成[7]。常被大众知道的肽类降糖药物有奥曲肽、利拉鲁肽、艾塞那肽等[8],这些多为胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂。
GLP-1受体激动剂的降糖效果明显,且低血糖风险小,没有显著的安全问题,即使在非糖尿病人群中,GLP-1受体激动剂可能会扩大其在治疗心血管疾病方面的用途[9]。但它常发生恶心、呕吐等胃肠道不良反应。另外此药物临床应用时间短,价格相对昂贵[10]。表1列出了各种研究人员对杏仁多肽降糖方面的研究。YUAN等[11]通过质谱鉴定,发现降糖组分含有的肽为RGL、LA、WH、LY、VF、LF、VW和FF。主要含有亮氨酸(L)、苯丙氨酸(F)和色氨酸(W)。此外,丛之慧[12]对杏仁肽进行虚拟筛选,发现了3种降糖肽PR、PGGD、PPK,主要以脯氨酸(P)为主。由此可以推断,疏水性氨基酸在降血糖方面起了关键作用。
表1 杏仁降糖肽
Table 1 Almond hypoglycemic peptides
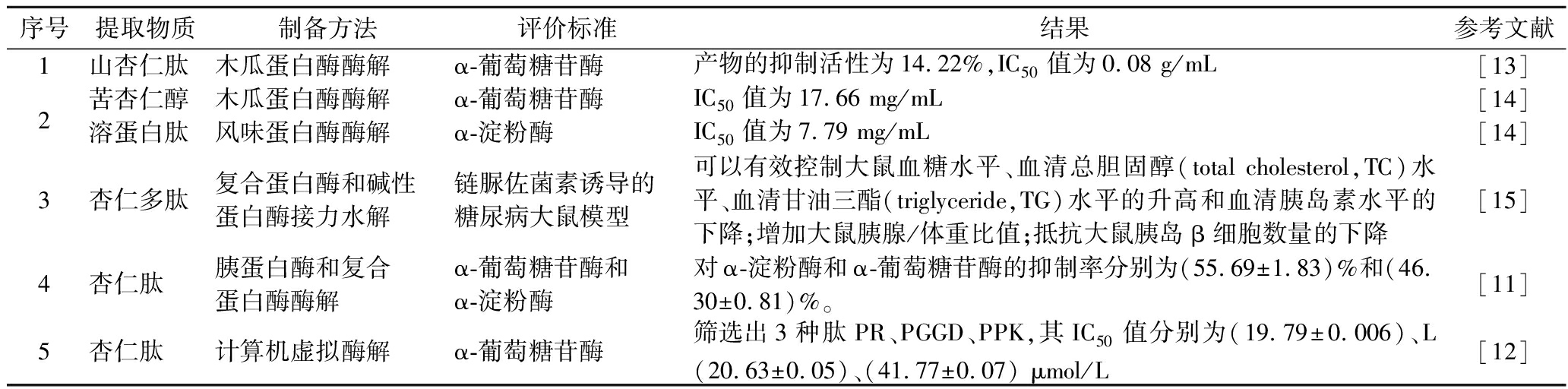
序号提取物质制备方法评价标准结果参考文献1山杏仁肽木瓜蛋白酶酶解α-葡萄糖苷酶产物的抑制活性为14.22%,IC50值为0.08 g/mL[13]2苦杏仁醇木瓜蛋白酶酶解α-葡萄糖苷酶IC50值为17.66 mg/mL[14]溶蛋白肽风味蛋白酶酶解α-淀粉酶IC50值为7.79 mg/mL[14]3杏仁多肽复合蛋白酶和碱性蛋白酶接力水解链脲佐菌素诱导的糖尿病大鼠模型可以有效控制大鼠血糖水平、血清总胆固醇(total cholesterol,TC)水平、血清甘油三酯(triglyceride,TG)水平的升高和血清胰岛素水平的下降;增加大鼠胰腺/体重比值;抵抗大鼠胰岛β细胞数量的下降[15]4杏仁肽胰蛋白酶和复合蛋白酶酶解α-葡萄糖苷酶和α-淀粉酶对α-淀粉酶和α-葡萄糖苷酶的抑制率分别为(55.69±1.83)%和(46.30±0.81)%。[11]5杏仁肽计算机虚拟酶解α-葡萄糖苷酶筛选出3种肽PR、PGGD、PPK,其IC50值分别为(19.79±0.006)、L(20.63±0.05)、(41.77±0.07) μmol/L[12]
1.2 多糖
已经发现具有降糖作用的多糖,例如南瓜多糖、大豆多糖、海藻多糖、酸浆果多糖、樟芝多糖等。目前已有研究阐明了杏仁的有效成分,其中多糖含量为1.73%[16]。彭妍琦[17]运用热水浸提法和酶法,从杏仁中提取出2种杏仁粗多糖(APS和ASDF)。APS由岩藻糖、鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、半乳糖醛酸和葡萄糖醛酸构成,其摩尔比为0.52∶1.18∶8.4∶11.76∶60.35∶2.45∶8.16∶2.78∶4.41。相较而言,ASDF不含甘露糖。在单糖含量方面,APS中占比较大的单糖依次为葡萄糖、半乳糖、阿拉伯糖;ASDF中占比较大的单糖则依次是半乳糖、阿拉伯糖、鼠李糖。
在杏仁中,PENG等[18]从杏仁渣(杏仁冷榨油的副产品)中用热水提取、除蛋白、脱色、醇沉后,经DEAE-52纤维素和SephadexG-100柱层析纯化,得到了杏仁中性多糖(AP-1)。AP-1主要由葡萄糖和微量的阿拉伯糖、半乳糖和甘露糖组成,分子质量为23.408 kDa。推测AP-1的主链由→4)-α-D-Glcp-(1→相互连接组成,支链为α-D-Glcp-(1→连接在→4,6)-α-D-Glcp-(1→的O-6位置。AP-1对α-葡萄糖苷酶有强抑制能力,这可能是因为结构中含有的α-(1→4)糖苷键在起作用。AP-1可作为具有降血糖活性的新型抗糖尿病产品进行探索。
1.3 苦杏仁苷
苦杏仁苷是芳香族氰苷类化合物,分子式C20H27NO11,分子质量为457.43 mg/mol,分子结构式如图1所示[19]。苦杏仁苷是传统中药苦杏仁的主要有效成分,主要是从杏仁、桃仁和其他蔷薇类植物的种子中提取出来,1803年由SCHRADER发现了此类物质,直到1830年ROBIQUET等才将其分离出[20]。
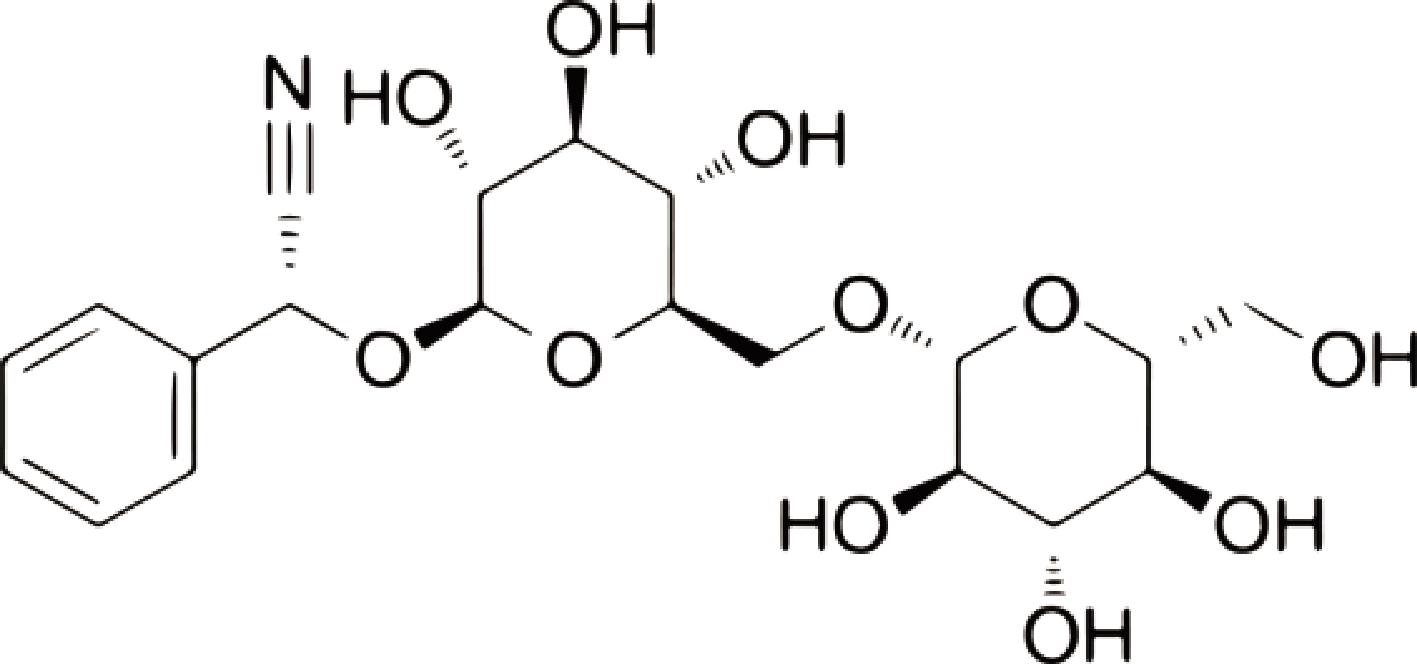
图1 苦杏仁苷结构式
Fig.1 Amygdalin structure
目前,国内外文献围绕苦杏仁苷抗炎、抗癌,以及增强免疫等药理作用展开了大量报道。值得注意的是,研究发现苦杏仁苷在降血糖方面同样具备一定的药理活性。表2列出了研究人员对苦杏仁苷在降糖方面上的研究。
表2 苦杏仁苷降糖作用
Table 2 Hypoglycemic effect of amygdalin

序号动物模型给药剂量给药方式结果参考文献1采用高脂饲料喂养结合链脲佐菌素注射的方法诱导C57BL/6雄性小鼠形成高脂血症糖尿病模型苦杏仁苷高剂量组为0.162 g/kg;低剂量组为0.040 5 g/kg,每天1次,持续9周灌胃给药苦杏仁苷能降低不同状态下小鼠血浆中TG和低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)水平[21]2链脲佐菌素诱导的糖尿病肾病雌性大鼠模型苦杏仁苷3个剂量组,分别为1、3、10 mg/kg,每组8只大鼠,每天1次,持续8周灌胃给药降低体内高血糖、炎症因子和氧化应激。此外,抑制 TGF-α1/Smad 信号通路和细胞外机制降解关键酶的调节也参与了苦杏仁苷抑制肾纤维化进展的机制[22]3链脲佐菌素诱导的糖尿病视网膜病变大鼠模型苦杏仁苷溶液为10 mg/kg前 3 d每天通过阴茎静脉给予,之后每2 d给药1次缓解糖尿病视网膜病变进展,降低糖化血红蛋白(glycated hemoglobin,HbA1c)、血糖水平[23]4用高脂饲料喂养结合链脲佐菌素注射的方法诱导SD雄性大鼠形成糖尿病肾病模型苦杏仁苷低剂量组为3 mg/kg、苦杏仁苷高剂量组为10 mg/kg、AMPK 抑制药组为2.5 mg/kg Compound C、苦杏仁苷高剂量+AMPK 抑制药组为10 mg/kg苦杏仁苷+2.5 mg/kg Compound C,每组10只,每天1次,持续8周苦杏仁苷组分别灌胃相应剂量的苦杏仁苷并腹腔注射等体积质量分数为0.9% NaCl;AMPK抑制药组组腹腔注射Compound C并灌胃等体积 0.9% NaCl苦杏仁苷可通过激活AMPK/mTOR信号通路,从而减轻糖尿病肾病大鼠肾小管上皮细胞损伤[24]5四氧嘧啶诱导的糖尿病雄性小鼠模型3 g/kg的苦杏仁苷腹腔注射苦杏仁苷可以高效清除由四氧嘧啶产生的有害高活性自由基,从而起到预防糖尿病的作用[25]
1.4 多酚
酚类化合物具有药性强、副作用小、生物活性高等优点,已经成为了药物活性成分的研究热点[26]。比起杏仁,多酚主要存在于杏仁皮中,是重要的活性物质。杏仁中含有多种多酚化合物,图2列举了6种杏仁多酚化合物[27]。
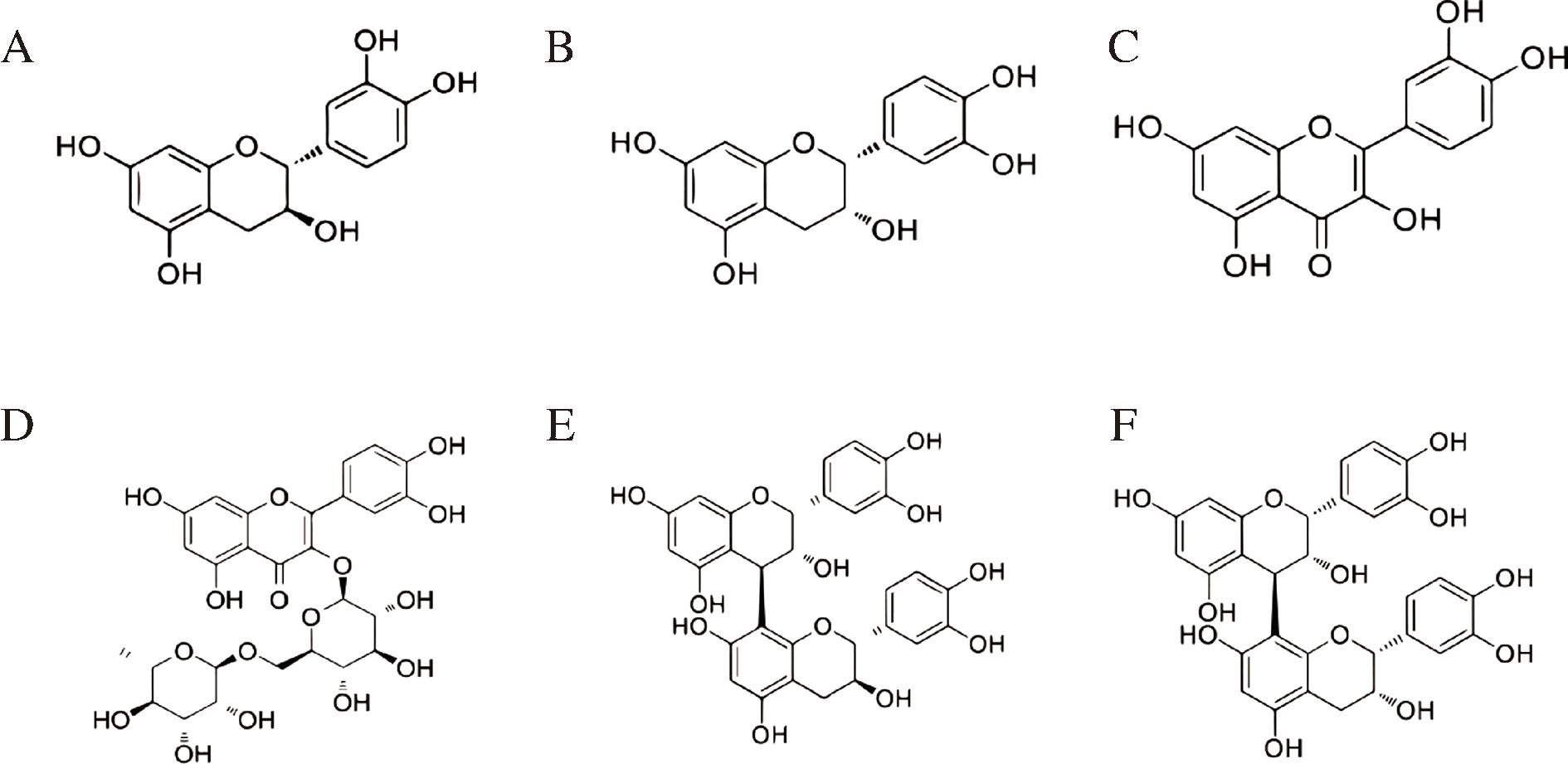
A-(+)-儿茶素;B-表儿茶素;C-槲皮素;D-芦丁;E-原花青素B1;F-原花青素B2
图2 杏仁中6种多酚化合物结构图
Fig.2 Structure of 6 polyphenols in almond
TSUJITA等[28]用70%(质量分数)丙酮提取杏仁皮多酚,超滤后用Sephadex LH-20柱和ODS柱纯化质谱显示,得到的多酚为聚黄烷-3-醇聚合物,对α-淀粉酶抑制率的IC50值为2.2 μg/mL,通过动物实验发现它抑制血糖上升效果呈剂量依赖性,且α-淀粉酶抑制活性增加时,血糖-时间曲线下面积的百分比线性下降,由此证明杏仁皮多酚能抑制碳水化合物吸收。BEN KHADHER等[29]通过系统分离法,发现环己烷、甲醇、二氯甲烷、乙酸乙酯、水提取物对α-淀粉酶都有抑制作用,但仅3个提取物对α-葡萄糖苷酶有抑制作用,依次为甲醇、二氯甲烷和乙酸乙酯提取物,通过高效液相色谱分析发现,主要成分是儿茶素、表儿茶素、芦丁等。儿茶素和表儿茶素的基本结构是黄烷-3-醇。KUMAR等[30]由甲醇提取杏仁多酚,除了发现对α-葡萄糖苷酶和α-淀粉酶有抑制作用外,还测定了二肽激肽酶Ⅳ的IC50值为162.9 μg/mL。
2 杏仁对Ⅱ型糖尿病患者血糖的影响
2.1 杏仁降血糖的临床研究
对于糖尿病患者来说,杏仁是一种理想的食物。它富含多种活性成分,能减缓食物的消化吸收速度,避免血糖快速上升,有助于控制血糖水平。BROWN等[31]发现食用杏仁作为早晨的零食,在实际有意义的程度上改善了急性高血糖,并减少了当天其余时间的能量摄入。GULATI等[32]的研究结果表明,在均衡的健康饮食中加入杏仁,对T2DM患者的腰围、TC、TG、LDL-C、HbA1c、超敏C反应蛋白、脉搏波传导速度都有改善的趋势,而且对血糖和心血管疾病产生了多种有利的影响。另外,建议在每次主餐前30 min食用20 g杏仁,经研究发现[33],这样可改善胰岛素、C肽、胰高血糖素水平以及持续葡萄糖检测系统中的葡萄糖变异性和血糖参数,但对高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)影响不大。LI等[34] 根据国家胆固醇教育计划第二阶段膳食指南来控制饮食。含有杏仁的饮食是把带皮全杏仁添加到餐中,以替代对照饮食20%的热量。研究证实了添加杏仁会降低血清中TC、LDL-C和LDL-C与HDL-C的比值,即杏仁的降胆固醇作用。进一步证实,杏仁添加到国家胆固醇教育计划第二阶段膳食中可以改善LDL-C边缘升高的糖尿病患者的血糖控制和降低体脂。
但BOWEN等[35]让有Ⅱ型糖尿病风险或已患Ⅱ型糖尿病的肥胖人员每日食用杏仁发现在HbA1c、体重、肝脏脂肪和转氨酶、心血管代谢健康和炎症指标方面,没有观察到组间差异(P>0.05)。然而在TC/HDL-C的比率方面,出现了显著的性别治疗时间交互作用(P<0.01),女性在食用杏仁后TC/HDL-C的比率显著降低,但男性则没有。CROUCH等[36]进行了口服葡萄糖耐量前30 min摄入低热量杏仁实验,发现显著降低了具有葡萄糖不耐受个体在1 h的高血糖反应。
2.2 杏仁与其他坚果降糖作用的对比
坚果可被分为树坚果和和地坚果。树坚果包括杏仁、核桃、开心果、腰果等;地坚果则主要指花生,它是我国百姓最常食用的坚果,与树坚果有类似的营养成分。它们都富含不饱和脂肪酸、蛋白质、膳食纤维及其他活性物质,可控制血糖、改善高脂血症,减少炎症反应和氧化应激,从而能降低心血管风险[37-38]。VIGUILIOUK等[37]对树坚果进行了糖尿病患者血糖影响的meta分析,发现树坚果使HbA1c降低0.07%及空腹血糖降低0.15 mmol/L,组间差异具有统计学意义(均P<0.05),说明树坚果在改善血糖方面具有调节作用。但也有研究发现食用坚果虽然对HbA1c和空腹血糖无影响,却显著降低了胰岛素抵抗指数和空腹胰岛素,即食用坚果可改善胰岛素敏感性[39]。用杏仁代表树坚果,花生代表地坚果,王丽丽[40]比较杏仁和花生对T2DM患者血糖、代谢指标及炎症指标的影响,发现花生可改善T2DM患者的空腹血糖检测,但杏仁不仅明显改善T2DM患者的空腹血糖值,还改善了患者的HbA1c及身体质量指数;在为期3个月的实验里,杏仁在改善HbA1c上比花生强,但在炎症指标的改善上稍弱些。此外,HOU等[41]更进一步地在基于低碳水化合物饮食的基础上研究花生和杏仁对血糖的影响,发现它们均能改善T2DM患者的空腹血糖和餐后2 h血糖。因此,无论是杏仁主要富含植物蛋白、多糖等活性物质,还是花生含有丰富的叶酸及植物甾醇等物质,它们在改善血糖方面都起到了一定的作用。
3 杏仁降糖相关干预作用及机制研究进展
进一步探究杏仁改善糖尿病的作用机制,可以为将杏仁提取物在临床应用中的合理使用提供理论依据。杏仁提取物可通过多种机制对糖尿病产生积极影响,其主要的干预作用见图3。
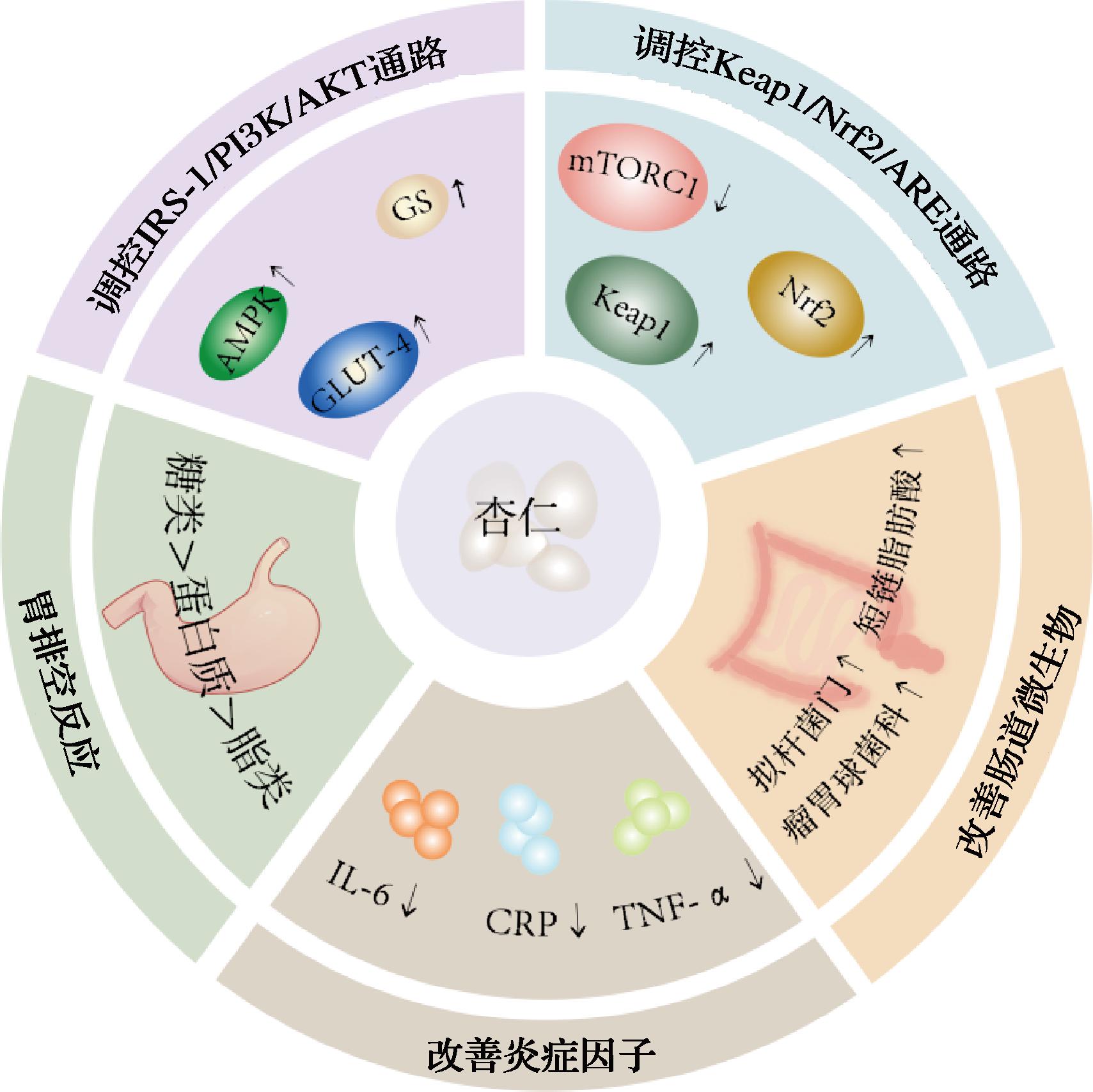
图3 杏仁在降糖方面的干预作用
Fig.3 The intervention role of almonds in lowering blood sugar
注:GLUT-4:葡萄糖转运蛋白4型(glucose transporter type 4);GS:糖原合成酶(glycogen synthase);AMPK:5′-单磷酸激活的蛋白激酶[adenosine 5′-monophosphate (AMP)-activated protein kinase];mTORC1/2:哺乳动物雷帕霉素靶蛋白复合物1/2(mammalian target of rapamycin complex 1/2);Keap1:Kelch样环氧氯丙烷相关蛋白1(Kelch-like ECH-associated protein 1);Nrf2:核呼吸因子2(nuclear factor erythroid-2 related factor 2);CRP:C反应蛋白(C-reactive protein)。
3.1 杏仁通过调控 IRS-1/PI3K/AKT相关通路蛋白质治疗糖尿病
ZENG等[42]认为 IRS-1/PI3K/AKT通路是影响胰岛素抵抗的关键通路。简单来说,如图4所示,活化的胰岛素受体底物1(insulin receptor substrate 1,IRS-1)激活磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K),再使其下游的信号分子蛋白激酶B(protein kinase B,Akt)磷酸化。PI3K是由p85调节亚基和p110催化亚基行成的异二构体,主要是Ⅰ类PI3K的A亚型参与胰岛素信号通路[43]。PI3K使磷酸肌醇依赖性蛋白激酶-1(phosphoinositide-dependent protein kinase-1,PDK1)活化,活化的PDK1通过磷酸化结构域位点导致AKT被激活。在调节糖代谢的通路上,下游里糖原合酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)和叉头框蛋白O(forkhead box protein O,FoxO)是重要的靶标,一个解除糖原合成酶的被抑制状态,促进细胞摄取葡萄糖合成糖原;另一个通过下调磷酸烯醇式丙酮酸羧激酶(phosphoenolpyruvate carboxykinase,PEPCK)和葡萄糖-6-磷酸酶(glucose-6-phosphatase,G6Pase)的表达来抑制糖异生。另外,该通路还可以作用于ATP-柠檬酸裂解酶(ATP-citrate lyase,ACLY)和内皮型一氧化氮合酶(endothelial nitric oxide synthase,eNOS)蛋白来影响脂肪酸合成以及心血管稳态,从而在脂质代谢、血糖调节、细胞生长等方面提供不可或缺的作用。
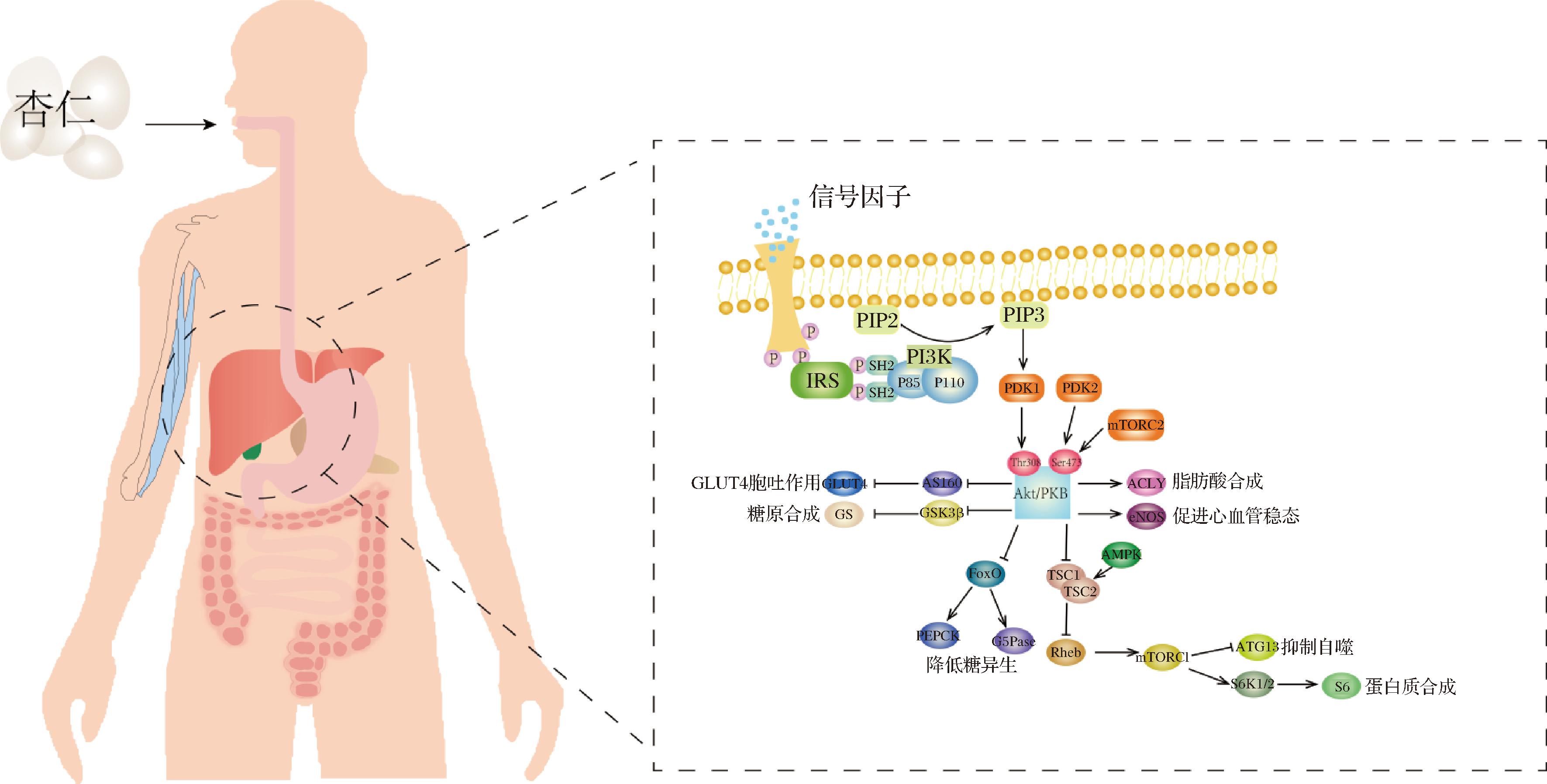
图4 胰岛素/PI3K/AKT通路参与调节葡萄糖
Fig.4 The insulin/PI3K/AKT pathway involved in the regulation of glucose
注:SH2:SH2结构域;PIP2:磷脂酰肌醇-4,5-二磷酸(phosphatidylinositol 4,5-bisphosphate);PIP3:磷脂酰肌醇-3,4,5-三磷酸(phosphatidylinositol 3,4,5-trisphosphate);PDK2:磷酸肌醇依赖性蛋白激酶-2(pyruvate dehydrogenase kinase 2);Thr308:苏氨酸308;Ser473:丝氨酸473;AS160:Akt底物160(Akt substrate of 160 kDa);TSC1/2:结节性硬化复合体1/2(tuberous sclerosis complex 1/2);Rheb:Ras同源富含亮氨酸的脑特异性蛋白(Ras homolog enriched in brain);ATG13:自噬相关蛋白13(autophagy-related protein 13);S6k1/2:核糖体蛋白S6激酶1/2(ribosomal protein S6 kinase 1/2);S6:核糖体蛋白S6。
丛之慧[12]在此基础上认为调控IRS-1/PI3K/Akt和AMPK通路可以改善胰岛素抵抗,杏仁肽处理后,与模型组相比,GLUT-4整体表达量跟易位现象显著升高,GSK-3β的Ser9磷酸化量跟GS表达水平显著增加。另外PI3K的Tyr317表达水平和Akt在Ser473的磷酸化水平得到了不同程度的改善,从而通过信号通路减轻胰岛素抵抗症状。总的来说,杏仁肽不仅能通过提高Ser9位GSK-3β磷酸化水平,提高GS表达水平,恢复AMPK的Thr172磷酸化,促进糖原合成,还可以通过上调GLUT-4蛋白的表达及转运来改善葡萄糖摄取。闫萌萌等[24]通过给大鼠灌食苦杏仁苷和AMPK/mTOR通路抑制药Compound C发现,与苦杏仁苷高剂量组相比,苦杏仁苷高剂量和Compound C组大鼠TNF-α、IL-1β、细胞凋亡率、p-mTOR/mTOR等水平均显著升高,p-AMPK/AMPK、Beclin1均显著降低,说明抑制该通路会加重损伤,进一步表明苦杏仁苷改善损伤的作用可能是通过激活AMPK/mTOR通路来实现的。
上述研究表明,杏仁可以降低血糖、改善胰岛素抵抗,其机制可能与调控机体的各类蛋白质的表达水平有关,通过调控IRS-1/PI3K/Akt通路、AMPK通路等,实现杏仁治疗糖尿病的相关药理作用。
3.2 杏仁通过调控 Keap1/Nrf2/ARE相关通路蛋白质治疗糖尿病
健康状况良好的情况下,人体对活性氧的生成和清除处于相约制衡的状态,但当人体内活性氧过度产生时,就会导致体内细胞受到氧化损伤,进而导致各种疾病的产生。抑制氧化应激,也就是抑制糖尿病及其并发症的发展。韩金承[44]通过醇酶法提取,得到主要成分是油酸甲酯的杏仁油,由体外和体内实验验证了杏仁油具有抗氧化能力,具体为苦杏仁油对1,1-二苯基-2-三硝基苯肼、超氧阴离子自由基、羟自由基清除力和对Fe3+的还原力都有一定的清除能力,能提升小鼠血清超氧化物歧化酶(superoxide dismutase,SOD)活力、降低丙二醛(malondialdehyde,MDA)含量。GAO等[45]同样是通过动物实验发现杏仁油使MDA下降,SOD和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)的活性增高,另外显著降低了高脂饮食大鼠的TC、TG和LDL-C水平,并提高了HDL-C水平。由此推测,这可能通过Nrf2/ARE通路发挥抗氧化作用。Nrf2在细胞内发挥着关键的抗氧化应激作用,主要在细胞质中存在。正常生理状态下,Nrf2 与Keap1的蛋白结合,这种结合使得Nrf2处于一种非活性状态,当受到氧化应激或化学物质诱导时,会使Keap1与Nrf2的结合能力下降,从而导致Nrf2被激活。当它进入细胞核后,会形成Nrf2-Maf异二聚体与 ARE结合,从而启动下游抗氧化酶基因的表达。下游抗氧化基因包括SOD基因、GSH-Px基因、HO-1基因、过氧化氢酶基因、谷胱甘肽-S-转移酶基因等。陈默[46]通过细胞实验发现杏仁肽使Keap1蛋白表达水平显著下降,Nrf2和HO-1的蛋白表达水平显著上升。刘蕊[47]用链脲佐菌素诱导T2DM雄性大鼠,分别用蒸馏水、杏仁油、葵花籽油灌胃4周。结果显示,杏仁油可以显著降低糖尿病大鼠Keap1蛋白,上调糖尿病大鼠肝脏组织中Nrf2、HO-1和NQO1蛋白的表达量。通过体外实验和体内实验都表明了杏仁的活性物质可以激活Nrf2/ARE信号通路,增加抗氧化酶的表达量,从而增加血液和肝脏中的抗氧化能力,减轻胰岛素抵抗,因此达到调节血糖水平的作用。
3.3 杏仁通过改善肠道微生物治疗糖尿病
健康的肠道环境是人体生理和代谢活动的重要环境,肠道菌群紊乱在糖尿病发病和发展过程中起着重要作用,图5为肠道菌群对胰岛素分泌的作用机制。健康人的肠道细菌组成更多样化,而肥胖或糖尿病患者的肠道微生物群多样性减少,条件致病菌更多,有益微生物群较少[48]。OJO等[49]研究发现以杏仁为基础的饮食可以促进产生短链脂肪酸的肠道微生物群的生长,与REN等[50]的研究结果一致。另外,在ZHAO等[51]的研究中发现,促进产生短链脂肪酸的菌通过GLP-1的产生改善了T2DM患者的HbA1c水平。胡安妮[52]在此基础上研究发现杏仁的低碳水化合物饮食模式能增加拟杆菌门数量、提高拟杆菌门/厚壁菌门相对丰度比、增加产短链脂肪酸菌群数量;同时维持空腹血浆GLP-1浓度于基线时水平,且GLP-1水平越高者其血糖控制效果越好。基于此,可初步推断基于杏仁的低碳水化合物饮食模式可能通过肠道菌群-SCFAS-GLP-1途径发挥降糖作用。
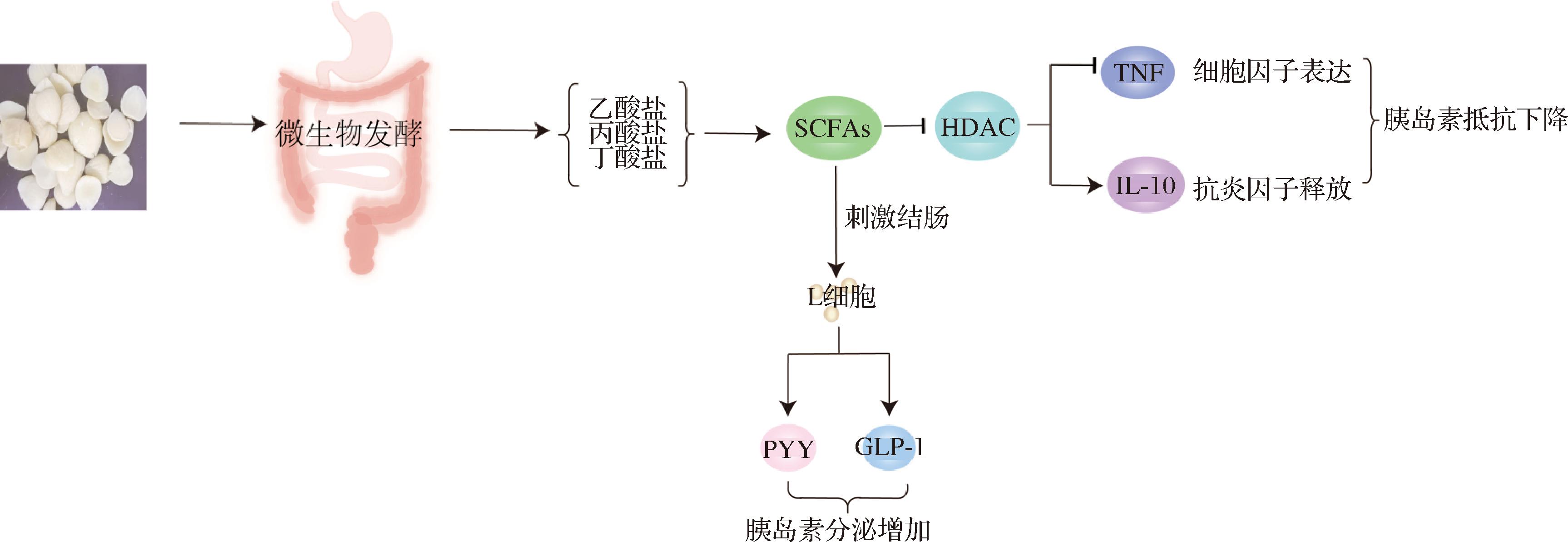
图5 肠道菌群对胰岛素分泌的作用机制
Fig.5 Mechanism of action of gut microbiota on insulin secretion
注:SCFAs:短链脂肪酸(short-chain fatty acids);TNF:肿瘤坏死因子(tumor necrosis factor);PYY:酪酪肽(peptide YY)。
在肠道中,优势门(约90%)以厚壁菌门和拟杆菌门为代表,包括乳杆菌属、芽孢杆菌属、梭菌属、肠球菌属和瘤胃球菌属(第一门)以及拟杆菌属和普雷沃菌属(第二门)[53]。瘤胃球菌科与胰岛素水平正相关,这被认为是调节血糖水平和肥胖的关键。CHOO等[54]研究发现,在超重或肥胖、血糖升高的成年人中,经常食用杏仁促进了粪便微生物组成的适度变化,特别是增加了瘤胃菌外家族中3个操作分类单元(operational taxonomic unit,OTU)的丰度,降低了粪便pH和水分含量。然而,这些变化与粪便短链脂肪酸含量或肠道通透性的显著变化无关。
以上研究表明,杏仁还能通过调节肠道微生物,产生短链脂肪酸,一方面达到增加GLP-1的效果,另一方面使瘤胃球菌属增加,从而对胰岛素抵抗有一定的改善作用,延缓糖尿病的发展速度,从而治疗疾病。
3.4 杏仁通过改善炎症因子治疗糖尿病
参与炎症反应的各种细胞因子被称为炎症因子,常见的有IL-6、TNF-α等因子。炎症标记物是指机体受到微生物入侵或组织损伤等炎症性刺激时,机体内含量骤然升高的蛋白。近年来可以用IL-6、TNF-α、CRP来反应炎症情况。炎症因子与糖尿病也有一定的关系,如TNF-α会间接使得胰岛素受体底物-1的丝氨酸残基磷酸化,从而阻隔胰岛素信号传递,使胰岛素敏感性下降,导致胰岛素抵抗。另外,IL-6还可以刺激脂肪细胞分解,使游离脂肪酸释放,从而抑制肌肉和肝脏对胰岛素的摄取和利用。
彭妍琦[17]探讨了杏仁多糖对细胞和动物的抗炎作用,在细胞里,杏仁多糖可降低IL-1β、TNF-α、IL-6和iNOS的mRNA表达,通过动物实验,又验证了可以降低细胞促炎因子TNF-α、IL-1β、IL-6和IL-18的mRNA表达量,并提升抗炎细胞因子IL-10的水平。此外,LIU等[55]对20例超重的T2DM患者进行为期4周的杏仁干预,结果显示,与对照组比较,杏仁可降低IL-6 10.3%、CRP 10.3%及TNF-α 15.7%。GULATI等[32]还发现食用杏仁24周后CRP有显著改善。由此可见,杏仁可改善T2DM患者的血糖、血脂及炎症反应。SWEAZEA等[56]发现在没有进一步饮食指导的情况下补充杏仁,与被指示维持其习惯饮食的对照组相比,杏仁治疗组的炎症生物标志物CRP显著降低。但也有不少研究人员发现食用杏仁对IL-6、CRP和TNF-α不显著[35,41,49],即杏仁无法改善炎症反应。
因此,随着代谢性炎症概念的提出,慢性炎症在糖尿病中的影响越来越被人们所关注,但杏仁是否可以改善炎症还存在一定的争议性,需要进一步的实验探究。
3.5 杏仁通过胃排空反应治疗糖尿病
胃排空是一个复杂的过程,指的是食物由胃进入十二指肠的过程。胃内促进排空的因素和十二指肠抑制排空的因素相互协调,使胃内容物能够以适当的速度进入十二指肠,保证食物的消化和吸收顺利进行。3种主要食物成分(糖类、蛋白质类、脂类)中糖类排空最快,蛋白质次之,脂类最慢。食物进入小肠后,受肠道神经和激素双重调节,会负反馈调节胃排空速率,延缓食物进入小肠,延缓葡萄糖在小肠内的吸收,维持餐后血糖在正常水平[57]。JOSSE等[58]观察发现在含有50 g碳水化合物的面包餐中添加90 g杏仁时,健康成人的餐后2 h血糖浓度峰值显著降低43%。这些研究人员认为杏仁的降血糖作用是因为杏仁富含脂肪和蛋白质,使胃排空率的降低。COHEN等[59]对随机分为2组的T2DM患者进行了一项小型慢性研究,2个干预组每周5 d分别吃杏仁补充剂(1盎司)和奶酪(2根),持续12周。干预后,杏仁组HbA1c水平显著降低。作者认为,观察到的杏仁降血糖作用可能是由于杏仁中主要含有脂肪和蛋白质,这使胃排空减慢;也可能是由于存在多酚,主要是里面的黄酮类化合物,有助于控制血糖水平,抑制淀粉酶。
故杏仁中含有大量的脂肪和蛋白质,其消化缓慢,可延缓胃排空及稀释的速度,可为机体持续供能[60],但胃排空率减慢是归因于脂肪和蛋白质成分的一种机制,很难说到底是哪种机制发挥了更重要的作用。还需要进一步对机制的研究来阐明杏仁降糖的主要机制。
4 结论与讨论
现有研究多围绕杏仁相关饮食来开展临床试验,来证明杏仁有降低血糖的功能。然而患者是服用的整杏仁,致使目前研究人员不清楚是杏仁哪一营养物质起作用。杏仁里含有多种营养物质,可以从杏仁里提取出蛋白、多糖、苦杏仁苷、多酚等活性物质。这篇综述就活性物质的降糖作用、杏仁饮食在改善血糖方面起作用以及杏仁降糖机制进行了总结。然而杏仁的活性物质复杂多样,研究人员对此了解有限,因此需要在未来研究中进一步筛选杏仁降糖活性物质,明确杏仁降糖的主要途径,深度挖掘其降糖机制。有助于在未来控制血糖、研发相关功能食品提供帮助。
[1] 薛紫鲸,张丹,郭龙,等.经典名方中苦杏仁的本草考证[J].中国实验方剂学杂志,2022,28(10):207-214.XUE Z J,ZHANG D,GUO L,et al.Herbal textual research on bitter almond in classic prescriptions[J].Chinese Journal of Experimental Traditional Medical Formulae,2022,28(10):207-214.
[2] 吴月亮,许淼,董胜君,等.不同产区苦杏仁营养成分分析[J].食品工业科技,2019,40(23):300-305.WU Y L,XU M,DONG S J,et al.Analysis of nutritional composition of bitter almond from different growing areas[J].Science and Technology of Food Industry,2019,40(23):300-305.
[3] NING C,JIAO Y H,WANG J Q,et al.Recent advances in the managements of type 2 diabetes mellitus and natural hypoglycemic substances[J].Food Science and Human Wellness,2022,11(5):1121-1133.
[4] CHATTOPADHYAY R,CHATTOPADHYAY R N,NANDY A,et al.Preliminary report on antihyperglycemic effect of a fraction of fresh leaves of Azadirachta indica (Beng.Neem)[J].Bulletin of the Calcutta School of Tropical Medicine,1987,35(2):29-33.
[5] LI W L,ZHENG H C,BUKURU J,et al.Natural medicines used in the traditional Chinese medical system for therapy of diabetes mellitus[J].Journal of Ethnopharmacology,2004,92(1):1-21.
[6] ONG K L,STAFFORD L K,MCLAUGHLIN S A,et al.Global,regional,and national burden of diabetes from 1990 to 2021,with projections of prevalence to 2050:A systematic analysis for the Global Burden of Disease Study 2021[J].Lancet,2023,402(10397):203-234.
[7] 王海东.五味子蛋白肽的制备和生物活性研究[D].长春:长春中医药大学,2023.WANG H D.Study on preparation and biological activity of Sehizandrae chinensis protein peptide[D].Changchun:Changchun University of Chinese Medicine,2023.
[8] 张晓艺,王晗,裴栋,等.食品蛋白来源的降血糖肽的研究进展[J].生物技术,2022,32(4):528-535;505.ZHANG X Y,WANG H,PEI D,et al.Research progress of hypoglycemic peptides derived from food protein[J].Biotechnology,2022,32(4):528-535;505.
[9] 柯志强,马倩倩,李丹,等.GLP-1受体激动剂对心血管作用的研究进展[J].中国药理学通报,2024,40(3):426-430.KE Z Q,MA Q Q,LI D,et al.Advances on cardiovascular effects of GLP-1RAs[J].Chinese Pharmacological Bulletin,2024,40(3):426-430.
[10] 郑彩云,林妹妹,戴亨纷.GLP-1受体激动剂致2型糖尿病患者胃肠道不良反应的网状Meta分析[J].中国新药与临床杂志,2024,43(6):460-468.ZHENG C Y,LIN M M,DAI H F.GLP-1 receptor agonists cause gastrointestinal adverse reaction in patients with type 2 diabetes mellitus:A network meta-analysis[J].Chinese Journal of New Drugs and Clinical Remedies,2024,43(6):460-468.
[11] YUAN X,LI P C,XIAO Z W,et al.Preparation and identification of hypoglycemic bioactive peptide from Amygdalus communis L.by multienzyme hydrolysis[J].Process Biochemistry,2024,136:292-300.
[12] 丛之慧.基于虚拟筛选杏仁降糖肽及纳米包埋技术研究[D].重庆:重庆三峡学院,2023.CONG Z H.Research on virtual screening of hypoglycemic peptides from almonds and nanoparticle encapsulation technology[D].Chongqing:Chongqing Three Gorges University,2023.
[13] 王晟.山杏(Armeniaca sibirica)仁蛋白辅助降血糖饮料开发[D].北京:北京林业大学,2014.WANG S.Development of antidiabetic beverage from apricot (Armeniaca sibirica) kernel protein[D].Beijing:Beijing Forestry University,2014.
[14] 武安琪.基于苦杏仁醇溶蛋白的降血糖肽饮料制备工艺研究[D].乌鲁木齐:新疆农业大学,2021.WU A Q.Preparation of a bitter almond kernel prolamin based hypoglycemic peptide drink[D].Urumqi:Xinjiang Agricultural University,2021.
[15] 刘雪峰.酶解杏仁蛋白制备活性多肽及其降血糖功能研究[D].呼和浩特:内蒙古农业大学,2010.LIU X F.Study on preparation of polypeptides by enzymolysis almond protein and their reducing blood glucose effectives[D].Hohhot:Inner Mongolia Agricultural University,2010.
[16] 李志洲,刘军海.甜杏仁有效成份分析及多糖的体外抗氧化性研究[J].氨基酸和生物资源,2008,30(4):34-36;41.LI Z Z,LIU J H.Study on composition and property of anti-oxidization of polysaccharides in sweet almond[J].Amino Acids &Biotic Resources,2008,30(4):34-36;41.
[17] 彭妍琦.杏仁多糖的结构表征及其改善溃疡性结肠炎的机制研究[D].沈阳:沈阳农业大学,2024.PEMG Y Q.Structural characterization of almond polysaccharides and their mechanism of amelioration of ulcerative colitis[D].Shenyang:Shenyang Agricultural University,2024.
[18] PENG Y Q,ZHANG Z H,CHEN W Y,et al.Structural characterization,α-glucosidase inhibitory activity and antioxidant activity of neutral polysaccharide from apricot(Armeniaca Sibirica L.Lam) kernels[J].International Journal of Biological Macromolecules,2023,238:124109.
[19] 雷甜甜.苦杏仁苷抑制LDLR-/-小鼠动脉粥样硬化的作用及机制研究[D].成都:电子科技大学,2020.LEI T T.The inhibiting effect and possible mechanisms of amygdalin on atherosclerosis in LDL receptor-deficient mice[D].Chengdu:University of Electronic Science and Technology of China,2020.
[20] 吕建珍,邓家刚.苦杏仁苷的药理作用研究进展[J].现代药物与临床,2012,27(5):530-535.LV J Z,DENG J G.Research progress in pharmacological effects of amygdalin[J].Drugs &Clinic,2012,27(5):530-535.
[21] 李彦灵.苦杏仁降血脂部位筛选及质量标准制定[D].广州:广州中医药大学,2013.LI Y L.Selecting the hypolipidemic parts of armeniacae semen and studying on its quality standard[D].Guangzhou:Guangzhou University of Chinese Medicine,2013.
[22] CHEN J W,HU Y B,MOU X,et al.Amygdalin alleviates renal injury by suppressing inflammation,oxidative stress and fibrosis in streptozotocin-induced diabetic rats[J].Life Sciences,2021,265:118835.
[23] LI S Y,LU S H,WANG L,et al.Effects of amygdalin on ferroptosis and oxidative stress in diabetic retinopathy progression via the NRF2/ARE signaling pathway[J].Experimental Eye Research,2023,234:109569.
[24] 闫萌萌,徐林丽,刘岩岩,等.苦杏仁苷对糖尿病肾病大鼠肾小管上皮细胞损伤的影响[J].中国临床药理学杂志,2024,40(7):1019-1023.YAN M M,XU L L,LIU Y Y,et al.Effects of amygdalin on renal tubular epithelial cell injury in diabetes nephropathy rats[J].The Chinese Journal of Clinical Pharmacology,2024,40(7):1019-1023.
[25] HEIKKILA R E,CABBAT F S.The prevention of alloxan-induced diabetes by amygdalin[J].Life Sciences,1980,27(8):659-662.
[26] 黄首瑜,方忠雪,孙长海,等.苦杏仁皮多聚多酚的结构研究[J].沈阳药科大学学报,2025,42(6):578-585.HUANG S Y,FANG Z X,SUN C H,et al.Compositional characterization of polymeric polyphenols from bitter almond skins[J].Journal of Shenyang Pharmaceutical University,2025,42(6):578-585.
[27] BOLLING B W.Almond polyphenols:Methods of analysis,contribution to food quality,and health promotion[J].Comprehensive Reviews in Food Science and Food Safety,2017,16(3):346-368.
[28] TSUJITA T,SHINTANI T,SATO H.α-Amylase inhibitory activity from nut seed skin polyphenols.1.Purification and characterization of almond seed skin polyphenols[J].Journal of Agricultural and Food Chemistry,2013,61(19):4570-4576.
[29] BEN KHADHER T,SASSI-AYDI S,AYDI S,et al.Phytochemical profiling and biological potential of Prunus dulcis shell extracts[J].Plants,2023,12(14):2733.
[30] KUMAR V,SACHAN R,RAHMAN M,et al.Prunus amygdalus extract exert antidiabetic effect via inhibition of DPP-IV:In-silico and In-vivo approaches[J].Journal of Biomolecular Structure and Dynamics,2021,39(11):4160-4174.
[31] BROWN R,WARE L,GRAY A R,et al.Snacking on almonds lowers glycaemia and energy intake compared to a popular high-carbohydrate snack food:An acute randomised crossover study[J].International Journal of Environmental Research and Public Health,2021,18(20):10989.
[32] GULATI S,MISRA A,PANDEY R M.Effect of almond supplementation on glycemia and cardiovascular risk factors in Asian Indians in north India with type 2 diabetes mellitus:A 24-week study[J].Metabolic Syndrome and Related Disorders,2017,15(2):98-105.
[33] GULATI S,MISRA A,TIWARI R,et al.Beneficial effects of premeal almond load on glucose profile on oral glucose tolerance and continuous glucose monitoring:Randomized crossover trials in Asian Indians with prediabetes[J].European Journal of Clinical Nutrition,2023,77(5):586-595.
[34] LI S C,LIU Y H,LIU J F,et al.Almond consumption improved glycemic control and lipid profiles in patients with type 2 diabetes mellitus[J].Metabolism,2011,60(4):474-479.
[35] BOWEN J,LUSCOMBE-MARSH N D,STONEHOUSE W,et al.Effects of almond consumption on metabolic function and liver fat in overweight and obese adults with elevated fasting blood glucose:A randomised controlled trial[J].Clinical Nutrition ESPEN,2019,30:10-18.
[36] CROUCH M A,SLATER R T 3rd.Almond “appetizer” effect on glucose tolerance test (GTT) results[J].Journal of the American Board of Family Medicine,2016,29(6):759-766.
[37] VIGUILIOUK E,KENDALL C W C,BLANCO MEJIA S,et al.Effect of tree nuts on glycemic control in diabetes:A systematic review and meta-analysis of randomized controlled dietary trials[J].PLoS One,2014,9(7):e103376.
[38] YU Z,MALIK V S,KEUM N,et al.Associations between nut consumption and inflammatory biomarkers[J].The American Journal of Clinical Nutrition,2016,104(3):722-728.
[39] TINDALL A M,JOHNSTON E A,KRIS-ETHERTON P M,et al.The effect of nuts on markers of glycemic control:A systematic review and meta-analysis of randomized controlled trials[J].The American Journal of Clinical Nutrition,2019,109(2):297-314.
[40] 王丽丽.不同种类坚果对2型糖尿病患者血糖控制的影响[D].苏州:苏州大学,2017.WANG L L.Effect of different types of nuts on glycemic control in patients with type 2 diabetes mellitus[D].Suzhou:Soochow University,2017.
[41] HOU Y Y,OJO O,WANG L L,et al.A randomized controlled trial to compare the effect of peanuts and almonds on the cardio-metabolic and inflammatory parameters in patients with type 2 diabetes mellitus[J].Nutrients,2018,10(11):1565.
[42] ZENG X Q,ZHANG C M,TONG M L,et al.Knockdown of NYGGF4 increases glucose transport in C2C12 mice skeletal myocytes by activation IRS-1/PI3K/AKT insulin pathway[J].Journal of Bioenergetics and Biomembranes,2012,44(3):351-355.
[43] 苏通.番石榴叶对2型糖尿病db/db小鼠肝脏PI3K/AKT信号通路的影响探究[D].北京:北京中医药大学,2023.SU T.Investigation of the Effect of Psidium guajava leaves on the PI3K/AKT signaling pathway in the liver of type 2 diabetic db/db mice[D].Beijing:Beijing University of Chinese Medicine,2023.
[44] 韩金承.苦杏仁油提取、抗氧化活性及微胶囊制备研究[D].锦州:锦州医科大学,2023.HAN J C.Study on extraction,antioxidant activity and micro-capsule preparation of bitter almond oil[D].Jinzhou:Jinzhou Medical University,2023.
[45] GAO Y,LI C,CHEN B,et al.Anti-hyperlipidemia and antioxidant activities of Amygdalus pedunculata seed oil[J].Food &Function,2016,7(12):5018-5024.
[46] 陈默.珍珠油杏杏仁蛋白和抗氧化肽的制备及功能活性研究[D].泰安:山东农业大学,2022.CHEN M.Preparation and functional activity of almond protein and antioxidant peptides from Zhenzhuyou apricot[D].Tai'an:Shandong Agricultural University,2022.
[47] 刘蕊.杏仁油对Ⅰ型糖尿病大鼠的保护作用及机制研究[D].保定:河北农业大学,2021.LIU R.Study on the protective effect and mechanism of almond oil on type I diabetic rats[D].Baoding:Hebei Agricultural University,2021.
[48] SU M,HU R,TANG T,et al.Review of the correlation between Chinese medicine and intestinal microbiota on the efficacy of diabetes mellitus[J].Frontiers in Endocrinology,2022,13:1085092.
[49] OJO O,WANG X H,OJO O O,et al.The effects of almonds on gut microbiota,glycometabolism,and inflammatory markers in patients with type 2 diabetes:A systematic review and meta-analysis of randomised controlled trials[J].Nutrients,2021,13(10):3377.
[50] REN M X,ZHANG H Y,QI J D,et al.An almond-based low carbohydrate diet improves depression and glycometabolism in patients with type 2 diabetes through modulating gut microbiota and GLP-1:A randomized controlled trial[J].Nutrients,2020,12(10):3036.
[51] ZHAO L P,ZHANG F,DING X Y,et al.Gut bacteria selectively promoted by dietary fibers alleviate type 2 diabetes[J].Science,2018,359(6380):1151-1156.
[52] 胡安妮.基于杏仁的低碳水化合物饮食方案应用于2型糖尿病患者的可行性分析及降糖机制探索[D].苏州:苏州大学,2020.HU A N.Feasibility of low carbohydrate diet based on almonds applied to type 2 diabetes mellitus and its mechanism of hypoglycemic effect[D].Suzhou:Soochow University,2020.
[53] CRACIUN C I,NEAG M A,CATINEAN A,et al.The relationships between gut microbiota and diabetes mellitus,and treatments for diabetes mellitus[J].Biomedicines,2022,10(2):308.
[54] CHOO J M,TRAN C D,LUSCOMBE-MARSH N D,et al.Almond consumption affects fecal microbiota composition,stool pH,and stool moisture in overweight and obese adults with elevated fasting blood glucose:A randomized controlled trial[J].Nutrition Research,2021,85:47-59.
[55] LIU J F,LIU Y H,CHEN C M,et al.The effect of almonds on inflammation and oxidative stress in Chinese patients with type 2 diabetes mellitus:A randomized crossover controlled feeding trial[J].European Journal of Nutrition,2013,52(3):927-935.
[56] SWEAZEA K L,JOHNSTON C S,RICKLEFS K D,et al.Almond supplementation in the absence of dietary advice significantly reduces C-reactive protein in subjects with type 2 diabetes[J].Journal of Functional Foods,2014,10:252-259.
[57] KUO P,RAYNER C K,HOROWITZ M.Gastric emptying,diabetes,and aging[J].Clinics in Geriatric Medicine,2007,23(4):785-808.
[58] JOSSE A R,KENDALL C W C,AUGUSTIN L S A,et al.Almonds and postprandial glycemia:A dose-response study[J].Metabolism,2007,56(3):400-404.
[59] COHEN A E,JOHNSTON C S.Almond ingestion at mealtime reduces postprandial glycemia and chronic ingestion reduces hemoglobin A1c in individuals with well-controlled type 2 diabetes mellitus[J].Metabolism,2011,60(9):1312-1317.
[60] COLLIER G,O’DEA K.The effect of coingestion of fat on the glucose,insulin,and gastric inhibitory polypeptide responses to carbohydrate and protein[J].The American Journal of Clinical Nutrition,1983,37(6):941-944.