5-羟基色氨酸(5-hydroxytryptophan,5-HTP),由色氨酸5′位羟基化形成,为非蛋白质组成的天然氨基酸。它可以通过血脑屏障,提高人脑中褪黑素的水平,减少体内细胞因子的产生,在情绪、睡眠、食欲及心血管功能的调节中起到关键作用[1]。目前,以5-HTP为主要原料的保健品已经在20多个国家和地区投入生产,具有广阔的市场需求和光明的应用前景。
目前,5-HTP主要从加纳籽中提取获得,但由于这种方法受到季节限制和进口依赖,难以满足庞大的市场需求[2]。化学合成法由于其繁琐的步骤和严苛的反应条件限制了其在大规模生产中的应用。因此,近年来研究人员将目光转向易操作、不受季节控制的微生物法生产5-HTP。ZHANG等[3]通过色氨酸羟化酶表达体系优化、L-色氨酸与四氢生物蝶呤(tetrahydrobiopterin,BH4)合成底盘细胞构建,实现了5 L生物反应器内8.58 g/L 5-HTP积累,但存在反应产物复杂、分离困难的缺点。
色氨酸羟化酶通过羟基化色氨酸生成5-HTP(图1)。真核来源的色氨酸羟化酶需要Fe2+和BH4作为辅因子,氧气作为共底物[4],催化色氨酸5′位羟基化生成5-HTP,同时生成过氧化氢。WANG等[5]通过半理性设计色氨酸羟化酶、核糖体结合位点优化与多酶催化体系构建,通过外源添加辅因子成功实现了89%的高摩尔转化率;SONG等[6]通过理性设计得到了TPH1双点突变体,将色氨酸羟化酶催化活性提升了2.06倍,实现了0.91 g/L的产物积累;WANG等[7]通过对TPH1进行C、N端截短优化成功使酶活提升2.6倍,通过酶的体外级联催化实现了73.6%的底物转化率和36.9 mmol/L的产物积累。尽管人源色氨酸羟化酶已取得了显著成果,但酶转化率仍有待提升。因此,需要挖掘更有潜力的色氨酸羟化酶。
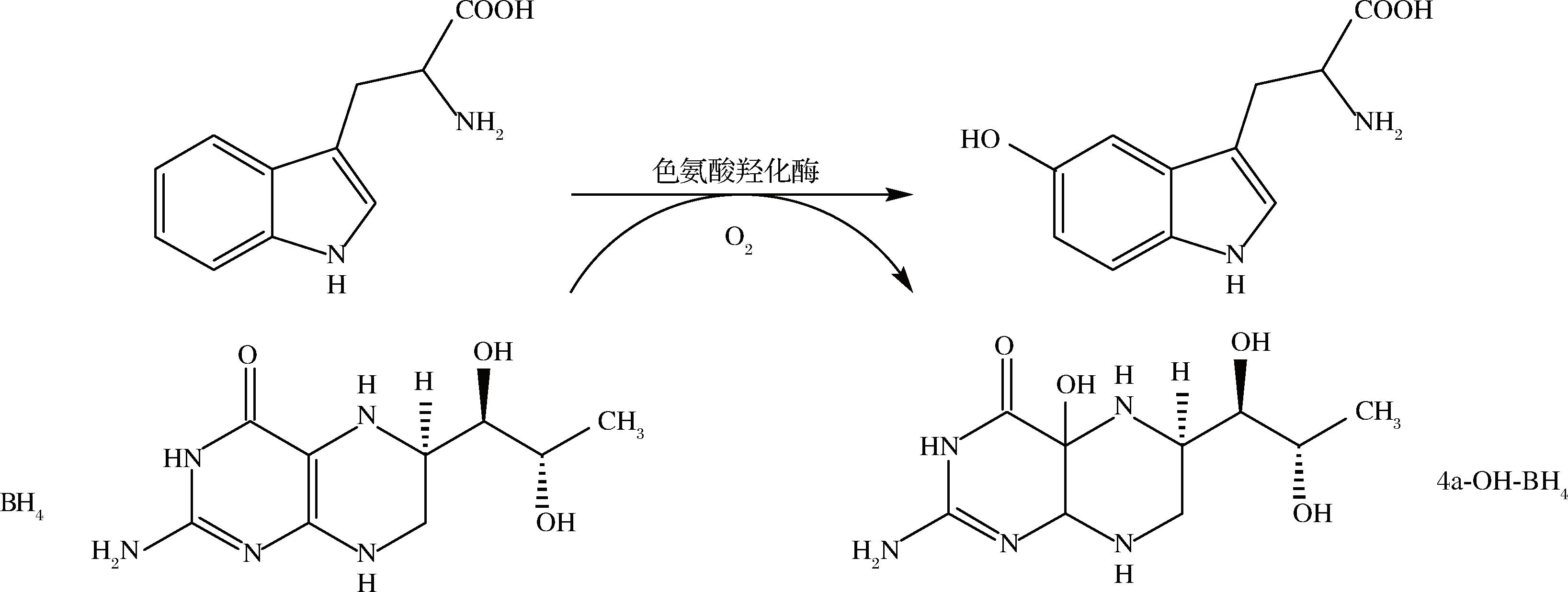
图1 色氨酸羟化酶催化合成5-HTP
Fig.1 Tryptophan hydroxylase catalyzes the synthesis of 5-HTP
本研究工作主要围绕线虫来源色氨酸羟化酶DJTPH开展。首先,通过敲除大肠杆菌BL21(DE3)中的色氨酸酶,减少底物和产物的降解。然后,通过添加促溶标签、N端截短、启动子优化以及产酶条件优化,成功提升了色氨酸羟化酶的表达量和催化活性,将底物质量转化率从7.5%提升至48%。最后,通过理性设计酶分子突变位点以及体外添加辅因子,实现了98%的底物质量转化率,为5-HTP的工业化生产提供了新的发展方向。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
大肠杆菌Escherichia coli BL21 (DE3)、质粒pET28a、质粒pTargetF-sgRNA和质粒pEcCas9均由作者所在实验室保藏。菌株B00~B12和质粒pET00~pET12由本研究构建。
本研究使用的质粒列于表1。
表1 本研究使用的质粒
Table 1 Plasmid used in this study
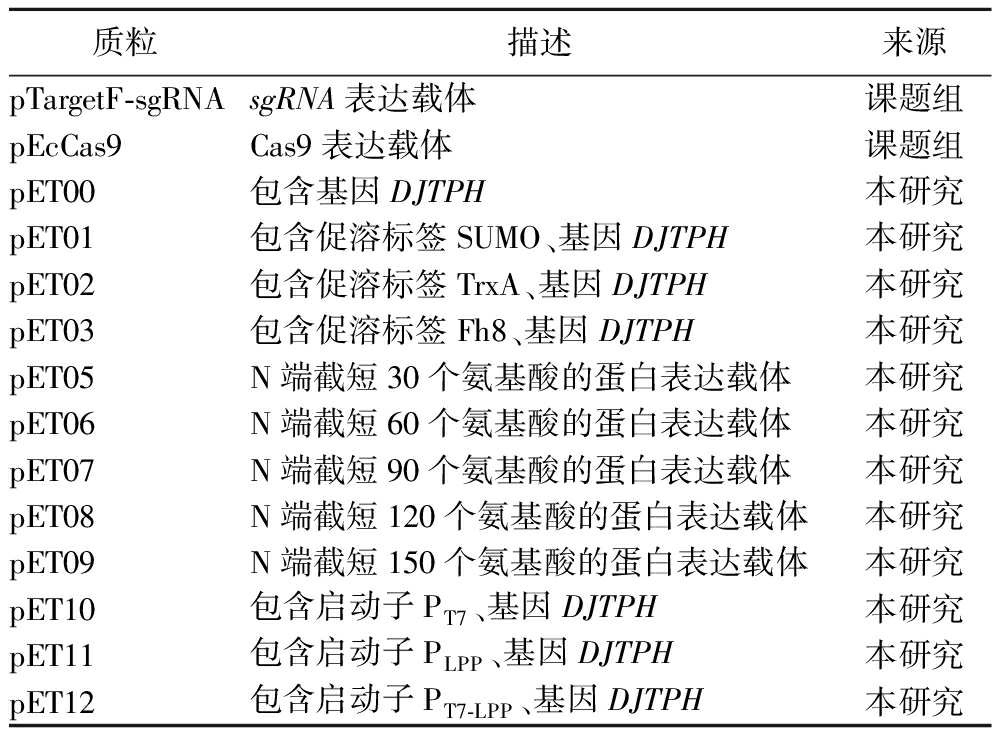
质粒描述来源pTargetF-sgRNAsgRNA表达载体课题组pEcCas9Cas9表达载体课题组pET00包含基因DJTPH本研究pET01包含促溶标签SUMO、基因DJTPH本研究pET02包含促溶标签TrxA、基因DJTPH本研究pET03包含促溶标签Fh8、基因DJTPH本研究pET05N端截短30个氨基酸的蛋白表达载体本研究pET06N端截短60个氨基酸的蛋白表达载体本研究pET07N端截短90个氨基酸的蛋白表达载体本研究pET08N端截短120个氨基酸的蛋白表达载体本研究pET09N端截短150个氨基酸的蛋白表达载体本研究pET10包含启动子PT7、基因DJTPH本研究pET11包含启动子PLPP、基因DJTPH本研究pET12包含启动子PT7-LPP、基因DJTPH本研究
注:小泛素样修饰蛋白(small ubiquitin-like modifier,SUMO); 硫氧还蛋白A(thioredoxin A,TrxA);formin 样蛋白(Fh8 tag,Fh8)。
1.1.2 主要试剂
氯化钠、酵母粉、蛋白胨、磷酸氢二钾、磷酸二氢钾、七水合硫酸亚铁等,国药集团化学试剂有限公司;4-羟乙基哌嗪乙磺酸缓冲液[4-(2-hydroxyethyl)piperazine-1-ethanesulfonic acid buffer,HEPES]、二硫苏糖醇(dithiothreitol,DTT)、卡那霉素、色氨酸,生工生物工程(上海)有限公司;BH4、过氧化氢酶,上海麦克林生化科技股份有限公司。
1.1.3 培养基和缓冲液
卢里亚-伯特尼(Luria-Bertani,LB)培养基(g/L):蛋白胨10,酵母膏5,氯化钠10,于121 ℃灭菌15 min。
缓冲溶液:50 mmol/L HEPES,pH值=7.5。
1.2 主要仪器与设备
培养箱,上海新苗公司;摇床,上海知楚公司;台式高速离心机,德国Eppendorf公司;Agilent 1260高效液相色谱,美国Agilent公司;超声波细胞破碎机,宁波新芝公司;UV-245型紫外-可见分光光度计,日本Shimadzu公司。
1.3 实验方法
1.3.1 质粒与片段构建
编码DJTPH的基因(GenBank No.BAF79887.1)交由苏州安升达生物科技有限公司进行密码子优化与序列合成。
利用美国国家生物技术信息中心National Center for Biotechnology Information (NCBI,https://www.ncbi.nlm.nih.gov)查找基因tnaA上下游300~500 bp核酸序列,设计引物通过一步克隆的方法合成基因同源重组片段。
利用CHOP CHOP网站(https://chopchop.cbu.uib.no/)设计sgRNA序列,选择打分较高的结果作为敲除目标基因的sgRNA序列。
以基因DJTPH和质粒pET28a为模板,DJTPH-F/DJTPH-R和pET28a-F/pET28a-R为引物,扩增模板DNA获得线性片段后,通过同源重组的方法组装成质粒pET00。
设计引物N30-F/N30-R克隆质粒pET28a-DJTPH,利用大肠杆菌自环化系统得到截短突变体质粒pET05。
设计引物T7-F/T7-R构建得到启动子优化质粒pET10,利用大肠杆菌自环化系统构建得到启动子优化质粒pET11-12。设计引物sgtnaA-F/sgtnaA-R扩增质粒pTargetF得到工具质粒pTargetF-sgtnaA。
1.3.2 菌株构建
将质粒pEcCas9导入菌株E.coli BL21 (DE3),获得菌株BpEcCas9;将菌株BpEcCas9制备成电转感受态,通过电转化法将质粒pTargetF-sgtnaA和重组片段导入到大肠杆菌BpEcCas9中,成功敲除色氨酸酶基因后,消除质粒pEcCas9和pTargetF-sgtnaA得到菌株B0。
将pET00-pET12质粒导入菌株B0中,获得表达菌株B00-B12。
1.3.3 蛋白表达
活化保藏的蛋白表达菌株,于37 ℃培养箱中培养12 h得到单菌落,将单菌落接种于3 mL含有卡那霉素的LB培养基中,于37 ℃培养12 h得到种子液。将体积分数为1%的种子液接种至50 ml LB液体培养基中,于37 ℃中培养至OD600值=0.6~0.8,加入IPTG至终浓度为0.5 mmol/L,于15 ℃诱导12 h。
取2 mL诱导后的菌液,8 000 r/min离心2 min后用1 mL Tris-HCl(pH值=7.2)重悬,用超声破碎仪进行破壁处理。取破壁后的粗酶溶液于12 000 r/min离心10 min得到可溶蛋白,变性后通过SDS-PAGE检测蛋白表达量。
1.3.4 酶促反应
1 mL的催化反应体系:50 mmol/L HEPES(pH 7.5)、0.4 g/L L-Trp、0.2 g/L BH4、4 μL 1 000 U过氧化氢酶、100 μmol/L FeSO4·7H2O和2.5 mmol/L DTT,30 ℃ 催化2 h后,于100 ℃处理粗酶反应液10 min,使酶完全变性,终止反应。
1.3.5 检测方法
催化反应溶液12 000 r/min离心5 min去除已变性蛋白后,上清液用甲醇稀释2倍。5-HTP标品用50%(体积分数)甲醇制备成质量浓度为0.1、0.2、0.4、0.8、1 g/L的5-HTP标准溶液。样品经0.22 μm有机系滤膜过滤后,用安捷伦1100系列高效液相色谱检测5-HTP含量。色谱柱:赛默飞反向C18柱,25 ℃;流动相为V(甲醇)∶V[10 mmol/L磷酸钾缓冲液(pH 6.5)]=12∶88;流速0.8 mL/min;检测时长:15 min。上样量10 μL;检测波长276 nm。
1.3.6 酶分子改造
于AlphaFold2(AlphaFold2.ipynb-Colab)预测蛋白质结构后,结合软件Discovery Studio对辅因子、底物和色氨酸羟化酶进行分子对接。通过对辅因子与色氨酸羟化酶结合位点间的作用力分析,对酶分子进行理性改造来增强辅因子与酶分子之间的作用力,从而改善酶的催化活性。
1.3.7 底物通道预测
于Moleonline(https://mole.upol.cz/)进行酶分子底物通道预测,通过分析底物通道的形态和大小,分析不同突变体催化活性变化的原因。
2 结果与分析
2.1 DJTPH的可溶性表达及表达量提升
对色氨酸羟化酶DJTPH进行诱导表达,并没有发现明显的蛋白条带(图2-c)。推测可能由于大肠杆菌无法提供真核来源色氨酸羟化酶折叠和修饰所需要的环境,导致表达的蛋白不具备正确的空间结构。而且,错误的空间结构会导致大肠杆菌内表达的色氨酸羟化酶易聚集形成包涵体,因而无法检测到可溶蛋白的表达[8]。本研究通过引入促溶标签、N端截短、启动子优化与酶表达条件优化,成功提高了蛋白表达量和底物转化率。
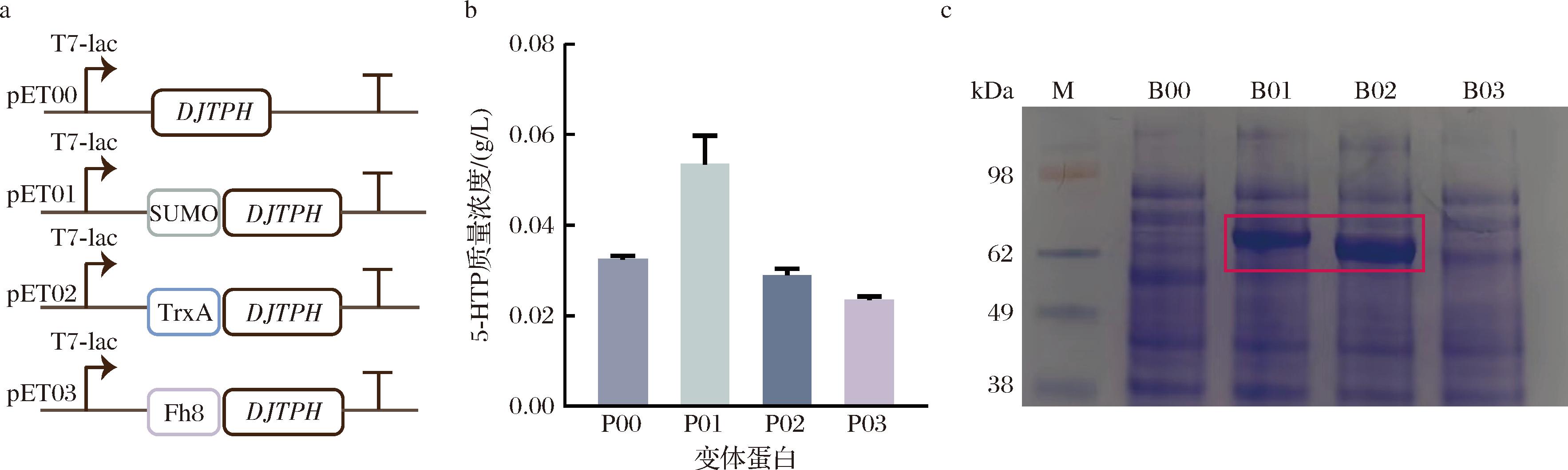
a-质粒构建;b-各菌株催化合成5-HTP产量;c-菌株的蛋白表达SDS-PAGE
图2 B00-B03蛋白表达及产量
Fig.2 B00-B03 protein expression and yield
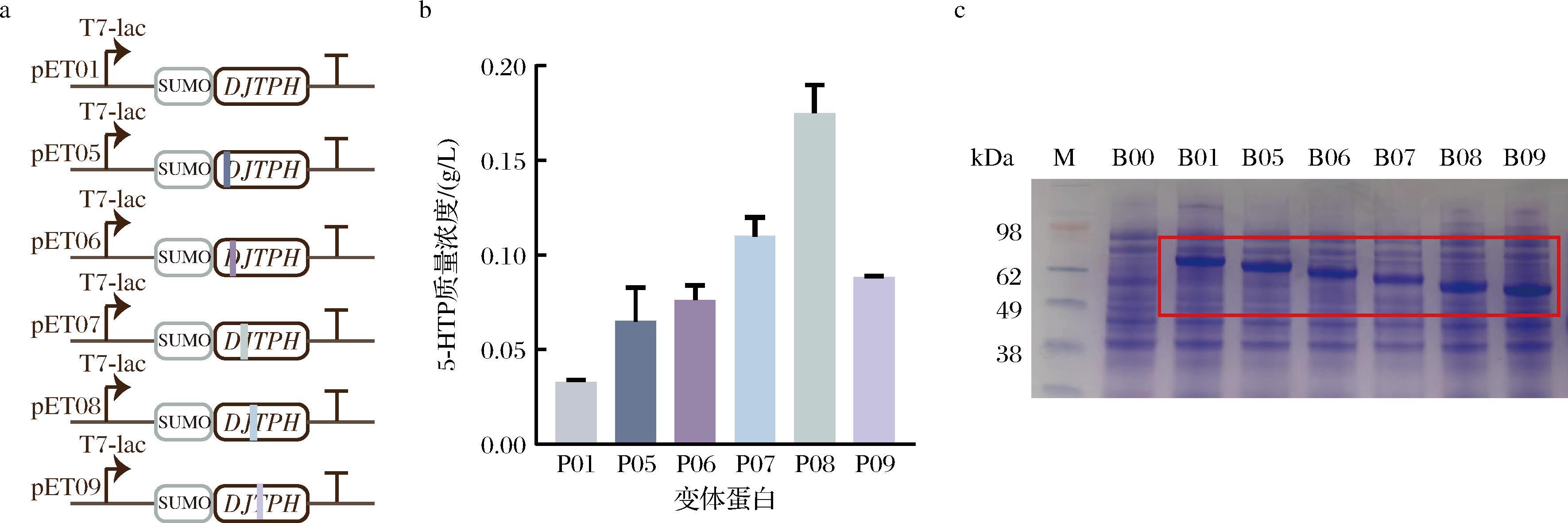
a-质粒构建;b-各菌株催化合成5-HTP产量;c-菌株蛋白表达SDS-PAGE
图3 B01-B09蛋白表达及产量
Fig.3 B01-B09 protein expression and yield
2.1.1 添加促溶标签
GUZZO等[9]通过在天冬氨酰-tRNA合酶N端融合SUMO促溶标签,将酶产量从0.56 mg提升至2.7 mg;CHEN等[10]通过融合麦芽糖结合蛋白(maltose binding protein,MBP),将Ring结构域蛋白产量提升80%。因此,本研究首先通过引入促溶标签来提升色氨酸羟化酶的可溶蛋白表达量。
考虑到较大的促溶标签会对蛋白结构有较大的影响[11],本研究选用分子质量较小的SUMO、TrxA[12]和Fh8[13]作为促溶标签,构建了质粒pET01~pET03和表达菌株B01~B03(图2-a)。
对改造后菌株B01~B03进行诱导(图2-c),与原始菌株B00对照发现:促溶标签SUMO与TrxA均有效的促进了色氨酸羟化酶的表达,且促溶标签SUMO将底物质量转化率提升至13.4%(图2-b)。比较分析认为,由于促溶标签SUMO来源于真核生物,对于一些需要在真核环境中正确折叠和修饰的蛋白促溶效果更好,更利于本研究中线虫来源色氨酸羟化酶的表达,因此选取SUMO作为后续改造的促溶标签[14]。
2.1.2 N端截短
WANG等[5]通过优化TPH2 C、N端截短氨基酸数量,使产量提升约5倍,酶半衰期增长了4.6倍。本研究构建了截短30、60、90、120、150个氨基酸的突变体蛋白质粒pET05~pET09(图3-a)。比较不同截短突变体的蛋白条带(图3-c)发现:N端截短并未明显提升蛋白表达量,且N端截短不同长度肽段对蛋白表达量没有影响。产量检测评估发现不同截短突变体的催化活性不同(图3-b),且N端截短120个氨基酸可将底物质量转化率提升至43.8%,最大程度上提升了酶的催化活性。
为了深入了解N端截短不同长度肽段对酶活性影响的作用机理,本研究预测了N端截短不同长度氨基酸色氨酸羟化酶的结构与底物通道。分析不同截短突变体蛋白的结构(图4)发现:随着N端截短长度的增加,蛋白的催化结构域更加松散,底物结合口袋体积更大,有助于底物与辅因子的碰撞与电荷交换。且截短N端氨基酸使得寡聚结构域空间结构变小,可以防止由于寡聚结构域的位移导致色氨酸较难进入底物结合口袋。
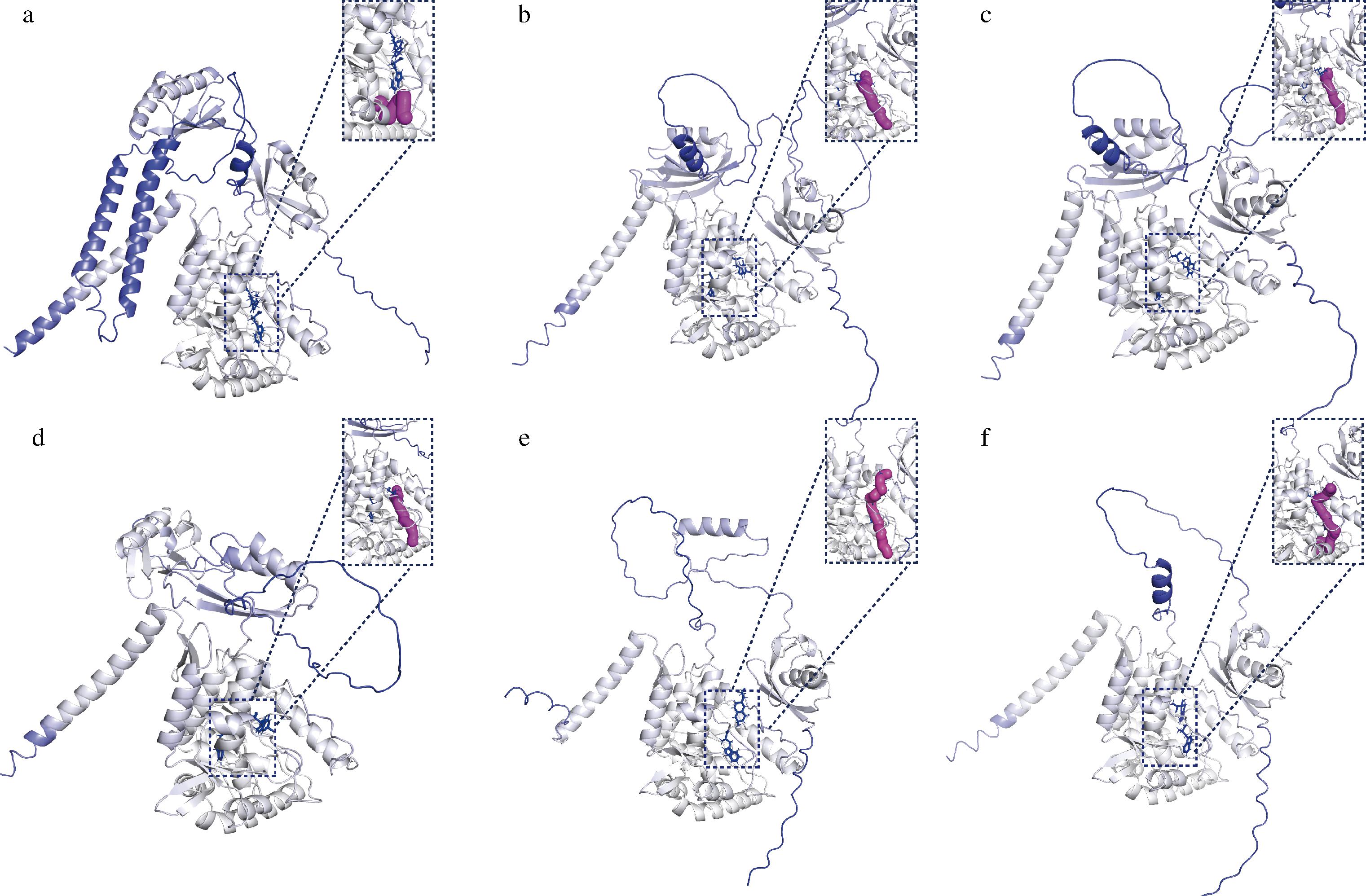
a-N端未截短时的蛋白结构与底物通道;b-N端截短30个氨基酸时的蛋白结构与底物通道;c-N端截短60个氨基酸时的蛋白结构与底物通道;d-N端截短90个氨基酸时的蛋白结构与底物通;e-N端截短120个氨基酸时的蛋白结构与底物通道;f-N端截短150个氨基酸时的蛋白结构与底物通道
图4 不同截短突变体蛋白结构及底物通道
Fig.4 Protein structures and substrate channels of different truncated mutants
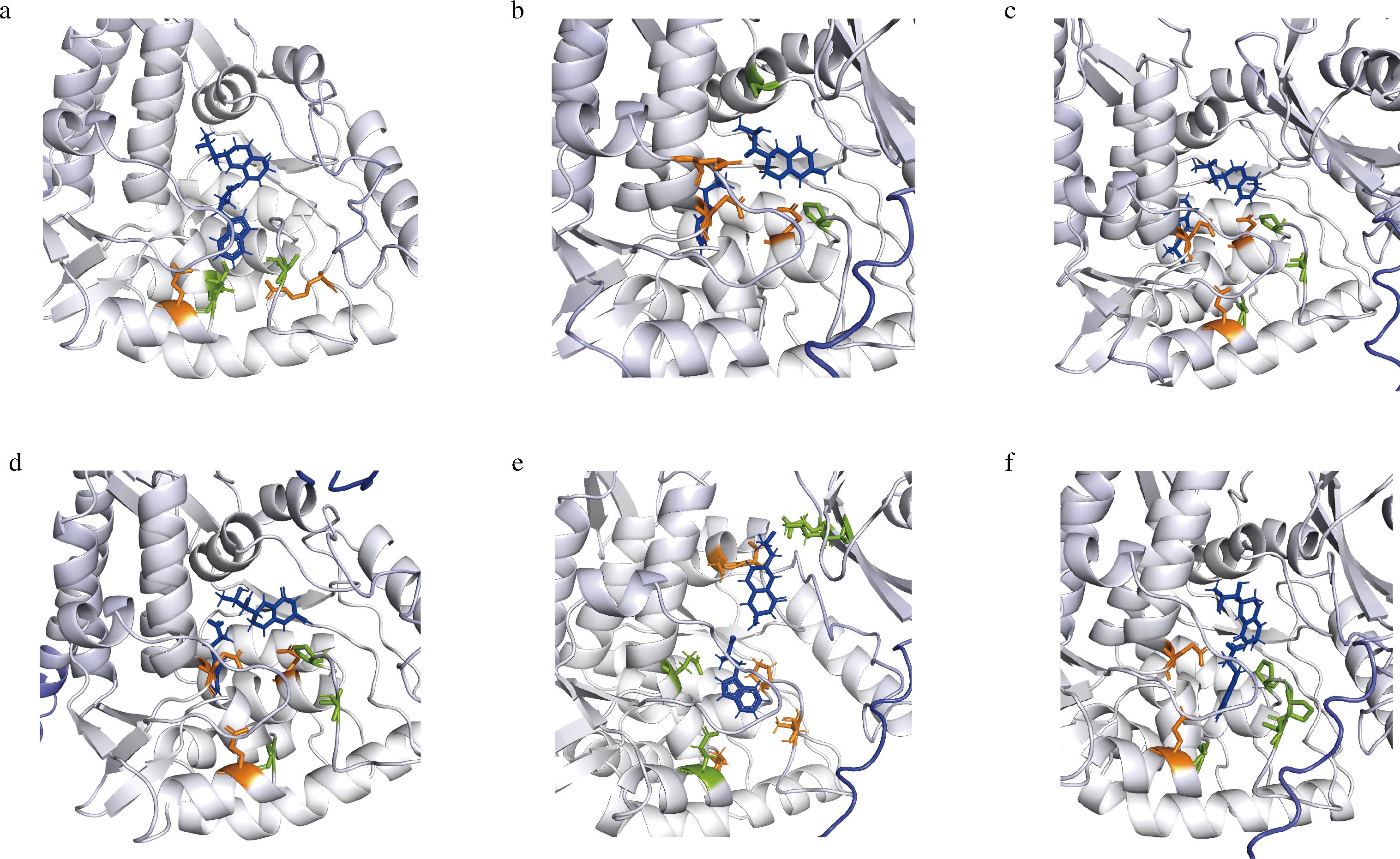
a-N端未截短时底物通道处亲电与亲水氨基酸;b-N端截短30个氨基酸时底物通道处亲电与亲水氨基酸;c-N端截短60个氨基酸时底物通道处亲电与亲水氨基酸;d-N端截短90个氨基酸时底物通道处亲电与亲水氨基酸;e-N端截短120个氨基酸时底物通道处亲电与亲水氨基酸;f-N端截短150个氨基酸时底物通道处亲电与亲水氨基酸
图5 不同截短突变体底物通道处亲电与亲水氨基酸
Fig.5 Electrophilic and hydrophilic amino acids at the substrate channels of different truncated mutants
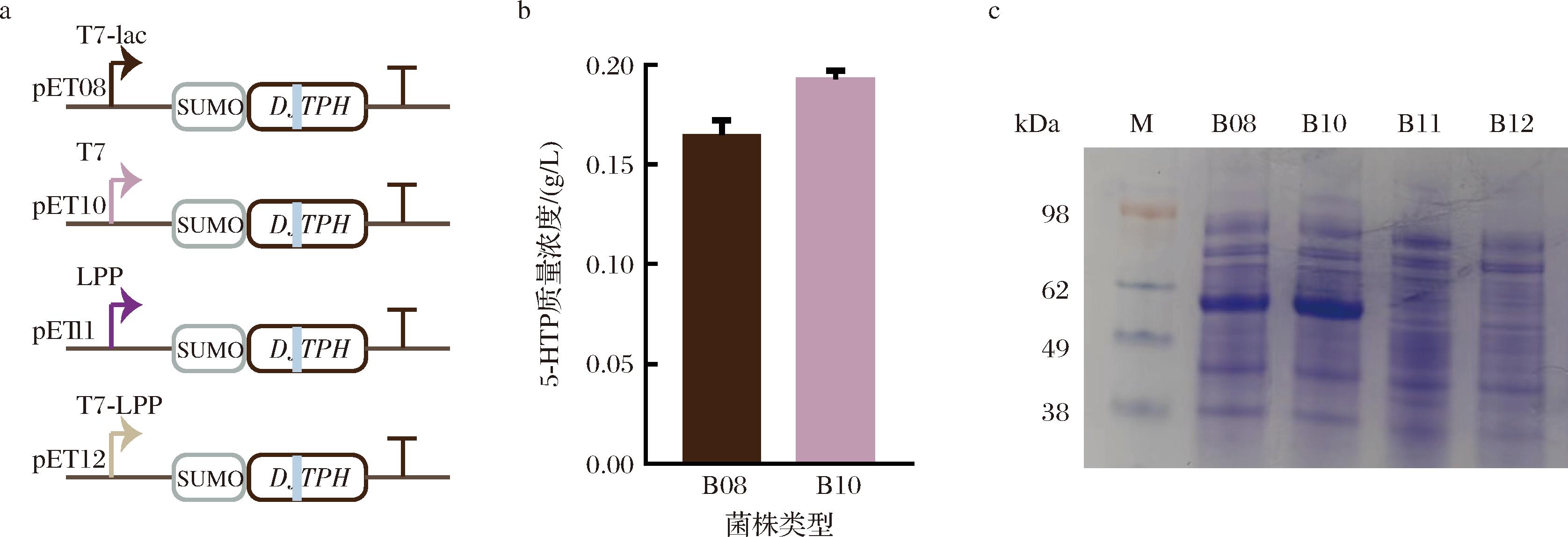
a-质粒构建;b-各菌株催化合成5-HTP产量;c-菌株蛋白表达SDS-PAGE
图6 B08-B12的蛋白表达及产量
Fig.6 B08-B12 protein expression and yield
分析酶分子稳定性(图4)发现(在图中的蛋白结构中,颜色越蓝代表该区域越稳定):随着蛋白截短长度的增加,蛋白质分子的稳定性逐渐降低,分子结构柔性增大。当截短至120个氨基酸时,分子结构稳定性最差,柔性最大,推测:蛋白分子柔性增大,有利于催化底物与辅因子的电子传递。
分析底物通道(图4)发现,随着N端截短氨基酸数量增加,底物通道与底物分子距离变近。且N端截短120、150个氨基酸时,底物通道包含辅因子的结合位点,贯穿色氨酸在酶分子中的催化路线,利于色氨酸与辅因子之间的电荷交换,有助于底物转化率的提升。结合产量检测结果(图3-b)分析,当N端截短120个氨基酸时,底物通道属于最舒展状态,底物分子进入与离开底物结合口袋的阻力最小,酶分子的催化活性有最大的提升。
通过对底物通道的进一步分析(图5)发现(图中橘黄色氨基酸为亲电氨基酸;绿色氨基酸为亲水氨基酸):N端截短120个氨基酸时,底物通道处亲水氨基酸和亲电氨基酸个数最多。且亲电和亲水氨基酸分布较为广泛,由此可以推测,亲电氨基酸有助于反应过程中的电子传递;亲水氨基酸可以使通道处水分子增多,形成更多的氢键,从而稳定底物通道处的电子传递。
2.1.3 启动子替换
基于文献报道,色氨酸羟化酶的表达均使用高强度启动子-T7启动子[15-17]。因此,本研究中通过使用高强度启动子T7、T7-lac、LPP-T7和LPP启动子(图6-a)对DJTPH的蛋白表达量进行优化,以进一步提高色氨酸羟化酶催化效率。比较不同启动子调控下的蛋白表达量(图6-c)可知,在T7与T7-lac启动子调控下,酶分子有较为明显的表达,且T7启动子可以明显提高蛋白表达量。结合产量检测(图6-b),T7启动子可以使酶分子有更高的活性,将底物质量转化率提升至48%。因此,在后续实验中选择T7启动子作为最优启动子。
2.1.4 诱导条件优化
诱导温度和IPTG浓度是调控异源蛋白表达的关键参数。首先探究了不同IPTG诱导浓度对色氨酸羟化酶表达和催化活性的影响。在不同IPTG诱导浓度下,蛋白表达量没有明显差别(图7-c),可能与T7启动子的泄露表达有关[18]。产量测定(图7-a)表明当IPTG诱导浓度为0.4 mmol/L时,色氨酸羟化酶催化活性最高,表明改造后的酶分子在0.4 mmol/L IPTG的诱导条件下可以正确表达其分子结构。
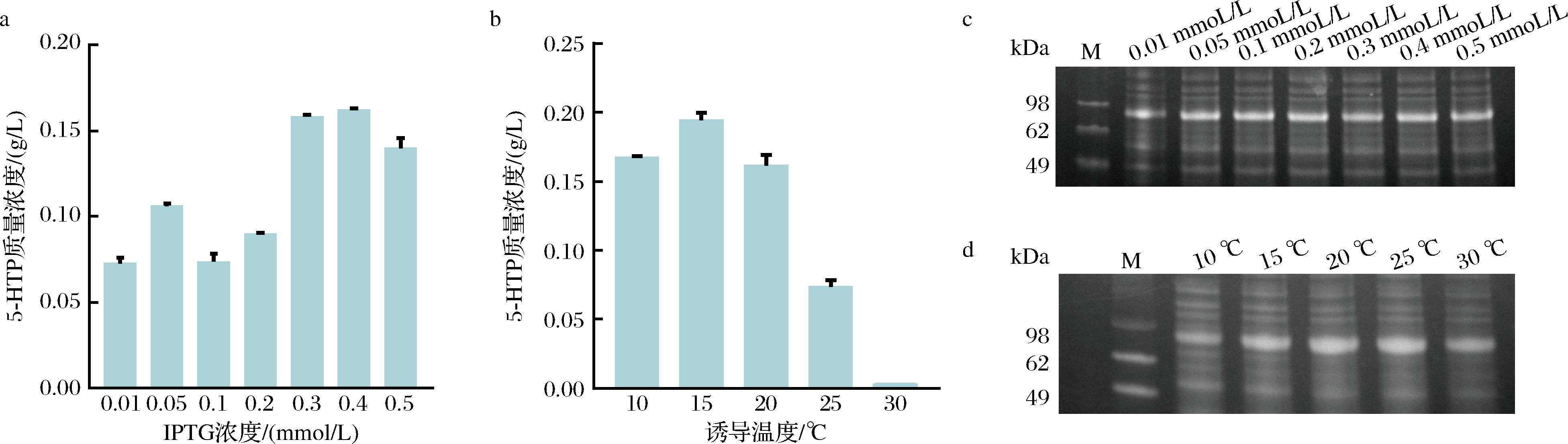
a-IPTG浓度优化产量;b-诱导温度优化产量;c-不同诱导IPTG浓度蛋白表达的SDS-PAGE;d-不同诱导温度蛋白表达的SDS-PAGE
图7 不同诱导条件下蛋白表达及产量
Fig.7 Protein expression and yield with different induction conditions
其次探究了不同诱导温度对色氨酸羟化酶表达及催化活性的影响。发现在不同温度下诱导的蛋白表达量有较大差别(图7-d),在20、25 ℃诱导时,蛋白表达量较高,但5-HTP产量较低(图7-b),表明诱导温度大于20 ℃会增加蛋白错误折叠的几率[19],从而降低酶活性。在10 ℃诱导时,蛋白表达量和5-HTP产量均较低,表明温度过低会影响菌株生长速度进而影响酶分子的表达。因此选择15 ℃作为后续改造的诱导温度。
通过酶表达条件优化,确定诱导条件为:在15 ℃条件下用0.4 mmol/L IPTG诱导酶分子表达,使底物质量转化率提升至48.5%。
2.2 酶分子改造
2.2.1 辅因子与底物结合口袋亲和力改造
基于文献报道,辅因子与酶分子之间的相互作用力大小以及辅因子在酶分子中的位置对酶催化活性有很大的影响[20-22]。分子对接结果发现:辅因子与色氨酸羟化酶的结合位点在底物通道入口处(图8-b),可能会导致辅因子不能与底物充分反应,不利于色氨酸的羟化。为了使辅因子结合位点深入底物结合口袋,本研究对标红位置氨基酸(图8-a、图8-d)进行理性设计,通过将其突变为具有同一性质,但侧链较短的氨基酸来试图减少底物结合口袋对辅因子的排斥力,增加底物结合口袋深部区域与辅因子的相互作用力。本研究根据以上原则,设计了突变体:L306S、Y305Q、E343D。
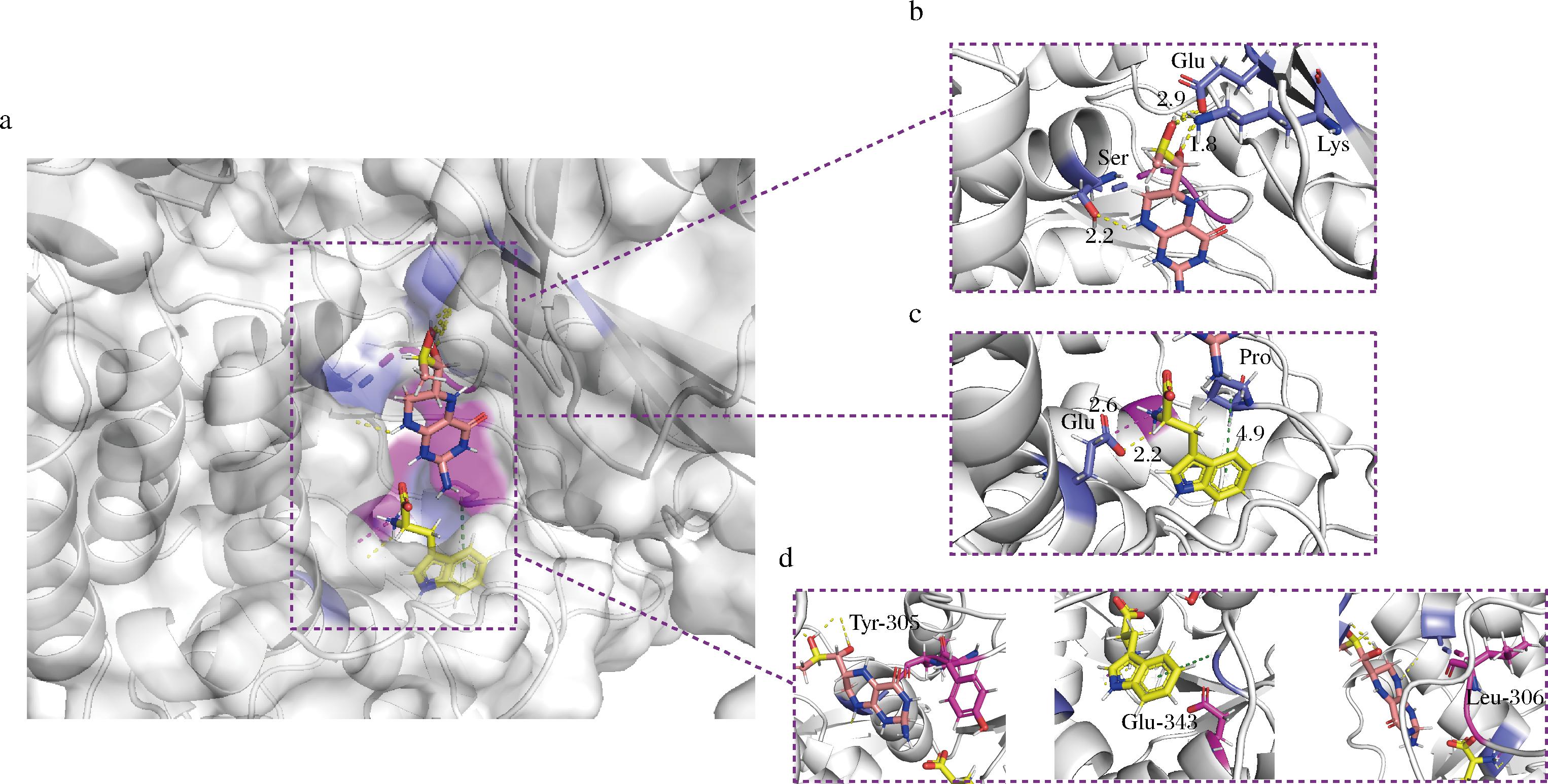
a-分子对接;b-辅因子与酶分子相互作用力分析;c-色氨酸与酶分子相互作用力;d-酶改造位点
图8 分子对接
Fig.8 Molecular docking
通过分子对接发现,突变体E343D可以改变酶分子与辅因子之间的相互作用力。该突变体将原来与辅因子形成氢键的34、27、308位氨基酸改变为321位氨基酸,将原来与辅因子形成范德华力的305、307、193、194位氨基酸改变为306、308、311、320、343、338、382位氨基酸,使辅因子的结合区域更深入底物结合口袋内部(图9-a、图9-b),有助于底物与辅因子之间的相互作用。体外酶催化分析(图9-c)发现,突变体E343D将底物质量转化率提升至98%。
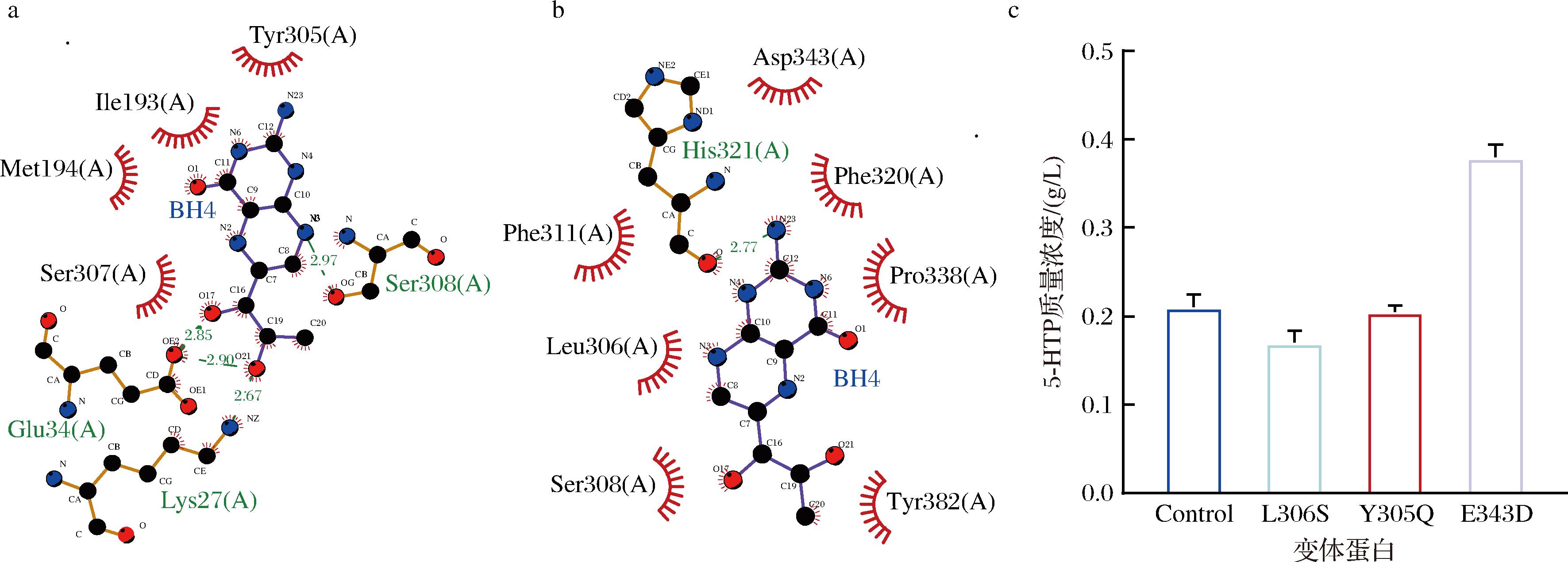
a-辅因子与B10相互作用力分析;b-辅因子与B10 E343D突变体相互作用力分析;c-不同突变体产量
图9 突变体分子对接及产量
Fig.9 Mutant molecule docking and yield
3 结论与讨论
5-HTP作为保健品的重要原料,具有广阔的市场需求。针对目前存在的转化率较低的问题,本研究通过色氨酸羟化酶的表达优化以及酶分子改造,成功提升了5-HTP的转化率。首先,通过编辑宿主细胞的基因组,敲除了色氨酸酶,减少了底物与产物的降解。通过添加促溶标签成功提高了色氨酸羟化酶的表达水平。通过截短酶分子N端120个氨基酸,使底物通道更加舒展,减小了底物分子进出底物结合通道的能量壁垒,并且增强了底物分子与辅因子之间的电子交换。通过启动子优化与酶表达条件优化,成功提升了色氨酸羟化酶的活性。最后,通过酶分子改造,将辅因子与酶分子的作用位点从较前端氨基酸27、34、308位氨基酸改变为较后端氨基酸321位氨基酸,使辅因子处于底物结合口袋中间位置,更利于底物和产物进出酶分子底物结合口袋;减少了辅因子与酶分子之间较强的氢键相互作用力,增加了较弱的范德华作用力,有利于反应后的辅因子及时离开底物结合口袋。在400 mg/L底物质量浓度下,实现了98%的质量转化率。将点突变与N端截短通道分析相结合,底物通道处大多数亲电氨基酸都为谷氨酸,后续可以将其突变为天冬氨酸,实验验证是否会对色氨酸转化率有进一步提升。但目前还存在一些问题,辅因子需要外源添加,价格较昂贵;酶分子的催化活性不够高等。后续可以针对这些问题进行改善:可以将辅因子循环基因整合至宿主细胞基因组中,使宿主细胞具有合成辅因子的能力;可以继续对该酶分子进行改造,进一步提升辅因子与酶分子的相互作用力,以期实现成本效益的平衡。
[1] GENDLE M H,YOUNG E L,ROMANO A C.Effects of oral 5-hydroxytryptophan on a standardized planning task:Insight into possible dopamine/serotonin interactions in the forebrain[J].Human Psychopharmacology,2013,28(3):270-273.
[2] LIU X X,ZHANG B,AI L Z.Advances in the microbial synthesis of 5-hydroxytryptophan[J].Frontiers in Bioengineering and Biotechnology,2021,9:624503.
[3] ZHANG Z,YU Z C,WANG J D,et al.Metabolic engineering of Escherichia coli for efficient production of L-5-hydroxytryptophan from glucose[J].Microbial Cell Factories,2022,21(1):198.
[4] SHEN B W,ZHANG L,ZHOU Y,et al.Efficient synthesis of 5-hydroxytryptophan in Escherichia coli by bifunctional utilization of whey powder as a substrate for cell growth and inducer production[J].Journal of Biotechnology,2024,393:100-108.
[5] WANG B B,XU J Z,LIU S,et al.Engineering of human tryptophan hydroxylase 2 for efficient synthesis of 5-hydroxytryptophan[J].International Journal of Biological Macromolecules,2024,260:129484.
[6] SONG F F,GU T,ZHANG L,et al.Rational design of tryptophan hydroxylation 1 for improving 5-hydroxytryptophan production[J].Enzyme and Microbial Technology,2023,165:110198.
[7] WANG B B,LIU S,WANG H D,et al.Efficient biosynthesis of high-value 5-hydroxytryptophan using a multienzyme cascade[J].Molecular Catalysis,2023,546:113274.
[8] JIANG R Z,YUAN S T,ZHOU Y L,et al.Strategies to overcome the challenges of low or no expression of heterologous proteins in Escherichia coli[J].Biotechnology Advances,2024,75:108417.
[9] GUZZO C M,YANG D C H.Systematic analysis of fusion and affinity tags using human aspartyl-TRNA synthetase expressed in E.coli[J].Protein Expression and Purification,2007,54(1):166-175.
[10] CHEN A Q,ZHANG L,GU S H,et al.Investigation of TtrD,an expressing recombinant fusion tag,in Escherichia coli[J].Protein Expression and Purification,2016,120:65-71.
[11] JO B H.An intrinsically disordered peptide tag that confers an unusual solubility to aggregation-prone proteins[J].Applied and Environmental Microbiology,2022,88(7):e00097-22.
[12] KI M R,PIL P.Fusion tags to enhance heterologous protein expression[J].Applied Microbiology and Biotechnology,2020,104(6):2411-2425.
[13] COSTA S J,COELHO E,FRANCO L,et al.The Fh8 tag:A fusion partner for simple and cost-effective protein purification in Escherichia coli[J].Protein Expression and Purification,2013,92(2):163-170.
[14] PEROUTKA III R J,ORCUTT S J,STRICKLER J E,et al.SUMO fusion technology for enhanced protein expression and purification in prokaryotes and eukaryotes[J].Methods in Molecular Biology,2011,705:15-30.
[15] MORA-VILLALOBOS J A,ZENG A P.Protein and pathway engineering for the biosynthesis of 5-hydroxytryptophan in Escherichia coli[J].Engineering in Life Sciences,2017,17(8):892-899.
[16] TEIGEN K,MCKINNEY J A,HAAVIK J,et al.Selectivity and affinity determinants for ligand binding to the aromatic amino acid hydroxylases[J].Current Medicinal Chemistry,2007,14(4):455-467.
[17] WANG Y Y,LIU W,PENG S G,et al.Enhancing thermostability of tryptophan hydroxylase via protein engineering and its application in 5-hydroxytryptophan production[J].International Journal of Biological Macromolecules,2024,264:130609.
[18] KANG Y,SON M S,HOANG T T.One step engineering of T7-expression strains for protein production:Increasing the host-range of the T7-expression system[J].Protein Expression and Purification,2007,55(2):325-333.
[19] HUYNH N H,DAVEY K,JIN B,et al.A statistical approach to boost soluble expression of E.coli-derived virus-like particles in shake-flask cultivation[J].Journal of Biotechnology,2022,347:56-66.
[20] VILLARINO L,CHORDIA S,ALONSO-COTCHICO L,et al.Cofactor binding dynamics influence the catalytic activity and selectivity of an artificial metalloenzyme[J].ACS Catalysis,2020,10(20):11783-11790.
[21] DOS SANTOS A M,DA COSTA C H S,MARTINS M,et al.Exploring the structural and dynamic properties of a chimeric glycoside hydrolase protein in the presence of calcium ions[J].International Journal of Molecular Sciences,2024,25(22):11961.
[22] MILLER A H,BLAGOVA E V,LARGE B,et al.Catch-and-release:The assembly,immobilization,and recycling of redox-reversible artificial metalloenzymes[J].ACS Catalysis,2024,14(5):3218-3227.