羽扇豆醇[lupeol,lup-20(29)-ene-3β-ol]是一种萜类化合物,广泛存在于多种药用植物和蔬果中[1],是羽扇豆烷型三萜的必需前体,经过C28氧化,最终转化为白桦脂醇和白桦脂酸,两者都是有价值的三萜化合物[2]。已有研究证实了羽扇豆醇及其衍生物如白桦脂酸等具有大量的生理活性,包括抗炎、抗氧化、降血糖、降血脂、抗癌、杀螨作用,在食品防腐、优化食品加工稳定性、功能性食品的开发以及医药等领域都有广泛的应用前景[1-3]。然而较低的天然含量和复杂的萃取条件使得植物萃取法得到的羽扇豆醇产量较低[4-5],无法满足羽扇豆醇工业应用的需求。近年来,合成生物学以其高效、经济、无污染地合成单一产物的特点而受到越来越多的关注,成为最适合于萜类化合物高产的技术,如在酵母中合成青蒿酸,产量为25 g/L,酵母中青蒿素的前体紫穗槐二烯的产量可达40 g/L以上[6-7]。酿酒酵母(Saccharomyces cerevisiae)和解脂耶氏酵母(Yarrowia lipolytica)等已被作为底盘细胞用于生物合成羽扇豆醇,其中Y.lipolytica的产量最高[8-10],达到411.72 mg/L。酵母作为真核生物,天然具备完整的甲羟戊酸(mevalonate pathway,MVA)途径,可直接生成三萜类化合物(如羽扇豆醇)的前体——角鲨烯。但其生长速度较慢,且真核细胞的复杂调控网络可能增加代谢工程难度。同时酵母的发酵成本较高,且羽扇豆醇的天然提取受限于植物资源。相比之下,大肠杆菌的培养成本低、发酵周期短,适合快速优化代谢途径和大规模生产。大肠杆菌中没有内源的三萜合成途径,因此异源合成的2,3-环氧化角鲨烯以合成羽扇豆醇为唯一方向,不会有通量流失的问题,因此大肠杆菌有希望成为羽扇豆醇高效合成的微生物底盘。大肠杆菌中羽扇豆醇的生物合成途径起始于丙酮酸与甘油醛-3-磷酸(glyceraldehyde-3-phosphate,G3P)在1-脱氧-D-木酮糖-5-磷酸合酶(1-deoxyxylulose-5-phosphate synthase,DXS)催化下的缩合反应。生成的2C-甲基-D-赤藓醇-4-磷酸(2-C-methyl-D-erythritol-4-phosphate,MEP)作为甲基赤藓糖醇磷酸(MEP)途径的核心中间体,参与异戊烯基焦磷酸(isopentenyl pyrophosphate,IPP)及其异构体二甲基烯丙基焦磷酸(dimethylallyl pyrophosphate,DMAPP)的合成。在法尼基焦磷酸合酶(farnesyl pyrophosphate synthase,FPS)作用下,IPP与DMAPP经逐步缩合生成法尼酰基焦磷酸(farnesyl pyrophosphate,FPP)。随后,角鲨烯合酶(squalene synthase,SQS)催化2分子FPP转化为角鲨烯,后者通过角鲨烯环氧酶(squalene epoxidase,SQE)的氧化作用生成2,3-环氧化角鲨烯。最终,该环氧化物在羽扇豆醇合酶(lupeol synthase,LUS)的立体专一性环化作用下形成羽扇豆醇(图1)。值得关注的是,在该合成途径中,DXS与异戊烯基焦磷酸异构酶(isopentenyl pyrophosphate isomerase,IDI)分别通过调控MEP合成起始步骤及IPP/DMAPP异构化平衡,共同构成代谢通路的关键限速节点。

图1 在大肠杆菌中构建的羽扇豆醇合成途径
Fig.1 The constructed synthesis pathway of lupeol in E.coli
注:1-脱氧木酮糖-5-磷酸(1-deoxyxylulose-5-phosphate,DXP);1-脱氧木酮糖-5-磷酸还原异构酶(1-deoxyxylulose-5-phosphate reductoisomerase,DXR);4-二磷酸胞苷-2-C-甲基-D-赤藓糖醇合酶(4-diphosphocytidyl-2-C-methyl-D-erythritol synthase,IspD);4-二磷酸胞苷-2-C-甲基-D-赤藓糖醇激酶(4-diphosphocytidyl-2-C-methyl-D-erythritol kinase,IspE);2-C-甲基-D-赤藓糖醇-2,4-环二磷酸合酶(2-C-methyl-D-erythritol 2,4-cyclodiphosphate synthase,IspF);1-羟基-2-甲基-2-(E)-丁烯基-4-二磷酸合酶[1-hydroxy-2-methyl-2-(E)-butenyl 4-diphosphate synthase,IspG];1-羟基-2-甲基丁烯基-4-二磷酸还原酶(1-hydroxy-2-methyl-butenyl 4-diphosphate reductase,IspH)。
然而,在大肠杆菌中异源合成羽扇豆醇的研究较少,这主要是由于缺乏羽扇豆醇的直接前体2,3-环氧化角鲨烯的内源合成途径[11]。在大肠杆菌中合成2,3-环氧化角鲨烯需要解决的关键问题在于其缺乏由LUS和SQE构成的氧化系统。该氧化系统的正常运行依赖于NADPH-细胞色素P450还原酶(NADPH-cytochrome P450 reductase,CPR)介导的电子传递过程,CPR通过向SQE和LUS传递电子维持其催化活性[12]。目前仅有一篇关于大肠杆菌合成羽扇豆醇的报道[13],该研究通过HPLC检测到目标产物,但未公开具体浓度数据,究其原因在于羽扇豆醇积累水平较低。因此该研究认为大肠杆菌作为底盘细胞在羽扇豆醇合成效率上不及酵母。
尽管大肠杆菌作为底盘微生物合成羽扇豆醇存在诸多限制因素,例如缺乏2,3-环氧化角鲨烯合成途径、依赖CPR的氧化系统(涉及LUS和SQE)效率不足,以及MEP途径中DXS和IDI等限速步骤,但本研究通过系统代谢工程策略尝试构建大肠杆菌羽扇豆醇合成体系:首先,选择与其他来源的SQS相比,具有更高的角鲨烯合成活性的人源(Homo sapiens)的SQS[13],而Y.lipolytica来源的SQE具有优异的异源表达特性,增强了氧化鲨烯的供应,并结合木榄(Bruguiera gymnorrhiza)源LUS的羽扇豆醇合成功能,协同表达以解决底物供给与催化效率的瓶颈[14],异源整合成功构建羽扇豆醇合成途径;其次,系统性评估3种CPR与SQE的氧化系统组合,通过发酵和产物检测对比3种菌株对羽扇豆醇和角鲨烯合成的影响,筛选获得最有利于羽扇豆醇的合成体系。为进一步提升产量,通过共过表达DXS与IDI强化MEP途径代谢通量,获得高产工程菌株LUEAMU。最终,采用摇瓶补料分批发酵工艺进一步提升羽扇豆醇的产量。
1 材料与方法
1.1 材料与试剂
2×Phanta Max Master Mix(Dye Plus)DNA聚合酶,Cycle Pure纯化试剂盒,Omega生物技术有限公司;ClonExpress Ultra一步克隆试剂盒,南京诺唯赞生物科技有限公司;快速质粒小提试剂盒,天根生化科技(北京)有限公司;PCR所用引物合成及测序由青岛生工生物科技有限公司提供;其他试剂及药品未作特殊说明均为国产分析纯。
LB培养基(g/L):蛋白胨10,酵母提取物5,NaCl 10。TB培养基(g/L):蛋白胨12,酵母提取物24,17 mmol/L KH2PO4,72 mmol/L K2HPO4,甘油4。大豆酪蛋白消化物培养基-改性(含甘露醇和硝酸盐)[soybean-casein digest medium modified (with mannitol and nitrate),SBMSN]培养基(g/L):蛋白胨12,酵母提取物24,KH2PO4 1.7,K2HPO4 11.42,MgCl2·6H2O 1,草酸铵1.42,吐温80 2。ZYP-5052培养基(g/L):蛋白胨10,酵母提取物5,1 mol/L的MgSO4 2,5052母液7.5。上述液体培养基加15~20 g/L的琼脂可配成相应的固体培养基,115 ℃灭菌30 min后备用。无菌的375 g/L 5052母液和200 g/L葡萄糖溶液使用时在超净台内加入(115 ℃灭菌30 min)。
1.2 仪器与设备
ZQZY-88BE全温振荡培养箱,上海知楚仪器有限公司;DHP-9051微生物培养箱,上海一恒科学仪器有限公司;HH-4A数显恒温水浴锅,国华(常州)仪器制造有限公司;GI80TW立式自动压力蒸汽灭菌器,致微(厦门)仪器有限公司;DK-8D数显恒温水浴锅,武汉瑞华仪器设备有限责任公司;Nano-200超微量核酸分析仪,杭州奥盛仪器有限公司。
1.3 实验方法
1.3.1 质粒构建
本研究涉及的所有质粒信息详见表1。其中,木榄(B.gymnorrhiza)来源的羽扇豆醇合酶BgLUS编码基因(GenBank ID:AB289586.1)序列从NCBI数据库获取,经大肠杆菌BL21(DE3)密码子偏好性优化后,由生工生物工程(上海)股份有限公司全基因合成。ScCPR的编码基因通过PCR从S.cerevisiae BY4741菌株基因组中扩增获得,YlSQE与YlCPR的编码基因则来源于Y.lipolytica PO1g基因组。异戊烯基焦磷酸异构酶基因(idi)及1-脱氧-D-木酮糖-5-磷酸合酶基因(dxs)通过PCR从大肠杆菌基因组中克隆。目标基因及质粒骨架等线性片段的扩增均采用2×Phanta Max Master Mix(Dye Plus)DNA聚合酶,所用特异性引物如表2所示。扩增产物经琼脂糖凝胶电泳验证后,使用Cycle Pure纯化试剂盒进行纯化。质粒构建采用ClonExpress Ultra一步克隆试剂盒完成无缝克隆,并通过质粒提取试剂盒按说明书进行质粒提取(图2)。
表1 本研究使用的质粒和菌株
Table 1 Plasmids and strains used in this research

名称相关信息来源质粒pTac15k-idi-dxsidi-dxs cassette in pTac15k本实验室保藏99a-hsqshsqs cassette in pTrc99a[15]99a-hsqs-ylsqe-bglusylsqe-bglus cassette in 99a-hsqs本实验构建99a-hsqs-sccpr-ylsqe-bglussccpr cassette in 99a-hsqs-ylsqe-bglus本实验构建99a-hsqs-ylcpr-ylsqe-bglusylcpr cassette in 99a-hsqs-ylsqe-bglus本实验构建99a-hsqs-atcpr-mcsqe-bglusatcpr-mcsqe cassette in 99a-hsqs-bglus本实验构建菌株UMEPpTac15k-idi-dxs cassette in E.coli BL21(DE3)本实验构建LUE99a-hsqs-ylsqe-bglus cassette in E.coli BL21(DE3)本实验构建LUEYC99a-hsqs-ylcpr-ylsqe-bglus cassette in E.coli BL21(DE3)本实验构建LUESC99a-hsqs-sccpr-ylsqe-bglus cassette in E.coli BL21(DE3)本实验构建LUEAM99a-hsqs-atcpr-mcsqe-bglus cassette in E.coli BL21(DE3)本实验构建LUESCU99a-hsqs-sccpr-ylsqe-bglus cassette in UMEP本实验构建LUEYCU99a-hsqs-ylcpr-ylsqe-bglus cassette in UMEP本实验构建LUEAMU99a-hsqs-atcpr-mcsqe-bglus cassette in UMEP本实验构建LUEU99a-hsqs-ylsqe-bglus cassette in UMEP本实验构建
表2 本研究使用的引物
Table 2 Primers used in this study

引物序列(5′-3′)ylsqe-FAATTAACAGGAACAGATGGTCACCCAACAGTCTylsqe-RTTCCTGTTCCTGCTAAGTCAGCTCGCTCCAAATsccpr-FAATTAACAGGAACAGATGTCCGATGACGGAGATsccpr-RGACCATCTGTTCCTGTTACCAGACATCTTCTTGylcpr-FAATTAACAGGAACAGATGGAGACGGACCCCTATGAC ylcpr-RCATCTGTTCCTGCTACCACACATCTTCCTGatcpr-FGCACCCAGAATTAACAGGAACAGATGCTGTGGmcsqe-RGAATTCCTGTTCCTGTTATTTCGCGCGCAGCGCCTGAbglus-FCAGGAACAGGAATTCATGTGGCGCCTGAAAATTGCbglus-RCCAAAACAGCCAAGCTTTTATCTAGATTAATCATTT99a-hsqs-FTAAAAGCTTGGCTGTTTTGG99a-hsqs-RTGCGAATGGTGCTAATAATC99a-hsqs-ylsqe-bglus-FACAGATGGTCACCCAACAGTCTGCA99a-hsqs-bglus-FCAGGAACAGGAATTCATGTGGCGCCTGAAAATTG99A-FCAGCAGGTGTTTAAAGGTGC99A-RCCTACTCTCGCATGGGGAGA99A-BgLUS-RAAACGCCACAGCAGATCGCT
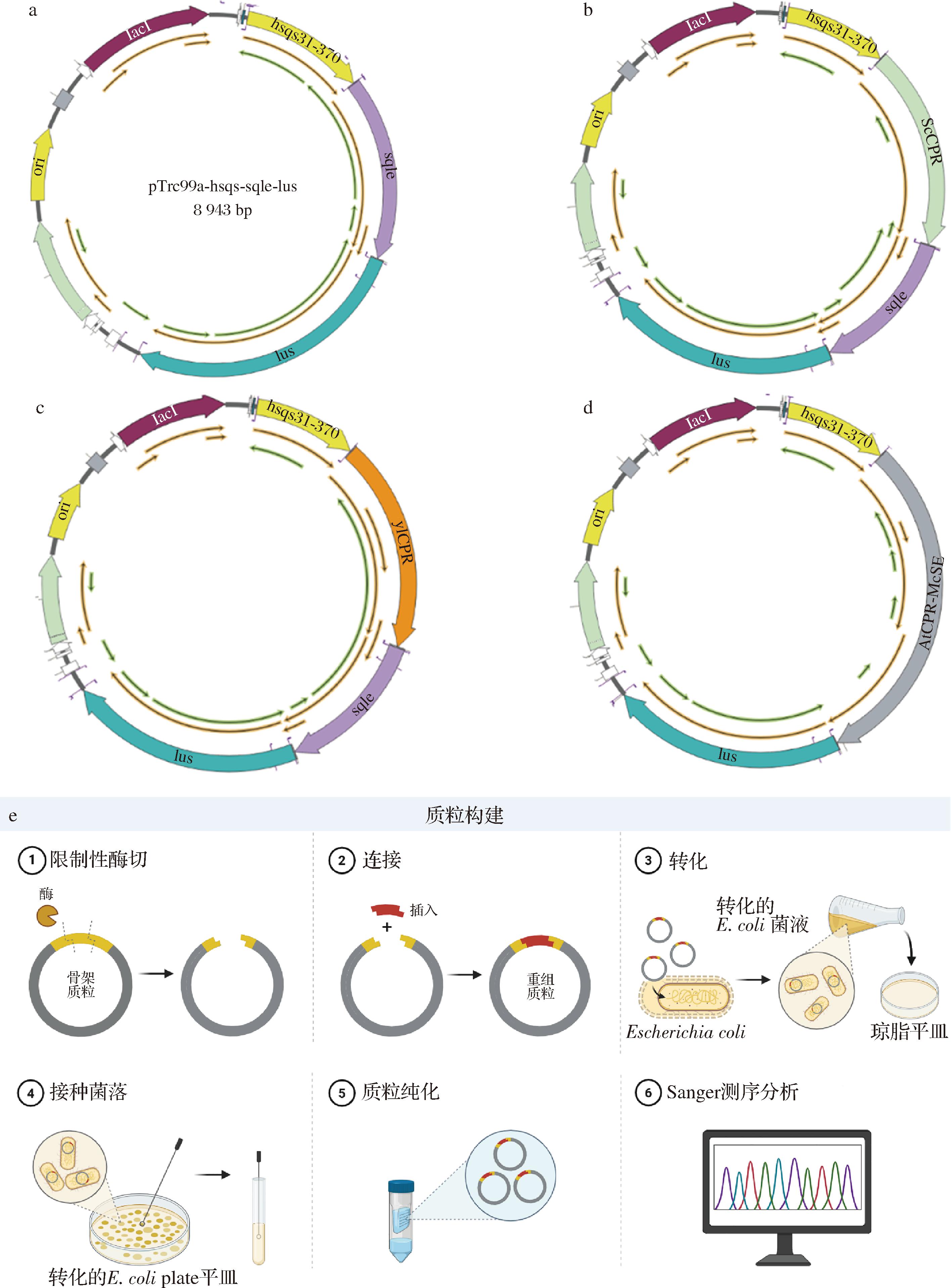
a-pTrc99a-hsqs-ylsqe-bglus;b-pTrc99a-hsqs-sccpr-ylsqe-bglus;c-pTrc99a-hsqs-ylcpr-ylsqe-bglus;d-pTrc99a-hsqs-atcpr-mcsqe-bglus;e-质粒构建流程
图2 本文构建的质粒图谱及质粒构建流程
Fig.2 Diagram of plasimds constructed in this paper and plasmid construction procedure
1.3.2 菌株构建
将成功构建的质粒分别转入大肠杆菌BL21(DE3),涂布于LB固体平板(含100 μg/mL氨苄青霉素和50 μg/mL卡那霉素)在37 ℃培养箱中培养12 h,构建LUE、LUEYC、LUESC及LUEAM 4种工程菌。过表达IDI和DXS,构建了MEP途径强化菌株UMEP。将各表达载体分别转化至大肠杆菌BL21(DE3)和UMEP宿主,涂布于LB固体平板(含100 μg/mL氨苄青霉素和50 μg/mL卡那霉素)在37 ℃培养箱中培养12 h,获得LUEU、LUEYCU、LUESCU及LUEAMU系列菌株。菌体培养采用LB培养基(含100 μg/mL氨苄青霉素和50 μg/mL卡那霉素),于37 ℃振荡培养8~10 h。所用到的各工程菌株详见表1。
1.3.3 摇瓶培养
首先将工程菌株接种于含相应抗生素的LB培养基(5 mL),37 ℃过夜培养。随后取培养液以2%接种量转接至含100 mL TB培养基的锥形瓶中,当OD600达到0.6~0.8时,添加终浓度0.1 mmol/L的异丙基硫代-β-D-半乳糖苷(isopropyl thio-β-D-galactoside,IPTG)诱导表达,并调整培养温度至25 ℃继续发酵48 h。为筛选最优培养基,分别采用LB、SBMSN、ZYP5052及添加不同浓度葡萄糖的TB培养基进行对比实验。其中,葡萄糖添加量依次为4、8、16、32、64 g/L,对应培养基命名为TBG4、TBG8、TBG16、TBG32、TBG64,培养条件与基础TB培养基一致。需特别说明的是,ZYP5052培养基采用2 g/L乳糖替代IPTG作为诱导剂,并于培养初始阶段添加。进一步在TB培养基中优化碳源配比,分别添加4、8、16、32、64、128 g/L的甘油,其余培养参数与上述条件保持一致。
1.3.4 摇瓶补料分批发酵
采用含64 g/L甘油的TB培养基作为基础,在500 mL摇瓶体系中进行补料分批发酵。具体操作流程如下:首先将种子液以2%接种量接入培养基,并在无菌条件下补充适量氨苄青霉素(100 μg/mL)与卡那霉素(50 μg/mL)。当菌体OD600达到0.6~0.8时,添加终浓度0.1 mmol/L的IPTG诱导蛋白表达。发酵参数设定为通气量1 vvm(体积比体积/分钟)、搅拌速率220 r/min、温度25 ℃,持续培养96 h。在发酵过程中,每24 h补充4 g/L甘油作为碳源,同时每36 h补加20%(体积分数)新鲜TB培养基以维持营养供给。
1.3.5 角鲨烯和羽扇豆醇的提取和定量方法
首先取1 mL发酵液于4 722×g离心5 min收集菌体,采用超纯水洗涤2次。随后将菌体重悬于400 μL丙酮中,分别通过25 min涡旋振荡或4 ℃静置过夜2种方式完成细胞裂解。裂解液经10 000×g离心10 min 后,收集上清液于-20 ℃保存待测。羽扇豆醇检测采用岛津LC-20AT型高效液相色谱系统,配备YMC-Pack Pro-C18反相色谱柱(4.6 mm×250 mm,5 μm)及二极管阵列检测器SPD-M40。色谱条件设定为:柱温35 ℃,流动相为甲醇(色谱纯),流速1.0 mL/min,检测波长201 nm。定量分析以Sigma-Aldrich公司提供的羽扇豆醇与角鲨烯标准品为参照。
2 结果与分析
2.1 大肠杆菌中羽扇豆醇合成途径的构建
由于大肠杆菌天然缺乏SQS、SQE及LUS,其自身无法合成羽扇豆醇。区别于已有微生物合成羽扇豆醇研究,本研究选取人(H.sapiens)源SQS(hSQS)、Y.lipolytica源SQE(YlSQE)及B.gymnorrhiza源LUS(BgLUS)构建内源合成途径。基于本课题组前期构建的99a-hsqs质粒骨架,通过共表达YlSQE与BgLUS,成功获得工程菌株LUE(图3-a)。然而,LUE菌株发酵产物中仅检测到少量羽扇豆醇(0.89 mg/L)。值得注意的是,SQE作为黄素依赖型氧化酶,其催化角鲨烯环氧化过程需依赖CPR介导的电子传递[16]。大肠杆菌因进化路径与原核代谢特性,天然缺乏真核型CPR系统[17],而是采用铁氧还蛋白(Fdx)/铁氧还蛋白还原酶(Fdr)系统传递电子,缺乏对真核P450的适配性,亟需异源CPR以重构高效电子传递路径,从而支持复杂天然产物的生物合成。因此,可以选择异源表达CPR以提升羽扇豆醇产量。
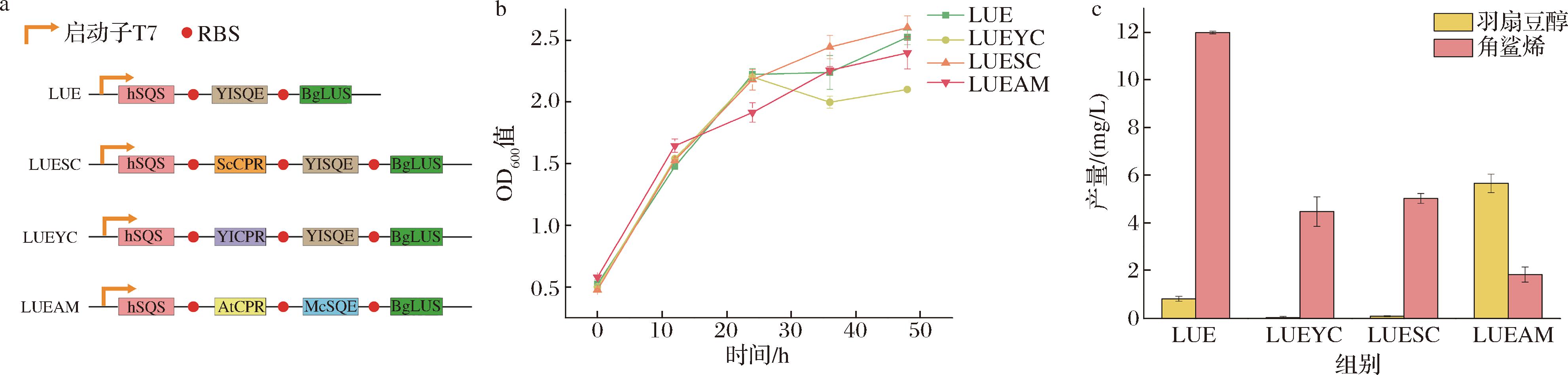
a-4个工程菌株的描述;b-每12 h检测4株菌的OD600值;c-通过HPLC检测和定量分析羽扇豆醇和角鲨烯的产量
图3 不同CPR/SQE体系对羽扇豆醇产量的影响
Fig.3 Effect of different CPR/SQE systems on lupeol production
2.2 不同CPR/SQE氧化体系对羽扇豆醇产量的影响
本研究为探究CPR对羽扇豆醇合成的影响,在工程菌株中分别表达ScCPR/YlSQE、YlCPR/YlSQE及AtCPR/McSQE 3种氧化系统,成功构建LUESC、LUEYC与LUEAM 3种工程菌(图3-a),菌株培养过程中的OD600如图3-b所示。如图3-c所示,LUEAM菌株的羽扇豆醇产量最高(5.37 mg/L),同时角鲨烯积累量最低(1.61 mg/L);而LUE菌株则呈现相反的代谢特征,其角鲨烯产量高达12.02 mg/L,但羽扇豆醇产量显著低于LUEAM。此外,LUEYC与LUESC菌株的角鲨烯产量均低于5 mg/L,且羽扇豆醇合成能力较弱。
尽管LUEAM菌株的羽扇豆醇产量达到5.37 mg/L,但仍远低于大肠杆菌萜类化合物的常规生产水平。由于4株工程菌的产物积累量均处于低水平,难以通过现有数据准确判定优势菌株。因此,如何通过代谢途径强化提升羽扇豆醇合成效率成为亟待解决的关键问题。
2.3 过表达DXS和IDI上调MEP途径提高羽扇豆醇产量
前期研究表明,MEP途径生成的IPP和DMAPP等前体供应不足,严重限制了大肠杆菌萜类化合物的合成效率[18-19]。为此,本研究将MEP途径DXS与IDI整合至表达载体,成功构建LUEU、LUESCU、LUEYLU及LUEAMU 4株MEP途径强化菌株(图4-a)。
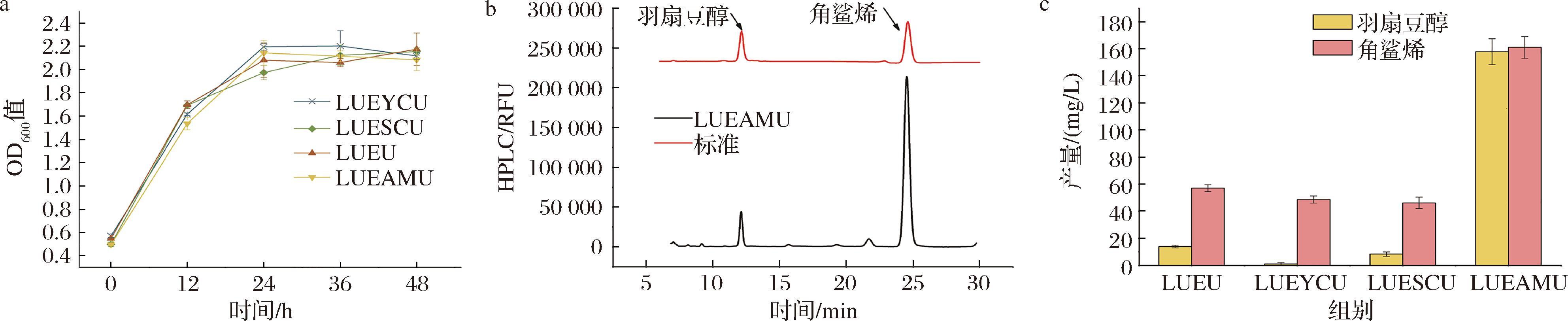
a-每12 h检测4株菌的OD600;b-E.coli LUEAMU产角鲨烯(24.53 min)和羽扇豆醇(12.118 min)的HPLC结果;c-不同菌株羽扇豆醇和角鲨烯的产量
图4 上调MEP途径提高羽扇豆醇的产量
Fig.4 Upregulation of MEP pathway for high production of lupeol
发酵产物的HPLC检测结果如图4-b所示,4株工程菌的羽扇豆醇与角鲨烯产量均呈现显著提升(图4-c)。其中,基于LUEAM菌株改造的LUEAMU表现尤为突出,其羽扇豆醇产量达155.25 mg/L,角鲨烯产量为164.25 mg/L,分别达到原始菌株LUEAM的28.91倍与88.78倍。值得注意的是,该产量较基础菌株LUE提升174.44倍,达到了大肠杆菌羽扇豆醇生物合成的最高产量。相较而言,其他3株工程菌的合成能力显著受限:LUEU、LUESCU、LUEYLU的角鲨烯与羽扇豆醇产量分别低于60、20 mg/L,其中LUEYLU菌株的羽扇豆醇合成量几近检测限。上述结果表明,LUEAMU菌株通过协同强化前体供应与氧化系统,成功突破代谢瓶颈,成为本研究筛选获得的高效合成菌株。
2.4 培养基组成对细胞生长和羽扇豆醇产量的影响
培养基通过为微生物生长和蛋白质表达提供营养和能量,在细胞培养和生物合成过程中发挥着至关重要的作用。就LUEAMU而言,不同培养基对羽扇豆醇的产量也有影响。LB培养基是大肠杆菌培养中最常用的培养基之一,其有机物含量占比为1.5%,但是其羽扇豆醇和角鲨烯的产量均低于20 mg/L。而调整碳源的比例可以对大肠杆菌培养过程中汲取能量的优化起到显著作用,葡萄糖是最常见的碳源物质之一,含2.5%(质量分数)葡萄糖的ZYP-5052培养基被广泛地应用于大肠杆菌的培养中。然而,这种培养基对羽扇豆醇的合成影响不大,角鲨烯和羽扇豆醇的产量均低于50 mg/L(图5-a)。葡萄糖含量较少时,因碳源不足导致产物合成量低,而超过一定含量的葡萄糖会导致乙酸在大肠杆菌中的过量合成,该化合物的存在会阻碍菌体继续生长,抑制蛋白的顺利表达。TB培养基是以甘油为碳源的培养基,由于甘油做碳源不易积累乙酸,是更优的碳源选择。此外,该培养基通过提高酵母提取物含量,提供了丰富的菌体生长所需营养物质。根据上一节的结果也验证了其具有高产羽扇豆醇的能力。因此,为了进一步提升羽扇豆醇的产量,在TB培养基中分别加入不同浓度的葡萄糖,以探讨2种碳源对大肠杆菌生长和羽扇豆醇合成的影响。当葡萄糖浓度为8 g/L时,其OD600值达到最高,羽扇豆醇的产量达到138.70 mg/L。然而,当葡萄糖浓度继续增加,超过8 g/L时,OD600和羽扇豆醇的产量都显著下降(图5-a)。当葡萄糖浓度达到64 g/L时,OD600值接近于零。最后,本研究还利用含吐温80的SBMSN培养基培养LUEAMU,并探索表面活性剂对亲油化合物羽扇豆醇合成的影响。结果表明,SBMSN可产生124.03 mg/L的羽扇豆醇(图5-a)。值得注意的是,在SBMSN的上清液中可检测到羽扇豆醇和角鲨烯,产量分别为57.89 mg/L和7.31 mg/L。综上所述,选择了TB培养基添加8 g/L的葡萄糖为基础,进一步优化甘油含量,以得到最适含量的2种碳源共同作用从而提高羽扇豆醇的产量。
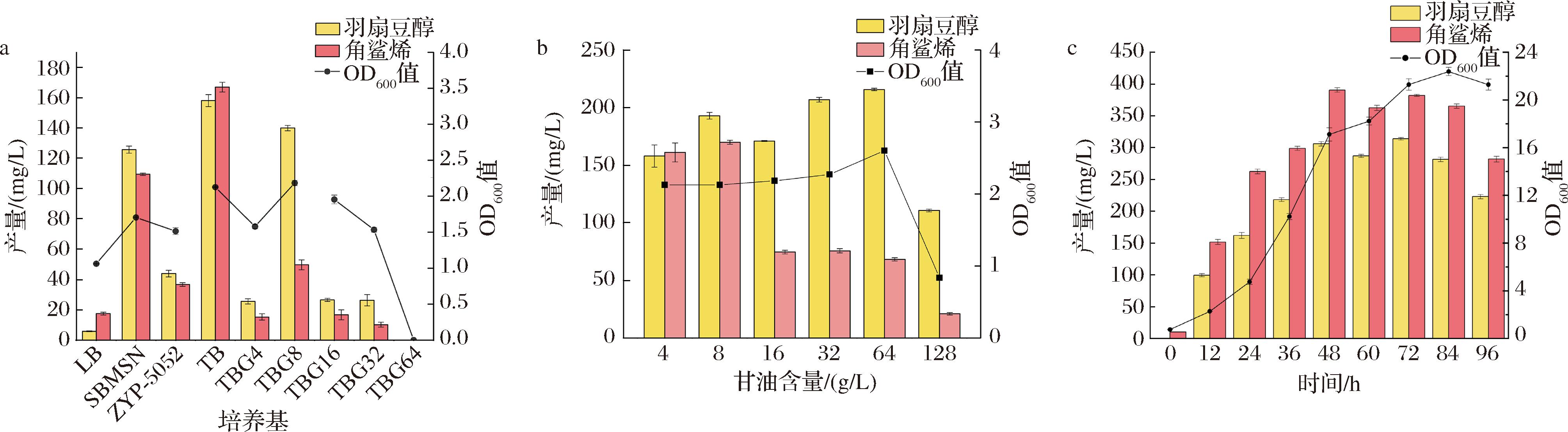
a-培养基对菌体生长和羽扇豆醇产量的影响;b-甘油含量对菌体生长和羽扇豆醇产量的影响;c-补料分批发酵过程中细胞生长、羽扇豆醇和角鲨烯产量的时间进程
图5 不同培养基对羽扇豆醇产量的影响
Fig.5 Effects of different media on lupeol yield
注:TBG4、TBG8、TBG16、TBG32、TBG64分别表示TB培养基中加入4、8、16、32、64 g/L葡萄糖。
2.5 优化甘油浓度以提高羽扇豆醇产量
甘油不仅是TB培养基的主要碳源,也是大肠杆菌MEP途径的直接原料。因此筛选最有益的甘油浓度对于优化LUEAMU的培养条件至关重要。本实验将TB中的甘油含量分别调整为8、16、32、64、128 g/L。结果表明,在甘油含量为8 g/L的条件下,角鲨烯的产量最高,达到171.05 mg/L,在甘油含量为64 g/L的条件下,羽扇豆醇的产量最高,达到214.87 mg/L。然而,当甘油含量增加到128 g/L时,羽扇豆醇的产量下降到111.49 mg/L(图5-b)。显然,64 g/L可视为LUEAMU生长的最佳甘油浓度,在后续放大实验中,该培养基可用作LUEAMU发酵的最佳培养基。
2.6 LUEAMU摇瓶补料分批发酵
基于前期优化结果,本研究采用含64 g/L甘油的TB培养基,在500 mL摇瓶体系中对LUEAMU菌株开展为期4 d的补料分批发酵实验。每24 h补充4 g/L甘油,每36 h补加20%(体积分数)新鲜培养基以维持长期培养需求。如图5-c所示,羽扇豆醇在36 h积累到218.20 mg/L,而经过48 h的补料分批培养后,OD600相对稳定,角鲨烯开始转化为羽扇豆醇,推动产量升至305.07 mg/L。当培养进行到72 h时,羽扇豆醇产量最高达313.95 mg/L(图5-c),较传统分批发酵提升1.46倍。随着羽扇豆醇产量的逐渐减少,补料分批发酵于96 h结束。
3 结论
本研究通过创新性酶组合策略在大肠杆菌中构建了羽扇豆醇内源合成途径。根据之前的研究,与其他SQS相比,H.sapiens源的SQS具有更高的角鲨烯合成活性[13]。而Y.lipolytica来源的SQE具有优异的异源表达特性,可高效催化2,3-环氧化角鲨烯的合成。B.gymnorrhiza来源的LUS虽在酵母中实现了功能验证[14],但其在微生物代谢工程合成体系中的应用尚未见报道。将这3种关键酶整合到大肠杆菌BL21(DE3)菌株中,从而构建了最初的工程化菌株LUE,并最终检测到羽扇豆醇产量为0.89 mg/L。经机制解析发现,羽扇豆醇产量较低与CPR的缺失密切相关——该酶作为电子传递载体,对角鲨烯环氧酶及羽扇豆醇合酶的催化活性具有决定性作用。因此,在后续工艺优化阶段引入外源CPR表达系统,旨在突破电子传递瓶颈以提升产物合成效率。
YlSQE是一种来自Y.lipolytica的蛋白质,它分别与同源YlCPR及S.cerevisiae源ScCPR组成YlCPR/YlSQE与ScCPR/YlSQE氧化系统。此外,采用拟南芥(Arabidopsis thaliana)源AtCPR与荚膜甲基球菌(Methylococcus capsulatus)源McSQE构建AtCPR/McSQE的系统在合成2,3-环氧化角鲨烯时效果显著[20]。因此本研究分别异源表达了3个CPR/SQE系统,为SQE和LUS提供了电子传递的环境,成功获得LUEYC、LUESC及LUEAM 3株工程菌,其羽扇豆醇产量显著提升。其中,LUEAM的羽扇豆醇产量最高(5.37 mg/L),是LUE的6.03倍。证实AtCPR/McSQE系统能高效推动角鲨烯向羽扇豆醇的转化,且AtCPR兼具介导2,3-环氧化角鲨烯合成与后续环化反应的电子传递功能。此外,还推测,LUEYC与LUESC菌株的低产现象可能源于ScCPR与YlCPR仅能协助YlSQE完成角鲨烯环氧化,而无法为BgLUS提供有效的电子传递支持,导致环化反应受阻。该发现揭示了不同CPR/SQE系统与LUS的适配性差异是制约羽扇豆醇合成效率的关键因素。
在之前的研究中,调控萜类化合物合成途径的普遍措施是过表达关键酶。对于MEP途径,DXS作为该途径的起始酶及限速酶,其催化功能依赖于硫胺素焦磷酸(thiamine pyrophosphate,TPP)结合的保守结构域[21]。IDI负责调控IPP与DMAPP的比例平衡[22],是萜类合成通路的关键限速节点。因此,本研究对上述4株工程菌实施IDI与DXS的过表达策略,通过协同强化前体代谢流以提升萜类合成效率。结果显示,4株工程菌均表现出更高的产羽扇豆醇和角鲨烯的能力,这意味着MEP途径的优化可以增强前体物质的供应,进一步促进大肠杆菌中羽扇豆醇的合成。值得注意的是,LUEAMU可以合成的最高产量羽扇豆醇(155.25 mg/L)和角鲨烯(164.25 mg/L),分别是LUEAM的28.91倍和88.78倍,是LUE的174.44倍。这表明DXS和IDI的过量表达可以有效地增加FPP的供应,从而增加角鲨烯和羽扇豆醇的积累。上述结果表明,通过代谢工程改造,如选择合适的CPR、上调关键限制酶等,确实可以解决在引言部分提出的大肠杆菌中可能存在的限制生产的问题,使得大肠杆菌成为生产羽扇豆醇的良好底盘细胞。
本研究通过对比不同工程菌株的代谢特征发现,MEP途径调控菌株LUEYCU的羽扇豆醇合成效率降低而角鲨烯产量显著提升,因此解脂耶氏酵母源CPR(YlCPR)向YlSQE与BgLUS的电子传递效率存在局限性;菌株LUEU与LUESCU则表现出角鲨烯与羽扇豆醇的协同增产效应,推测其机制在于FPP的充足积累可部分补偿CPR缺失对YlSQE酶活的影响。类似现象在拟南芥源SQE(AtSQE)的研究中亦有报道——该酶在大肠杆菌中可不依赖CPR自主催化2,3-环氧化角鲨烯的合成[23]。另外,LUESCU与LUEAMU的产量差异主要源于SQE来源差异导致的催化效率不同,其中AtCPR/McSQE氧化系统展现出更优的异源适配性。综合评估表明,LUEAMU菌株凭借AtCPR与McSQE的高效协同作用,成为本研究筛选获得的最优羽扇豆醇合成工程菌株。
培养基的选择显著影响LUEAMU中羽扇豆醇的产量。尽管作为大肠杆菌常规培养体系,其1.5%有机氮含量可满足基础生长需求,但羽扇豆醇产量始终低于20 mg/L,难以满足工业化生产需求。相比之下,添加2.5%(质量分数)葡萄糖的ZYP-5052培养基是一种无需额外添加诱导剂的替代培养基,乳糖可通过代谢生成半乳糖实现蛋白表达自诱导[24]。然而,ZYP-5052中羽扇豆醇产量较低,可能是由于细胞增殖所需的葡萄糖供应不足。ZYP-5052在促进羽扇豆醇合成方面优于LB,突出了葡萄糖在细胞生长和产物生产中的重要性。在TB基础培养基中添加8 g/L葡萄糖时,菌体OD600达峰值,羽扇豆醇产量提升至138.70 mg/L,而64 g/L的葡萄糖导致生长抑制和羽扇豆醇合成停止。研究证实适宜碳氮比可协同促进细胞生长与产物合成,甘油作为TB培养基中的关键碳源,显著促进了羽扇豆醇的合成。添加了吐温80的SBMSN在上清液和细胞中均检测到了羽扇豆醇的产生,这可能是因为吐温80通过增溶作用促进亲脂性产物羽扇豆醇的胞外分泌。综上所述,TB培养基因其丰富的碳源、较高的酵母抽提物含量、丰富的氨基酸和微量元素,能够维持细胞的生长和蛋白表达,是培养LUEAMU的首选培养基。在含8 g/L甘油的TB培养基中培养LUEAMU,角鲨烯产量为171.05 mg/L。当甘油添加量提高到64 g/L时,羽扇豆醇产量提高到214.87 mg/L,比初始水平提高了1.38倍。相反,添加128 g/L的甘油抑制了LUEAMU的生长和蛋白表达,导致羽扇豆醇的产量降低至111.49 mg/L。因此,确定了64 g/L的甘油添加量为既能保证LUEAMU高效生长又能最大化羽扇豆醇合成的最优条件。
为了进一步提高羽扇豆醇的产量并缓解传统发酵中的底物限制问题,本研究进行了补料分批发酵。经此补料分批发酵后,羽扇豆醇产量显著提高,且发酵产物中仍存在大量角鲨烯,表明后续补料方式可支持羽扇豆醇的连续合成,具有一定的羽扇豆醇产量放大潜力。结果表明,发酵48 h时,羽扇豆醇的产量可达305.07 mg/L,接近72 h时的最大产量313.95 mg/L。因此,综合考虑培养时间和培养成本,摇瓶最佳培养时间为48 h。
综上所述,本研究在大肠杆菌中构建了羽扇豆醇的合成途径,并通过代谢工程手段调控代谢流以提升其产量,在大肠杆菌中实现了313.95 mg/L的羽扇豆醇最高产量。本研究表明,大肠杆菌可以作为一种高效的羽扇豆醇生产底盘。
[1] SIDDIQUE H R,SALEEM M.Beneficial health effects of lupeol triterpene:A review of preclinical studies[J].Life Sciences,2011,88(7-8):285-293.
[2] FUKUSHIMA E O,SEKI H,OHYAMA K,et al.CYP716A subfamily members are multifunctional oxidases in triterpenoid biosynthesis[J].Plant &Cell Physiology,2011,52(12):2050-2061.
[3] PAPI REDDY K,SINGH A B,PURI A,et al.Synthesis of novel triterpenoid (lupeol) derivatives and their in vivo antihyperglycemic and antidyslipidemic activity[J].Bioorganic &Medicinal Chemistry Letters,2009,19(15):4463-4466.
[4] RAMOS-HERN NDEZ J A,CALDER
NDEZ J A,CALDER N-SANTOYO M,NAVARRO-OCA
N-SANTOYO M,NAVARRO-OCA A A,et al.Use of emerging technologies in the extraction of lupeol,α-amyrin and β-amyrin from sea grape (Coccoloba uvifera L.)[J].Journal of Food Science and Technology,2018,55(7):2377-2383.
A A,et al.Use of emerging technologies in the extraction of lupeol,α-amyrin and β-amyrin from sea grape (Coccoloba uvifera L.)[J].Journal of Food Science and Technology,2018,55(7):2377-2383.
[5] LIU S Y,XU F,LIU L J,et al.A convenient synthesis of lupeol from betulin[J].Industrial Crops and Products,2015,74:494-496.
[6] PADDON C J,WESTFALL P J,PITERA D J,et al.High-level semi-synthetic production of the potent antimalarial artemisinin[J].Nature,2013,496(7446):528-532.
[7] WESTFALL P J,PITERA D J,LENIHAN J R,et al.Production of amorphadiene in yeast,and its conversion to dihydroartemisinic acid,precursor to the antimalarial agent artemisinin[J].Proceedings of the National Academy of Sciences of the United States of America,2012,109(3):E111-E118.
[8] ZHANG J L,BAI Q Y,PENG Y Z,et al.High production of triterpenoids in Yarrowia lipolytica through manipulation of lipid components[J].Biotechnology for Biofuels,2020,13:133.
[9] BRÖKER J N,MÜLLER B,VAN DEENEN N,et al.Upregulating the mevalonate pathway and repressing sterol synthesis in Saccharomyces cerevisiae enhances the production of triterpenes[J].Applied Microbiology and Biotechnology,2018,102(16):6923-6934.
[10] LIN X N,AN T Y,FU D N,et al.Optimization of central carbon metabolism by Warburg effect of human cancer cell improves triterpenes biosynthesis in yeast[J].Advanced Biotechnology,2023,1(4):4.
[11] JIANG M,STEPHANOPOULOS G,PFEIFER B A.Toward biosynthetic design and implementation of Escherichia coli-derived-derived paclitaxel and other heterologous polyisoprene compounds[J].Applied and Environmental Microbiology,2012,78(8):2497-2504.
[12] LEONARD E,KOFFAS M A G.Engineering of artificial plant cytochrome P450 enzymes for synthesis of isoflavones by Escherichia coli[J].Applied and Environmental Microbiology,2007,73(22):7246-7251.
[13] QIAO W B,ZHOU Z L,LIANG Q,et al.Improving lupeol production in yeast by recruiting pathway genes from different organisms[J].Scientific Reports,2019,9:2992.
[14] BASYUNI M,OKU H,TSUJIMOTO E,et al.Triterpene synthases from the Okinawan mangrove tribe,Rhizophoraceae[J].The FEBS Journal,2007,274(19):5028-5042.
[15] LIU Z,ZHANG Y N,SUN J N,et al.A novel soluble squalene-hopene cyclase and its application in efficient synthesis of hopene[J].Frontiers in Bioengineering and Biotechnology,2020,8:426.
[16] RENAULT H,BASSARD J E,HAMBERGER B,et al.Cytochrome P450-mediated metabolic engineering:Current progress and future challenges[J].Current Opinion in Plant Biology,2014,19:27-34.
[17] HAUSJELL J,HALBWIRTH H,SPADIUT O.Recombinant production of eukaryotic cytochrome P450 s in microbial cell factories[J].Bioscience Reports,2018,38(2):BSR20171290.
[18] DAS A,YOON S H,LEE S H,et al.An update on microbial carotenoid production:Application of recent metabolic engineering tools[J].Applied Microbiology and Biotechnology,2007,77(3):505-512.
[19] LIU H W,WANG Y,TANG Q,et al.MEP pathway-mediated isopentenol production in metabolically engineered Escherichia coli[J].Microbial Cell Factories,2014,13(1):135.
[20] LI D S,ZHANG Q,ZHOU Z J,et al.Heterologous biosynthesis of triterpenoid dammarenediol-II in engineered Escherichia coli[J].Biotechnology Letters,2016,38(4):603-609.
[21] JADAUN J S,SANGWAN N S,NARNOLIYA L K,et al.Over-expression of DXS gene enhances terpenoidal secondary metabolite accumulation in rose-scented Geranium and Withania somnifera:Active involvement of plastid isoprenogenic pathway in their biosynthesis[J].Physiologia Plantarum,2017,159(4):381-400.
[22] HARADA H,MISAWA N.Novel approaches and achievements in biosynthesis of functional isoprenoids in Escherichia coli[J].Applied Microbiology and Biotechnology,2009,84(6):1021-1031.
[23] TAKEMURA M,TANAKA R,MISAWA N.Pathway engineering for the production of β-amyrin and cycloartenol in Escherichia coli:A method to biosynthesize plant-derived triterpene skeletons in E.coli[J].Applied Microbiology and Biotechnology,2017,101(17):6615-6625.
[24] STUDIER F W.Protein production by auto-induction in high-density shaking cultures[J].Protein Expression and Purification,2005,41(1):207-234.