近年来我国慢性病如肥胖、糖尿病等患病率呈逐年上升趋势,这与过度追求主食精细化以及饮食结构失衡有着密切的关系[1]。因此调整膳食结构、促进全谷物消费至关重要。糙米是一种全谷物食品,保留了除谷壳以外的所有成分[2]。糙米可分为普通糙米和有色糙米,都是以未精加工的形式食用,统称为糙米。全谷物是膳食多酚的重要来源,具有重要的抗氧化特性和生物活性[3]。但其难煮、难吃、难贮藏等缺点不易被大众接受,从而限制了其作为主食的消费潜力。
国内外的研究通常采用物理、化学和生物法,或多种方法协同作用的方式,对糙米表皮结构及其组织成分进行改良,从而提升其蒸煮特性和食用品质[4]。然而,每种方法都存在一定的局限性。生物发酵是一种利用微生物代谢过程生产化合物的环保、安全和高效的技术[5]。通过微生物及其酶对糙米基质进行生物化学修饰的过程,为改善糙米品质提供一种新思路。其中半固态发酵不仅拓宽了固态发酵的基质范围,而且与液态发酵相比,具有产物浓度高、能耗低等优点。
目前,国内外研究多采用单菌种或混合菌种固态发酵常规糙米,对乳酸菌半固态发酵有色糙米的研究较少。本研究以3种全谷物糙米、红米和黑米即“三色糙米”为研究对象,通过单因素和正交试验,筛选各谷物对应的最佳发酵菌种和最优发酵条件。在最佳发酵菌株和最优发酵条件的基础上,探究乳酸菌半固态发酵对3种谷物生物活性成分和抗氧化性能的影响。为全谷物米制蒸煮食品加工共性关键技术研究提供技术支撑和理论依据,为我国慢性病防控和全谷物推广提供理论参考和实践指导。
1 材料与方法
1.1 材料与试剂
原料:糙米、红米和黑米,洋县(中国陕西汉中),名称分别为BRR、RER和BLR。植物乳植杆菌(Lactiplantibacillus plantarum)NO.1~8是从人体肠道菌群中分离出来的冻干粉,保存于江南大学食品科学与资源挖掘全国重点实验室。嗜酸乳杆菌(Lactobacillus acidophilus,简称SS)和干酪乳酪杆菌(Lacticaseibacillus casei,简称干),北京BIOBW生物技术有限公司,并在本实验室保存。
试剂:Folin-Ciocalteu试剂、DPPH、6-羟基-2,5,7,8-四甲基铬-2-羧酸(Trolox)、酚类和花青素标准品,美国Sigma-Aldrich公司;MRS液体培养基、MRS固体培养基,青岛希望生物科技有限公司。除另有说明外,其他化学试剂均为分析纯。
1.2 仪器与设备
AX224ZH/E电子分析天平,奥豪斯仪器(常州)有限公司;UV-3200紫外分光光度计,上海美谱达仪器有限公司;LXJ-Ⅱ高速离心机,上海安亭科学仪器厂;synergy HTX酶标仪,中国Gene Company有限公司。
1.3 实验方法
1.3.1 菌株的活化、传代及接种
先用MRS液体培养基对菌种活化传代2次,37 ℃静置培养18~24 h。将第三代菌株以体积分数3%的接种量接种到经固定固液比浸泡灭菌后的糙米中,37 ℃发酵。发酵过程中,间歇性地晃动发酵容器。将发酵后的糙米在50 ℃热风干燥烘至表面干燥,糙米的含水量低于14%(质量分数)。将发酵后的糙米干燥后脱气密封包装,即得成品。
1.3.2 原始菌株的生长曲线及分子生物学鉴定
将上述二代菌株以体积分数为3%的接种量接种到MRS液体培养基中,置于37 ℃恒温摇床中以120 r/min的转速进行24 h培养。培养过程中每隔2 h取样1次,使用分光光度计在600 nm波长下测定样品吸光值,并以空白MRS液体培养基作为对照组。
参照朱春霞等[6]的方法,采用16 s rDNA序列对发酵菌株进行鉴定。具体实验步骤如下:首先提取乳酸菌基因组DNA作为PCR扩增的模板,构建50 μL反应体系,其中包括2 μL模板DNA,1.5 μL 10 mmol上下游引物,25 μL 2×Taq酶,并以ddH2O补至50 μL。PCR扩增程序设置为:94 ℃预变性5 min;94 ℃变性1 min,64 ℃退火45 s,72 ℃延伸1 min,循环35次;72 ℃延伸8 min。吸取PCR产物5 μL与1 mL Loading buffer混合,用1.0%(质量分数)琼脂糖凝胶电泳,电压为80 V。电泳结束后用溴化乙锭染色20~30 min。经凝胶电泳验证扩增产物后,将样品送至上海生工生物工程技术服务有限公司进行序列测定。
1.3.3 最佳发酵菌株的筛选
对上述发酵产物的蒸煮时间进行测定并做感官评价,以感官评价和最佳蒸煮时间为评价指标,筛选各谷物对应的最佳发酵乳酸菌。
1.3.4 发酵条件的工艺优化
1.3.4.1 单因素试验
根据预实验结果,在各谷物对应的最佳发酵菌株的基础上。考察发酵时间(4、6、8、10、12 h)、接菌量(1%、2%、3%、4%、5%,体积分数)、米水比(1∶0.6、1∶0.7、1∶0.8、1∶0.9、1∶1,g∶mL)和发酵温度(25、28、31、34、37 ℃)对发酵有色糙米的影响。以发酵产物的感官评价和最佳蒸煮时间为评价指标进行单因素试验。
1.3.4.2 正交试验
基于单因素试验确定的条件,采用L9(34)正交试验设计,以发酵产物感官品质和蒸煮时间作为关键评价指标进行工艺优化。筛选各谷物对应的最佳发酵条件。具体因素水平设置见表1~表3。
表1 糙米发酵条件正交试验因素水平
Table 1 Orthogonal test factor levels for brown rice fermentation conditions
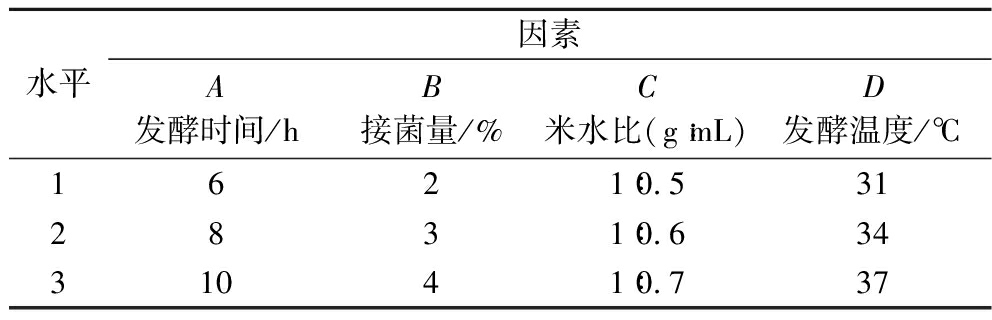
水平因素A发酵时间/hB接菌量/%C米水比(g∶mL)D发酵温度/℃1621∶0.5312831∶0.63431041∶0.737
表2 红米发酵条件正交试验因素水平
Table 2 Orthogonal test factor levels for red rice fermentation conditions
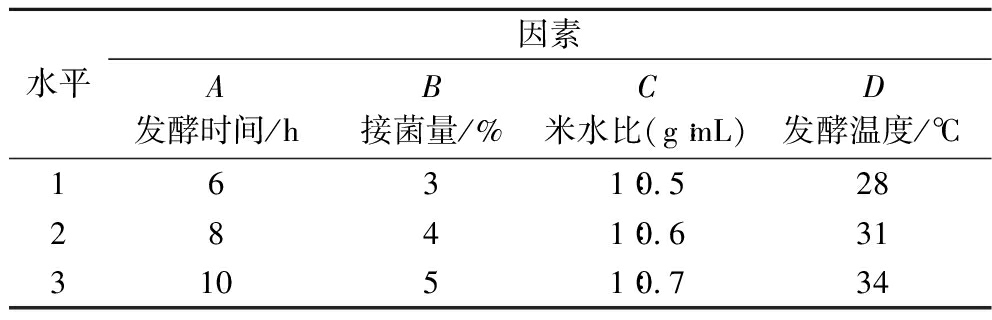
水平因素A发酵时间/hB接菌量/%C米水比(g∶mL)D发酵温度/℃1631∶0.5282841∶0.63131051∶0.734
表3 黑米发酵条件正交试验因素水平
Table 3 Orthogonal test factor levels for black rice fermentation conditions
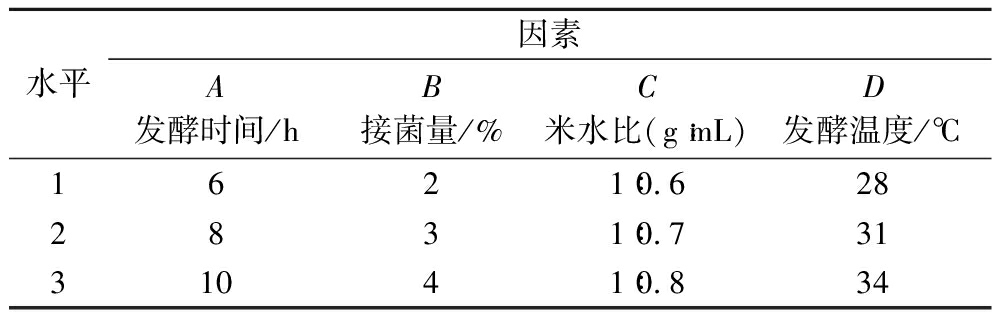
水平因素A发酵时间/hB接菌量/%C米水比(g∶mL)D发酵温度/℃1621∶0.6282831∶0.73131041∶0.834
1.3.5 浸泡吸水率的测定
糙米浸泡吸水率的测定参照吴艺婕[7]的方法,计算如公式(1)所示:
糙米浸泡吸水率![]()
(1)
1.3.6 最佳蒸煮时间的测定
糙米的最佳蒸煮时间参照MOHAPATRA等[8]的方法。
1.3.7 感官评价最佳蒸煮时间的测定
依据GB/T 15682—2008《粮油检验 稻谷、大米蒸煮食用品质感官评价方法》评分标准,组建了由10名经过专业感官评估培训的品评小组,对糙米饭的气味、外观、滋味、适口性和质地五个感官指标进行系统评价。本研究得到江南大学食品学院的支持,并通过了伦理审查。10名小组成员还签署了知情同意书。
1.3.8 酚类化合物的提取
准确称取糙米粉(80目),1∶2(g∶mL)加入体积分数80%甲醇混合均匀,常温超声提取90 min,4 000 r/min离心10 min,收集上清液,重复提取3次。合并上清液于40 ℃旋转蒸干后用80%(体积分数)甲醇定容,即为游离酚。将提取完游离酚的残渣在室温条件下加入4 mol/L NaOH溶液避光涡旋1 min,混匀室温搅拌水解1 h。随后,用浓盐酸调节pH至酸性。接着加入乙酸乙酯萃取5 min,4 000 r/min离心10 min。此操作重复3次。将溶液在45 ℃下旋转蒸干后,用体积分数80%甲醇定容,即为结合酚。游离酚和结合酚均保存于4 ℃冰箱,并在1周内进行分析。
1.3.9 总酚、总黄酮、花青素含量及抗氧化性的测定
参考ZENG等[9]的方法测定样品中总酚、总黄酮、花青素含量和抗氧化性并做修改。具体而言,总酚含量测定采用Folin-Ciocalteu比色法,结果以每克干重样品中没食子酸当量(μg GAE/g DW)表示。总黄酮含量测定则通过优化NaNO2-AlCl3·6H2O比色法测定,结果以每克干重样品中芦丁当量(μg TE/g DW)表示。花青素含量测定采用pH示差法,结果以每克干重样品中矢车菊素-3-葡萄糖苷当量(μg Cy/g DW)表示。抗氧化活性评价采用DPPH自由基清除法、ABTS阳离子自由基清除法以及铁离子还原能力(Ferric reducing ability of plasma,FRAP)法进行测定,其中DPPH自由基和ABTS阳离子自由基清除能力以清除率表示,FRAP值则以每克干重样品的当量(μg Trolox/g DW)表示。
1.4 数据处理与统计分析
所有实验数据使用Origin 2024、GraphPad Prism 8进行绘图。采用IBM SPSS统计26(SPSS Inc.,Chicago,IL,USA),通过方差分析(analysis of variance,ANOVA)和Tukey事后检验确定样本间的统计平均差异。所有实验组均为3个重复,当P<0.05时,差异被认为是显著的。数据结果以“平均值±标准差”表示。
2 结果与分析
2.1 菌株的生长曲线及分子生物学鉴定
由图1-A可知,相同培养条件下(37 ℃,24 h),不同菌株生长曲线呈“S”型,总体而言,在600 nm下OD值在17~19 h达到峰值。为保证单因素原则,故确定不同菌株的最佳培养时间为18 h。
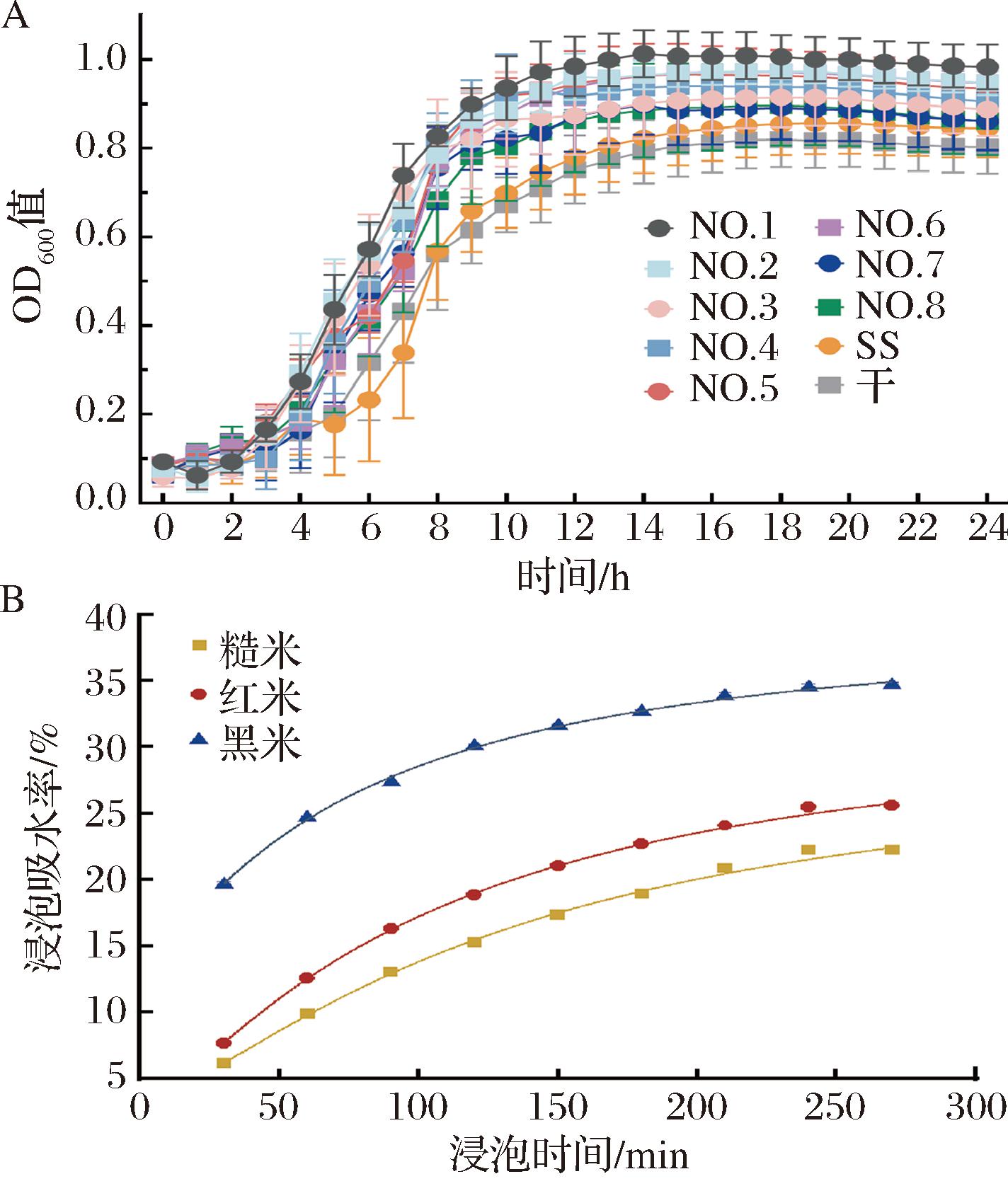
A-菌株的生长曲线;B-谷物浸泡吸水率
图1 菌株的生长曲线和谷物浸泡吸水率
Fig.1 Growth curves of strains and grain soaking water absorption
注:图中NO.1~8分别表示L.plantarum NO.1~8。
适宜的吸水率能软化糙米结构,促进乳酸菌的生长和代谢。浸泡时间过短,吸水不足,可能导致发酵不均匀;时间过长,则可能引发微生物污染或营养成分流失[10]。通过测定吸水率,可以优化浸泡时间,确保糙米在发酵前达到理想的含水量,从而提高发酵效率和产品质量。因此,提前测定糙米的浸泡吸水率是优化发酵工艺的关键步骤。通过测定谷物浸泡吸水率,如图1-B所示,各谷物的浸泡吸水率在4 h基本达到饱和,故确定各谷物发酵前浸泡4 h。
将测序得到的序列与GenBank数据库中的序列进行比对分析,指数超过95%,可以鉴定到种水平。如表4所示,其结果显示菌株NO.1~2、NO.4~8为L.plantarum,NO.3为戊糖乳杆菌(Lactobacillus pentosus)。
表4 菌株鉴定结果
Table 4 Strain identification results
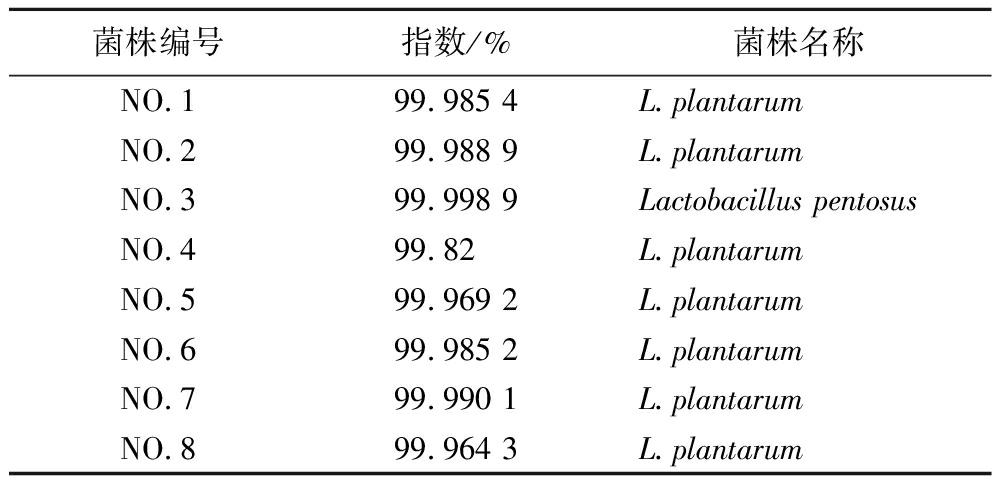
菌株编号指数/%菌株名称NO.199.985 4L.plantarumNO.299.988 9L.plantarumNO.399.998 9Lactobacillus pentosusNO.499.82L.plantarumNO.599.969 2L.plantarumNO.699.985 2L.plantarumNO.799.990 1L.plantarumNO.899.964 3L.plantarum
2.2 最佳发酵菌株的筛选
发酵过程中,乳酸菌分泌的酶(如淀粉酶、蛋白酶)分解糙米中的大分子物质,如淀粉和蛋白质,生成小分子糖类和氨基酸,不仅改善口感,还缩短蒸煮时间[11]。如图2所示,相同的发酵条件下,NO.4菌株发酵的糙米的最佳蒸煮时间最短且感官评分较高,故糙米对应的最佳发酵菌株为NO.4。同理红米和黑米对应的最佳发酵菌株为NO.1。
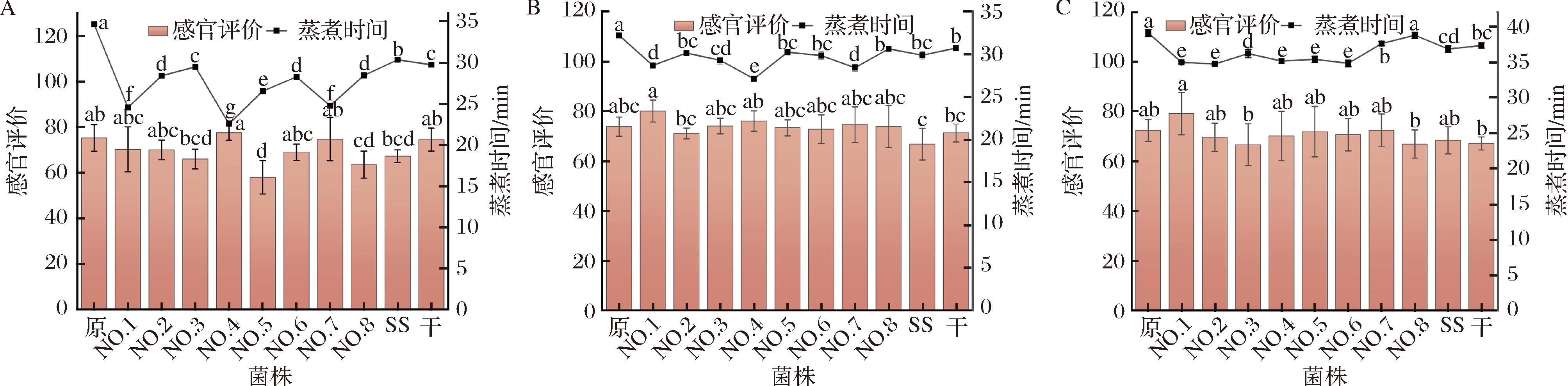
A-糙米;B-红米;C-黑米
图2 不同菌株对谷物感官评价和最佳蒸煮时间的影响
Fig.2 Effect of different strains of bacteria on sensory evaluation and optimal cooking time of grains
注:不同小写字母表示差异显著(P<0.05)(下同);原表示对照,即相同条件下未接入菌株(未发酵)。
2.3 单因素试验
感官评价即通过人的感官(视觉、嗅觉、味觉、触觉等)对发酵糙米的外观、香气、口感、质地等进行综合评估。最佳蒸煮时间是指使发酵糙米达到理想食用品质所需的最短加热时长,该指标能够有效反映发酵处理对谷物蒸煮特性的改良程度。
由图3-A1~图3-C1可知,糙米在发酵8 h时感官评价最高,最佳蒸煮时间最短。红米和黑米也出现相同的变化规律。因此,糙米、红米和黑米对应的最佳发酵时间均为8 h。

A1~A4-糙米;B1~B4-红米;C1~C4-黑米
图3 不同发酵参数对谷物感官评价和最佳蒸煮时间的影响
Fig.3 Effect of different fermentation parameters on sensory evaluation and optimal cooking time of grains
由图3-A2~图3-C2可知,糙米和黑米在接菌量为体积分数3%时感官评价最高,最佳蒸煮时间最短。红米在接菌量为体积分数4%时感官评价最高,最佳蒸煮时间最短。因此,糙米和黑米对应的最佳接菌量为体积分数3%,红米对应的最佳接菌量为体积分数4%。
由图3-A3~图3-C3可知,糙米和红米在米水比为1∶0.6(g∶mL)时感官评价最高,最佳蒸煮时间最短。黑米在米水比为1∶0.7(g∶mL)时感官评价最高,最佳蒸煮时间最短。因此,糙米和红米对应的最佳米水比为1∶0.6(g∶mL),黑米对应的最佳米水比为1∶0.7(g∶mL)。
由图3-A4~图3-C4可知,糙米在发酵温度为34 ℃时感官评价最高,最佳蒸煮时间最短。红米和黑米在发酵温度为31 ℃时感官评价最高,最佳蒸煮时间最短。因此,糙米对应的最佳发酵温度为34 ℃,红米和黑米对应的最佳发酵温度为31 ℃。
2.4 正交试验结果
根据单因素试验结果,通过糙米分析表5中的正交试验极差结果发现,就感官评价而言,各因素的影响程度依次为A>B>C>D,最佳组合方案为A2B2C2D2。从最佳蒸煮时间来看,各因素的影响程度表现为D>B>A>C,最优组合方案为A2B2C1D1。
表5 糙米正交试验结果
Table 5 Results of orthogonal test on brown rice
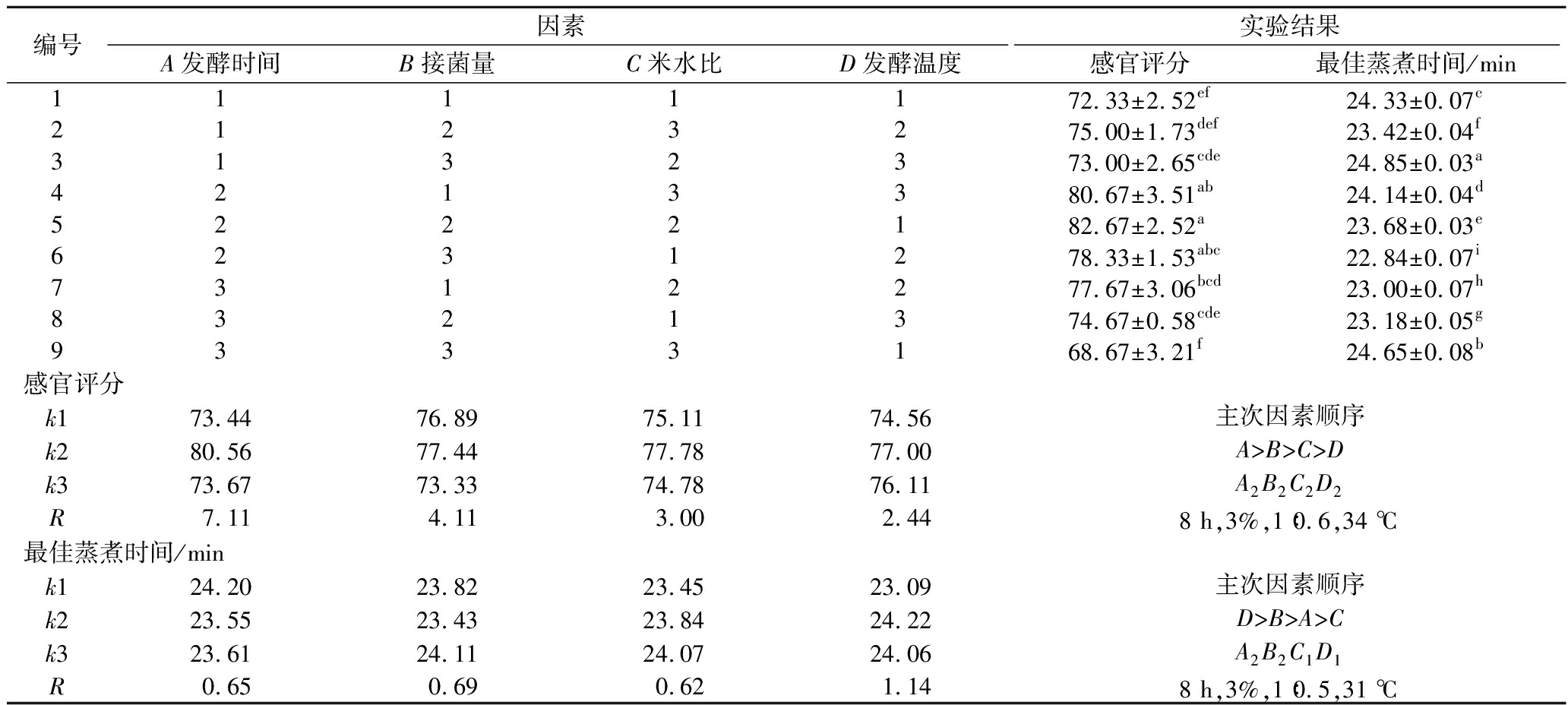
编号因素实验结果A发酵时间B接菌量C米水比D发酵温度感官评分最佳蒸煮时间/min1111172.33±2.52ef24.33±0.07c2123275.00±1.73def23.42±0.04f3132373.00±2.65cde24.85±0.03a4213380.67±3.51ab24.14±0.04d5222182.67±2.52a23.68±0.03e6231278.33±1.53abc22.84±0.07i7312277.67±3.06bcd23.00±0.07h8321374.67±0.58cde23.18±0.05g9333168.67±3.21f24.65±0.08b感官评分k173.4476.8975.1174.56k280.5677.4477.7877.00k373.6773.3374.7876.11R7.114.113.002.44主次因素顺序A>B>C>DA2B2C2D28 h,3%,1∶0.6,34 ℃最佳蒸煮时间/mink124.2023.8223.4523.09k223.5523.4323.8424.22k323.6124.1124.0724.06R0.650.690.621.14主次因素顺序D>B>A>CA2B2C1D18 h,3%,1∶0.5,31 ℃
注:不同小写字母表示差异显著(P<0.05)(下同)。
由于不同因素对各指标影响程度不同,对表5结果进行方差分析和显著性检验,结果见表6,除了发酵时间,其他3个因素对糙米的感官评价影响显著(P<0.05);各因素对糙米的最佳蒸煮时间均产生了显著影响(P<0.05)。通过比较F值发现,以感官评价为指标的各因素的影响程度依次为A>B>C>D;而以最佳蒸煮时间为指标的各因素影响程度则表现为D>A>B>C,这一结果比直观分析更为精确。因素A、B、C在感官评价的排序优于在最佳蒸煮时间的顺序,因而优先考虑感官评价,最终选择A2B2C2;而因素D在最佳蒸煮时间中的排序更为靠前,表明发酵温度对最佳蒸煮时间的影响超过感官评价,故而选D1。故最优方案为A2B2C2D1,即发酵时间8 h、接菌量3%,米水比1∶0.6,发酵温度31 ℃。后期实验中发酵糙米的制备均采用此工艺参数。
表6 糙米方差分析
Table 6 ANOVA for brown rice
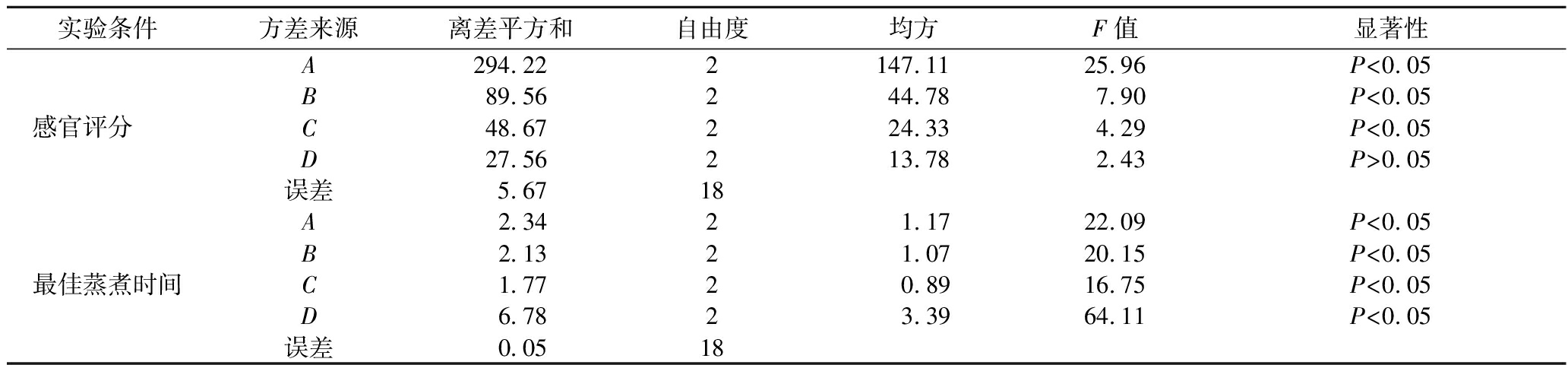
实验条件方差来源离差平方和自由度均方F值显著性感官评分 A294.222147.1125.96P<0.05B89.56244.787.90P<0.05C48.67224.334.29P<0.05D27.56213.782.43P>0.05误差5.6718最佳蒸煮时间A 2.342 1.1722.09P<0.05B2.1321.0720.15P<0.05C1.7720.8916.75P<0.05D6.7823.3964.11P<0.05误差0.0518
根据单因素试验结果,通过红米分析表7中的正交试验极差结果发现,就感官评价而言,各因素的影响程度依次为C>D>A>B,最佳组合方案为A3B1C2D2。从最佳蒸煮时间来看,各因素的影响程度表现为D>C>B>A,最佳组合方案为A1B1C1D2。
表7 红米正交试验结果
Table 7 Results of orthogonal test on red rice
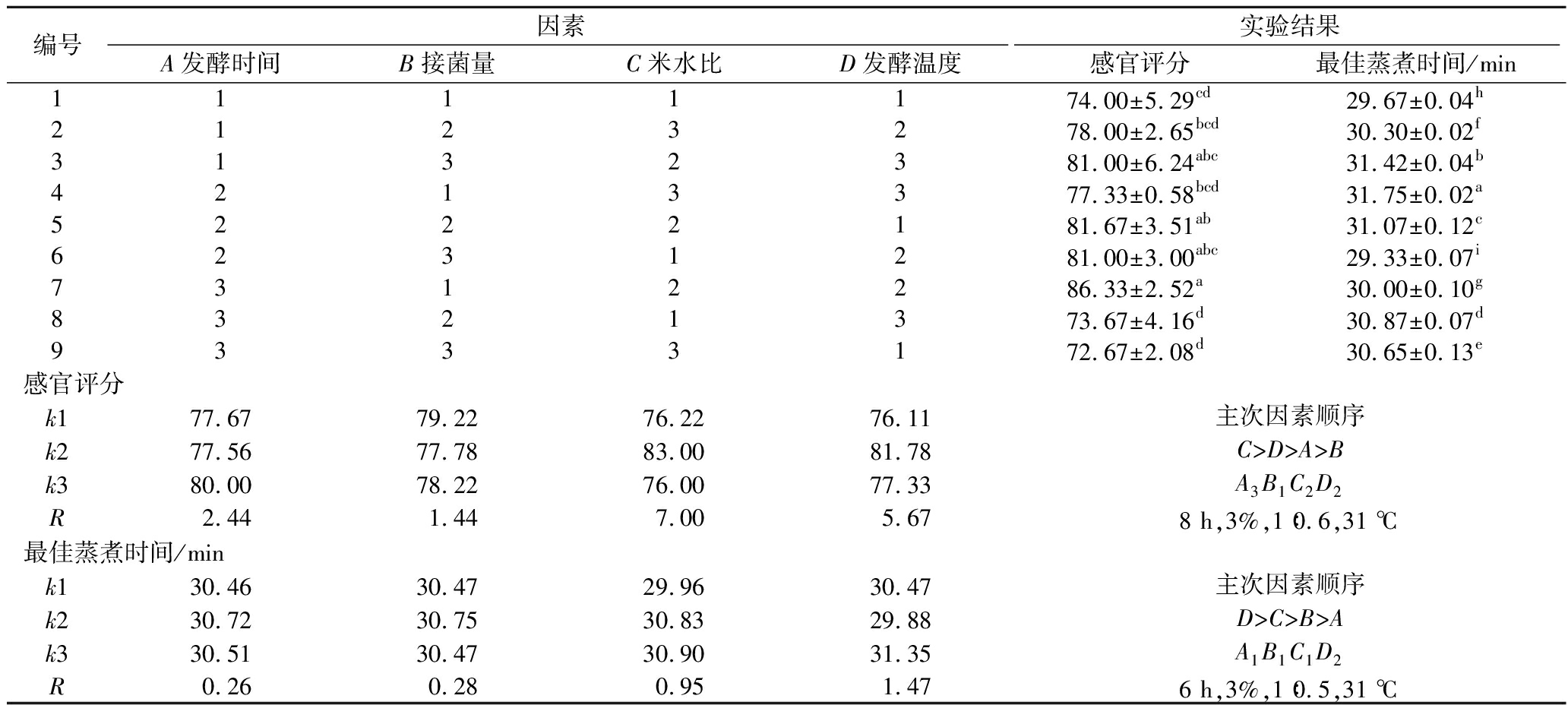
编号因素实验结果A发酵时间B接菌量C米水比D发酵温度感官评分最佳蒸煮时间/min1111174.00±5.29cd29.67±0.04h2123278.00±2.65bcd30.30±0.02f3132381.00±6.24abc31.42±0.04b4213377.33±0.58bcd31.75±0.02a5222181.67±3.51ab31.07±0.12c6231281.00±3.00abc29.33±0.07i7312286.33±2.52a30.00±0.10g8321373.67±4.16d30.87±0.07d9333172.67±2.08d30.65±0.13e感官评分k177.6779.2276.2276.11k277.5677.7883.0081.78k380.0078.2276.0077.33R2.441.447.005.67主次因素顺序C>D>A>BA3B1C2D28 h,3%,1∶0.6,31 ℃最佳蒸煮时间/mink130.4630.4729.9630.47k230.7230.7530.8329.88k330.5130.4730.9031.35R0.260.280.951.47主次因素顺序D>C>B>AA1B1C1D26 h,3%,1∶0.5,31 ℃
由于不同因素对各指标影响程度不同,对表7结果进行方差分析和显著性检验,结果见表8,除接菌量,其他3个因素对红米的感官评价影响显著(P<0.05);米水比和发酵温度对红米的最佳蒸煮时间影响显著(P<0.05),发酵时间和接菌量对最佳蒸煮时间的影响未达到显著水平(P>0.05)。通过方差分析发现,不同评价指标下各影响因素的重要性排序存在差异:就感官评价而言,影响因素的重要性排序为C>D>A>B;而以最佳蒸煮时间为评价指标时,其重要性排序则为D>C>B>A,该结果较直观分析更为精确。因素A和C在感官评价的排序优于在最佳蒸煮时间的排序,这表明感官评价应作为首要考虑因素,因而选取A3C2;相比之下,因素B和D在最佳蒸煮时间的排序更为靠前,说明接菌量和发酵温度对最佳蒸煮时间的影响程度显著大于其对感官评价的影响,基于此选择B1D2。故最优方案为A3B1C2D2,即发酵时间10 h、接菌量3%,米水比1∶0.6,发酵温度31 ℃。后期实验中发酵红米的制备均采用此工艺参数。
表8 红米方差分析
Table 8 ANOVA for red rice
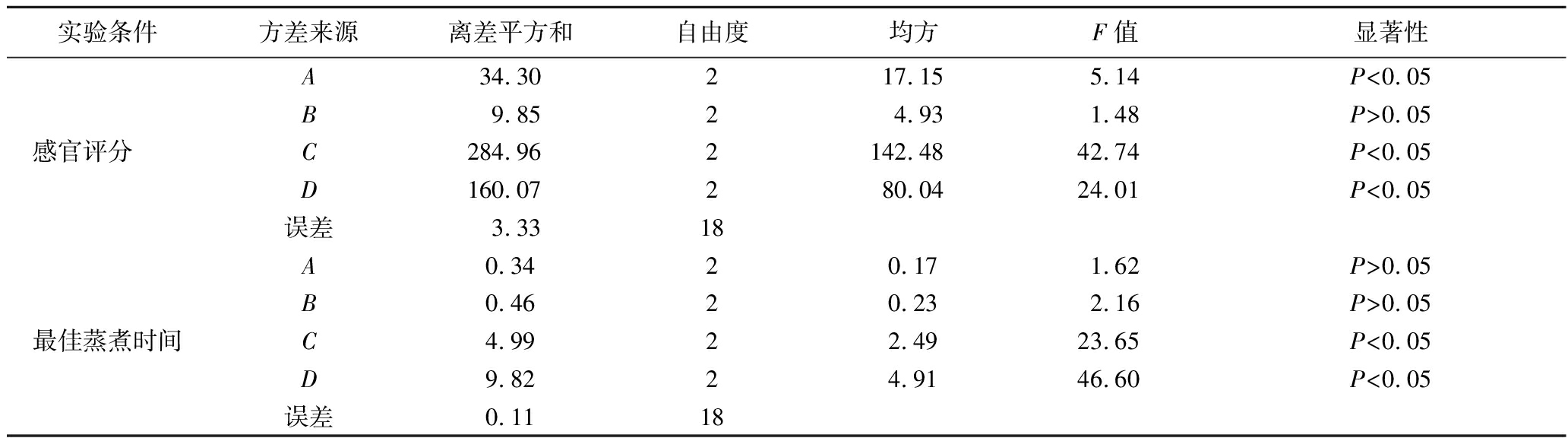
实验条件方差来源离差平方和自由度均方F值显著性感官评分 A34.30 217.15 5.14 P<0.05B9.85 24.93 1.48 P>0.05C284.96 2142.48 42.74 P<0.05D160.07 280.04 24.01 P<0.05误差3.33 18最佳蒸煮时间A0.34 20.17 1.62 P>0.05B0.46 20.23 2.16 P>0.05C4.99 22.49 23.65 P<0.05D9.82 24.91 46.60 P<0.05误差0.11 18
根据单因素试验结果,通过黑米分析表9中的正交试验极差结果发现,就感官评价而言,各因素的影响程度依次为D>A>C>B,最佳组合方案为A3B2C2D1。从最佳蒸煮时间来看,各因素的影响程度表现为A>D>C>B,最佳组合方案为A2B3C2D2。
表9 黑米正交试验结果
Table 9 Results of orthogonal test on black rice
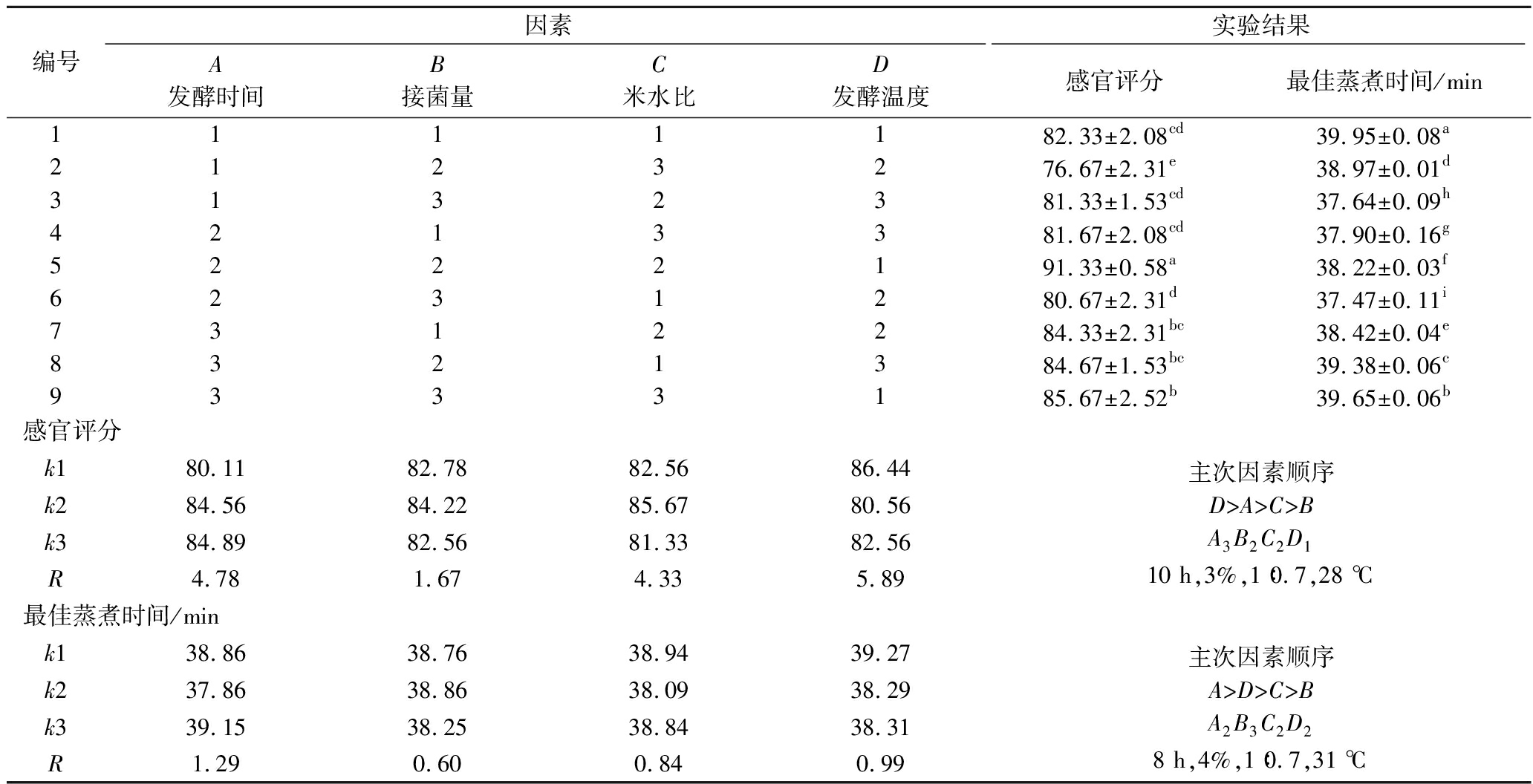
编号因素实验结果A发酵时间B接菌量C米水比D发酵温度感官评分最佳蒸煮时间/min1111182.33±2.08cd39.95±0.08a2123276.67±2.31e38.97±0.01d3132381.33±1.53cd37.64±0.09h4213381.67±2.08cd37.90±0.16g5222191.33±0.58a38.22±0.03f6231280.67±2.31d37.47±0.11i7312284.33±2.31bc38.42±0.04e8321384.67±1.53bc39.38±0.06c9333185.67±2.52b39.65±0.06b感官评分k180.1182.7882.5686.44k284.5684.2285.6780.56k384.8982.5681.3382.56R4.781.674.335.89主次因素顺序D>A>C>BA3B2C2D110 h,3%,1∶0.7,28 ℃最佳蒸煮时间/mink138.8638.7638.9439.27k237.8638.8638.0938.29k339.1538.2538.8438.31R1.290.600.840.99主次因素顺序A>D>C>BA2B3C2D28 h,4%,1∶0.7,31 ℃
由于不同因素对各指标影响程度不同,对表9结果进行方差分析和显著性检验,结果见表10,除接菌量,其他3个因素对黑米的感官评价影响显著(P<0.05);各因素对黑米的最佳蒸煮时间的影响均达到显著水平(P<0.05)。通过比较F值发现,以感官评价为指标的各因素的影响程度依次为D>A>C>B;而以最佳蒸煮时间为指标的各因素影响程度则表现为A>D>C>B,比直观分析更为准确。因素A在最佳蒸煮时间的排序优于在感官评价的排序,因而优先考虑最佳蒸煮时间,最终选择A2;因素B和C对2个指标均具有显著影响,但由于本实验以感官评价为主要参考指标,因此在因素选择时优先考虑感官评价,最终选择B3C2;因素D在感官评价的排序优于在最佳蒸煮时间的排序,因而优先考虑感官评价,故选取D1。故最优方案为A2B2C2D1,即发酵时间8 h、接菌量3%,米水比1∶0.7,发酵温度28 ℃。后期实验中发酵黑米的制备均采用此工艺参数。
表10 黑米方差分析
Table 10 ANOVA for black rice
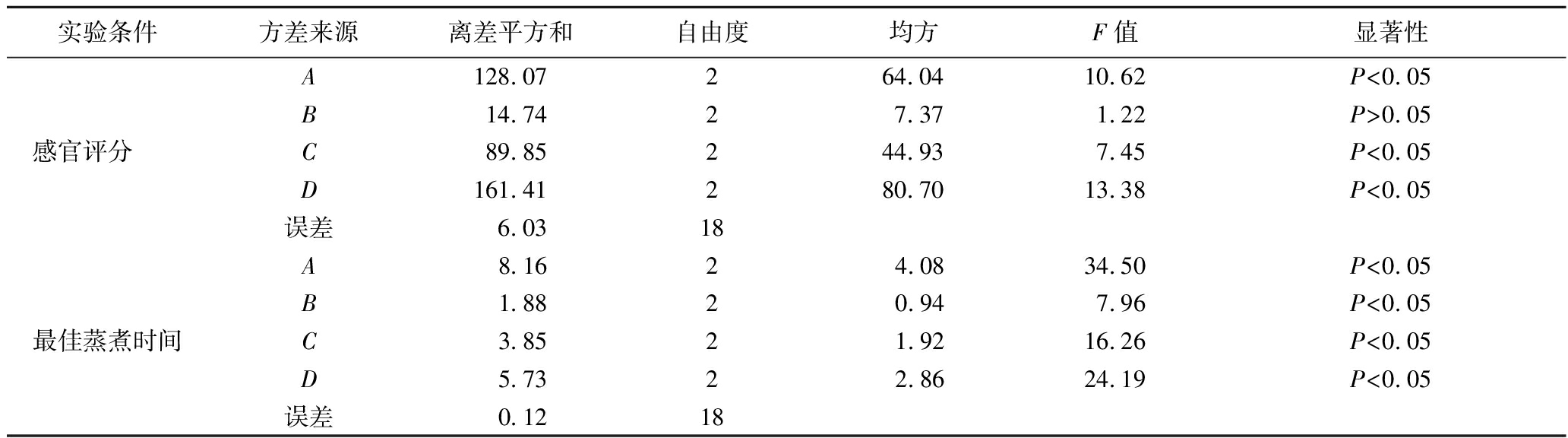
实验条件方差来源离差平方和自由度均方F值显著性感官评分 A128.07 264.04 10.62 P<0.05B14.74 27.37 1.22 P>0.05C89.85 244.93 7.45 P<0.05D161.41 280.70 13.38 P<0.05误差6.03 18最佳蒸煮时间A 8.16 2 4.08 34.50 P<0.05B1.88 20.94 7.96 P<0.05C3.85 21.92 16.26 P<0.05D5.73 22.86 24.19 P<0.05误差0.12 18
2.5 乳酸菌半固态发酵对糙米感官及蒸煮时间的影响
由表11可知,发酵前糙米、红米和黑米的感官评分分别为75.25、73.75、72.50,发酵后的感官评分分别为82.67、86.33、91.33,表明综合感官特征明显改善,有显著性差异(P<0.05)。一方面,发酵产生了独特的风味,谷物与菌株发酵时挥发性化合物的释放,包括醇类、酸类、酯类、酮类和醛类等使各谷物的气味得到改善[12]。另一方面,菌株在发酵过程中产生的淀粉酶、纤维素酶和蛋白酶等使各谷物皮层软化、剥落和溶解,这些变化不仅削弱了皮层的阻滞,有助于淀粉的糊化[13],而且有利于挥发性化合物的释放。总体而言,发酵显著改善了糙米的食用品质,使糙米饭更容易被大众接受。
表11 发酵前后谷物的感官评价和最佳蒸煮时间
Table 11 Sensory evaluation and optimal cooking time of grains before and after fermentation
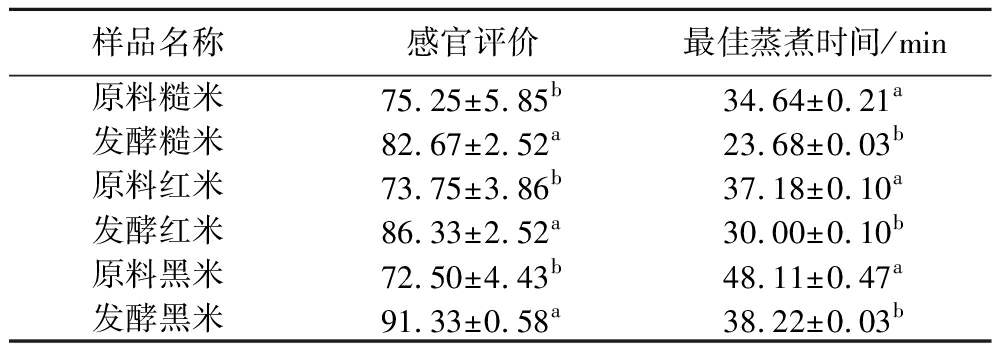
样品名称感官评价最佳蒸煮时间/min原料糙米75.25±5.85b34.64±0.21a发酵糙米82.67±2.52a23.68±0.03b原料红米73.75±3.86b37.18±0.10a发酵红米86.33±2.52a30.00±0.10b原料黑米72.50±4.43b48.11±0.47a发酵黑米91.33±0.58a38.22±0.03b
由表10可知,发酵前后各谷物的蒸煮时间均显著缩短(P<0.05),糙米、红米和黑米由原来的34.64、37.18、48.11 min分别显著缩短至23.68、30.00、38.22 min,几乎缩短19%~32%。发酵能够使糙米皮层结构发生改变,水分扩散效率显著提升,同时淀粉颗粒因吸水作用产生膨胀现象。在蒸煮过程中,这一变化有利于水分向米粒内部的快速渗透,增强了淀粉分子与水分子间的相互作用[14],从而加速了糊化反应的进行,进而缩短蒸煮时间。
2.6 乳酸菌半固态发酵对糙米多酚类物质的影响
多酚和类黄酮是天然抗氧化剂,具有出色的清除自由基的能力,可有效预防氧化应激引起的癌症和心血管疾病[15]。在发酵过程中,不同谷物中游离态和结合态的总酚(total phenolic acid,TPC)、总黄酮(total flavone of camellia,TFC)和花青素(anthocyanidins,TAC)的含量变化如图4所示。随着发酵时间的延长,糙米、红米和黑米中总酚和总黄酮含量均呈现显著上升趋势(P<0.05)。与此同时,花青素含量(糙米忽略不计)则显著下降(P<0.05)。可能是由于花青素等可溶性多酚在发酵前因水溶性损失而减少;另一个可能的解释是花青素的结构不稳定,乳酸菌产生的酶可将花青素降解为小分子化合物[16]。
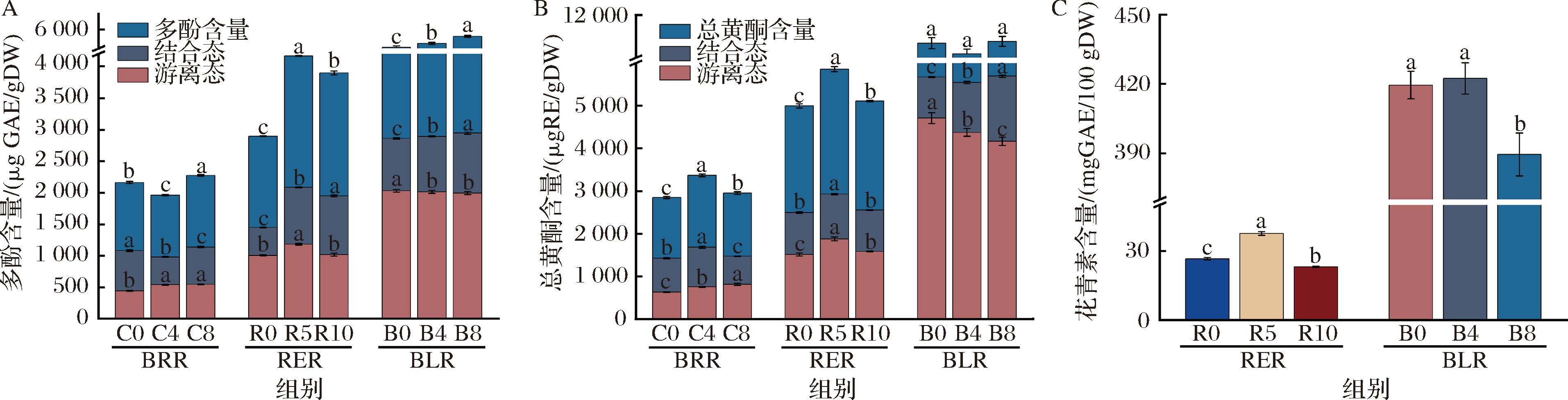
A-总酚含量(TPC);B-总黄酮含量(TFC);C-花青素含量(TAC)
图4 半固态发酵对谷物总酚、总黄酮和花青素的影响
Fig.4 Effect of semi-solid fermentation on total phenols,total flavonoids and anthocyanins of grains
注:C0、R0、B0:发酵前;C4、R5、B4:发酵过程中;C8、R10、B8:发酵后。
发酵后糙米的总酚含量由1 079.97 μg GAE/g DW上升到1 137.05 μg GAE/g DW,红米的总酚含量由1 446.33 μg GAE/g DW上升到1 948.28 μg GAE/g DW,黑米的总酚由2 859.17 μg GAE/g DW上升到2 946.58 μg GAE/g DW。糙米游离酚含量持续增加,结合酚含量逐渐下降,黑米则与之相反,红米游离酚含量先上升后下降,结合酚含量逐渐增加。研究表明,在谷物发酵过程中,游离酚和结合酚的含量变化主要受微生物发酵过程中产生多种酶的影响[17]。谷物中的多酚类物质,除了以游离形式存在于细胞液泡中的可溶性多酚外,还有一部分以不溶形式与细胞壁结构、半纤维素、纤维素以及蛋白质等成分结合[17]。微生物在生长繁殖过程中会产生的多种酶,如果胶酶、纤维素酶和蛋白酶,这些酶能够水解共价键,从而释放结合酚。此外,微生物在发酵过程中产生的α-淀粉酶还能催化淀粉分解为葡萄糖,作为微生物自身生长的碳源,进而最大限度地释放多酚[18]。
发酵后糙米游离黄酮含量持续增加,结合黄酮含量逐渐下降,黑米则与之相反,糙米和红米总黄酮含量先上升后下降,黑米变化不显著。黄酮类物质含量变化可能受多重因素影响:a)发酵过程中产生的酸性环境可能导致黄酮类化合物发生分解;b)热风干燥过程中的高温条件易使热敏性游离黄酮发生降解。这些过程可能破坏与黄酮结合的大分子物质结构,促使结合型黄酮向游离态转化。游离态黄酮在后续加工环节中可能存在不稳定性,导致其含量出现不同程度的损失[19]。c)在谷物发酵过程中,游离黄酮可以通过微生物的代谢作用转化为结合黄酮。总体来说,游离黄酮在短期内可能更有益,因为它们可以更快地被吸收和利用。然而,结合黄酮在某些情况下也可能提供更持久的效果,尤其是在肠道微生物的帮助下。这些酚类化合物不仅赋予糙米独特的风味和颜色,还对健康有潜在益处,包括降低慢性疾病的风险。
2.7 乳酸菌半固态发酵对糙米抗氧化性的影响
通过DPPH自由基清除能力测定、ABTS阳离子自由基清除能力测定和FRAP铁离子还原能力测定3种方法,系统考察了谷物在半固态发酵前、中、后3个时期的抗氧化特性。如图5所示,结果表明糙米和黑米的DPPH自由基清除能力分别由89.66%、67.08% 上升到95.57%、81.66%,红米则没有显著性差异。
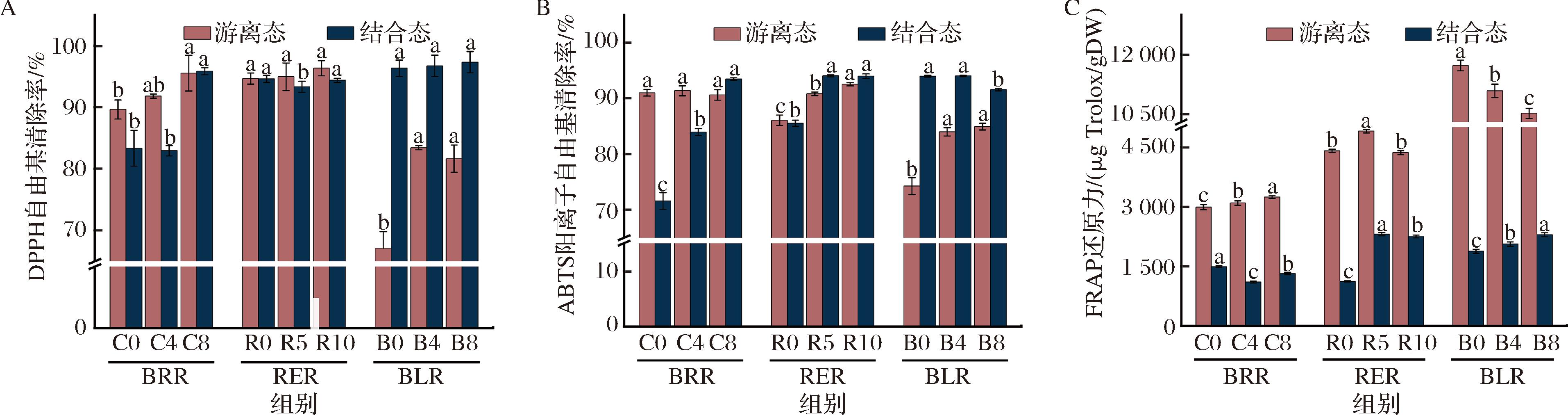
A-DPPH自由基清除能力;B-ABTS阳离子自由基清除能力;C-FRAP铁离子还原能力
图5 半固态发酵对谷物抗氧化特性的影响
Fig.5 Effect of semi-solid fermentation on the antioxidant properties of grains
注:C0、R0、B0:发酵前;C4、R5、B4:发酵过程中;C8、R10、B8:发酵后。
与JUNG等[20]报告的结果相反,大多数发酵米糠的DPPH自由基清除活性在发酵后呈现下降趋势。这一现象可能与糙米中的多酚类等生物活性物质的含量变化有关,已有研究表明,谷物中多酚类物质的含量与其体外抗氧化能力呈显著正相关[21]。本研究中糙米DPPH自由基清除能力的提升可能与其发酵过程中多酚类物质的含量变化有关。
糙米、红米和黑米的ABTS阳离子自由基清除能力分别由71.61%、85.56%和74.28%上升到93.53%、94.04%和84.96%。造成这种变化的可能原因是发酵过程中释放了更多的酚类化合物。某些酚类化合物具有较大的电子脱定位,能够吸引和结合更多的自由基,从而增强清除自由基的能力[22]。
糙米、红米和黑米的FRAP铁离子还原能力分别由2 992.32、1 120.74、1 881.02 μg Trolox/g DW上升到3 245.83、2 2 251.3、2 299.46 μg Trolox/g DW。这种趋势的产生,可能与发酵过程中水解反应生成的多种抗氧化分子(包括肽、氨基酸及可溶性多糖等),以及微生物代谢过程中新合成的生物活性物质共同作用有关[23],这些物质的协同效应不仅提升了体系的抗氧化性能,同时也反映了多酚类物质与其他生物活性成分之间的相互作用机制。
3 结论
在这项研究中,基于单因素试验结果,通过正交试验优化得到3种谷物对应的最佳发酵菌株和最佳发酵条件。在此工艺参数下,经发酵处理后,3个品种糙米的感官品质显著提升,感官评分较未发酵样品提高14%~26%。在蒸煮过程中,水分能更快地渗透至米粒内部,蒸煮时间被大大缩短了,显著提升了糙米的蒸煮食用品质。此外,乳酸菌发酵处理显著增加了多酚、类黄酮的含量,其抗氧化活性较未发酵得到有效提升,有色糙米的功能营养质量得到了改善。研究证实,乳酸菌发酵处理不仅改善了有色糙米的食用品质,还显著提升了其功能营养成分含量,使产品更具市场竞争力,因而对消费者更具吸引力。本研究建立的发酵工艺为全谷物食品加工提供了可靠的技术支撑,对开发高附加值糙米产品具有重要指导意义。
[1] MUHIHI A,GIMBI D,NJELEKELA M,et al.Consumption and acceptability of whole grain staples for lowering markers of diabetes risk among overweight and obese Tanzanian adults[J].Globalization and Health,2013,9(1):26.
[2] MAITI S,BANIK A.Strategies to fortify the nutritional values of polished rice by implanting selective traits from brown rice:A nutrigenomics-based approach[J].Food Research International,2023,173:113271.
[3] ZHAO G H,ZHANG R F,DONG L H,et al.The effects of different enzymes on the liberation of bound phenolics from rice bran dietary fibre and their antioxidant activities[J].Food Bioscience,2023,56:103449.
[4] YU Y,PAN F,RAMASWAMY H S,et al.Effect of soaking and single/two cycle high pressure treatment on water absorption,color,morphology and cooked texture of brown rice[J].Journal of Food Science and Technology,2017,54(6):1655-1664.
[5] PRAVEEN M,BROGI S.Microbial fermentation in food and beverage industries:Innovations,challenges,and opportunities[J].Foods,2025,14(1):114.
[6] 朱春霞,孙万成,罗毅皓.青稞酒酿造副产物及自然发酵驼乳乳酸菌分离鉴定及多样性分析[J].食品与发酵工业,2025,51(7):115-121.ZHU C X,SUN W C,LUO Y H.Isolation,identification,and diversity analysis of lactic acid bacteria in highland barley wine brewing by-products and naturally fermented camel milk[J].Food and Fermentation Industries,2025,51(7):115-121.
[7] 吴艺婕.不同蒸煮条件对黑米饭品质及低GI特性的影响[D].武汉:华中农业大学,2022.WU Y J.Effects of different cooking conditions on the quality and low GI characteristics of black rice[D].Wuhan:Huazhong Agricultural University,2022.
[8] MOHAPATRA D,BAL S.Cooking quality and instrumental textural attributes of cooked rice for different milling fractions[J].Journal of Food Engineering,2006,73(3):253-259.
[9] ZENG Z C,LUO S J,LIU C M,et al.Phenolic retention of brown rice after extrusion with mesophilic α-amylase[J].Food Bioscience,2018,21:8-13.
[10] ZHU L,YU C T,YIN X T,et al.Effects of soaking on the volatile compounds,textural property,phytochemical contents,and antioxidant capacity of brown rice[J].Foods,2022,11(22):3699.
[11] YANG Y T,LIU Y T,DUAN Z P,et al.Differences in the chemical composition and physicochemical properties between brown rice kernels and brown rice flours after Lactobacillus fermentation and their impact on the qualities of brown rice noodles[J].LWT,2025,215:117219.
[12] ZHANG D Q,TAN B.Effects of different solid-state fermentation ratios of S.cerevisiae and L.plantarum on physico-chemical properties of wheat bran and the quality of whole wheat bread[J].Journal of the Science of Food and Agriculture,2021,101(11):4551-4560.
[13] 程鑫,李永富,史锋,等.乳酸菌发酵对糙米蒸煮性能和食用品质的影响[J].中国粮油学报,2018,33(5):1-7.CHENG X,LI Y F,SHI F,et al.Effect of lactic acid bacteria fermentation on cooking performance and edible quality of brown rice[J].Journal of the Chinese Cereals and Oils Association,2018,33(5):1-7.
[14] ZHANG D Q,YE Y J,TAN B.Comparative study of solid-state fermentation with different microbial strains on the bioactive compounds and microstructure of brown rice[J].Food Chemistry,2022,397:133735.
[15] PORRO C,BENAMEUR T,CIANCIULLI A,et al.Functional and therapeutic potential of Cynara scolymus in health benefits[J].Nutrients,2024,16(6):872.
[16] HUANG Y X,ZHOU S Y,ZHAO G H,et al.Destabilisation and stabilisation of anthocyanins in purple-fleshed sweet potatoes:A review[J].Trends in Food Science &Technology,2021,116:1141-1154.
[17] CHEN G,LIU Y,ZENG J R,et al.Enhancing three phenolic fractions of oats (Avena sativa L.) and their antioxidant activities by solid-state fermentation with Monascus anka and Bacillus subtilis[J].Journal of Cereal Science,2020,93:102940.
[18] ROASA J,DE VILLA R,MINE Y,et al.Phenolics of cereal,pulse and oilseed processing by-products and potential effects of solid-state fermentation on their bioaccessibility,bioavailability and health benefits:A review[J].Trends in Food Science &Technology,2021,116:954-974.
[19] YI C P,XIE L,CAO Z F,et al.Effects of rice bran fermented with Lactobacillus plantarum on palatability,volatile profiles,and antioxidant activity of brown rice noodles[J].International Journal of Food Science and Technology,2022,57(8):5048-5056.
[20] JUNG T D,SHIN G H,KIM J M,et al.Comparative analysis of γ-oryzanol,β-glucan,total phenolic content and antioxidant activity in fermented rice bran of different varieties[J].Nutrients,2017,9(6):571.
[21] LI R,LI Z J,WU N N,et al.The effect of cold plasma pretreatment on GABA,γ-oryzanol,phytic acid,phenolics,and antioxidant capacity in brown rice during germination[J].Cereal Chemistry,2023,100(2):321-332.
[22] LEI Q,WANG J Y,LI Q L,et al.Effects of Latilactobacillus delbrueckii fermentation on the bioconversion and antioxidant capacity of phenolic compounds in quinoa sprouts[J].Food Bioscience,2024,59:104190.
[23] SPAGGIARI M,RICCI A,GALANI L,et al.Solid state lactic acid fermentation:A strategy to improve wheat bran functionality[J].LWT,2020,118:108668.