氨基葡萄糖(glucosamine,GlcN)是一种天然存在的氨基糖类,广泛存在于动物和植物的细胞壁中,尤其是关节软骨、皮肤和结缔组织中。作为一种重要的生物分子,氨基葡萄糖不仅参与细胞外基质的合成,还在调节关节健康、促进软骨修复以及缓解关节炎症等方面发挥着重要作用[1-2]。随着对关节疾病治疗需求的增加,GlcN及其衍生物(如氨基葡萄糖硫酸盐和氨基葡萄糖盐酸盐)逐渐成为临床研究的重点方向[3-4]。此外,GlcN还具有多种生物活性特性:即抗癌[5-6]、抗氧化[7-8]、抑菌[9]、抗病毒[10]功能,并被广泛应用于医药、饲料、保健食品[11]、化妆品等领域。
目前,氨基葡萄糖的主要生产途径包括壳聚糖提取技术、微生物发酵合成技术和生物催化技术。壳聚糖提取法通常依赖于甲壳类动物外骨骼,经过脱乙酰化处理获得氨基葡萄糖,但高温的反应条件和浓酸的使用,造成了能源浪费和环境污染等问题[12];微生物发酵法则通过特定微生物菌种的代谢作用合成氨基葡萄糖[13],尽管微生物发酵法具备较高的生态效益和生产可控性,但产物合成后分离工作冗杂[14-15];而生物催化法是通过生物酶将壳聚糖或N-乙酰氨基葡萄糖(N-acetylglucosamine,GlcNAc)脱乙酰化生成GlcN。基于绿色发展理念,为了突破微生物发酵工艺限制并打通工业化生产,利用温和高效且经济可行的生物酶催化技术来替代传统的酸水解工艺将是一种更理想的方式。
GlcNAc脱乙酰酶来源广泛且功能多样,研究较多的具有催化GlcNAc单体脱乙酰活性的酶有壳二糖脱乙酰酶、N-乙酰氨基葡萄糖-6-磷酸(N-acetylglucosamine-6-phosphate,GlcNAc-6-P)脱乙酰酶、肽聚糖脱乙酰酶和几丁质脱乙酰酶。然而,大部分已报道的脱乙酰酶具有专一性较低、表达量不高以及活性不足等问题[16]。近年来具有生产应用潜力的GlcNAc脱乙酰酶报道很少。LYU等[17]首次报道了一种来源于海洋环杆菌(Cyclobacterium marinum)的GlcNAc脱乙酰酶CmCBDA,马佳菲等[18]从卡西姆氏环杆菌(Cyclobacterium qasimii)中克隆得到了GlcNAc脱乙酰酶CqCBDA,这2种脱乙酰酶的酶学性质优越,具有应用于GlcN生产的潜力。QIU等[19]从大肠杆菌(Escherichia coli)中筛选出4种GlcNAc脱乙酰酶,但存在表达效率不高、催化效率低或反应温度过高的问题。目前,尚未发现鲍曼不动杆菌(Acinetobacter baumannii)中编码GlcNAc脱乙酰酶基因的报道。
本研究利用基因工程技术,获得了来源于A.baumannii具有脱乙酰活性的基因(AcbaCBDA),完成了对其克隆、表达及纯化,对其进行了酶学特性表征,AcbaCBDA表现出优异的催化性能,旨在为工业生产GlcN提供有应用价值的理论依据。
1 材料与方法
1.1 材料与试剂
A.baumannii菌种和载体pET-30a(+)由本实验室保藏;E.coli BL21(DE3)和E.coli Mach1 T1菌株,天根科技有限公司;PCR引物以及重组质粒pET30a(+)-AcbaCBDA,南京擎科生物科技有限公司;高保真PrimeSTAR HS DNA聚合酶、dNTP Mixture(2.5 mmol/L),南京巨匠生物技术公司;DNA试剂盒,Lembio生物公司;T4 DNA连接酶,Takara公司。
1.2 仪器与设备
Thermo Multiscan FC型酶标仪,赛默飞世尔科技有限公司;超声波细胞破碎仪Soniprep 150,MSE公司;超声破碎仪,杰瑞远仪器有限公司;液相色谱仪,日本岛津公司;聚合酶链反应基因扩增仪,珠海黑马医学仪器有限公司。
1.3 实验方法
1.3.1 重组AcbaCBDA的检索与序列分析
从NCBI数据库中搜寻到A.baumannii基因组中有编码GlcNAc脱乙酰酶的潜在序列,该蛋白属Pig-L家族脱乙酰酶。搜索下载相关9个脱乙酰酶氨基酸序列(Pig-L家族),利用Genedoc软件进行同源性分析,MEGA软件建立系统发育树,方法为Neighbor-Joining,Bootstrap设置为1 000。
1.3.2 重组AcbaCBDA的克隆及表达载体构建
以A.baumannii菌株为模板,设计引物如表1所示(下划线处为对应酶切位点),配制25 μL反应体系:12.5 μL 2 × Rapid Tag Master Mix、0.5 μL菌株模板、0.5 μL前后引物、10 μL H2O。PCR扩增条件如下:95 ℃,3 min;95 ℃变性1 min,55 ℃退火0.5 min,72 ℃延伸1 min,30个循环;72 ℃延伸7 min;4 ℃保温10 min。采用10%(质量分数)琼脂糖凝胶电泳分析PCR扩增产物,使用DNA回收试剂盒回收目的基因片段。
表1 PCR扩增引物序列
Table 1 Primers for PCR amplification

引物序列(5′-3′)AcbaCBDA-FwCATATGGGAACTTTGAAGCATCAcbaCBDA-RvCTCGAGAAATACACACGAAGAATGAATC
将目的基因片段连接至载体pGEM-T,将重组质粒导入E.coli Mach1 T1感受态细胞,利用蓝白斑筛选原理,以M13通用引物,挑选阳性克隆子进行PCR鉴定;提取克隆成功的重组质粒,使用限制性核酸内切酶Nde Ⅰ和Xho Ⅰ分别酶切重组质粒与pET-30a(+)载体,利用T4连接酶将目的基因片段与载体连接,将连接产物直接转入E.coli Mach1 T1感受态细胞中,挑选阳性克隆子测序。
1.3.3 重组AcbaCBDA的体外表达和纯化
本研究采用E.coli BL21(DE3)感受态作为宿主菌种,将重组质粒pET30a(+)-AcbaCBDA导入菌种细胞;将菌株接种至5 mL卡那霉素质量浓度为50 μg/mL的LB培养基,37 ℃条件下进行过夜培养;将菌体全部转入400 mL LB液体培养基中扩大培养,当菌液密度(以OD600计)达到0.5~0.7时,加入400 μL 异丙基-β-D-硫代半乳糖苷(1 mol/L)溶液,18 ℃条件下诱导反应18 h;诱导结束后,离心(4 000 r/min,20 min),弃去上清液;使用10 mL磷酸缓冲液(500 mmol/L,pH 7.5)复溶菌体沉淀,细胞破碎(200 W,20 min),再次离心(10 000 r/min,20 min,4 ℃),保留上清液,利用亲和层析镍柱对目的蛋白进行纯化。使用SDS-PAGE对蛋白质样品进行分析。
1.3.4 蛋白定量和酶活性检测
1.3.4.1 蛋白定量检测和酶活性检测
向1 mL考马斯亮蓝溶液中加入100 μL适当稀释的酶液(等量等离子水为空白对照)放置3 min;使用酶标仪测定样品吸光度(595 nm),根据标准曲线,计算纯酶液中的蛋白含量[20]。
以GlcNAc溶液(20 mmol/L)为反应底物,检测重组AcbaCBDA的脱乙酰活性。采用薄层层析法,使用V(正丁醇)∶V(乙醇)∶V(水)=5∶3∶2的延展剂分离样品,用DPA(4 g二苯胺、4 g苯胺、5 mL磷酸和50 mL丙酮)显色,初步测定酶是否具有GlcNAc脱乙酰活性。利用高效液相色谱进一步确定酶是否具有活性,HPLC条件:反相C18色谱柱 Hyperclone 5 μmol/L ODS120 Å(4.60 mm ID×250 mm);流动相A为质量分数为1%四氢呋喃(tetrahydrofuran,THF)、0.5%(质量分数)磷酸和0.2%(质量分数)正丁胺的水溶液;流动相B为乙腈;流速为1 mL/min;进样量为10 μL;激发波长为360 nm,发射波长为425 nm。样品被2-氨基苯甲酸(2-aminobenzoic acid,2-AA)标记后,经HPLC检测[21]。
1.3.4.2 酶活力检测
邻苯二甲醛(o-phthalaldehyde,OPA)能与氨基集团结合,反应生成的衍生物在340 nm处具有吸光值[21],采用此方法用于酶活性分析。取96孔板,取10 μL不同浓度的GlcN(0、50、100、200、500 μmol/L、1、2、5 mmol/L)标准品,加入100 μL OPA试剂,每个浓度设置4个平行,测得数据并制作标准曲线见图1。当底物浓度为0~5 mmol/L时,标准曲线呈现线性状态,说明该方法可应用于脱乙酰酶的活性测定。
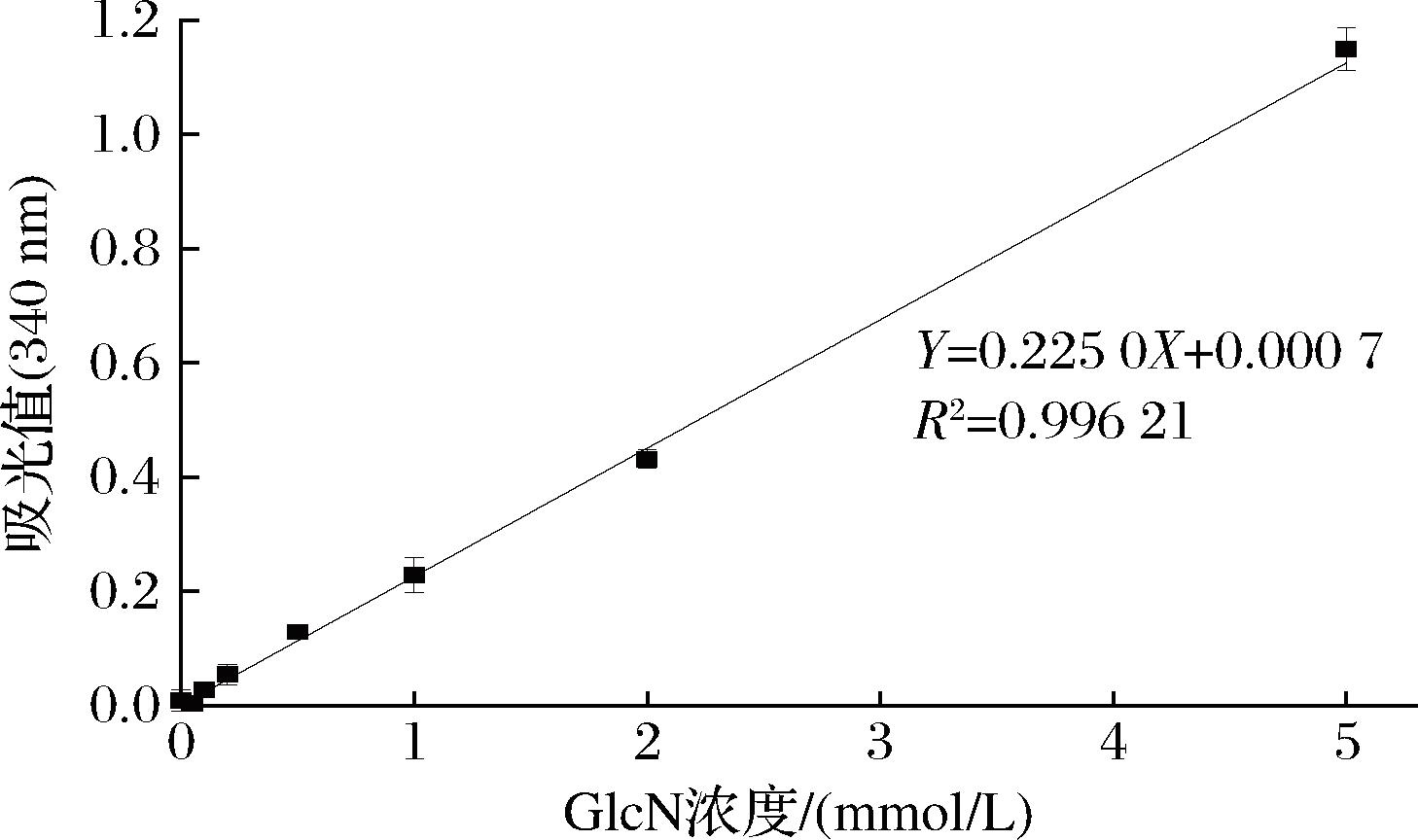
图1 标准曲线
Fig.1 Standard curve
重组AcbaCBDA与GlcNAc反应体系如表2所示,在37 ℃下分别孵育不同时间:0、15、30 min、1、2、4、8 h,反应结束加入25 μL氯仿,剧烈振荡终止反应,离心,取上清液,酶标仪测定吸光值。每个反应设置4个平行,计算酶活性。酶活性单位(U)定义:每分钟生成1 μmol/Lol GlcN所需的脱乙酰酶量为1个酶活性单位。
表2 反应体系
Table 2 Reaction system

试剂体积/μLPB buffer (500 mmol/L pH 7.5)10GlcNAc (500 mmol/L)5AcbaCBDA (6 mg/mL)10
1.3.5 重组AcbaCBDA的酶学特性表征
1.3.5.1 最适温度的测定
在pH 7.5的条件下,重组AcbaCBDA分别于16、25、30、37、42、50、60 ℃的温度下进行反应,反应体系和操作方法按照酶标仪测定酶活性的操作进行,以最高酶活性为100%计算其他温度下的相对酶活性。
1.3.5.2 最适pH的测定
在最适温度条件下,于pH值分别为4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0、9.5、10.0、10.5的缓冲液中测定酶活性。
1.3.5.3 金属离子对重组AcbaCBDA活性影响的测定
在最适温度和pH条件下,向反应体系中分别添加2 mmol/L金属离子(Mg+、Ca2+、Zn2+、Ni+、Mn2+、K+、Cu2+、Li+)和EDTA,以EDTA和不加任何金属离子体系为对照组,测定酶活性,定义不添加任何金属离子组的酶活性为100%,计算不同金属离子影响下的相对酶活性。
1.3.5.4 重组AcbaCBDA的温度稳定性
在4、25、37、42、50 ℃条件下,将重组AcbaCBDA分别孵育0、10、30 min、1、2、6、12、24、72、96 h。在最适温度和pH条件下,测定酶活性,最高酶活性定义为100%,计算不同温度和孵育时间下的相对酶活性。
1.3.5.5 酶动力学常数
在最适条件下,设置不同浓度的GlcNAc(0~400 mmol/L)为底物,进行酶动力学检测,计算酶的Vmax、Km、Kcat和Kcat/Km值。
1.3.6 定点突变
根据同源序列比对结果,利用Quick-change定点突变的方法,分别将AcbaCBDA的Asp54突变为Asn和His160突变为Ser。突变反应体系:10 μL 5×PS buffer、0.5 μL PrimeSTAR DNA Polymerase(5 U/μL)、各1 μL正向/反向引物、0.2 μL质粒模板(135 mg/mL)、4 μL dNTP(2.5 mmol/L)和33 μL无菌水。PCR反应程序为98 ℃预变性50 s,66 ℃退火延伸8 min,循环18次;68 ℃终延伸8 min,16 ℃持续5 min后降温至4 ℃保存。突变引物设计如表3所示。经测序,将突变成功的D54 N和H160S质粒导入BL21(DE3)感受态细胞中表达纯化并测定活性。
表3 引物设计
Table 3 Primer design
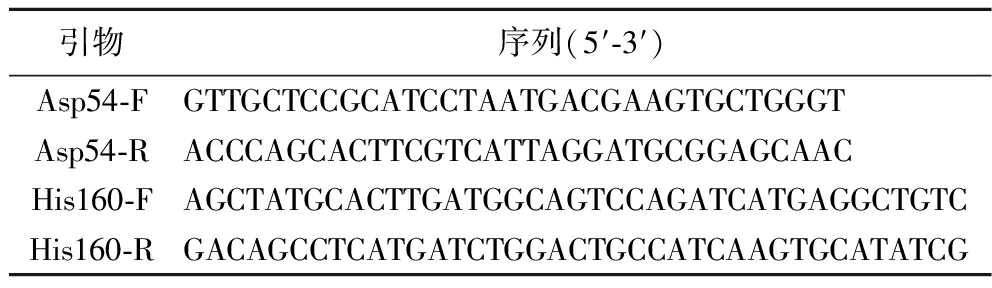
引物序列(5′-3′)Asp54-FGTTGCTCCGCATCCTAATGACGAAGTGCTGGGTAsp54-RACCCAGCACTTCGTCATTAGGATGCGGAGCAACHis160-FAGCTATGCACTTGATGGCAGTCCAGATCATGAGGCTGTCHis160-RGACAGCCTCATGATCTGGACTGCCATCAAGTGCATATCG
1.3.7 重组AcbaCBDA与底物分子GlcNAc的分子对接
使用Alphafold3(https://alphafoldserver.com/)对目标蛋白进行三维结构预测。从PubChem数据库下载GlcNAc结构文件,使用Auto Dock Vina v1.2.5软件进行半柔性对接,以His52、Asp54、Asp55、His160、His163的空间位置作为活性空腔,设置对接盒子大小为(21.7×20.8×23.2) Å3,中心坐标为(-4.7,-4.4,0.6),对接时将exhaustiveness值设置为32。使用PyMOL软件对结果进行可视化。
1.4 数据统计分析
采用EXCEL 2021和GraphPad Prism 10对数据进行统计分析,以Origin 2021制图。
2 结果与分析
2.1 重组AcbaCBDA的基因克隆、载体构建与序列分析
以Acinetobacter baumannii菌株为模板进行PCR扩增后,采用琼脂糖凝胶电泳对扩增产物进行鉴定和分离,PCR扩增结果如图2所示,得到与目的基因长度(792 bp)基本相符的条带,经过目的基因的富集、双酶切、连接与测序,成功得到带有AcbaCBDA基因的重组质粒。
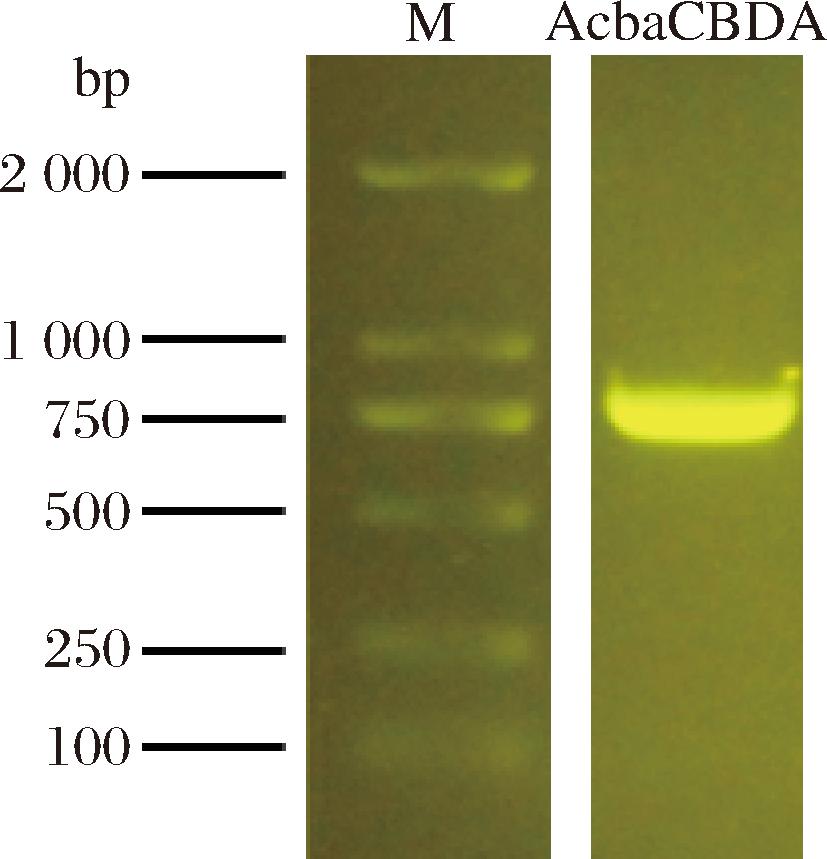
M-DNA Marker标准品。
图2 重组AcbaCBDA的PCR扩增结果
Fig.2 PCR amplification results of recombinant AcbaCBDA
系统发育树结果如图3-a所示,NCBI对AcbaCBDA基因的信息显示AcbaCBDA属于Pig-L家族脱乙酰酶,该家族基因特点为序列相似程度不高但共有关键氨基酸残基位点[22],系统发育树结果也显示AcbaCBDA与其他脱乙酰酶的同源性不高,这可能是因为它们序列相似度较低。同源序列比对结果如图3-b所示,AcbaCBDA基因序列中存在与其他Pig-L家族脱乙酰酶的高保守位点,故确定重组AcbaCBDA为Pig-L家族脱乙酰酶。
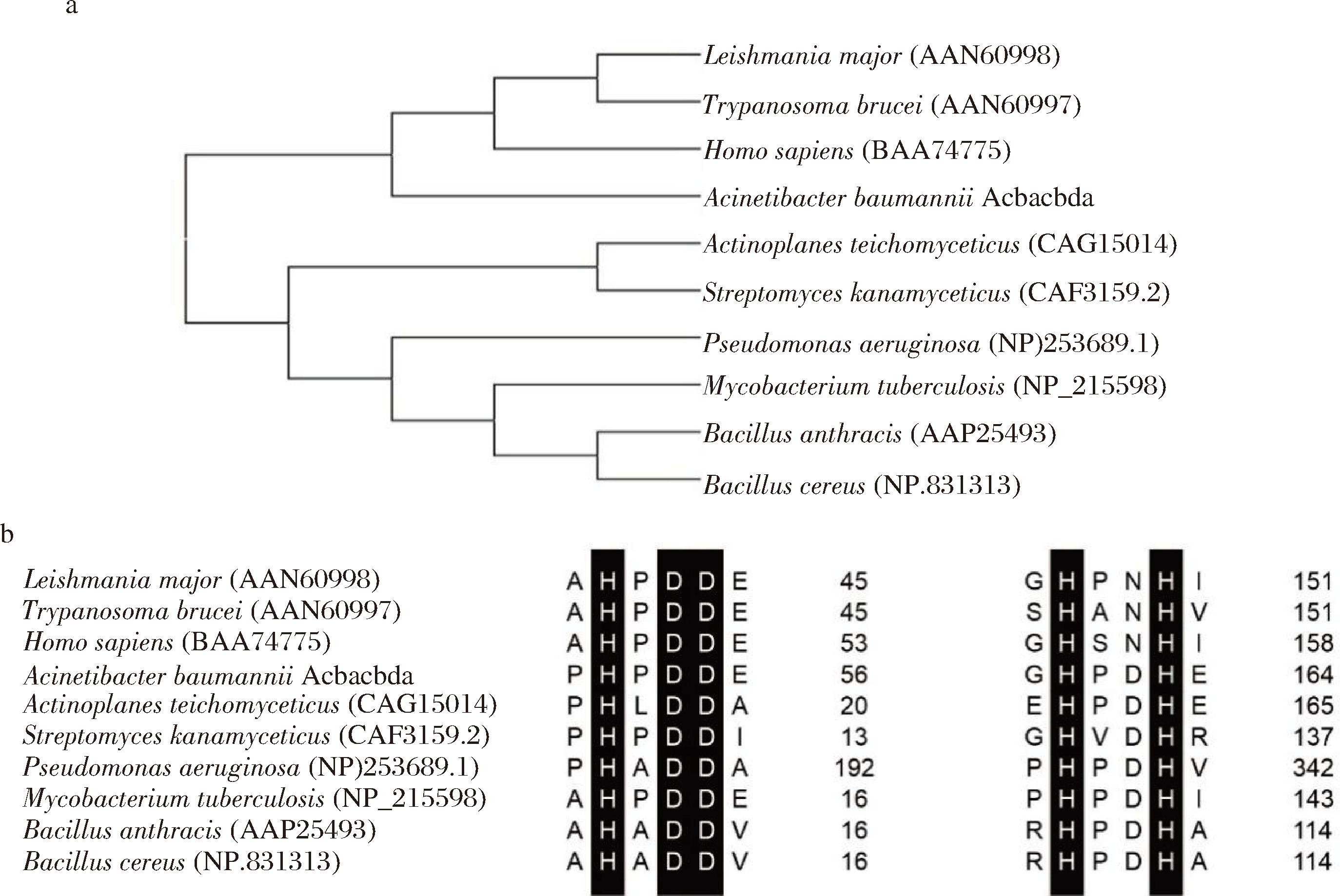
A-进化树分析;B-序列比对
图3 重组AcbaCBDA的同源性分析
Fig.3 Homology analysis of recombinant AcbaCBDA
2.2 重组AcbaCBDA的SDS-PAGE分析
重组质粒pet30a(+)-AcbaCBDA成功被导入到E.coli BL21(DE3)中并成功被诱导表达。实验采用SDS-PAGE的技术对其分子质量及纯化后蛋白纯度进行检测,如图4所示。纯化后的AcbaCBDA蛋白条带单一,表观分子质量为29.6 kDa,与理论分子质量相符。
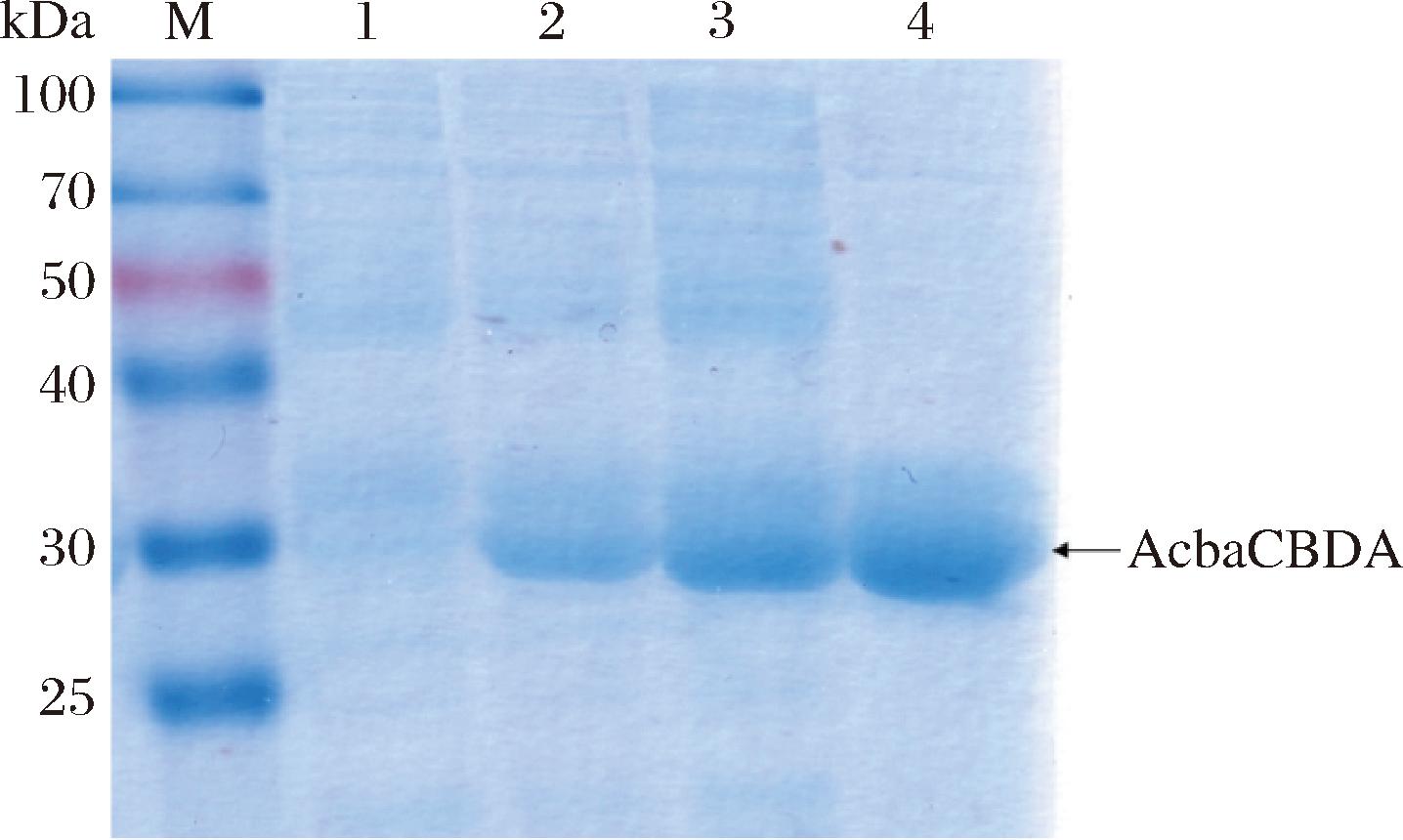
M-蛋白Marker标准品;泳道1-诱导前菌体;泳道2-诱导后菌体;泳道3-细胞破碎后上清液;泳道4-纯化后蛋白。
图4 重组AcbaCBDA的SDS-PAGE分析
Fig.4 SDS-PAGE analysis of recombinant AcbaCBDA
2.3 重组AcbaCBDA的蛋白定量检测和酶活性检测
2.3.1 蛋白定量检测和酶活性检测
经过数据处理得到BSA标准蛋白线性回归方程为y=0.064 5x+0.617 3,R2=0.990 9,经代入计算,纯化后的AcbaCBDA的表达质量浓度为18.7 mg/mL,经换算,每升菌液能表达467.5 mg酶。
薄层色谱法(thin layer chromatography,TLC)检测结果(经DPA染色后)如图5所示。过夜反应后,GlcNAc底物全部被转化成了GlcN,表明重组AcbaCBDA具有N-乙酰氨基葡萄糖脱乙酰酶活性。液相色谱检测结果如图6所示,GlcNAc(出峰时间约为17.5 min)与GlcN(出峰时间为7 min)的出峰时间相距很大,说明此方法可以检测GlcNAc和GlcN的含量变化,实验组色谱图显示底物GlcNAc基本被AcbaCBDA转化成GlcN,进一步证实重组AcbaCBDA具有GlcNAc脱乙酰活性。
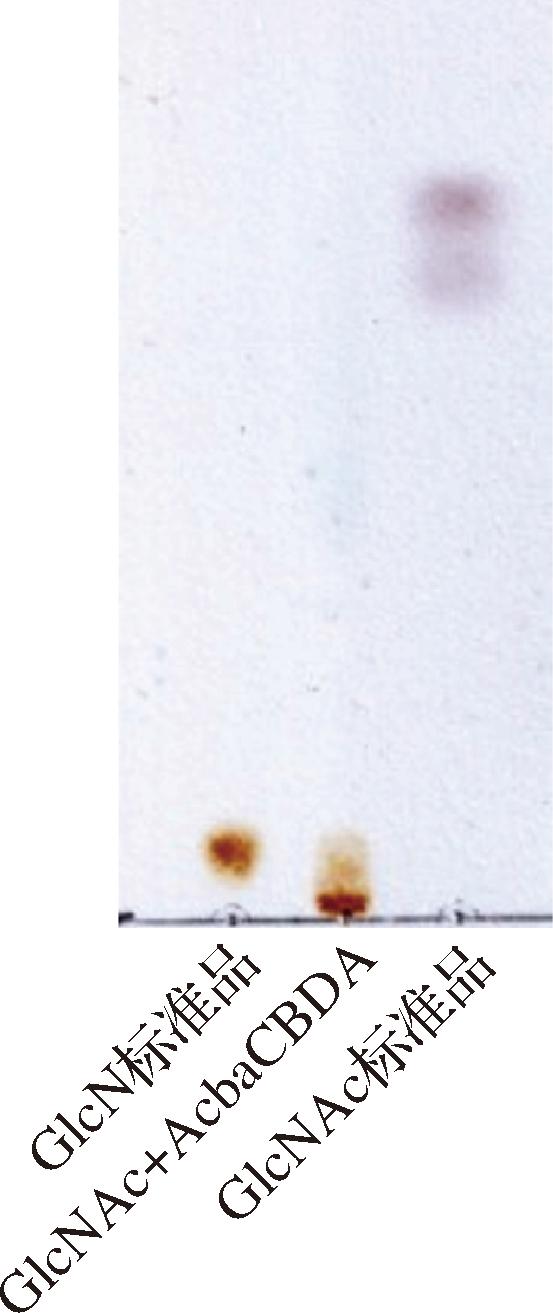
图5 TLC检测重组AcbaCBDA活性
Fig.5 TLC detection of recombinant AcbaCBDA activity
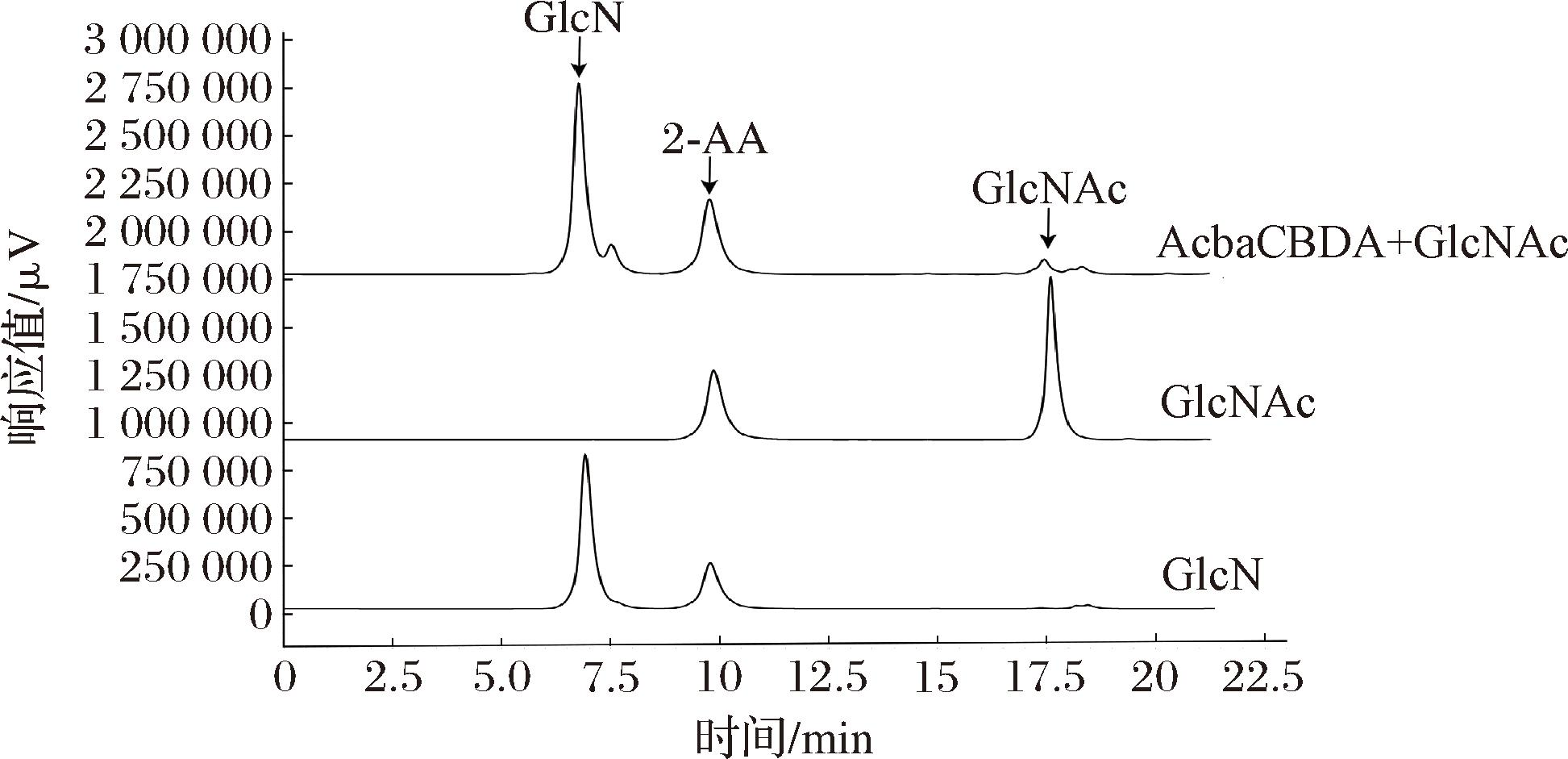
图6 HPLC检测重组AcbaCBDA活性
Fig.6 HPLC detection of recombinant AcbaCBDA activity
2.3.2 酶活性检测
重组AcbaCBDA与GlcNAc(终浓度为100 mmol/L)反应生成的GlcN含量随时间变化如图7所示,反应前2 h 反应速度最快,之后反应速度逐渐减慢,产物量随时间延长逐渐达到最大值,同时反应速率慢慢趋于零。经计算,重组AcbaCBDA的比酶活力为17.82 U/mg。
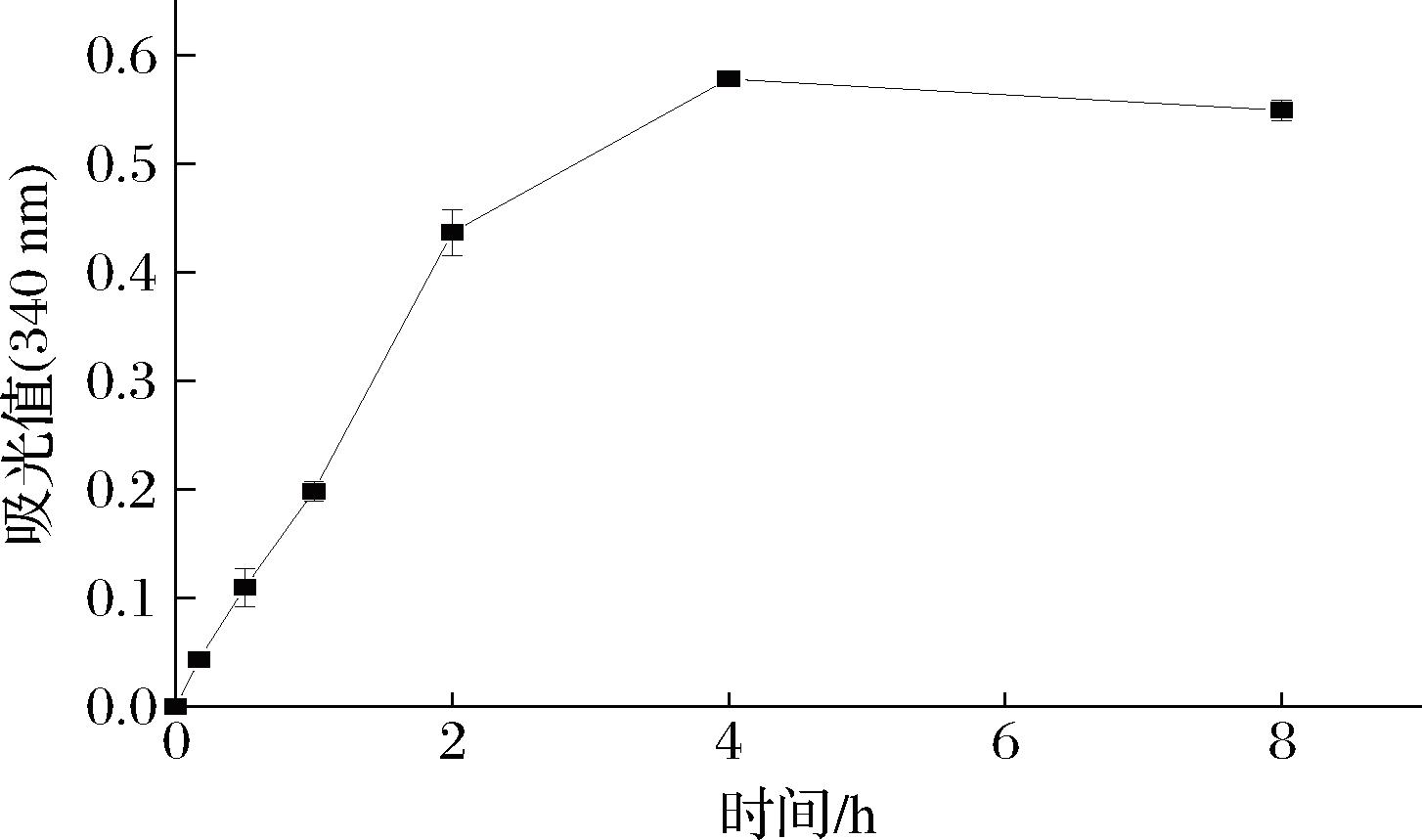
图7 酶活性检测
Fig.7 Enzyme activity detection
2.4 酶学性质分析
2.4.1 温度对重组AcbaCBDA酶活性的影响
图8-a是重组AcbaCBDA的最适温度检测结果,重组AcbaCBDA的最适温度为25 ℃,在16~37 ℃下保持70%以上的酶活性。温度达到25 ℃后,随着温度的上升酶的活性大幅度下降,达50 ℃时,酶完全失活。在工业生产时,高温会使GlcN褐变[23],已报道的、可应用于生产的脱乙酰酶属于高温酶,温度集中在50~100 ℃,其中最适温度多为60~90 ℃[24]。AcbaCBDA能在中低温的条件下催化生产GlcN,有利于减少GlcN褐变损失。
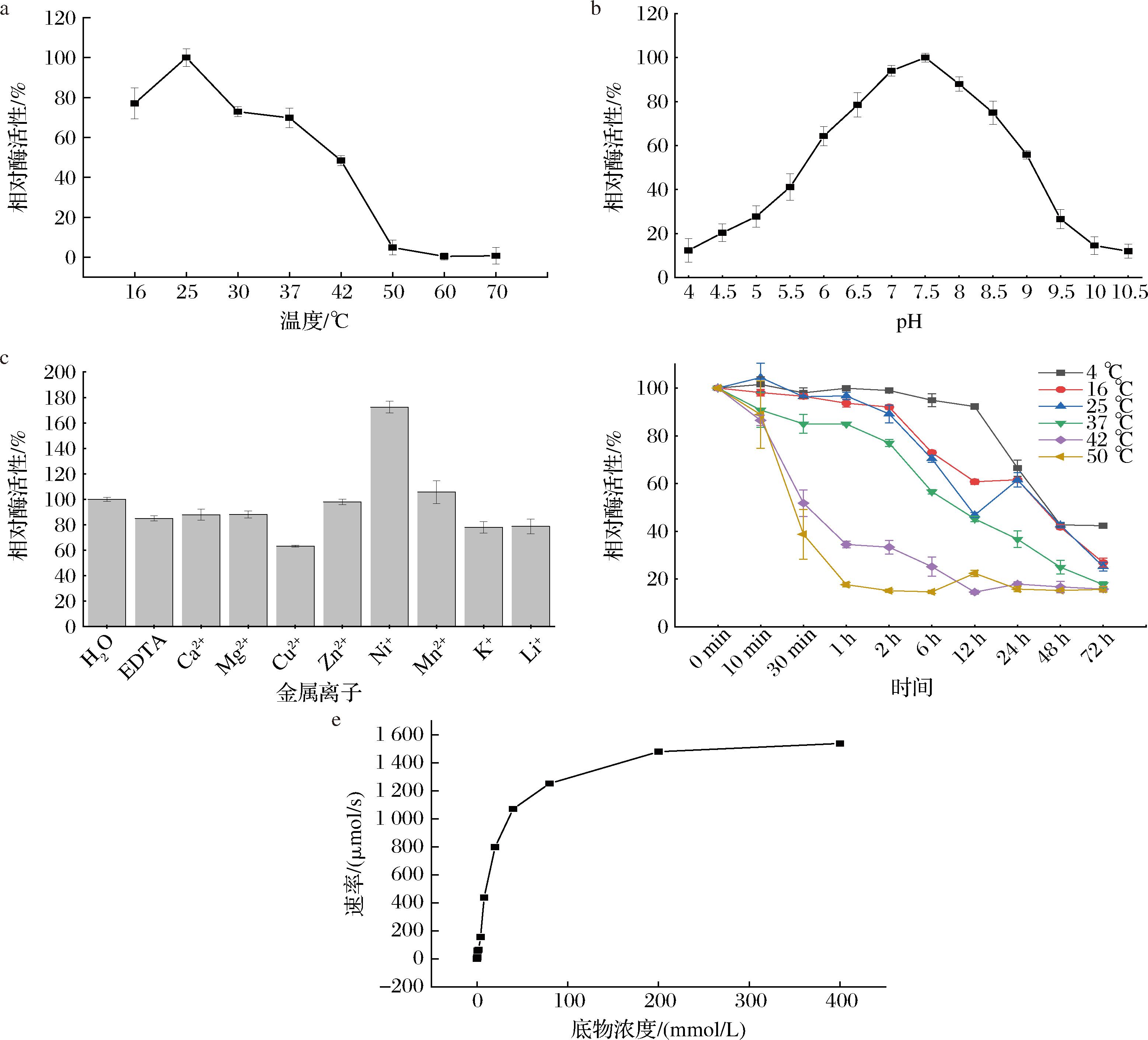
a-最适温度;b-最适pH;c-金属离子依赖性;d-温度稳定性;e-米氏方程曲线
图8 重组AcbaCBDA的酶学特性特定
Fig.8 Determination of enzymatic characterization of recombinant AcbaCBDA
2.4.2 pH对重组AcbaCBDA酶活性的影响
重组AcbaCBDA的最适pH测定结果如图8-b所示,重组AcbaCBDA的最适pH值为7.5,在pH值为6.5~8.5时,酶活性在80%以上,pH<6或者>9时,酶活性在60%以下。GlcN的褐变随着pH值的升高而加剧,且pH值在7.8~9.2,褐变最严重[23]。在偏酸性pH条件下AcbaCBDA仍能保持较高的活性,相比于CmCBDA(最适pH值为9)[21]更有利于减少GlcN褐变的产生。
2.4.3 金属离子对重组AcbaCBDA酶活性的影响
金属离子通常与酶的辅基形成配合物,稳定酶的高级结构、促进底物与酶结合以及降低催化反应的活化能,故研究金属离子对酶活性的影响具有重要意义。不同金属离子对重组AcbaCBDA酶活性的影响结果如图8-c所示。EDTA组酶活性与未添加金属离子组酶活性相差不大,说明AcbaCBDA不是金属离子依赖型酶。Ni+对酶活性有促进作用,使酶活性提高了70%,而Cu2+的引入则对酶活性有抑制作用,为对照的60%。其他金属离子对重组酶活性的影响较小。
2.4.4 重组AcbaCBDA的温度稳定性
将AcbaCBDA在不同温度下孵育不同的时间,测定酶残余酶活性的结果如图8-d所示。结果显示,AcbaCBDA在4 ℃条件下,酶活性能维持12 h不下降;在16 ℃和25 ℃孵育6 h后,活性均降低70%左右;在37 ℃孵育6 h后,活性降低60%左右;在42 ℃和50 ℃下孵育,酶活性随时间急剧下降,42 ℃孵育12 h或50 ℃孵育1 h,酶活性水平便达到最低水平。综上,重组AcbaCBDA不属于耐热酶。
2.4.5 动力学参数测定结果
在最适反应条件下,以GlcNAc溶液(0~400 mmol/L)作为底物,探究重组AcbaCBDA的酶动力学常数,通过GraphPad prism软件计算其动力学常数,动力学拟合曲线见图8-e。AcbaCBDA的Vmax为1.712 μmol/s,Km值为23.2 mmol/L,Kcat和Kcat/Km分别为121.41 s-1和5.23 (s·mmol/L)-1。已报道的GlcNAc脱乙酰酶中只有C.qasimii源的脱乙酰酶的Km值(3.9 mmol/L)低于AcbaCBDA,但其Kcat/Km值只有1.64 (s·mmol/L)-1,说明该酶催化效率低于AcbaCBDA。
其他脱乙酰酶如C.marinum源的脱乙酰酶Km值为48 mmol/L[21],Kcat/Km值为1.3 (s·mmol/L)-1、E.coli源的脱乙酰酶的Km值为194.8 mmol/L[19],Kcat/Km值只有0.73 (s·mmol/L)-1,底物亲和性和催化效率均低于AcbaCBDA。综上,相比绝大多数脱乙酰酶,AcbaCBDA与底物GlcNAc有更高的亲和力和酶催化效率。
2.5 定点突变结果
将突变成功的2个突变体蛋白表达纯化后与GlcNAc反应,得到的结果如图9所示,TLC结果表明,54号位的Asp突变为Asn后,突变酶完全失活,而160号位的His突变为Ser后,突变酶只有微弱活性。Asp54决定了酶是否有活性,而His160对酶活性的影响较小。因重组蛋白经亲和层析镍柱纯化,纯化蛋白液中可能有镍离子残留,2.4.3节结论得出镍离子能显著提高酶活性,故推测His160其可能是金属离子结合残基,突变后的酶因不能结合金属离子而导致酶活性下降。综上,Asp54与His160是重组酶的关键催化残基。
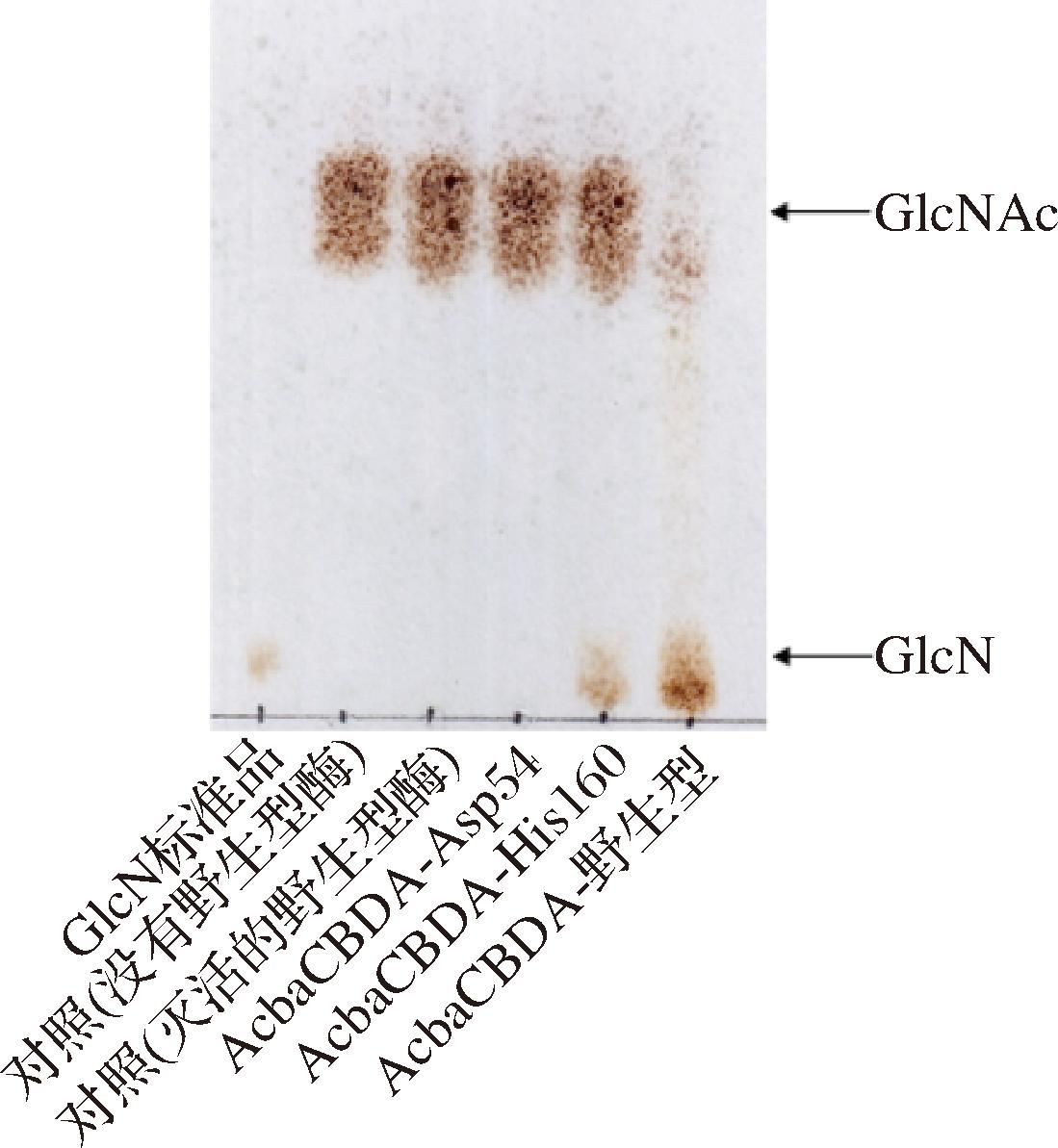
图9 检测AcbaCBDA突变体的活性
Fig.9 Detection of activity of AcbaCBDA mutants
2.6 分子对接结果
如图10-a所示,目标蛋白的三维结构模型整体呈球形,包含3层(α/β/α)三明治特征结构,由7个反向平行的β-折叠和7个α-螺旋组成。Alphafold3给出的预测模板建模(pTM)分数为0.95,说明此蛋白本次预测结构准确性较高。重组AcbaCBDA与底物小分子GlcNAc对接结果如图10-b所示,此构象结合位点的结合能为-6.7 kcal/mol,亲和力最高,故选择此构象进行分析。Gln227、Tyr187、His163、His160、Arg101、Asp55、Asp54、His52与底物形成氢键相互作用,这些氢键将小分子稳定在蛋白中央的活性口袋。该模型GlcNAc分子与蛋白结合的氨基酸残基与Pig-L家族高度保守位点相同,进一步说明对接结果和同源性分析结果的准确性。
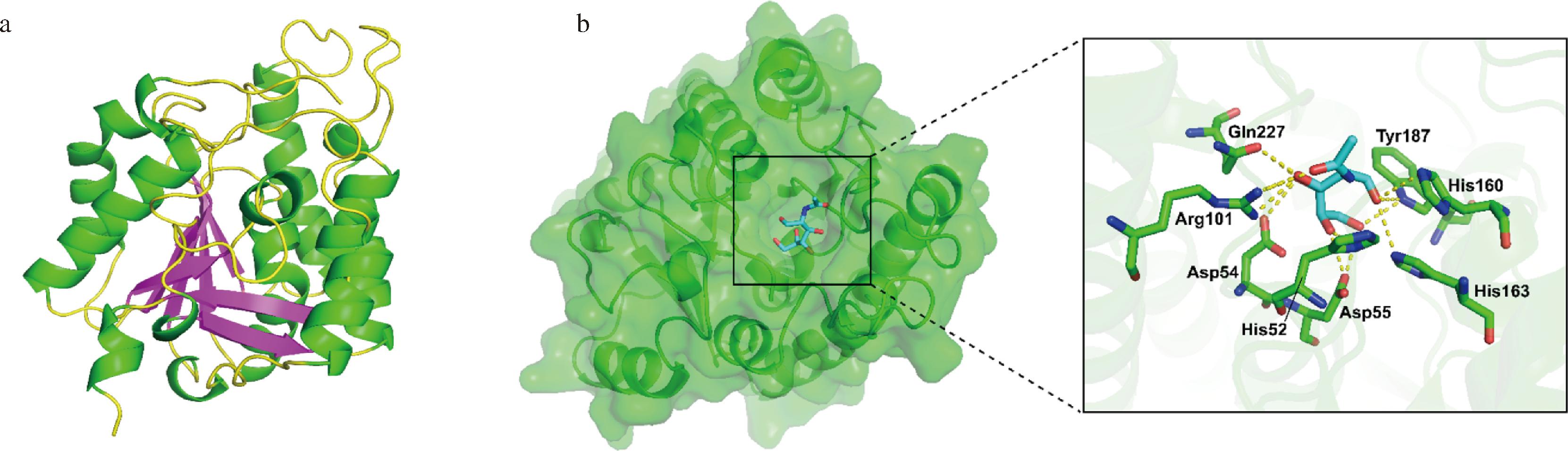
a-蛋白预测模型;b-相互作用
图10 分子对接图
Fig.10 Molecular docking diagram
3 讨论与结论
本研究从细菌A.baumannii中获得了一种编码GlcNAc脱乙酰酶的基因AcbaCBDA。同源性分析及多序列比对结果证实重组AcbaCBDA归属于Pig-L家族。重组AcbaCBDA在反应温度为25 ℃、pH 7.5的条件下具有最佳催化活性,最适温度低于大部分脱乙酰酶(最适温度大都高于37 ℃)[24],在16 ℃环境下仍有80%的相对活性,高温会使GlcN发生褐变,故该酶比其他脱乙酰酶更适用于GlcN工业生产。该酶在4 ℃条件下活性可保持12 h不变,而在中高温环境下其稳定性较差,表明AcbaCBDA不是耐热酶。重组AcbaCBDA不是金属依赖性酶,但Ni+的引入能使酶的催化效率提高0.7倍,而Cu2+的引入能使其降低40%。AcbaCBDA对GlcNAc的Km值为23.2 mmol/L,低于大多数脱乙酰酶[21],说明该酶对底物GlcNAc的亲和力高。定点突变分析发现,Asp54和His160是调控AcbaCBDA活性的关键氨基酸位点。分子对接结果显示,底物GlcNAc分子与蛋白上多种氨基酸残基以氢键结合,被紧紧包围与处于蛋白中央的活性口袋,这有利于重组AcbaCBDA对底物的高度选择。综上所述,重组AcbaCBDA酶学性质优异,相比于其他GlcNAc脱乙酰酶,反应条件更温和,催化效率更高,重组AcbaCBDA在酶法生产GlcN中具有潜在的价值。后续可通过突变技术寻求温度稳定性更好的突变体以进一步满足生产需要。
[1] IMAGAWA K,DE ANDRÉS M C,HASHIMOTO K,et al.The epigenetic effect of glucosamine and a nuclear factor-kappa B (NF-kB) inhibitor on primary human chondrocytes:Implications for osteoarthritis[J].Biochemical and Biophysical Research Communications,2011,405(3):362-367.
[2] HENROTIN Y,LAMBERT C.Chondroitin and glucosamine in the management of osteoarthritis:An update[J].Current Rheumatology Reports,2013,15(10):361.
[3] 张廷婷.盐酸氨基葡萄糖关节腔注射用温敏凝胶的制备及其对骨关节炎的药效研究[D].雅安:四川农业大学,2019.ZHANG Y T.Preparation of thermosensitive in situ gel of glucosamine hydrochloride for intra-articular injection and its pharmacological effects on osteoarthritis[D].Ya’an:Sichuan Agricultural University,2019.
[4] 徐敏.盐酸氨基葡萄糖治疗膝关节半月板损伤患者的临床效果分析[J].中国实用医药,2025,20(1):21-25. XU M.Analysis of the clinical effect of glucosamine hydrochloride treatment on patients with Meniscus knee injury[J].China Practical Medicine,2025,20(1):21-25.
[5] KANTOR E D,NEWTON C C,GIOVANNUCCI E L,et al.Glucosamine use and risk of colorectal cancer:Results from the Cancer Prevention Study II Nutrition Cohort[J].Cancer Causes &Control,2018,29(3):389-397.
[6] HOSEA R,HARDIANY N S,OHNEDA O,et al.Glucosamine decreases the stemness of human ALDH(+) breast cancer stem cells by inactivating STAT3[J].Oncology Letters,2018,16(4):4737-4744.
[7] XING R E,LIU S,GUO Z Y,et al.The antioxidant activity of glucosamine hydrochloride in vitro[J].Bioorganic &Medicinal Chemistry,2006,14(6):1706-1709.
[8] BASIRI F,RAD A,MAHDIAN D,et al.Effects of glucosamine against morphine-induced antinociceptive tolerance and dependence in mice[J].Journal of Biomedical Science,2019,26(1):21.
[9] JAMIALAHMADI K,SOLTANI F,NABAVI FARD M,et al.Assessment of protective effects of glucosamine and N-acetyl glucosamine against DNA damage induced by hydrogen peroxide in human lymphocytes[J].Drug and Chemical Toxicology,2014,37(4):427-432.
[10] SONG N,QI Q,CAO R Y,et al.MAVS O-GlcNAcylation is essential for host antiviral immunity against lethal RNA viruses[J].Cell Reports,2019,28(9):2386-2396.e5.
[11] 迟海林,李菲菲,张李伟,等.氨基葡萄糖类物质在保健食品中的应用及研究进展[J].食品工业科技,2023,44(8):437-445.CHI H L,LI F F,ZHANG L W,et al.Application and research progress of glucosamine in health food[J].Science and Technology of Food Industry,2023,44(8):437-445.
[12] 张阿磊,魏国光,张弛,等.几丁质资源生物降解和高值转化的研究进展[J].合成生物学,2024,5(6):1279-1299.ZHANG A L,WEI G G,ZHANG C,et al.Research progress on bio-degradation and valuable bio-conversion of chitinous resources[J].Synthetic Biology Journal,2024,5(6):1279-1299.
[13] YANG Y X,WANG J H,YAO M D,et al.An update on the review of microbial synthesis of glucosamine and N-acetylglucosamine[J].World Journal of Microbiology and Biotechnology,2023,39(4):93.
[14] CHEN X,LIU L,LI J H,et al.Improved glucosamine and N-acetylglucosamine production by an engineered Escherichia coli via step-wise regulation of dissolved oxygen level[J].Bioresource Technology,2012,110:534-538.
[15] LIU Y F,LIU L,SHIN H D,et al.Pathway engineering of Bacillus subtilis for microbial production of N-acetylglucosamine[J].Metabolic Engineering,2013,19:107-115.
[16] NAQVI S,CORD-LANDWEHR S,SINGH R,et al.A recombinant fungal chitin deacetylase produces fully defined chitosan oligomers with novel patterns of acetylation[J].Applied and Environmental Microbiology,2016,82(22):6645-6655.
[17] LYU Y M,LABORDA P,HUANG K,et al.Highly efficient and selective biocatalytic production of glucosamine from chitin[J].Green Chemistry,2017,19(2):527-535.
[18] 马佳菲,秦臻,范立强,等.Cyclobacterium qasimii脱乙酰酶的异源表达及酶学性质[J].食品科学技术学报,2020,38(6):39-46;54.MA J F,QIN Z,FAN L Q,et al.Heterologous expression and enzymatic properties of N-acetylglucosamine deacetylase from Cyclobacterium qasimii[J].Journal of Food Science and Technology,2020,38(6):39-46;54.
[19] QIU M,DAI X H,HU J L,et al.Gene mining,recombinant expression and enzymatic characterization of N-acetylglucosamine deacetylase[J].Turkish Journal of Biochemistry,2025,50(1):116-125.
[20] BRADFORD M M.A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J].Analytical Biochemistry,1976,72(1-2):248-254.
[21] 吕永梅.N-乙酰氨基葡萄糖单体特异性脱乙酰酶CmCBDA的挖掘及其在氨基葡萄糖和唾液酸糖苷物质全酶法合成中的作用[D].南京:南京农业大学,2020.LYU Y M.Discovery of N-acetylglucosamine (GlcNAc) monomer specific deacetylase CmCBDA and its function in the biocatalytic synthesis of glucosamine and sialosides[D].Nanjing:Nanjing Agricultural University,2020.
[22] LIEBENS V,DEFRAINE V,VAN DER LEYDEN A,et al.A putative de-N-acetylase of the PIG-L superfamily affects fluoroquinolone tolerance in Pseudomonas aeruginosa[J].Pathogens and Disease,2014,71(1):39-54.
[23] 步芬,李博,徐光富,等.壳寡糖/氨基葡萄糖非酶褐变研究进展[J].食品工业,2013,34(5):181-185.BU F,LI B,XU G F et al.The research on progress of nonenzymic browning of chitooligomers and glucosamine[J].The Food Industry,2013,34(5):181-185.
[24] JIANG Z,LV X Q,LIU Y F,et al.Biocatalytic production of glucosamine from N-acetylglucosamine by diacetylchitobiose deacetylase[J].Journal of Microbiology and Biotechnology,2018,28(11):1850-1858.