桑树(Morus alba L.)属于桑科桑属,其果实称桑葚,又名桑椹、桑枣,是中国传统的可食用水果,桑葚酸甜适宜、开胃可口,含有丰富的营养物质和白藜芦醇、花青素等多种天然药理活性成分,具有调节免疫、抗氧化、调节血糖血脂水平等保健功能[1]。近年来,随着消费者对天然功能性食品需求的增加,桑葚的种植规模和产业链持续扩展,但其贮运困难、成熟期短暂且集中成熟于易受病虫害侵袭的雨季等缺点,限制了桑葚产业的发展[2]。桑树品种‘46C019’为台湾地区选育的桑果品种,平均单果重4.6 g,果长3 cm,横径2 cm。因其果量大、果实硬和一年多次结果的特点[3]。目前‘46C019’已被引种于广东省潮汕地区并广泛种植,当地俗称“潮汕桑”。国家蚕桑产业技术体系-广州综合试验站研发的果桑周年挂果技术,使桑葚能从当年10月至次年5月持续挂果[4],实现了桑葚反季节供应,如今‘46C019’与周年挂果技术的结合已经在汕头地区得到较为广泛的应用,当地将3~4月正常上市的桑葚称为“春果”,10~12月反季节上市的桑葚称为“秋果”。有研究发现,反季节栽培的桑葚相较于正常季节栽培的桑葚糖度更高、含水量更低、耐贮性更好,且反季栽培能科学规避春季病虫害多发等问题,有效缓解桑葚在春季集中上市且成熟期短暂的矛盾[5-6]。在‘46C019’春果与秋果的实际生产中也观察到,相同的贮藏条件下,秋果相较于春果更不易发生腐烂自溶,但秋果在常温(25 ℃)环境下的保鲜时间仍不超过2 d。
贮藏温度是影响桑葚贮藏品质的重要因素,适宜的贮藏温度能够抑制桑葚代谢强度,延缓果实衰老软化,延长贮藏期。目前桑葚贮藏时常见的温度条件为4 ℃,销售时常见的货架温度为15 ℃左右。近冰温(near freezing temperature,NFT)贮藏技术是一种非冻结保鲜技术,通过抑制生理代谢活动达到保鲜作用,被称为是继冷藏、气调之后的第三代保鲜技术[7]。李亚玲等[8]研究发现,近冰温贮藏可有效推迟杏果实冷害发生时间并降低冷害发生率;胡凯雪等[9]的研究表明,近冰温贮藏可以降低嘉宝果的质量损失率和腐烂率,延缓嘉宝果乙醇发酵进程和提高抗氧化性。王香君等[10]的研究表明,近冰温贮藏能有效抑制桑葚呼吸强度、失重率和腐烂指数的上升,延缓果实硬度下降,保持桑葚品质。然而,结合前期产业调研和相关研究发现,桑葚秋果的果实品质和贮藏特性都与春果存在差异[5-6],需要开展针对性研究。
目前有关桑葚贮藏技术研究多数集中于正常季节成熟的春季桑葚[11-12],涉及广东地区特色的桑葚秋果贮藏保鲜技术研究未报道。本研究以主产于广东汕头地区‘46C019’桑葚秋果为试验材料,比较-0.5 ℃(近冰温)、4 ℃(低温)和15 ℃(模拟货架)贮藏环境下桑葚秋果的贮藏品质、细胞壁组分及相关代谢酶活性变化,旨在为桑葚秋果的采后贮运保鲜提供新思路。
1 材料与方法
1.1 材料与试剂
供试材料为桑树品种‘46C019’的秋果,于2023年12月1日采摘于广东省汕头市金灶镇。挑选色泽为紫红色、八九分成熟、无明显机械损伤、果肉饱满的完好果实。采用方形多孔塑料盒分装,每盒(120±5.0) g,外罩广东省蚕业与农产品加工研究所自主研发的聚乙烯醇透湿袋,厚度0.012 mm,O2透过率0.079 cm3/(m2·d·0.1 mPa)[13],置于-0.5 ℃(近冰温)、4 ℃(低温)和15 ℃(模拟货架)3种环境下贮藏(温度误差皆在0.5 ℃范围内),分别记录为NFT(近冰温组)、LT(low temperatures,低温组)和SS(simulated shelf,模拟货架组)3组。于当天进行一次取样,记为0 d。NFT组与LT组桑葚秋果均于贮藏后5、15、25、30 d分别取样,SS组桑葚秋果于贮藏后2、4、6 d进行取样。每个处理每次取3盒样品。将部分样品用液氮冷冻存于-80 ℃冰箱内,用于后续品质指标测定。
甲醇、冰醋酸,天津市大茂化学试剂厂;乙醇,天津市富宇精细化工有限公司;硫酸、丙酮,广东广试试剂科技有限公司;无水乙酸钠、三氯乙酸(trichloroacetic acid,TCA),福晨(天津)化学试剂有限公司;硫代巴比妥酸(thiobarbituric acid,TBA)、愈创木酚,上海源叶生物科技有限公司;所有试剂盒均购于苏州科铭生物技术有限公司。
1.2 仪器与设备
SZ61体视显微镜,奥林巴斯公司;Synergy LX型多功能酶标仪,美国伯腾仪器有限公司;JW-1042高速冷冻离心机,安徽嘉文仪器装备有限公司;热电偶线,奥米佳测量技术(上海)有限公司;物性测试仪,北京微讯超技仪器技术有限公司;HH-3A数显恒温水浴锅,国华(常州)仪器制造有限公司;恒温恒湿箱,上海龙跃仪器设备有限公司;DY-200B全温型恒温培养摇床,天津市泰斯特仪器有限公司。
1.3 实验方法
1.3.1 桑葚秋果冰点的测定
挑选10个质量相同、大小均匀的桑葚秋果并编号,将热电偶线的探头刺入到果实中心,再将果实放入-20 ℃的冰箱中,每10 s自动记录一次温度,待果实完全结冰后,将记录仪的数据导入计算机中,取均值。以测定时间为横坐标,桑葚秋果的中心温度作为纵坐标,绘制桑葚秋果冰点曲线,确定其冰点温度。
1.3.2 表观观察、自溶指数和腐烂率
使用体视显微镜观察桑葚秋果的表观变化,并进行拍照记录。
自溶指数参考赵云峰[14]的方法,按照果肉自溶面积大小把果肉自溶程度分为5级:果实饱满有弹性的为0级;果肉轻微软化,自溶面积在1/4以下的为1级;果肉少量出水流汁,自溶面积在1/4~1/2的为2级;果肉出水较严重,发皱软化,自溶面积在1/2~3/4的为3级;果肉出水很严重,自溶面积在3/4以上的为4级。取样时随机挑选50颗桑葚,重复3次。如公式(1)所示:
自溶指数![]()
(1)
式中:L,褐变等级;n,该级果数,个;N,总果数,个。
采用计数法测定果实的腐烂率,取样时随机挑选50颗桑葚,重复3次。腐烂率计算如公式(2)所示:
腐烂率![]()
(2)
1.3.3 硬度、呼吸速率和失重率
使用物性测试仪测定硬度,设定程序为测试深度为5.0 mm,探头直径为5 mm,速度为1 mm/s;每处理随机取30颗果实进行测定,取平均值,单位以N表示。
呼吸速率测定参考曹建康[15]的方法,略有修改。使用便携式二氧化碳检测仪测量,从每个处理组中随机抽取50 g左右果实放入气密的玻璃罐(3.2 L)中,同时将便携式CO2检测仪也置入玻璃罐,密封后计时6 min,记录初始CO2浓度(0 min)及之后每分钟的CO2浓度(共7次)。计算相邻2次读数的差值,得到6个数值。清除罐内气体后再次重复测量:2次,共获得18个数据点。呼吸速率以每千克果蔬(鲜重)每秒释放的CO2质量表示,单位为mg/(kg·s)。
采用称量法测定果实的失重率,取样时随机选取3盒桑葚秋果称质量,取平均值。计算如公式(3)所示:
失重率![]()
(3)
式中:m0,该盒桑葚秋果的初始质量,g;m1,取样时桑葚秋果的质量,g。
1.3.4 丙二醛(malondialdehyde,MDA)
参考曹建康[15]的方法,略有修改。称取0.5 g使用液氮冷冻并打成粉末的桑葚果肉样品,加入5 mL 100 g/L TCA溶液,混合均匀,离心机4 ℃、10 000×g离心20 min,收集上清液备用。取1 mL上清液,对照管加入1 mL 100 g/L TCA溶液,试验管加入2 mL 6.7 g/L TBA溶液,混匀,沸水浴20 min,冷却后于4 ℃、10 000×g离心10 min。测定上清液在450、532、600 nm 波长处的吸光值。重复3次。
1.3.5 总酚、类黄酮和花青素
参考曹建康[15]的方法,略有修改。称取1.0 g样品粉末,加入预冷的1%(体积分数)HCl-甲醇溶液摇匀,定容至10 mL,于4 ℃避光20 min,期间摇晃数次,过滤,取滤液,利用多功能酶标仪分别在波长280、325、600、530 nm处测定吸光度值,重复3次。以每克(鲜重)样品在波长280 nm处吸光度值表示总酚的相对含量,单位为OD280值/g;在波长325 nm处吸光度值表示类黄酮的相对含量,单位为OD325值/g;在波长530、600 nm处吸光度值之差表示花青素的相对含量,单位为(OD530-OD600)/g。
1.3.6 过氧化物酶(peroxidase,POD)
参考曹建康[15]的方法,略有修改。称取1 g样品粉末,加入5.0 mL预冷好的提取缓冲液并充分振荡混合,于离心机4 ℃、12 000×g离心30 min,收集上清液存为酶提取液。在试管中加入3.0 mL 25 mmol/L愈创木酚溶液和50 μL酶提取液,最后加入200 μL 0.5 mol/L H2O2溶液启动反应,同时立即开始计时,于15 s时利用酶标仪在波长470 nm处测定吸光度值,此后每隔1 min记录1次,至少获取6个数据,重复3次。计算每分钟吸光度变化值ΔOD470值,以每克样品(鲜重)每分钟吸光度变化值增加1时为1个过氧化物酶活性单位,单位是ΔOD470/(min·g)。
1.3.7 原果胶和可溶性果胶
参考曹建康[15]的方法,略有修改。称取0.5 g样品粉末于15 mL离心管中,加入95%(体积分数)乙醇至满刻度,沸水浴30 min,每10 min补充乙醇1次。冷却到室温后于8 000 r/min离心15 min,弃去上清液。于沉淀中加入10 mL蒸馏水,50 ℃保温30 min,冷却到室温后于8 000 r/min离心15 min,收集上清液于25 mL容量瓶,再用少量水洗涤沉淀,离心后并入容量瓶中,加蒸馏水定容,此为可溶性果胶待测液。再向原离心管中的沉淀加入10 mL 0.5 mol/L硫酸溶液,沸水浴60 min,冷却后离心,收集上清液于25 mL容量瓶,再用少量水洗涤沉淀,离心后并入容量瓶中,加蒸馏水定容,此为原果胶待测液。分别吸取1 mL待测液加入5 mL浓硫酸,沸水浴20 min,冷却后加入0.5 mL 1.5 g/L咔唑乙醇,避光静置30 min,在波长530 nm处测定吸光度值。重复3次。制作半乳糖醛酸标准曲线,以生成半乳糖醛酸的质量分数表示可溶性果胶与原果胶含量。
1.3.8 纤维素和半纤维素
纤维素和半纤维素均使用苏州科铭生物技术有限公司试剂盒测定。
1.3.9 细胞壁代谢酶
多聚半乳糖醛酸酶(polygalacturonase,PG)、果胶甲酯酶(pectin methylesterase,PE)、果胶裂解酶(pectin lyase,PL)、纤维素酶(cellulase,CL)均使用苏州科铭生物技术有限公司试剂盒测定。
1.4 数据处理
使用Excel 16整理数据;使用IBM SPSS Statistics 26软件进行显著性分析(*为P<0.05,**为P<0.01,***为P<0.001);使用Origin 2021作图。
2 结果与分析
2.1 桑葚秋果冰点确定
如图1所示,桑葚秋果置于-20 ℃冰箱一段时间后果实的中心温度迅速下降到-5.1 ℃左右,此为桑葚秋果的生物过冷点。果实组织为适应极低温环境释放出潜热,使温度回升到-1.6 ℃左右,此为桑葚秋果的生物结冰点,而后随时间缓慢冰结。由于个体差异、冷库温度波动等因素影响,在使用近冰温技术贮藏果蔬时,一般将贮藏温度设定为略高于冰点的温度,以避免冷害或冻害现象发生[9]。因此,为避免桑葚秋果在贮藏时发生冻结,本实验的近冰温贮藏温度设定为-0.5 ℃。
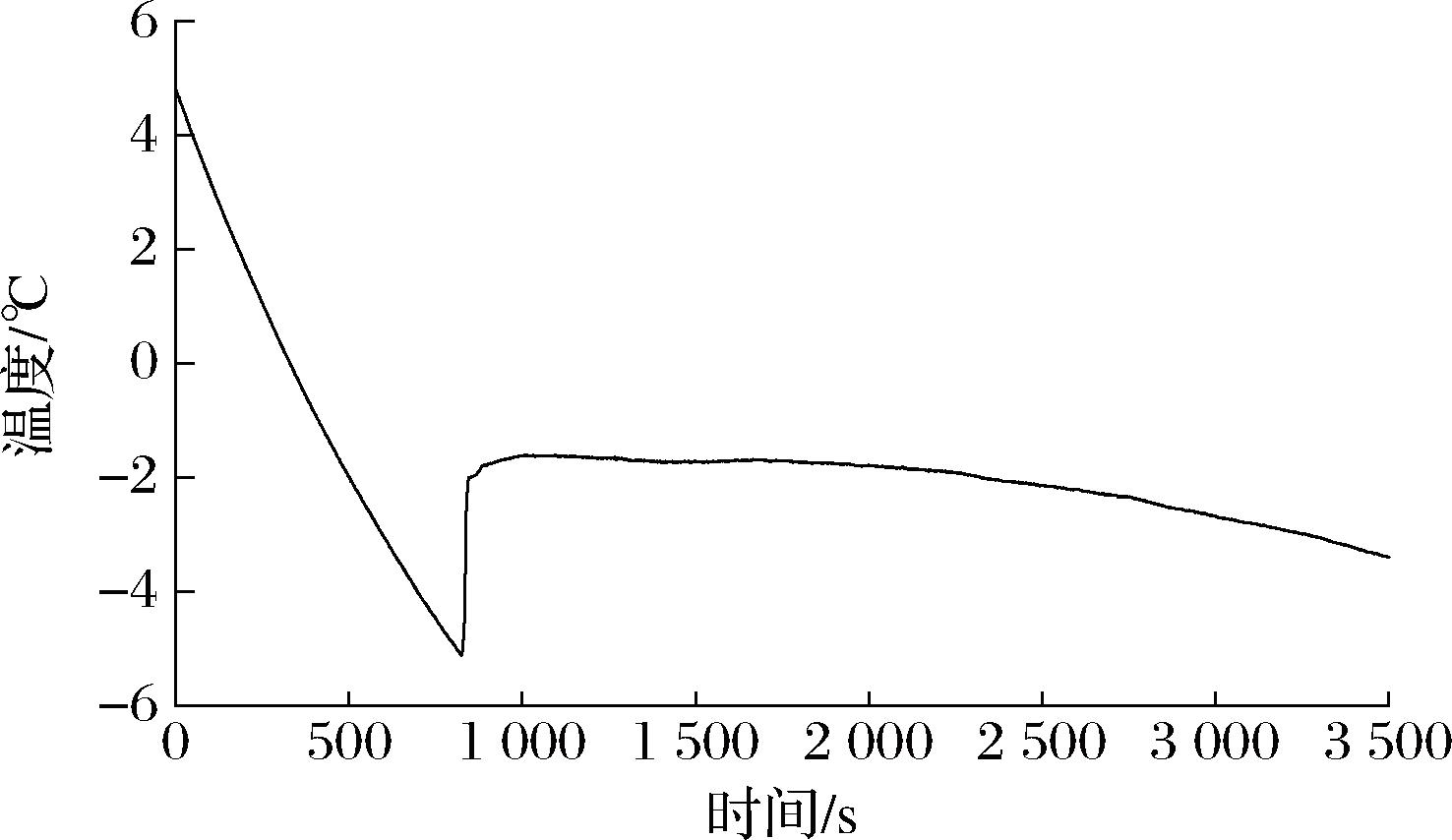
图1 桑葚秋果冰点曲线
Fig.1 Freezing point curve of mulberry autumn fruit
注:为保持冰点曲线的美观,已将误差线隐去。
2.2 不同温度贮藏下桑葚秋果的表观、自溶指数和腐烂率变化
不同温度贮藏下桑葚秋果的表观变化如图2-A所示,随着贮藏期的延长,桑葚秋果表面从光滑变皱缩,随后出现裂口和溢出汁液,内容物大量流失。NFT组在贮藏5 d时仅少数瘦果出现皱缩,15 d时自溶程度略有增加,果面出现裂口,25 d时果实流汁明显,30 d时果实表面明显干瘪软化,但仍保持较为完整的形状。LT组于贮藏5 d时出现小面积皱缩,15 d时皱缩现象加重并出现裂口,25 d时裂口增多,果实软化严重,内含物质明显减少,比NFT组同期果实更加干瘪,30 d时果实出现大面积自溶,汁水大量流出,瘦果之间界限模糊,基本丧失商品性。SS组于贮藏2 d 时便出现轻微软化,4 d时果面裂口明显并伴有汁水流出,6 d时出现大面积自溶,丧失商品性。
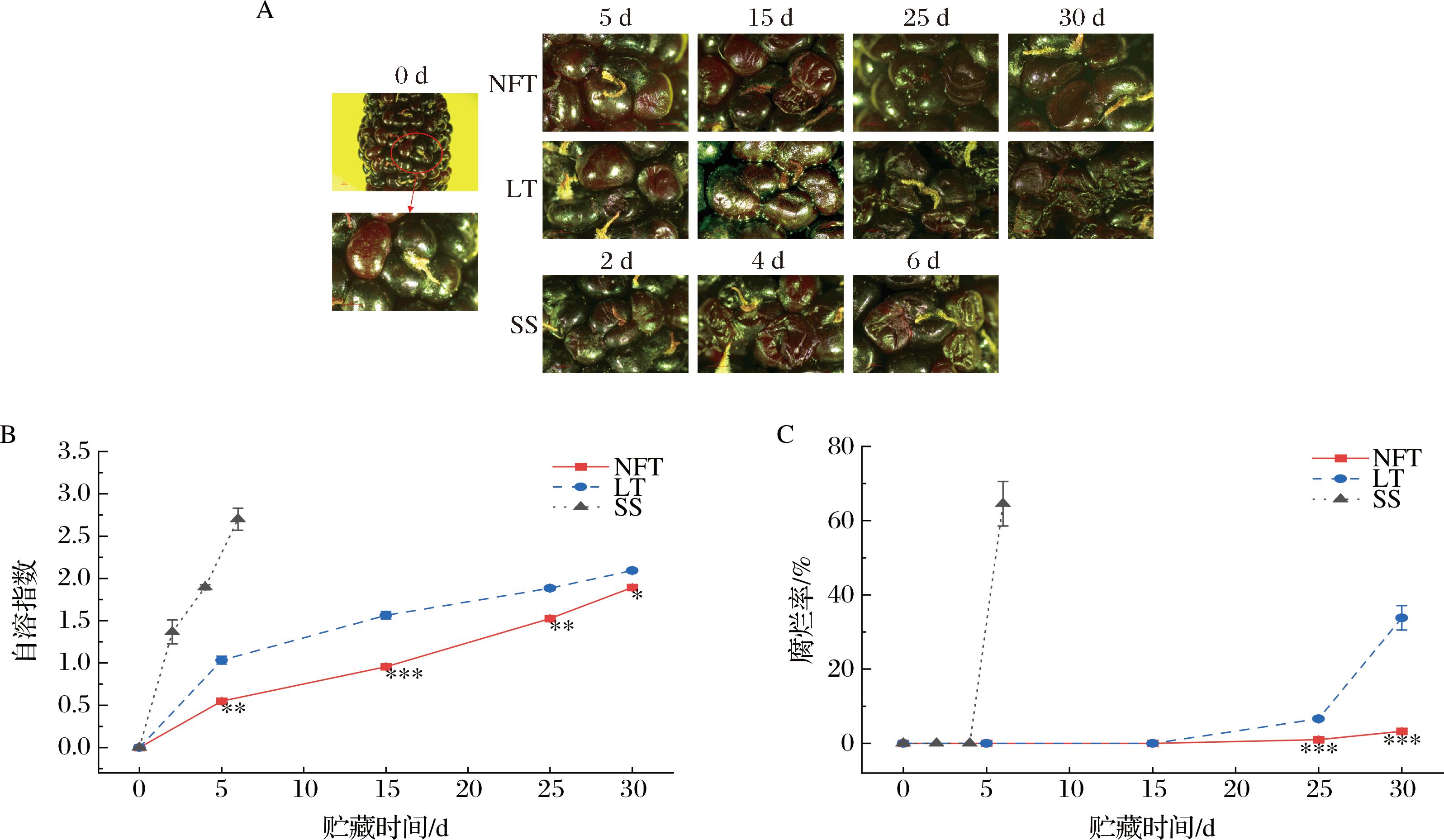
A-表观;B-自溶指数;C-腐烂率
图2 不同温度贮藏下桑葚秋果的表观、自溶指数和腐烂率变化
Fig.2 Changes in the apparent,aril breakdown index and decay rate of mulberry autumn fruit under different temperature storage
注:*,水平P<0.05显著;**,水平P<0.01显著;***,水平P<0.001极显著(下同)。
不同温度贮藏下桑葚秋果的自溶指数如图2-B所示,随贮藏时间延长而增加。SS组桑葚秋果的自溶指数增长迅速,6 d时便达到2.7,基本丧失商品价值。NFT组的自溶指数在贮藏期间始终显著低于LT组。0~5 d时NFT组与LT组自溶指数增长较快,5 d时分别达到0.65和1.03;5~25 d增长速度放缓,25 d时分别达到1.52和1.88;25 d后增长速度再次加快,于30 d时分别达到1.89和2.09。不同温度贮藏下桑葚秋果的腐烂率如图2-C所示,随贮藏时间而增加。SS组于6 d时腐烂率达到64.53%,基本失去商品性,之后不再取样。25 d时,NFT组和LT组桑葚秋果开始出现腐烂,腐烂率分别为1%和6.59%,形成极显著差异(P<0.001)。30 d时,NFT组腐烂率仅为3.23%,而LT组的腐烂率高达33.82%,极显著高于NFT组(P<0.001)。
综上所述,与4 ℃和15 ℃贮藏相比,近冰温贮藏能显著抑制桑葚秋果的采后自溶现象,减少霉变腐烂,保持桑葚秋果较高的贮藏品质。
2.3 不同温度贮藏下桑葚秋果的硬度、呼吸速率、失重率和MDA变化
硬度是衡量果实品质的重要指标之一,其数值降低是采后贮运过程中的常见现象,与果实成熟老化密切相关。如图3-A所示,不同温度贮藏下桑葚秋果的硬度随贮藏时间延长而不断降低。贮藏期间,NFT组的硬度始终保持最大,LT组次之。SS组的硬度下降速度最快,于贮藏6 d时便降至1.38 N。NFT组和LT组在贮藏0~5 d期间硬度下降较快,这可能是由于贮藏初期果实的呼吸作用和蒸腾作用较强,物质损耗明显;5~25 d时NFT组显著较LT组高(P<0.05);25 d后2组硬度加速下降,这可能与25 d时果实出现腐烂有关;30 d时NFT组和LT组硬度分别为1.33、1.51 N,相比0 d时分别下降0.8、0.98 g。试验结果表明,近冰温贮藏能有效保持桑葚秋果硬度,延缓果实软化。在西梅和李等水果中也发现类似现象[16-17],近冰温贮藏相较普通低温贮藏更能保持果实硬度,缓解果实软化进程。
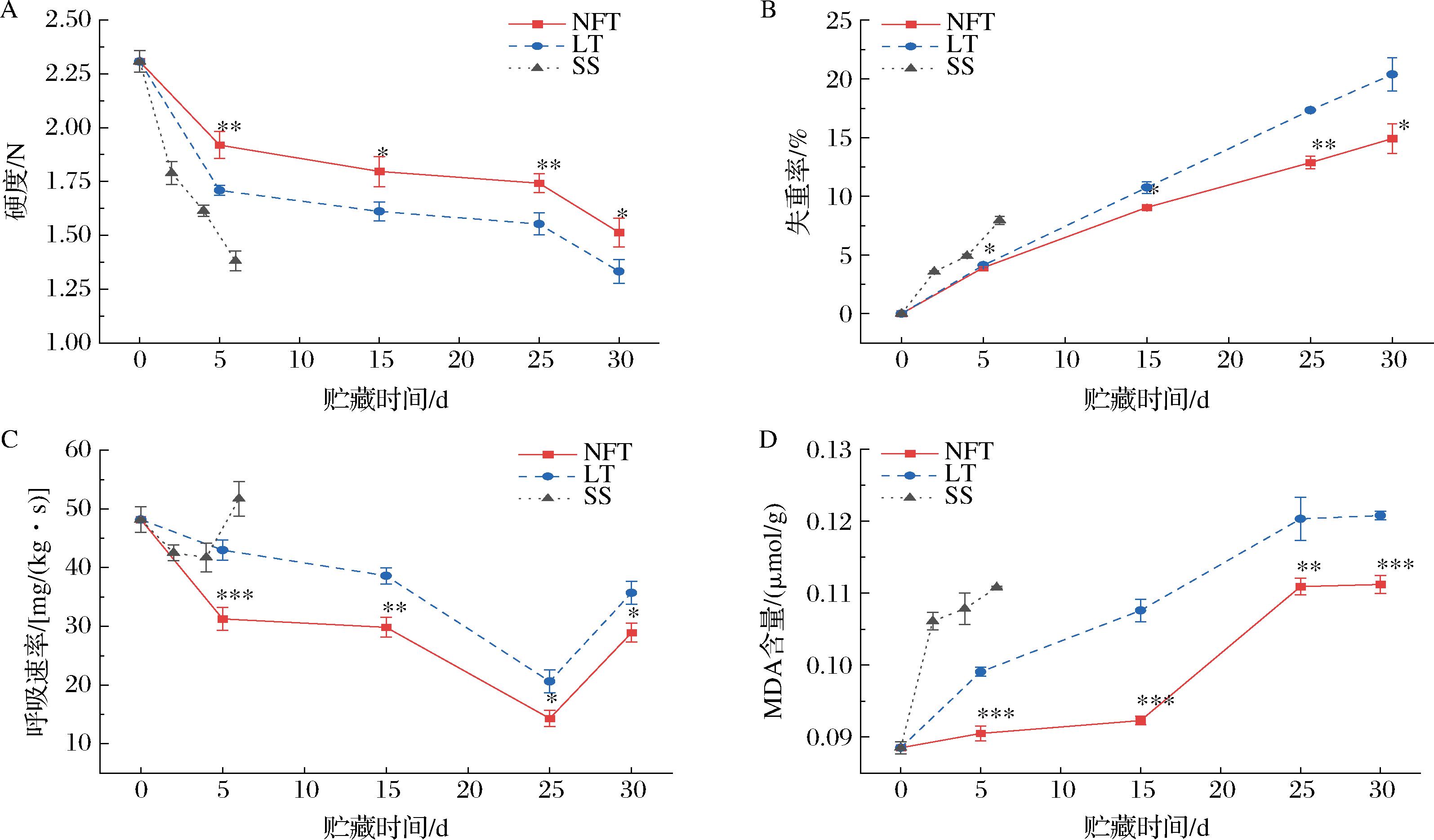
A-硬度;B-呼吸速率;C-失重率;D-MDA含量
图3 不同温度贮藏下桑葚秋果的硬度、呼吸速率、失重率和MDA含量变化
Fig.3 Changes in hardness,respiration rate,weight loss rate,and MDA content of mulberry autumn fruit under different temperature storage
呼吸作用是植物消耗氧气分解各类有机物并释放能量的过程,是导致植物成熟、衰老等生理现象的主要原因之一。如图3-B所示,不同温度贮藏下桑葚秋果的呼吸速率呈现先下降后上升的趋势。贮藏期间,NFT组桑葚秋果始终保持较低的呼吸速率,且显著低于LT组(P<0.05)。贮藏0~25 d期间,NFT组和LT组呼吸速率逐渐下降,25 d时2组降至最低,分别为14.32、20.64 mg/(kg·s);25 d后急速回升,推测这可能是由于此时果实出现腐烂,导致呼吸作用加剧。SS组桑葚秋果在贮藏0~4 d期间呼吸速率低于LT组,但于6 d时急速升高至53.72 mg/(kg·s),这可能与此时SS组桑葚秋果高度腐烂有关。有研究认为将果实贮藏在近冰温度下能在保持果实细胞完整的情况下将呼吸作用抑制在较低水平,通过降低代谢损失、减少微生物滋生保持果实贮藏品质[18],本试验结果也表明,近冰温贮藏下桑葚秋果呼吸速率被显著抑制,4 ℃对桑葚秋果的抑制效果次之。
失重是导致果实采后萎蔫变质的重要因素,主要源于果实蒸腾作用等导致的水分散失,以及呼吸和代谢作用消耗的养分。如图3-C所示,不同温度贮藏下桑葚秋果的失重率随时间延长不断上升。NFT组的失重率始终显著低于LT组(P<0.05),30 d时NFT组失重率仅为14.92%,而LT组达到20.38%,这可能是因为近冰温贮藏能更有效地抑制桑葚秋果的蒸腾作用和呼吸作用,从而减少水分和营养物质的消耗[19]。SS组桑葚秋果在贮藏6 d时失重率为7.85%,但之后由于腐烂率激增,停止取样。
植物器官在衰老或逆境条件下会发生膜脂过氧化作用,产生自由基对细胞膜造成破坏,MDA是其产物之一,通常将它作为脂质过氧化指标,继而间接表征植物器官衰老程度[11]。如图3-D所示,不同温度贮藏下桑葚秋果的MDA含量随贮藏时间延长而呈现上升的趋势。贮藏过程中,NFT组桑葚秋果的MDA含量始终显著低于LT组(P<0.01)。30 d时,NFT组和LT组的MDA含量分别为0.11、0.12 μmol/g,与贮藏初期相比分别增长0.023、0.032 μmol/g;形成极显著差异(P<0.001)。SS组的MDA含量最高,于6 d时便达到0.11 μmol/g。近冰温贮藏能显著降低桑葚秋果中的MDA积累,保持果实品质。
胡凯雪等[9]的研究发现,相比于5 ℃低温贮藏,近冰温(0±0.2) ℃能有效降低嘉宝果的失重率和腐烂率,延缓嘉宝果总酚和类黄酮含量的下降,减缓过氧化物酶和过氧化氢酶活性的下降,减缓超氧阴离子的产生速率和H2O2生成,进一步减少MDA积累和细胞膜透性增加。文钰等[16]的研究亦表明,与1~2 ℃和4~6 ℃贮藏相比,近冰温(-1~-1.5 ℃)可以显著维持西梅果实的硬度,降低果实的呼吸强度,有效调控西梅果实采后活性氧代谢的平衡,从而减少MDA积累与细胞膜透性的上升。综上所述,近冰温贮藏能显著延缓桑葚秋果采后软化,抑制呼吸作用,降低失重率,减少桑葚秋果采后的质量损失。
2.4 不同温度贮藏下桑葚秋果的总酚、类黄酮、花青素和POD活性变化
酚类物质是植物中广泛分布的次生代谢产物,具有较强的抗氧化能力,能抑制脂膜过氧化,延缓果实衰老,同时类黄酮和花青素也是果实气味和颜色的重要组成部分[20]。
如图4-A所示,不同温度贮藏下桑葚秋果的总酚相对含量均呈现先上升后下降的趋势,这可能是因为果实贮藏过程中酚类物质会出现积累的现象[21]。NFT组、LT组和SS组总酚相对含量峰值分别出现在25、5、2 d,且30 d时,NFT组的总酚相对含量保持在3.39 ΔOD280值,仍比LT组的总酚相对含量高0.067 ΔOD280值。结果表明,近冰温贮藏可以延缓桑葚秋果总酚相对含量峰值的出现,减少酚类物质的消耗,从而保持较高的营养价值和抗氧化能力。如图4-B所示,不同温度贮藏下桑葚秋果的类黄酮相对含量呈现先上升后下降的趋势。5~15 d时NFT组桑葚秋果的类黄酮相对含量显著高于LT组(P<0.05),25 d时NFT组和LT组的类黄酮相对含量达到峰值,分别为0.53、0.52 ΔOD325值,没有显著性差异,这表明近冰温贮藏可以有效抑制桑葚秋果类黄酮的消耗,且在贮藏前中期效果更为明显。而SS组桑葚秋果的类黄酮相对含量峰值于2 d出现,为0.53 ΔOD325值,之后迅速下降,6 d时便降至0.47 ΔOD325值。如图4-C所示,不同温度贮藏下桑葚秋果的花青素相对含量呈现先上升后下降的趋势。5 d时,NFT组桑葚秋果的花青素相对含量低于LT组,之后持续积累;25 d时,NFT组与LT组花青素相对含量达到峰值,分别为1.87(ΔOD530-ΔOD600)、1.78 (ΔOD530-ΔOD600),NFT组显著高于LT组(P<0.05);30 d时,2组花青素相对含量分别降至1.77(ΔOD530-ΔOD600)、1.70 (ΔOD530-ΔOD600),NFT组仍保持较高水平,这表明近冰温贮藏可以有效延缓桑葚秋果花青素的损耗。而SS组花青素相对含量于2 d达到峰值,之后迅速下降,6 d时降至1.52 (ΔOD530-ΔOD600)。
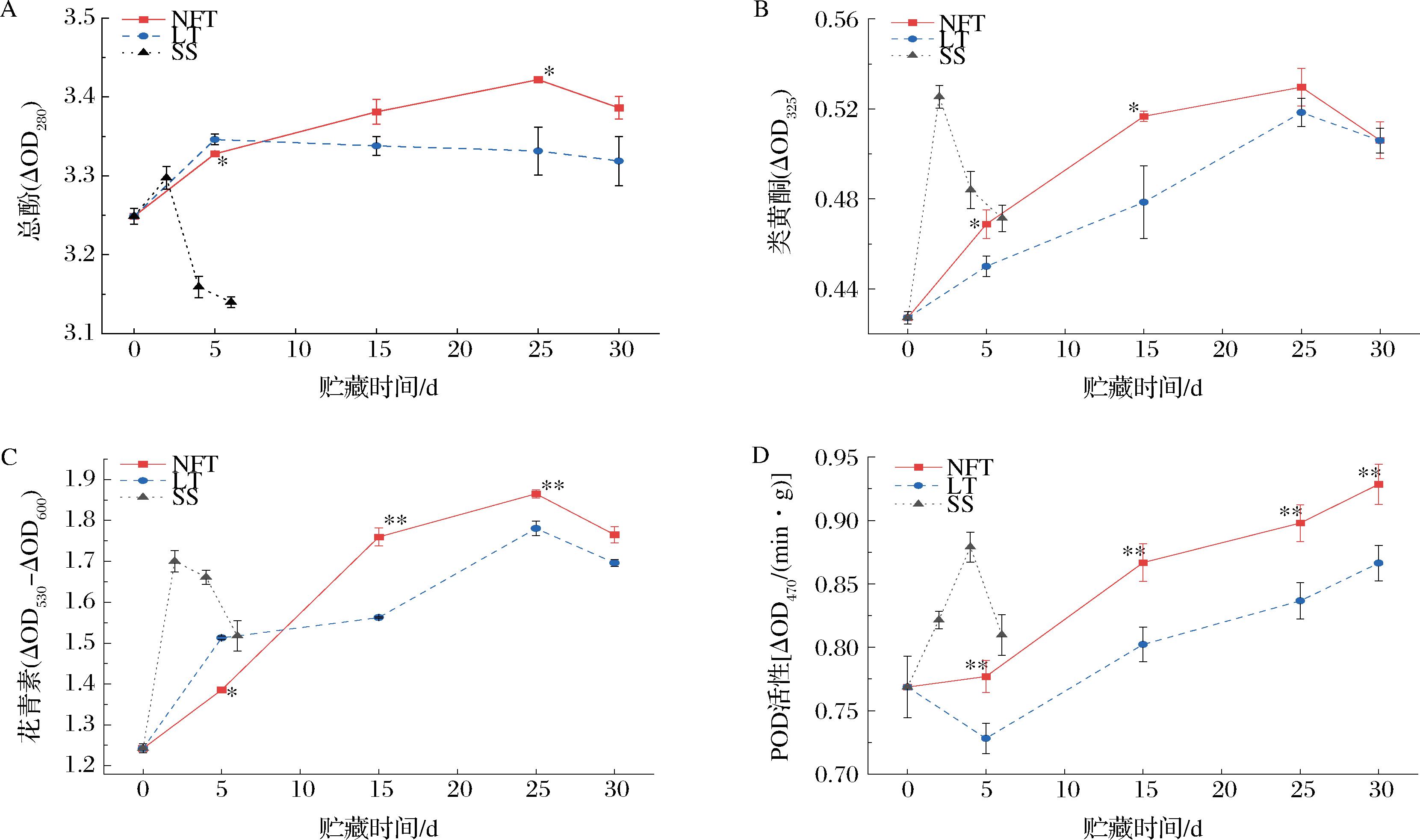
A-总酚;B-类黄酮;C-花青素;D-POD
图4 不同温度贮藏下桑葚秋果的总酚、类黄酮、花青素相对含量和POD活性变化
Fig.4 Changes in total phenolic,flavonoid,anthocyanin relative content,and POD activity of mulberry autumn fruit under different storage temperatures
FAN等[21]的研究表明,NFT可以有效降低杏采后抗氧化物质的消耗,延缓总酚和类黄酮含量峰值的出现,并减缓贮藏后期二者含量的下降,本试验结果与其类似;ZHAO等[22]的研究表明,近冰温贮藏在贮藏前期延缓甜樱桃花青素的合成,但在贮藏后期使其保持较高水平,本章试验结果中也有类似现象,在0~5 d时NFT组桑葚秋果的花青素含量低于LT组,但随着果实花青素的不断积累,15 d后NFT组的花青素含量始终高于LT组。综上所述,近冰温贮藏可显著减少桑葚秋果中酚类物质的消耗,保持较高的总酚、类黄酮和花青素含量,从而提高果实抗氧化能力,延缓果实采后品质劣变,延长果实贮藏期。
POD是植物中重要的氧化还原酶,有清除活性氧,保护细胞正常生物代谢的作用,较高的POD活性可以减轻贮藏期间活性氧对细胞组织的损伤,提高果实耐贮性[23]。如图4-D所示,NFT组与LT组桑葚秋果的POD活性均呈现持续上升的趋势,且NFT组始终显著高于LT组(P<0.05)。30 d时,NFT组POD活性仍比LT组高0.062 ΔOD470/(min·g)。SS组的POD活性呈现先上升后下降的趋势,于4 d时达到峰值,之后开始下降,6 d时为0.81 ΔOD470/(min·g)。MA等[17]和胡凯雪等[9]的研究认为近冰温贮藏可以通过影响果实采后的POD活性,维持果实中的活性氧平衡,提高果实的抗氧化能力,减少果实中MDA的积累。本试验也发现与4 ℃和15 ℃贮藏相比,近冰温贮藏保持果实较高的POD活性和较低的MDA含量。
综上所述,近冰温贮藏可有效减少桑葚果实中酚类物质的消耗,保持较高的总酚、类黄酮和花青素含量,并维持较高的POD活性,从而提高果实抗氧化性,延缓果实采后品质劣变,延长贮藏期。
2.5 不同温度贮藏下桑葚秋果的细胞壁各组分变化
高等植物细胞壁主要由纤维素、半纤维素和果胶物质等大分子物质组成,纤维素和半纤维素构成细胞壁的分子骨架,果胶物质对细胞壁结构稳定性起关键作用[24],因而桑葚采后软化腐烂与细胞壁各组分的降解密切相关。
如图5-A所示,不同温度贮藏下桑葚秋果的原果胶含量总体呈现下降趋势。贮藏期间,NFT组桑葚秋果始终保持较高的原果胶含量,直至25 d后才出现明显的下降趋势,且始终显著高于LT组(P<0.05),30 d时NFT组的原果胶含量为0.30%,比LT组高0.062%。这表明近冰温贮藏能更有效地保持果实原果胶含量,从而延缓果实软化自溶。如图5-B所示,不同温度贮藏下桑葚秋果的可溶性果胶含量总体呈现上升趋势。5 d时,NFT组与LT组桑葚秋果的可溶性果胶含量分别为0.35%和0.32%,形成显著差异(P<0.05);15~25 d期间,2组可溶性果胶含量持续上升,且NFT组始终低于LT组;30 d时,NFT组与LT组可溶性果胶含量分别为0.32%和0.37%,形成显著差异(P<0.01)。随着桑葚秋果在贮藏过程中的成熟与衰老,原果胶会不断被水解酶降解成可溶性果胶,导致可溶性果胶含量增加。本研究结果表明近冰温贮藏能延缓原果胶降解,减少可溶性果胶含量的积累。如图5-C所示,NFT组和LT组桑葚秋果的纤维素含量总体呈现先上升后下降的趋势,5~15 d期间2组无显著差异;25~30 d期间NFT组和LT组的纤维素含量均形成极显著差异(P<0.001);30 d时,NFT组纤维素含量为28.52 mg/g,比LT组高2.02 mg/g。SS组纤维素含量随时间延长呈现下降趋势,于6 d时降至最低值19.16 mg/g。因此,近冰温贮藏可以有效抑制桑葚秋果纤维素讲解,尤其在贮藏中后期效果更为明显。如图5-D所示,不同温度贮藏下桑葚的半纤维素含量总体呈现先上升后下降的趋势。NFT组半纤维素含量在贮藏期间始终显著高于LT组;15 d时,2组半纤维素含量达到峰值,形成极显著差异(P<0.001),之后开始下降,30 d时分别降至20.46、17.51 mg/g,亦形成极显著差异(P<0.001)。SS组桑葚秋果半纤维素含量在4 d时达到峰值,之后逐渐下降,6 d时降至14.79 mg/g。这表明近冰温贮藏可以有效抑制桑葚秋果半纤维素的降解,维持细胞壁结构稳定。
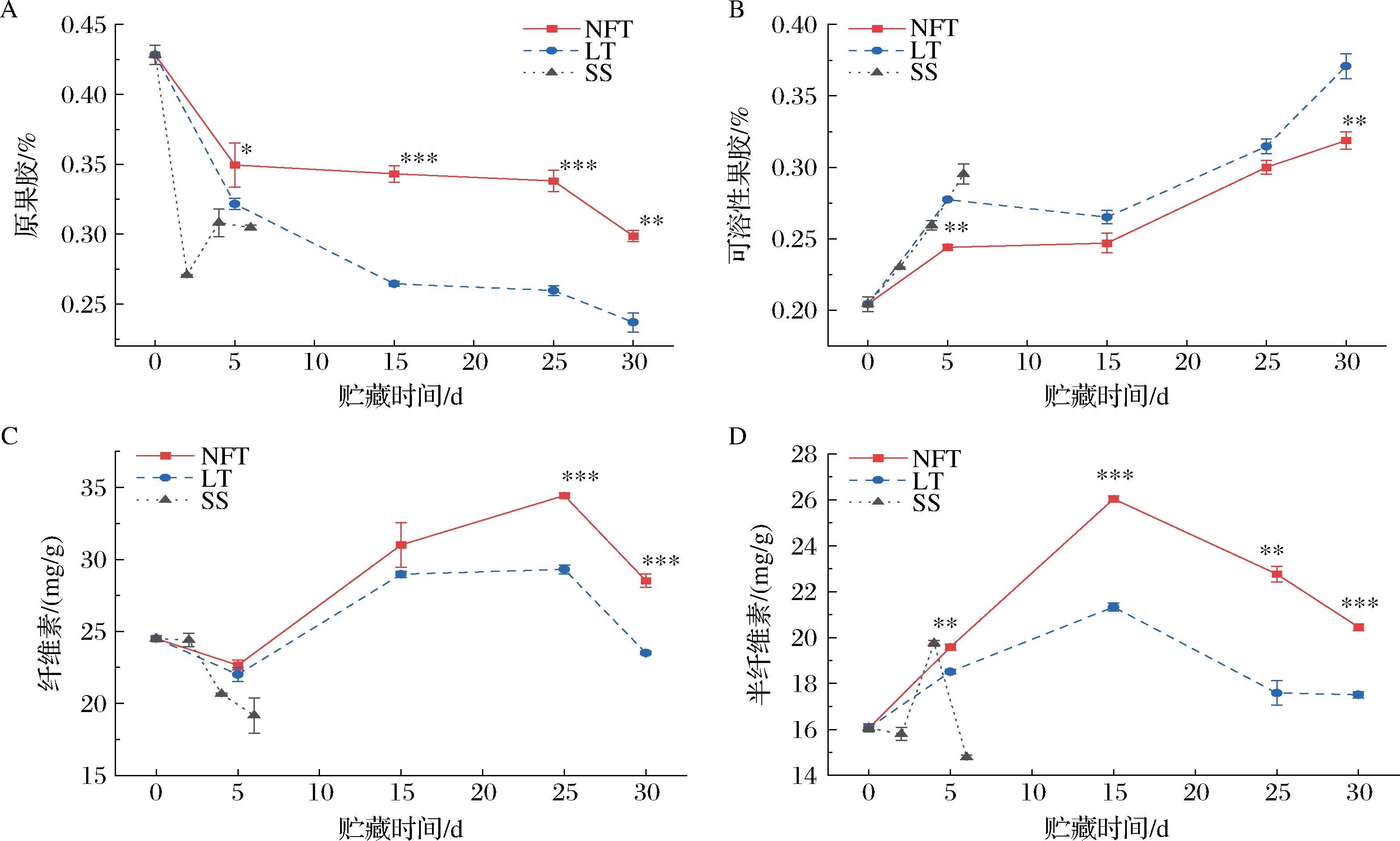
A-原果胶;B-可溶性果胶;C-纤维素;D-半纤维素
图5 不同温度贮藏下桑葚秋果的原果胶、可溶性果胶、纤维素和半纤维素含量变化
Fig.5 The contents of raw pectin,soluble pectin,cellulose,and hemicellulose in mulberry autumn fruit were changed under different temperature storage
果实后熟软化过程与细胞壁结构被破坏,纤维素、半纤维素和果胶等细胞壁组分降解有关[25]。随着贮藏时间延长,细胞壁中不可溶性的原果胶逐渐降解为可溶性果胶等物质,同时作为分子骨架的纤维素和半纤维素降解,导致细胞壁崩解,进而加剧自溶腐烂的发生[24],本试验数据显示,在贮藏过程中桑葚秋果的原果胶含量呈现下降趋势,于贮藏0~5 d期间下降速度较快,5~25 d期间下降速度放缓,25 d之后下降速度再次加快,与桑葚秋果硬度下降的规律几乎一致,这说明桑葚秋果的软化可能主要与原果胶含量变化有关;纤维素和半纤维素含量呈现先上升后下降的趋势,这可能是由于桑葚秋果在贮藏过程中水分流失严重,其他物质被大量降解,导致水不溶性纤维占比加大[24]。综上所述,近冰温贮藏的桑葚秋果中原果胶、纤维素和半纤维素含量均显著高于4、15 ℃贮藏,且可溶性果胶含量维持在较低水平,表明近冰温贮藏能有效维持桑葚秋果细胞壁结构完整性,显著延缓果实软化进程,在杏[26]和西葫芦[27]的研究中也有类似规律,即果实贮藏在近冰温条件下可显著抑制果胶和纤维素降解,从而维持更高的果实硬度。
2.6 不同温度贮藏下桑葚秋果的细胞壁代谢酶活性变化
细胞壁各组分变化受多种细胞壁代谢酶的共同调控。PG具有降解果胶的功能,通常被视作调控果肉质地软化的关键酶,目前研究普遍认为PE本身并非果实软化的关键酶,而是通过将果胶分子从高甲酯化转化为低甲酯化状态,从而促进PG对果胶的水解,起到果实软化的先导作用,在二者的协同水解下促使果胶结构发生改变;PL是主要作用于植物细胞壁的解聚酶,能够降解高度甲酯化果胶,从而加速果蔬细胞壁降解、组织软化及衰老;CL是一种能够分解含β-1,4糖苷键半纤维素的水解酶,多被认为与果实成熟软化有关[28-29]。
如图6-A所示,5~15 d NFT组的PG活性始终显著低于LT组(P<0.01),25 d时达到峰值,为15.49 mg/(h·g),此时显著高于LT组(P<0.01);LT组的PG活性随贮藏时间延长而持续下降,30 d时降至5.12 mg/(h·g);SS组的PG活性呈现先上升后下降的趋势,于2 d时达到峰值,之后不断下降,6 d时降至29.46 mg/(h·g)。结果表明,近冰温贮藏能有效抑制桑葚秋果的PG酶活性,尤其在贮藏前期可以使其保持在较低水平。如图6-B所示,不同温度贮藏下桑葚秋果的PE活性呈现先上升后下降的趋势。NFT组和LT组的PE活性均在5 d达到峰值,之后逐渐下降,30 d时分别降至1.49、1.73 U/g。在贮藏期间,NFT组的PE活性始终显著低于LT组(P<0.05)。SS组的PE活性于2 d时达到峰值,之后逐渐下降,6 d时降至2.14 U/g。结果表明,近冰温贮藏能有效抑制桑葚秋果的PE活性,4 ℃贮藏的抑制效果次之。如图6-C所示,不同温度贮藏下桑葚的PL活性呈现先上升后下降的趋势。NFT组、LT组和SS组桑葚秋果的PL活性峰值分别出现在25、15、2 d,之后不断下降。NFT组的峰值晚于LT组出现,因而在30 d时出现了NFT组显著较LT组高的现象,结果表明近冰温贮藏能有效推迟桑葚秋果PL活性峰值的出现,从而延缓果实软化。不同温度贮藏下桑葚的CL活性如图6-D所示,呈现先上升后下降的趋势。NFT组、LT组和SS组的CL活性峰值分别出现在25、152 d时,之后不断下降。15 d时NFT组的CL活性显著低于LT组(P<0.05);25 d时NFT组达到峰值32.52 mg/(h·g),因而与同时期LT组失去显著性,但仍低于LT组;30 d时NFT组与LT组的PL活性分别为25.72、29.17 mg/(h·g),NFT组显著低于4 ℃(P<0.05)。结果表明,近冰温贮藏可以有效降低桑葚CL活性,延缓其活性峰值的出现,从而减少细胞壁降解,保持桑葚秋果采后品质。
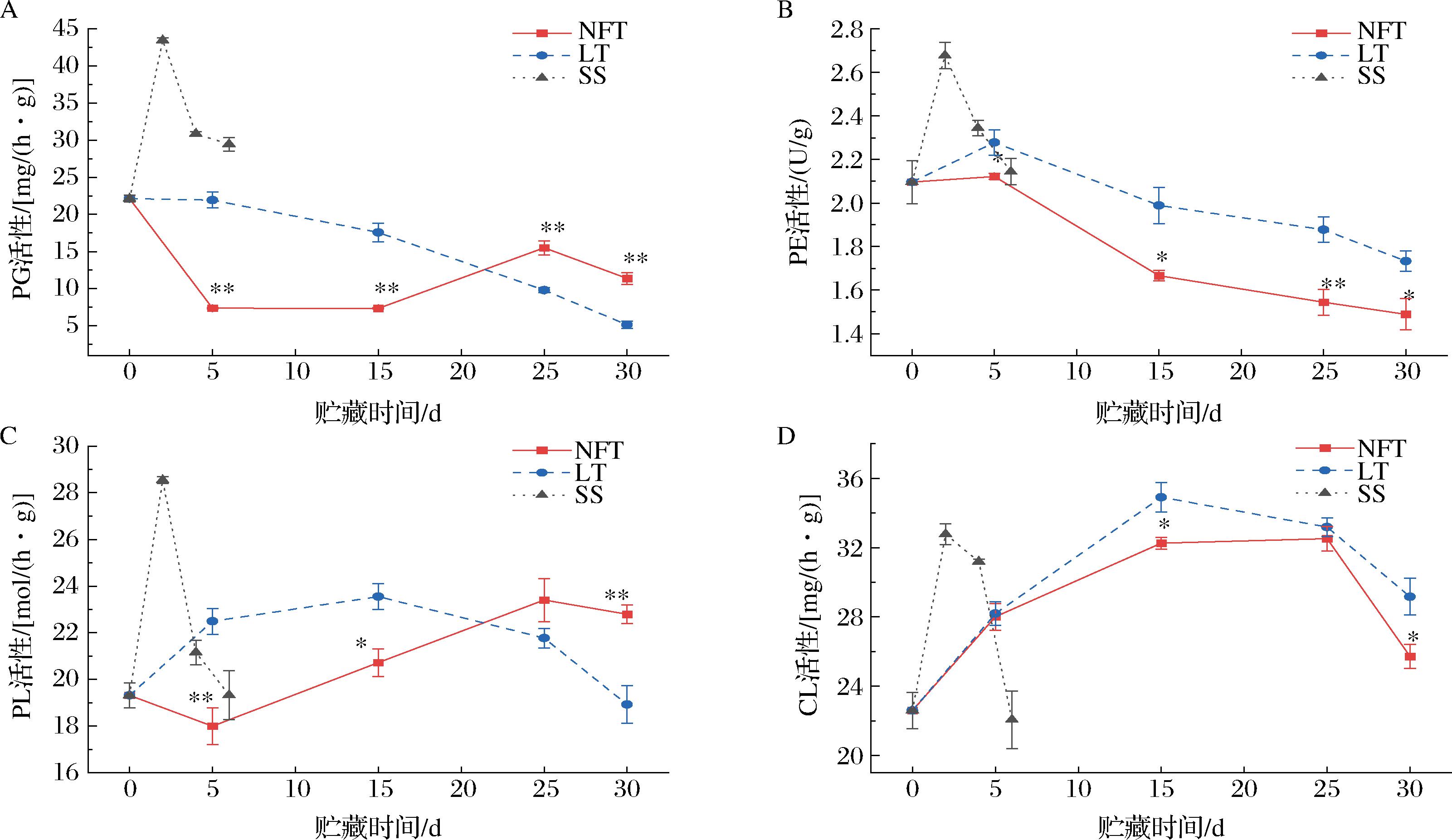
A-PG活性;B-PE活性;C-PL活性;D-CL活性
图6 不同温度贮藏下桑葚秋果的PG、PE、PL和CL活性变化
Fig.6 Changes of PG,PE,PL,and CL activities of mulberry autumn fruit under different temperature storage
在果实软化的过程中,各类细胞壁代谢酶单独或协同作用,引发中胶层解离、纤维素解聚、细胞壁结构解体等过程[30]。本试验结果显示,近冰温贮藏的桑葚秋果均出现PG、PL和CL等活性高峰延后出现的现象。虽然PE活性峰值的出现时间未受影响,但其活性始终保持在较低水平。现有研究认为果胶甲酯酶并非是直接导致果实软化的关键酶,而是通过将高甲酯化果胶分子转化为低甲酯化状态,为PG对果胶的水解创造条件,起到果实软化的先导作用[28],近冰温贮藏的桑葚秋果在贮藏5~15 d PG活性较低,可能与其PE活性持续处于较低水平密切相关。YANG等[30]的研究表明,近冰温贮藏可以抑制新疆杏细胞壁代谢酶活性,从而保持较高的果胶和纤维素含量,CARVAJAL等[26]的研究也表明,近冰温贮藏抑制PG、PE和CL和相关基因表达,从而抑制![]() 可溶性果胶和纤维素的溶解,还通过显微镜观察到近冰温贮藏延缓了果胶部分的降解,保护了细胞壁结构不松动。
可溶性果胶和纤维素的溶解,还通过显微镜观察到近冰温贮藏延缓了果胶部分的降解,保护了细胞壁结构不松动。
综上所述,近冰温贮藏可以有效降低桑葚秋果细胞壁代谢酶活性,延缓酶活性峰值的出现,保持果实品质,这也与前文腐烂率、硬度、细胞壁组分含量等指标的结果相对应。
3 结论
本试验探究了桑葚秋果在-0.5 ℃(近冰温)、4 ℃(低温)和15 ℃(模拟货架)3种贮藏条件下的采后贮藏品质变化。结果显示,近冰温贮藏30 d的果实仍保持较高硬度、较低腐烂率和自溶指数;而4、15 ℃贮藏的桑葚秋果分别于25、6 d即出现较严重腐烂率、失重率和果实自溶,商品性降低。近冰温贮藏可有效降低桑葚秋果的呼吸速率,延缓类黄酮和花青素的降解,维持总酚含量,保持较高的POD活性,抑制MDA积累,提升抗氧化能力;减缓原果胶、纤维素和半纤维素等细胞壁组分的降解,抑制PG、PL、CL等细胞壁代谢酶活性,从而维持桑葚秋果细胞壁结构的完整性。综上所述,近冰温贮藏能有效保持桑葚秋果采后品质,具有较好的推广价值。
[1] YANG X L,YANG L,ZHENG H Y.Hypolipidemic and antioxidant effects of mulberry (Morus alba L.) fruit in hyperlipidaemia rats[J].Food and Chemical Toxicology,2010,48(8-9):2374-2379.
[2] 孙雅楠,哀嘉彬,唐爱妙,等.浙江桑葚菌核病的病原菌鉴定及其对4种杀菌剂的抗性检测[J].果树学报,2020,37(12):1934-1940.SUN Y N,AI J B,TANG A M,et al.Identification of pathogenic fungi causing mulberry fruit sclerotiniose and their resistance to four fungicides in Zhejiang[J].Journal of Fruit Science,2020,37(12):1934-1940.
[3] 魏晓军.台湾果桑的引种及栽培技术[J].农业科技通讯,2006(4):48.WEI X J.Introduction and cultivation techniques of fruit mulberry in Taiwan[J].Bulletin of Agricultural Science and Technology,2006(4):48.
[4] 罗国庆.应用周年挂果技术助力广东省果桑产业发展[J].蚕学通讯,2021,41(3):59.LUO G Q.Application of annual fruit technology to promote the development of fruit mulberry industry in Guangdong[J].Newsletter of Sericultural Science,2021,41(3):59.
[5] MO R L,QIU C Y,HUANG S,et al.High-quality off-season mulberry fruit (Morus laevigata Wall.) induced by summer pruning[J].Notulae Botanicae Horti Agrobotanici Cluj-Napoca,2024,52(2):13569.
[6] 楼文美,刘培刚,朱爱青,等.义乌市引进秋期桑椹露天反季节栽培技术初探[J].中国蚕业,2024,45(2):7-9.LOU W M,LIU P G,ZHU A Q,et al.Preliminary study on the technique of open-air counter-seasonal cultivation of autumn mulberry in Yiwu[J].China Sericulture,2024,45(2):7-9.
[7] IKEGAYA A,OHBA S,NAKAJIMA T,et al.Practical long-term storage of strawberries in refrigerated containers at ice temperature[J].Food Science &Nutrition,2020,8(9):5138-5148.
[8] 李亚玲,崔宽波,石玲,等.近冰温贮藏对杏果实冷害及活性氧代谢的影响[J].食品科学,2020,41(7):177-183.LI Y L,CUI K B,SHI L,et al.Effect of near freezing temperature storage on chilling injury and active oxygen metabolism of apricot fruit[J].Food Science,2020,41(7):177-183.
[9] 胡凯雪,邱秋萍,刘顺枝,等.近冰温贮藏对嘉宝果采后品质和抗氧化活性的影响[J].食品科学,2024,45(11):258-266.HU K X,QIU Q P,LIU S Z,et al.Effect of near-freezing temperature storage on postharvest quality and antioxidant activity of jabuticaba[J].Food Science,2024,45(11):258-266.
[10] 王香君,殷浩,刘刚,等.采后桑椹冰温保鲜研究[J].食品工业,2020,41(9):193-198.WANG X J,YIN H,LIU G,et al.Study on controlled freezing-point storage treatment on the preservation of mulberry[J].The Food Industry,2020,41(9):193-198.
[11] 张莉会,乔宇,陈学玲,等.不同保鲜剂对桑葚贮藏期间品质的影响[J].现代食品科技,2018,34(5):47-55.ZHANG L H,QIAO Y,CHEN X L,et al.Effects of different preservatives on the quality of mulberry during storage[J].Modern Food Science and Technology,2018,34(5):47-55.
[12] 骆宇立,陈俊杰,李倩,等.不同温度下桑葚失重率与质构特性的相关性分析[J].食品科技,2022,47(11):43-50.LUO Y L,CHEN J J,LI Q,et al.Correlation analysis of weight loss rate and texture characteristics of mulberry at different temperatures[J].Food Science and Technology,2022,47(11):43-50.
[13] 蒋汉蓉,贺立红,王玲,等.常温下不同包装方式对甘薯抑芽作用及品质的影响[J].南方农业学报,2024,55(6):1744-1752.JIANG H R,HE L H,WANG L,et al.Effects of different packaging methods on sprout suppression and quality of sweet potato at room temperature[J].Journal of Southern Agriculture,2024,55(6):1744-1752.
[14] 赵云峰.细胞壁代谢在龙眼采后果肉自溶发生过程中的作用[D].福州:福建农林大学,2005.ZHANG Y F.The role of cell wall metabolism in aril breakdown of postharvest Longan fruit[D].Fuzhou:Fujian Agriculture and Forestry University,2005.
[15] 曹建康.果蔬采后生理生化实验指导[M].北京:北京轻工业出版社,2017.CAO J K.Experiment Guidance of Postharvest Physiology and Biochemistry of Fruits and Vegetables[M].Beijing:China Light Industry Press,2017.
[16] 文钰,杨莉玲,刘岚,等.近冰温贮藏对西梅的采后品质及活性氧代谢的影响[J].食品与发酵工业,2024,50(11):270-276.WEN Y,YANG L L,LIU L,et al.Effects of near-freezing temperature storage on postharvest quality and reactive oxygen species metabolism of prunes[J].Food and Fermentation Industries,2024,50(11):270-276.
[17] MA Y Y,ZHANG W D,CHENG S B,et al.Postharvest storage at near-freezing temperature maintained the quality and antioxidant properties of Prunus domestica L.cv.Ximei fruit[J].Scientia Horticulturae,2022,293:110720.
[18] 刘倍毓,邓利玲,胡小芳,等.冰温技术在果蔬贮藏保鲜中的应用研究进展[J].食品与发酵工业,2011,37(12):109-112.LIU B Y,DENG L L,HU X F,et al.Advances of controlled freezing point technology applied on the storage of fruits and vegetables[J].Food and Fermentation Industries,2011,37(12):109-112.
[19] ONO S,YASUTAKE D,YOKOYAMA G,et al.Closed chamber system for easily measuring the respiration rate of intact fruits[J].Environment Control in Biology,2022,60(1):33-37.
[20] 刘晴晴,李勇,张明霞,等.紫色桑葚和白色桑葚总酚含量、抗氧化能力及代谢指纹图谱差异分析[J].江苏农业学报,2022,38(3):813-820.LIU Q Q,LI Y,ZHANG M X,et al.Differences in total phenol content,antioxidant activity and metabolic fingerprint between purple mulberry and white mulberry[J].Jiangsu Journal of Agricultural Sciences,2022,38(3):813-820.
[21] FAN X G,JIANG W B,GONG H S,et al.Cell wall polysaccharides degradation and ultrastructure modification of apricot during storage at a near freezing temperature[J].Food Chemistry,2019,300:125194.
[22] ZHAO H D,LIU B D,ZHANG W L,et al.Enhancement of quality and antioxidant metabolism of sweet cherry fruit by near-freezing temperature storage[J].Postharvest Biology and Technology,2019,147:113-122.
[23] LIU H,JIANG W B,CAO J K,et al.Changes in extractable and non-extractable polyphenols and their antioxidant properties during fruit on-tree ripening in five peach cultivars[J].Horticultural Plant Journal,2019,5(4):137-144.
[24] 哈比江·开乃斯,李新豫,赵蕾,等.不同成熟度杏果实低温贮藏条件下的品质变化规律[J].经济林研究,2024(3):105-119.KAINAISI H B J,LI X Y,ZHAO L,et al.Quality changes of apricot fruits with di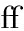 erent maturity under low temperature storage conditions[J].Non-wood Forest Research,2024(3):105-119.
erent maturity under low temperature storage conditions[J].Non-wood Forest Research,2024(3):105-119.
[25] 李萍,廖康,赵世荣,等.杏果实发育成熟过程中细胞壁组分和水解酶活性的变化[J].新疆农业大学学报,2013,36(4):298-303.LI P,LIAO K,ZHAO S R,et al.Variation of cell wall and hydrolasesin apricot fruit during development and maturing process[J].Journal of Xinjiang Agricultural University,2013,36(4):298-303.
[26] CARVAJAL F,PALMA F,JAMILENA M,et al.Cell wall metabolism and chilling injury during postharvest cold storage in zucchini fruit[J].Postharvest Biology and Technology,2015,108:68-77.
[27] JIA K N,WANG W,ZHANG Q,et al.Cell wall integrity signaling in fruit ripening[J].International Journal of Molecular Sciences,2023,24(4):4054.
[28] ZHENG L,XU Y X,LI Q,et al.Pectinolytic lyases:A comprehensive review of sources,category,property,structure,and catalytic mechanism of pectate lyases and pectin lyases[J].Bioresources and Bioprocessing,2021,8(1):79.
[29] POSÉ S,PANIAGUA C,MATAS A J,et al.A nanostructural view of the cell wall disassembly process during fruit ripening and postharvest storage by atomic force microscopy[J].Trends in Food Science &Technology,2019,87:47-58.
[30] YANG W T,LIU Y X,SANG Y Y,et al.Influences of ice-temperature storage on cell wall metabolism and reactive oxygen metabolism in Xinjiang (Diaogan) apricot[J].Postharvest Biology and Technology,2021,180:111614.