非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)是一种以肝细胞发生大泡性或微泡性脂肪变性为主要病理特征,炎症和纤维化为主要进展标志的肝脏代谢疾病,其发生发展与胰岛素抵抗(insulin resistance,IR)、肥胖、2型糖尿病等代谢综合症密切相关[1]。流行病学数据表明[2],我国NAFLD的患病率高达29.88%,提示NAFLD已然成为日益严重的公共卫生问题。NAFLD发病机制复杂,逐渐从“双重打击假说”(第一击:肝细胞脂肪堆积,第二击:氧化应激、炎症)发展为“多重打击学说”,后者则更多强调多因素(IR,脂毒性,胆固醇代谢异常,肠道菌群失调等),以及多器官(肠道、脂肪组织等)互相协同作用,共同加剧NAFLD发生发展[1]。其中,核因子-κB(nuclear factor-κB,NF-κB)与NOD样受体蛋白3(NOD-like receptor family pyrin domain containing protein 3,NLRP3)以协同或级联机制共同驱动的炎症信号通路表达在“多重打击假说”中扮演重要角色。一方面,肝细胞内脂毒性及氧化应激激活NF-κB通路启动上游炎症启动,诱导TNF-α、IL-6等促炎因子表达直接加剧肝细胞损伤,而线粒体活性氧累积、内质网应激发NLRP3炎性小体组装,继而通过半胱氨酸天冬氨酸蛋白酶-1(cysteinyl aspartate specific proteinase-1,caspase-1)切割IL-1β前体释放成熟促炎因子,导致肝细胞焦亡及星状细胞活化[3];另一方面,肠道菌群稳态失调导致屏障损伤,内毒素脂多糖(lipopolysaccharide,LPS)及菌群代谢产物经门静脉入肝,并通过Toll样受体4(toll-like receptor 4,TLR4)激活NF-κB信号通路表达,NF-κB继而上调NLRP3转录,NLRP3释放的IL-1β通过自分泌增强NF-κB活性,进而放大炎症级联[4],提示抑制NF-κB及NLRP3介导的炎症信号通路表达是治疗NAFLD的有效靶点。
姜黄素(curcumin,CUR)作为一种姜黄(Curcuma longa L.)根茎中的一种结晶状黄色的多酚化合物(分子质量:368.39 g/mol)[]5,可通过靶向多种信号通路,有效发挥抗炎和抗氧化的药理学作用,因此被广泛应用于NAFLD的治疗过程中[6]。值得注意的是,CUR不仅可以通过减轻IR,抑制氧化应激反应等作用机制减少肝脏脂肪沉积[7],还可通过调节肠道微生物群组成及其代谢产物介导“肠-肝轴”交叉对话,并通过抑制TLR4/NF-κB信号通路,减轻肝脏炎症和脂肪变性[8]。近年来,在多靶点协同调控机制的疾病治疗策略下,“药物+生活方式”联合干预的多模式干预手段逐渐应用于NAFLD的靶向治疗方案中[9],有研究指出CUR联合有氧运动(aerobic exercise,AE)可分别从药理层面和能量代谢层面调动多器官交互产生叠加效应,并通过增强自噬水平[10]、调节肠道菌群稳态[11]等多个机制改善NAFLD。然而,CUR联合AE对NAFLD小鼠肠道菌群的影响效果存在一定争议,相较于单一CUR或AE干预,联合干预并未进一步增加肠道菌群稳态的改善效果[12]。目前,抗阻运动(resistance exercise,RE)作为治疗NAFLD的另一种潜在非药物治疗手段,能够通过激活过氧化物酶体增殖物激活受体γ(peroxisome proliferator-activated receptor gamma,PPARγ)信号通路[13],显著上调肝脏中脂肪酸β-氧化关键基因表达促进游离脂肪酸的分解代谢[14],进而减少肝脏脂质沉积并防治NAFLD。但RE是否能够通过调节肠道菌群改善NAFLD目前暂无报道,同时CUR联合RE干预是否能够产生更好的增益效果尚且不知。基于以上研究背景,本研究通过16S rRNA测序分析CUR、RE单独干预,以及两者联合干预后NAFLD小鼠肠道菌群的变化情况,并分析肝脏中NF-κB和NLRP3介导的炎症信号通路的激活程度,旨在为药物联合运动干预防治NAFLD提供新的治疗靶点和思路。
1 材料与方法
1.1 材料与试剂
CUR,上海麦克林生化科技股份有限公司;RIPA强裂解液、苯甲基磺酰氟蛋白酶抑制剂,碧云天生物技术有限公司;甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)比色法检测试剂盒,南京建成生物公司;NF-κB、NLRP3、微管蛋白,成都正能技术有限公司,IL-1β、TNF-α,武汉三鹰生物技术有限公司;10%聚丙烯酰胺凝胶电泳(polyacrylamide gel electrophoresis,PAGE)凝胶制备试剂盒、三色预染蛋白Mark,上海雅酶生物医药科技有限公司;苏木精-伊红(hematoxylin and eosin,H&E)染色试剂盒,武汉赛维尔生物科技有限公司。
1.2 仪器与设备
ZL-013动物跑台,安徽耀坤生物科技有限公司;51029702超净工作台、Multiskan FC酶标仪,赛默飞世尔科技公司;AG 5428高速离心机,Eppendorf公司;Tissuelyer-24多样品组织研磨机,上海净信实业发展公司;PowerPac Basic电泳仪和转膜仪,Bio-Rad公司;MiniChemi 420化学发光成像仪,北京赛智创业科技有限公司;RM 2126石蜡切片机,Leica公司;BX51显微镜,Olympus Corporation公司。
1.3 实验动物
8周龄雄性C57BL/6小鼠60只,SPF级,购置于湖南斯莱克景达实验动物有限公司,体质量约为17~21 g,实验动物使用许可编号:SCXK(湘)2019-0004。所有小鼠饲养于标准无病原体环境中,温度条件为(23±1) ℃,湿度条件为(55±5)%,光照条件为12 h光暗循环,饮食条件为自由摄食饮水,垫料每周更换2次。实验方案遵循动物研究“3R原则”,研究遵循的程序符合负责动物试验委员会(吉首大学)所制订的伦理学标准,并经吉首大学生物医学伦理委员会批准(审批号为JSDX-2024-0126)。
1.4 实验方法
1.4.1 动物造模及干预方案
小鼠适应性喂养1周后,随机分为空白对照组(control,CON,n=12)和NAFLD造模组(n=48),CON组以10%脂肪供能的普通饲料喂养,而造模组以60%脂肪供能的高脂饲料喂养,高脂饲料配方:组成(质量分数):31.6%猪油+25.8%酪蛋白+16.1%麦芽糊精+9.5%蔗糖+6.5%纤维素+6.5%混合矿物质+3.2%大豆油+0.4% L-胱氨酸+0.3%酒石酸氢胆碱+0.1%混合维生素;能量供应:60%脂肪+20%碳水化合物+20%蛋白质;正常饲料即基础生长繁殖饲料,持续12周喂养后,每组随机各取3只小鼠进行肝脏病理学检测,并结合体质量、血脂变化情况评判模型造模结果。小鼠饲料喂养条件不变,继续维持8周实验干预,并将造模成功小鼠随机分为继续高脂膳食饲养(high-fat diet,HFD)组,单一CUR给药干预组(CUR组),单一抗阻运动干预组(RE组),CUR给药和联合运动干预组(CUR_RE组),CUR组和CUR_RE组(训练前0.5 h)以100 mg/kg[15-16]的剂量CUR灌胃,而其余组灌胃等体积生理盐水,1次/日;RE组和CUR_RE组小鼠进行爬梯抗阻训练,其余组则放置于爬梯相同时间,抗阻运动方案参考前人研究方案[17]:采用改良攀爬装置(1.10 m×0.18 m,80°倾斜,横档间距1 cm)进行负重训练,通过尾部配重系统调节负荷。实验前经1周适应性训练后评估最大自主负重能力(maximum voluntary carrying capacity,MVCC):以初始负荷为体质量75%逐次增加5 g配重,当小鼠连续3次未能完成攀爬时,取前次负荷为MVCC。
正式训练包含10轮攀爬(首尾轮无负重作为热身/冷却阶段,第2~9轮采用75% MVCC负荷),攀爬过程中实施标准化触觉刺激引导(臀部轻触≤3 s滞留时促发运动),5 次/周。实验过程RE组和CUR_RE组共排除3只无法完成抗阻训练的小鼠,最终组各纳入10只小鼠用作后续实验分析。于20周实验干预结束后,间隔24 h进行组织取材,具体实验方案如图1 所示。
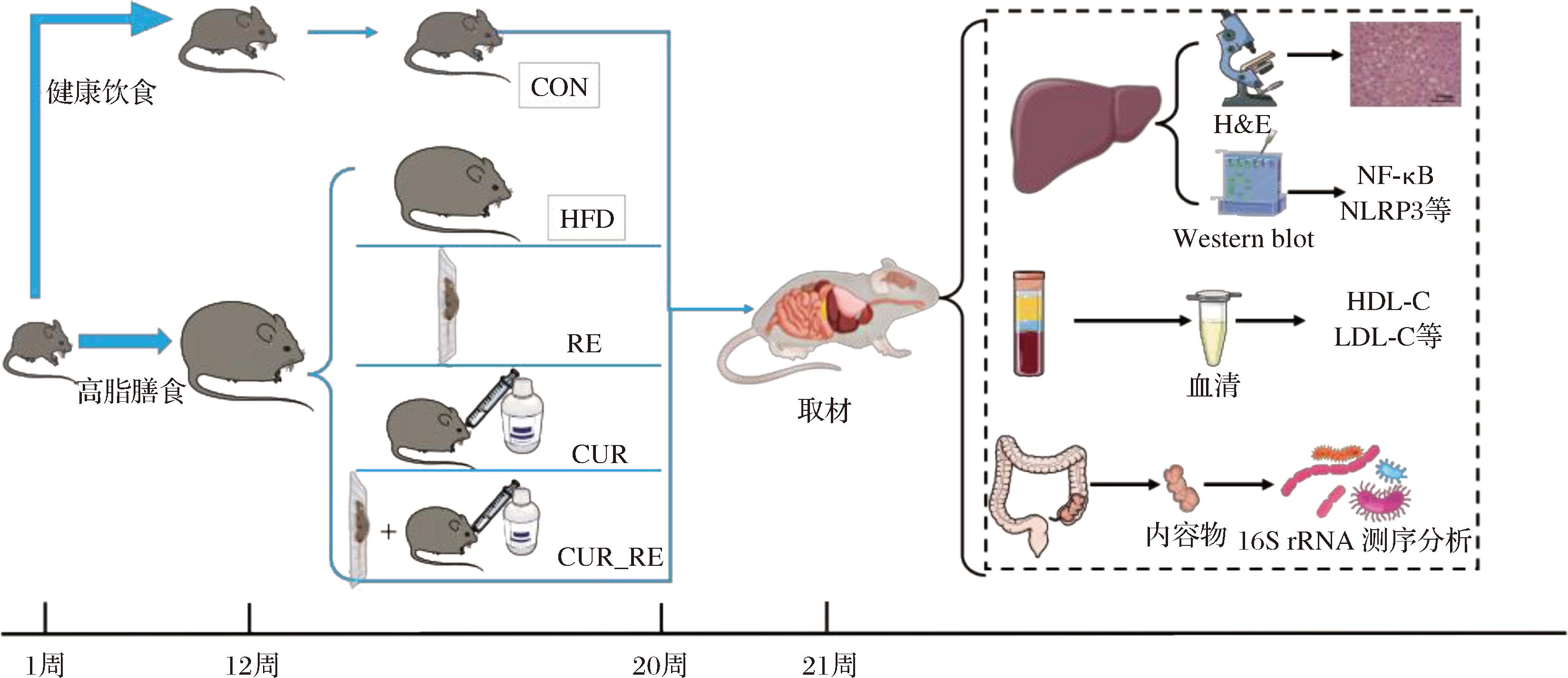
图1 实验流程图
Fig.1 The flowchart of experiment
1.4.2 血清生化分析
实验结束后小鼠禁食过夜,随后将小鼠麻醉后固定于解剖台并进行眼球取血,血液常温静置2 h,离心(4 ℃,1 000 r/min,20 min)处理后取上层血清,采用比色法对血清中肝功能指标(ALT、AST)、血脂(TG、TC、HDL-C、LDL-C)进行检测,检测方法参照相应检测试剂盒说明书进行。
1.4.3 肝脏H&E染色
小鼠麻醉后断颈处死后固定于解剖台,打开胸腔室后迅速将肝脏取出,置于40 g/L多聚甲醛溶液中固定,石蜡包埋后切片,使用二甲苯脱蜡,梯度酒精水化,采用H&E进行染色,梯度乙醇溶液进行脱水处理并用中性树胶封片,使用显微镜进行图像观察、拍照和采集。
1.4.4 Western blot检测
断颈处死小鼠后迅速分离肝脏组织,于-80 ℃速冻保存。称取组织按料液比1∶10(g∶mL)加入RIPA强裂解液,经低温组织研磨仪(60 Hz,60 s)匀浆后,4 ℃ 10 000×g离心10 min获取上清液。采用BCA法进行蛋白定量,与5×SDS-PAGE Loading Buffer混合后95 ℃金属浴变性10 min。使用10%(质量分数)分离胶进行垂直电泳,并采用湿转法将蛋白转移至聚偏二氧乙烯膜。5%(质量分数)脱脂牛奶室温封闭1 h后,依次进行一抗(4 ℃过夜)及二抗(山羊抗兔IgG,体积比1∶5 000,室温1 h)孵育,TBST室温洗膜3次×10 min。滴加ECL化学发光显影液后通过成像仪曝光并拍摄条带,最后通过ImageJ软件分析条带灰度值。
1.4.5 肠道微生物测序和生物信息学分析
小鼠麻醉断颈处死后,使用无菌剪刀和镊子在盲肠的尖部进行横切,确保切口平整且不损伤内容物,立即将盲肠内容物轻轻挤压至提前标记好的抗凝冻存管中。盲肠内容物样本经QIAamp DNA Stool Mini试剂盒提取总DNA后,采用特异性引物338F/806R扩增16S rRNA基因V3~V4区。扩增产物通过Illumina MiSeq PE300平台完成双端测序(测序服务由上海美吉生物医药科技有限公司提供)。原始数据经QIIME1.9.1预处理后,以97%相似度聚类为操作分类单元(operational taxonomic units,OTUs),并通过RDP Classifier算法(置信度阈值0.7)进行物种注释。基于Majorbio云平台完成生物信息学分析,其中:α多样性通过mothur 1.30.2计算多样性指数;β多样性采用Bray-Curtis距离矩阵进行主坐标分析(principal coordinates analysis,PCoA)和非度量多维尺度分析(non-metric multidimensional scaling,NMDS);组间差异菌群通过线性判别分析效应量分析筛选(定线性判别分析>3,P<0.05),鉴定从门到属水平的显著性差异分类单元。
1.5 数据分析
实验结果所有数据以“平均值±标准差”表示,使用Graphpad Prism 8作图,采用SPSS 22.0对实验数据进行统计分析。数据进行方差齐性检验后,单变量分析部分,采用t检验进行两两组间比较;多组间比较采用单因素方差分析。显著性差异为P<0.05,非常显著差异为P<0.01。采用斯皮尔曼相关分析对显著变化的肠道菌群与NAFLD相关指标进行相关性分析。
2 结果与讨论
2.1 12周高脂膳食诱导NAFLD模型的造模结果
由图2-a所示,12周造模后,高脂饲养小鼠血清TC(P<0.05)、TG浓度(P<0.01)较对照组小鼠显著升高;图2-b结果所示,高脂饲养小鼠肝脏可见明显脂肪颗粒;综上,血清TC、TG指标和H&E染色结果表明高脂饲养小鼠已形成高血脂和脂肪肝,即高脂膳食诱导NAFLD小鼠模型造模成功。有研究指出[18],8周高脂膳食可造成小鼠肝脏出现肝细胞脂滴的早期积累,但尚未达到显著的病理改变;但至12周时,HFD诱导的脂质沉积进一步加重,肝细胞体积增大且胞浆内脂滴数量明显增多,肝索排列逐渐紊乱,提示NAFLD已从单纯性肝脂肪变性向脂肪性肝炎逐渐发展,本研究结果支持上述结论。
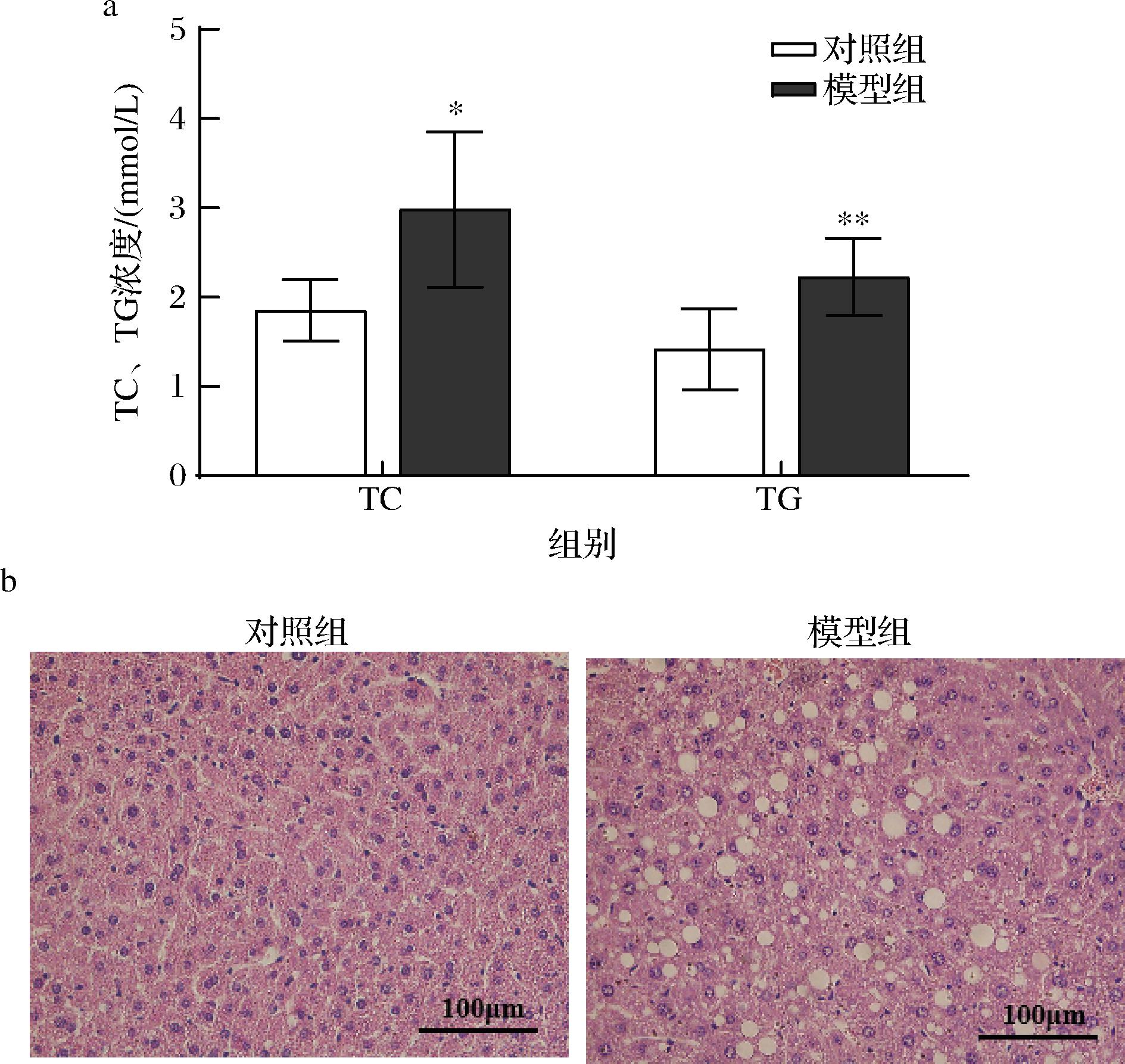
a-TC、TG变化;b-肝脏病理变化
图2 高脂膳食诱导NAFLD模型结果
Fig.2 Results of high-fat diet-induced NAFLD model
注:*代表与CON组比,*P<0.05,**P<0.01。
2.2 不同干预方式对NAFLD小鼠健康指数的影响
如图3所示,HFD组体质量、肝指数、BMI指数和Lee’s指数显著高于CON组(P<0.001);CUR组、CUR_RE组体质量、肝指数、BMI指数和Lee’s指数显著低于HFD组(P<0.05);RE组体质量、肝指数相比与HFD组显著降低(P<0.05),BMI指数和Lee’s指数有一定改善但无明显差异(P>0.05),提示就健康指数而言,联合治疗组的治疗效果优于单一药物治疗或运动干预。
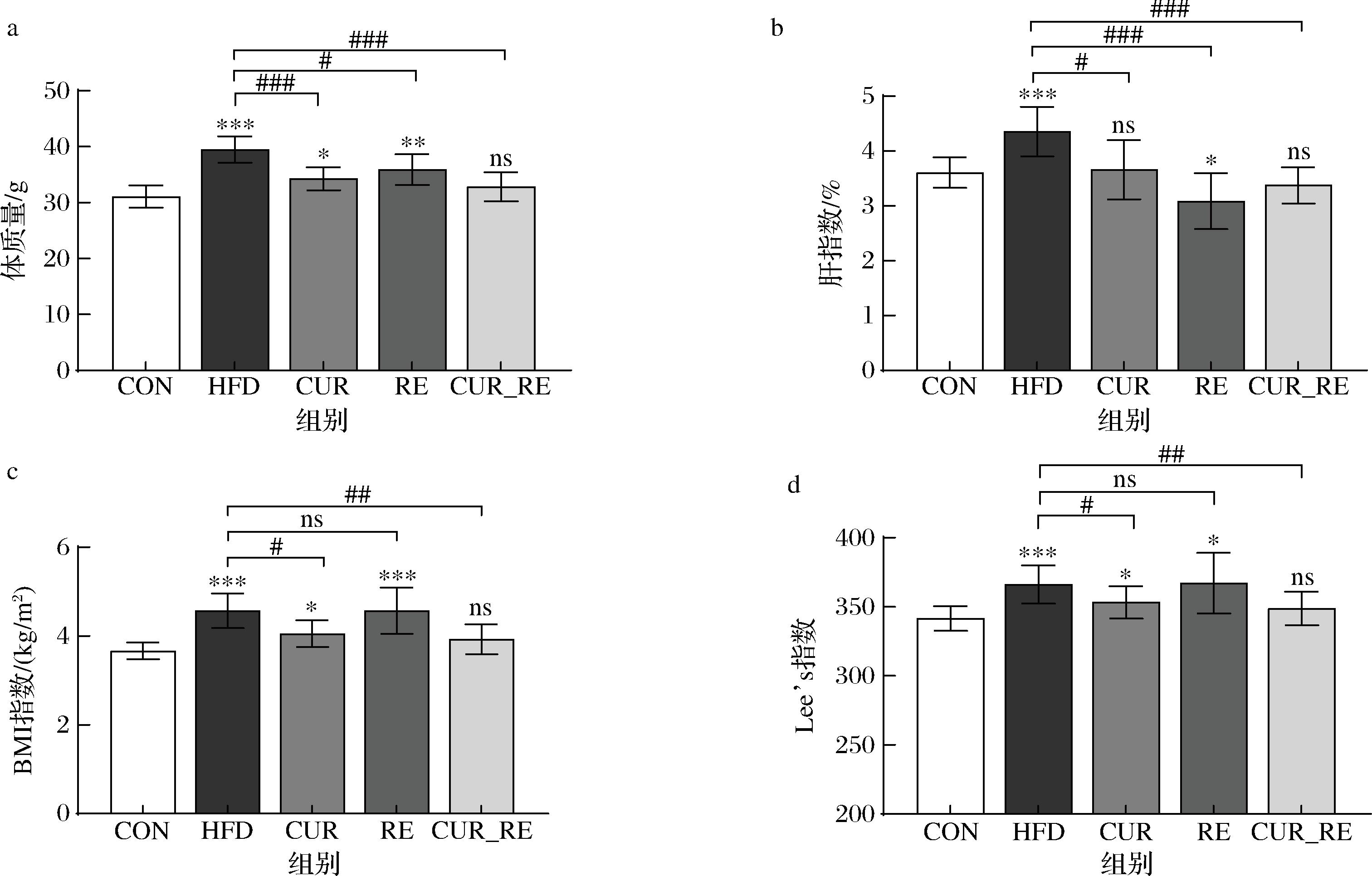
a-体质量;b-肝指数;c-BMI指数;d-Lee’s指数
图3 不同干预方式对NAFLD小鼠健康指数的影响
Fig.3 Effects of different intervention methods on health index of NAFLD mice
注:*代表与CON组比,*P<0.05,** P<0.01,*** P<0.001;#代表与HFD组比,# P<0.05,##P<0.01,###P<0.001;ns代表P>0.05(下同)。
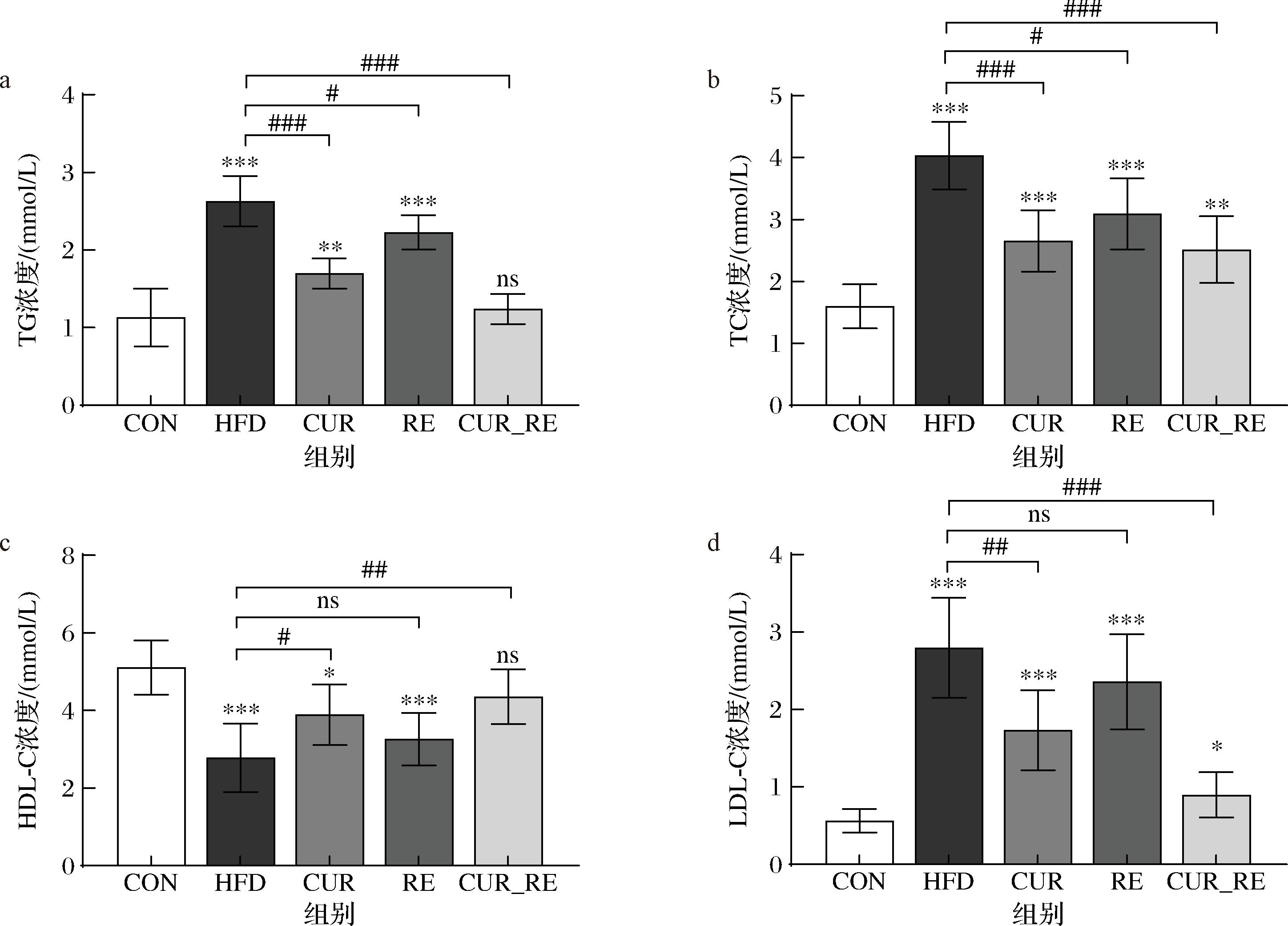
a-TG浓度;b-TC浓度;c-HDL-C浓度;d-LDL-C浓度
图4 不同干预方式对NAFLD小鼠血脂水平的影响
Fig.4 Effects of different intervention methods on lipid levels in NAFLD mice
2.3 不同干预方式对NAFLD小鼠血脂水平的影响
如图4所示,HFD组血清LDL-C、TC、TG含量显著高于CON组(P<0.001);CUR组、CUR_RE组较HFD组血清LDL-C、TC、TG含量显著下调,RE组具有一定效果但无显著差异。血清HDL-C浓度HFD组显著低于CON组(P<0.001),CUR组、CUR_RE组、RE组较HFD组均有所上升,RE组改善效果无显著差异。综上,CUR、CUR_RE、RE均能有效改善高脂饲养所导致的高血脂,其中联合干预效果最显著,能够恢复至CON组相似水平。研究表明[19],CUR能够通过激活AMPK/PPARγ信号通路抑制肝脏脂肪合成并加速脂肪酸β氧化,调节胆汁酸代谢激活法尼醇X受体(farnesoid X receptor,FXR)表达直接调控脂代谢基因表达,增强脂肪组织的产热和褐变能力等机制缓解血脂异常;而RE也可通过上调肝脏中脂肪酸β-氧化基因表达促进游离脂肪酸的分解代谢[14],研究结果进一步证实联合治疗对血脂改善效果更佳。
2.4 不同干预方式对NAFLD小鼠肝脏组织形态和功能的影响
各组别肝组织形态如图5-a所示,CON组肝组织结构完整,无脂肪颗粒沉积;HFD组出现严重肝细胞变性,表现为细胞大小形态不一,部分肝细胞空泡变性;RE组相较HFD组脂质沉积面积显著降低(P<0.05),但有部分脂肪堆积;CUR组、CUR_RE组脂肪沉积改善效果更为明显(P<0.05)。由图5-b、图5-c可知,与CON组相比,HFD组、CUR组、RE组血清中ALT、AST含量显著(P<0.05)升高;与HFD组相比,AST含量无显著差异(P>0.05)RE组CUR组、CUR_RE组ALT显著降低。
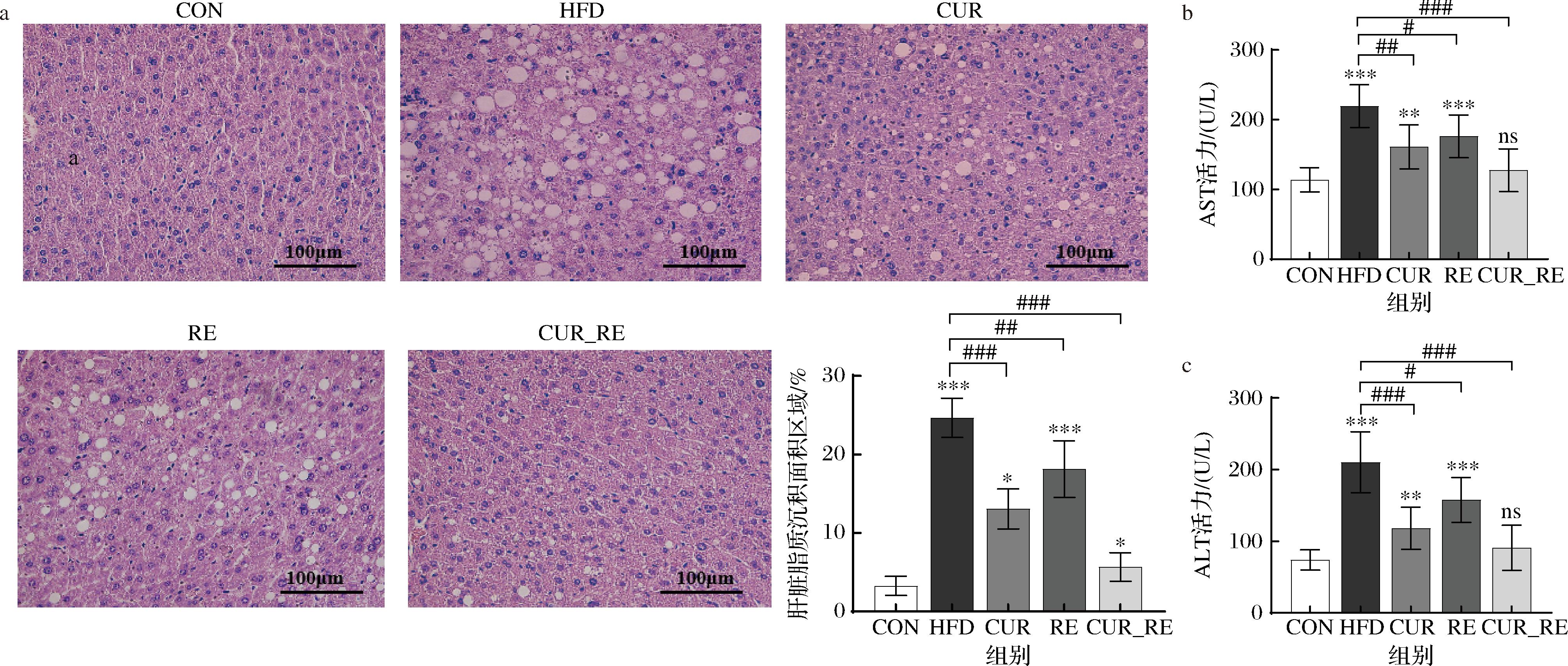
a-肝脏H&E染色及定量分析;b-AST;c-ALT
图5 不同干预方式对NAFLD小鼠肝组织形态和功能的影响
Fig.5 Effects of different intervention methods on the morphology and function of liver tissue in NAFLD mice
结果表明,RE组和CUR组HFD小鼠的肝脏脂肪沉积均得到有效改善,CUR_RE组效果最佳。这与前人研究结果一致,胡戈等[10]也发现联合干预组对于高脂膳食诱导的脂肪肝病理和肝脏功能的改善效果更佳。
2.5 不同干预方式对NAFLD小鼠肝脏炎症信号通路相关蛋白的影响
Western blot实验结果表明(图6),与CON组相比,HFD组NLRP3、NF-κB、IL-1β、TNF-α蛋白表达量显著升高(P<0.05);与HFD组相比,CUR组、CUR_RE组NLRP3、NF-κB、IL-1β、TNF-α蛋白表达量显降低(P<0.05);与HFD组相比,RE组NLRP3蛋白表达量降低但无显著差异(P>0.05),NF-κB、IL-1β、TNF-α蛋白表达量显降低(P<0.05);CUR_RE组NLRP3、NF-κB、IL-1β、TNF-α蛋白表达量与CON组相比均无显著差异(P>0.05)。综合来看,CUR组和CUR_RE组均能有效改善HFD诱导的肝脏炎症反应,且联合干预在抑制炎症方面表现出更显著的效果。已有研究报道称,CUR可通过降低NF-κB p65的磷酸化水平减少其进入细胞核的能力显著下调NF-κB表达[20],以及直接作为NLRP3抑制剂阻断NLRP3的组装和激活[21],本研究结果进一步支持CUR所具备的抗炎能力。然而,RE组的抗炎效果不佳,这可能与持续高强度运动诱发运动性免疫抑制有关。研究指出[22],高强度运动通过激活交感神经-肾上腺髓质轴促使儿茶酚胺(肾上腺素/去甲肾上腺素)和皮质醇大量释放,后者直接抑制淋巴细胞增殖及免疫因子分泌紊乱,造成免疫功能障碍。然而联合治疗组的抗炎效果最好,提示CUR不仅可以直接改善NAFLD病理炎症,在联合运动干预时还能够抑制运动过程中的负面效果(免疫抑制),从而更为有效防治NAFLD。
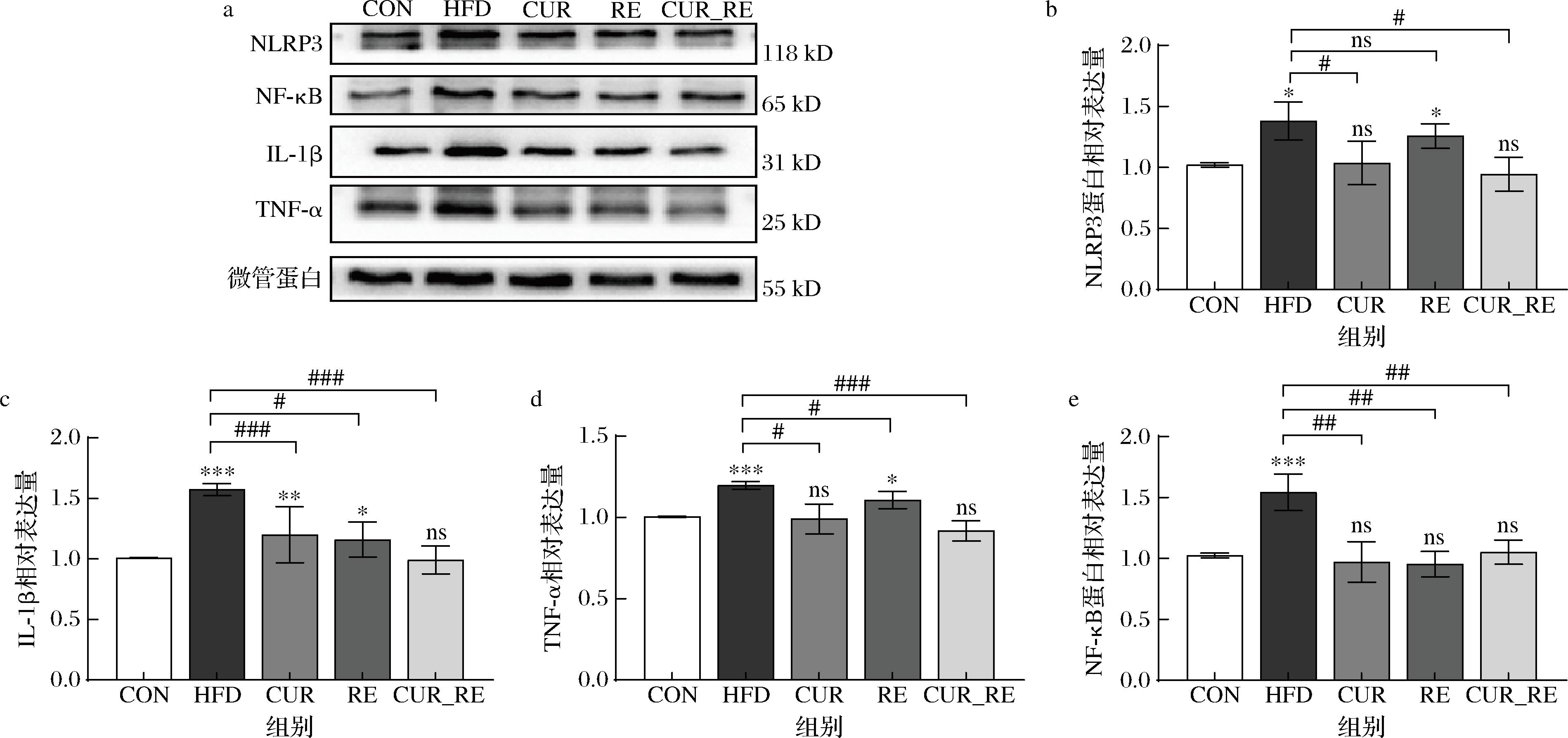
a-WB条带;b-NLRP3表达量;c-IL-1β表达量;d-TNF-α表达量;e-NF-κB表达量
图6 不同干预方式对肝脏炎症信号通路相关蛋白的影响
Fig.6 Effects of different intervention methods on proteins related to liver inflammatory signaling pathways in NAFLD mice
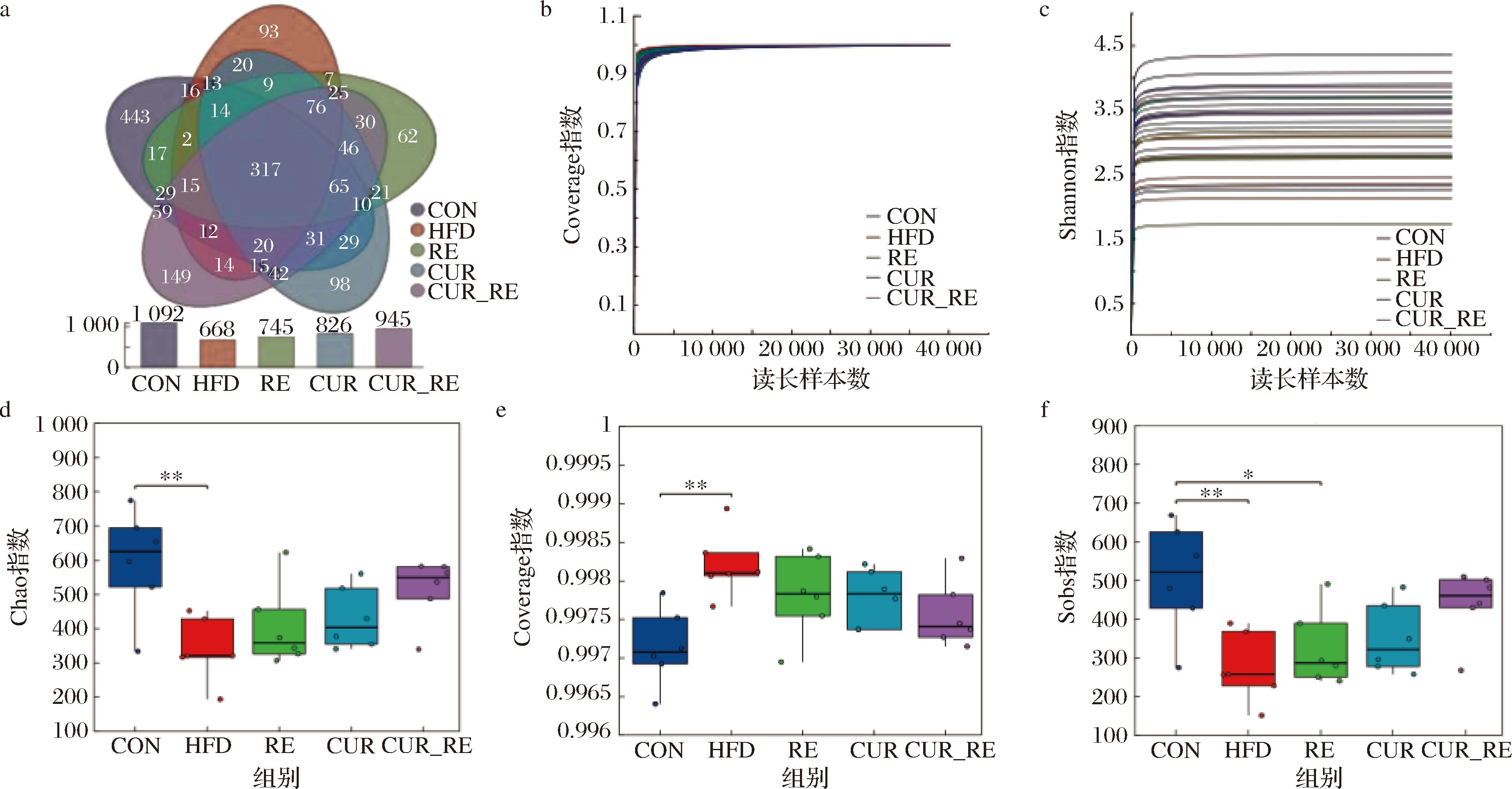
a-Venn图;b-Coverage稀释曲线;c-Shannon稀释曲线;d-Chao组间差异;e-Coverage组间差异;f-Sobs组间差异
图7 不同干预方式对肠道菌群α多样性的影响
Fig.7 Effects of different intervention methods on α diversity of intestinal flora
注:*代表显著性差异,P<0.05,**代表极显著性差异,P<0.01(下同)。
2.6 不同干预方式对NAFLD小鼠肠道菌群的影响
2.6.1 不同干预方式对NAFLD小鼠肠道菌群α多样性的影响
Venn图结果显示(图7-a),5个组别共同包含317个OTUs。α指数是评估肠道菌群物种多样性的有效指标,基于OTUs分析Coverage指数(图7-b)及Shannon指数(图7-c)发现,随着物种数量增加,两指数的稀释曲线趋势均逐渐趋于平缓,表明此次送样样本的群落丰富度、多样性及覆盖度良好,测序深度合理可靠,可充分反映小鼠盲肠内容物中绝大多数肠道微生物信息。组间差异检验结果表明,Chao(P=0.014 6),Coverage(P=0.023 8)和Sob(P=0.018 4)在5个组别中的差异显著;且与CON组相比,HFD组Coverage值极显著增加(P<0.01),Chao值和Sobs值极显著降低(P<0.01),而RE组Sobs值也显著降低(P<0.05)(图7-d~图7-f),研究结果表明HFD组菌群物种多样性显著减少。
2.6.2 不同干预方式对NAFLD小鼠肠道菌群β多样性的影响
β多样性用于评估组间肠道微生物群的组成的相似性和差异性,β多样性分析显示,CON组肠道菌群组成与其他组间存在显著差异。基于Bray-Curtis距离的PCoA和NMDS分析表明,在OTU(PCoA:R=0.445 1,P=0.001;NMDS:R2=0.345 4,P=0.001)和属水平(PCoA:R=0.407 4,P=0.001;NMDS:R2=0.369 6,P=0.001)上,CON组与其他4组显著分离,但其余组样本呈现聚集趋势(图8-a,图8-b,图8-d,图8-e)。门水平上各组群落结构差异均不显著(PCoA:R=0.116,P=0.04;NMDS:R2=0.319,P=0.02)(图8-c,图8-f)。结果说明高脂膳食会造成肠道菌群β多样性在OTU和属水平发生显著改变。
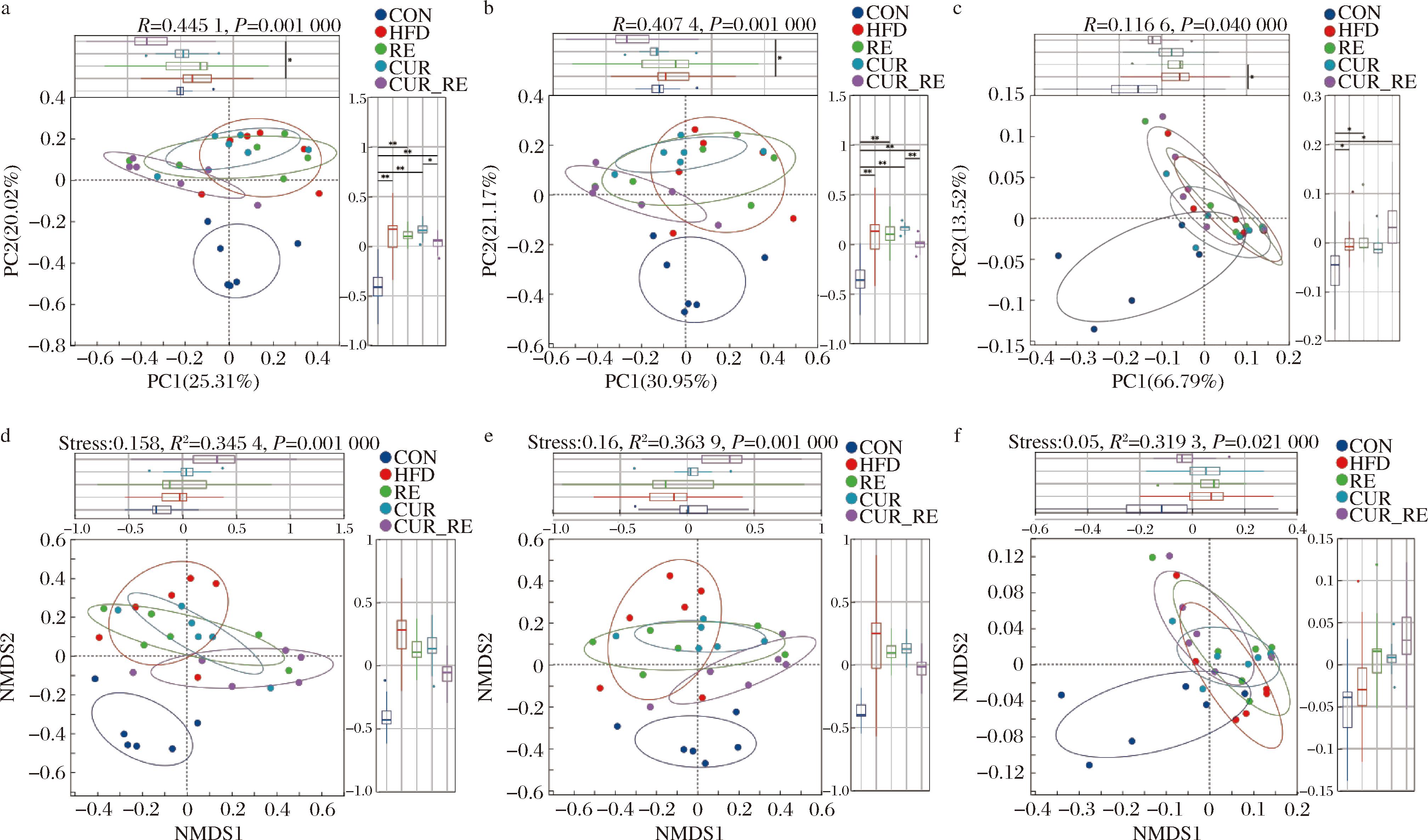
a-OTU水平PcoA分析;b-属水平PcoA分析;c-门水平PcoA分析;d-OTU水平NMDS分析;e-属水平NMDS分析;f-门水平NMDS分析
图8 不同干预方式对肠道菌群β多样性的影响
Fig.8 Effects of different intervention methods on β diversity of gut microbiota
2.6.3 不同干预方式对NAFLD小鼠肠道菌群组成的影响
门水平和属水平的肠道菌群群落分析如图9-a和图9-c所示,在门水平上,Firmicutes、Desulfobacterota、Bacteroidota、Actinobacteriota、Patescibacteria等为优势菌门。Firmicutes/Bacteroidota比值是衡量肠道菌群稳态的重要指标之一[23],其比值升高表明肠道菌群稳态失调,研究结果显示HFD组和RE组F/B比值较CON组极显著升高(P<0.01),前人研究指出Firmicutes主要参与宿主的能量代谢过程,其能够更高效地分解复杂碳水化合物,增加宿主的能量获取效率从而诱导肥胖,而Bacteroidota则与免疫调节相关,高脂膳食通过诱导剧烈的炎症反应影响宿主的免疫系统和肠道屏障功能,间接抑制Bacteroidota生长[24]。而CUR组和CUR_RE组较HFD组显著降低(P<0.05)(图9-b),表明单一CUR、以及联合干预能够改善肠道菌群稳态失衡。在属水平上,Dubosiella、Lactobacillus、unclassified_f__Lachnospiraceae、Faecalibaculum等菌属在所有组别中为优势菌属。其中,Faecalibaculu相对丰度的变化在组间具有显著性差异(P<0.05),具体而言:与CON组相比,HFD组极显著增加(P<0.001),但在3个干预组中其相对丰度均显著降低(P<0.05),其中CUR_AE组极显著降低且恢复至CON组相似水平(P<0.001)。结合门水平和属水平菌群的变化结果,提示联合干预对菌群组成的调节效果最佳(图9-d)。

a-门水平组成;b-F/B比值;c-属水平组成;d-Faecalibaculuc相对丰度组间比较;e-线性判别分析效应量分析
图9 不同干预方式对肠道菌群组成的影响
Fig.9 Effects of different intervention methods on microflora composition
注:*代表与CON组比,*P<0.05,** P<0.01,*** P<0.001;#代表与HFD组比,# P<0.05,##P<0.01,###P<0.001。
利用线性判别分析效应量分析各组丰度显著变化的物种(图9-e),设定线性判别分析值>3。结果发现,HFD组显著富集Faecalibaculum、Coriobacteriaceae_UCG-002、Escherichia-Shigella等菌属;RE组显著富集的菌属为Enterococcus;CUR组显著富集Streptococcus、Staphylococcus、Staphylococcaceae、Leuconostoc等;CUR_RE组显著富集Blautia、Roseburia、Lachnospiraceae_UCG-006等菌属。
2.7 肠道菌群与生理指标,炎症指标的相关性分析
如图10所示,采用Spearman分析对各组小鼠肠道显著富集的菌属与生理指标、炎症指标进行相关性分析。结果发现,Faecalibaculum相对丰度与生理指标中的临床指标(质量,Lee’s,BMI、肝指数)呈显著正相关(r=0.39~0.463,P<0.05),与血脂指标LDL-C、TC、TG呈显著正相关(r=0.501~0.596,P<0.05),但与HDL-C呈显著负相关(r=-0.416 P<0.05),与肝功能指标(AST、ALT)呈显著正相关(r=0.529~0.668,P<0.05);与所有炎症指标呈极显著正相关(r=0.431~0.668,P<0.01)。前已述及,HFD组Faecalibaculum相对丰度显著增加,而CUR、RE、及CUR_RE组显著降低,提示药物或/和运动干预减少Faecalibaculum相对丰度可能与改善外周脂质代谢、降低肝脏炎症反应有关,从而对高脂膳食诱导的脂肪肝发挥保护效益,其中两者联合的作用效果更佳。此外,Lachnospiraceae_NK4A136_group、Desulfovibrio和norank_f_Muribaculaceae相对丰度则与生理指标中的部分临床指标,血脂和肝功能指标呈显著负相关(P<0.05),而与炎症指标NF-κB呈显著负相关(P<0.05),已有研究证实三者与维持肠道屏障完整性和免疫系统稳态密切相关[25-26],本研究结果进一步支持三者作为益生菌在改善脂代谢紊乱中发挥一定的抗炎作用。
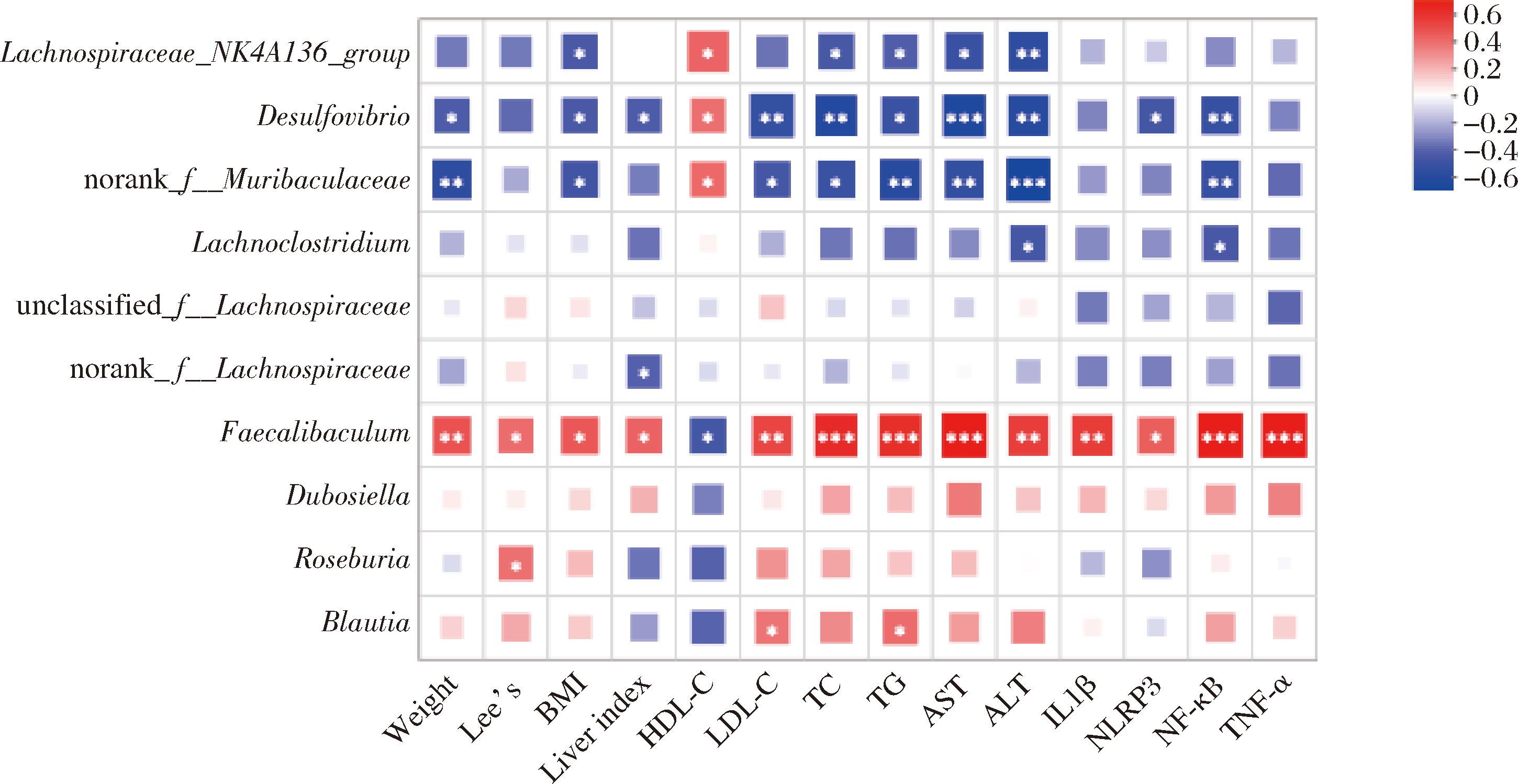
图10 肠道菌群与代谢指标、炎症指标相关性
Fig.10 Correlation between gut microbiota and physiological and inflammatory indicators
注:*代表有显著性差异,*P<0.05,** P<0.01,*** P<0.001。
3 结论
综上所述,本研究采用单一CUR、RE、以及两者联合干干预,探讨了不同干预手段对高脂膳食诱导NAFLD的改善作用和肠道菌群的影响。单一CUR能降低体质量、肝指数、血脂和肝脏脂肪沉积,抑制炎症信号蛋白表达;单一RE干预在降低体质量和肝指数上有效,但对血脂和肝脏脂肪沉积的调节及抗炎作用较弱;两者联合干预不仅在降低体质量、肝指数、血脂和肝脏脂肪沉积上优于单干预组,且抑制炎症信号蛋白表达更为有效。高脂膳食导致Faecalibaculum相对丰度在HFD组中显著增加,其相对丰度与代谢紊乱生理指标和炎症指标呈显著正相关,但CUR、CUR联合RE干预均显著降低其相对丰度,提示在不同干预手段下肠道菌群的变化可能与NAFLD改善效果存在一定的关联。然而,目前的证据尚不足以直接证明肠道菌群在干预机制中的核心作用。本研究证实CUR联合RE干预能够通过协同互作机制更为有效地缓解NAFLD,为临床多模式治疗提供新策略,但肠道菌群与炎症之间的直接因果关系尚且不知,未来的研究可通过粪菌移植或菌株定植实验进一步解析菌群代谢物对炎症通路的靶向调控作用。
[1] WANG S D,YIN J H,LIU Z J,et al.Metabolic disorders,inter-organ crosstalk,and inflammation in the progression of metabolic dysfunction-associated steatotic liver disease[J].Life Sciences,2024,359:123211.
[2] GU Y,GUO C N,LIU Z Q,et al.The trend in incidence of non-alcoholic fatty liver disease and its impact on cirrhosis and liver cancer:An analysis from Global Burden of Disease 2021[J].Public Health,2025,242:79-86.
[3] WAYAL V,WANG S D,HSIEH C C.Novel bioactive peptides alleviate Western diet-induced MAFLD in C57BL/6 J mice by inhibiting NLRP3 inflammasome activation and pyroptosis via TLR4/NF-κB and Keap1/Nrf2/HO-1 signaling pathways[J].International Immunopharmacology,2025,148:1141177.
[4] ZHOU M,LV J Y,CHEN X L,et al.From gut to liver:Exploring the crosstalk between gut-liver axis and oxidative stress in metabolic dysfunction-associated steatotic liver disease[J].Annals of Hepatology,2025,30(1):101777.
[5] ZHANG H J,KANG R,SONG T C,et al.Advances in relieving exercise fatigue for curcumin:Molecular targets,bioavailability,and potential mechanism[J].Journal of Food Science,2024,89(8):4604-4619.
[6] HANDU D,STOTE K,PIEMONTE T.Evaluating bioactive-substance-based interventions for adults with MASLD:Results from a systematic scoping review[J].Nutrients,2025,17(3):453.
[7] SHAN X M,XU X Y,WANG L J,et al.Dietary curcumin supplementation attenuates hepatic damage and function abnormality in a chronic corticosterone-induced stress model in broilers[J].The Journal of Steroid Biochemistry and Molecular Biology,2024,243:106579.
[8] HONG T,JIANG X,ZOU J,et al.Hepatoprotective effect of curcumin against bisphenol A-induced hepatic steatosis via modulating gut microbiota dysbiosis and related gut-liver axis activation in CD-1 mice[J].The Journal of Nutritional Biochemistry,2022,109:109103.
[9] RONG L,ZOU J Y,RAN W,et al.Advancements in the treatment of non-alcoholic fatty liver disease (NAFLD)[J].Frontiers in Endocrinology,2022,13:1087260.
[10] 胡戈,秦菲,曹建民,等.姜黄素复合有氧运动对非酒精性脂肪肝大鼠肝功能的改善作用[J].食品科学,2025,46(10):178-187.HU G,QIN F,CAO J M,et al.Effect of curcumin combined with aerobic exercise on liver function in rats with nonalcoholic fatty liver disease[J].Food Science,2025,46(10):178-187.
[11] YANG J,ZOU J,MAI H Y,et al.Curcumin protects against high-fat diet-induced nonalcoholic simple fatty liver by inhibiting intestinal and hepatic NPC1L1 expression via down-regulation of SREBP-2/HNF1α pathway in hamsters[J].The Journal of Nutritional Biochemistry,2023,119:109403.
[12] 王丽,吉喆,周海涛,等.姜黄素联合有氧运动对高脂饮食大鼠肠道菌群调节作用研究[J].营养学报,2022,44(5):498-504.WANG L,JI Z,ZHOU H T,et al.Combined effects of curcumin and aerobic exercise on intestinal microflora in rats fed a high fat diet[J].Acta Nutrimenta Sinica,2022,44(5):498-504.
[13] NIKROO H,HOSSEINI S R A,FATHI M,et al.The effect of aerobic,resistance,and combined training on PPAR-α,SIRT1 gene expression,and insulin resistance in high-fat diet-induced NAFLD male rats[J].Physiology &Behavior,2020,227:113149.
[14] DAMASCENO DE LIMA R,FUDOLI LINS VIEIRA R,ROSETTO MU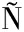 OZ V,et al.Time-restricted feeding combined with resistance exercise prevents obesity and improves lipid metabolism in the liver of mice fed a high-fat diet[J].American Journal of Physiology.Endocrinology and Metabolism,2023,325(5):E513-E528.
OZ V,et al.Time-restricted feeding combined with resistance exercise prevents obesity and improves lipid metabolism in the liver of mice fed a high-fat diet[J].American Journal of Physiology.Endocrinology and Metabolism,2023,325(5):E513-E528.
[15] PENG X Y,DAI C S,LIU Q W,et al.Curcumin attenuates on carbon tetrachloride-induced acute liver injury in mice via modulation of the Nrf2/HO-1 and TGF-β1/Smad3 Pathway[J].Molecules,2018,23(1):215.
[16] 颜惠敏,吕欣晨,宋雯燕,等.姜黄素调控肠道菌群及其代谢物提高小鼠运动表现[J].2025,51(8):37-44.YAN H M,LV X C,SONG W Y,et al.Curcumin modulates gut microbiota and its metabolites to improve exercise performance in mice[J].Food and Fermentation Industries,2025,51(8):37-44.
[17] HORNBERGER T A Jr,FARRAR R P.Physiological hypertrophy of the FHL muscle following 8 weeks of progressive resistance exercise in the rat[J].Canadian Journal of Applied Physiology,2004,29(1):16-31.
[18] 余晨歌,黄晶,席艳,等.单纯高脂饮食诱导2型糖尿病小鼠模型的构建及病理改变的评价[J].生理学报,2024,76(3):385-393.YU C G,HUANG J,XI Y,et al.Construction of a mouse model of type 2 diabetes induced by high fat diet alone and evaluation of pathological changes[J].Acta Physiologica Sinica,2024,76(3):385-393.
[19] SERVIDA S,PIONTINI A,GORI F,et al.Curcumin and gut microbiota:A narrative overview with focus on glycemic control[J].International Journal of Molecular Sciences,2024,25(14):7710.
[20] FENG D,ZOU J,SU D F,et al.Curcumin prevents high-fat diet-induced hepatic steatosis in ApoE-/- mice by improving intestinal barrier function and reducing endotoxin and liver TLR4/NF-κB inflammation[J].Nutrition &Metabolism,2019,16:79.
[21] YIN H P,GUO Q,LI X,et al.Curcumin suppresses IL-1β secretion and prevents inflammation through inhibition of the NLRP3 inflammasome[J].The Journal of Immunology,2018,200(8):2835-2846.
[22] MOIR H,HUGHES M G,POTTER S,et al.Exercise-induced immunosuppression:Roles of reactive oxygen species and 5′-AMP-activated protein kinase dephosphorylation within immune cells[J].Journal of Applied Physiology,2010,108(5):1284-1292.
[23] LIU Y,JIN Y,LI J,et al.Small bowel transit and altered gut microbiota in patients with liver cirrhosis[J].Frontiers in Physiology,2018,9:470.
[24] STOJANOV S,BERLEC A,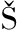 TRUKELJ B.The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J].Microorganisms,2020,8(11):1715.
TRUKELJ B.The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J].Microorganisms,2020,8(11):1715.
[25] LI Y,CHEN G H,HU X H,et al.Assessing causal relationships between gut microbiota and psoriasis:evidence from two sample Mendelian randomization analysis[J].Scientific Reports,2024,14:8831.
[26] YAN C,HUANG S H,DING H F,et al.Adverse effect of oxidized cholesterol exposure on colitis is mediated by modulation of gut microbiota[J].Journal of Hazardous Materials,2023,459:132057.