便秘是一种现代社会中普遍存在的生理问题,主要表现为排便频率降低和排便困难,其根本原因在于粪便中水分含量不足[1]。受工作压力及生活方式等因素影响,约70%的人群处于亚健康状态,其中以胃肠道功能紊乱最为常见,而便秘则是这一群体中普遍存在的症状。长期便秘可能导致结肠过度扩张,进而影响其正常的蠕动功能。当便秘发生时,肠道传输时间延长,可能导致肠道内有害菌群过度繁殖,同时有益菌群比例下降,最终影响肠道微生态平衡[2]。作为人体重要的排毒器官,肠道功能的异常可能导致毒素蓄积,进而影响其他器官的正常运作,慢性便秘与多种疾病风险增加密切相关,包括炎症性肠病和结直肠癌等[3]。通过摄入功能性食品来改善身体状况和生理功能,已成为帮助亚健康人群恢复健康的重要途径。因此,这种方法目前被广泛认为是维护和增强肠道健康的有效策略[4]。
益生菌作为一类对宿主健康具有多重益处的微生物,在改善和维持肠道微环境方面发挥着重要作用,对缓解便秘症状具有显著的干预效果[5]。其作用机制主要包括:通过竞争性排斥病原体、分泌抗菌物质以及调节肠道pH值等方式,促进有益菌群的增殖,同时抑制有害菌的生长[6]。此外,益生菌能够代谢产生短链脂肪酸,特别是丁酸,这种物质不仅能够增强肠道蠕动,还能刺激平滑肌收缩,从而加速肠道内容物的传输,有效缓解便秘[7]。益生菌对肠道动力学的整体调节也具有重要意义,它们能够通过调控胃肠道的运动功能包括激活肠神经系统以及增强肠道的感觉和运动反应来改善肠道功能。值得注意的是,肠道是多种调节胃肠道运动和反应的激素的重要来源,而益生菌可能通过影响这些激素的分泌,进而对排便功能产生调节作用[8]。
乳果糖作为一种广泛应用于慢性功能性便秘治疗的药物,其作用机制主要通过增加肠道内水分含量和刺激肠道动力来促进排便。由于其不被人体吸收的特性,乳果糖具有较高的安全性[9]。低纤维膳食能够导致粪便体积和含水量的降低、肠道蠕动减缓、菌群平衡破坏等多种负面情况的发生,最终导致便秘,以低纤维膳食饲养小鼠也能诱导便秘,且与人体由于不良生活饮食习惯导致便秘的情况接近,因此被用于实验性便秘的研究[10]。新疆阿勒泰地区草场丰茂,畜牧资源丰富,人口除汉族外,还有维吾尔族、哈萨克族、蒙古族等36个少数民族,多民族混居造就独特的饮食习惯,当地牧民喜食自然发酵酸奶,阿勒泰地区牧民酸奶缺乏科学研究,对酸奶中的微生物也研究不足。本研究旨在探究鼠李糖乳酪杆菌AFY01(Lacticaseibacillus rhamnosus AFY01,LR-AFY01)对低纤维膳食诱导的便秘的干预效果。通过动物实验,本研究系统评估了LR-AFY01对肠道动力学的影响,并深入分析了其在调节肠道菌群、增强肠道蠕动能力以及维持肠壁屏障功能等方面的潜在作用。本研究从肠道微生物学的视角出发,致力于推动便秘调节机制的深入研究,期望为便秘患者提供一种创新的治疗策略,以改善其治疗效果和临床预后。
1 材料与方法
1.1 材料与试剂
本研究团队2022年8月采集新疆阿勒泰地区牧民自制自然发酵酸奶,吸取40 mL自然发酵酸奶放入无菌离心管中,置于4 ℃食品采样箱内,再转运至实验室4 ℃冰箱保存备用。
本研究采用雌性无特定病原体(specific pathogen free,SPF)级昆明小鼠作为实验对象,小鼠6周龄,体重(22±2) g。实验动物由湖南斯莱克景达实验动物有限公司提供,该公司持有实验动物生产许可证,编号为SYXK(湘)2024-0019。本实验已获得重庆第二师范学院重庆市功能性食品协同创新中心实验动物伦理委员会的批准,伦理审查编号为202502003B。本研究的所有动物实验程序均遵循3R原则,全程严格遵循国家标准GB/T 35892—2018《实验动物福利伦理审查指南》以及《赫尔辛基宣言》的相关规定,确保实验动物福利和伦理要求得到充分保障。
低纤维膳食,参考易若琨等[11]的方法制备小鼠饲料,重庆腾鑫生物技术有限公司。
细胞因子肿瘤坏死因子-α(tumor necrosis factor-alpha,TNF-α)、干扰素-γ(interferon-gamma,IFN-γ)、白细胞介素-6(interleukin-6,IL-6)、白细胞介素-10(interleukin-10,IL-10)、超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)、谷胱甘肽过氧化物酶(glutathione per oxidase,GSH-Px)、丙二醛(malondialdehyde,MDA)、血清胃动素(motilin,MTL)、内皮素-1(endothelin-1,ET-1)、血管活性肠肽(vasoactive intestinal peptide,VIP)、乙酰胆碱酯酶(acetylcholinesterase,AchE)、P物质(substance P,SP)、生长抑素(somatostatin,SS)检测试剂盒,上海酶联生物科技有限公司;苏木精-伊红(hematoxylin and eosin,H&E)染色液,长沙艾碧维生物科技有限公司;TriQuick Reagent总RNA提取试剂、TaqMan One Step RT-qPCR Kit、猪胆盐,北京索莱宝科技有限公司;PCR引物,美国赛默飞公司。双歧杆菌、肠球菌胆汁七叶苷叠氮钠、Man-Rogosa-Sharp (MRS)、伊红美蓝(eosin methylene blue,EMB)、山梨醇麦康凯(sorbitol MacConkey,SMAC)培养基,北京陆桥技术股份有限公司;细菌基因组DNA提取试剂盒,天根生化科技(北京)有限公司;巯基乙酸钠,惠兴生化试剂有限公司;胃蛋白酶,天津市众联化学试剂有限公司;活性炭,天津市大茂化学试剂厂。
1.2 仪器与设备
BI-150A 生化培养箱,施都凯仪器设备(上海)有限公司;Biomate3S 紫外可见分光光度计、Stepone Plus定量PCR仪,美国赛默飞公司;BX43正置显微镜,日本奥林巴斯公司。
1.3 方法
1.3.1 菌株的分离纯化
准确量取1 mL自然发酵酸奶样品,使用无菌生理盐水进行10倍梯度稀释,直至稀释度为10-6。随后,选取10-4、10-5、10-6三个稀释梯度的菌液各100 μL,分别进行平板涂布。将涂布平板置于37 ℃恒温培养箱中培养48 h,期间密切观察并详细记录菌落的形态特征。培养结束后,从平板上挑选具有不同形态特征的菌落,进行划线分离操作。将划线后的平板再次置于37 ℃恒温培养箱中培养48 h。培养完成后,再次挑选板上不同形态的单菌落进行划线分离。重复上述划线分离步骤2~3次,直至获得形态特征完全一致的纯单菌落。
1.3.2 菌株DNA提取
将经过纯化处理的疑似目标菌株接种于MRS肉汤培养基中,置于37 ℃恒温培养箱中培养24 h。培养结束后,采用细菌基因组DNA提取试剂盒,按照标准操作流程进行DNA提取。提取完成后,对获得的DNA样品进行编号,并妥善保存于-20 ℃低温冰柜中,以备后续实验使用。
1.3.3 菌株基因组DNA的PCR扩增及检测
对提取的菌株DNA进行PCR扩增,反应体系:上游引物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)1 μL,下游引物1495R(5′-CTACGGCTACCTTGTTACGA-3′)1 μL,2 × Taq plus Buffer 12.5 μL,模板DNA 1 μL,用无菌ddH2O补足至25 μL。同时,以无菌超纯水替代模板DNA作为阴性对照。PCR扩增程序设置为:94 ℃预变性5 min;随后进行29个循环,每个循环94 ℃变性30 s、55 ℃退火30 s、72 ℃延伸1 min;最后72 ℃延伸5 min。扩增完成后,取5 μL PCR产物进行琼脂糖凝胶电泳检测,琼脂糖质量分数为1.5%,电泳条件为110 V、45 min。电泳检测,将PCR产物送至深圳华大基因股份有限公司进行测序。测序获得的序列使用NCBI数据库中的BLAST(basic local alignment search tool)程序进行比对分析,以确定目标菌株的种属信息。
1.3.4 菌株耐受0.3%胆盐能力检测
在含0.2%巯基乙酸盐的MRS(MRS broth with thioglycollate,MRS-THIO)培养基中加入猪胆盐,使其终浓度达到0.3%,随后在121 ℃条件下高压灭菌15 min。将活化后的5 mL菌液以2%(体积分数)的接种量分别接种至不含胆盐的MRS-THIO培养基和含0.3%胆盐的MRS-THIO培养基中,同时以未接种菌液的MRS-THIO培养基作为空白对照。将接种后的培养基置于37 ℃恒温培养箱中培养24 h。培养结束后,测定不同胆盐浓度培养基的OD600值,并按照公式(1)计算菌株对胆盐的耐受力[11]:
胆盐耐受能力![]()
(1)
式中:OD1, 含0.3%胆盐培养基OD600值;OD2,不含胆盐培养基OD600值;OD0, 空白培养基OD600值。
1.3.5 菌株耐受人工胃液能力检测
实验用人工胃液由0.2% NaCl和0.35%胃蛋白酶(质量分数)组成,使用1 mol/L HCl溶液将配制好的人工胃液pH调至3.0,随后用0.22 μm膜过滤除菌。然后在超净工作台中,取5 mL培养好的含菌培养基于10 mL无菌离心管中,以3 000 r/min离心10 min,弃去上清液并收集菌体。向菌体中加入等体积(5 mL)无菌生理盐水,充分混制成菌悬液。取1 mL菌悬液与9 mL pH 3.0的人工胃液混合,立即取1 mL混合液作为人工胃液处理0 h的样品。剩余9 mL混合液置于恒温水浴摇床(37 ℃,150 r/min)中培养3 h。分别对0 h和3 h时的样品进行10倍梯度稀释,选择合适稀释梯度采用平板涂布法测定活菌数。将涂布后的MRS固体培养基置于37 ℃培养箱中培养48 h,按公式(2)计算菌株在人工胃液中的存活率[11]:
存活率![]()
(2)
1.3.6 低纤维膳食小鼠便秘模型
将100只昆明小鼠随机均分为5组:正常组、低纤维膳食便秘(low-fiber diet,LFD)组、LFD+乳果糖组(阳性对照组)、LFD+LR-AFY01L组(LR-AFY01L低浓度剂量组)、LFD+LR-AFY01H组(LR-AFY01H高浓度剂量组)。正常组小鼠给予普通饲料,其余各组小鼠给以低纤维饲料,持续5周,LFD组小鼠每日排便颗粒数低于正常组50%即为造模成功。然后LFD+乳果糖组小鼠每日灌胃给予1次剂量为1.5 g/kg的乳果糖,LFD+LR-AFY01L组和LFD+LR-AFY01H组每日分别灌胃给予1次剂量为1×108 CFU/kg 和1×109 CFU/kg的LR-AFY01菌悬液,持续1周。随后,每组20只小鼠均分为2部分:10只小鼠用于观察灌胃100 g/L活性炭冰水溶液(灌胃剂量0.1 mL/10 g)小鼠首次排出黑粪所需时间,所有小鼠排出黑便后通过颈椎脱臼法处死小鼠后采用眼眶取血和解剖取结肠组织进行后续实验,另外10只小鼠同样灌胃0.1 mL/10 g 的10%活性炭冰水溶液,30 min后通过颈椎脱臼法处死,仅用于测定活性炭在小肠内的推进距离。小肠推进率按公式(3)计算[10-11]:
小肠推进率![]()
(3)
1.3.7 小鼠血清生物活性物质和神经递质测定
将小鼠血液进行离心处理10 min(4 500 r/min)后收集上清液,获得血清。按试剂盒使用说明书检测小鼠血清中MTL、VIP、AchE、SP、ET-1、SS的水平。
1.3.8 小鼠结肠组织氧化相关因子和炎症细胞因子测定
取0.1 g小鼠结肠,加入0.9 mL生理盐水中进行匀浆, 4 500 r/min离心分离10 min,去上清液按试剂盒使用说明书检测小鼠结肠组织中氧化相关因子SOD、CAT、GSH-Px、MDA和炎症细胞因子TNF-α、IFN-γ、IL-6、IL-10的水平。
1.3.9 小鼠结肠组织氧化相关因子和炎症细胞因子测定
取0.1 g小鼠结肠,加入0.9 mL生理盐水中进行匀浆,然后在 4 500 r/min下离心分离10 min,去除上清液,按试剂盒使用说明书检测小鼠结肠组织中氧化相关因子SOD、CAT、GSH-Px、MDA和炎症细胞因子TNF-α、IFN-γ、IL-6、IL-10的水平。
1.3.10 小鼠组织的病理学检测
解剖小鼠后取出0.5 cm结肠后将其固定于10%甲醛溶液中24 h。随后,将组织置于95%乙醇中进行脱水处理,再以二甲苯浸泡组织块以置换乙醇,使组织透明化。接下来,将透明化的组织块包埋于熔融石蜡中完成浸润,并使用切片机进行切片。对获得的肠组织切片进行H&E染色,制备成病理切片。最后,在显微镜下观察组织染色后的病理学结果。
1.3.11 小鼠结肠组织的mRNA表达测定
取约50 mg小鼠结肠组织,剪切成小块,按1.3.8节方法匀浆后,加入1 mL TriQuick Reagent,充分搅拌至完全裂解。接着向样品中加入三氯甲烷,充分混匀后,于4 ℃条件下以3 000 r/min冷冻离心15 min。取上清液,加入等体积异丙醇,混匀后再次在4 ℃、3 000 r/min条件下冷冻离心20 min。弃去上清液,用75%乙醇洗涤沉淀,随后在4 ℃、3 000 r/min条件下冷冻离心15 min,弃去上层水相。静置3~5 min后,加入20 μL RNase-Free water溶解沉淀,备用。将RNA原液与RNase-Free water按体积比1∶49稀释混匀,使用微量分光光度计测定RNA的浓度和纯度。若测得的A260/A280比值在1.8~2.0之间,则表明RNA纯度符合实验要求,将RNA浓度调整至1 μg/μL。按照TaqMan One Step RT-qPCR试剂盒说明书,向反应体系中加入4 μL RNA溶液及上下游引物各5 μL(表1),配制50 μL反应体系。将反应体系置于PCR仪中进行扩增,反应条件如下:95 ℃初始变性5 min,随后进行40个循环,每个循环包括95 ℃ 10 s、60 ℃ 20 s和72 ℃ 20 s。实验以β-肌动蛋白(β-actin)作为内参基因,采用2-ΔΔCT法计算各目的基因mRNA的相对表达量[12]。
表1 小鼠结肠组织中基因表达检测用PCR引物序列
Table 1 PCR primer sequence for gene expression detection in mouse colonic tissue

基因表达上游引物序列下游引物序列TPH15′-CCATCTTCCGAGAGCTAAACAAA-3′5′-TCTTCCCGATAGCCACAGTATT-3′SLC6A45′-CTCCGCAGTTCCCAGTACAAG-3′5′-CACGGCATAGCCAATGACAGA-3′HTR3a5′-TCCTGAGGACTTCGACAATGT-3′5′-CCCCACGTCCACAAACTCAT-3′HTR45′-TCTGGATGTCCTACTTACCACAG-3′5′-GCAGCAGATGGCGTAATACCT-3′β-catenin5′-ATGGAGCCGGACAGAAAAGC-3′5′-TGGGAGGTGTCAACATCTTCTT-3′WNT3A5′-CTCCTCTCGGATACCTCTTAGTG-3′5′-CCAAGGACCACCAGATCGG-3′AMPKα15′-GTCAAAGCCGACCCAATGATA-3′5′-CGTACACGCAAATAATAGGGGTT-3′mTOR5′-CAGTTCGCCAGTGGACTGAAG-3′5′-GCTGGTCATAGAAGCGAGTAGAC-3′AQP35′-CCTTGGCATCTTGGTGGCT-3′5′-AGGAAGCACATTGCGAAGGT-3′AQP85′-ACACCAATGTGTAGTATGGACCT-3′5′-TGACCGATAGACATCCGATGAAG-3′β-actin5′-CATGTACGTTGCTATCCAGGC-3′5′-CTCCTTAATGTCACGCACGAT-3′
1.3.12 小鼠肠道内容物中微生物分析
称取小鼠肠道内容物约0.5 g,加入4.5 mL无菌生理盐水,充分振荡混匀后静置5 min。取上清液进行10倍梯度稀释,直至稀释度为10-6。将各梯度稀释液分别接种至相应培养基上,双歧杆菌接种至双歧杆菌培养基上厌氧环境下37 ℃培养48 h,乳杆菌接种至MRS培养基上需氧环境下37 ℃培养48 h,肠球菌接种至肠球菌胆汁七叶苷叠氮钠培养基上需氧环境下37 ℃培养24 h,肠杆菌接种至EMB培养基上需氧环境下37 ℃培养24 h,产气荚膜梭菌接种至SMAC培养基上厌氧环境下37 ℃培养24 h。培养结束后,进行菌落平板计数,计算单位质量粪便中各菌落的数量(CFU/g)。
1.4 数据统计学分析
所有实验均设置3次平行重复,结果以“平均值±标准偏差”表示。此外,采用单因素方差分析(ANOVA)对各组数据间的差异进行统计学评估,显著性水平设定为P<0.05。
2 结果与分析
2.1 分离菌株的种属及体外抗性
从自然发酵酸奶中分离出一株微生物,经BLAST程序比对分析表明,该菌株与 GenBank 数据库中已知鼠李糖乳酪杆菌(GenBank 登录号:CP053619.1)的同源性均达100%。该菌株在pH 3.0人工胃液中的存活率达到(94.27±3.46)%,同时在0.3%胆盐中的存活率也达到(86.19±2.86)%,具有非常好的体外抗性。研究显示,益生菌要进入人体肠道定殖,需具备良好的抗胃酸和胆盐能力,实验室条件下体外抗人工胃酸和胆盐的检测能够有效的模拟体内的情况,初步判断菌株是否具有益生菌潜质[11]。本研究中分离坚定出的鼠李糖乳酪杆菌初步具备益生菌的潜质,被命名LR-AFY01,已被保存于中国微生物菌种保藏管理委员会普通微生物中心,菌种保藏编号为CGMCC No.27362,被用于后续研究。
2.2 便秘小鼠首次排出黑色粪便颗粒时间和活性炭推进率
由图1可知,小鼠24 h禁食后灌胃活性炭水,正常组小鼠排粪时间最短,为(57±5)min;而LFD组排粪时间显著延长至(169±11)min(P<0.05)。为验证实验方法的可靠性,本研究选用临床治疗便秘的有效药物乳果糖作为阳性对照,与LFD组相比,乳果糖(LFD+乳果糖组)干预显著(P<0.05)缩短了小鼠的排黑粪时间[(80±4)min]。LR-AFY01也表现出良好的促肠道蠕动作用,其中LFD+LR-AFY01H组的排黑粪时间[(65±5) min]低于LFD+乳果糖组,显示出更优的促排效果。同时,如图1-b所示,各组小鼠在小肠推进功能方面存在显著差异。正常组表现出最优的肠道运动功能,其小肠活性炭排出率均显著高于其他各组(P<0.05)。相比之下,LFD组由于便秘模型的建立,其小肠推进率均处于最低水平。经乳果糖干预后,LFD+乳果糖组小鼠的肠道运动功能得到明显改善,小肠推进率较模型组显著(P<0.05)提高。然而,LFD+乳果糖组的上述指标仍低于LFD+LR-AFY01H组,略高于LFD+LR-AFY01L组。研究显示,实验室条件下活性炭水通过肠道排出黑便的时间和在小肠中的推进率测定可以直观地判断便秘状态,也用于评价功能性物质抑制便秘的效果[11]。本研究中实验结果也证实LR-AFY01具备抑制便秘的效果。
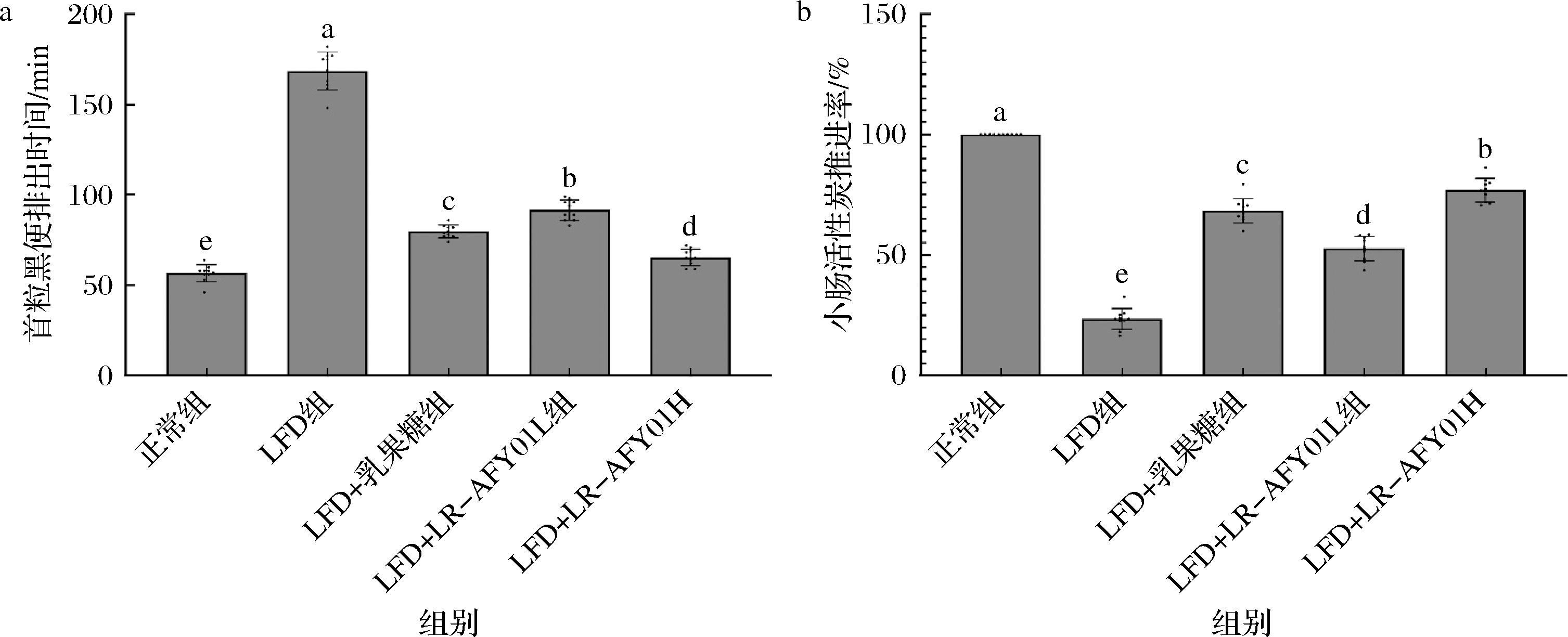
a-首次排出黑色粪便颗粒时间;b-小肠活性炭推进率
图1 便秘小鼠首次排出黑色粪便颗粒时间和活性炭推进率
Fig.1 Time of first excretion of black fecal particles in constipated mice and activated carbon propulsion rate
注:不同小写字母表示组间差异具有统计学意义(P<0.05)(下同)。
2.3 便秘小鼠血清MTL、VIP、AchE、SP、ET-1和SS水平
如图2所示,各组小鼠血清指标检测结果显示正常组小鼠血清中MTL、VIP、AchE和SP水平均显著高于其他实验组,但ET-1和SS水平显著低于其余各组(P<0.05)。同时LFD+LR-AFY01H组小鼠血清的MTL、VIP、AchE、SP、ET-1和SS水平最为接近正常组,MTL、VIP、AchE和SP水平显著高于LFD+乳果糖、LFD+LR-AFY01H和LFD组,ET-1和SS水平显著低于上述3组(P<0.05)。MTL是一种重要的胃肠肽类激素,其主要生理功能包括刺激肠道平滑肌收缩、促进胃蛋白酶原分泌,在维持正常肠道运动和排便功能中发挥关键作用。VIP具有舒张平滑肌、扩张血管及促进肠道分泌的作用,其水平降低可导致肠道运动,是引发便秘的重要机制之一。AchE通过调节肠道收缩运动及促进黏液分泌,在维持正常肠道排泄功能中起重要作用,其活性增强有助于促进肠道内容物排出,预防便秘发生。SP作为胃肠道神经系统中的关键兴奋性神经递质,通过激活神经激肽1受体发挥多重生理作用,不仅能够显著增强胃肠道平滑肌的收缩力,还可刺激小肠和结肠黏膜上皮细胞的水分及电解质分泌,从而有效促进胃肠道的节律性蠕动。生长抑素通过抑制胃肠道平滑肌的收缩,降低胃肠道的蠕动速度,从而导致肠道内容物的通过效率下降,进而加剧便秘症状。ET-1在生理状态下以微量形式存在,参与多器官功能的稳态调节。然而,在血管内皮损伤等病理条件下,ET-1的过量释放可导致中枢神经系统损伤、神经元功能障碍及血管收缩,进而抑制肠道蠕动,严重时可诱发机械性肠梗阻[13]。实验结果显示LR-AFY01能够调节便秘小鼠血清MTL、VIP、AchE、SP、ET-1和SS水平,且高剂量下调节能力强于乳果糖,具备更好的便秘抑制效果。
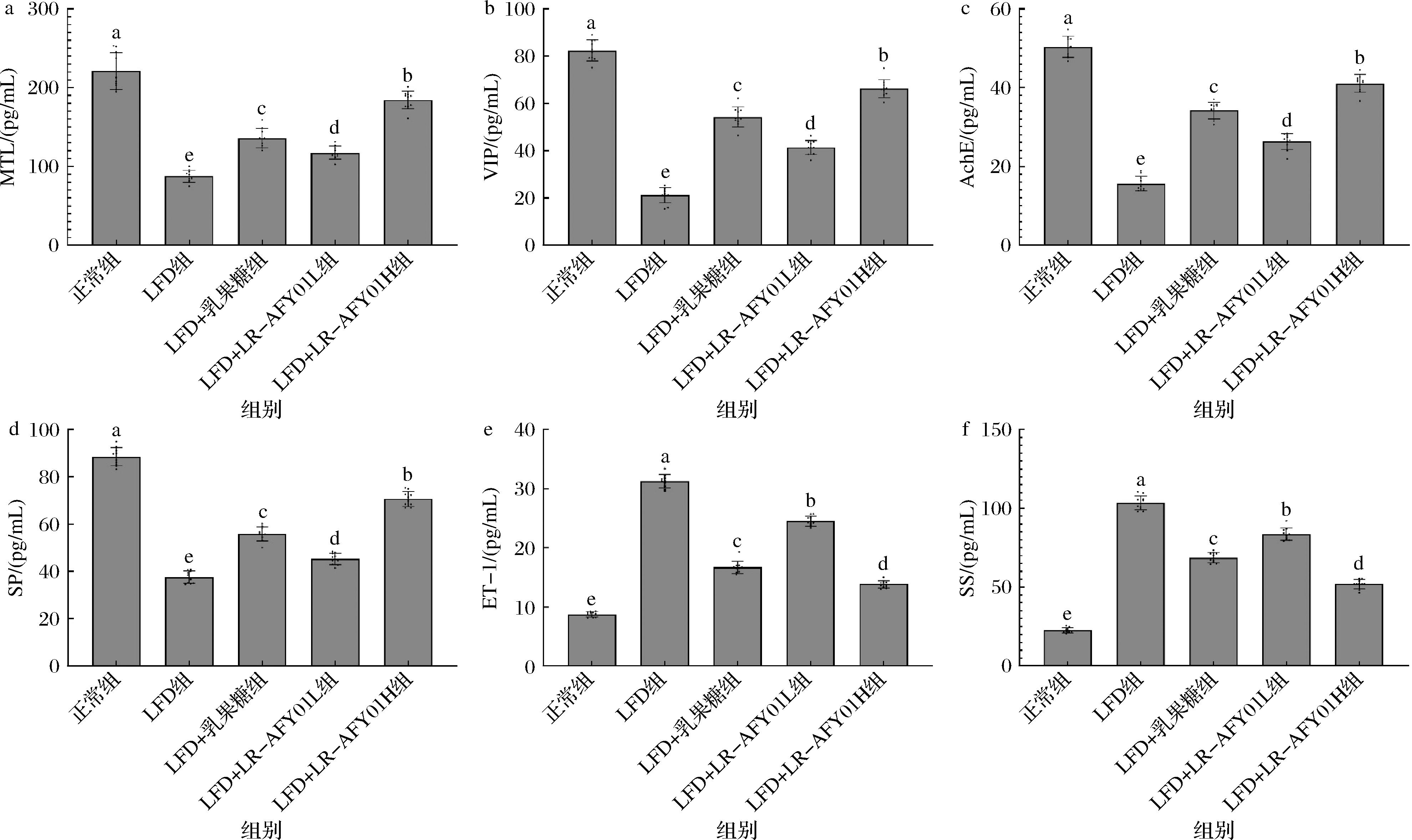
a-MTL;b-VIP;c-AchE;d-SP;e-ET-1;f-SS
图2 便秘小鼠血清MTL、VIP、AchE、SP、ET-1和SS水平
Fig.2 Serum MTL, VIP, AchE, SP, ET-1, and SS levels in constipated mice
2.4 便秘小鼠结肠组织氧化应激反应因子水平
如图3所示,LFD组小鼠结肠组织表现出最低的SOD、CAT、GSH-Px水平和最高的MDA水平,正常组则表现出和LFD组相反的趋势,具有最高的SOD、CAT、GSH-Px水平和最低的MDA水平。LFD+LR-AFY01H组的SOD、CAT、GSH-Px水平显著高于LFD+乳果糖组、LFD+LR-AFY01L组和LFD组,MDA水平显著低于LFD+乳果糖组、LFD+LR-AFY01L组和LFD组(P<0.05),但LFD+乳果糖组和LFD+LR-AFY01L组上述氧化相关因子无显著差异(P>0.05)。研究显示便秘影响肠道菌群平衡,使有害菌占比增加,有害菌产生的毒素引发氧化应激;同时,低纤维膳食造成肠道蠕动受阻,消化后的废弃物质在肠道中产生的毒性物质也不断积累,加剧了氧化应激[14]。SOD、CAT、GSH-Px都是机体内常见的抗氧化酶,MDA则是机体氧化损伤后出现的物质,上述抗氧化酶和MDA的水平能直接反映肠道氧化应激损伤的情况[15]。本研究结果显示,LR-AFY01能够抑制低纤维膳食便秘造成的肠道氧化应激,且高剂量的LR-AFY01效果明显,乳果糖和低剂量的LR-AFY01对氧化应激的调节作用不强。

a-SOD;b-CAT;c-GSH-Px;d-MDA
图3 便秘小鼠结肠组织氧化应激反应因子水平
Fig.3 Oxidative stress factor levels in colon tissue of constipated mice
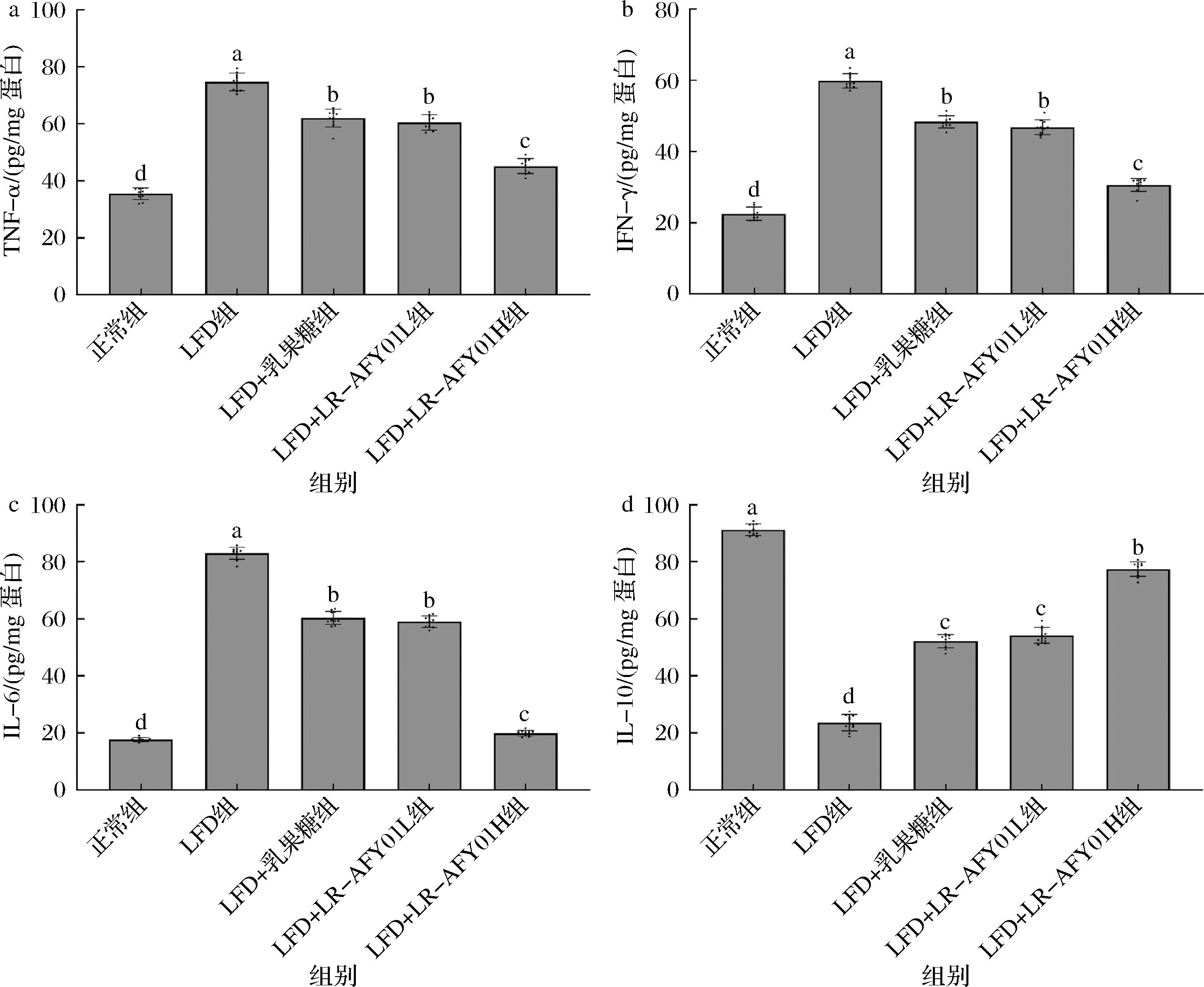
a-TNF-α;b-IFN-γ;c-IL-6;d-IL-10
图4 便秘小鼠结肠组织细胞因子水平
Fig.4 Cytokine levels in colon tissue of constipated mice
2.5 便秘小鼠结肠组织炎症细胞因子水平
如图4所示,LFD+LR-AFY01H组小鼠结肠组织中的TNF-α、IFN-γ、IL-6细胞因子水平显著低于除正常组外其余各组,IL-10则显著高于除正常组外其余各组(P<0.05)。LFD+乳果糖组的TNF-α、IFN-γ、IL-6、IL-10细胞因子水平与LFD+LR-AFY01L组之间无显著差异(P>0.05)。研究显示便秘导致肠道运动紊乱,肠道出现炎症反应,肠道由于氧化应激产生的自由基和肠道内积累的毒性物质进一步加剧炎症,造成肠道损伤,形成便秘与炎症的持续恶性循环[16]。肠道出现炎症的时候,TNF-α和IFN-γ会明显上升,肠道炎症的加剧也通过造成肠道神经系统功能损伤导致肠道收缩和蠕动能力受影响,从而加剧便秘。IL-6是重要的促炎因子,能够加剧炎症和影响平滑肌功能,导致和加剧便秘;IL-10作为抗炎因子,通过减轻炎症和改善免疫力起到调节肠道功能,缓解便秘的效果[17]。本研究实验结果显示,LR-AFY01作为有益微生物,调节了结肠中的炎症细胞因子水平,进而起到抑制便秘的效果,而乳果糖对炎症细胞因子的调节能力不强。
2.6 便秘小鼠结肠组织病变情况
如图5所示,正常组小鼠结肠黏膜结构完整,上皮细胞排列整齐,腺体分布均匀,隐窝形态正常,未见溃疡性病变。LFD组小鼠结肠组织呈现显著的炎症性改变,表现为大量炎性细胞浸润,伴有广泛坏死性病变及隐窝脓肿。LFD+乳果糖组小鼠结肠炎症程度较模型组明显减轻,炎性细胞浸润减少,隐窝结构破坏得到部分改善。值得注意的是,LFD+LR-AFY01H组仅表现为轻微炎症细胞浸润,隐窝结构基本保持完整。剂量效应分析表明,与低剂量LR-AFY01L相比,高剂量LR-AFY01H降低了结肠组织的病理损伤程度。综合评估显示,LR-AFY01在减轻便秘所致结肠病理改变方面表现出优于乳果糖的治疗效果。
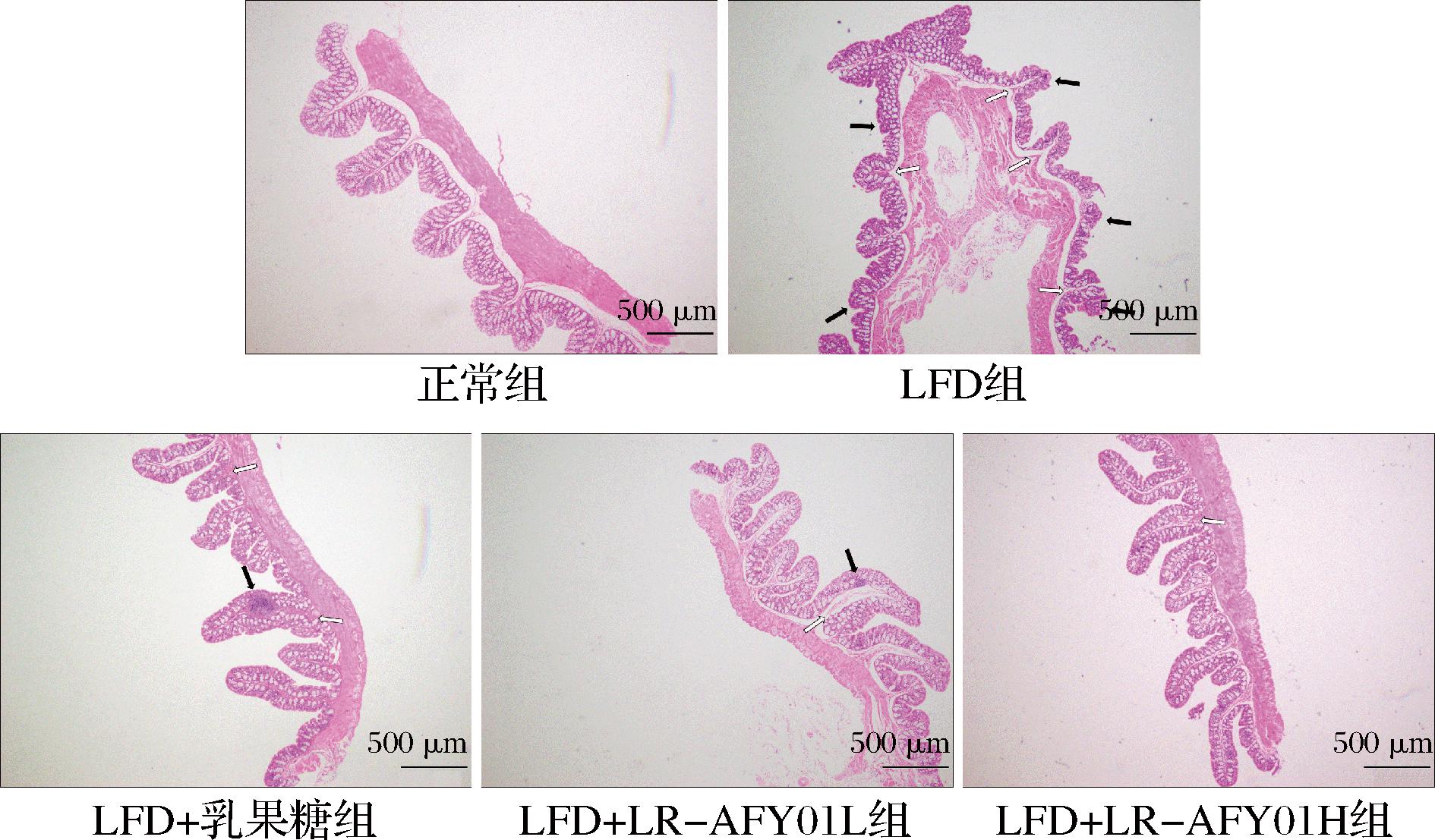
图5 便秘小鼠结肠组织病变情况
Fig.5 Colonic tissue lesions in constipated mice
注:黑色箭头为炎症细胞浸润,白色箭头为隐窝形态破坏
2.7 便秘小鼠结肠组织mRNA表达强度
由图6所示,低纤维膳食导致小鼠发生便秘后LFD组小鼠结肠组织的色氨酸羟化酶1(tryptophan hydroxylase 1,TPH1)、5-羟色胺受体3a(5-hydroxytryptamine receptor 3a, HTR3a)、HTR4、β-连环蛋白(beta-catenin,β-catenin)、Wnt家族成员3A(Wnt family member 3A,WNT3A)、AMP激活蛋白激酶α1(AMP-activated protein kinase alpha 1,AMPKα1)、水通道蛋白3(aquaporin 3,AQP3)、AQP8 mRNA表达强度相比正常组显著下降,而溶质载体家族6成员4(solute carrier family 6 member 4,SLC6A4)、哺乳动物雷帕霉素靶蛋白(mechanistic target of rapamycin,mTOR)表达显著上升(P<0.05)。相比LFD组,LR-AFY01干预的2组小鼠(LFD+LR-AFY01L组、LFD+LR-AFY01H组)均能够显著上调TPH1、HTR3a、HTR4、β-catenin、WNT3A、AMPKα1、AQP3、AQP8表达和下调SLC6A4、mTOR表达(P<0.05)。LFD+乳果糖组对上述表达的调控能力较弱。能够轻微的调节上述表达强度,趋势与LR-AFY01干预组相同。5-羟色胺(5-hydroxytryptamine, 5-HT)在肠道中起到了促进肠道蠕动的重要作用,TPH1 是合成5-HT的关键酶;而SLC6A4则是5-HT的转运体,过度表达的情况下大量回收5-HT,加剧便秘;HTR3a和HTR4分别是5-HT的离子型受体和G 蛋白偶联受体,起到促进5-HT的分泌,从而发挥调节肠道蠕动抑制便秘的作用[18]。Wnt信号通路中β-catenin和WNT3A基因都具有促进肠道中细胞增殖和分化的作用,对于便秘造成的肠道损伤具有很好的调节和修复作用,从而缓解便秘[19]。AMPKα1能够调节肠道细胞的能量代谢,从而影响肠道细胞的正常生理活动,AMPKα1保持在正常水平能够保持肠道功能的正常运行;mTOR也与肠道细胞的增殖和代谢有密切关系,便秘状态下mTOR过度表达,从而造成肠道功能紊乱[20]。AQP3和AQP8在肠道中调控水分转运,AQP3和AQP8的表达下降造成肠道水分吸收减少,粪便干燥,排便困难;同时AQP8还参与电解质的转运,调节肠道生理活动,AQP8的异常表达也对肠道的运动有明显影响[21]。本研究证实低纤维膳食造成的便秘使TPH1、HTR3a、HTR4、β-catenin、WNT3A、AMPKα1、AQP3、AQP8 mRNA表达下降,SLC6A4、mTOR表达增强,LFD+LR-AFY01对便秘造成的上述表达异常有明显的调节和恢复作用,而乳果糖在调节5-HT、Wnt/β-catenin、AMPK和AQPs信号通路的效果不强,可能是由于乳果糖调节便秘的机制主要是其渗透性和细菌发酵作用,自身不被吸收,对机体的上述信号通路起到的影响微弱。
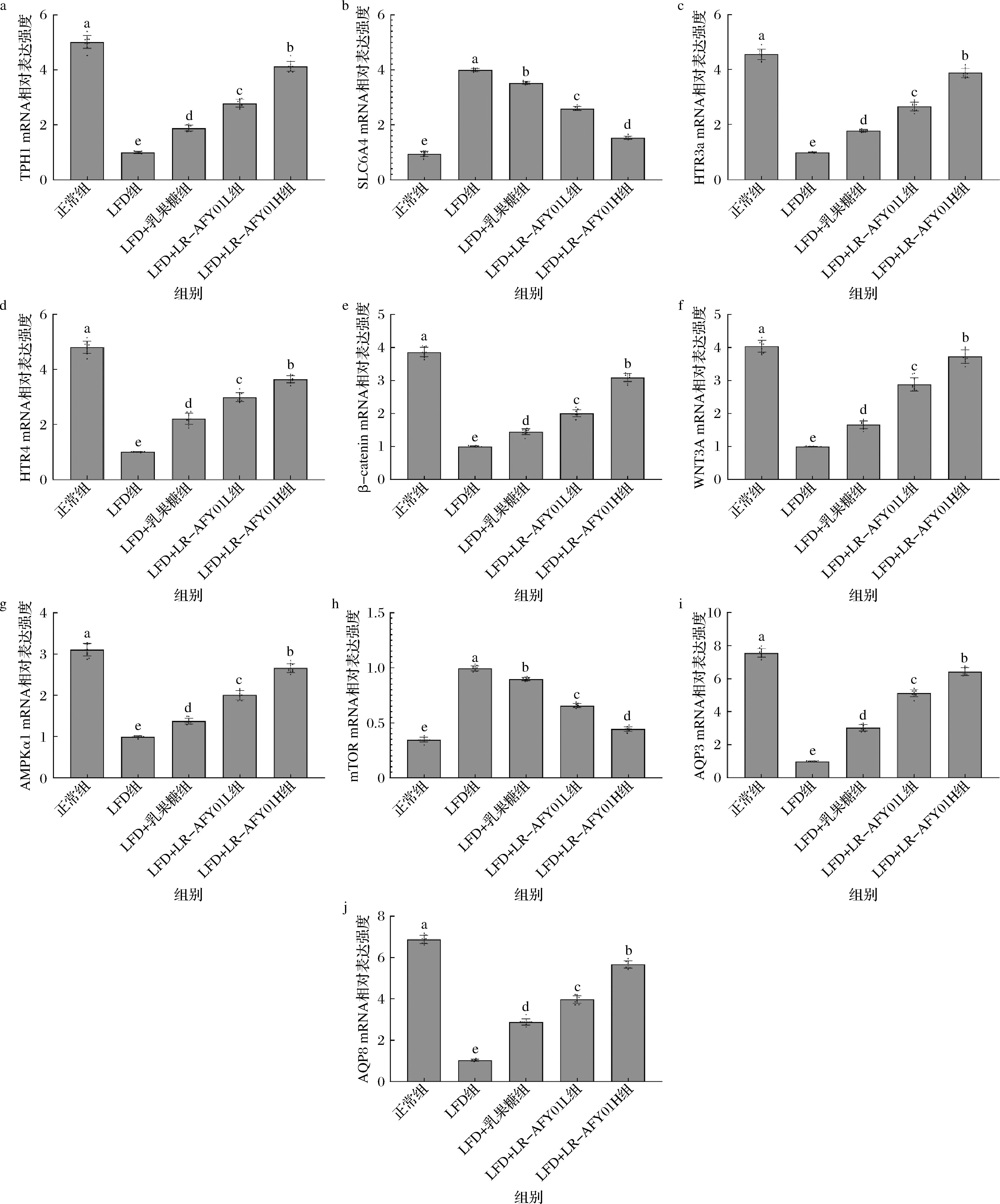
a-TPH1;b-SLC6A4;c-HTR3a;d-HTR4;e-β-catenin;f-WNT3A;g-AMPKα1;h-mTOR;i-AQP3;j-AQP8
图6 便秘小鼠结肠组织mRNA表达强度
Fig.6 mRNA expression level of in colon tissue of constipated mice
2.8 便秘小鼠肠道内容物中重要微生物的数量
如表2所示,与正常组小鼠相比,LFD组小鼠肠道中乳杆菌和双歧杆菌的数量显著降低(P<0.05),而肠球菌、肠杆菌和产气荚膜梭菌的数量则显著增加(P<0.05)。LR-AFY01能够促进小鼠体内乳杆菌和双歧杆菌的增殖,同时抑制肠球菌、肠杆菌和产气荚膜梭菌的生长,且乳杆菌能够大幅度增加,肠杆菌数量变化较小。LR-AFY01H对肠道内容物中微生物的调节作用强于LR-AFY01L,乳果糖的调节作用最弱。乳杆菌和双歧杆菌都是肠道中的有益菌,能够产生短链脂肪酸的有益代谢物质,通过这些有益代谢物质发挥调节肠道环境和促进肠道蠕动的作用,从而缓解便秘[22]。肠球菌和产气荚膜梭菌作为条件致病菌,具有破坏肠道菌群平衡的不利作用,肠球菌和产气荚膜梭菌数量的增加会抑制有益菌的生长,从而导致或加重便秘[23]。肠杆菌的过度增殖也可能抑制乳杆菌和双歧杆菌的生长,从而造成肠道菌群平衡被破坏,导致便秘[24]。因此调控肠道菌群中的肠球菌、肠杆菌、产气荚膜梭菌、乳杆菌和双歧杆菌保持平衡有利于抑制便秘,恢复肠道健康。本研究中LR-AFY01起到了调节肠道菌群,抑制便秘的作用。
表2 便秘小鼠肠道内容物中重要微生物的数量
Table 2 Quantity of important microorganisms in the intestinal contents of constipated mice
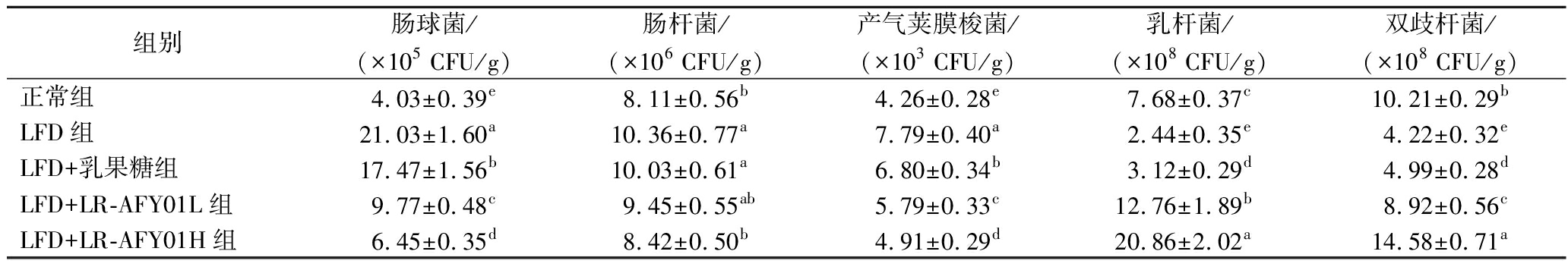
组别肠球菌/(×105 CFU/g)肠杆菌/(×106 CFU/g)产气荚膜梭菌/(×103 CFU/g)乳杆菌/(×108 CFU/g)双歧杆菌/(×108 CFU/g)正常组4.03±0.39e8.11±0.56b4.26±0.28e7.68±0.37c10.21±0.29bLFD组21.03±1.60a10.36±0.77a7.79±0.40a2.44±0.35e4.22±0.32eLFD+乳果糖组17.47±1.56b10.03±0.61a6.80±0.34b3.12±0.29d4.99±0.28dLFD+LR-AFY01L组9.77±0.48c9.45±0.55ab5.79±0.33c12.76±1.89b8.92±0.56cLFD+LR-AFY01H组6.45±0.35d8.42±0.50b4.91±0.29d20.86±2.02a14.58±0.71a
注:不同小写字母表示差异显著(P<0.05)。
3 结论
本研究采用低纤维膳食诱导便秘小鼠模型,检验了从新疆自然发酵酸奶中分离出的新菌株LR-AFTY01的便秘抑制效果。结果显示LR-AFTY01对低纤维膳食便秘具有很好的抑制效果,其主要作用机制较为复杂,LR-AFTY01通过调节肠道菌群,调控5-HT、Wnt/β-catenin、AMPK和AQPs信号通路抑制结肠氧化应激和炎症反应,从而抑制便秘,保持肠道健康。由此可见,LR-AFTY01是1株可作为便秘抑制和肠道健康的益生菌,但是其对人体的确切作用还需要进一步的研究和验证。
[1] YAN J M, WU M L, ZHAO W, et al.Effects of probiotics and its fermented milk on constipation:A systematic review[J].Food Science and Human Wellness, 2023, 12(6):2124-2134.
[2] XU X Q, WANG Y L, LONG Y Y, et al.Chronic constipation and gut microbiota:Current research insights and therapeutic implications[J].Postgraduate Medical Journal, 2024, 100(1190):890-897.
[3] YANG W Y, JIANG C Y, SHAO Y J, et al.Evaluating the link between the dietary intake of vitamin B and constipation:A population-based study[J].Frontiers in Nutrition, 2025, 12:1594644.
[4] MA T, ZHOU M T, ZHANG X R, et al.Mung bean starch-derived fermented liquid alleviates constipation via 5-HT modulation and gut microbiota regulation:An in vivo study[J].Foods, 2025, 14(14):2483.
[5] ARA JO M M, BOTELHO P B.Probiotics, prebiotics, and synbiotics in chronic constipation:Outstanding aspects to be considered for the current evidence[J].Frontiers in Nutrition, 2022, 9:935830.
JO M M, BOTELHO P B.Probiotics, prebiotics, and synbiotics in chronic constipation:Outstanding aspects to be considered for the current evidence[J].Frontiers in Nutrition, 2022, 9:935830.
[6] YUE T J, LU Y N, DING W L, et al.The role of probiotics, prebiotics, synbiotics, and postbiotics in livestock and poultry gut health:A review[J].Metabolites, 2025, 15(7):478.
[7] HIGASHI B, MARIANO T B, DE ABREU FILHO B A, et al.Effects of fructans and probiotics on the inhibition of Klebsiella oxytoca and the production of short-chain fatty acids assessed by NMR spectroscopy[J].Carbohydrate Polymers, 2020, 248:116832.
[8] BRASZCZY SKA-SOCHACKA J, SOCHACKI J, MIK M.The gut’s secret code:Bowel microbiota as a biomarker for adaptation[J].Nutrients, 2025, 17(13):2117.
SKA-SOCHACKA J, SOCHACKI J, MIK M.The gut’s secret code:Bowel microbiota as a biomarker for adaptation[J].Nutrients, 2025, 17(13):2117.
[9] 李文元, 王一琳, 杨辉, 等.双歧杆菌四联活菌片联合乳果糖治疗儿童功能性便秘的效果观察[J].中国实用医刊, 2025, 52(12):94-97.
LI W Y, WANG Y L, YANG H, et al.Observation on the effect of Bifidobacterium quadruple viable tablets combined with lactulose in the treatment of functional constipation in children[J].Chinese Journal of Practical Medicine, 2025, 52(12):94-97.
[10] 齐丽娟, 聂燕敏, 张维, 等.小鼠低纤维膳食便秘模型的初步研究[J].毒理学杂志, 2019, 33(5):357-360.
QI L J, NIE Y M, ZHANG W, et al.A study on the low fiber diet-induced constipation in a mouse model[J].Journal of Toxicology, 2019, 33(5):357-360.
[11] 易若琨, 骞宇, 王强, 等.植物乳杆菌YS-1对活性炭诱导小鼠便秘的预防作用[J].食品科学, 2017, 38(17):238-243.
YI R K, QIAN Y, WANG Q, et al.Preventive effect of Lactobacillus plantarum YS-1 on activated carbon-induced constipation in mice[J].Food Science, 2017, 38(17):238-243.
[12] 赵欣, 谭晓红, 刘新红, 等.植物乳植杆菌GXFF202402调节小鼠肠易激综合征干预痔疮的效果[J].食品与发酵工业, 2025, 51(15):41-50.
ZHAO X, TAN X H, LIU X H, et al.Effect of Lactiplantibacillus plantarum GXFF202402 on the intervention of hemorrhoids in mice with irritable bowel syndrome[J].Food and Fermentation Industries, 2025, 51(15):41-50.
[13] TAN F, KONG C S.Inhibitory effect of Lactiplantibacillus plantarun HFY11 on compound diphenoxylate-induced constipation in mice[J].Biomolecules, 2025, 15(3):358.
[14] 魏佳捷, 刘志峰.肠道菌群与功能性便秘的研究进展[J].国际儿科学杂志, 2025, 52(4):243-247.
WEI J J, LIU Z F.Progress on intestinal flora and functional constipation[J].International Journal of Pediatrics, 2025, 52(4):243-247.
[15] 宫健伟, 叶蕾, 张秀丽, 等.地黄饮子对脑缺血再灌注模型大鼠血清、脑组织SOD, CAT和GSH-Px及MDA的影响[J].中国实验方剂学杂志, 2013, 19(14):247-250.
GONG J W, YE L, ZHANG X L, et al.Effects of Dihuang Yinzi on the SOD, CAT, GSH-Px activities and MDA contents in the serum and brain of cerebral ischemia-reperfusion model rats[J].Chinese Journal of Experimental Traditional Medical Formulae, 2013, 19(14):247-250.
[16] 徐玉洁, 张亚峰, 许翠萍, 等.便秘状态下肠道菌群变化对脂代谢的影响[J].世界华人消化杂志, 2020, 28(9):341-346.
XU Y J, ZHANG Y F, XU C P, et al.Effect of intestinal flora changes on lipid metabolism in constipation[J].World Chinese Journal of Digestology, 2020, 28(9):341-346.
[17] 徐伟立, 齐晓杨, 李萌, 等.便秘患儿肠道菌群改变调控先天免疫淋巴细胞3、白细胞介素-22、胶质源性神经营养因子表达影响肠神经发育机制[J].中华实验外科杂志, 2025, 42(4):720-726.
XU W L, QI X Y, LI M, et al.Changes of intestinal flora in children with constipation regulate the expression of innate immune lymphocytes 3, interleukin-22 and glial-derived neurotrophic factor and affect the development mechanism of intestinal nerves[J].Chinese Journal of Experimental Surgery, 2025, 42(4):720-726.
[18] CHAO G, WANG Y, ZHANG S.Colonic mucosal gene expression in irritablebowel syndrome rats by the liquid chip technology[J].International Journal of Experimental Pathology, 2016;9(10):10751-10755.
[19] 吕胜, 王欣, 辛鑫, 等.祛湿化瘀方抑制Wnt3a/β-catenin/VEGF信号通路保护肠道血管屏障治疗实验性NAFLD的机制研究[J].中华中医药杂志, 2024, 39(5):2485-2490.
LYU S, WANG X, XIN X, et al.Study on the mechanism of Qushi Huayu recipe inhibiting Wnt3a/β-catenin/VEGF signaling pathway and protecting intestinal vascular barrier in the treatment of experimental NAFLD[J].China Journal of Traditional Chinese Medicine and Pharmacy, 2024, 39(5):2485-2490.
[20] LEE Y K, PARK S Y, KIM Y M, et al.Suppression of mTOR via Akt-dependent and-independent mechanisms in selenium-treated colon cancer cells:Involvement of AMPKalpha1[J].Carcinogenesis, 2010, 31(6):1092-1099.
[21] 钱海华, 徐天舒, 曾莉, 等.通便颗粒调节慢传输型便秘大鼠结肠水通道蛋白3, 水通道蛋白8表达的研究[J].中国实验方剂学杂志, 2014, 20(24):180-184.
QIAN H H, XU T S, ZENG L, et al.Experimental study of Tongbian Granules on the regulation of AQP3 and AQP8 expression in colon of rats with slow transit constipation[J].Chinese Journal of Experimental Traditional Medical Formulae, 2014, 20(24):180-184.
[22] 李思童, 贾晓蒙, 杨玲, 等.乳杆菌及双歧杆菌缓解便秘的机制[J].中国微生态学杂志, 2023, 35(7):778-783.
LI S T, JIA X M, YANG L, et al.Mechanism of Lactobacillus and Bifidobacterium in relieving constipation[J].Chinese Journal of Microecology, 2023, 35(7):778-783.
[23] 胡根彪, 尹燕, 王红丽.婴幼儿功能性便秘肠道菌群特征及影响因素Logistic回归分析[J].中国现代医生, 2019, 57(16):54-57.
HU G B, YIN Y, WANG H L.Logistic regression analysis of intestinal flora characteristics and influencing factors in infants with functional constipation[J].China Modern Doctor, 2019, 57(16):54-57.
[24] 龙泽荣, 王建平, 王怀宁, 等.便秘型肠易激综合征的肠道微生态学研究[J].医师进修杂志, 2005, 28(23):16-17;19.
LONG Z R, WANG J P, WANG H N, et al.A study on microecology of intestinal tract in patients with constipated type of irritable bowel syndrome[J].Journal of Postgraduates of Medicine, 2005, 28(23):16-17;19.