类食品乳杆菌[1](Lactobacillus paralimentarius)作为一种重要的乳酸菌,深度参与酸面团、泡菜、奶酪等传统发酵食品生产过程[2],其代谢产物对食品风味、保质期及功能特性具有显著影响。近年来,随着合成生物学与代谢工程的发展,乳杆菌因其食品安全性、益生特性及酸性环境耐受能力,逐渐成为食品工业和生物医药领域的研究热点。
同源重组[3]、转座子突变[4]、锌指核酸酶[5]等传统基因编辑技术在乳酸菌中普遍存在效率低、步骤繁琐且难以实现多位点同步编辑的问题。随着时代发展第三代基因编辑技术CRISPR/Cas9系统已成功应用于部分乳酸菌的基因编辑[6-9]。OH等[10]利用单链DNA辅助CRISPR/Cas9系统成功在罗伊氏粘液乳杆菌(Limosilactobacillus reuteri)中实现高效点突变;SONG等[11]使用CRISPR/Cas9系统在乳酸乳球菌(Lactococcus lactis)中实现基因的敲除,效率达到50%;HUANG等[12]使用RecE/T系统辅助CRISPR/Cas9成功对植物乳植杆菌(Lactiplantibacillus plantarum)与短乳杆菌(Lactobacillus brevis)实现了高效的基因编辑,编辑效率达50%~100%。
虽然CRISPR/Cas9技术已成功运用于多种乳酸菌基因编辑,但是L.paralimentarius相较于L.plantarum等模式乳酸菌在遗传背景上存在的差异使得基于CRISPR/Cas9基因编辑平台的建立仍存在较大挑战[13]。此外,目前乳酸菌中的基因编辑工具多局限于单一位点,多基因的编辑依赖于多次质粒的构建与转化,使得实验流程较长,这严重限制了其作为细胞工厂的应用潜力。因此,开发一种高效、无痕且支持多基因同步编辑的工具,对加速类食品乳杆菌的代谢工程研究及工业应用至关重要。
本研究构建了适用于L.paralimentarius的CRISPR-Cas9基因编辑系统,并通过优化质粒大小、sgRNA框架构建结构以及辅助同源修复机制,实现了单轮实验中对多个基因的精准编辑。该系统采用温度敏感型质粒递送CRISPR组件,通过多sgRNA框架的快速构建与多重同源修复臂的协同作用,可同步完成多基因敲除。这一突破显著提升了转化效率与编辑效率,为类食品乳杆菌的高通量功能基因组学研究及复杂代谢网络调控提供了关键技术支撑。本文详述了该工具的构建策略、优化过程及在多基因编辑中的应用实例,以期为乳杆菌的多基因改造提供潜在解决方案。
1 材料与方法
1.1 实验材料
1.1.1 菌种与质粒
本研究中所用菌种与主要质粒如表1所示。
表1 本研究中所用菌种与主要质粒
Table 1 Strains and major plasmids used in this study
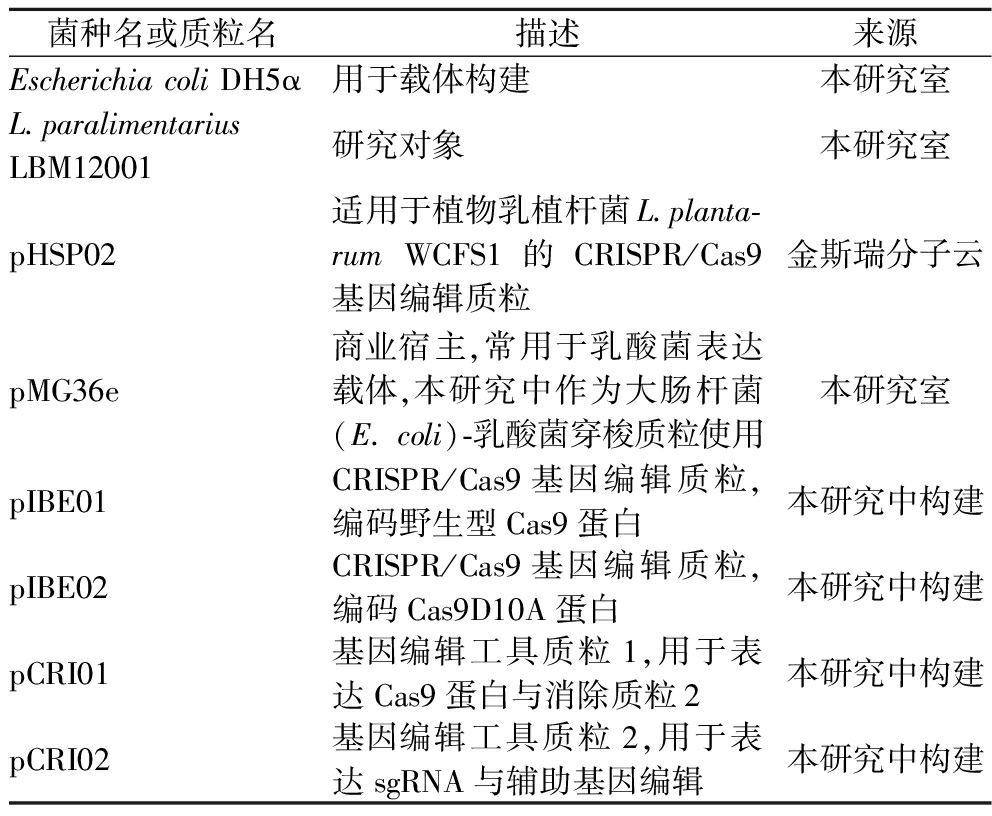
菌种名或质粒名描述来源Escherichia coli DH5α用于载体构建本研究室L.paralimentarius LBM12001 研究对象本研究室pHSP02适用于植物乳植杆菌L.planta-rum WCFS1的CRISPR/Cas9基因编辑质粒金斯瑞分子云pMG36e商业宿主,常用于乳酸菌表达载体,本研究中作为大肠杆菌(E. coli)-乳酸菌穿梭质粒使用本研究室pIBE01CRISPR/Cas9基因编辑质粒,编码野生型Cas9蛋白本研究中构建pIBE02CRISPR/Cas9基因编辑质粒,编码Cas9D10A蛋白本研究中构建pCRI01基因编辑工具质粒1,用于表达Cas9蛋白与消除质粒2本研究中构建pCRI02基因编辑工具质粒2,用于表达sgRNA与辅助基因编辑本研究中构建
1.1.2 本研究中所用引物
本研究所用引物均由SnapGene 6.0.2设计,由生工生物工程(上海)股份有限公司合成(表2)。
表2 本研究中所用主要引物与其序列(5′~3′)
Table 2 Sequences (5′-3′) of the main primers used in this study

引物名称序列(5′~3′)Cas9-FTCAGTCACCTCCTAGCTGACTCAAP23-RCTGCAGCGAAAAGCCCTGsgRNA-FGTTTTAGAGCTAGAAATAGsgRNA-RAAAGTGGCACCGAGTCGGTGCLpaMAHR-up-FTCCCAATGGCTTTGGATGAALpaMAHR-up-RTGAAATAACCTCTCATTTTTAAAAATTTGLpaMAHR-down-FAGAGGTGCTTAATTTGCAAAAACALpaMAHR-down-RAGAGGTGAAGATAGTATTGACCAGTCTTUgpAHR-up-FCAAAGAACGATGTTAAAAAGGCTCTUgpAHR-up-RATAATCGCACCCTTACTTTTTTTTAGUgpAHR-down-FTTTAGCTTTAGAACTTTGATTCTGGAAUgpAHR-down-RTTATCAGGACTATCGTAGACGCTCTTUlpRTF1HR-up-FTGGGACCAGCAACGCTTTGUlpRTF1HR-up-RGAATTCCCCTCCATACATCACAAUlpRTF1HR-down-FATTGTTACCGATAACATCAAACAAAGCUlpRTF1HR-down-RTGTTAGGTTCATGTCCATTGACTTGAmpR-FAAACAAATAGGGGTTCCGCGAmpR-RTTACCAATGCTTAATCAGTGAGrep-FTTTTTATGATTACAAAGTGATACACTAACTTTrep-RTCATTTTATTTCCCCCGTTTCALpaMA-FATGAATACACCAGCAATTTATCATCGLpaMA-RCTATTTAACTAATGCAAATCCTTTAGGATUgpA-FATGGCAAAAAAAGAAATTAATTATAAAGCUgpA-RTTACTTAACAGCACCTGATGTGACACUlpRTF1-FATGACCACTTTATTAGATGTAGCAAAAAUlpRTF1-RTTAATCCCTCAATGTACCACCTAAAC
1.1.3 酶与试剂
高保真PCR扩增酶PrimeSTAR MAX、限制性内切酶,Takara宝生物工程(大连)有限公司;同源重组试剂盒,Vazyme诺唯赞公司。
1.2 实验方法
1.2.1 分子生物学实验方法
1.2.1.1 E.coli DH5α化学感受态细胞制备
甘油管保藏的DH5α菌株在LB固体平板上划线活化,37 ℃静置培养后挑取单菌落至20 mL液体LB培养基中,37 ℃ 200 r/min摇床过夜培养。吸取500 μL菌液接种至50 mL液体LB培养基中,37 ℃,转速200 r/min培养至OD600值达到0.4~0.6。将摇瓶冰上静置30 min,随后分装至50 mL离心管内,4 000 r/min离心10 min,收集菌体弃上清液。每50 mL菌液收集的菌体,添加5 mL预冷的A液,轻轻吹吸混匀,冰上静置30 min。4 000 r/min离心10 min,收集菌体弃上清液。每50 mL菌液收集的菌体,添加1.5 mL预冷的B液,轻轻吹吸混匀,每100 μL分装至预冷的1.5 mL EP管内于-80 ℃保存。其中A液为:20 mmol/L CaCl2,80 mmol/L MgCl2溶液;B液为:100 mmol/L CaCl2,15%甘油(体积分数)。
1.2.1.2 L.paralimentarius LBM12001电转化感受态的制备
甘油管保藏的L.paralimentarius LBM12001菌株在琼脂MRS固体平板上划线活化,37 ℃静置培养后挑取单菌落至20 mL液体MRS培养基中,37 ℃静置培养24 h。取2 mL过夜培养物接种到50 mL MRS液体培养基中(含蔗糖0.4 mol/L、甘氨酸5 g/L),37 ℃,转速200 r/min培养至OD600值为0.3~0.4。菌液装至预冷的离心管中,冰上静置30 min。4 ℃,5 000 r/min离心10 min收集菌体,弃上清液。电转化缓冲液(含蔗糖0.4 mol/L、甘氨酸5 g/L)4 ℃,5 000 r/min离心5 min洗涤菌体2次,弃上清液收集菌体至预冷的离心管中,冰上静置10 min。加入电转化缓冲液重悬菌体。4 ℃,5 000 r/min离心10 min,弃上清液。重新加入1 mL电转化缓冲液重悬菌体,按每管100 μL分装至提前预冷的1.5 mL EP管内,置于-80 ℃保存。
1.2.1.3 pMG36e-Promoter-eGFP质粒构建
pMG36e-Promoter-eGFP质粒的构建方法如图1所示。Promoter-eGFP片段通过重叠延伸PCR连接在一起,随后通过同源重组方法与线性化的载体pMG36e连接。
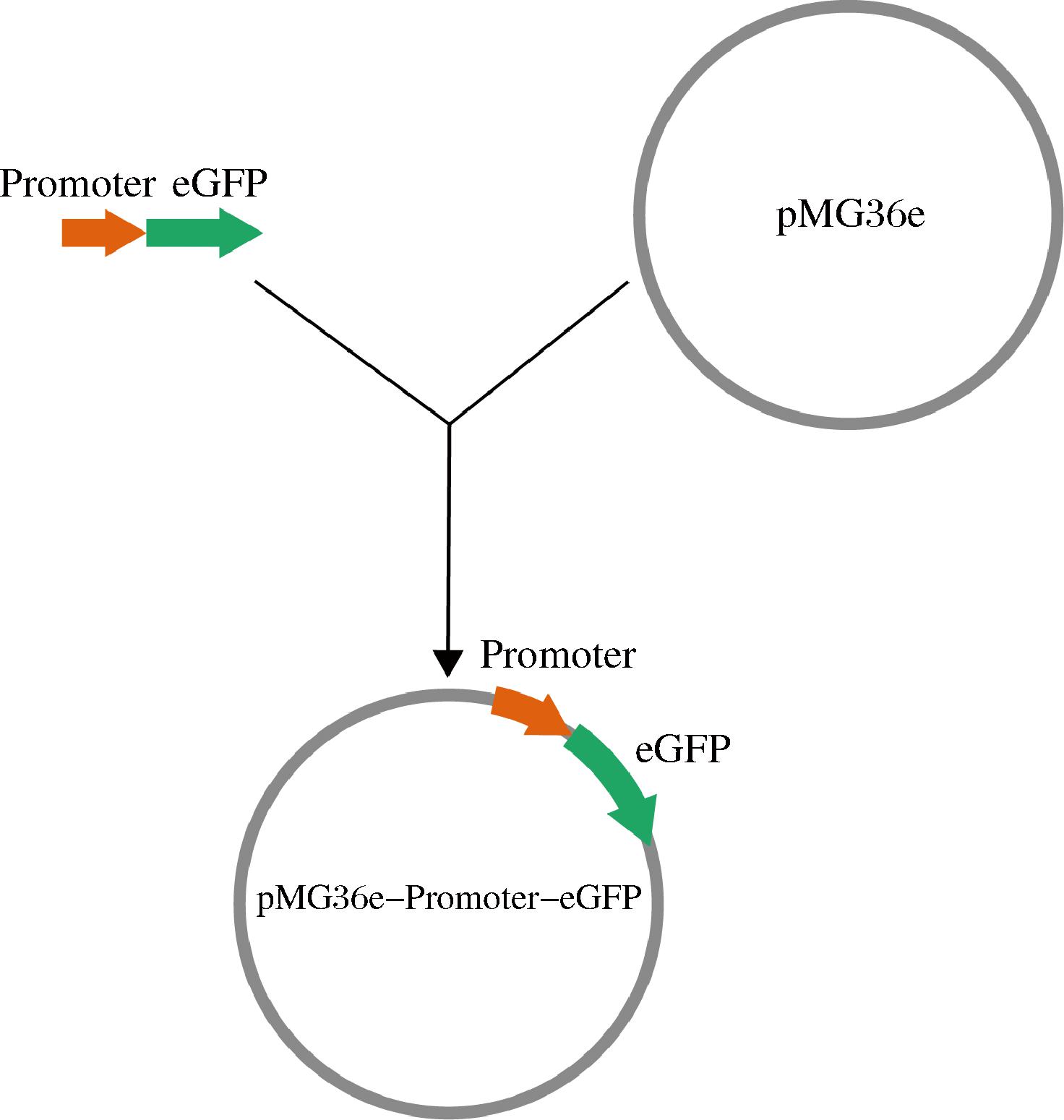
图1 pMG36e-Promoter-eGFP质粒构建示意图
Fig.1 Schematic diagram of the construction of the pMG36e-Promoter-eGFP plasmid
1.2.1.4 含sgRNA质粒的构建
对应基因的sgRNA由GeniousPrime 8.0.1设计。sgRNA通过全质粒PCR方法[14]挂载至质粒相应位置。
1.2.1.5 含同源修复模板质粒的构建
选择对应基因的上下游各500 bp作为同源臂,上下游同源臂通过重叠延伸PCR连接为同源修复模板。同源修复模板通过同源重组试剂盒连接至质粒相应位置。
1.2.1.6 L.paralimentarius LBM12001电转化、基因编辑方法
构建完毕的载体通过化学转化法转化至E.coli DH5α中复制,挑取含有氨苄青霉素抗性的琼脂LB平板上的阳性转化子提取质粒,随后使用真空干燥浓缩仪富集质粒质量浓度至50 ng/μL。吸取10 μL质粒加入100 μL L.paralimentarius LBM12001感受态中2.5 kV、5 ms条件下进行电转化。电转化后的菌液加入900 μL温育MRS培养基后于37 ℃下复苏培养2 h。培养结束后的菌液置于EP管中8 000 r/min离心1 min,弃去900 μL上清液,剩余菌液均匀涂布在含氨苄青霉素抗性的琼脂MRS平板上,37 ℃静置培养48 h。
1.2.2 荧光强度测定方法
将野生型L.paralimentarius LBM12001和L.paralimentarius LBM12001/pMG36e-promoter-eGFP菌株于相应的琼脂MRS培养基上划线活化,37 ℃静置培养24 h,挑取单菌落分别转接至MRS和含红霉素抗性的MRS液体培养基中培养24 h后,8 000 r/min离心10 min收集菌体。离心所得菌体用100 mmol/L,pH值为7.5的Tris-HCl缓冲溶液洗涤2次,重悬混匀后吸取200 μL加入96孔板,在激发光波长488 nm与发射光波长509 nm下,使用酶标仪测量其荧光强度,每组样品3组平行实验。
1.3 数据处理
本研究所有实验统计数据使用GraphPad Prism 8.0.2进行t检验分析,比较数据组间是否具有显著性差异性。
2 结果与分析
2.1 基于CRISPR-Cas9技术的单质粒基因编辑平台的构建
2.1.1 电转化条件的选择
乳酸菌间的差异使得不同乳酸菌的电转化条件有所不同,需要根据宿主自身做出调整。在Lactobacillus属中,影响电转化效率的主要因素为感受态细胞的细胞壁状态、电转化时缓冲液与细胞内的渗透压平衡以及合适的转化电压。在对数生长期前期,细胞正处于快速分裂和生长的状态,细胞膜相对较薄且具有较高的通透性。这种通透性使得外源DNA能够更容易地进入细胞,从而提高电转化的效率。此外,处于此阶段的细胞生长代谢处于最活跃的阶段,拥有更强的应对外界刺激的能力,因而能降低电转化过程导致的死亡率。测定L. paralimentarius LBM12001生长曲线(图2),选择培养3 h的L. paralimentarius LBM12001制备感受态,此时细胞处于对数生长期前期。
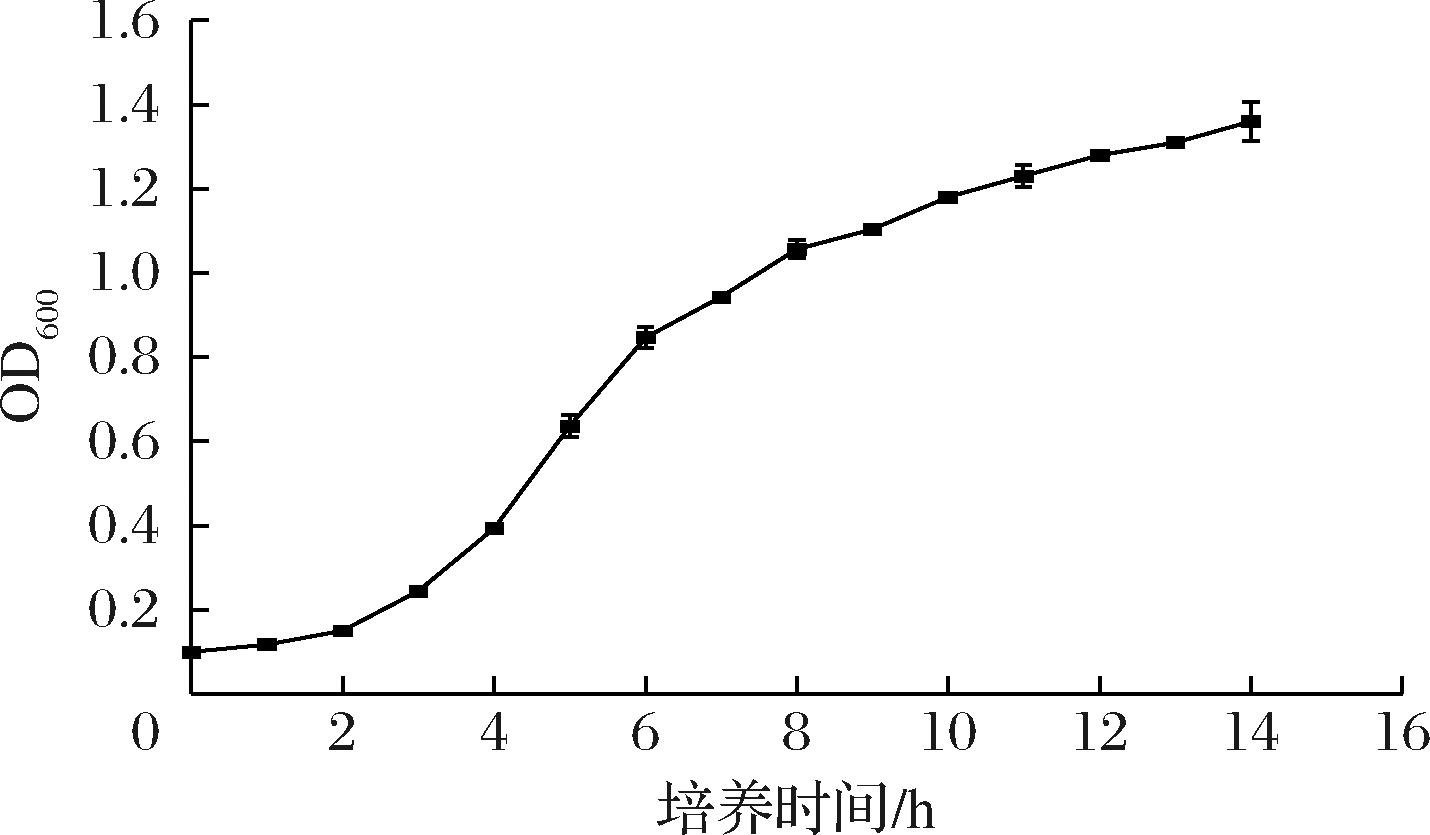
图2 类食品乳杆菌的生长曲线
Fig.2 Growth curve of L.paralimentarius LBM12001
甘氨酸能够替代乳酸菌细胞壁肽聚糖层中的D-丙氨酸,使得其形成更为松散的肽聚糖结构,从而使细胞壁的通透性增加,更易于外源DNA进入。蔗糖可作为渗透压保护剂,其可维持乳酸菌的细胞渗透压平衡,防止细胞在电转化过程中因渗透压变化而破裂。合适的电压可以确保乳酸菌或其他细菌细胞在电转化过程中的膜孔化程度恰到好处,从而提高外源DNA进入效率,提升转化效率,并减少细胞损伤和死亡。选用广谱宿主质粒pMG36e作为E. coli DH5α-L.paralimentarius LBM12001穿梭质粒,以含有红霉素抗性的琼脂MRS平板上产生转化子的个数为基准探究L. paralimentarius LBM12001的最适电转化条件。研究结果(图3)显示当转化电压为2.5 kV时,添加终体积分数为1%的甘氨酸、0.4 mol/L的蔗糖可以显著提升转化子的数量(P<0.05)。
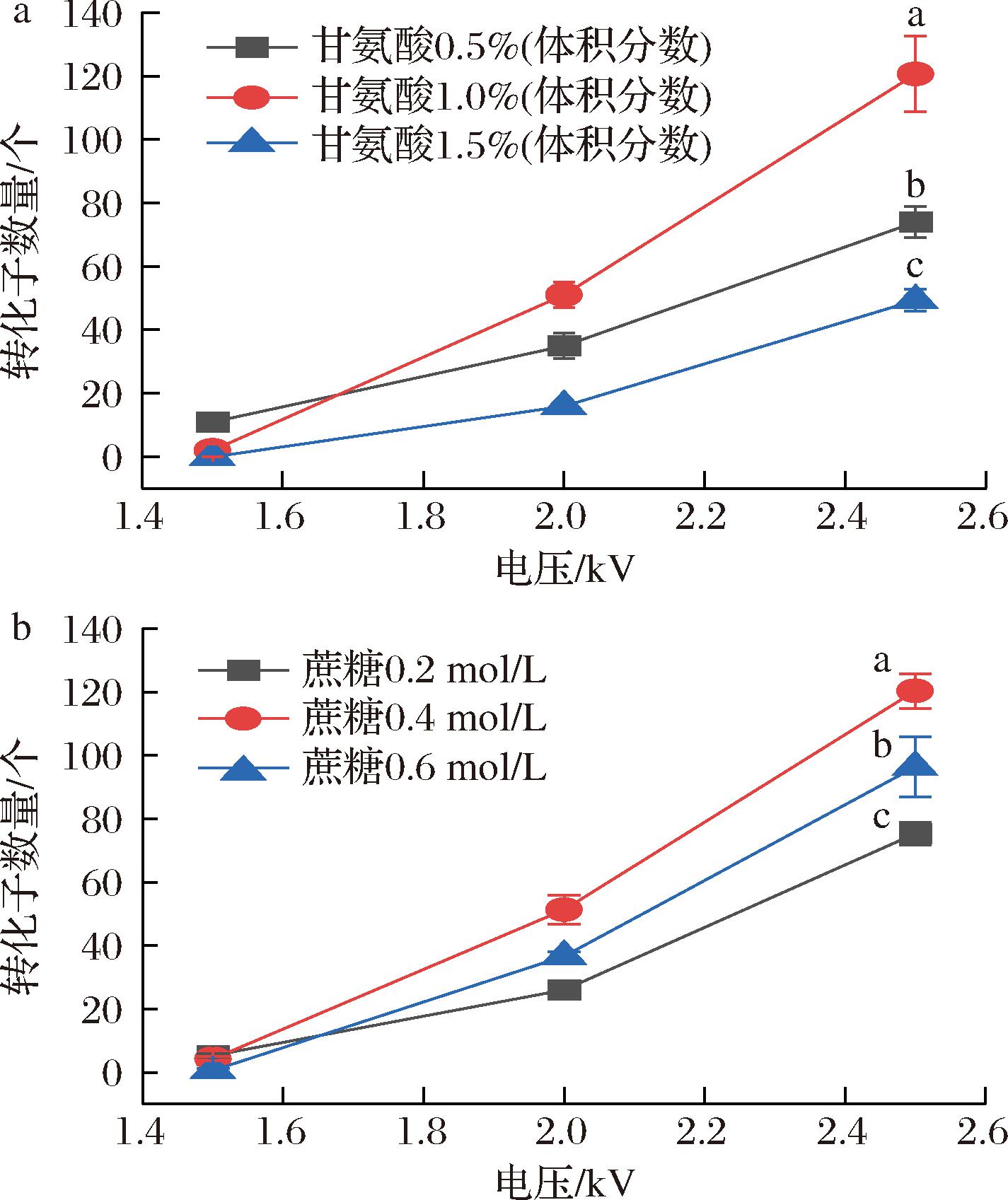
a-不同甘氨酸体积分数;b-不同蔗糖浓度
图3 类食品乳杆菌在不同电转化条件下产生的转化子数量
Fig.3 Effect of electroporation conditions on the number of transformants in L.paralimentarius LBM12001
注:不同小写字母表示差异显著(P<0.05)(图4同)。
2.1.2 强启动子的筛选
为了确保CRISPR/Cas9相关元件的高效表达,根据已有文献报道初步筛选乳酸菌中常用的启动子P23[15]、P32[16]、P44[17]、Pldh[18]。这些启动子具有不同的表达强度和特异性,选择合适的启动子对于提高目的基因的表达效率至关重要。将pMG36e-Promoter-eGFP表达载体转化至L.paralimentarius中,按照1.2.2节所述方法测定荧光强度,结果如图4所示。
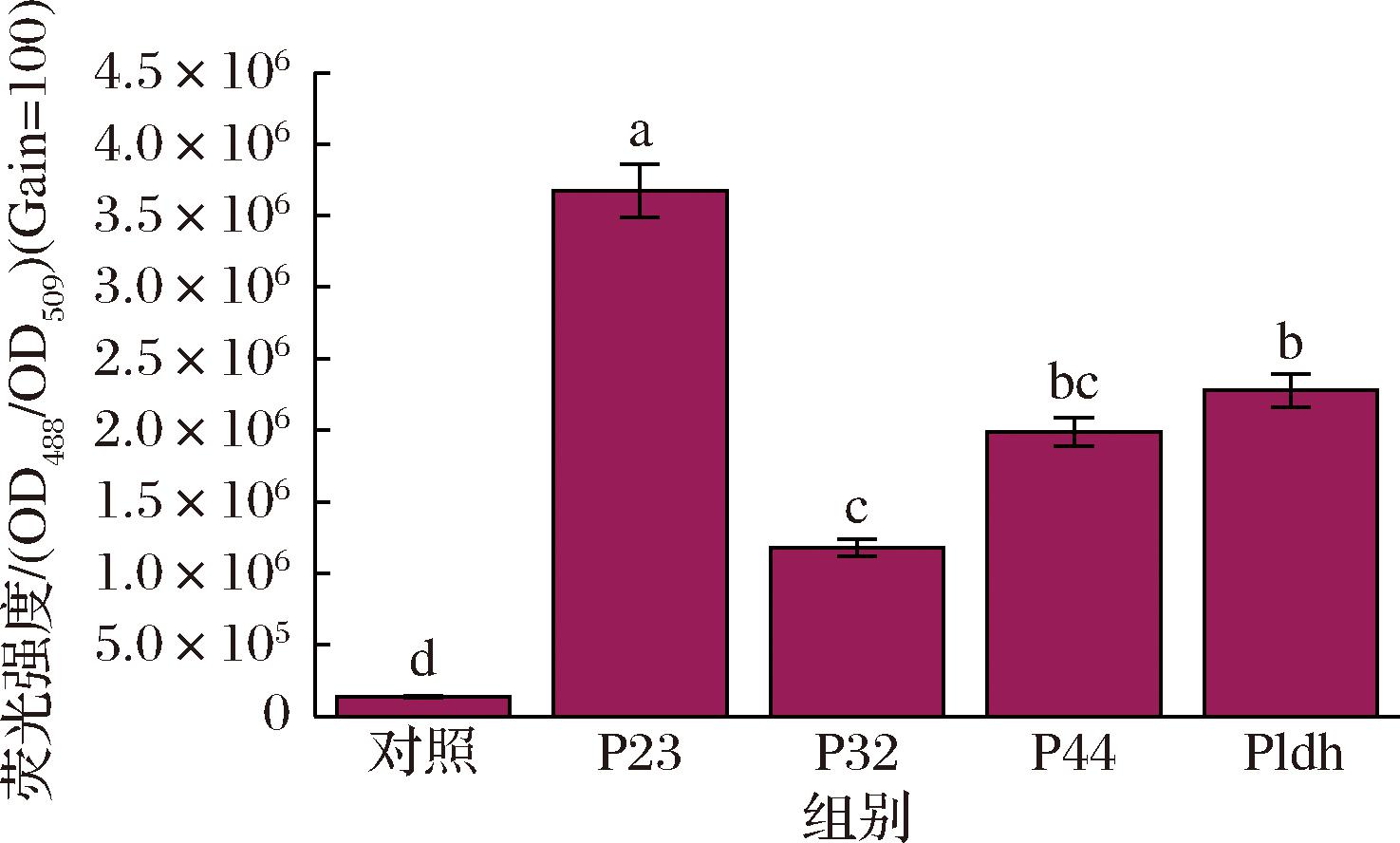
图4 以pMG36e为表达载体,不同启动子串联表达eGFP的荧光强度
Fig.4 Fluorescence intensity under the control of different promoters using pMG36e as the expression vector
诸多组成型启动子如P23、Pldh、P44在L.paralimentarius中均表现出良好的活性,其中Pldh、P44强度差异较小(P>0.05),P23启动子介导的表达载体荧光强度最高,是次强启动子Pldh的1.61倍(P<0.05),故选用P23启动子调控CRISPR/Cas9相关元件的表达。
2.1.3 基于CRISPR/Cas9技术的基因编辑质粒构建
编辑质粒的设计思路是其能够稳定表达Cas9蛋白与sgRNA,质粒上同时编码同源修复模板。通过预实验发现L.paralimentarius与E.coli同时对氨苄青霉素敏感,因而选用氨苄抗性基因(AmpR)作为筛选标记。编辑质粒pIBE01构建流程如图5所示。
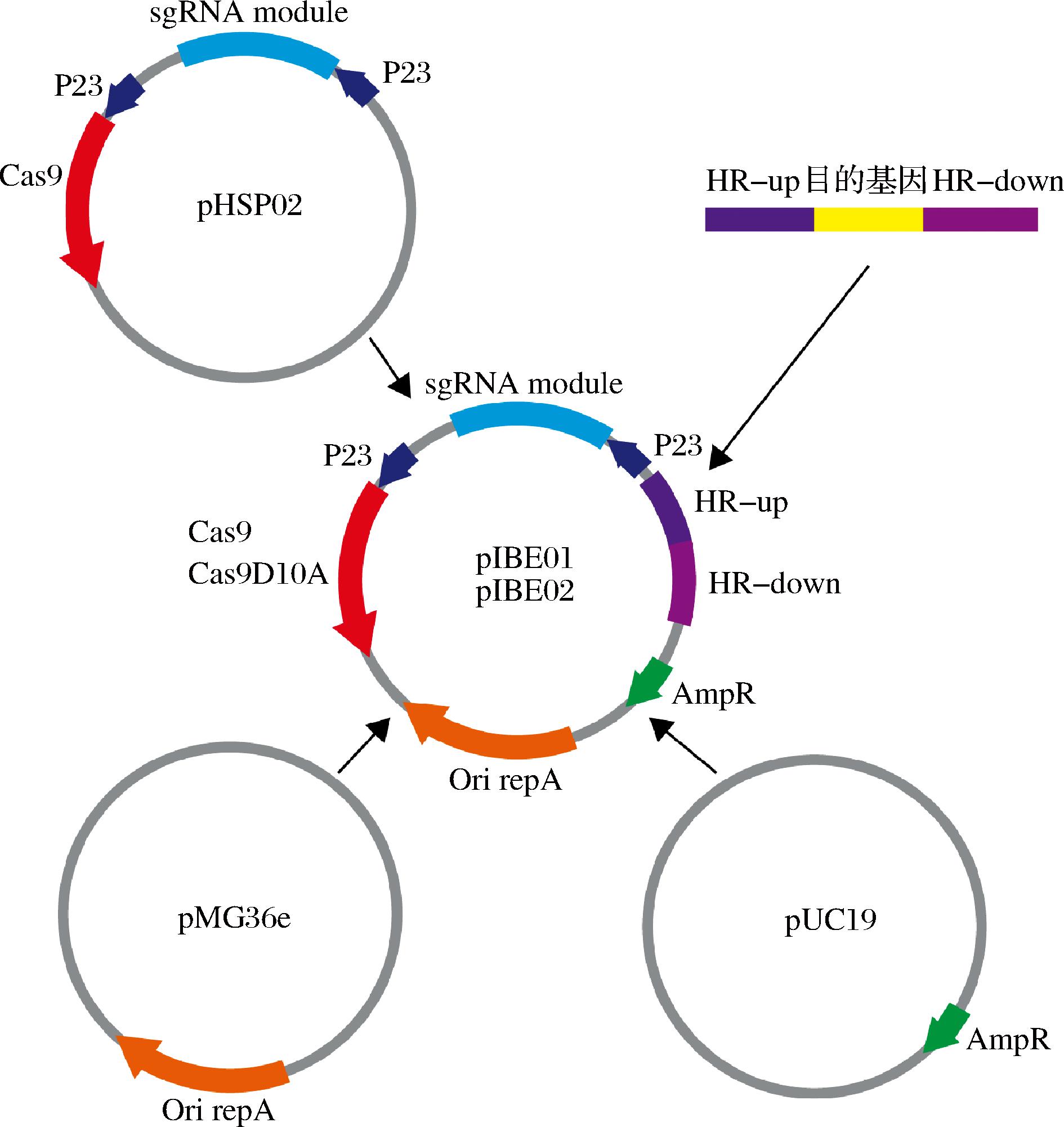
图5 基因编辑质粒pIBE的构建流程缩略图
Fig.5 Schematic diagram of the construction process of the gene editing plasmid pIBE
此外为了预防Cas9蛋白引发的DNA双链断裂对L.paralimentarius LBM12001潜在的致死性,同时从质粒pLCNICK[10]中扩增了Cas9蛋白的突变体版本Cas9D10A并替换pIBE中的Cas9,Cas9D10A相较于Cas9其中一个DNA切割域失活失去了DNA切割能力,因而在基因组中引发更为温和的DNA单链断裂,此质粒命名为pIBE02。
按照1.2.3节、1.2.4节的方法构建基因LpaMA敲除质粒pIBE01-ΔLpaMA、pIBE02-ΔLpaMA。基因编辑后挑取平板上的转化子,接种至5 mL液体MRS培养基中培养24 h后提取基因组。用LpaMA-F/LpaMA-R为上下游引物,以各个转化子的基因组为模板进行PCR,部分PCR产物的凝胶电泳结果如图6所示。除4号泳道的条带清晰可见外,1、2、3、5、6号泳道均有模糊条带。将PCR产物送测序,测序图谱结果显示同一位置显示多种碱基信号,提示可能存在混合基因型。
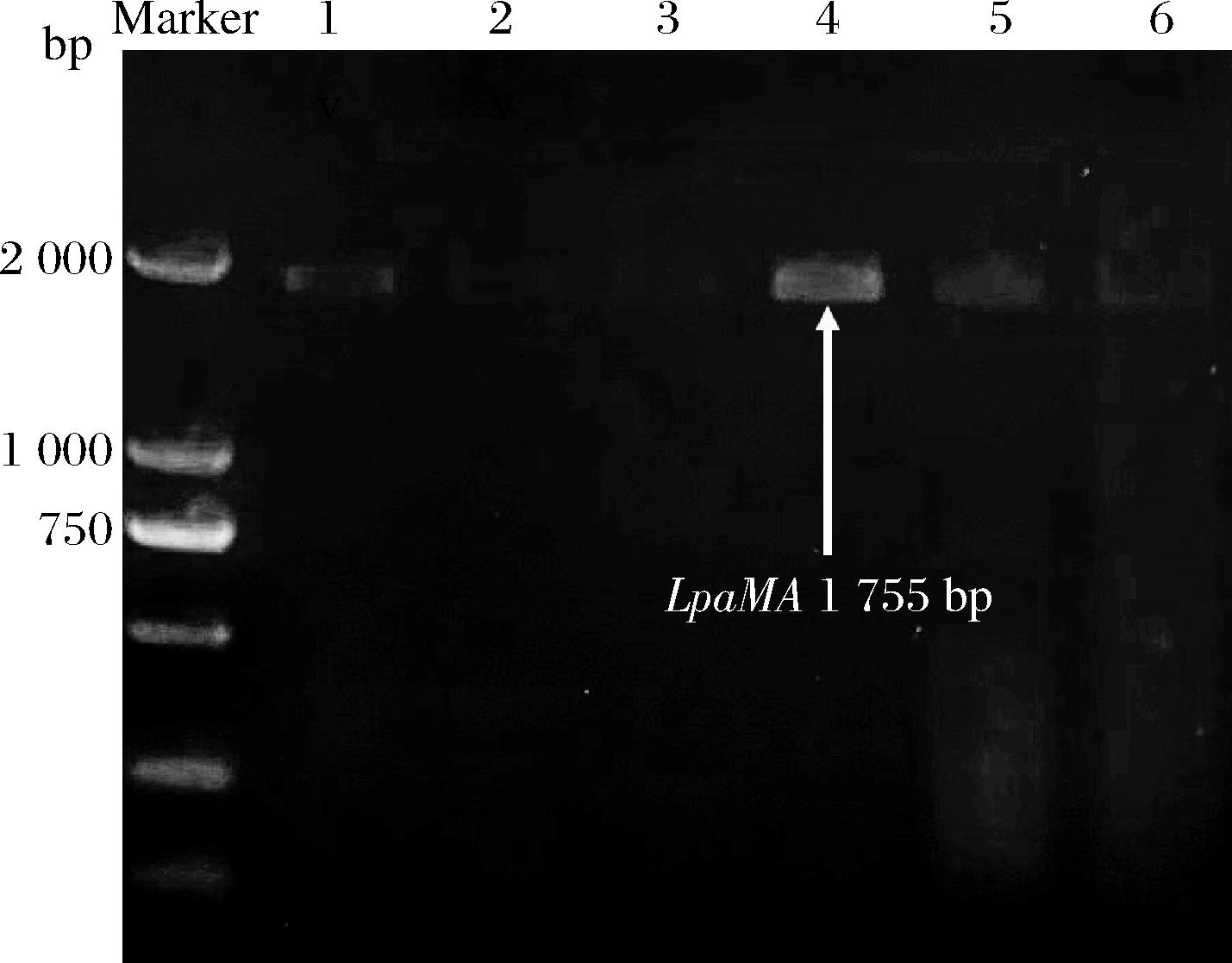
图6 经pIBE01-ΔLpaMA、pIBE02-ΔLpaMA编辑后的部分PCR凝胶电泳验证结果
Fig.6 Gel electrophoresis verifications of some edited samples with pIBE01/02-ΔLpaMA
经pIBE01、pIBE02编辑所得转化子的基因组测序统计结果如图7所示。最终统计结果显示装载Cas9蛋白的pIBE01-ΔLpaMA产生了(24±2)个转化子达到了(67±7)%阳性率,编码Cas9D10A的编辑质粒pIBE02-ΔLpaMA产生了(40±5)个转化子,然而尽管pIBE02产生的转化子数量显著多于pIBE01(P<0.05)但其中阳性率不足25%,且多为混合突变型。在乳酸菌的基因编辑中,Cas9D10A与Cas9蛋白的切割时机显著影响编辑效率。SONG等[19]的研究发现,乳酸菌中染色体单拷贝特性导致:复制前单链切割可能引发全细胞突变,而复制后切割仅影响单个姐妹染色体,导致子代细胞基因型异质。这种混合基因型菌落会显著增加筛选难度。虽然Cas9蛋白引发的双链断裂对L.paralimentarius LBM12001具有可耐受毒性,但其阳性编辑率优势明显。基于编辑效率和筛选成本的综合考量,Cas9蛋白更适合作为该菌株的基因编辑工具。
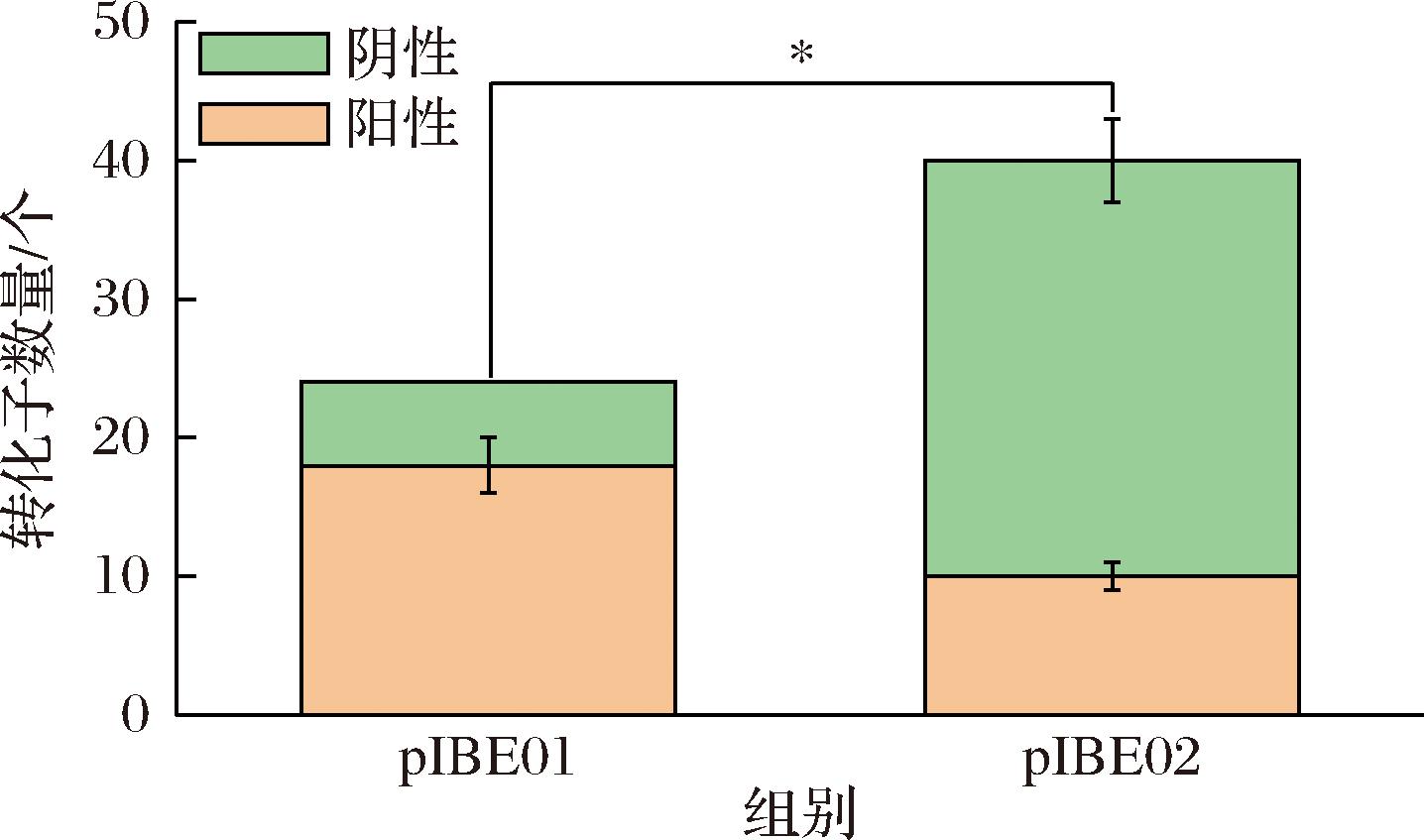
图7 基因编辑质粒pIBE01-ΔLpaMA、pIBE02-ΔLpaMA产生的阴性与阳性转化子数量
Fig.7 Number of transformants generated by the gene editing plasmids pIBE01-ΔLpaMA and pIBE02-ΔLpaMA
注:*表示差异显著(P<0.05)。
2.2 基于CRISPR/Cas9技术的质粒基因编辑平台的优化
构建能够满足工业应用需求的L.paralimentarius LBM12001细胞工厂,需要一种高效的基因组规模编辑工具,以便精确、快速地对多个基因进行大规模改造,从而提升其生产性能和产物合成效率。利用pIBE单质粒编辑系统尝试对L.paralimentarius LBM12001进行多基因编辑。选定LpaMA、UgpA(ABC转运蛋白酶)与UlpRTF1基因作为研究对象,分别构建编辑质粒pIBE01-ΔLpaMAΔUgpA与pIBE01-ΔLpaMAΔUgpAΔUlpRTF1用于获取L.paralimentarius LBM12001 ΔLpaMAΔUgpA与L.paralimentarius LBM12001 ΔLpaMAΔUgpAΔUlpRTF1菌株,编辑质粒pIBE01-ΔLpaMAΔUgpA构建示意图如图8所示,pIBE01-ΔLpaMAΔUgpAΔUlpRTF1运用类似的方法构建。
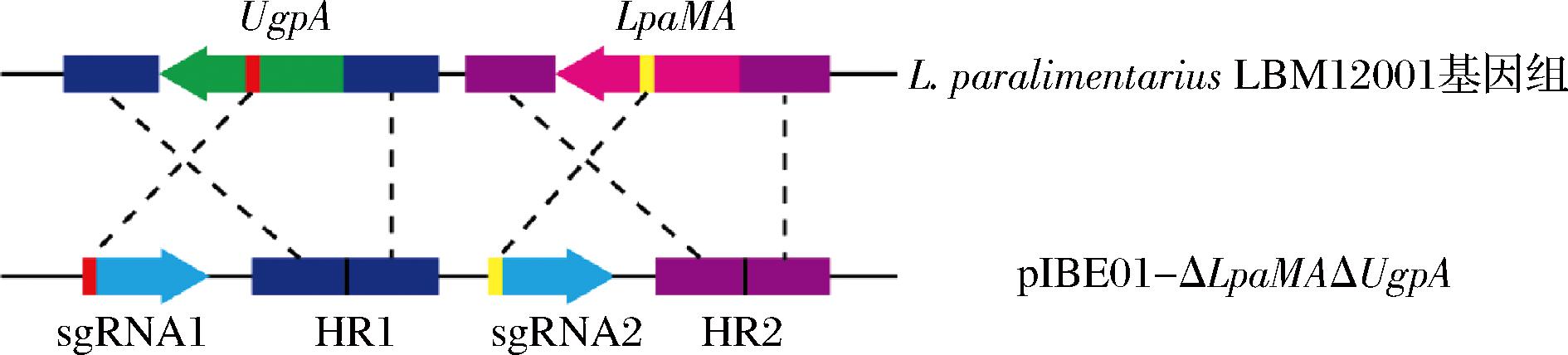
图8 编辑质粒pIBE01-ΔLpaMAΔUgpA构建示意图
Fig.8 Schematic diagram of the plasmid pIBE01-ΔLpaMAΔUgpA
抗性平板上所有转化子的测序结果统计在表3。结果显示,随着编辑基因的数量增加转化子的数量与正确阳性突变率大幅下降,ΔLpaMAΔUgpA与ΔLpaMAΔUgpAΔUlpRTF1生成的转化子数量与阳性突变率显著低于ΔLpaMA(P<0.05),推测其原因是编码在质粒上的修复模板数增加,使得质粒大小过大难以穿过电转化形成的孔隙,此外多个Cas9蛋白-sgRNA复合体引发的基因组多位点断裂给宿主带来的DNA修复压力过大可能也是引发此现象的原因。
表3 质粒pIBE01介导的基因编辑测序统计结果
Table 3 Sequencing and statistical results of gene editing mediated by plasmid pIBE01
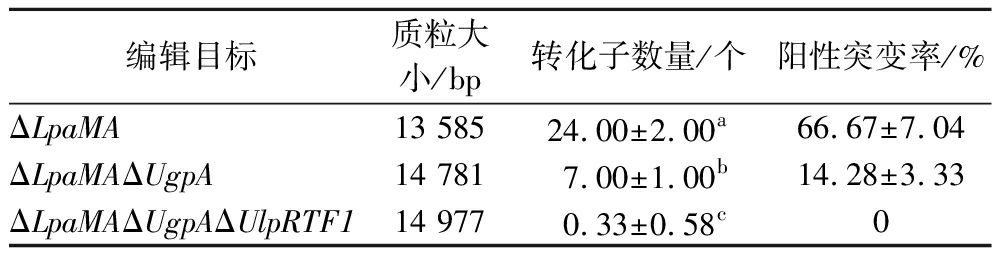
编辑目标质粒大小/bp转化子数量/个阳性突变率/%ΔLpaMA13 58524.00±2.00a66.67±7.04ΔLpaMAΔUgpA14 7817.00±1.00b14.28±3.33ΔLpaMAΔUgpAΔUlpRTF114 9770.33±0.58c0
注:不同小写字母表示差异显著(P<0.05)。
在编辑工作完成后缺乏便捷、高效消除质粒的手段,只得靠多次传代使质粒丢失;随着编辑基因数量的上升,编辑质粒pIBE01的体积会随着编码相应的同源修复模板而增大,使得质粒难以穿过电转化产生的细胞壁空隙;多sgRNA载体的构建耗时耗力,严重拖慢了多基因位点突变工程菌株的构建速度。从这些缺陷入手优化编辑工具pIBE01,新构建的质粒编辑工具如图9所示。
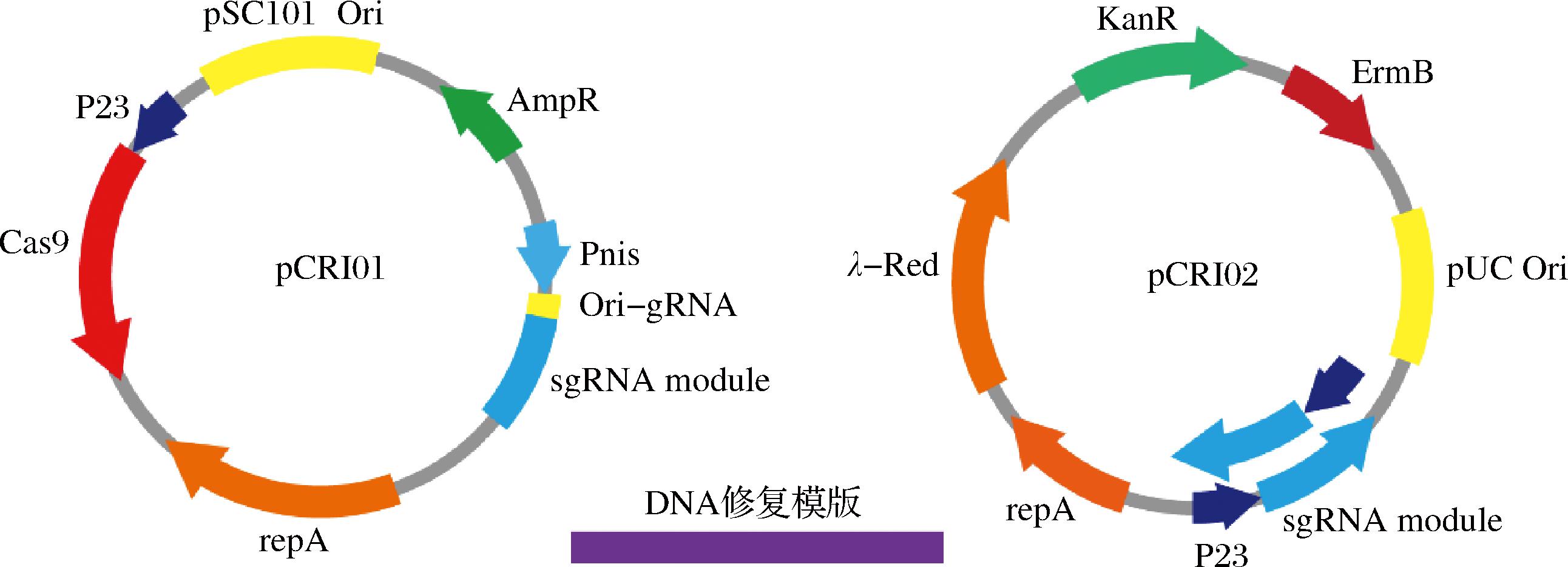
图9 双质粒基因编辑质粒缩略示意图
Fig.9 Schematic diagram of dual-plasmid gene editing plasmid
质粒体积较大会严重影响质粒的转化效率,通过在原有pIBE01质粒的基础上优化质粒构成,将其拆分为pCRI01(8 880 bp)与pCRI02(6 740 bp)。其中pCRI01主要用于表达Cas9蛋白,为了便于质粒的消除引入了pSC101温度敏感复制子[20],此复制子在37 ℃下无法复制,确保pCRI01的便捷消除。此外为了便于消除质粒pCRI02,pCRI01配备了靶向pCRI02复制子的sgRNA,此sgRNA受Pnis启动子[21]诱导表达,当pCRI02表达sgRNA结束后用终质量浓度100 ng/μL 的Nicin诱导pCRI01中的sgRNA表达,切割pCRI02的复制子消除质粒;pCRI02上装载sgRNA,用于导向Cas9蛋白至目的基因。另外在pCRI02中引入了经物种密码子优化后的λ噬菌体来源的λ-Red重组酶系统[14, 22]。λ-Red重组由Exo、Beta和Gam这3种蛋白质介导,Exo是一种核酸外切酶,可以沿着5′~3′方向降解外源双链DNA,产生单链DNA。Beta是一种单链DNA结合蛋白,可以保护单链DNA并促进它与染色体DNA的同源配对。Gam蛋白是一种抑制剂,可以阻止细菌自身的RecBCD酶降解外源DNA,这使得同源修复模板无需编码在质粒上,进一步提升了基因编辑效率。为了便于多sgRNA的挂载,还构建了另一个版本的pCRI02-1,此版本中P23-sgRNA module表达元件与原版本方向相反,多sgRNA的装载方式采用经典的BioBricks方法[23],其构建示意图如图10所示。
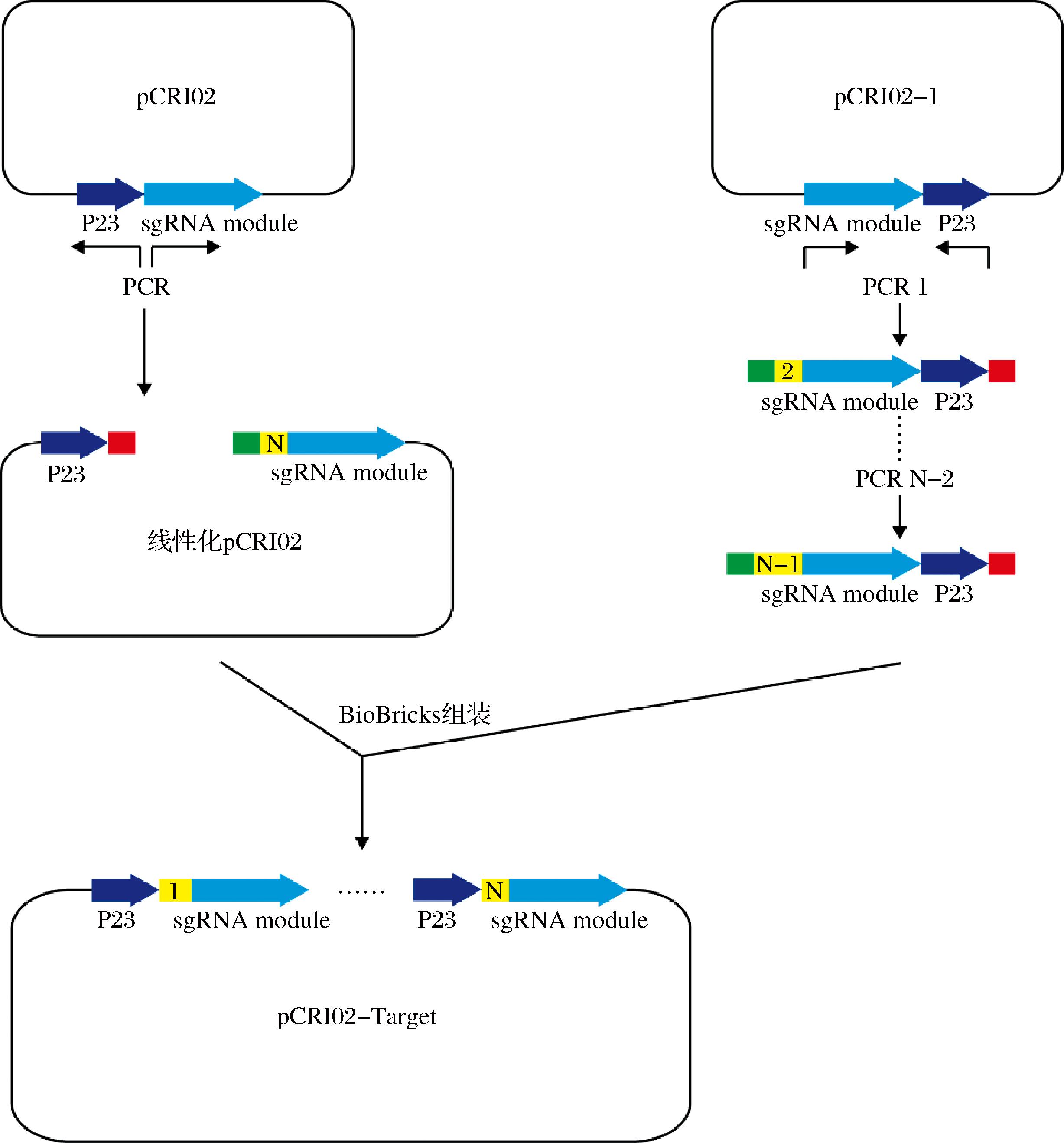
图10 BioBricks方法组装多sgRNA编辑质粒pCRI02-Target原理示意图
Fig.10 Schematic diagram of the principle for constructing multi-sgRNA editing plasmid pCRI02-Target using the BioBricks method
注:■代表Xbai;■代表SpeI;N代表第N个目的基因的sgRNA。
对新建立的基因编辑工具pCRI01与pCRI02进行功能验证,选定基因LpaMA、UgpA、UlpRTF1为研究对象,分别构建菌株L.paralimentarius LBM12001 ΔLpaMA、L.paralimentarius LBM12001 ΔLpaMAΔUgpA、L.paralimentarius LBM12001 ΔLpaMAΔUgpAΔUlpRTF1。按照上述方法构建对应的编辑质粒pCRI01与pCRI02,与pIBE01进行基因编辑,其结果如图11所示。
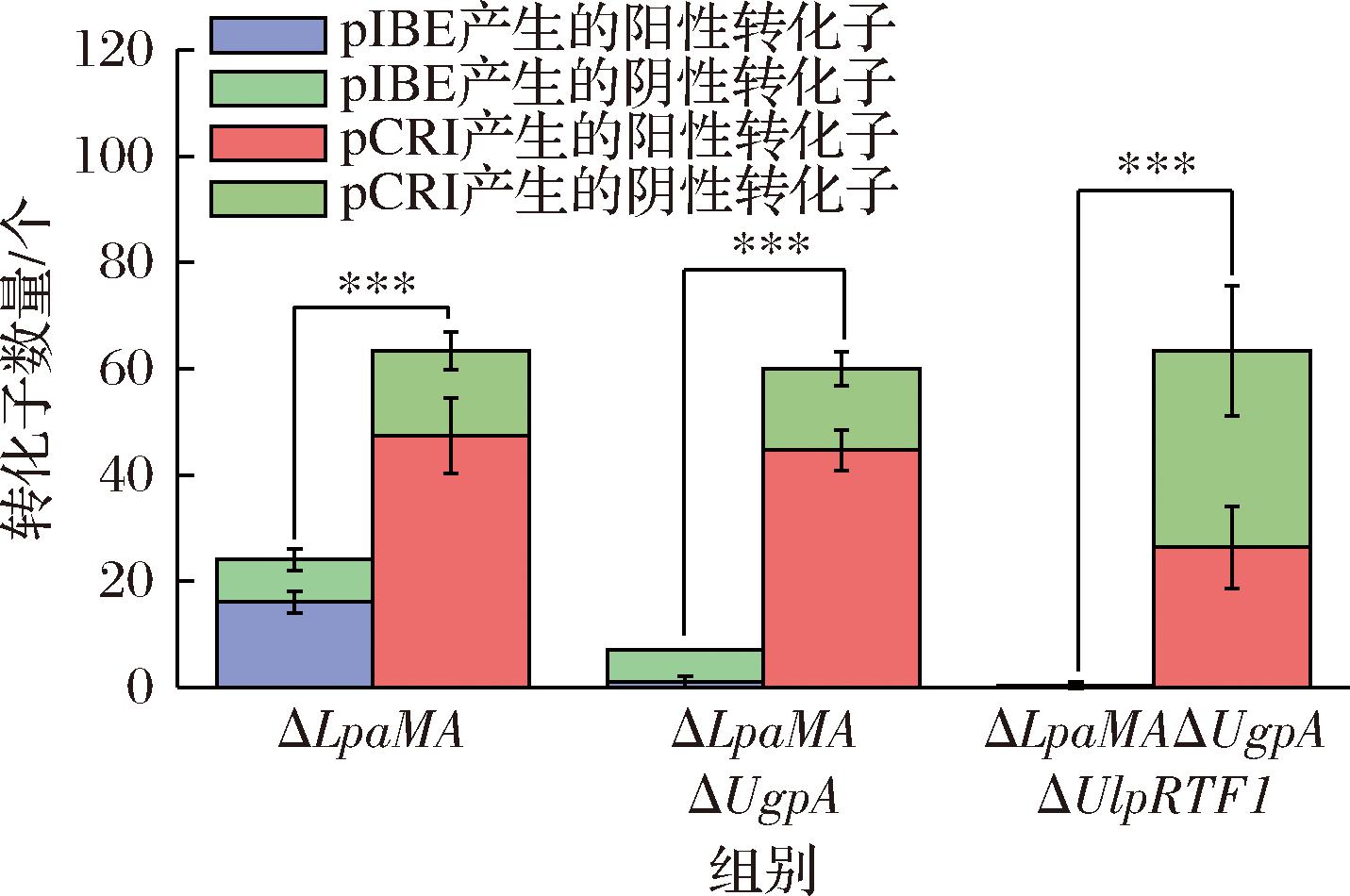
图11 基因编辑质粒pIBE与pCRI产生的阴性转化子与阳性转化子
Fig.11 Negative and positive transformants generated by gene editing plasmids pIBE and pCRI
注:***表示P<0.001。
将大体积质粒pIBE01拆分为小体积的pCRI01与pCRI02双质粒体系后,抗性筛选后的转化子的数量显著提升,在单基因敲除实验中,pCRI02质粒产生了(63±11)个转化子,显著多于pIBE01产生的(24±2)个(P<0.001)。多基因敲除实验中的提升更为明显,敲除LpaMA与UgpA的实验中,pCRI02产生了(60±7)个转化子,近似是pIBE01产生转化子数量的10倍(P<0.001),而在敲除LpaMA、UgpA与UlpRTF1三基因的实验中,pIBE01没有产生转化子,而pCRI02生成了(57±8)个转化子,这进一步表明在优化质粒体积后的电转化效率得到了巨大提升。在编辑效率方面,改进后的编辑工具在单基因与双基因的敲除实验中均达到了75%左右的阳性突变率,在三基因的敲除实验中实验效率有所降低,低至(46±7)%。得益于λ-Red重组系统的辅助,pCRI质粒介导的基因编辑效率得到较大提高。
pIBE01与pCRI介导单基因编辑的主要实验流程如表4所示。当进行单基因编辑任务时pIBE01需要6 d时间,当需要对多个基因进行编辑时需重复第3~4天的工作,需要时长为(4+2 N) d;pCRI系统进行单基因编辑时,需要5 d时间,进行多基因编辑时为确保编辑效率应根据编辑基因数目调整策略,以3个基因为1组进行多轮编辑。pCRI相较于pIBE系统在多基因位点编辑任务中能节约大量时间。例如当对9个基因进行编辑时pIBE系统需要22 d,而pCRI系统仅需要10 d。
表4 质粒pIBE01与pCRI完成基因编辑的主要流程
Table 4 Main process of gene editing using plasmids pIBE01 and pCRI

编辑工具与实验流程pIBE01pCRI第1天构建pIBE01-sgRNA载体扩增同源修复模板构建pCRI02-sgRNA载体扩增同源修复模板第2天构建pIBE-sgRNA-同源修复模板载体电转化第3天电转化37 ℃静置培养第4天37 ℃静置培养转化子测序第5天转化子测序质粒消除第6天质粒消除
本小节成功构建并优化了适用于L.paralimentarius LBM12001的高效CRISPR/Cas9多基因编辑平台。通过开发双质粒系统,并结合质粒体积优化与λ-Red重组酶辅助的同源修复机制,显著提升了电转化效率及多基因同步编辑能力。相比以往文献中报道的乳酸菌CRISPR/Cas9系统[6],该方法利用BioBricks模块化设计和λ-Red介导的同源重组,不仅解决了大质粒转化效率低、多sgRNA构建繁琐以及辅助同源修复机制效率低下的问题,同时引入温度敏感型质粒和自靶向诱导型sgRNA,实现了质粒的便捷消除,使得多基因编辑周期缩短至单轮实验内完成。
3 结论与讨论
本研究构建的双质粒CRISPR/Cas9编辑平台在L.paralimentarius中实现了多基因同步无痕编辑,为其作为细胞工厂应用于代谢网络重构和产物合成路径优化方面提供了一种高效工具。主要内容包括:利用双质粒系统与λ-Red辅助同源修复大幅提高了转化效率与编辑精度;温度敏感质粒与自靶向sgRNA的策略有效实现了编辑后质粒的快速清除。
该编辑平台的建立不仅为类食品乳杆菌的工程化改造提供了一种新方法,也为非模式乳酸菌的遗传改造提供了宝贵的实践案例。未来可通过进一步优化sgRNA设计策略提升编辑效率;可探索基因插入、调控元件整合及构建新的代谢通路,以满足更复杂的代谢工程需求。随着合成生物学在非模式乳酸菌中的发展,本研究所建立的技术体系,可为乳酸菌在功能性食品开发及高价值化合物生物合成中的工业化应用提供有力支撑。
[1] LHOMME E, LATTANZI A, DOUSSET X, et al.Lactic acid bacterium and yeast microbiotas of sixteen French traditional sourdoughs[J].International Journal of Food Microbiology, 2015, 215:161-170.
[2] OKOYE C O, DONG K, WANG Y L, et al.Comparative genomics reveals the organic acid biosynthesis metabolic pathways among five lactic acid bacterial species isolated from fermented vegetables[J].New Biotechnology, 2022, 70:73-83.
[3] RADECKE S, RADECKE F, CATHOMEN T, et al.Zinc-finger nuclease-induced gene repair with oligodeoxynucleotides:Wanted and unwanted target locus modifications[J].Molecular Therapy, 2010, 18(4):743-753.
[4] KUSANO H, ONODERA H, KIHIRA M, et al.A simple Gateway-assisted construction system of TALEN genes for plant genome editing[J].Scientific Reports, 2016, 6:30234.
[5] LEENHOUTS K, BUIST G, BOLHUIS A, et al.A general system for generating unlabelled gene replacements in bacterial chromosomes[J].Molecular and General Genetics MGG, 1996, 253(1):217-224.
[6] LV X Q, LI Y, XIU X, et al.CRISPR genetic toolkits of classical food microorganisms:Current state and future prospects[J].Biotechnology Advances, 2023, 69:108261.
[7] SONG X, ZHANG X Y, XIONG Z Q, et al.CRISPR-Cas-mediated gene editing in lactic acid bacteria[J].Molecular Biology Reports, 2020, 47(10):8133-8144.
[8] GOH Y J, BARRANGOU R.Portable CRISPR-Cas9(N) system for flexible genome engineering in Lactobacillus acidophilus, Lactobacillus gasseri, and Lactobacillus paracasei[J].Applied and Environmental Microbiology, 2021, 87(6):e02669-20.
[9] MU Y L, ZHANG C X, LI T H, et al.Development and applications of CRISPR/Cas9-based genome editing in Lactobacillus[J].International Journal of Molecular Sciences, 2022, 23(21):12852.
[10] OH J H, VAN PIJKEREN J P.CRISPR-Cas9-assisted recombineering in Lactobacillus reuteri[J].Nucleic Acids Research, 2014, 42(17):e131.
[11] SONG X, LIU L, LIU X X, et al.Single-plasmid systems based on CRISPR-Cas9 for gene editing in Lactococcus lactis[J].Journal of Dairy Science, 2021, 104(10):10576-10585.
[12] HUANG H, SONG X, YANG S.Development of a RecE/T-assisted CRISPR-Cas9 toolbox for Lactobacillus[J].Biotechnology Journal, 2019, 14(7):1800690.
[13] LEENAY R T, VENTO J M, SHAH M, et al.Genome editing with CRISPR-Cas9 in Lactobacillus plantarum revealed that editing outcomes can vary across strains and between methods[J].Biotechnology Journal, 2019, 14(3):1700583.
[14] JIANG Y, CHEN B, DUAN C L, et al.Multigene editing in the Escherichia coli genome via the CRISPR-Cas9 system[J].Applied and Environmental Microbiology, 2015, 81(7):2506-2514.
[15] KONG L H, XIONG Z Q, SONG X, et al.Characterization of a panel of strong constitutive promoters from Streptococcus thermophilus for fine-tuning gene expression[J].ACS Synthetic Biology, 2019, 8(6):1469-1472.
[16] BISWAS I, JHA J K, FROMM N.Shuttle expression plasmids for genetic studies in Streptococcus mutans[J].Microbiology, 2008, 154(Pt 8):2275-2282.
[17] QUE Y A, FRANÇOIS P, HAEFLIGER J A, et al.Reassessing the role of Staphylococcus aureus clumping factor and fibronectin-binding protein by expression in Lactococcus lactis[J].Infection and Immunity, 2001, 69(10):6296-6302.
[18] 袁世豪, 张海琳, 鞠宁, 等.不同组成型启动子对乳酸菌表达系统外源基因表达影响的比较[J].中国畜牧兽医, 2023, 50(11):4370-4380.
YUAN S H, ZHANG H L, JU N, et al.Comparison of the effect of different constitutive promoters on exogenous gene expression in Lactobacillus expression system[J].China Animal Husbandry &Veterinary Medicine, 2023, 50(11):4370-4380.
[19] SONG X, HUANG H, XIONG Z Q, et al.CRISPR-Cas9(D10A) nickase-assisted genome editing in Lactobacillus casei[J].Applied and Environmental Microbiology, 2017, 83(22):e01259-17.
[20] SHAO B, RAMMOHAN J, ANDERSON D A, et al.Single-cell measurement of plasmid copy number and promoter activity[J].Nature Communications, 2021, 12(1):1475.
[21] LIU F F.Biosynthesis, processing and engineering of circularin A[D].Groningen:University of Groningen, 2023.
[22] NEWING T P, BREWSTER J L, FITSCHEN L J, et al.Redβ177 annealase structure reveals details of oligomerization and λ Red-mediated homologous DNA recombination[J].Nature Communications, 2022, 13:5649.
[23] RAUTRAY P, ROY A, EISENBART B.Application of bio-bricks &its benefits[J].Proceedings of the Design Society, 2023, 3:603-612.