乌鸡又名乌骨鸡、竹丝鸡,味道甘甜、性平,具有强身健体等功效。从中医学角度来说,乌鸡也被誉为滋补气血、益阴养颜的夫人良药[1]。温氏天露土乌鸡具有“7黑”特征,“黑嘴、黑眼、黑皮、黑肉、黑骨、黑脚、黑胶质”,土乌鸡生长环境优良,同时喂养五谷食料、天然水,给予高标准营养,如此生态条件下生长的鸡群,富含黑胶质、微量元素,低脂高蛋白,营养丰富,与其他品种乌鸡相似[2]。现在的人们更喜欢通过炖煮乌鸡汤的方法去食用,因为乌鸡汤相较其他汤类富含各种营养元素,ZOU等[3]研究发现,经过炖煮得到的鸡汤蛋白质等营养成分的溶出比其他方式更好。但在不同品种乌鸡的对比中发现略阳乌鸡的脂肪、黑色素及鲜味氨基酸等含量高于其他品种[4-5]。
衰老是随着年龄增长而出现的不可逆现象,衰老是一个氧化的过程,且许多病理过程的核心是氧化应激和衰老[6-7]。不健康的老龄化会同时伴随着心血管疾病、糖尿病等慢性疾病,有效的抗衰老已成为健康老龄化的必要条件[8],因此研究食品抗衰老的机理,开发延缓衰老的产品具有很大的现实意义。TU等[9]从泰和乌鸡肌肉中分离出黑色素,通过体外抗氧化指标证明其具有很强的抗氧化活性。刘茜等[10]使用略阳乌鸡汤干预D-半乳糖造模的小鼠,发现干预后的小鼠各脏器及血清中的过氧化氢酶(catalase,CAT)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)和超氧化物歧化酶(superoxide dismutase,SOD)活性显著升高,且乌鸡汤能抑制丙二醛(malondialdehyde,MDA)含量的积累,说明略阳乌鸡汤具有抗衰老的功效。但目前对于天露土乌鸡的抗衰老研究尚未深入。
秀丽隐杆线虫(Caenorhabditis elegans)是一种经典的模式生物,具有寿命短[11]、活动范围小、观察方便、实验周期短和基因组序列完整[12]等优点,其具有超过60%的人类同源基因[13]。目前,国内外已有大量将线虫模型应用于抗氧化、抗衰老、调节脂质代谢和防治神经退行性疾病的研究,构建了衰老模型、中枢系统模型[14-15]及肥胖模型[16]。本研究以秀丽隐杆线虫为模型,通过测定线虫寿命、运动能力、应激抵抗能力及体内抗氧化酶活力,探究天露土乌鸡汤(Tianlu black-bone chicken soup,TBCS)抗氧化、抗衰老的作用机制,以期为TBCS进一步开发利用成抗氧化、抗衰老功能性食品提供理论依据。
1 材料与方法
1.1 材料与试剂
市售天露土乌鸡(养殖天数75 d),广东温氏佳润食品有限公司;N2野生型秀丽隐杆线虫,美国秀丽隐杆线虫遗传中心;大肠杆菌OP50,上海南方模式生物科技股份有限公司;技术琼脂粉、胰蛋白胨、NaCl、链霉素硫酸盐,广东环凯微生物科技有限公司;CaCl2、MgSO4、K2HPO4、Na2HPO4、磷酸缓冲液,天津市环茂试剂厂;质量分数30%H2O2、乙醚,广州市化学试剂厂;CAT、SOD、GSH-Px体内抗氧化酶生化分析试剂盒、微量MDA分析试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
Labserv K3酶标仪,赛默飞世尔科技(中国)有限公司;JIDI-17R微量高速冷冻离心机,广州吉迪仪器有限公司;220FS火焰原子吸收光谱仪,瓦里安澳大利亚有限公司;L-8900全自动氨基酸分析仪,日立高新技术公司;SPX-150B-Z生化培养箱,上海博迅实业有限公司;PL203万分之一天平,上海舍岩仪器有限公司;LS-75HD高压灭菌锅,上海申安医疗器械厂;Varioskan TM LUX多功能酶标仪,美谷分子仪器(上海)有限公司;MZ101体视显微镜,广州市明美光电技术有限公司;Axio Observer A1倒置荧光显微镜,德国蔡司科学仪器有限公司;VCA800细胞破碎仪,美国康涅狄格州纽敦市超声材料公司。
1.3 实验方法
1.3.1 TBCS的制备
将天露土乌鸡的鸡头、爪、内脏去除,用清水清洗干净,按照鸡肉∶水=1∶4(质量比)将整鸡置于锅中,不添加任何调料,待水沸腾后开始计时,准确炖煮2 h。煮完得到的鸡汤通过分液漏斗先去除表面油分,随后将汤体放入-20 ℃冻存,为TBCS原汤样品。参考文献[17-18]的方法,对TBCS的蛋白质、脂肪、微量元素、游离氨基酸等基本成分进行测定。
1.3.2 实验分组
根据利树婵等[19]的方法并稍作修改,共分为4组:空白对照组(K)、TBCS高剂量组(WH)、TBCS中剂量组(WM)、TBCS低剂量组(WL)。K为双蒸水与OP50菌液以体积比1∶1混合;WH为炖煮出的TBCS样品与OP50菌液以体积比1∶1混合,不经过稀释;WM和WL分别为TBCS和双蒸水以体积比1∶2和1∶5稀释,并将稀释后的样品与OP50菌液以体积比1∶1混合。
1.3.3 TBCS对秀丽隐杆线虫体内抗衰老指标评价
1.3.3.1 线虫的培养传代及同期化
在20 ℃培养箱中于涂有大肠杆菌OP50的标准固体培养基(nematode growth medium,NGM)上培养线虫。秀丽隐杆线虫生长周期分为4个阶段,经过L1~L4期后即变为成虫,为雌雄同体,传代时将成虫转移至涂有大肠杆菌的新培养基上即可。
同期化是指通过实验操作,使原本处于不同发育阶段的线虫群体统一到同一特定时期,以确保实验材料的一致性。首先将线虫进行培养,至产卵期后在孵化出新虫之前用M9缓冲液将其冲下至EP管中,用1 mL裂解液(NaClO4∶NaOH∶H2O=1∶1∶1,体积比)将其裂解,在低速小离心机上离心振荡2 min,去除上清液后用M9缓冲液冲洗2次,再次离心后去除上清液,保留0.4 mL左右含有线虫的液体,用移液枪将其混匀并滴于含有大肠杆菌的NGM区域,48 h后虫卵发育成成虫,同期化完成,可进行后续实验。
1.3.3.2 线虫的寿命的测定
参考CUI等[20]的方法将同期化完成的成虫挑取在涂有样品的NGM上,每组3个板,每个板30条虫,在恒温20 ℃培养箱培养。从挑取时刻开始,记为第0天,前6 d每日转至滴有样品的新NGM板上,6 d后每隔1 d转1次板,记录每日的生存死亡线虫数,直至线虫全部死亡。线虫死亡标准:用线虫挑虫针刺碰其身体,若无任何反应即死亡。同时每日还需剔除异常死亡虫数:1)爬在培养基壁上至干死线虫数;2)转板操作失误造成的线虫死亡数;3)钻进培养基内丢失的线虫数。最后完成记录绘制线虫生存曲线。
1.3.3.3 线虫运动能力的测定
参考吕晨豪等[21]的方法,分为3个部分:线虫运动评价、线虫弯曲频率、线虫摆头次数。运动评价实验与线虫寿命实验同时进行,在线虫实验进行至1、4、8、12、16 d进行。
线虫运动评价:分为A、B、C 3个等级,其中A等级为线虫不需触碰能够自主运动;B等级为线虫无自主运动,挑虫针触碰其身体后会自主运动;C等级为用挑虫针触碰其身体后不会自主运动,只会做摆头运动。
弯曲频率与线虫摆头次数实验方法:用样品干预线虫5 d,每组挑取其中10条线虫,分别测定其30 s内身体做正弦运动的次数以及30 s内摆头的次数。
1.3.3.4 线虫生殖能力的测定
参考李苏婉等[22]的方法,将同期化完成的线虫挑取在涂有样品的NGM上,每组5个板,每个板2条虫,每天将板上的线虫转移至新板上,并将旧板于20 ℃恒温培养箱中培养48 h后进行计数,记录每日产卵量直至线虫不再产卵。
1.3.3.5 线虫抗应激能力测定
热应激实验:参考黄少杰等[23]的方法,用样品干预同期化完成的线虫5 d,转移至空白NGM上,每组3个板,每个板20条虫,随即将板放置在37 ℃培养箱中,每隔1 h记录线虫的生存死亡数量,至所有线虫死亡。
氧化应激实验:参考张余威等[24]的方法,用样品干预同期化完成的线虫5 d,转移至空白NGM上,每组3个板,每个板20条虫,随即转移至含有质量分数为0.1%H2O2的NGM上,每隔1 h记录线虫的生存死亡数量,至所有线虫死亡。
1.3.3.6 线虫体内脂褐质水平测定
参考刘泽坤等[25]的方法,用样品干预同期化完成的线虫7 d,每组1个板,每个板20条虫,干预完后用M9缓冲液将板上所有线虫冲洗至EP管,用左旋咪唑碱麻醉线虫后转移至2%琼脂糖凝胶垫片上,随后在倒置荧光显微镜下(激发波长365 nm、发射波长420 nm)通过单色数码相机获取线虫荧光图像,再用Image J软件对图像进行荧光强度分析测定。
1.3.3.7 线虫体内抗氧化酶活性测定
参考XU等[26]的方法用样品干预同期化完成的线虫5 d,每组3个板,每个板100条虫。干预完成后用M9缓冲液将线虫冲下至EP管中,随即加入研磨珠并在冷冻研磨机上(60 Hz,10 min)研磨,研磨完成放入高速离心机以12 000 r/min离心10 min,吸取上清液,根据说明书要求进行测定。
1.4 数据统计与分析
所有测定的实验结果均用“平均值±标准差”表示,采用Graphpad 8.0 Prism和Excel 2003进行数据作图与处理,使用one-way ANOVA分析法进行多组间显著性分析,P<0.05表示有统计学显著差异,P<0.01表示统计学差异极其显著。
2 结果与分析
2.1 TBCS基本营养成分
乌鸡汤因其高营养价值和独特的药用功效,被广泛用于滋补保健。微量元素是维持机体正常代谢活动的重要营养素,是生命活动和健康老化的重要组成部分。必需氨基酸在抗衰老中起着关键作用,是维持机体正常代谢、修复细胞损伤和延缓老化的重要营养素,如亮氨酸通过激活mTOR信号通路促进蛋白质合成,防止肌肉流失,改善与衰老相关的代谢问题[27]。如表1所示,TBCS蛋白质含量达到1.88 g/100 mL,脂肪含量为1.39 g/100 mL,对比中国食物成分表中的鸡汤具有更高的蛋白和更低的脂肪[28]。微量元素中,TBCS的钙元素和钾元素显著高于其他元素,镁元素和锌元素含量也较高。镁元素和锌元素对减缓衰老都有一定的作用,如硒元素可以重塑由氧化应激引起的渐进和自发的生理变化,参与抗氧化防御[29-30]。TBCS的游离氨基酸分析结果表明,牛磺酸、谷氨酸、丝氨酸、丙氨酸、苏氨酸、甘氨酸、精氨酸的含量显著高于其他氨基酸,其中此汤中牛磺酸含量为达到67.02 mg/L。研究表明,牛磺酸缺乏可能加速衰老进程,而补充牛磺酸有助于延缓衰老[31],提示其可能通过补充牛磺酸,发挥潜在的抗衰老作用。
表1 TBCS基本营养成分
Table 1 Basic nutritional composition of TBCS
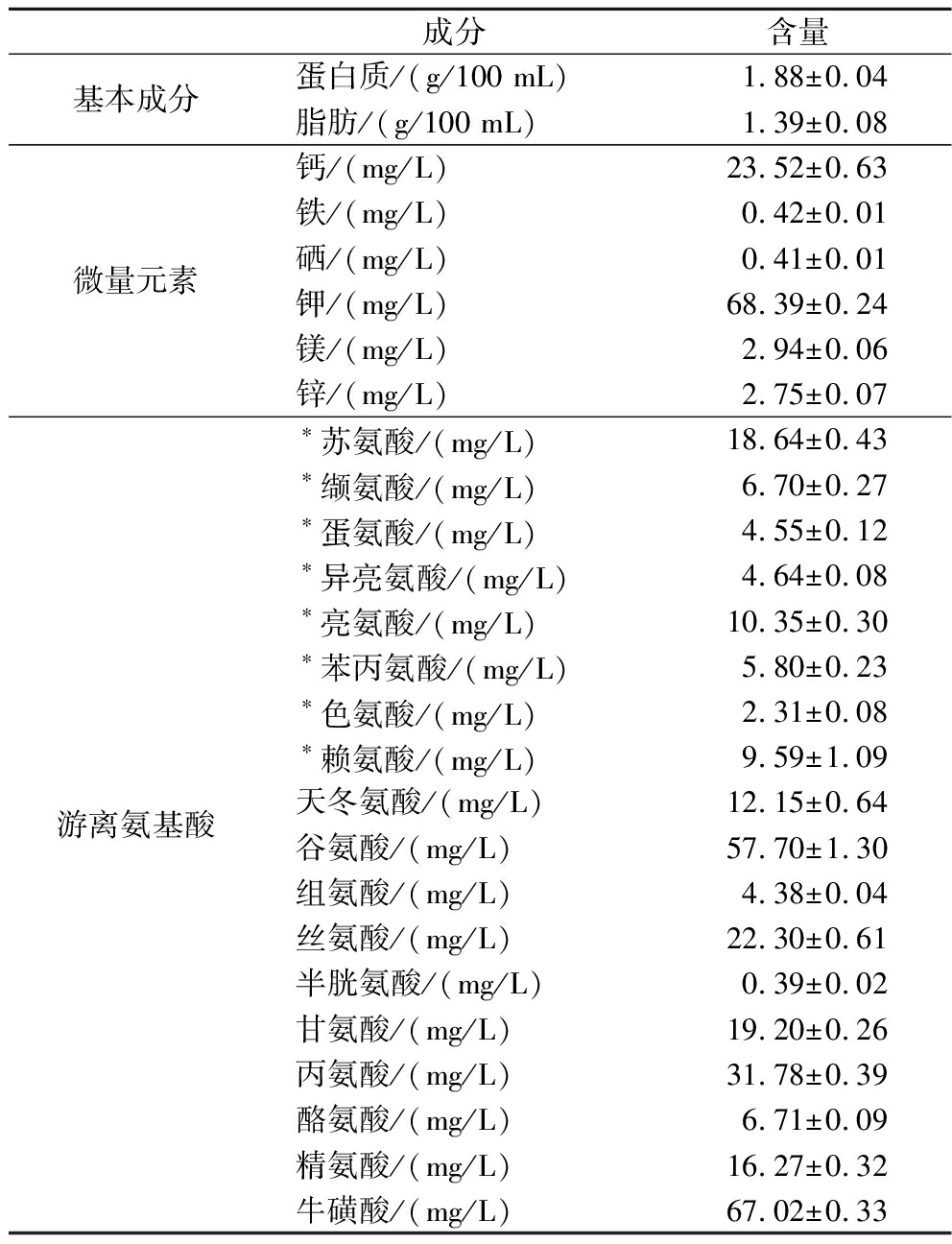
成分含量基本成分蛋白质/(g/100 mL)1.88±0.04脂肪/(g/100 mL)1.39±0.08微量元素钙/(mg/L)23.52±0.63铁/(mg/L)0.42±0.01硒/(mg/L)0.41±0.01钾/(mg/L)68.39±0.24镁/(mg/L)2.94±0.06锌/(mg/L)2.75±0.07游离氨基酸∗苏氨酸/(mg/L)18.64±0.43∗缬氨酸/(mg/L)6.70±0.27∗蛋氨酸/(mg/L)4.55±0.12∗异亮氨酸/(mg/L)4.64±0.08∗亮氨酸/(mg/L)10.35±0.30∗苯丙氨酸/(mg/L)5.80±0.23∗色氨酸/(mg/L)2.31±0.08∗赖氨酸/(mg/L)9.59±1.09天冬氨酸/(mg/L)12.15±0.64谷氨酸/(mg/L)57.70±1.30组氨酸/(mg/L)4.38±0.04丝氨酸/(mg/L)22.30±0.61半胱氨酸/(mg/L)0.39±0.02甘氨酸/(mg/L)19.20±0.26丙氨酸/(mg/L)31.78±0.39酪氨酸/(mg/L)6.71±0.09精氨酸/(mg/L)16.27±0.32牛磺酸/(mg/L)67.02±0.33
注:*必需氨基酸。
2.2 TBCS秀丽隐杆线虫抗衰老实验
2.2.1 TBCS对秀丽隐杆线虫寿命的影响
秀丽隐杆线虫的寿命是评价衰老的重要指标[32]。如图1和表2所示,经过TBCS干预的线虫比空白对照组K的线虫的平均寿命、中位寿命及最长寿命都有提高。其中,WH、WM、WL的平均寿命对比空白组分别提高了27.16%、26.05%以及20.00%,且WH、WM、WL对比起空白对照组均具有显著性差异(P<0.05)。此外,TBCS还能提高线虫的最长寿命,空白组最长寿命约为24 d,WH组的最长寿命可达约28 d。以上结果表明经过TBCS的干预能够有效延长线虫的寿命。TBCS牛磺酸含量较高,有研究表明牛磺酸可以提高线虫的寿命延缓衰老[33],与该结果相似。
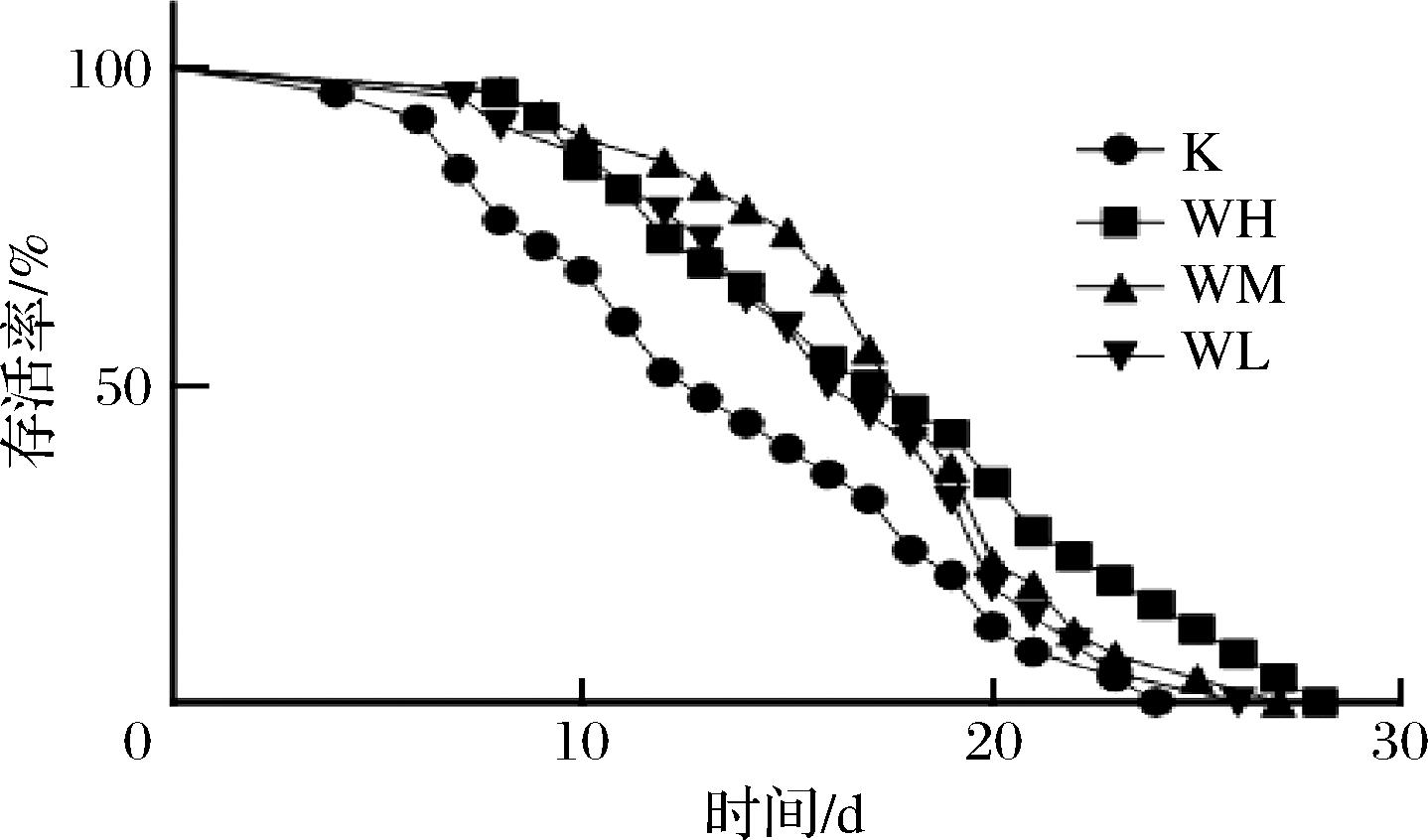
图1 TBCS对秀丽隐杆线虫寿命的影响
Fig.1 Effect of TBCS on the longevity of C.elegans
表2 TBCS对秀丽隐杆线虫平均寿命、中位寿命及最长寿命的影响
Table 2 Effect of TBCS on mean, median, and maximum life span of C.elegans
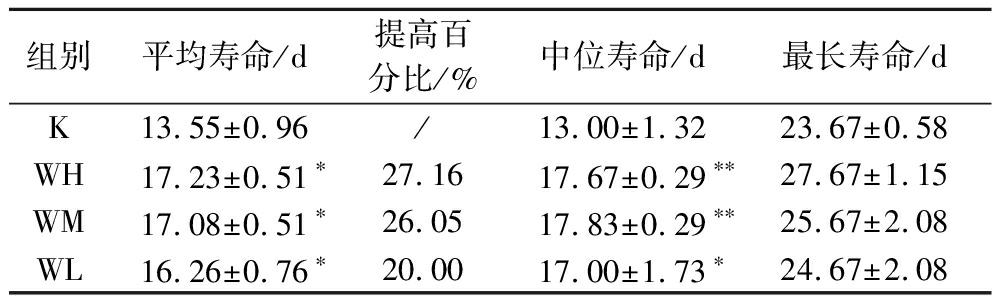
组别平均寿命/d提高百分比/%中位寿命/d最长寿命/dK13.55±0.96/13.00±1.3223.67±0.58WH17.23±0.51∗27.1617.67±0.29∗∗27.67±1.15WM17.08±0.51∗26.0517.83±0.29∗∗25.67±2.08WL16.26±0.76∗20.0017.00±1.73∗24.67±2.08
注:*P<0.05;**P<0.01,与空白组比较(下同)。
2.2.2 TBCS对秀丽隐杆线虫运动能力的影响
如图2-a所示,线虫运动能力随着时间的推移活力不断下降,在第0天和第4天,各组的运动能力差别不大。在第8天时,空白对照组出现C等级线虫,而经过TBCS干预的线虫组均未出现,大部分仍为A等级,小部分为B等级。到第12天的时候,空白对照组和WL的C等级线虫占比相近,而WH和WM的乌鸡汤组线虫出现少部分C等级,空白对照组中A等级线虫占比最少,仅45.50%。第16天时,每组大部分为B等级,A等级对比第12天显著性减少,最少为空白组,占比13.30%,最多为WH和WM,分别占比32.30%和31.10%,C等级线虫中仍是空白组占比最多。如图2-b和2-c所示,经过干预后TBCS组线虫摆头次数及弯曲频率比空白对照组都有一定程度上的提高,其中WH在统计学上具有显著性(P<0.05)。有研究表明,乌鸡汤具有一定的抗疲劳功能[34],与本研究结果相似,说明经过TBCS的干预,能够有效提高线虫的运动能力。
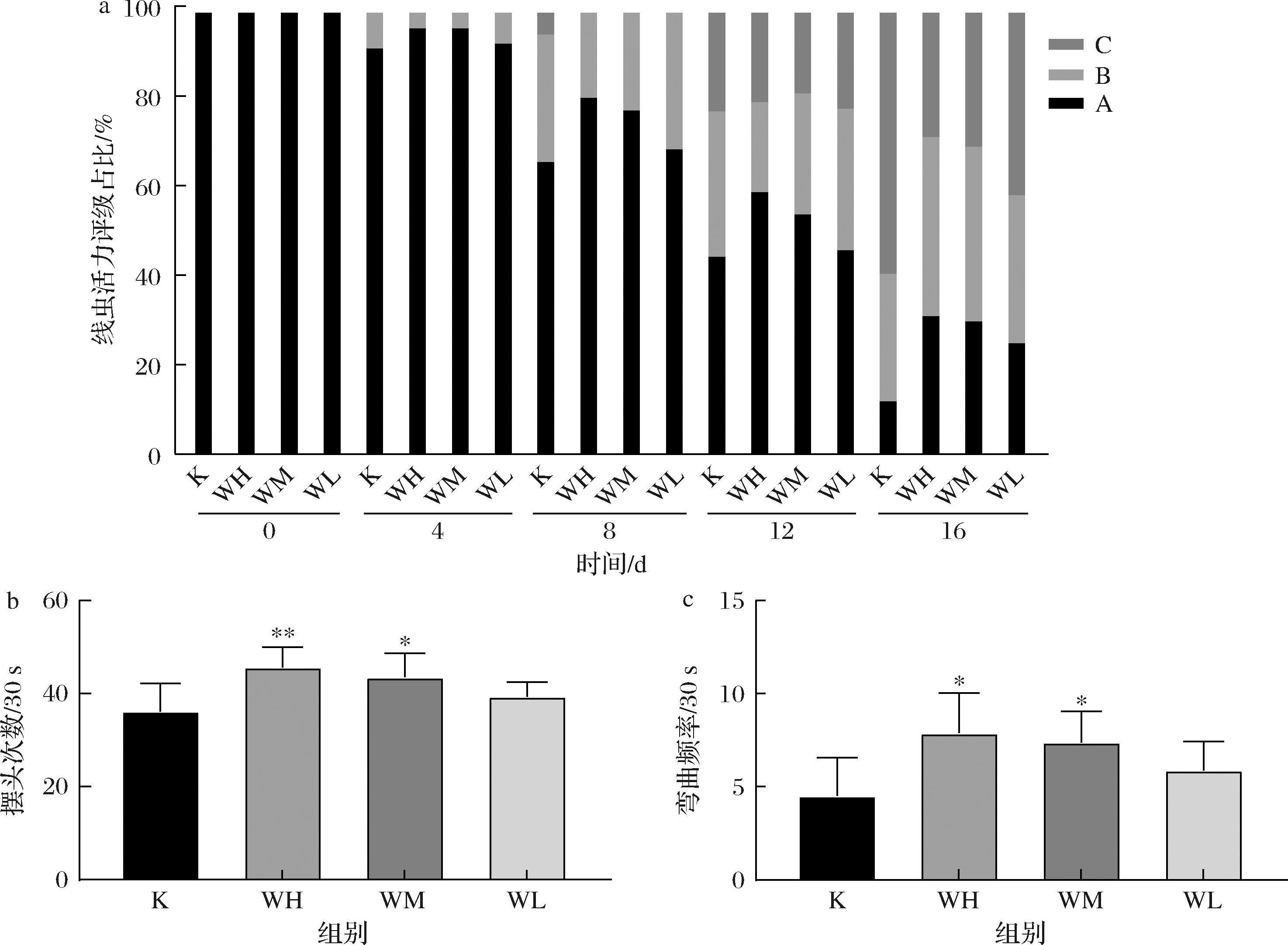
a-线虫运动能力评价;b-线虫摆头次数;c-线虫弯曲频率
图2 TBCS对秀丽隐杆线虫运动能力的影响
Fig.2 Effect of TBCS on locomotion ability of C.elegans
注:*P<0.05,**P<0.01,与空白组比较。
2.2.3 TBCS对秀丽隐杆线虫生殖能力的影响
如图3-a所示,线虫在经过TBCS干预的前3 d的产卵量较大,第3天开始线虫产卵量开始下降,直到第5天产卵量最少,几乎不产卵,但是每天各组线虫间并无显著性差异。如图3-b所示,可以看出WH和WM总产卵量最多,但是各组相比并无显著性差异。说明线虫经过TBCS的干预后,在提高线虫平均寿命的同时并不会对其生殖能力造成损伤。
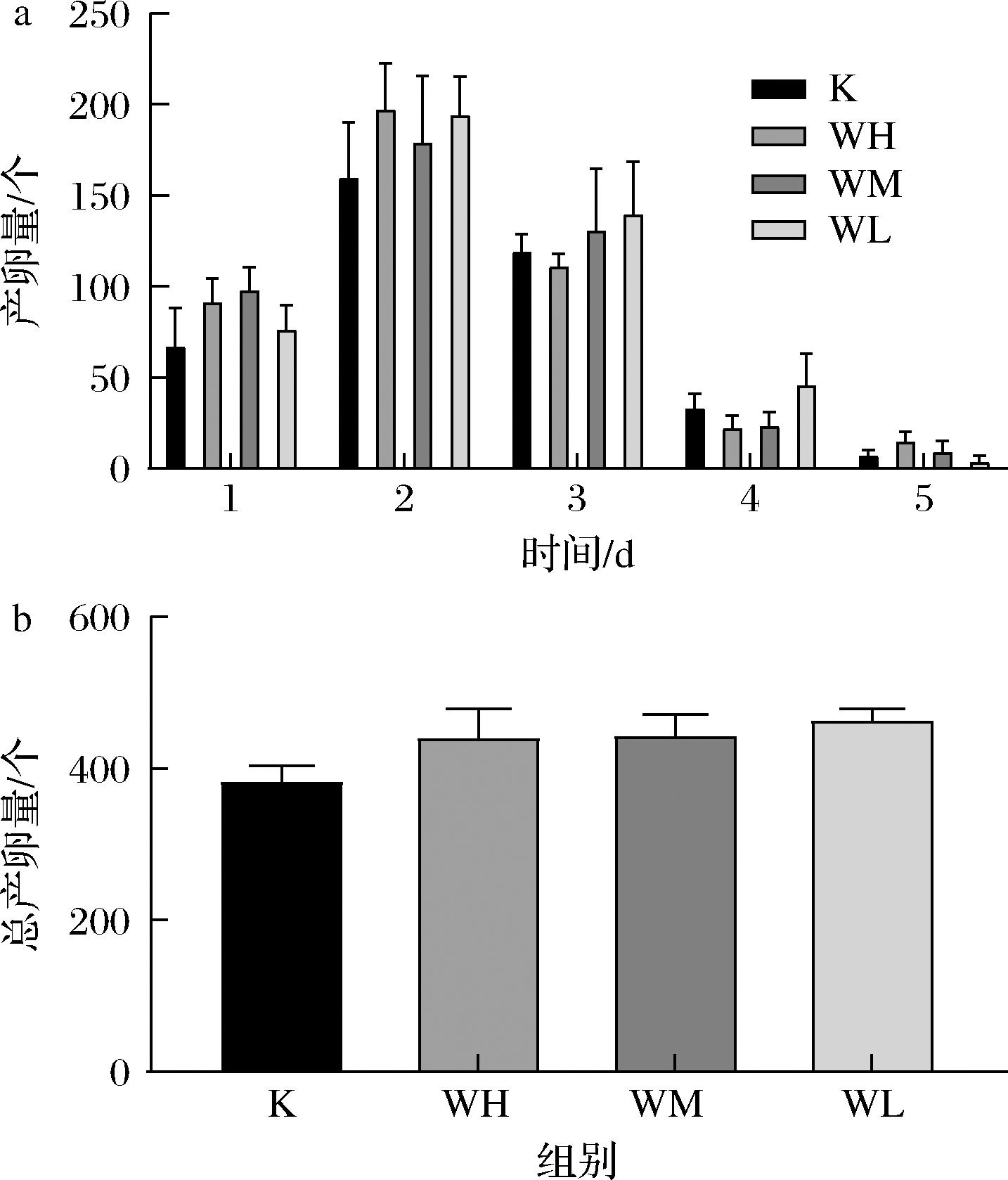
a-日产卵量;b-总产卵量
图3 TBCS对秀丽隐杆线虫生殖能力的影响
Fig.3 Effect of TBCS on reproductive ability of C.elegans
2.2.4 TBCS对秀丽隐杆线虫抗应激能力的影响
秀丽隐杆线虫抗应激能力与衰老密切相关,随着线虫年龄的增长,其应对环境压力的能力逐渐减弱,这些生理变化导致细胞内有害物质堆积,进而促进机体老化[35]。TBCS对秀丽隐杆线虫抗应激能力的影响结果如图4及表3所示,在热应激的结果中,经过WH和WM干预的线虫抗热应激能力显著提高,平均寿命分别提高24.27%和21.09%。WH最长寿命达到16 h,WM最长寿命达到15 h,WL和空白对照组最长寿命分别为14 h和13 h,说明TBCS能够显著提高线虫的抗热应激能力。在抗氧化应激的实验中,利用了质量分数为0.1%的H2O2构建氧化环境,造成线虫的氧化损伤,结果可看出经过TBCS的干预线虫抗氧化应激能力也有明显提高,空白对照组平均寿命为4.00 h,WH和WM跟空白对照组对比提升较为明显,分别提升41.25%和31.25%,但在平均寿命上对比空白对照组无显著性差别。在最长寿命中,WH和WM组线虫最长达到12 h,而WL和空白对照组最长仅为10 h和8 h,说明TBCS能够提高抗氧化应激能力,且随着剂量的提高而提高,具有剂量依赖性。有研究表明,亮氨酸、异亮氨酸和缬氨酸能改善线粒体自噬,清除受损线粒体等进而提高线虫抗应激能力[36],TBCS中含有丰富的游离氨基酸成分,因此推测TBCS对线虫抗应激能力的提升与此有关。
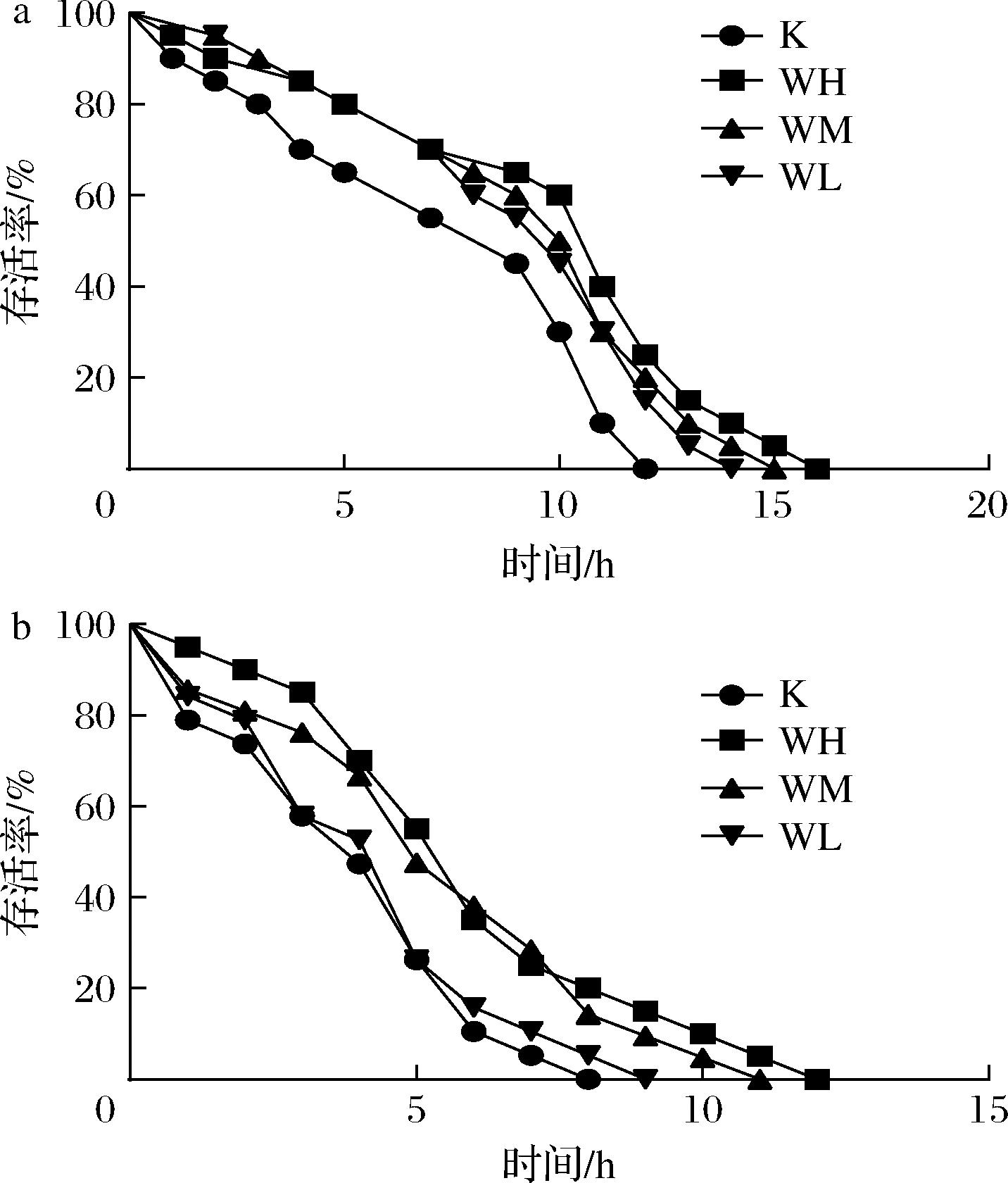
a-热应激实验;b-氧化应激实验
图4 TBCS对秀丽隐杆线虫抗应激能力的影响
Fig.4 Effect of TBCS on stress resistance of C.elegans
表3 TBCS对秀丽隐杆线虫抗应激寿命的影响
Table 3 Effect of TBCS on stress resistance lifespan of C.elegans
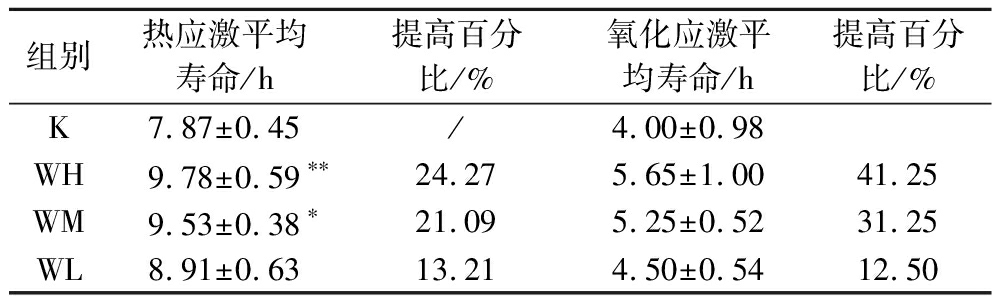
组别热应激平均寿命/h提高百分比/%氧化应激平均寿命/h提高百分比/%K7.87±0.45/4.00±0.98WH9.78±0.59∗∗24.275.65±1.0041.25WM9.53±0.38∗21.095.25±0.5231.25WL8.91±0.6313.214.50±0.5412.50
2.2.5 TBCS对秀丽隐杆线虫脂褐质水平的影响
脂褐质是一种在生物体整个生命周期中逐渐形成的色素颗粒,主要由自噬和脂质过氧化过程中的代谢产物聚合而成。由于它难以被降解,会在溶酶体内不断沉积,进而削弱溶酶体的功能,导致细胞代谢废物的清除效率降低,这种积累现象与衰老进程密切相关,因此常被用作衡量衰老程度的生物学标志物[37]。如图5、图6所示,经过TBCS干预的线虫荧光强度比空白对照组线虫荧光强度暗,说明空白对照组的线虫脂褐素堆积较TBCS组的高,脂褐质素堆积较为明显。从测定的平均荧光强度值上看,可看出WH组和WM组的比于空白对照组具有极其显著差异(P<0.01),其中空白对照组是WH组脂褐质荧光强度的3.13倍(P<0.001),差异极其显著。此外,WL的平均荧光强度值相比WH也具有显著性差异(P<0.05),说明TBCS对线虫体内脂褐质水平的影响还具有剂量依赖性。关于细胞和生物体衰老的主流观点之一是脂褐质素在细胞内逐渐积累,导致细胞和器官功能衰退,也叫衰老的自由基理论[38]。有研究表明乌鸡体内黑色素含量高,其能有效地清除自由基水平[39],该实验结果也表明TBCS能够明显改善脂褐质的堆积水平。
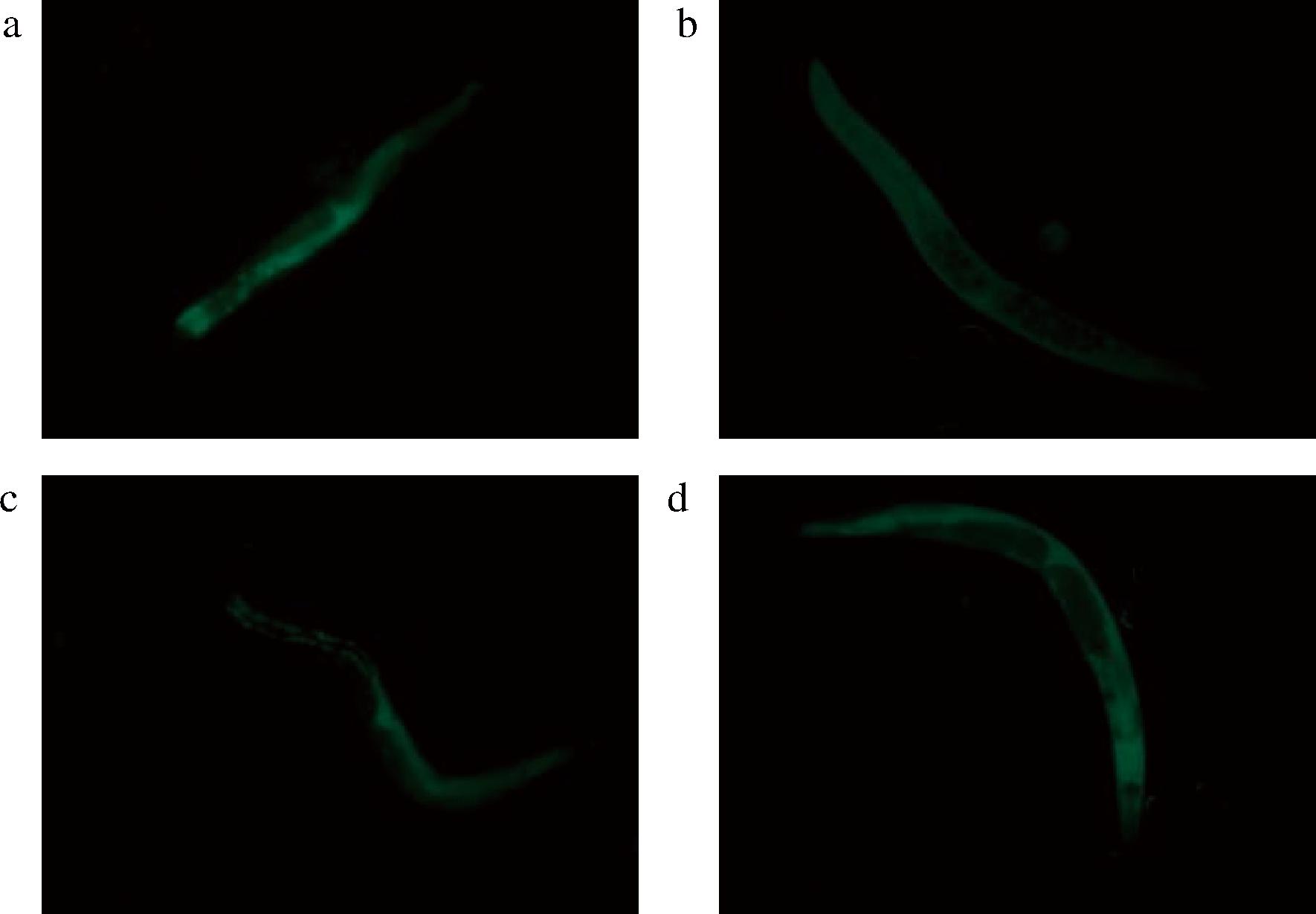
a-K;b-WH;c-WM;d-WL
图5 L4期秀丽隐杆线虫脂褐质水平荧光图像(×100)
Fig.5 Fluorescence image of lipofuscin levels in C.elegans L4 stage (×100)
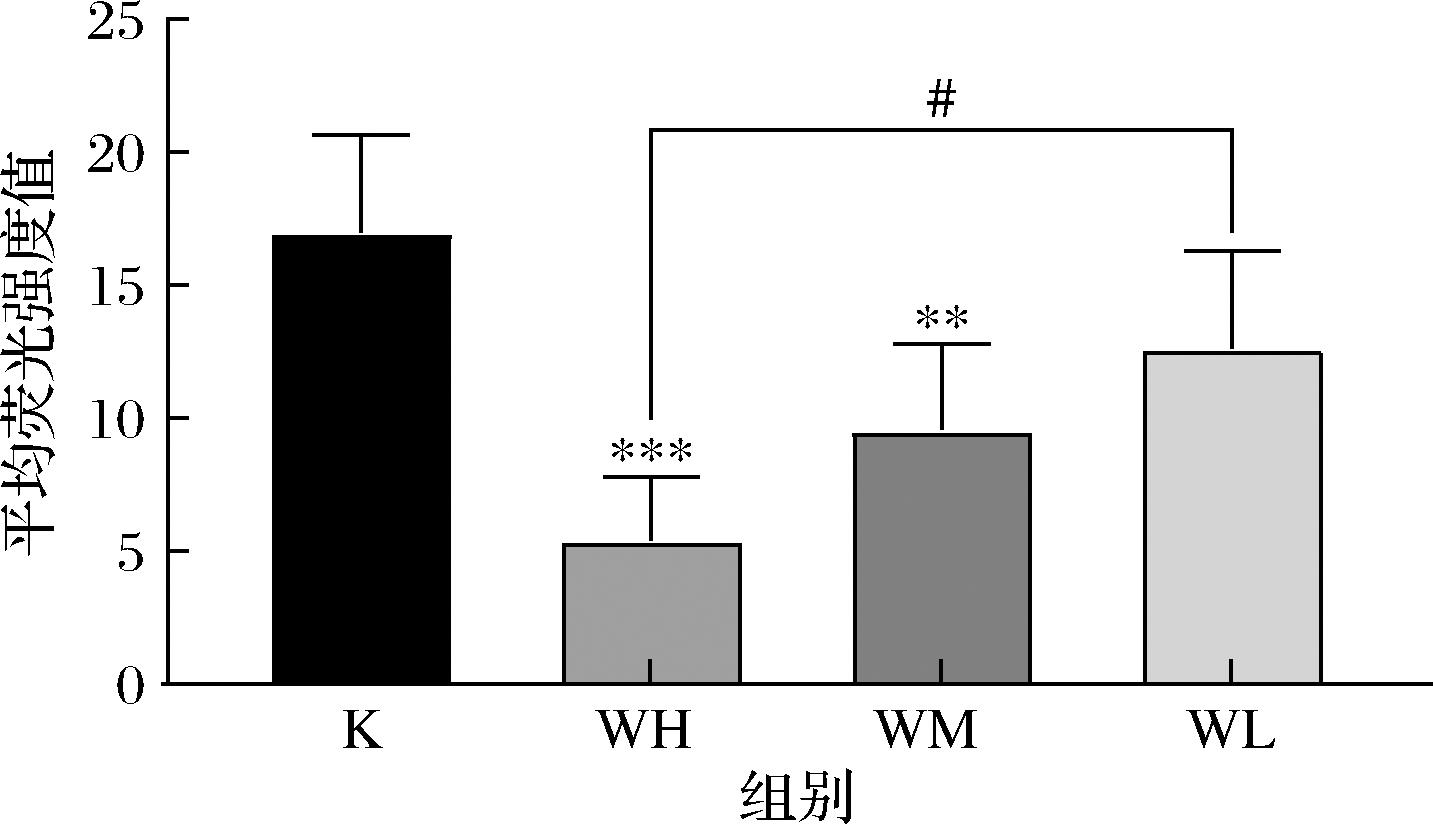
图6 TBCS对秀丽隐杆线虫脂褐质水平平均荧光强度值的影响
Fig.6 Effect of TBCS on the average fluorescence intensity of lipofuscin levels in C.elegans
注:*P<0.05,**P<0.01,***P<0.001,与空白组比较;#P<0.05,与WH比较(下同)。
2.2.6 TBCS对秀丽隐杆线虫体内抗氧化酶活性及丙二醛含量的影响
在秀丽隐杆线虫中,SOD、CAT以及GSH-Px等抗氧化酶系统在调控氧化还原平衡中发挥核心作用,已有研究证实,随着线虫衰老,其体内的活性氧含量逐渐积累,而抗氧化酶的活性则呈现下降趋势,进而引发蛋白质氧化、脂质过氧化及DNA损伤的累积,最终影响其寿命[40]。如图7-a和图7-b所示,经过TBCS干预的线虫能够显著性提高体内的SOD和CAT活力,其中WH、WM、WL均能显著性提高CAT活力(P<0.05),WH极其显著(P<0.001)。SOD活力中WH对比空白对照组提高了75.74%,具有显著性差异(P<0.05),提示其可能通过稳定SOD酶活性来增强抗氧化防御。如图7-c所示,不同质量浓度的TBCS均能提高线虫体内GSH-Px活力,其中WH和WM线虫体内的GSH-Px活力对比空白对照组显著性提高(P<0.01),具有剂量依赖。MDA是脂质过氧化的最终产物之一,其含量变化与细胞氧化损伤及衰老进程密切相关。如图7-d所示,线虫体内MDA的积累在经过TBCS的干预后都具有不同程度的降低,WH、WM、WL比空白对照组分别降低33.15%、31.45%、15.51%,说明TBCS能有效抑制线虫生长过程中体内MDA的积累,且具有剂量-效应关系。研究表明,略阳乌鸡汤能显著增强小鼠体内抗氧化酶活性并降低MDA含量,从而延缓衰老[10]。本研究结果与之相符,说明TBCS可能通过改善抗氧化系统,上调体内抗氧化酶CAT、SOD等的活性,降低体内MDA水平,有效发挥其抗衰老作用。
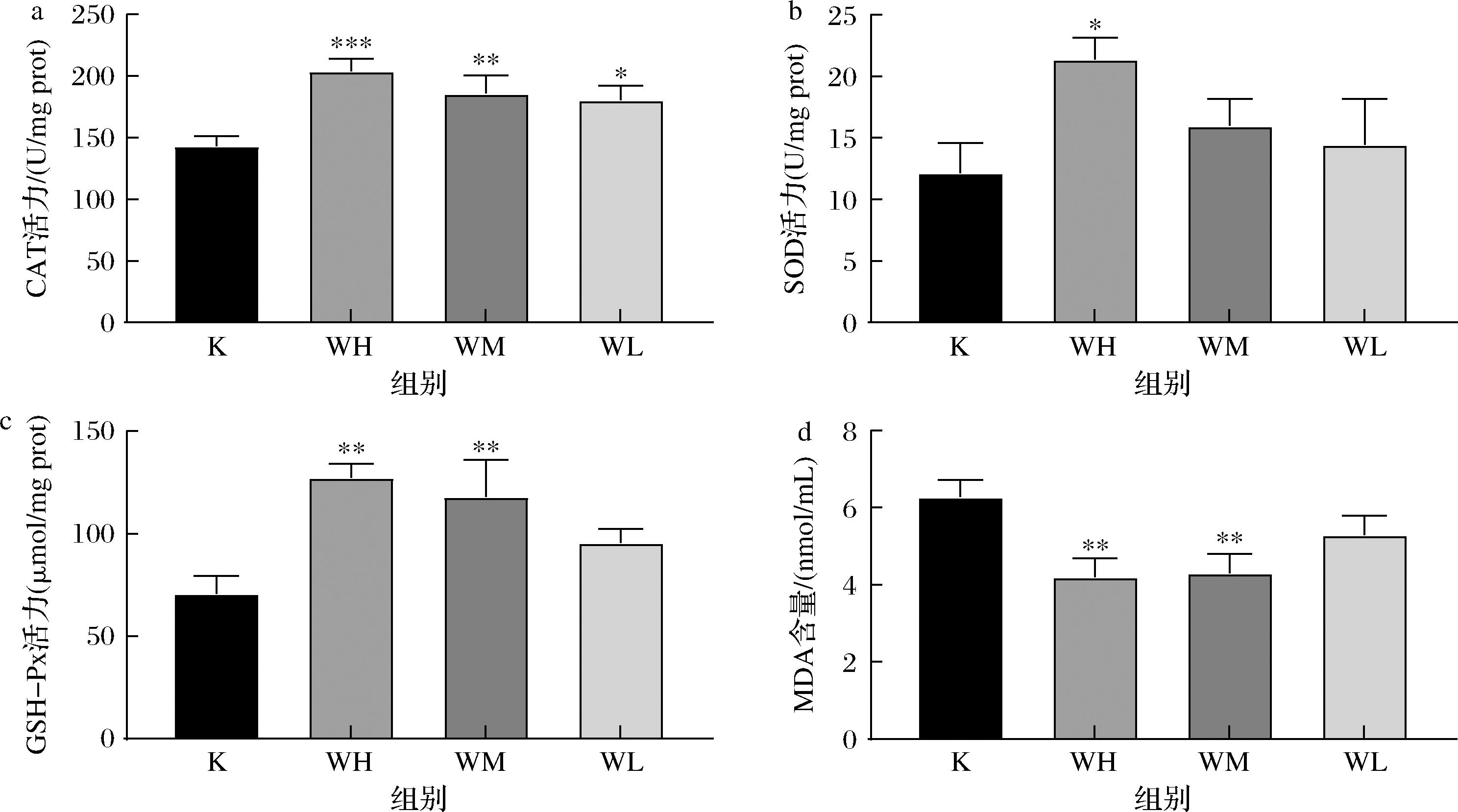
a-CAT水平;b-SOD水平;c-GSH-Px水平;d-MDA含量
图7 TBCS对秀丽隐杆线虫体内抗氧化酶活性及丙二醛含量的影响
Fig.7 Effect of TBCS on antioxidant enzyme activity in C.elegans
3 结论与讨论
本实验通过测定TBCS的营养成分,包括蛋白质、脂肪、微量元素及游离氨基酸含量,再使用秀丽隐线虫模型,评价了不同浓度TBCS对于线虫体内抗衰老的作用。结果表明,TBCS的蛋白含量高,脂肪含量较低,富含多种微量元素、游离氨基酸,牛磺酸达到67.02 mg/L,具有很高的营养价值,能够有效通过多种机制作用于人体,改善代谢,延缓衰老。线虫实验中发现,用TBCS饲喂线虫对比空白组均能有效提高线虫平均寿命和运动能力,平均寿命提高27.16%,且在此同时不会损伤线虫的生殖能力。除此之外TBCS还能显著提高线虫的抗应激能力,热应激和氧化应激条件下存活时间分别提高24.27%和41.25%。此外,TBCS能够显著降低线虫体内脂褐质素和MDA的堆积,显著提高线虫体内抗氧化酶CAT、SOD、GSH-Px的活力。综上所述,本研究制备的TBCS对秀丽隐杆线虫具有良好的抗氧化与抗衰老的作用。然而,本研究仍存在一定局限性,如线虫模型与高等动物的差异、TBCS关键活性成分尚未明确、分子机制需进一步解析等。未来需结合哺乳动物实验和更深入的机制研究,以推动TBCS在抗衰老功能食品中的应用。本研究同时也为TBCS抗衰老作用机制的研究提供了有力依据,也为乌鸡汤健康食品的开发提供参考。
[1] 王永寿. 乌骨鸡:女性滋补良药[J].临床研究, 1998(2):15.
WANG Y S.Black-bone chicken:A nourishing medicine for women[J].Medicine and Health Care, 1998(2):15.
[2] 王景升, 张时煌, 王彤, 等.泰和乌鸡肉营养成分特征分析[J].经济动物学报, 2019, 23(1):23-28.
WANG J S, ZHANG S H, WANG T, et al.Characteristics analysis of nutritional components in meat of Taihe silky fowl[J].Journal of Economic Animal, 2019, 23(1):23-28.
[3] ZOU J, XU M J, ZOU Y F, et al.Chemical compositions and sensory characteristics of pork rib and Silkie chicken soups prepared by various cooking techniques[J].Food Chemistry, 2021, 345:128755.
[4] 马博闻, 杨欣婷, 余雅男, 等.不同品种乌鸡肌肉品质与仿生感官评价研究[J].食品工业科技, 2024, 45(22):217-224.
MA B W, YANG X T, YU Y N, et al.Evaluation of muscle quality and biomimetic sensory evaluation of different breeds of black-boned chicken[J].Science and Technology of Food Industry, 2024, 45(22):217-224.
[5] 何洋, 杜彦丽, 王坤, 等.乌骨鸡黑色素合成、转运及分布机制的研究进展[J].中国家禽, 2020, 42(9):89-95.
HE Y, DU Y L, WANG K, et al.Research progress on synthesis, transport and distribute of melanin mechanisms in black-bone chicken[J].China Poultry, 2020, 42(9):89-95.
[6] WANG H P, BASISTY N, QU J H, et al.Editorial:Multi-omics studies on aging and age-related diseases[J].Frontiers in Cell and Developmental Biology, 2024, 12:1374424.
[7] BARRERA-V ZQUEZ O S, MONTENEGRO-HERRERA S A, MART
ZQUEZ O S, MONTENEGRO-HERRERA S A, MART NEZ-ENR
NEZ-ENR QUEZ M E, et al.Selection of Mexican medicinal plants by identification of potential phytochemicals with anti-aging, anti-inflammatory, and anti-oxidant properties through network analysis and chemoinformatic screening[J].Biomolecules, 2023, 13(11):1673.
QUEZ M E, et al.Selection of Mexican medicinal plants by identification of potential phytochemicals with anti-aging, anti-inflammatory, and anti-oxidant properties through network analysis and chemoinformatic screening[J].Biomolecules, 2023, 13(11):1673.
[8] GOTO S.Is biological aging a treatable disease? A consideration based on proposed mechanisms of aging[J].Yakugaku Zasshi, 2024, 144(4):419-429.
[9] TU Y G, SUN Y Z, TIAN Y G, et al.Physicochemical characterisation and antioxidant activity of melanin from the muscles of Taihe Black-bone silky fowl (Gallus gallus domesticus Brisson)[J].Food Chemistry, 2009, 114(4):1345-1350.
[10] 刘茜, 赵浩名, 王令, 等.略阳乌鸡汤对D-半乳糖致衰老小鼠不同组织的保护作用[J].食品工业科技, 2022, 43(17):402-409.
LIU X, ZHAO H M, WANG L, et al.Protective effect of Lüeyang black-bone chicken soup on different tissues of D-galactose-induced aging mice[J].Science and Technology of Food Industry, 2022, 43(17):402-409.
[11] WU C Y, DAVIS S, SAUDAGAR N, et al.Caenorhabditis elegans as a convenient animal model for microbiome studies[J].International Journal of Molecular Sciences, 2024, 25(12):6670.
[12] SEHGAL E, WOHLENBERG C, SOUKUP E M, et al.High-resolution reconstruction of a C.elegans ribosome sheds light on evolutionary dynamics and tissue specificity[J].RNA, 2024, 30(11):1513-1528.
[13] ZHU A, ZHENG F L, ZHANG W J, et al.Oxidation and antioxidation of natural products in the model organism Caenorhabditis elegans [J].Antioxidants, 2022, 11(4):705.
[14] KHAJEZADE M, GOLIAEI S, VEISI H.A game-theoretical network formation model for C.elegans neural network[J].Frontiers in Computational Neuroscience, 2019, 13:45.
[15] ONODERA K, TORIKAI H.A novel design method of simplified central nervous system model of C.elegans based on hybrid dynamics of sequential logic and numerical integration[J].IEICE Electronics Express, 2023, 20(10):20230110.
[16] 贾董浩, 周心雨, 詹恩琪, 等.苦瓜多糖和皂苷对秀丽隐杆线虫脂代谢的调节作用[J].粮食与食品工业, 2023, 30(5):28-32.
JIA D H, ZHOU X Y, ZHAN E Q, et al.Effects of bitter melon polysaccharides and saponins on lipid metabolism in C.elegans[J].Cereal &Food Industry, 2023, 30(5):28-32.
[17] HU B, HAN L Y, KONG H L, et al.Preparation and emulsifying properties of trace elements fortified gum Arabic[J].Food Hydrocolloids, 2019, 88:43-49.
[18] 邹金浩, 林耀盛, 杨怀谷, 等.岭南黄鸡炖鸡汤过程中营养及风味物质的变化[J].现代食品科技, 2021, 37(11):328-337.
ZOU J H, LIN Y S, YANG H G, et al.Changes of nutrients and flavor substances in Lingnan yellow chicken stewed chicken soup[J].Modern Food Science and Technology, 2021, 37(11):328-337.
[19] 利树婵, 陈扬, 李雅琪, 等.发酵祛湿汤体外抗氧化活性及对秀丽隐杆线虫抗衰老作用[J].现代食品科技, 2024, 40(3):39-47.
LI S C, CHEN Y, LI Y Q, et al.Antioxidant activity of fermented Qushi decoction in vitro and its anti-aging effect on Caenorhabditis elegans[J].Modern Food Science &Technology, 2024, 40(3):39-47.
[20] CUI X D, ZHANG B R, LI Z, et al.Zhuyeqing liquor promotes longevity through enhancing stress resistance via regulation of SKN-1 and HSF-1 transcription factors in Caenorhabditis elegans[J].Experimental Gerontology, 2023, 174:112131.
[21] 吕晨豪, 李俊健, 陈昶安, 等.发酵陈皮水提物体外抗氧化活性及对秀丽隐杆线虫抗衰老作用[J].食品工业科技, 2023, 44(17):428-437.
LÜ C H, LI J J, CHEN C A, et al.Anti-aging and in vitro antioxidant effects of water extracts of fermented pericarpium citri reticulatae on Caenorhabditis elegans[J].Science and Technology of Food Industry, 2023, 44(17):428-437.
[22] 李苏婉, 郝梦真, 姜玉池, 等.高氯酸盐对秀丽隐杆线虫生长发育的影响[J].中国食品学报, 2024, 24(6):155-164.
LI S W, HAO M Z, JIANG Y C, et al.Effect of perchlorate on the growth and development of Caenorhabditis elegans and its mechanism[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(6):155-164.
[23] 黄少杰, 陈宏著, 钟淳菲, 等.铁皮石斛叶多糖对秀丽隐杆线虫体内抗衰老作用[J].食品科学, 2022, 43(21):203-208.
HUANG S J, CHEN H Z, ZHONG C F, et al.Anti-aging effect of polysaccharide from Dendrobium officinale leaves in Caenorhabditis elegans[J].Food Science, 2022, 43(21):203-208.
[24] 张余威, 赵文俊, 李伟杰, 等.灭活芽孢杆菌DU-106对秀丽隐杆线虫的抗衰老作用[J].食品科学, 2023, 44(23):134-141.
ZHANG Y W, ZHAO W J, LI W J, et al.Anti-aging effect of inactivated Bacillus sp.DU-106 in Caenorhabditis elegans[J].Food Science, 2023, 44(23):134-141.
[25] 刘泽坤, 贺小芳, 洪颖, 等.山药多糖延缓秀丽隐杆线虫衰老的药效评价及作用机制研究[J].世界中医药, 2024, 19(4):473-480.
LIU Z K, HE X F, HONG Y, et al.Pharmacodynamic evaluation and mechanism of Chinese yam polysaccharides in delaying senescence of Caenorhabditis elegans[J].World Chinese Medicine, 2024, 19(4):473-480.
[26] XU Q X, ZHENG B S, LI T, et al.Hypsizygus marmoreus extract exhibited antioxidant effects to promote longevity and stress resistance in Caenorhabditis elegans[J].Food &Function, 2023, 14(21):9743-9754.
[27] DILLON E L.Nutritionally essential amino acids and metabolic signaling in aging[J].Amino Acids, 2013, 45(3):431-441.
[28] 杨育才, 王雪峰, 王桂瑛, 等.鸡汤的研究现状及展望[J].食品工业科技, 2019, 40(7):285-289;295.
YANG Y C, WANG X F, WANG G Y, et al.Research status and development trend of chicken soup[J].Science and Technology of Food Industry, 2019, 40(7):285-289;295.
[29] BAARZ B R, RINK L.Rebalancing the unbalanced aged immune system-A special focus on zinc[J].Ageing Research Reviews, 2022, 74:101541.
[30] BJØRKLUND G, SHANAIDA M, LYSIUK R, et al.Selenium:An antioxidant with a critical role in anti-aging[J].Molecules, 2022, 27(19):6613.
[31] SINGH P, GOLLAPALLI K, MANGIOLA S, et al.Taurine deficiency as a driver of aging[J].Science, 2023, 380(6649):eabn9257.
[32] ZHANG S W, LI F, ZHOU T, et al.Caenorhabditis elegans as a useful model for studying aging mutations[J].Frontiers in Endocrinology, 2020, 11:554994.
[33] WAN Q L, FU X D, MENG X, et al.Hypotaurine promotes longevity and stress tolerance via the stress response factors DAF-16/FOXO and SKN-1/NRF2 in Caenorhabditis elegans[J].Food &Function, 2020, 11(1):347-357.
[34] 朱方. 泰和乌鸡抗疲劳功能及黑色素抗氧化功能研究[D].杭州:浙江大学, 2012.
ZHU F.Anti-fatigue effect of Taihe silky fowl and anti-oxidant effect of silky fowl melanin[D].Hangzhou:Zhejiang University, 2012.
[35] WENTZ J M, MENDENHALL A R, BORTZ D M.Pattern formation in the longevity-related expression of heat shock protein-16.2 in Caenorhabditis elegans[J].Bulletin of Mathematical Biology, 2018, 80(10):2669-2697.
[36] PU Q Y, YANG F, ZHAO R, et al.Investigation of the potential ameliorative effects of DHA-enriched phosphatidylserine on bisphenol A-induced murine nephrotoxicity[J].Food and Chemical Toxicology, 2023, 180:114012.
[37] PAPAEVGENIOU N, HOEHN A, GRUNE T, et al.Lipofuscin effects in Caenorhabditis elegans ageing model[J].Free Radical Biology and Medicine, 2017, 108:S48.
[38] BARBOUTI A, LAGOPATI N, VEROUTIS D, et al.Implication of dietary iron-chelating bioactive compounds in molecular mechanisms of oxidative stress-induced cell ageing[J].Antioxidants, 2021, 10(3):491.
[39] 黄燕, 何劲, 雷帮星, 等.乌鸡黑色素提取方法及其应用研究进展[J].农产品加工, 2017(17):56-57;63.
HUANG Y, HE J, LEI B X, et al.Research progress in extraction methods and application of melanin from black bone chicken[J].Farm Products Processing, 2017(17):56-57;63.
[40] SUN S Q, GAO N, HU X Q, et al.SOD3 overexpression alleviates cerebral ischemia-reperfusion injury in rats[J].Molecular Genetics &Genomic Medicine, 2019, 7(10):e00831.