鼠李糖乳酪杆菌是乳酪杆菌属的一种益生菌,革兰氏阳性菌,无质粒,通常存在于人和动物消化系统的肠道中[1]。一些研究发现鼠李糖乳酪杆菌在动物与人体消化系统的极端环境中仍能保持活性,在肠道内定植后改善肠道微生态,从而发挥调节血糖、调节血脂、缓解腹泻和预防直肠癌[2]等健康效益。由此可见,鼠李糖乳酪杆菌对人体或动物的疾病预防与治疗具有广阔的应用前景。
益生元包括低聚糖类、多糖类和蛋白质水解物等,是指能够选择性地促进益生菌增殖和代谢的一类物质[3]。杨诗沅等[4]发现桑枝低聚糖对乳酸菌具有良好的促增殖效果,最大增殖率可达396.3%;李艳丽等[5]在培养基中添加4 g/L的玉米芯低聚木糖,枯草芽孢杆菌增殖率提高到183%。有学者通过动物实验证实益生元在生物体肠道中促进有益菌的增殖,如MA等[6]给小鼠灌胃莲子低聚糖,不仅降低了肠道菌群的厚壁菌门/拟杆菌门(F/B)值,还显著增加了粪便中的双歧杆菌属的相对丰度。此外,CHENG等[7]在小鼠粪便中添加豌豆低聚糖进行体外发酵,发现低聚糖添加量为15 g/L时,乳杆菌属和罗氏菌属的相对丰度显著增加。与之相反,大肠杆菌和志贺氏菌显著减少。课题组前期研究发现从桑椹中提取桑椹多糖(mulberry polysaccharide,MPS),经酶解后分离纯化制备得桑椹低聚糖,促鼠李糖乳酪杆菌增殖能力优于MPS和商品化益生元——低聚半乳糖(galactooligosaccharide,GOS)。对桑椹低聚糖进行结构表征,凝胶渗透色谱显示平均分子质量为 987 Da;经GC-MS检测单糖组成,其仅含有半乳糖;且糖醛酸和硫酸盐含量分别为56 mg/g和83.5 mg/g。由于该桑椹低聚糖由单一半乳糖构成,且聚合度为6,所以命名为桑椹低聚半乳糖(mulberry galacto-oligosaccharide,MGO)[8]。在培养基中添加MGO后,鼠李糖乳酪杆菌培养密度上升,而这一过程可能是MGO影响了鼠李糖乳酪杆菌的胞内代谢,目前其机理尚不明确。
蛋白质组学技术用于测定蛋白质的相对丰度,可了解生物体蛋白质合成时受环境因素影响而发生的整体变化。在微生物领域中,常利用的蛋白质组学方法之一是差异性方法,该方法可研究各种应激、药物、培养条件等对微生物的影响,并识别具有表达差异的蛋白质[9]。目前,蛋白质组学已经广泛应用于益生菌研究领域,如探究Ca2+对植物乳植杆菌胞外多糖生物合成的影响[10]、揭示副干酪乳酪杆菌高效利用菊粉的机制[11]、分析卵形拟杆菌和长双歧杆菌长亚种在木聚糖中的互作利用情况[12]等。
本研究基于前期发现MGO促鼠李糖乳酪杆菌增殖,及利用转录组学探究其基因表达变化的基础上,进一步采用串联质量标签(tandem mass tags,TMT)定量蛋白质组学技术,深入探究MGO对鼠李糖乳酪杆菌蛋白质代谢过程的具体影响,旨在为提升鼠李糖乳酪杆菌发酵剂的生产品质提供理论支撑。
1 材料与方法
1.1 材料与仪器
鼠李糖乳酪杆菌EN-08,保存于广东省农业科学院蚕业与农产品加工研究所,课题组在桑椹中分离筛选鉴定;MRS培养基,广东环凯微生物科技有限公司;GOS,上海源叶生物科技有限公司;β-甘露聚糖酶(50 U/mg),上海瑞永生物科技有限公司;碘乙酰胺、三乙基碳酸氢铵缓冲液(triethylammonium bicarbonate buffer,TEAB)、氨水,Sigma公司;PierceTM BCA蛋白质检测试剂盒、预染蛋白阶梯、Bond-BreakerTM TCEP 溶液、LC/MS级水、LC/MS级乙腈、LC/MS级甲醇、LC/MS级甲酸、TMT试剂,美国Thermo公司;蛋白酶抑制剂,Bimake公司。
Vortex-Genie 2型漩涡混匀仪,美国SI公司;Spectra Max plus384型酶标仪,美国Molecular Devices公司;Centrifuge 5430 R型高速冷冻离心机,德国Eppendorf公司;Orbitrap Exploris 480质谱仪、Vanquish F型超高效液相色谱仪,美国Thermo公司;Evosep One液相色谱仪,丹麦Evosep公司;MS105DU型分析天平,美国Mettler Toledo公司;Fielda-650D型超声波细胞破碎仪,江苏波场智能科技股份有限公司;Tanon-3500R型全自动数码凝胶图像分析系统,上海天能科技有限公司。
1.2 实验方法
1.2.1 MPS的制备
参考LI等[8]的方法,桑椹经80 ℃水浴浸提3 h,重复3次并合并提取液,抽滤,浓缩,用4倍体积无水乙醇醇沉,4 ℃静置过夜,离心取沉淀得到MPS。
1.2.2 MGO的制备
MPS与50 g/L β-甘露聚糖酶在50 ℃下酶解4 h,冷冻干燥后使用纤维素DEAE-52和Sephadex G-100柱层析进一步分离纯化得到MGO[13],随后冷冻干燥备用。
1.2.3 菌种活化、培养及样品收集
取出-80 ℃保存的鼠李糖乳酪杆菌EN-08,接种于MRS培养基中,180 r/min、37 ℃下培养18 h。活化后菌液接种于MRS培养基中培养18 h,按1%接种量接种于3个处理组中(MPS、MGO和GOS终浓度为40 g/L的200 mL MRS培养基),以不添加益生元的MRS液体培养基作为对照组,37 ℃、180 r/min培养18 h,发酵结束后,离心获得菌沉淀,-80 ℃冷冻保存。每个样品设置3个重复。
1.2.4 蛋白质提取
取出适量的冷冻样品加入振荡管,添加蛋白质裂解液(6 mol/L盐酸胍+10 g/L SDS,含蛋白酶抑制剂)。高通量组织研磨仪均质3次,每次均质40 s。在低温条件下裂解30 min,期间每隔5 min充分混匀。裂解后在4 ℃、12 000×g离心30 min,收集上清液,通过BCA法测定蛋白含量[14]。
1.2.5 蛋白质鉴定及分析
1.2.5.1 蛋白质酶解标记
取提取的蛋白100 μg,利用TEAB调节其浓度至100 mmol/L,加入TCEP将其浓度调整至10 mmol/L,37 ℃水浴60 min。加入碘乙酰胺调节其浓度至40 mmol/L,避光室温反应40 min。随后加入6倍体积4 ℃预冷的丙酮,-20 ℃静止5 h,8 000×g离心30 min,取沉淀。将沉淀完全溶解于100 μL 100 mmol/L 的TEAB中,随后按照胰蛋白酶与蛋白质质量比1∶50加入胰蛋白酶,37 ℃过夜酶解。
从-20 ℃取出TMT试剂,待其恢复至室温后,向其加入乙腈并涡旋均匀。100 μg多肽加入一管TMT试剂,然后在室温下孵育2 h。加入羟胺后在室温下继续反应30 min。将等量的标记产物合并到同一管中,并使用真空浓缩仪将其抽干。
1.2.5.2 RPLC分离液相串联质谱分析
多肽样品使用含有2% (体积分数)乙腈(经氨水调节至pH值=10)的UPLC上样缓冲液进行溶解,随后在反相C18柱(ACQUITY UPLC BEH C18,规格为1.7 μm, 2.1 mm×150 mm,Waters,USA)上进行高pH条件下的液相色谱分离。流动相A为2% (体积分数)乙腈(氨水调节至pH值=10),流动相B为80%(体积分数)乙腈(氨水调节至pH值=10),0~1.9 min,0%~0% B;1.9~2 min,0%~5% B;2~17 min,5%~5% B;17~18 min,5%~10% B;18~35.5 min,10%~30% B;35.5~38 min,30%~36% B;38~39 min,36%~42% B;39~40 min,42%~100% B;40~44 min,100% B;44~45 min,100%~0% B;45~48 min,0%~0% B。在214 nm紫外波长下检测,流量200 μL/min,洗脱时间48 min。
采用液相色谱串联质谱技术(Evosep One系统与Obitrap Exploris 480质谱仪的结合)进行质谱分析。肽段首先溶解于质谱专用上样缓冲液,利用C18色谱柱(150 μm×15 cm,Evosep)分离44 min,体积流量300 nL/min。A相0.1% (体积分数)甲酸水溶液,B相100% (体积分数)乙腈加0.1% (体积分数)甲酸,0~2 min,5%~5% B;2~30 min,5%~38% B;30~40 min,38%~90% B;40~44 min,90%~90% B。MS扫描范围(m/z) 350~1 500,采集模式为DDA,碎裂方式为HCD;一级质谱分辨率60 000,二级分辨率15 000,动态排除时间30 s。
1.2.5.3 蛋白鉴定
质谱数据经Proteome DiscovererTMSoftware 2.4分析,采用的数据库为UniProt。搜库过程中肽段鉴定的错误发现率(false discovery rate,FDR)设置为FDR≤0.01。
1.2.6 数据分析
将实验所得数据结果,由上海美吉生物医药科技有限公司协助上传至美吉云平台(cloud.majorbio.com)以进行下一步分析。利用R语言中stats包的t.test函数计算样本间显著性差异的P值,并同时求出组间差异倍数。显著性检验P<0.05。利用KEGG数据库对差异蛋白涉及的代谢通路进行分析,GO对所有的差异蛋白进行注释和功能聚类分析。
2 结果与分析
2.1 全蛋白相关性分析和主成分分析
统计处理组和对照组的菌株全蛋白分子质量数据,计算样本之间的Pearson相关系数并绘制可视化热图。相关系数的数值对应颜色深浅,颜色越接近红色表明样本间蛋白相似度越高。如图1所示,同组的3个平行样本之间对应的颜色皆为红色,且相关系数都在0.6以上,说明同组平行全蛋白差异较小,实验结果具有较高精确性。MPS处理组、MGO处理组与MRS对照组之间对应的颜色为深蓝色和浅蓝色,差异性较大,这说明鼠李糖乳酪杆菌EN-08经MPS或MGO发酵培养后,全蛋白的组成发生显著变化,MPS与MGO均能影响菌株蛋白质的表达。而GOS组全蛋白与MRS组相比,差异相对较小。
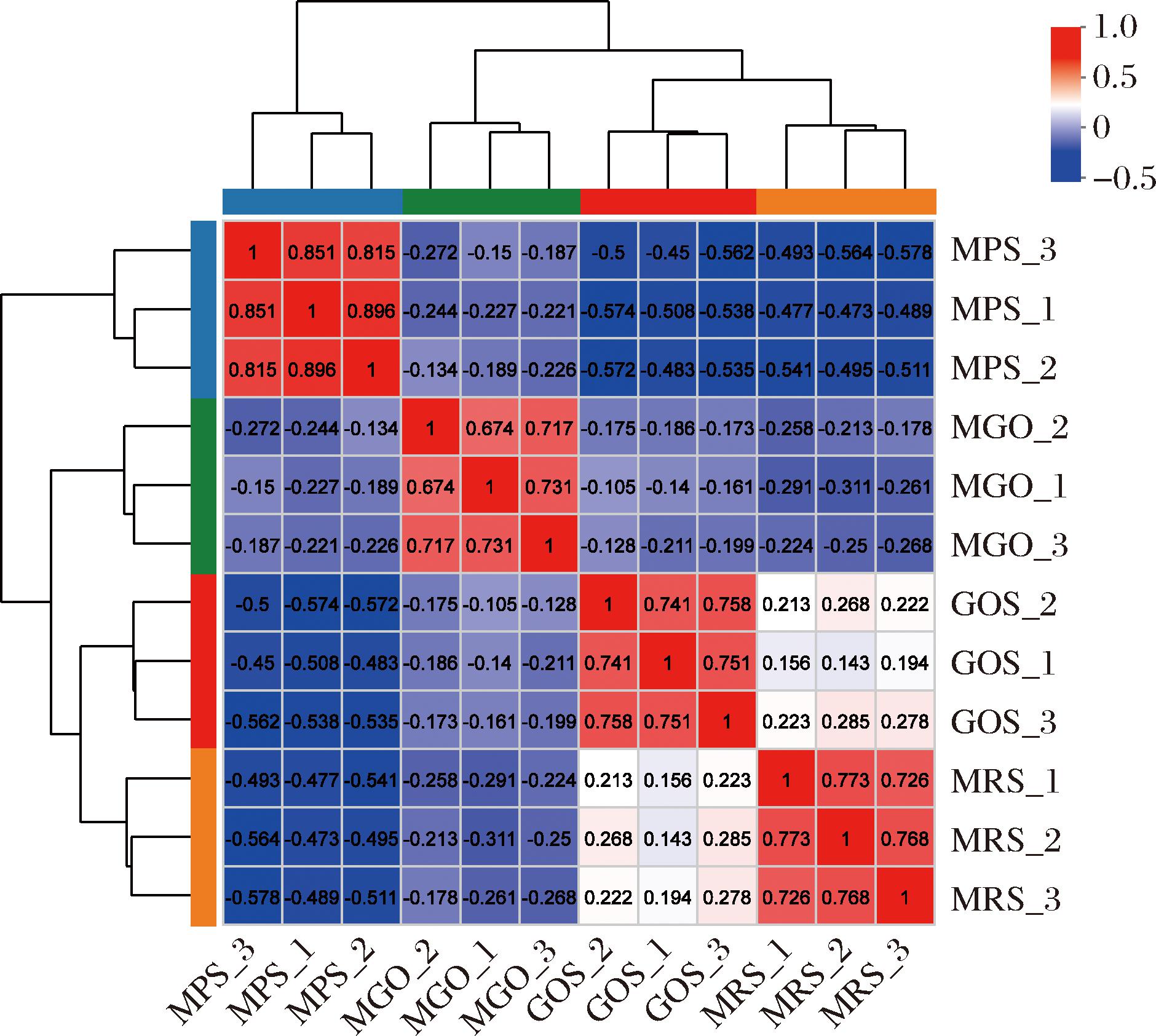
图1 Pearson相关性热图
Fig.1 Pearson correlation heat map
注:_1、_2、_3表示3个平行组(下同)。
图2的主成分分析显示了样本间的相似性, PC1和PC2的方差贡献率分别为33.90%、22.00%,共反映了全部信息的55.90%。4个组之间距离较远,表明不同处理组的全蛋白存在差异。此外,MRS对照组与MGO、MPS的距离较远,与GOS组距离最近,说明MRS组与MGO组、MPS组相似度较小,与GOS相似度较高。
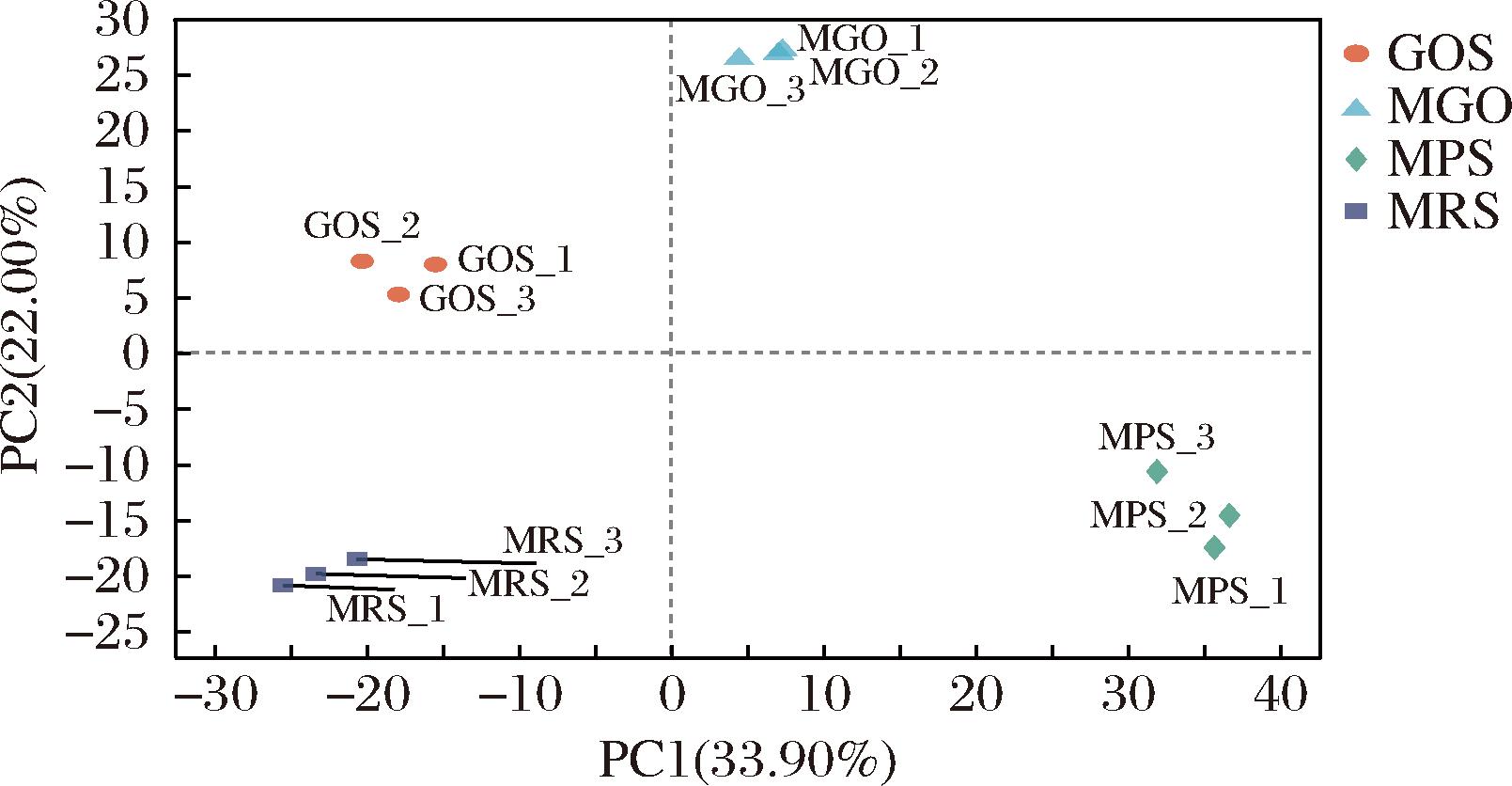
图2 主成分分析
Fig.2 Principal component analysis
2.2 比较组差异蛋白
参考许家齐等[15]的表达值倍数(fold change,FC)变化并适当调整。以FC≥1.2,FC≤0.83,作为差异蛋白的筛选阈值,图3揭示了各处理组对比空白对照组引起的上调或下调差异蛋白的情况。可以清晰地看出,这3种糖类物质对鼠李糖乳酪杆菌EN-08蛋白质表达的影响效果由大到小排序是:MPS、MGO、GOS。该结果可能是MPS能特异地对鼠李糖乳酪杆菌EN-08的基因转录进行正向调控导致的[16]。GOS vs MRS 的差异蛋白较少,有93个。而MPS vs MRS的差异蛋白有290个,MGO vs MRS 有192个,其中MGO组上调蛋白有110个,下调蛋白有82个。此外,图4展示了GOS vs MRS 组、MGO vs MRS 组和MPS vs MRS 组独有的差异蛋白分别是31、65、178个,3个处理组共有的差异蛋白有23个。
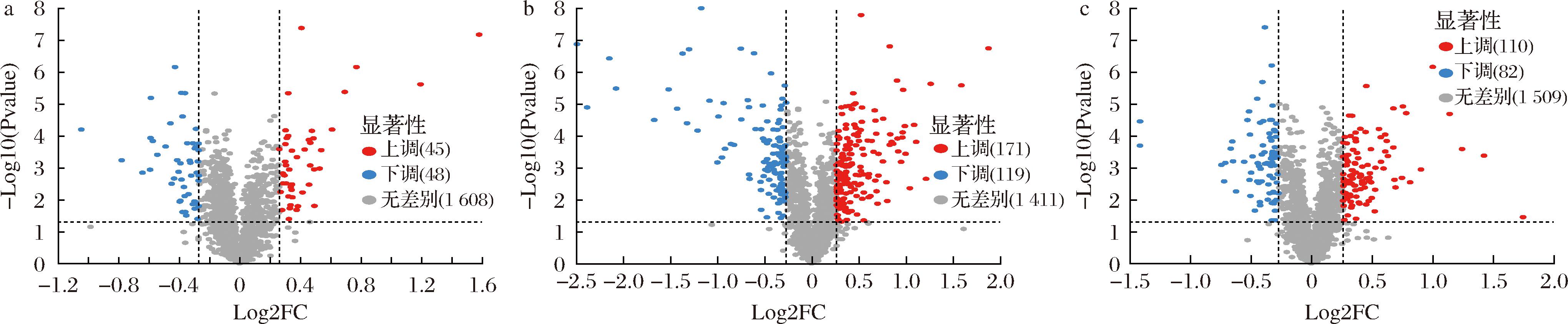
a-GOS vs MRS差异蛋白火山图;b-MPS vs MRS差异蛋白火山图;c-MGO vs MRS差异蛋白火山图
图3 不同益生元处理后差异蛋白的火山图
Fig.3 Volcano diagram of differential proteins after treatment with different prebiotics
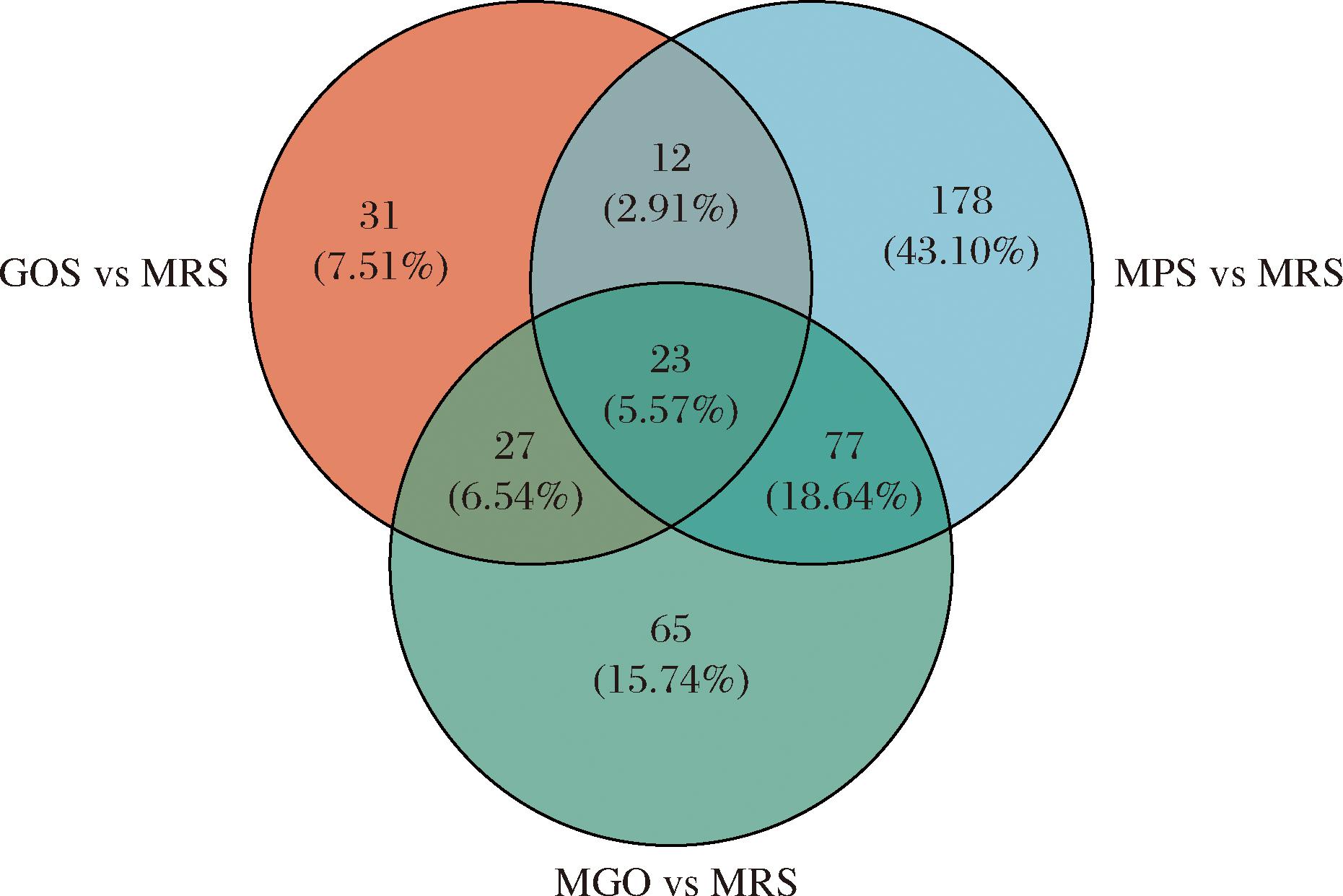
图4 不同益生元处理下的差异蛋白韦恩图
Fig.4 Venn diagram of differential proteins under different prebiotic treatments
2.3 MGO处理组差异蛋白KEGG分析
前期研究表明,与添加MPS与GOS相比,含有 MGO的培养基在培养鼠李糖乳酪杆菌过程中,生长速率显著上升,且在24 h菌含量最高[13]。将MGO组和MRS对照组的蛋白序列进行KEGG数据库比对,得到MGO vs MRS上调差异蛋白的注释信息(图5)。KEGG通路注释显示,MGO与MRS上调差异蛋白主要注释于代谢和环境信息处理中。在代谢进程中,注释到碳水化合物代谢通路下的上调差异蛋白有17个,其中与果糖和甘露糖代谢相关的蛋白个数为9,与半乳糖代谢相关的蛋白个数为3。由于微生物的生命活动大部分涉及到碳水化合物代谢[17],提高碳水化合物的利用能力有助于增强微生物在不同环境下的适应性[18],说明添加MGO可能有利于促进菌株的增殖。环境信息处理进程结果显示,关于膜运输的差异蛋白有16个,其中与ABC转运器相关的蛋白有8个,ABC转运系统能够将营养物质或代谢产物特异性运输到细胞内外,具有ATP依赖性,使用细胞内的ATP能量来驱动跨膜转运[19]。
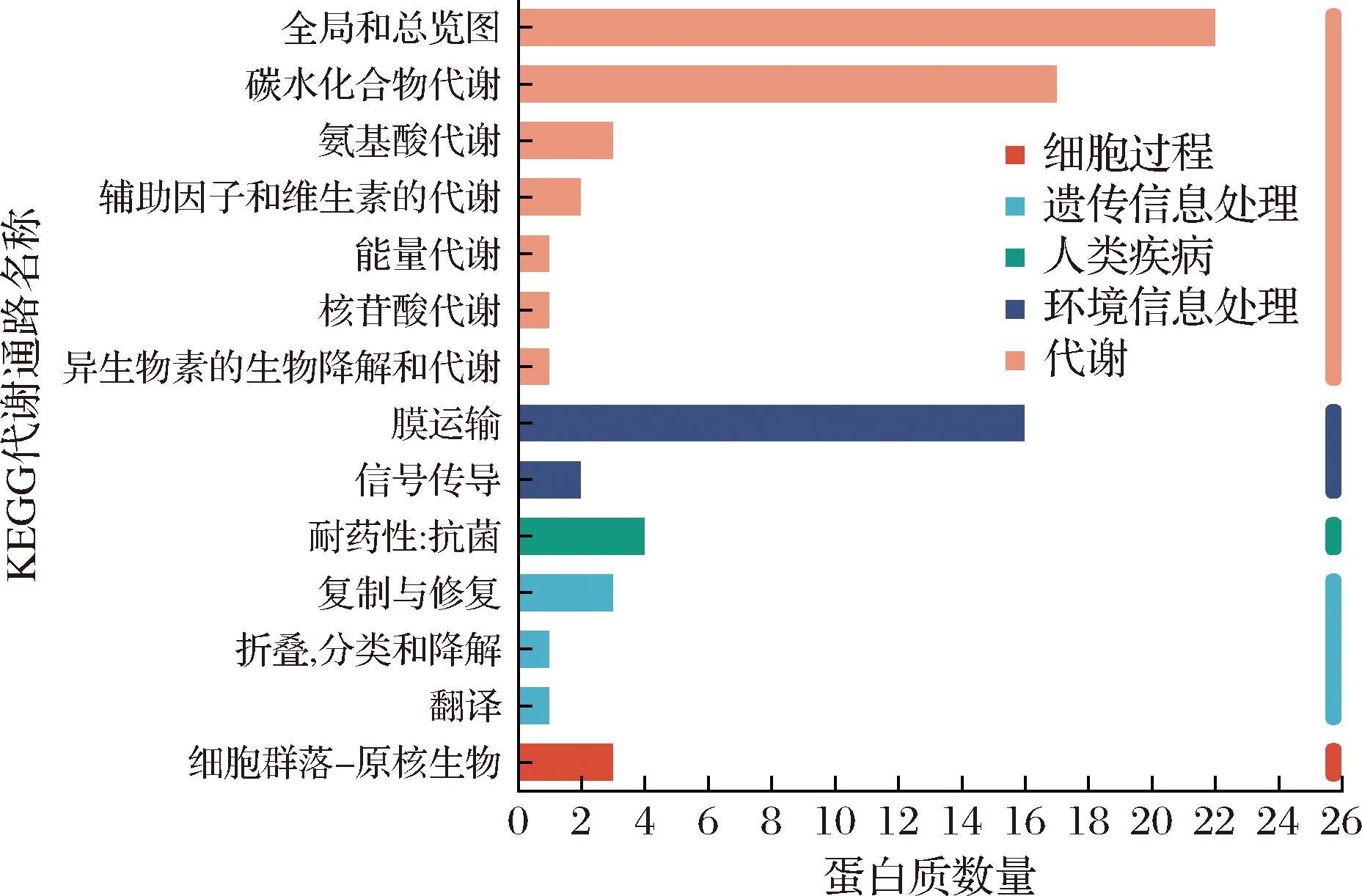
图5 MGO vs MRS上调表达蛋白质KEGG功能注释
Fig.5 KEGG functional annotation of upregulated proteins in MGO vs MRS
对MGO组差异表达蛋白集进行KEGG通路富集分析,从而确定显著上调的通路。结果见图6,在α=0.01的显著水平下,存在2个差异蛋白代谢通路显著富集,分别是果糖和甘露糖代谢以及磷酸转移酶系统(phosphotransferase system,PTS),富集因子分别为0.219 5和0.228 6。在果糖和甘露糖代谢途径中,过量表达的蛋白包括果糖二磷酸醛缩酶、塔格糖-6-磷酸激酶和甘露醇-1-磷酸5-脱氢酶。果糖二磷酸醛缩酶在糖代谢途径中发挥关键作用,可在乳酸菌中将1,6-二磷酸果糖转化二羟基丙酮磷酸盐,对糖酵解、糖异生至关重要[20]。塔格糖-6-磷酸激酶主要与戊糖代谢相关,将D-塔格糖-6-磷酸进一步磷酸化为D-塔格糖-1,6-二磷酸[21]。甘露醇-1-磷酸5-脱氢酶可能参与甘露醇的代谢,初步将甘露醇氧化为甘露糖,有利于后续参与到糖酵解途径中。在工业生产MGO-鼠李糖乳酪杆菌合生元时,通过实时监测果糖二磷酸醛缩酶、塔格糖-6-磷酸激酶和甘露醇-1-磷酸5-脱氢酶等蛋白的表达含量变化,可评估发酵速率并确定发酵终点。在PTS中,过量表达的组分有PTS果糖转运蛋白亚基、PTS甘露醇特异性EIICB成分、PTS山梨糖醇特异性IIA组分。PTS是碳水化合物运输系统,用于细胞摄取外界碳源(如葡萄糖、葡萄糖酸等),同时磷酸化。在碳源的利用和代谢调控中发挥着重要作用。添加MGO后,依赖PTS的糖转运可能提升MGO在鼠李糖乳酪杆菌EN-08的利用效率,加速菌体能量代谢。与前期研究中发现的促增殖能力结果相符。
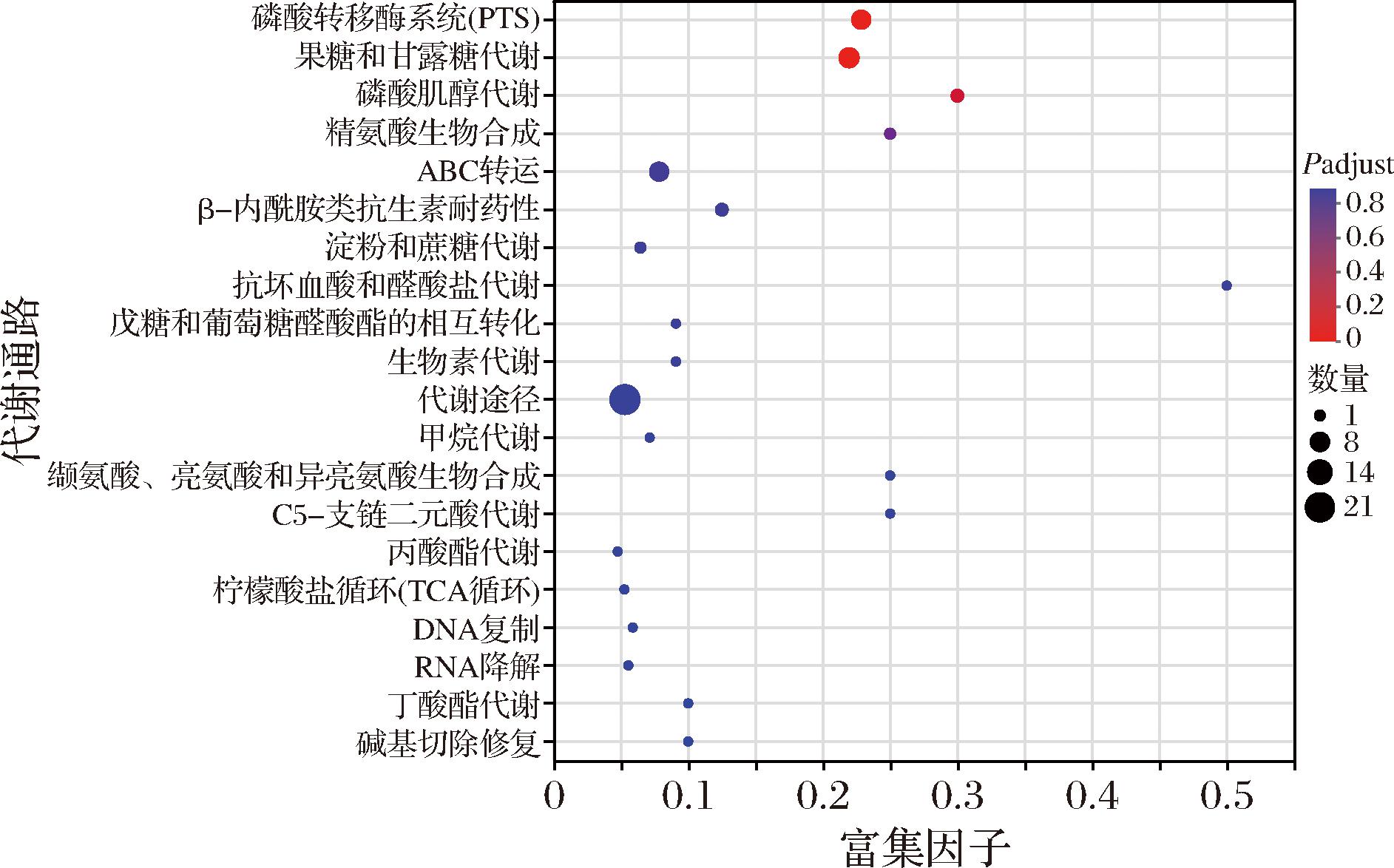
图6 MGO vs MRS上调表达蛋白质KEGG富集分析
Fig.6 KEGG enrichment analysis of upregulated proteins in MGO vs MRS
MGO在鼠李糖乳酪杆菌EN-08内的代谢涉及大量蛋白,MGO作为由半乳糖单一碳源构成的益生元,因此推测半乳糖代谢为碳分解代谢的核心途径,在MGO促乳杆菌增殖过程中必然发生变化,通过与无益生元MRS培养基中比较半乳糖代谢通路的异同,对随生长速率变化的蛋白生理功能进一步分析。由图7可以看出,MRS培养基添加MGO后鼠李糖乳酪杆菌EN-08的半乳糖代谢通路中发生上调的蛋白是D-半乳糖酸脱水酶(D-galactonate dehydratase,EC:4.2.1.6)、尿苷三磷酸-葡萄糖-1-磷酸尿苷酰转移酶(UTP-glucose-1-phosphate uridylyltransferase,EC:2.7.7.9)和半乳糖醇PTS通透酶(galactitol PTS permease、galactitol PTS system EIIA component,EC:2.7.1.200)。
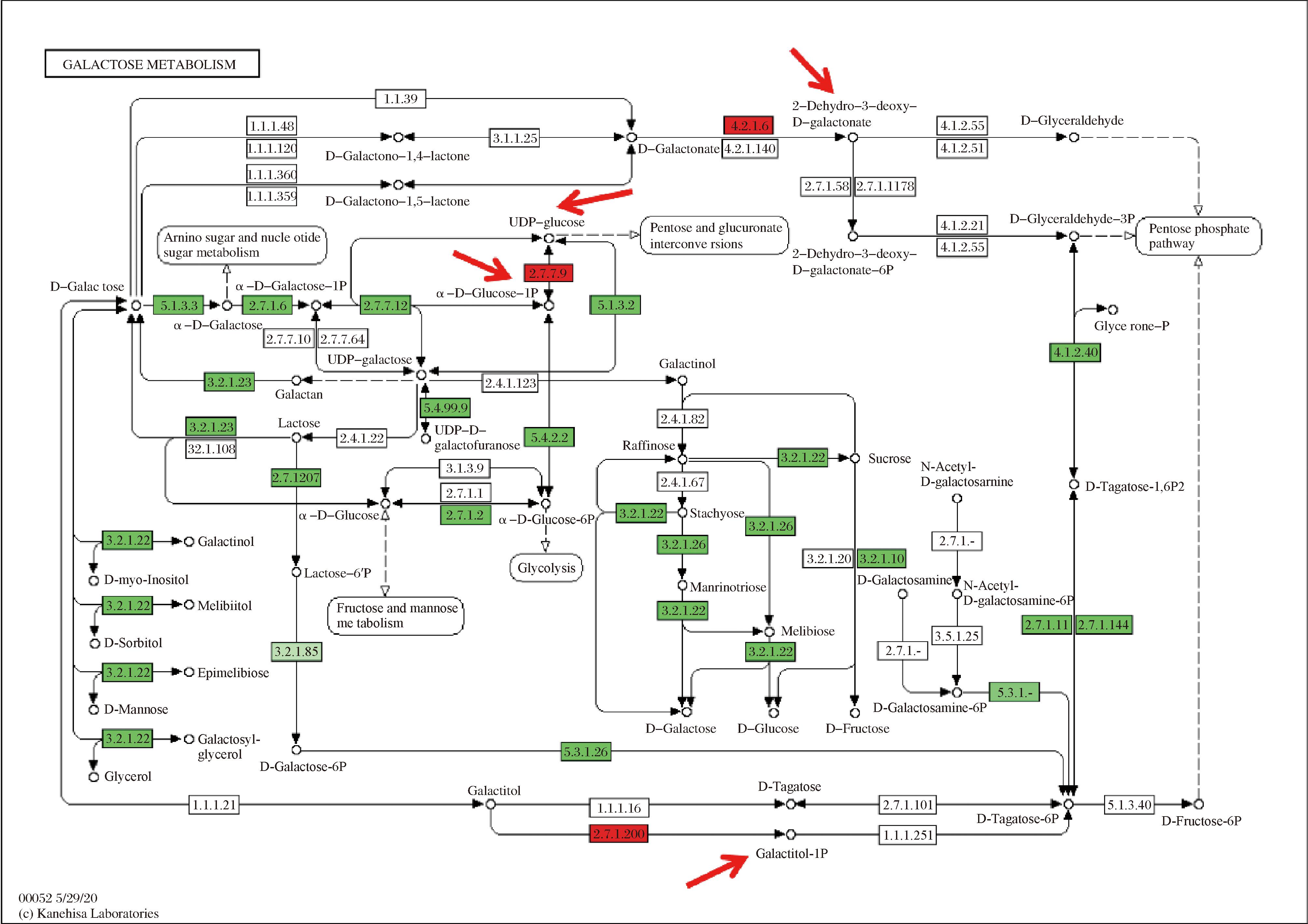
图7 MGO vs MRS半乳糖代谢通路变化
Fig.7 Alterations in the galactose metabolic pathway in MGO vs MRS
注:红色标记为上调蛋白,红色箭头指向上调蛋白作用位点。Galactose metabolism:半乳糖代谢;D-Galactono-1,4-lactone:D-半乳糖-1,4-内酯;D-Galactono-1,5-lactone:D-半乳糖-1,5-内酯;Amino sugar and nucleotide sugar metabolism:氨基糖和核苷酸糖代谢;D-Galactose:D-半乳糖;α-D-Galactose-1P:α-D-半乳糖-1-磷酸;α-D-Galactose:α-D-半乳糖;α-D-Glucose-1P:α-D-葡萄糖-1-磷酸;UDP-glucose:UDP-葡萄糖;UDP-galactose:UDP半乳糖;Galactan:半乳聚糖;Lactose:乳糖;Galactinol:肌醇半乳糖苷;D-myo-inositol:肌醇;Melibiitol:美利比糖醇;D-Sorbitol:D-山梨糖醇;Epimelibiose:表蜜二糖;D-Mannose:D-甘露糖;Galactosyl glycerol:甘油葡萄糖苷;Glycerol:甘油;α-D-Glucose:α-D-葡萄糖;Lactose-6′P:乳糖-6′-磷酸;D-Galactose-6P:D-半乳糖-6-磷酸;Fructose and mannose metabolism:果糖和甘露糖代谢;UDP-D-galactofuranose:UDP-D-呋喃半乳糖;α-D-Glucose-6P:α-D-葡萄糖-6-磷酸;Glycolysis:糖酵解;D-Galactonate:D-半乳糖醛酸;Pentose and glucuronate interconversions:戊糖和葡萄糖醛酸的相互转化;2-Dehydro-3-deoxy-D-galactonate:2-脱氢-3-脱氧-D-半乳糖醛酸;2-Dehydro-3-deoxy-D-galactonate-6P:2-脱氢-3-脱氧-D-半乳糖醛酸-6-磷酸;D-Glyceraldehyde:D-甘油醛;D-Glyceraldehyde-3P:D-甘油醛-3-磷酸;Pentose phosphate pathuay:磷酸戊糖途径;Glycerone-P:甘油酮磷酸;D-Tagatose-1,6P2:D-塔格糖-1,6-二磷酸;Galactinol:肌醇半乳糖苷;Raffinose:棉子糖;Sucrose:蔗糖;Stachyose:水苏糖;Manninotriose:甘露三糖;Melibiose:蜜二糖;D-Galactose:D-半乳糖;D-Glucose:D-葡萄糖;D-Galactosaminey:D-半乳糖胺;D-Galactosamine-6P:D-半乳糖胺-6-磷酸;D-Fructose:D-果糖;N-Acetyl-D-galactosamine-6P:N-乙酰-D-半乳糖胺-6-磷酸;N-Acetyl-D-galactosamine:N-乙酰-D-半乳糖胺;Galactitol:半乳糖醇;D-Tagatose:D-塔格糖;Galactitol-1P:半乳糖醇-1-磷酸;D-Tagatose-6P:D-塔格糖-6-磷酸;D-Fructose-6P:D-果糖-6-磷酸。
D-半乳糖酸脱水酶对D-半乳糖酸盐具有高度特异性。D-半乳糖酸盐作为一种广泛存在的糖酸,已被证实是肠道细菌的碳源之一[22]。当外源性D-半乳糖酸被细菌摄取后,D-半乳糖酸脱水酶催化其脱水反应,生成2-脱氢-3-脱氧-D-半乳二酸,随后进入磷酸化过程。尿苷三磷酸-葡萄糖-1-磷酸尿苷酰转移酶(UGPase)是一种焦磷酸酶,能够可逆催化葡萄糖-1-磷酸转化为UDP-葡萄糖。UDP-葡萄糖不仅是微生物利用半乳糖的关键中间体,也是合成糖原的必要底物[23]。因此,UGPase在细胞的能量代谢和糖类合成过程中发挥着重要作用。半乳糖醇PTS通透酶是磷酸烯醇式丙酮酸依赖性糖转运PTS的一种成分[24]。该系统仅存在于原核生物中,同时将其底物从周质或细胞外间隙转运到细胞质中并磷酸化。
2.4 MGO处理组差异蛋白GO分析
利用GO注释对上调差异蛋白从分子功能、生物学过程和细胞组分进行分析,GO注释结果如图8所示,在分子功能分类中,差异上调蛋白具有ATP依赖性活性(ATP-dependent activity,6个蛋白)、转运体活性(transporter activity,11个蛋白)、连接(binding,22个蛋白)、催化活性(catalytic activity,48个蛋白)等方面的功能。差异上调蛋白参与的生物学过程包括细胞过程(cellular process,25个蛋白)、代谢过程(metabolic process,23个蛋白)、定位(localization,13个蛋白)、对刺激的反应(response to stimulus,3个蛋白)和生物调节(biological regulation,1个蛋白)。从细胞组分的角度看,上调的蛋白基本位于细胞解剖实体(cellular anatomical entity,42个蛋白)和含蛋白质复合物(protein-containing complex,5个蛋白)中。
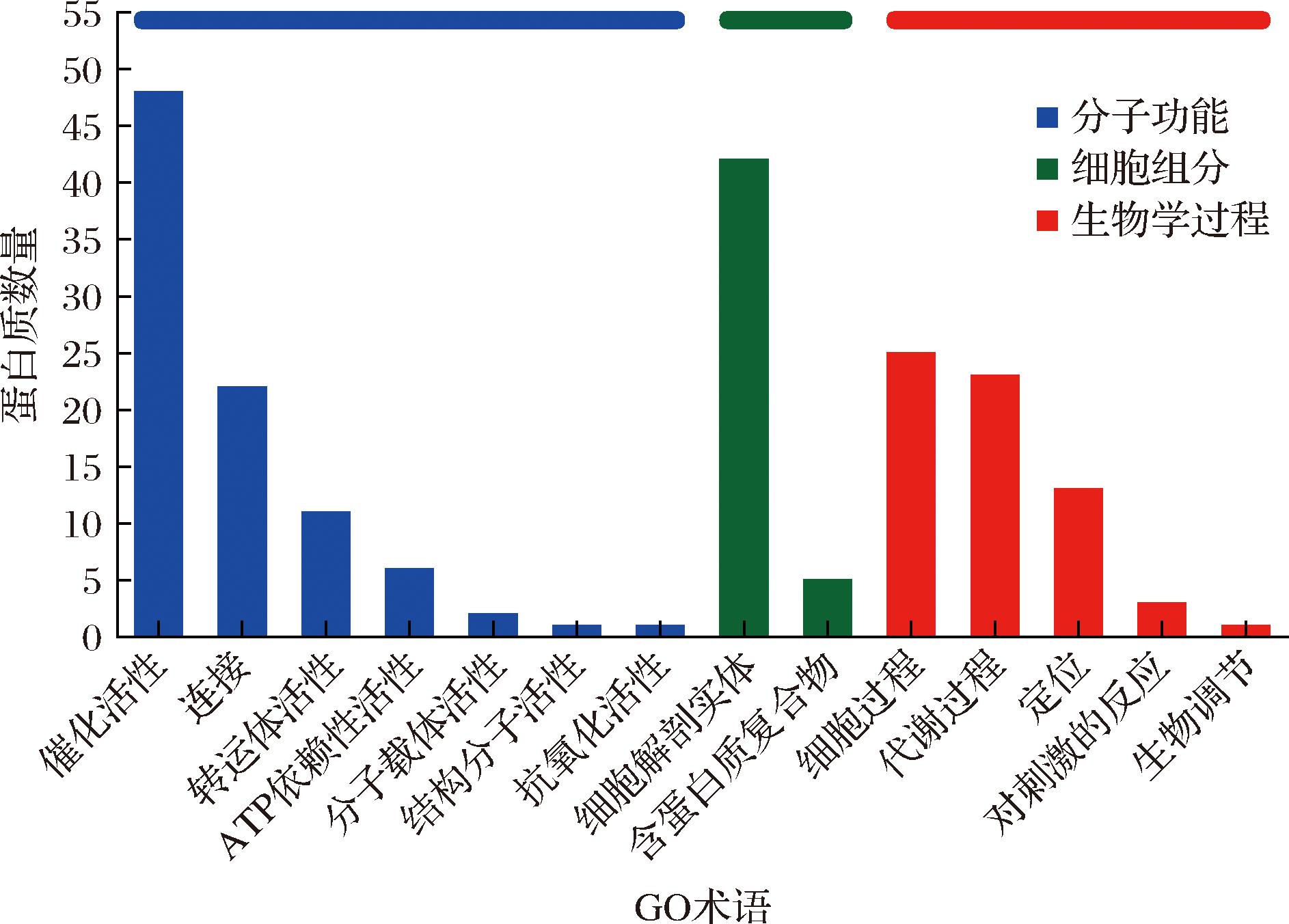
图8 MGO vs MRS上调表达蛋白质GO功能注释
Fig.8 GO functional annotation of upregulated proteins in MGO vs MRS
3 结论与讨论
采用TMT定量蛋白质组学技术分析MGO对鼠李糖乳酪杆菌EN-08蛋白质表达的影响。结果表明,MGO的添加显著改变了菌株的全蛋白表达。通过KEGG通路注释发现,MGO引起的上调差异蛋白主要体现在碳水化合物代谢以及膜运输方面。KEGG 富集分析发现差异蛋白质显著富集于果糖和甘露糖代谢以及PTS等通路。GO注释显示上调差异蛋白主要具有催化活性、连接、转运体活性功能,主要参与细胞过程和代谢过程,并且大部分分布于细胞解剖实体中。MGO对鼠李糖乳酪杆菌EN-08蛋白调控的细致关联机理,则需进一步深究。
[1] 单强, 王雪, 朱要宏, 等.鼠李糖乳杆菌抗炎机制及其在防治家畜疾病中的应用前景[J].畜牧兽医学报, 2023, 54(11):4537-4550.
SHAN Q, WANG X, ZHU Y H, et al.Application prospect of anti-inflammatory mechanism of Lactobacillus rhamnosus and its prevention and treatment in livestock diseases[J].Acta Veterinaria et Zootechnica Sinica, 2023, 54(11):4537-4550.
[2] SANKLECHA M, VERMA L, PAI U, et al.Lactobacillus rhamnosus GG evaluation in acute diarrhea (LEAD):An observational study[J].Cureus, 2022, 14(4):e24594.
[3] 刘波, 刘通通, 张祥奎, 等.益生元及其应用研究进展[J].食品与药品, 2021, 23(5):485-492.
LIU B, LIU T T, ZHANG X K, et al.Research progress of prebiotics and their applications[J].Food and Drug, 2021, 23(5):485-492.
[4] 杨诗沅, 邹宇晓, 胡腾根, 等.桑枝低聚糖促乳酸菌生长活性优化研究[J].食品科学技术学报, 2020, 38(2):66-72.
YANG S Y, ZOU Y X, HU T G, et al.Optimization of growth promoting activity of Ramulus mori oligosaccharide on lactic acid bacteria[J].Journal of Food Science and Technology, 2020, 38(2):66-72.
[5] 李艳丽, 许少春, 柳永, 等.低聚木糖的制备及其对益生菌体外增殖的作用[J].浙江大学学报(农业与生命科学版), 2011, 37(3):245-251.
LI Y L, XU S C, LIU Y, et al.Preparation of xylo-oligosaccharides and its effect on in vitro proliferation of probiotics[J].Journal of Zhejiang University (Agriculture and Life Sciences), 2011, 37(3):245-251.
[6] MA X Q, ZHENG Z C, WANG Q, et al.The modulation effect of lotus (Nelumbo nucifera Gaertn.) seeds oligosaccharides with different structures on intestinal flora and action mode of growth effects on Bifidobacterium in vivo and in vitro[J].Food Chemistry, 2023, 419:136057.
[7] CHENG Y X, ZHAO R Q, QIAO M W, et al.The pea oligosaccharides could stimulate the in vitro proliferation of beneficial bacteria and enhance anti-inflammatory effects via the NF-κB pathway[J].Foods, 2024, 13(4):626.
[8] LI E N, YANG S Y, ZOU Y X, et al.Purification, characterization, prebiotic preparations and antioxidant activity of oligosaccharides from mulberries[J].Molecules, 2019, 24(12):2329.
[9] ASLAM B, BASIT M, NISAR M A, et al.Proteomics:Technologies and their applications[J].Journal of Chromatographic Science, 2017, 55(2):182-196.
[10] JIANG Y Y, ZHANG M, ZHANG Y, et al.Calcium (Ca(2+))-regulated exopolysaccharide biosynthesis in probiotic Lactobacillus plantarum K25 as analyzed by an omics approach[J].Journal of Dairy Science, 2021, 104(3):2693-2708.
[11] VEGA-SAGARD A M, CABEZ
A M, CABEZ N E C, DELGADO J, et al.Screening microbial interactions during inulin utilization reveals strong competition and proteomic changes in Lacticaseibacillus paracasei M38[J].Probiotics and Antimicrobial Proteins, 2024, 16(3):993-1011.
N E C, DELGADO J, et al.Screening microbial interactions during inulin utilization reveals strong competition and proteomic changes in Lacticaseibacillus paracasei M38[J].Probiotics and Antimicrobial Proteins, 2024, 16(3):993-1011.
[12] VEGA-SAGARD A M, DELGADO J, RUIZ-MOYANO S, et al.Proteomic analyses of Bacteroides ovatus and Bifidobacterium longum in xylan bidirectional culture shows sugar cross-feeding interactions[J].Food Research International, 2023, 170:113025.
A M, DELGADO J, RUIZ-MOYANO S, et al.Proteomic analyses of Bacteroides ovatus and Bifidobacterium longum in xylan bidirectional culture shows sugar cross-feeding interactions[J].Food Research International, 2023, 170:113025.
[13] LI E N, ZHU Q L, PANG D R, et al.Analysis of Lactobacillus rhamnosus GG in mulberry galacto-oligosaccharide medium by comparative transcriptomics and metabolomics[J].Frontiers in Nutrition, 2022, 9:853271.
[14] JIANG P F, CHEN X W, QIAN L, et al.Integrated transcriptomic and proteomic analysis of the physiological changes of the liver in domesticated Eurasian perch, Perca fluviatilis[J].Comparative Biochemistry and Physiology Part D:Genomics and Proteomics, 2022, 41:100957.
[15] 许家齐, 郑新飞, 冯燕, 等.基于蛋白质组学研究冷冻干燥对副干酪乳杆菌PC-01细胞活性的影响[J].中国食品学报, 2023, 23(3):177-186.
XU J Q, ZHENG X F, FENG Y, et al.Effects of freeze-drying on the activity of Lactobacillus paracasei PC-01 cells based on proteomics[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(3):177-186.
[16] 冯佳, 吴昊, 王斌斌, 等.全局调控因子CodY在益生菌中的研究进展[J].食品与发酵工业, 2016, 42(10):227-233.
FENG J, WU H, WANG B B, et al.Advances in research on global regulatory factor CodY of probiotics[J].Food and Fermentation Industries, 2016, 42(10):227-233.
[17] WARDMAN J F, BAINS R K, RAHFELD P, et al.Carbohydrate-active enzymes (CAZymes) in the gut microbiome[J].Nature Reviews Microbiology, 2022, 20(9):542-556.
[18] CUI Y H, WANG M H, ZHENG Y K, et al.The carbohydrate metabolism of lactiplantibacillus plantarum[J].International Journal of Molecular Sciences, 2021, 22(24):13452.
[19] VAN VEEN H W, KONINGS W N.The ABC family of multidrug transporters in microorganisms[J].Biochimica et Biophysica Acta (BBA) - Bioenergetics, 1998, 1365(1-2):31-36.
[20] QIU Y J, QIU Z Y, XIA J, et al.Co-expression of xylose transporter and fructose-bisphosphate aldolase enhances the utilization of xylose by Lactococcus lactis IO-1[J].Applied Biochemistry and Biotechnology, 2023, 195(2):816-831.
[21] SCHOENENBERGER B, KIND S, MEIER R, et al.Efficient biocatalytic synthesis of D-tagatose 1, 6-diphosphate by LacC-catalysed phosphorylation of D-tagatose 6-phosphate[J].Biocatalysis and Biotransformation, 2020, 38(1):53-63.
[22] SINGH S, GOLA C, SINGH B, et al.D-galactonate metabolism in enteric bacteria:A molecular and physiological perspective[J].Current Opinion in Microbiology, 2024, 81:102524.
[23] ZHOU Y C, BU Z Y, QIAN J, et al.The UTP-glucose-1-phosphate uridylyltransferase of Brucella melitensis inhibits the activation of NF-κB via regulating the bacterial type IV secretion system[J].International Journal of Biological Macromolecules, 2020, 164:3098-3104.
[24] NOBELMANN B, LENGELER J W.Molecular analysis of the gat genes from Escherichia coli and of their roles in galactitol transport and metabolism[J].Journal of Bacteriology, 1996, 178(23):6790-6795.