两歧双歧杆菌(Bifidobacterium bifidum)作为功能益生菌在食品和医药领域具有重要应用价值,但其工业化培养过程长期受限于氮源利用效率低下这一瓶颈问题。两歧双歧杆菌的基因组学研究表明,该菌缺失胞壁蛋白酶[1],且缺乏完整的氨基酸转运系统[2],因而难以有效利用传统氮源。现有工业化培养多采用商品化的酵母浸粉与蛋白胨,然而此类氮源针对性差,存在2个关键缺陷:其一,酵母浸粉中游离氨基酸含量较高,两歧双歧杆菌利用受限;其二,常用的蛋白胨中大分子质量的肽含量高,该菌无法利用,进而导致氮源利用率低。近年来研究揭示,两歧双歧杆菌脯氨酸转运蛋白ProP和OpuE缺失[3],使其无法将游离脯氨酸转运进入胞内。然而,基因组研究显示两歧双歧杆菌具备完整的寡肽转运(oligopeptide permease, Opp)系统,偏好利用短肽[4],在人为补充含有脯氨酸的短肽后,两歧双歧杆菌活菌数显著提升[3]。
因此,制备一种两歧双歧杆菌可以利用的富含脯氨酸的肽可能是提升其氮源利用率,进而提高生长密度的潜在路线。但是这决定了目标肽段的设计需严格遵循菌株的氮源利用特征,除需要富含脯氨酸外,还需满足该菌对底物的其他选择性。例如,研究表明含有脯氨酸、亮氨酸且分子质量<2 kDa的亲水性肽更易被利用[5-6],在靶向制备时应予以考虑,以实现氮源的精准适配。此外,维持氨基酸平衡也至关重要:靶向制备的肽需提供额外半胱氨酸以弥补该菌对其合成能力的缺陷,并控制甲硫氨酸含量,避免因过量而抑制菌体生长[7]。
本研究提出“特征肽靶向制备”的创新策略,旨在制备符合两歧双歧杆菌特异性转运及代谢特征的脯氨酸肽,从而提升其氮源利用效率与生物量,为推进该菌的工业化生产提供新思路。
1 材料与方法
1.1 菌株与试剂
1.1.1 菌株
两歧双歧杆菌(B.bifidum)CCFM1301,江南大学食品微生物菌种保藏中心。
培养条件:在厌氧工作站中37 ℃恒温培养,厌氧气组成(N2∶CO2∶H2复配体积比为7∶2∶1)。
1.1.2 试剂与培养基
葡萄糖、无水乙酸钠、柠檬酸氢二铵、K2HPO4·3H2O、MgSO4·7H2O、MnSO4·H2O、KH2PO4、Na2HPO4、NaCl、吐温-80、半胱氨酸盐酸盐、胰蛋白酶,国药集团化学试剂有限公司;酵母浸粉(LP0021B)、胰蛋白胨(LP0042B),赛默飞世尔科技有限公司;酪蛋白,北京百灵威科技有限公司;碱性蛋白酶、木瓜蛋白酶、中性蛋白酶、风味蛋白酶,北京索莱宝科技有限公司;乳清蛋白,上海博飞美科化学科技有限公司;谷蛋白(小麦),上海阿拉丁生化科技股份有限公司。
MRS液体培养基(g/L):胰蛋白胨10、酵母浸粉5、牛肉浸膏10、葡萄糖20、无水乙酸钠2、柠檬酸氢二铵2、K2HPO4·3H2O 2.6、MgSO4·7H2O 0.1、MnSO4·H2O 0.05、吐温-80 1 mL/L、半胱氨酸盐酸盐1。115 ℃、20 min高压灭菌。
氮源筛选培养基(g/L):氮源1,葡萄糖5,K2HPO4·3H2O 7,Na2HPO4 7,半胱氨酸盐酸盐1。pH 6.5,115 ℃、20 min高压灭菌。
半胱氨酸缓冲液(g/L):半胱氨酸盐酸盐0.5,KH2PO4 6.0,Na2HPO4 4.5,NaCl 4.0,吐温-80 0.6。pH 6.8~7.0,115 ℃、20 min高压灭菌。
1.2 仪器与设备
T&J-MiniPod 1Lx8迷你平行生物反应器,迪必尔生物工程有限公司;Waters 1525高效液相色谱仪,美国沃特世公司;DAWN HELEOS 8+高效凝胶排阻色谱系统,美国怀雅特技术公司;Evolution One紫外可见光分光光度计、UltiMate 3000系统,美国赛默飞世尔科技科技公司;K1100全自动凯式定氮仪、SH420消解仪,山东海能科学仪器有限公司;Electrotek厌氧工作站,英国依莱泰科公司。
1.3 实验方法
1.3.1 富含脯氨酸的蛋白的筛选
从BIOPEP数据库(https://biochemia.uwm.edu.pl/biopep/start_biopep.php)和NCBI数据库(https://www.ncbi.nlm.nih.gov/protein)中下载动物蛋白和植物蛋白的序列,并统计各种蛋白质中20种氨基酸的占比。将具有相同物种来源和相同名称的蛋白质归类,并计算每种蛋白质中各类氨基酸的平均占比。最终,结合两歧双歧杆菌的氮源利用特征,从中筛选出最适蛋白。
1.3.2 蛋白水解肽制备
富含脯氨酸的蛋白的酶解方法:向生物平行反应器中加入配制好的70 g/L的蛋白溶液,调节温度和pH值为蛋白酶的最适反应条件,按照4 000 U/g蛋白的添加量加入蛋白酶。酶解完成后,将酶解液置于沸水浴10 min,待酶解液冷却至室温后,使用0.22 μm陶瓷膜粗过滤酶解液,再通过2 000 Da有机卷式膜截取小分子肽,冻干,得到酶解蛋白肽。具体制备条件见表1。
表1 不同蛋白酶的酶解条件
Table 1 Enzymatic conditions of different proteases
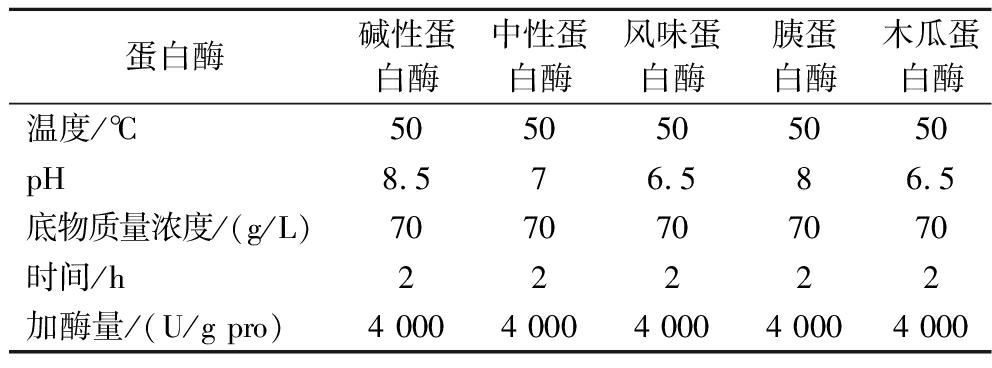
蛋白酶碱性蛋白酶中性蛋白酶风味蛋白酶胰蛋白酶木瓜蛋白酶温度/℃5050505050pH8.576.586.5底物质量浓度/(g/L)7070707070时间/h22222加酶量/(U/g pro)4 0004 0004 0004 0004 000
促进两歧双歧杆菌生长的有益蛋白的分步酶解方法与上述方法类似,但为多步水解,蛋白浓度为70 g/L,反应温度为50 ℃,具体制备条件见表2。
表2 促进两歧双歧杆菌生长的有益蛋白的分步酶解条件
Table 2 Enzymatic hydrolysis conditions of beneficial proteins promoting the growth of B.bifidum
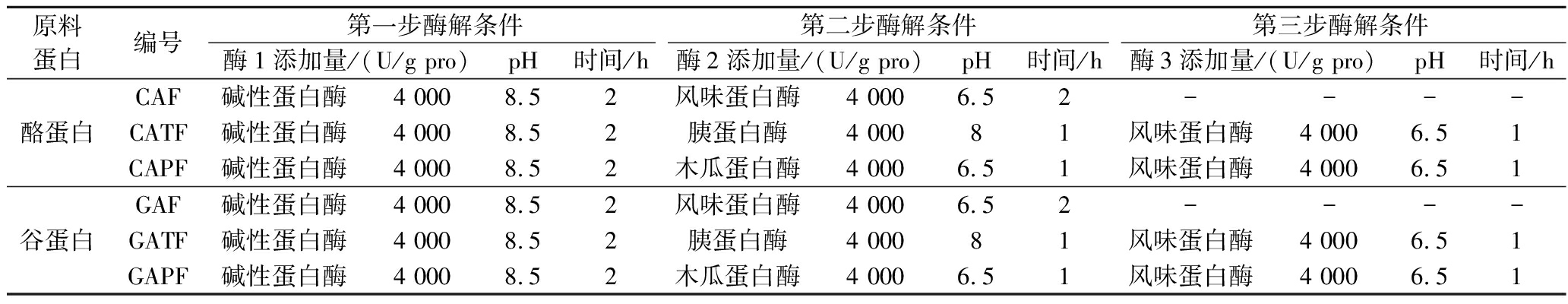
原料蛋白编号第一步酶解条件第二步酶解条件第三步酶解条件酶1添加量/(U/g pro)pH时间/h酶2添加量/(U/g pro)pH时间/h酶3添加量/(U/g pro)pH时间/h酪蛋白CAF碱性蛋白酶4 0008.52风味蛋白酶4 0006.52----CATF碱性蛋白酶4 0008.52胰蛋白酶4 00081风味蛋白酶4 0006.51CAPF碱性蛋白酶4 0008.52木瓜蛋白酶4 0006.51风味蛋白酶4 0006.51谷蛋白GAF碱性蛋白酶4 0008.52风味蛋白酶4 0006.52----GATF碱性蛋白酶4 0008.52胰蛋白酶4 00081风味蛋白酶4 0006.51GAPF碱性蛋白酶4 0008.52木瓜蛋白酶4 0006.51风味蛋白酶4 0006.51
注:经碱性蛋白酶、风味蛋白酶水解得到的酪蛋白肽(casein peptides hydrolyzed by alkaline protease and flavourzyme, CAF);经碱性蛋白酶、胰蛋白酶、风味蛋白酶水解得到的酪蛋白肽(casein peptides hydrolyzed by alkaline protease, trypsin and flavourzyme, CATF);经碱性蛋白酶、木瓜蛋白酶、风味蛋白酶水解得到的酪蛋白肽(casein peptides hydrolyzed by alkaline protease, papain and flavourzyme. CAPF);经碱性蛋白酶、风味蛋白酶水解得到的谷蛋白肽(glutenin peptides hydrolyzed by alkaline protease and flavourzyme, GAF);经碱性蛋白酶、胰蛋白酶、风味蛋白酶水解得到的谷蛋白肽(glutenin peptides hydrolyzed by alkaline protease, trypsin and flavourzyme, GATF);经碱性蛋白酶、木瓜蛋白酶、风味蛋白酶水解得到的谷蛋白肽(glutenin peptides hydrolyzed by alkaline protease, papain and flavourzyme, GAPF)。
1.3.3 蛋白水解肽初步筛选
以1 g/L水解肽为氮源配制氮源筛选培养基。将两歧双歧杆菌CCFM1301接种后,取接种后样液,使用分光光度计测得0 h的OD600-0 h,培养12 h,再次测定其终点OD600-12 h,计算OD600-12 h-OD600-0 h得到ΔOD600。
1.3.4 菌株肽利用相关基因的挖掘
从uniprot数据库(https://www.uniprot.org)中分别下载两歧双歧杆菌的肽转运系统、肽酶系统的蛋白序列。使用BLAST(v2.11.0)(https://ftp.ncbi.nlm.nih.gov/blast/executables/blast+/)中的makeblastdb.exe建立本地数据库,随后使用blastp.exe进行基因挖掘。
两歧双歧杆菌CCFM1301的基因组信息由江南大学食品微生物菌种保藏中心提供。
1.3.5 蛋白模拟切割
从NCBI数据库中下载谷蛋白和酪蛋白的相关蛋白序列。各蛋白来源:α-酪蛋白ID:NP_851372.1;β-酪蛋白ID:XP_014335713.2;k-酪蛋白ID:AAI02121.1;低分子质量谷蛋白(LWM-GS)ID:AGO17759.1;高分子质量谷蛋白(LWM-GS)ID:AAU04841.1。
从BRENDA和Prosperous Plus数据库中调研并汇总常见蛋白酶的酶切位点。使用ProteinCutter (https://software.cr-hana.upol.cz/proteincutter/index.php)对获取的蛋白序列进行模拟酶切。
1.3.6 OppA蛋白与多肽序列的分子对接
OppA蛋白使用AlphaFold 2.3.2进行建模(OppA蛋白序列来自CCFM1301的全基因组数据)。
使用Discovery Studio 2019(v19.1.10)采取CDOCKER进行分子对接,以肽结合蛋白为受体,肽为配体,Top Hits设为1,Pose Cluster Radius设为0.5,其余参数默认。
1.3.7 多肽样品分子质量分布测定
参考黄伟乾等[8]的方法并略加修改,使用凝胶排阻色谱法对肽的分子质量进行测定。色谱柱为TSKgel 2000 SWXL(300 mm×7.8 mm),流动相为乙腈-水-三氟乙酸(三者体积比为45∶55∶0.1),流速为0.5 mL/min,紫外检测波长为220 nm。
1.3.8 多肽样品氨基酸组成测定
酸水解氨基酸样品制备:在水解管中添加100.0 mg肽溶于6 mL 6 mol/L的盐。氮吹3 min后,将水解管置于120 ℃的烘箱,水解22~24 h。取1 mL水解液,旋转蒸发至干,并用适量超纯水复溶待测。
游离氨基酸测定:样品无需酸水解,超纯水配制5 mg/mL的肽液待测。
氨基酸测定方法参考了WANG等[9]和YU等[10]的方法,加以修改。
1.3.9 生长指标测定
生长曲线:按照20 mL/L接种量,将两歧双歧杆菌接种至培养基中,每隔2 h使用紫外分光光度计测定菌液的OD600。
代时:代时的测定参照高欣伟[11]的方法。
活菌数:取0.5 mL菌液,半胱氨酸缓冲液进行梯度稀释至10-6、10-7、10-8。取1 mL稀释液置于培养皿中央,每个梯度3个平行,倒入10~20 mL固体MRS培养基,培养48 h后计数。
单位氮源产生的活菌数:通过测定8、12、16、20 h时的氮源消耗量与活菌数,计算单位氮源产生的活菌数,用来比较2种氮源的转化效率,按公式(1)计算:
单位氮源产生的活菌数![]()
(1)
式中:Na,a时刻氮源总量;Nb,b时刻氮源总量;Sa,a时刻的活菌数;Sb,b时刻的活菌数。氮源的含量通过凯式定氮法测定。
1.3.10 数据统计与分析
实验均重复3次,数据表示为“平均值±标准偏差”。使用Excel 2021、GraphPad Prism 9进行分析与绘图,GraphPad Prism 9软件进行单因素方差分析(Tukey检验),P<0.05表示具有显著性差异。
2 结果与讨论
2.1 富脯氨酸蛋白的筛选
以高脯氨酸含量、高亮氨酸含量、低甲硫氨酸含量、含有半胱氨酸、氨基酸种类完整这5个指标来挑选底物蛋白。表3是常见商业蛋白的氨基酸分布情况。在商业蛋白中,脯氨酸含量从高到低依次为明胶、麦醇溶蛋白(小麦)、麦醇溶蛋白(大麦)、麦谷蛋白(小麦)、酪蛋白、大豆蛋白、乳清蛋白和芝麻蛋白。其中小麦醇溶蛋白和大麦醇溶蛋白虽然都含有较高含量的脯氨酸,但小麦来源的Ω-醇溶蛋白和大麦来源的C-大麦醇溶蛋白豆不含有两歧双歧杆菌需要的半胱氨酸,因此不选择这2种蛋白作为底物蛋白。芝麻蛋白中的2S种子贮藏蛋白则含有较高含量的甲硫氨酸(10.81%),可能会抑制两歧双歧杆菌生长,且脯氨酸(2.03%)和亮氨酸含量(4.73%)相较于其他几种蛋白偏低。乳清蛋白虽然脯氨酸含量较低,但其含有较多的亮氨酸和半胱氨酸。
表3 常见商业蛋白中脯氨酸、亮氨酸、半胱氨酸和甲硫氨酸的组成分析
Table 3 Composition analysis of proline, leucine, cysteine and methionine in common commercial proteins
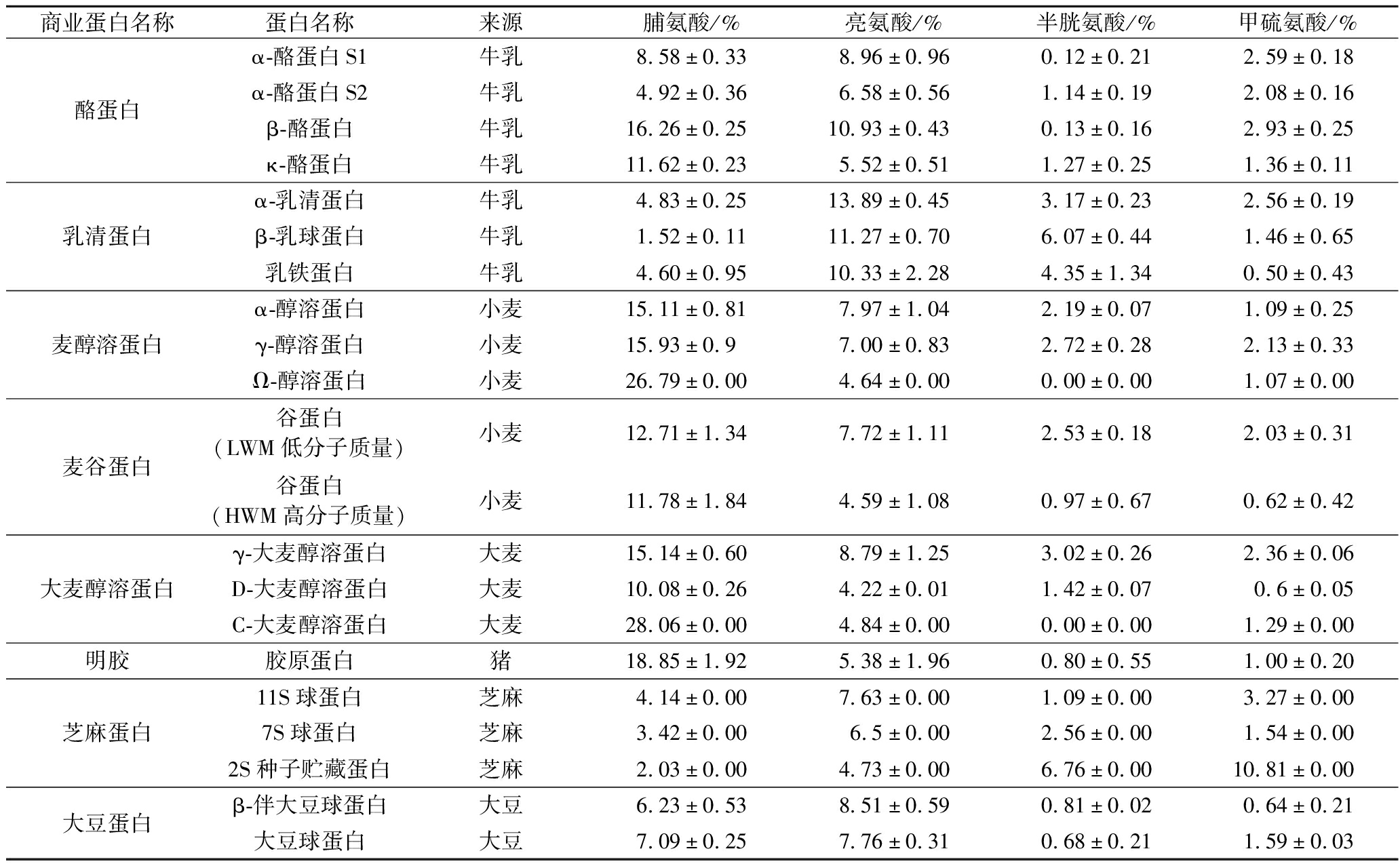
商业蛋白名称蛋白名称来源脯氨酸/%亮氨酸/%半胱氨酸/%甲硫氨酸/%酪蛋白α-酪蛋白S1牛乳8.58±0.338.96±0.960.12±0.212.59±0.18α-酪蛋白S2牛乳4.92±0.366.58±0.561.14±0.192.08±0.16β-酪蛋白牛乳16.26±0.2510.93±0.430.13±0.162.93±0.25κ-酪蛋白牛乳11.62±0.235.52±0.511.27±0.251.36±0.11乳清蛋白α-乳清蛋白牛乳4.83±0.2513.89±0.453.17±0.232.56±0.19β-乳球蛋白牛乳1.52±0.1111.27±0.706.07±0.441.46±0.65乳铁蛋白牛乳4.60±0.9510.33±2.284.35±1.340.50±0.43麦醇溶蛋白α-醇溶蛋白小麦15.11±0.817.97±1.042.19±0.071.09±0.25γ-醇溶蛋白小麦15.93±0.97.00±0.832.72±0.282.13±0.33Ω-醇溶蛋白小麦26.79±0.004.64±0.000.00±0.001.07±0.00麦谷蛋白谷蛋白(LWM低分子质量)小麦12.71±1.347.72±1.112.53±0.182.03±0.31谷蛋白(HWM高分子质量)小麦11.78±1.844.59±1.080.97±0.670.62±0.42大麦醇溶蛋白γ-大麦醇溶蛋白 大麦15.14±0.608.79±1.253.02±0.262.36±0.06D-大麦醇溶蛋白 大麦10.08±0.264.22±0.011.42±0.070.6±0.05C-大麦醇溶蛋白大麦28.06±0.004.84±0.000.00±0.001.29±0.00明胶胶原蛋白猪18.85±1.925.38±1.960.80±0.551.00±0.20芝麻蛋白11S球蛋白芝麻4.14±0.007.63±0.001.09±0.003.27±0.007S球蛋白芝麻3.42±0.006.5±0.002.56±0.001.54±0.002S种子贮藏蛋白芝麻2.03±0.004.73±0.006.76±0.0010.81±0.00大豆蛋白β-伴大豆球蛋白大豆6.23±0.538.51±0.590.81±0.020.64±0.21大豆球蛋白大豆7.09±0.257.76±0.310.68±0.211.59±0.03
最终,选择了酪蛋白、乳清蛋白、麦谷蛋白、明胶、大豆蛋白这5种蛋白作为底物进行下一步的研究。
2.2 促进两歧双歧杆菌生长的有益蛋白的筛选
研究表明,两歧双歧杆菌偏好利用短肽[3]。本研究选择酶切位点广泛、活性大、易于获得的商业化蛋白酶对原料蛋白进行酶解以制备短肽。有研究选用酶切位点广泛、酶活性高的碱性蛋白酶、木瓜蛋白酶、胰酶等对酪蛋白进行酶解,制备的1 kDa以下的氨基酸和小肽达到70%以上[12]。图1是市面上各类水解酶的酶切位点及其位点数量。切割位点5个以上的蛋白酶有碱性蛋白酶、蛋白酶K、木瓜蛋白酶、风味蛋白酶和中性蛋白酶。其中蛋白酶K有8个切割位点,但价格昂贵不易获得,不适合用于制备蛋白胨,因此不选用该酶。而胰蛋白酶虽然只作用于蛋白的精氨酸和赖氨酸2个位点,但其活性高,切割效率高,常用作蛋白酶解,因此选用了胰蛋白酶。最终选择碱性蛋白酶、木瓜蛋白酶、中性蛋白酶、风味蛋白酶和胰蛋白酶用作初步酶解。
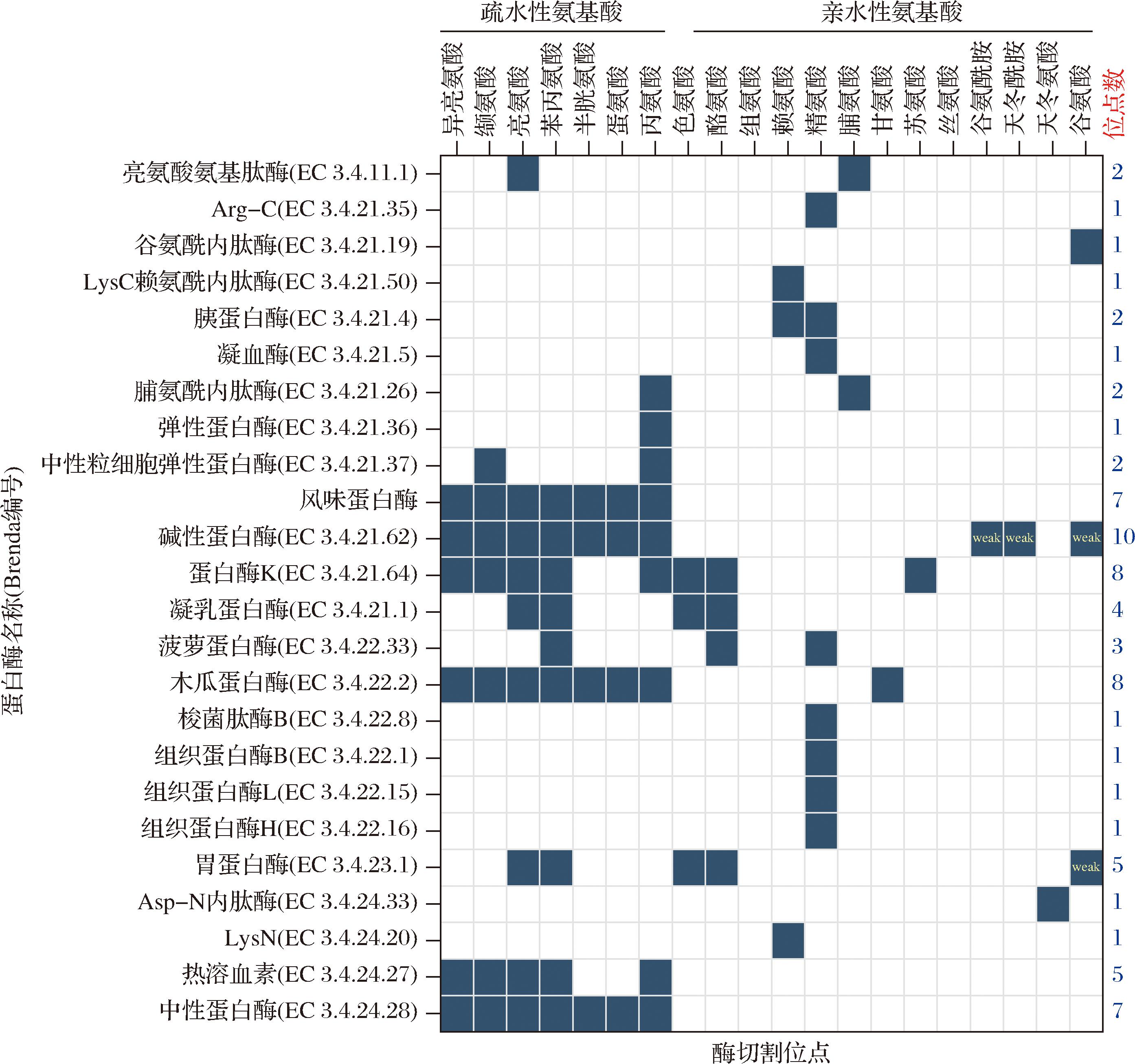
图1 蛋白酶的酶切位点
Fig.1 Site of protease digestion
依据表1中的酶解条件,使用上述5种酶对2.1节选取的5种原料蛋白进行酶解,得到了25种水解肽。以MRS为对照组,在限氮培养基下将这25种氮源用于两歧双歧杆菌的培养。表4显示,乳清蛋白肽的促进生长效果非常明显,其中WA最好,OD600为0.445±0.009,远远超出对照组MRSN(0.203±0.009)。高海燕[13]研究发现,双歧杆菌在乳蛋白水解物的替代培养基中,活菌数约为对照MRS的1.4倍。逯莹莹[14]的研究发现,乳清蛋白的水解程度可能是促进益生菌增殖的关键因素之一,在最佳水解程度下效果最为明显。除了乳清蛋白肽,酪蛋白肽和谷蛋白肽对两歧双歧杆菌的生长促进作用也较为显著,5种酪蛋白肽中,除了CF培养下与对照组无显著差异,其他4种蛋白肽的效果相较于MRS都显著提升;而5种麦谷蛋白肽中仅有GA和GP效果显著,其他3种肽与MRSN的效果无显著差异。类似的,熊昌武等[15]也发现谷物蛋白水解物用于嗜酸乳杆菌培养,效果要好于其他蛋白胨。此外,大豆蛋白肽和明胶肽对两歧双歧杆菌的生长没有起到促进,生长效果反而低于对照组MRS。酪蛋白和谷蛋白富含脯氨酸且产生的肽可显著促进两歧双歧杆菌生长,因此以这2种蛋白为底物进一步酶解制备可以被两歧双歧杆菌利用的脯氨酸肽。
表4 两歧双歧杆菌在酶解肽作为氮源的培养基的生长情况
Table 4 Growth of B.bifidum in a culture medium with hydrolyzed peptides as a nitrogen source
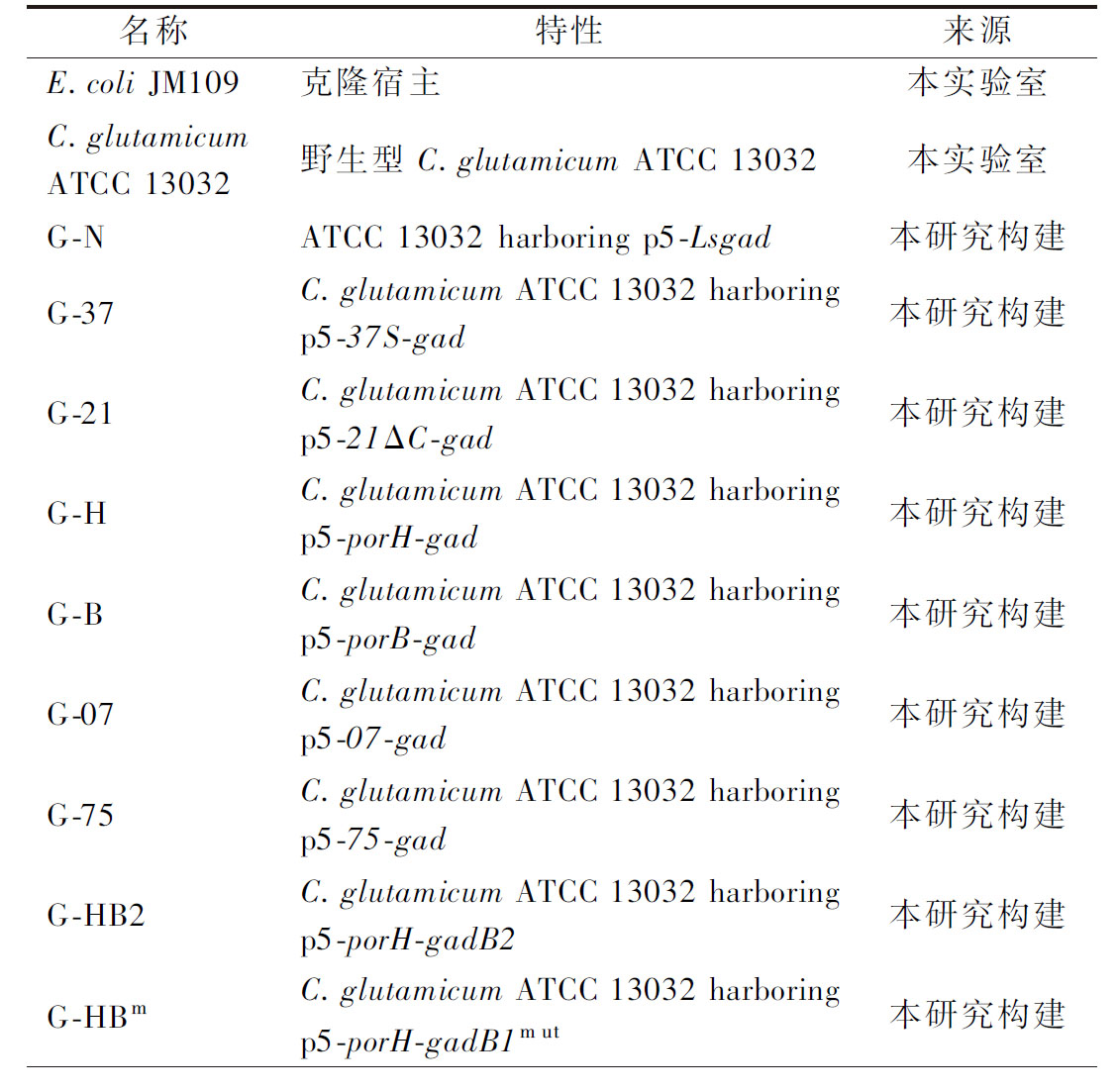
续表4
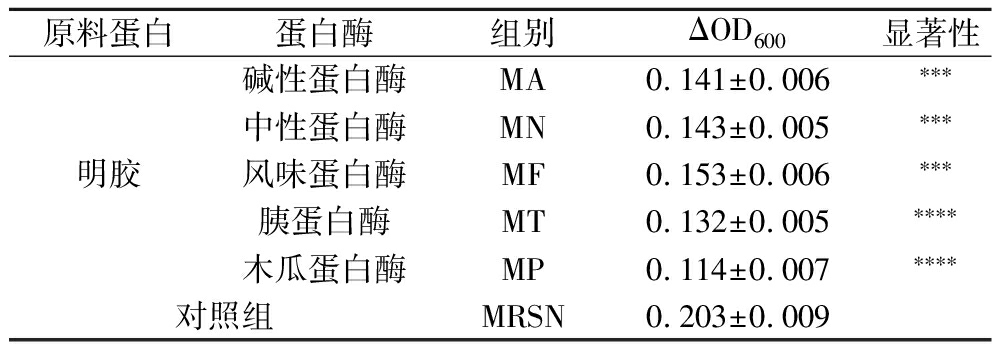
原料蛋白蛋白酶组别ΔOD600显著性明胶碱性蛋白酶MA0.141±0.006∗∗∗中性蛋白酶MN0.143±0.005∗∗∗风味蛋白酶MF0.153±0.006∗∗∗胰蛋白酶MT0.132±0.005∗∗∗∗木瓜蛋白酶MP0.114±0.007∗∗∗∗对照组MRSN0.203±0.009
注:与1 g/L MRSN比较:ns表示差异不显著,*表示差异显著P<0.05,**表示P<0.01,***表示P<0.001,****表示P<0.000 1。
2.3 底物蛋白的酶切产物预测及与两歧双歧杆菌寡肽结合蛋白的分子对接研究
肽段在胞内会被肽酶进一步分解成更短的短肽和氨基酸,而双歧杆菌胞内存在氨基肽酶、脯氨酸残基特异性肽酶、二肽酶和内肽酶等多种肽酶[16]。本研究挖掘了两歧双歧杆菌CCFM1301的相关肽酶基因,结果表明,该菌缺乏PepI(proline iminopeptidase, PepI)、PepR(prolinase R, PepR)、PepQ(prolyl aminopeptidase Q, PepQ)这3种肽酶(图2-c)。这3种肽酶切割处在肽段两端的脯氨酸。相比之下,该菌仍保留的肽酶PepP(aminopeptidase P)、PepX(X-prolyl dipeptidyl aminopeptidase)可作用于肽段中部的脯氨酸,而Pap(prolyl aminopeptidase)仅作用于含脯氨酸的二肽,不对寡肽起作用[17]。这表明CCFM1301可能更倾向于切割脯氨酸位于肽链中间的肽段。因此,在选取蛋白酶时,需避开可特异性切割脯氨酸的酶,以防止酶解后脯氨酸直接暴露于肽链末端。

a-制备脯氨酸肽的酶解策略;b-常见商用蛋白酶的切割位点情况;c-两歧双歧杆菌CCFM1301拥有的肽酶;d-预测肽中脯氨酸肽的比例及预测肽与OppA分子对接成功率;e-分子对接示意图
图2 脯氨酸肽制备策略、蛋白的酶切产物预测及肽与OppA的分子对接情况
Fig.2 Preparation strategy of proline-containing peptides, prediction of protein cleavage products, and molecular docking of peptides with OppA
研究还表明,两歧双歧杆菌偏好利用长度2、3、9的短肽,以及亲水性的肽[3]。结合这些肽利用特征以及上述的肽酶切割特点,依据酶切特征给出了制备脯氨酸肽的酶切策略(图2-a)。首先选取酶切位点最广泛的碱性蛋白酶进行酶切以产生短肽,此外,该酶对疏水性氨基酸的特异性作用会使蛋白质的疏水性残基暴露在肽两端,为后续的外切酶作用创造了条件(图2-b)。在反应结束后还可以加入另一种与碱性蛋白酶作用位点相异的酶进一步水解,使得肽段进一步缩小。从图2-b可以看出,胰蛋白酶、蛋白酶K、胰凝乳蛋白酶、菠萝蛋白酶、木瓜蛋白酶和胃蛋白酶都具有碱性蛋白酶不具有的作用位点。但考虑到蛋白酶K、胰凝乳蛋白酶、菠萝蛋白酶价格昂贵,不适用氮源制备的场景,因此不予选用。而胃蛋白酶(最适pH=2)的与碱性蛋白酶(最适pH=8.5)最适反应pH差距过大,酶解过程中的pH调整会带来大量盐离子,影响氮源纯度。因此,最终选择了胰蛋白酶和木瓜蛋白酶。在制备得到尽可能小的多肽后,接着是引入具有外切酶特性的风味蛋白酶切除位于碳端或氮源的疏水性氨基酸,以提升肽端整体的亲水性。最后,以酪蛋白和谷蛋白以酶解底物共制定了6种酶切方案,其中酪蛋白3种(CAF、CATF、CAPF),谷蛋白3种(GAF、GATF、GAPF)。
为了初步验证酶切方案的可行性,首先使用Protein Cutter工具预测了这几种方案会产生的肽的序列。图2-d热图上方的柱形图显示了酶切得到的肽中脯氨酸肽的占比,结果表明产生的肽中脯氨酸肽占到总体的35.2%~62.5%。为了进一步验证预测得到的肽是否可以被两歧双歧杆菌CCFM1301转运,将菌株的OppA蛋白与这些预测肽进行了分子对接。图2-e为分子对接示意图。软件Discovery studio会将可以成功对接的蛋白与肽输出,并显示其对接形态与受力情况。图2-d中热图则显示了CCFM1301的OppA与预测肽之间的分子对接成功率。CCFM1301_0493与3种酪蛋白肽的对接成功率均高于90%。而对谷蛋白肽,OppA与肽的总体对接成功率要低于酪蛋白肽,但依然有至少有77.5%的肽可以被CCFM1301转运。Opp系统的OppA是决定肽转运特征的关键蛋白[18],将模拟得到的肽与菌株的OppA进行了分子对接来判断得到的肽是否能被其结合并转运。类似的,也有学者通过分子对接模拟OppA与肽的结合来探究长双歧杆菌OppA的底物特异性[19]。
由此,上述酶切方案得到的肽绝大部分都可以被两歧双歧杆菌的肽转运蛋白结合并转运,计划按照这些酶切策略制定酶切方案进行下一步制备。
2.4 富含脯氨酸肽的酶解制备及氨基酸组成与分子质量大小分析
参考CUI等[3]研究中的蛋白酶解工艺,制定了6种蛋白胨的制备方法(表2),并按照方法进行了制备,最终得到了6种脯氨酸肽。测定这6种肽的总体氨基酸组成和游离氨基酸组成,结果如图3-a所示。6种肽中游离脯氨酸含量较低,说明脯氨酸均以肽链的形式存在,这与选用的不作用于脯氨酸的蛋白酶有关。图3-a还显示,大量异亮氨酸、缬氨酸、亮氨酸、苯丙氨酸、半胱氨酸在酶解后游离,这可能是由于风味蛋白酶的使用,将大量处在肽段边缘的疏水性氨基酸切割下来,从而提高了肽的整体亲水性。图3-b分子质量分布的结果则显示,这6种肽中目标分子质量180~2 000 Da的肽组分较高,分别占到86.15%、90.08%、85.9%、80.12%、84.28%和72.49%,其中又以180~500 Da的短肽为主。从表征结果看,酶解制备的脯氨酸肽满足了制备需求。
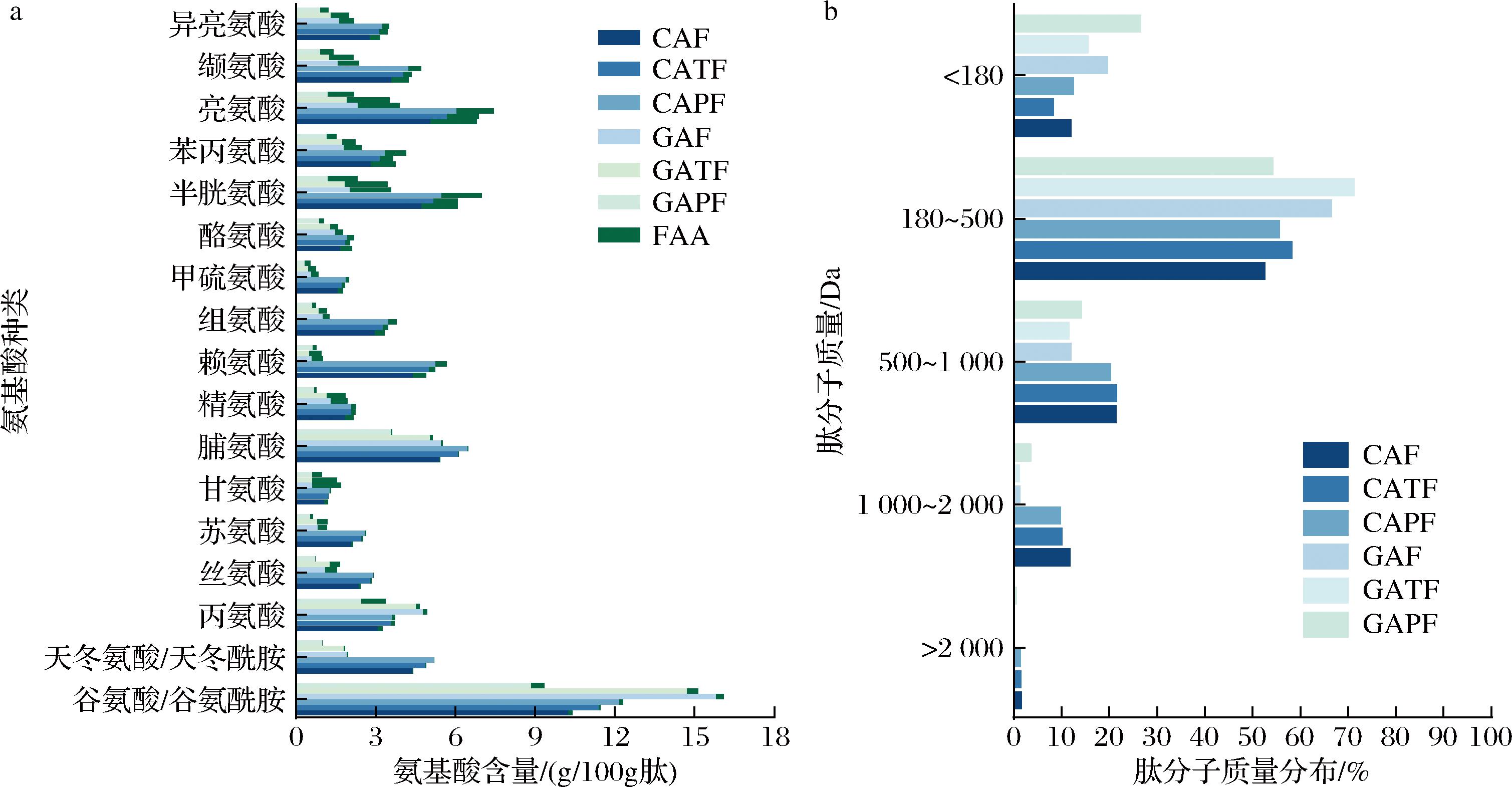
a-氨基酸组成;b-分子质量分布
图3 脯氨酸肽氨基酸组成与分子质量大小
Fig.3 Amino acid composition and molecular weight of proline-containing peptides
注:本小节中所用样品均由底物蛋白经酶解后获得,已通过陶瓷膜去除杂蛋白后经2 000 Da超滤膜截取小分子质量肽。
2.5 不同富含脯氨酸肽的复配对两歧双歧杆菌生长的影响
以氮源添加总量为2 g/L的MRS作为对照组,在限氮培养基下测定不同脯氨酸肽培养下两歧双歧杆菌的ΔOD600,同时将2.2节中筛选到的对两歧双歧杆菌生长具有显著促进作用的乳清蛋白肽WA一同作为参照。如图4-a所示,乳清蛋白肽WA(ΔOD600=1.585)和酪蛋白肽CAF(ΔOD600=0.640)、CAPF(ΔOD600=0.608)培养下,两歧双歧杆菌的生长均优于MRS对照组(ΔOD600=0.565),而其中WA的效果最好,CAF次之。文献表明,乳清蛋白肽氨基酸含量均衡,必需氨基酸含量充足,被认为是氨基酸含量的金标准[20]。JANER等[21]也发现从甜奶酪乳清中分离出的酪蛋白巨肽和浓缩乳清蛋白可促进乳双歧杆菌在牛奶中的生长。虽然乳清蛋白肽脯氨酸含量低于酪蛋白,但其富含生长因子[22],这可能是其效果优于其他氮源的原因。
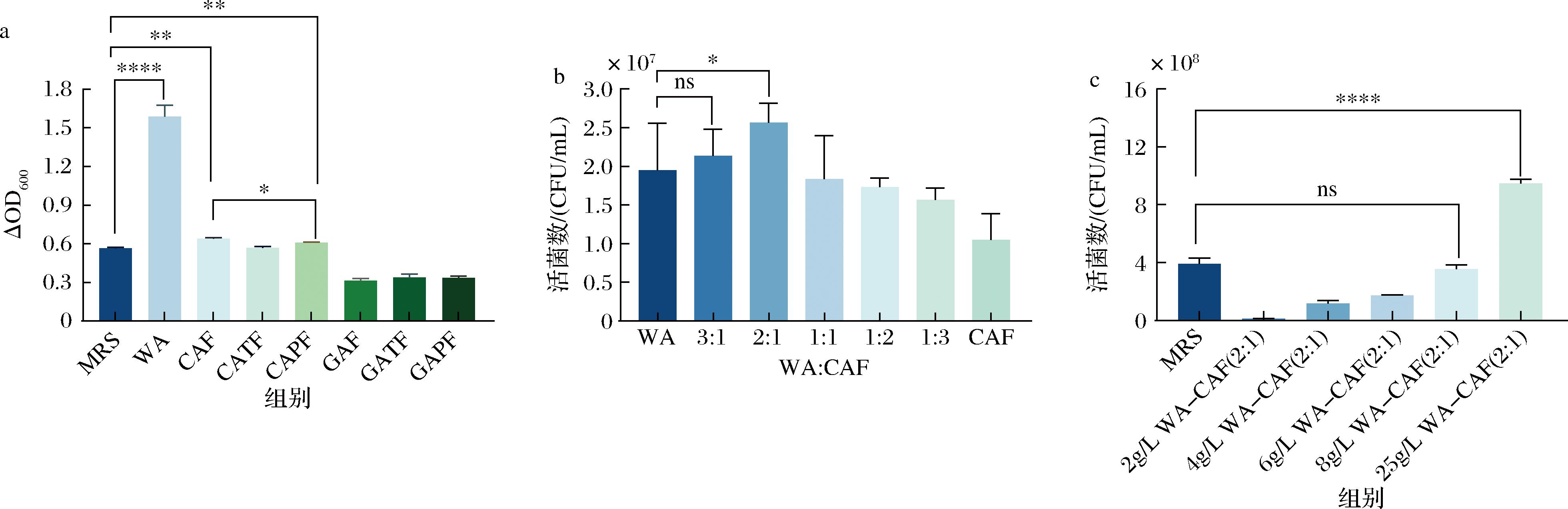
a-不同脯氨酸肽培养下两歧双歧杆菌的ΔOD600;b-WA与CAF不同添加比例下两歧双歧杆菌的活菌数;c-不同脯氨酸肽添加量培养下两歧双歧杆菌的活菌数
图4 不同的脯氨酸肽复配下两歧双歧杆菌生长情况
Fig.4 Growth of B.bifidum under different combinations of proline-containing peptides
注:图中ns表示差异不显著,*表示差异显著P<0.05,**表示P<0.01,***表示P<0.001,****表示P<0.000 1(下同)。
为了进一步提高两歧双歧杆菌对氮源的利用率,将WA和CAF以不同质量比(3∶1、2∶1、1∶1、1∶2、1∶3)复配后,按照2 g/L的添加量用于两歧双歧杆菌的培养,测得生长12 h后的活菌数。图4-b显示,随着WA的占比增大,活菌数逐渐增多,当比例为2∶1时活菌数达到最大值(2.56±0.23)×107 CFU/mL,再次增大乳清蛋白WA的比例,活菌数反而下降,3∶1时降为(2.13±0.31)×107 CFU/mL。因此,当WA∶CAF混合比例为2∶1时两歧双歧杆菌生长的最好。复配可以使得氮源之间营养成分互补后协同作用,补充单一氮源的营养短板。有研究在两歧双歧杆菌的氮源优化实验中将酵母蛋白胨YP和酵母浸粉FM985进行复配,发现一些复配比例下,菌株生长有所提升[23]。
在WA∶CAF为2∶1的比例下按照不同氮源添加量(2、4、6、8、25 g/L)培养两歧双歧杆菌,测定活菌数,对照组为氮源添加量25 g/L的MRS。结果如图4-c所示,8 g/L WA-CAF的氮源培养下,两歧双歧杆菌的活菌数达到(3.55±0.26)×108 CFU/mL,对照组MRS则为(3.90±0.32)×108 CFU/mL,两者之间没有显著差异。而25 g/L WA-CAF培养下活菌数达到(9.47±0.24)×108 CFU/mL,约为对照组的2.43倍,这说明同样氮源添加量培养下,菌体生长密度显著提升。结果表明,当WA∶CAF(2∶1)的添加量达到8 g/L时,活菌数与氮源添加总量为25 g/L 的MRS相当,这初步说明,相比于MRS中的氮源,两歧双歧杆菌对WA∶CAF(2∶1)的利用率更高。
2.6 优化后氮源对两歧双歧杆菌生长和氮源利用的影响
为了充分评价富含脯氨酸肽的氮源WA-CAF对两歧双歧杆菌生长的促进效果,进一步比较了其在2种氮源培养下的生长与氮源利用情况。以25 g/L氮源添加量的MRS为对照,测定了在8 g/L的WA-CAF(2∶1)培养下CCFM1301的生长曲线、代时、活菌数和单位氮源产生的活菌数(图5)。
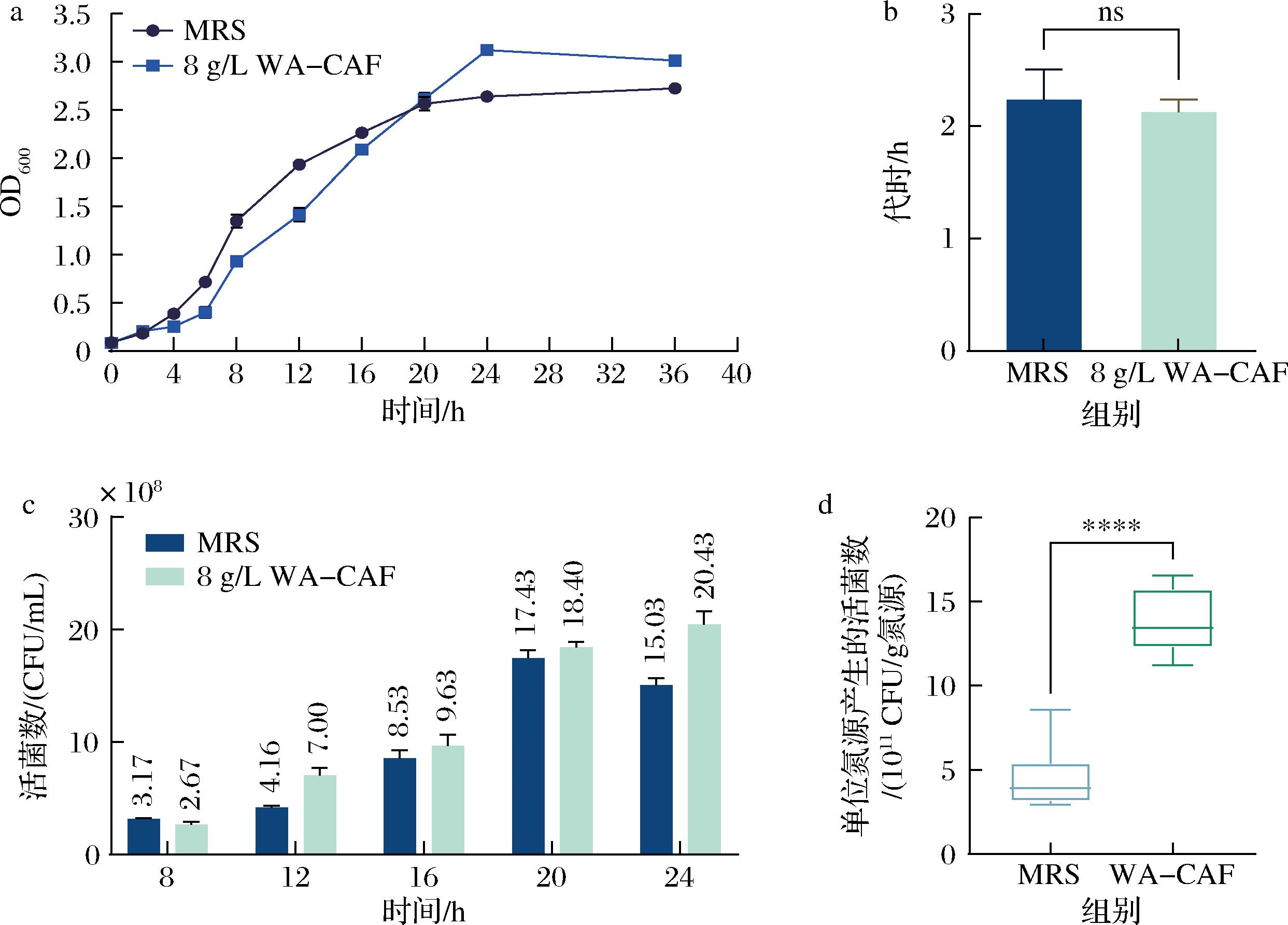
a-生长曲线;b-代时;c-活菌数;d-单位质量氮源产生的活菌数
图5 两歧双歧杆菌在优化后氮源培养下的生长和氮源利用情况
Fig.5 Growth and nitrogen source utilization of B. bifidum under optimized nitrogen source culture
如图5-a所示,WA-CAF组的生长上限高于MRS,具有更长的对数期,但两者的生长速率(代时)分别为2.23±0.19和2.13±0.08,没有显著差异(图5-b)。图5-c显示了2种氮源培养下两歧双歧杆菌的活菌数变化。24 h时,WA-CAF组最终活菌数达到(2.04±0.1)×109 CFU/mL,相较于MRS提升了35%。田睿等[23]在20 mL体系中优化两歧双歧杆菌的氮源培养基,所使用的商业蛋白胨添加20 g/L时效果最佳,活菌数为(2.24±0.24)×109 CFU/mL,与本研究中WA-CAF组终末菌量相当。但本研究的氮源添加总量仅占其40%,由此说明WA-CAF培养基在商业氮源中也具有显著优势。
进一步测定2种氮源培养下两歧双歧杆菌利用单位氮源产生的活菌数。如图5-d所示,WA-CAF培养下每克氮源产生的活菌数达到(1.38±0.18)×1012 CFU/g氮源,而MRS培养下这一数值是(0.46±0.18)×1012 CFU/g氮源,相较于后者,提升了约198.5%。上述实验结果表明:WA-CAF相较于MRS可以被两歧双歧杆菌高效转化并提升其活菌数,对该菌的工业化生产具有重大意义。
3 结论
本研究优选5种富含脯氨酸的蛋白和5种具备多位点高活性的蛋白酶,结合菌株培养从中筛选出了1种对两歧双歧杆菌生长最有效果的乳清蛋白肽(WA)和2种高含脯氨酸且对生长有益的底物蛋白(酪蛋白、谷蛋白)。结合两歧双歧杆菌的氮源利用特性与肽酶特征制定了多步酶解策略,利用计算机工具预测了酶解肽,将预测的肽段与菌株肽转运的关键蛋白OppA结合,验证了策略的可行性。
酶解制备得到了6种富含脯氨酸的肽,将它们与一种乳清蛋白肽都用作培养,发现乳清蛋白肽(WA)与酪蛋白肽(CAF)复配(2∶1),添加量8 g/L时菌株生长便与MRS相当。测定8 g/L WA-CAF(2∶1)与25 g/L MRS培养下两歧双歧杆菌的生长曲线、代时、活菌数、和单位氮源产生活菌数。结果表明,两者代时无差异,但前者活菌数达(2.04±0.1)×109 CFU/mL,单位氮源产生活菌数为(1.38±0.18)×1012 CFU/g氮源,相较于传统MRS培养基分别提升35%和198.5%。
[1] 汪文丽. 双歧杆菌氮源利用的选择性及特征分析[D].无锡:江南大学, 2021.
WANG W L.Selectivity and characteristic analysis of nitrogen source utilization by Bifidobacteria[D].Wuxi:Jiangnan University,
[2] ZAFAR H, SAIER M H Jr.Comparative analyses of the transport proteins encoded within the genomes of nine Bifidobacterium species[J].Microbial Physiology, 2022, 32(1-2):30-44.
[3] CUI S M, GU Z M, WANG W L, et al.Characterization of peptides available to different bifidobacteria[J].LWT, 2022, 169:113958.
[4] FERRARIO C, DURANTI S, MILANI C, et al.Exploring amino acid auxotrophy in Bifidobacterium bifidum PRL2010[J].Frontiers in Microbiology, 2015, 6:1331.
[5] HUANG L Y, WU Y W, FAN Y, et al.The growth-promoting effects of protein hydrolysates and their derived peptides on probiotics:Structure-activity relationships, mechanisms and future perspectives[J].Critical Reviews in Food Science and Nutrition, 2025, 65(22):4401-4420.
[6] 汪文丽, 崔树茂, 唐鑫, 等.两歧双歧杆菌F35氮源利用的差异性解析[J].食品与发酵工业, 2021, 47(19):21-28.
WANG W L, CUI S M, TANG X, et al.Various nitrogen source utilization in Bifidobacterium bifidum F35[J].Food and Fermentation Industries, 2021, 47(19):21-28.
[7] GU Z M, TANG X, MAO B Y, et al.Mechanism analysis of methionine inhibiting growth of Bifidobacterium bifidum[J].Food Bioscience, 2024, 57:103611.
[8] 黄伟乾, 霍玟希, 罗浩, 等.凝胶色谱法(GPC)检测特殊膳食食品中小分子肽的分子量分布的研究[J].现代食品, 2021, 27(17):192-195.
HUANG W Q, HUO W X, LUO H, et al.Research on molecular weight distribution of small molecule peptides in special dietary foods in gel chromatography[J].Modern Food, 2021, 27(17):192-195.
[9] WANG D Y, HU M Y, TANG X, et al.Characterization of physicochemical properties and flavor profiles of fermented Chinese bamboo shoots (Suansun) from Liuzhou and Guilin[J].Food Bioscience, 2023, 56:103125.
[10] YU H Y, ZHAO J, LI F H, et al.Characterization of Chinese rice wine taste attributes using liquid chromatographic analysis, sensory evaluation, and an electronic tongue[J].Journal of Chromatography B, 2015, 997:129-135.
[11] 高欣伟, 崔树茂, 唐鑫, 等.长双歧杆菌的最适底物解析和高密度发酵工艺优化[J].食品与发酵工业, 2021, 47(19):12-20.
GAO X W, CUI S M, TANG X, et al.Optimization of substrate in high-density fermentation of Bifidobacterium longum[J].Food and Fermentation Industries, 2021, 47(19):12-20.
[12] 莫玲. 基于助眠功能的山羊乳蛋白肽的制备、鉴定及作用机制研究[D].无锡:江南大学, 2024.
MO L.Preparation, identification, and mechanism of goat milk protein peptide based on sleep-enhancing function[D].Wuxi:Jiangnan University, 2024.
[13] 高海燕. 乳清蛋白水解物在乳酸菌培养基中的应用研究[D].呼和浩特:内蒙古农业大学, 2012.
GAO H Y.The application of whey protein hydrolysates in lactic bacteria culture[D].Hohhot:Inner Mongolia Agricultural University, 2012.
[14] 逯莹莹, 赵丽双, 刘丽波, 等.乳清蛋白适度水解与其致敏性及益生菌生长的相关性[J].乳业科学与技术, 2018, 41(6):1-5.
LU Y Y, ZHAO L S, LIU L B, et al.Correlation between moderately hydrolyzed whey protein and its allergenicity and probiotics growth[J].Journal of Dairy Science and Technology, 2018, 41(6):1-5.
[15] 熊昌武, 朱亚军, 张彦, 等.小麦蛋白水解物对嗜酸乳杆菌(Lactobacillus acidophilus)生长的影响研究[J].中国酿造, 2024, 43(7):171-176.
XIONG C W, ZHU Y J, ZHANG Y, et al.Effect of wheat protein hydrolysate on the growth of Lactobacillus acidophilus[J].China Brewing, 2024, 43(7):171-176.
[16] MIERAU I, KUNJI E R, LEENHOUTS K J, et al.Multiple-peptidase mutants of Lactococcus lactis are severely impaired in their ability to grow in milk[J].Journal of Bacteriology, 1996, 178(10):2794-2803.
[17] WALTER R, SIMMONS W H, YOSHIMOTO T.Proline specific endo- and exopeptidases[J].Molecular and Cellular Biochemistry, 1980, 30(2):111-127.
[18] KLEPSCH M M, KOVERMANN M, LÖW C, et al.Escherichia coli peptide binding protein OppA has a preference for positively charged peptides[J].Journal of Molecular Biology, 2011, 414(1):75-85.
[19] CHAI H H, HAM J S, KIM T H, et al.Identifying ligand-binding specificity of the oligopeptide receptor OppA from Bifidobacterium longum KACC91563 by structure-based molecular modeling[J].Arabian Journal of Chemistry, 2022, 15(11):104198.
[20] VASILEVA-TONKOVA E, NUSTOROVA M, GUSHTEROVA A.New protein hydrolysates from collagen wastes used as peptone for bacterial growth[J].Current Microbiology, 2007, 54(1):54-57.
[21] JANER C, PEL EZ C, REQUENA T.Caseinomacropeptide and whey protein concentrate enhance Bifidobacterium lactis growth in milk[J].Food Chemistry, 2004, 86(2):263-267.
EZ C, REQUENA T.Caseinomacropeptide and whey protein concentrate enhance Bifidobacterium lactis growth in milk[J].Food Chemistry, 2004, 86(2):263-267.
[22] ZENG X R, WANG Y J, YANG S D, et al.The functionalities and applications of whey/whey protein in fermented foods:A review[J].Food Science and Biotechnology, 2024, 33(4):769-790.
[23] 田睿, 石阳阳, 杨睿, 等.两歧双歧杆菌F35培养基优化及恒定pH发酵研究[J].中国乳品工业, 2025, 53(1):19-25.
TIAN R, SHI Y Y, YANG R, et al.Research on medium optimization and constant-pH fermentation of Bifidobacterium bifidum F35[J].China Dairy Industry, 2025, 53(1):19-25.